高一化学物质的量浓度3
高中化学 2.3 第3课时 物质的量浓度教案 新人教版必修第一册-新人教版高一第一册化学教案

第3课时物质的量浓度课程标准核心素养1.了解物质的量浓度的含义和应用,体会定量研究对化学科学的重要作用。
2.能基于物质的量认识物质的组成及其化学变化,并运用物质的量、摩尔质量、气体摩尔体积、物质的量浓度之间的相互关系进行简单计算。
3.能配制一定物质的量浓度的溶液。
1.变化观念:认识物质的量浓度在化学定量研究中的重要作用。
2.宏观辨识与微观探析:建立物质的量浓度的概念,基于物质的量浓度定量认识物质的组成及物质的化学变化。
3.科学探究:选择常见实验仪器、装置和试剂,配制一定物质的量浓度的溶液。
物质的量浓度及其计算1.概念:单位体积的溶液里所含溶质B的物质的量,符号为c B,常用单位为mol/L或mol·L-1。
2.表达式:c B=n BV,其中的“V”指的是溶液的体积,而非溶剂的体积。
3.简单计算(1)已知溶液中某种离子的浓度,求其他离子的浓度溶液中阴、阳离子的物质的量浓度之比=化学组成中的离子个数之比。
例如:Na2SO4溶液中,c(SO2-4)=1 mol·L-1,则c(Na+)=2__mol·L-1,c(Na2SO4)=1__mol·L-1。
(2)已知一定体积的溶液中溶质的质量计算浓度例如:2.0 g NaOH固体溶于水配成500 mL溶液,则该溶液的浓度为__0.1__mol·L-1。
(3)标准状况下,一定体积的气体溶于水形成V L 溶液计算浓度例如:标准状况下,11.2 L HCl 气体溶于水配成200 mL 溶液,则该溶液的浓度为2.5__mol·L -1。
1.物质的量浓度与溶质的质量分数的换算 (1)换算公式:c B =1 000ρw Mmol ·L -1M :溶质B 的摩尔质量(单位:g·mol -1);ρ:溶液密度(单位:g·mL -1);w :溶质的质量分数。
(2)推导方法设溶液体积为1 L ,则c B =n BV=ρ g ·mL -1×1 000 mL ×wM g ·mol -11 L =1 000ρw Mmol ·L -1。
2.3.3 物质的量浓度(课件)高一化学(人教版2019必修第一册)

2. NA表示阿伏加德罗常数的值,下列关于0.2 mol/L K2SO4溶液的说 法正确的是( C )
A.1 000 mL水中所含K+、SO总数为0.3 NA B.500 mL溶液中有0.1 NA个K+ C.1 L溶液中K+的浓度为0.4 mol/L D.1 L溶液中SO42-的浓度是0.4 mol/L
(B )
A.0.3 mol·L-1
B.0.8 mol·L-1
C.0.4 mol·L-1
D.0.5 mol·L-1
第3课时 物质的量浓度
Thanks 谢谢观看
/
L)
课堂检测
1. 20 ℃时饱和NaCl溶液的密度为ρ g·cm-3,物质的量浓度为c
mol·L-1,则下列说法中不正确的是( D )
A.温度低于20 ℃时,饱和NaCl溶液的浓度小于c mol·L-1 B.此溶液中NaCl的质量分数为×100% C.20 ℃时,密度小于ρ g·cm-3的NaCl溶液是不饱和溶液 D.20 ℃时,饱和NaCl溶液的溶解度S= g
除特殊说明体积可相加,其它用
V溶液
m溶液
溶液
溶质B可以是单质、化合物,也可以是分子、离子及其特定组合
思考与讨论
1. 以下几种溶液中,哪种溶液里溶质B的物质的量浓度为2mol/L?
(1) 从1L 2mol/LNaCl溶液取出一半。 √ (2) 将2molNaCl固体溶于1L的水中。 × (3) 将2molNaCl固体溶于水,形成1L溶液。 √ (4) 将80g的NaOH固体溶于1L水中。 ×
3. 100 mL0.5 mol/LMgCl2 溶液和 200 mL1 mol/LNaCl 溶液混合后
(忽略体积变化),溶液中Cl-的物质的量浓度为( C )
第二章 第三节 物质的量浓度(第3课时) 课件 高一化学人教版(2019)必修第一册

×100%
溶质质量+溶剂质量
要从质量分数为60%的NaCl溶液
60%
当中取出含有30g NaCl的溶液,需
要称取多少克溶液?
实验过程中,为了操作方便,取用溶液时, 一般量取它的体积,而不是称量其质量。
物质的量浓度
取用溶液时,更多的是量取溶液的体积。如果知道 每升溶液里所含溶质的物质的量,就可以快速的知道任 意体积溶液中溶质的物质的量了。
配制250mL 1.0mol/L H2SO4溶液,需要18mol/L H2SO4溶液的体积是多少?
(1)标准状况下,33.6L HCl 气体配成 0.5L 盐酸, 其物 质的量浓度为 3 mol/L。
(2)物质的量浓度为2mol/L的硫酸溶液500mL, 含硫酸的 物质的量为 1 mol 。
(3)10 mol HCl能配成 5 L 物质的量浓度为2mol/L的盐 酸。
体检的一些指标常用物质的量定义: 单位体积溶液里含有溶质B 的物质的 量,称为B的物质的量浓度。
即1L溶液中所含溶质B的物质的量
2. 符号: CB
3. 单位: mol / L 或 mol·L-1
4.
公式: CB =
nB V
物质的量浓度(mol/L)=
溶质的物质的量(mol) 溶液的体积(L)
离子物质的量浓度
1molMgCl2含有 1 molMg2+, 2 molCl【例】1mol/L MgCl2溶液,各微粒的物质的量浓度:
c(MgCl2) = 1 mol/L c(Mg2+) = 1 mol/L c(Cl-) = 2 mol/L
C(离子)=C(物质)×离子下标
【练习】 1. 0.5mol/L H2SO4,c(H1+m)=ol/L ;c(S0O.542m-)o=l_/L____ 2. 0.1mol/L Al2(SO4)3,c(Al03+.2)=mol/L ;c(SO0.432m-)=ol_/L__ 3. Na2CO3溶液中c(Na+)=2mol/L,c(Na2C1Om3)o=l_/L____
高一化学物质的量浓度

实验所需仪器
• 烧杯、容量瓶、玻璃棒、胶头滴管、托 盘天平、药匙(固体溶质使用)、量筒 (液体溶质使用)
新课标人教版课件系列
《高中化学》
必修1
化学计量在实验中的应用(3)
1.2.3《物质的量浓度》
教学目标
• 知识与能力 • 1、使学生理解物质的量浓度的概念,了解物质
的量浓度与质量分数的区别。 • 2、掌握配制一定物质的量浓度的溶液的方法。 • 重点、难点: • 1、物质的量浓度的概念、有关物质的量浓度的
简单计算 • 2、物质的量浓度与质量分数的区别 • 3、一定物质的量浓度的溶液的配制方法
1、什么叫溶液?溶液是由什么组成的?
一种或几种物质分散到另一种物质里 形成均一的、稳定的混合物,叫做溶 液。溶液由溶质和溶剂组成。 2、什么是溶液中溶质的质量分数?
溶质的质量分数=
溶质质量 溶液质量
×100%
一、物质的量浓度
二、一定物质的量浓度溶液的配制
在实验室用Na2CO3固体配制 500mL0.1mol/LNa2CO3溶液
∵n(Na2CO3)=c(Na2CO3) ×V[Na2CO3(aq)] =0.1mol/L×0.5L=0.05mol
∴m(Na2CO3)=n(Na2CO3) ×M(Na2CO3) =0.05mol×106g/mol=5.3g
误差分析及讨论
1、下列操作对实验结果有何影响(偏高、偏低、无 影响)?
称量时,Na2CO3固体与砝码的位置颠倒。
天平的砝码生锈。
高中一年级化学 物质的量浓度
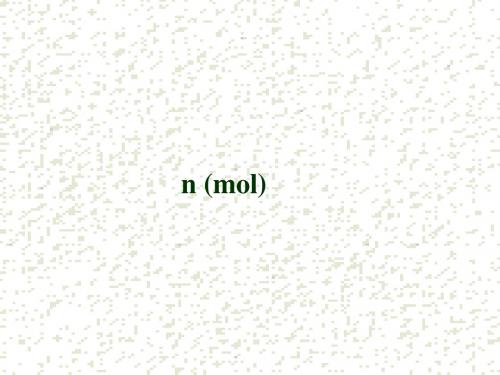
n = c. V
即c = n / V
N NA(mol-1)
m(g) M(g/mol)
n (mol)
V(L ) 22.4(L/mol)
c ( mol/L) . V (L )
§3 物质的量浓度
一、物质的量浓度 单位体积溶液里所含溶质的物质的量来 表示溶液组成的物理量。 单位是 mol/L 或者 mol/m3 , 用c表示。 二、关于物质的量浓度的计算 1、关于物质的量浓度概念的计算
V[NaCl(aq)]
=
0.4mol
0.25 L
= 1.6mol/L
练习2. 标况下44.8L HCl溶于水配 成500mL溶液。计算所得溶液中溶质的 物质的量浓度。
解:
n(HCl)
练习2. 标况下44.8L HCl溶于水配 成500mL溶液。计算所得溶液中溶质的 物质的量浓度。
解:
n(HCl) =
n(NaCl) =
=
= 0.4mol
c(NaCl) =
n(NaCl )
V[NaCl(aq)]
练习1 将23.4gNaCl溶于水,配成250mL溶
液。计算所得溶液中溶质的物质的量浓度。 解: m (NaCl) M (NaCl) 23.4g 58.5g/mol
n(NaCl) =
=
= 0.4mol
c(NaCl) =
V Vm
=
44.8L 22.4L/mol
=2mol
c (HCl) =
n
V
练习2. 标况下44.8L HCl溶于水配 成500mL溶液。计算所得溶液中溶质的 物质的量浓度。
解:
n(HCl) =
V Vm
=
44.8L 22.4L/mol
高一化学物质的量浓度3

高一化学知识点解读:物质的量浓度

第三节物质的量浓度1.相关溶液的知识网络2.溶液体积、密度、溶质质量分数之间的关系对于任意溶质B的水溶液,溶液体积V[B(aq)]、溶液密度ρ[B(aq)]和溶质质量分数w(B)之间的关系是:m[B(aq)]=V[B(aq)]×ρ[B(aq)]m(B)=m[B(aq)]×w(B)=V[B(aq)]×ρ[B(aq)]×w(B)3.一定溶质质量分数的溶液稀释的规律一定溶质质量分数的溶液,稀释前后,溶质质量保持不变。
设稀释前溶液的质量为m1、溶质质量分数为w1,稀释后溶液的质量为m2、溶质质量分数为w2,则:m1w1=m2w2课本知识导学使用课本知识诠解重要提示1.物质的量浓度(1)定义:以单位体积溶液里所含溶质B的物质的量来表示溶液组成的物理量叫做溶质B的物质的量浓度。
(2)公式:c(B)n(B)/V单位:mol·L B或mol·m-3(3)含义:在1L溶液中含有1mol的溶质,这种溶液中溶质的物质的量浓度就是1mol·L B。
2.一定物质的量浓度溶液的配制(1)常用仪器①配制中必须用到的仪器有容量瓶、烧杯、玻璃棒、胶头滴管,托盘天平或量筒。
②容量瓶是配制准确浓度的溶液的仪器,是细梨形、平底的玻璃瓶,瓶中配有磨口玻璃塞或塑料颈都有标线。
常用规格有50mL、100mL、250mL、500mL、1000mL等。
(2)天平的使用方法①称量前先把游码拨到标尺的零刻度处,检查天平的摆动是否平衡,如未达到平衡,能够调节左、右的平衡螺母,使天平平衡。
②在托盘天平两个盘上各放一张相同质量的纸,然后把要称量的药品放在纸上称量,潮湿的或具有腐蚀性的药品必须放在玻璃器皿里称量。
③称量物放在左盘,砝码要用镊子夹取,先加质量大的砝码,再加质量小的砝码,最后移动游码。
④称量完毕应把砝码放回砝码盒中,把游码移回零刻度处。
(3)物质的量浓度溶液的配制①操作步骤:a.计算→计算所需溶质的质量或体积。
物质的量浓度课件-高一化学人教版(2019)必修第一册

实验目的
练习容量瓶的使用方法 练习配制一定物质的量浓度的溶液 加深对物质的量浓度概念的认识
实验用品
烧杯、容量瓶(100mL)、胶头滴管、量简、玻璃棒、药匙、滤纸、天平、 NaCI、蒸馏水。
烧杯 容量瓶(100mL) 胶头滴管 量简 玻璃棒 药匙 托盘天平
实验用品
配制一定物质的量浓度溶液专用仪器——容量瓶 (1)容量瓶的结构与规格
1、定义: 以单位体积溶液里所含溶质B的物质的量来表 示溶液组成的物理量,叫做溶质B的物质的量浓度。
2、符号:cB 34、、表单达位式:m:olc/B L=(mnVoBl∙L-1)
V是指溶液的体积,单位为L; n是指溶质的物质的量,单位为mol; c是指溶质的物质的量浓度,单位为mol/L。
物质的量浓度
②药品中含有杂质
③容量瓶内有蒸馏水
误差分析
3.定容时仰视、俯视的误差分析 分析定容时俯视、仰视对结果的影响时
要确保按眼睛视线→刻度线→凹液面最低点的次序,做到“三点一线”。
仰视液面高于刻度线
仰视刻度线, 导致溶液体积偏大,
浓度偏小
俯视液面低于刻度线
俯视刻度线 导致溶液体积偏小
浓度偏大
1.用“偏大”“偏小”或“无影响”填空
不可以
可以将过冷或过热的溶液转 移到容量瓶中吗?
实验用品
配制一定物质的量浓度溶液专用仪器——容量瓶
选择容量瓶应遵循 “大而近”的原则:所 配溶液的体积等于或 略小于容量瓶的容积
我该如何选择容量瓶的规格?
使用前还有需 要注意的吗?
使用前需要检 验是否漏水。
那怎样检漏呢?
实验用品
配制一定物质的量浓度溶液专用仪器——容量瓶 (2)容量瓶使用前检查是否漏水的方法
高一化学必修1第一章第二节 物质的量浓度

思考:为何不直接在容量瓶中溶解?
物质溶解时常伴有放热吸热现象,使容量瓶体 积不准。
二、一定物质的量浓度的溶液的配制:
步 骤 1.计算 2.称量 3.溶解
配制250mL 0.5mol•L-1的NaCl溶液 仪器: 一定要指明容量瓶的规格
250ml容量 瓶、 烧杯、玻璃棒
转移时:
4.转移
注 意 事 项
1.溶液要先冷却至室温; 2.要用玻璃棒引流,避免液体洒在瓶外。
思考:如果液体洒在瓶外对浓度有怎样的影响?
溶质的质量减少,浓度偏低。
二、一定物质的量浓度的溶液的配制:
步 骤
配制250mL 0.5mol•L-1的NaCl溶液
1.计算 2.称量 3.溶解
4.转移 5.洗涤
洗涤时:
注 意 事 项
1、用少量蒸馏水洗涤 烧杯和玻璃棒2-3次;
6.有关溶液反应的计算
1 . 中 和 1 升 0.5 mol/LnaOH 溶 液 , 需 要 多 少 升 1 mol/LH2SO4溶液?
2.中和50mL 2 mol/LHNO3溶液共用去了NaOH溶液 80mL ,求此 NaOH 溶液的物质的量浓度和溶质的质 量分数。(NaOH溶液的密度为1.05g/mL)
1 、 0.5mol/L 的 NaCl 溶液 250mL ,所含 的溶质的质量是多少克?物质的量是 多少?溶质的微粒数分别是多少? 2、2L 1mol/L的H2SO4溶液,含溶质的 物质的量为 mol,含H+ 个,SO42个。 3、浓度为1mol/L的酒精(难电离)和 硫酸铝溶液(完全电离)各1L ,求它 们溶液中含溶质微粒各是多少?
南 京 市 鼓 楼 医 院 检验报告单 检验编号 南京大学医学院附属鼓楼医院
2.3.3物质的量浓度课件高一上学期化学人教版

第3课时 物质的量浓度
导入
实验中总会接触到各种形态的化学物质。它们有的是固态的,有 的是气态的,有的是液态的。
氯化钠固体
盐酸溶液
氨气
导入 在实验中,根据需求不同,我们会选用不同浓度的溶液。例如:
用浓硫酸充当吸水剂,用稀硫酸做反应物。
怎么区分“浓”和“稀” 呢?
提示:可以先通过物质的量浓度的定义,根据nB = cB·V,求得NaOH的物质的量。然后通过质量与物质的 量的关系,根据m = n·M,求得NaOH的质量。
[练习1]
判断题:
(1)将1gNaCl溶于水制成1L溶液 ,则c=1mol/L ; ( x ) (2)将1molNaCl溶于1L水中,则c=1mol/L; ( x )
一、物质的量浓度
(1)定义:表示单位体积(1L)溶液里所含溶质B的物质的量, 叫做B的物质的量浓度。
(2)公式:CB=
如果1L溶液中含有1mol溶质,这种溶液中溶质 的物质的量浓度就是1mol/L。
(3)单位:
nB: mol V: L 溶液的总体积
CB: mol/L
思考·讨论 配制500mL0.1mol/L的NaOH溶液,需要NaOH的质 量是多少?
保证溶质全部转入容量瓶中
只要加入的洗涤液液面不超过容量瓶刻度线, 就没有影响
浓溶液配制稀溶液 在化学实验中我们经常使用的是溶液,如
1mol/L的盐酸溶液。若要配制250mL这种盐酸溶液, 需要12mol/L的HCl溶液多少毫升?
原则:溶液在稀释前后,溶质的质量或物质的量保持不变。
C(浓溶液) ·V(浓溶液)= C(稀溶液) ·V(稀溶液)
实验目的:精确地配置100mL1.00mol/L的NaCl溶液
高一化学-第三节物质的量浓度 最新

二.溶液的配制
2.配一定物质的量浓度的溶液
1)仪器:
2)步骤: 计算:算出固体溶质的质量或液体溶质的体积。 称量:用天平称取固体溶质质量,用量简量取所需液体溶质的体积。 溶解:将固体或液体溶质倒入烧杯中,加入适量的蒸馏水(约为所 配溶液体积的 1/6 ),用玻璃棒搅拌使之溶解,冷却到室温后,将 溶液引流注入容量瓶里。 洗涤、定容:用适量蒸馏水将烧杯及玻璃棒洗涤 2-3次,将洗涤液 注入容量瓶。振荡,使溶液混合均匀,然后继续往容量瓶中小心地 加水,直到液面接近刻度 1 - 2m处,改用胶头滴管加水,使溶液凹 面恰好与刻度相切。把容量瓶盖紧,再振荡摇匀。 摇匀、转移
1)用量筒取液体试剂时,洗量筒的液体不能再 倒入烧杯中 2)烧杯及玻璃棒的洗涤液要倒入容量瓶中 3)在液面接近容量瓶的刻度线2—3cm时,应 改用胶头滴管 4)读数时,视线应与溶液的凹液面恰好相切 V1读数偏大 5)容量瓶是配制溶液的容器,不是装试剂用的 V2正确读数 6)若用浓硫酸配制稀硫酸时,一定要注意将浓 V3读数偏小 硫酸慢慢用玻璃棒引流到水中。切不可相反操 作!
二.溶液的配制
实验室需要480mL0.1mol/L的硫酸铜溶液。以下操作正确 的是( D ) A .称取7.68g硫酸铜,加入500mL水 B .称取12 .0g胆矾配成500mL溶液 C .称取8 .0g硫酸铜,加入500mL水 D .称取12 .5g胆矾配成500mL溶液
★一定物质的量浓度溶液的配制注意事项
★容量瓶的使用
检查容量瓶是否漏水的方法:
往瓶内加入一定量水,塞好瓶塞。用食指摁住瓶塞,另一只手托住 瓶底,把瓶倒立过来,观察瓶塞周围是否有水漏出。如果不漏水, 将瓶正立并将瓶塞旋转180O后塞紧,仍把瓶倒立过来,再检查是否 漏水。
高中化学第三节物质的量第3课时物质的量浓度课件新人教版必修第一册

1 mol
特别提醒
对物质的量浓度的理解 (1)溶质用物质的量表示,而不是质量,如给出溶质的质量或气体的 体积时,要换算成物质的量。 (2)“溶质”指溶液中的溶质,可以指化合物也可以指离子或其他特 定 组 合 , 分 析 溶 质 时 要 注 意 有 关 变 化 。 如 : Na 、 Na2O 、 Na2O2 H2O NaOH,溶液中的溶质都是NaOH。 (3)表达式中“V”指溶液的体积,不是溶剂的体积,也不是溶质体积 和溶剂体积之和,要根据混合后溶液的密度计算溶液体积。V的单位 是升(L)。 (4)溶质的物质的量浓度是溶液的固有属性之一,当从一定物质的量 浓度的溶液中取出任意体积的溶液时,其物质的量浓度、密度、质量 分数不变,但随溶液体积的变化,溶质的质量、物质的量不同。
第3课时 物质的量浓度
学业基础 学考评价
核心素养
核心微网络
素养新要求
1. 认识物质的量浓度的含义。 2.学会物质的量浓度的简单计算方法。 3.学会配制一定物质的量浓度的溶液。 4.了解并应用浓溶液稀释的计算原理。
学业基础
一、物质的量浓度
单位体积
物质的量
cB
mol·L-1 nB V
mol/L
核心素养
目标1 物质的量浓度的基本计算和判断 例1 下列溶液中物质的量浓度为1 mol·L-1的是( ) A.将40 g NaOH溶解在1 L水中 B.将22.4 L HCl气体溶于水配成1 L溶液 C.将1 L 10 mol·L-1浓盐酸加入9 L水中 D.将10 g NaOH溶解在少量水中,再加蒸馏水直到溶液体积为250
A.硫酸铜的物质的量为0.5 mol B.溶于500 mL水中 C.溶解后溶液的总体积为500 mL D.溶解后溶液的总体积为1 L
高一化学物质的量浓度

0. 2
选择
下列各溶液中,Na+ 浓度最大的是 ( B )
(A)4L 0. 5 mol/L NaCl 溶液 C (Na+) = 0. 5 mol/L×1 = 0. 5 mol/L (B)1L 0. 3 mol/L Na2SO4 溶液 C (Na+) = 0. 3 mol/L×2 = 0. 6 mol/L
步 骤
配制500mL 0.2mol•L-1的NaCl溶液
1.计算 2.称量 3.溶解 4.转移 1. 溶液要先冷却至 室温 2. 要用玻璃棒引流
容量瓶 1. 构造:梨形、细颈、磨口、平底 2. 特点: ①标明温度和容积
②有不同规格(100mL、250mL、 500mL、1000mL等) ③容量瓶上只有一条刻线而无 刻度
别取出100mL、50mL、20mL,所取 出溶液的物质的量浓度分别是多少? 所含溶质的物质的量又是多少? 都是1mol/L 0.1mol 0.05mol 0.02mol
练习二 . 请计算
溶质
80g NaOH
V(aq) 1L
C(mol/L) 2 2 1 0.2
98g H2SO4
11.7g NaCl 1.12 ____ L HCl ( 标准状况下)
小结:容量瓶的使用六忌
一忌用容量瓶进行溶解(体积不准确) 二忌直接往容量瓶倒液(洒到外面) 三忌加水超过刻度线(浓度偏小) 四忌读数仰视或俯视(仰视浓度偏小, 俯视浓度偏大) 五忌不洗涤玻璃棒和烧杯(浓度偏小) 六忌配制好的溶液存放于容量瓶中(容量 瓶是量器,不是容器)
练习 2
用18 mol/L 硫酸配制 100 mL 1.0mol/L 硫酸,若实验仪 器有
2023年高一化学教案物质的量的浓度[第二、三课时](精选3篇)
](https://img.taocdn.com/s3/m/e2df7eb6f71fb7360b4c2e3f5727a5e9856a270a.png)
2023年高一化学教案物质的量的浓度[第二、三课时](精选3篇)第二课时:物质的量的浓度的计算公式和单位知识目标:1. 理解物质的量的浓度的概念;2. 掌握物质的量的浓度的计算公式;3. 了解物质的量的浓度的常用单位。
教学过程:一、复习通过回顾前一课时的学习内容,检查学生对物质的量的概念的理解情况。
二、引入1. 向学生展示一个饮料瓶,问:“你们喝的饮料瓶上都印有信息如何‘每100ml含糖量12g’,那这些数据是什么意思呢?”2. 引导学生思考,解释物质的量的浓度的概念。
三、讲解1. 讲解物质的量的浓度的计算公式:浓度=溶质的物质的量/溶液的体积。
2. 介绍物质的量的浓度的常用单位:mol/L,简写为mol/L或M。
四、实例演练通过几个实例演练,让学生掌握物质的量的浓度的计算方法和单位。
五、拓展通过举例介绍如何计算稀释溶液的浓度,拓展学生的知识。
六、归纳总结让学生总结物质的量的浓度的计算公式和单位,并写在笔记本上。
作业:完成课堂上的实例演练,做好笔记。
第三课时:物质的量的浓度的实验测定知识目标:1. 了解物质的量的浓度的实验测定方法;2. 掌握使用容量瓶和量筒等实验仪器进行物质的量的浓度的实验测定;3. 练习物质的量的浓度的实验设计。
教学过程:一、引入1. 让学生观察两瓶溶液,一瓶是稀释的酸溶液,另一瓶是浓缩的酸溶液,问:“如何通过实验测定这两瓶溶液的物质的量的浓度?”2. 引导学生思考,激发学生的学习兴趣。
二、讲解1. 讲解物质的量的浓度的实验测定方法:通过实验仪器测量溶质的质量和溶液的体积,计算物质的量的浓度。
2. 介绍使用容量瓶和量筒等实验仪器进行物质的量的浓度的实验测定的步骤和注意事项。
三、演示实验通过演示实验,展示使用容量瓶和量筒等实验仪器进行物质的量的浓度的实验测定的过程。
四、实验设计让学生设计一个实验,通过实验测定一个未知溶液的物质的量的浓度。
五、实验操作让学生进行实验操作,完成实验测定未知溶液的物质的量的浓度。
1.3.3物质的量浓度+课件2024-2025学年高一化学上学期鲁科版(2019)必修第一册

2.选择什么量器准确加水至100mL?
配置一定物质的量浓度的溶液
如何配置100mL0.4mol·L-1的氯化钠溶液?
➢ 溶质质量:2.34g ➢ 溶液体积100mL ➢ 实验仪器
100mL容量瓶
容量瓶是细颈、梨形的平底玻 璃瓶,瓶口配有磨口玻璃塞或 塑料塞,使用前要检漏 容量瓶上标有温度和容积,表 示在所指温度下瓶内液体的凹 液面与容量瓶颈部的刻度线相 切时,液体体积恰好与瓶上标 注的容积相等 容 量 瓶 规 格 有 100mL 、 250mL 、 500mL、1000mL
Na2SO4的物质的量是__2____mol,Na+的物质的量是__4___mol ③若氯化镁MgCl2溶液中Mg2+浓度为0.4mol·L-1,则溶液中Cl-浓度为_0_.8__mol·L-1
物质的量浓度及其计算
下列溶液中Cl-浓度最大的是( B )
A.0.5mol·L-1氯化镁MgCl2溶液 B.0.4mol·L-1氯化铁FeCl3溶液 C.0.8mol·L-1氯化钠NaCl溶液 D.0.5mol·L-1氯化氢HCl溶液
配置一定物质的量浓度的溶液
3.计算
求溶液浓度:浓度=
溶质质量 相对质量 × 溶液体积
需要把体积单位换成 L .
所需NaOH质量:m=浓度 × 体积 × 相对分子质量
所需浓硫酸体积:浓度1 × 体积1=浓度2 × 体积2
不需要单位换算
需要把体积单位换成 L .
配置一定物质的量浓度的溶液
思考 1. 配制100mL物质的量浓度为0.5mol·L-1的NaOH溶液,需要溶 质的质量为____________g
2.3.3 物质的量浓度-高一化学课件(人教版2019必修第一册)

物质的量浓度到底有什么意义?
65g 98g
微观 1mol 1mol
161g 2g 1mol 1mol
cB
1.将1gNaCl溶于水制成1L溶液,则c(NaCl)=1mol·L-1 溶质用物质的量表示,不是用质量表示。
2.将1molNaCl溶于1L水制成溶液,则c(NaCl)=1mol·L-1 V是溶液的体积,不是溶剂的体积。
度为1mol·L-1。
(__X_____)
“溶液体积不是溶剂体积”: 58.5gNaCl的物质的量为1mol,但溶于1L水后的
溶液体积不是1L,故浓度不是1mol·L-1
在200ml的稀盐酸里溶有0.73gHCl,试计算溶液的物质的 量浓度是多少?
由公式:cB = nB/V nB = mB/MB
cB = nB/V=
0.02mol 0.2L
-1 =0.1mol·L
8gCuSO4可配制成0.2mol·L-1CuSO4溶液多少毫升?
我两个手举栗子
由公式:cB = nB/V nB = mB/MB
0.05mol
V = nB/cB= 0.2mol·L-1 =0.25L=250mL
把22.4L(标况下)HCl气体溶解在水中配成2LHCl溶液, 此时盐酸的物质的量浓度为多少?
由公式:cB = nB/V nB = V/Vm
1mol
cB = nB/V= 2L
-1 =0.5mol·L
实验室里有一瓶浓度为98%的浓硫酸,其密度 为1.84g/mL,化学老师要制作一个新的标签, 用物质的量浓度来表示这瓶浓硫酸溶液的组成, 同学们知道该怎么写吗?
单位换算
密度ρ=1.84g/mL
1.NA表示阿伏加德罗常数的值。下列有关1mol HCl的说法正确的是A.质C 量
高一化学必修1:物质的量浓度

高一化学必修1:物质的量浓度今天小编给大家讲讲高一化学必修1:物质的量浓度,希望可以帮助到大家。
【知识梳理】一、物质的量浓度概念1、物质的量浓度:从单位体积的溶液里所含溶质B的物质的量来表示溶液组成的物理量叫做溶质B的物质的量浓度。
符号为c(B),单位有mol/L(或mol·L―1)等。
注意:(1)溶质可以是物质,也可以是分子或离子。
(2)溶质是用物质的量表示而不是质量表示;体积表示溶液的体积,而不表示溶剂的体积,并且体积单位为L。
(3)溶液具有均一性,即从一定物质的量浓度的溶液中取出任意体积的溶液,物质的量浓度保持不变,但随溶液体积的变化溶质的物质的量不同。
(4)带结晶水的物质溶于水后,溶质是不含结晶水的化合物,溶剂中的水包括结晶水。
2、溶质的物质的量(n)、溶液的物质的量浓度、溶液的体积三者关系3、N、m、V(气体)、cB之间的转换关系:二、物质的量浓度与溶液溶质的质量分数内容物质的量浓度质量分数定义以单位体积溶液里含有溶质的物质的量来表示溶液组成用溶质质量与溶液质量之比来表示溶液组成溶质的单位mol g溶液的单位L g计算公式物质的量浓度(mol·L-1)=质量分数=特点体积相同,物质的量浓度也相同的任何溶液里含有溶质的物质的量相同质量相同,溶质的质量分数也相同的任何溶液里含有溶质的质量相同两者的关系总结:物质的量浓度与溶质质量分数的换算:(w为溶质质量分数)三、一定物质的量浓度溶液配制(一)容量瓶的使用及注意事项实验室配制一定物质的量浓度的溶液一般用容量瓶。
比较常用的容量瓶的规格有100 mL、250 mL、500 mL和l 000 mL。
1.容量瓶为细颈、梨形玻璃容器,带有磨口玻璃塞。
容量瓶瓶口配有磨口玻璃塞或橡胶塞。
容量瓶上标有刻度线、适用温度、容量。
使用前一定要检查容量瓶是否漏液,方法是:向瓶内加一定量水,塞好瓶塞,用左手食指顶住瓶塞,右手托住瓶底,将容量瓶倒置,看是否有水漏出。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
