各医疗机构药品生产经营企业001
Q001医院安全生产事故隐患排查指引
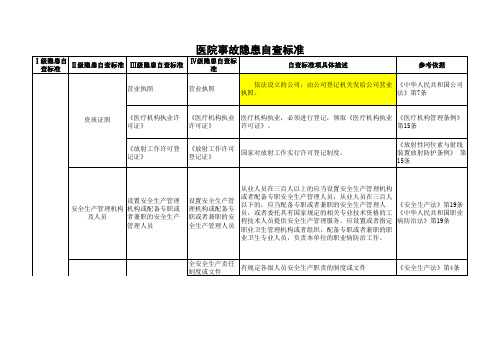
基础管理
职业病防治计划及 实施方案
职业病防治计划 及实施方案
应当制定职业病防治计划或实施方案。
《中华人民共和国职业 病防治法》第19条
职业卫生管理制度 或操作规程
职业卫生管理制 度或操作规程
应建立健全职业卫生管理制度或操作规程:1、职业 危害防治责任制度;2、职业危害告知制度;3、职业 危害申报制度;4、职业健康宣传教育培训制度;5、 《中华人民共和国职业 职业危害防护设施维护检修制度;6、从业人员防护 病防治法》第19条,《 用品管理制度;7、职业危害日常监测管理制度;8、 作业场所职业健康监督 从业人员职业健康监护档案管理制度;9、岗位职业 管理暂行规定》第11条 健康操作规程;10、法律、法规、规章规定的其他职 业危害防治制度。
意识和应急措施、自救互救知识;(六)生产安全事故
案例。
专业培训
专业培训
对从事医疗废物分类收集、运送、暂时贮存、处置等 工作的人员和管理人员,进行相关法律和专业技术、 安全防护以及紧急处理等知识的培训。
《医疗卫生机构医疗废 物管理办法》第29条
生产经营单位的特种作业人员必须按照国家有关规定
特种作业人员培训
《安全生产法》第17 条; 《生产安全事故应急预 案管理办法》(安监总 局第17号令)第七条
专项应急预案和现场处置方案。
应急预案
应急救援
应急救援组织
应急保障
中央管理的总公司的综合应急预案和专项应急预案,
报国务院国有资产监督管理部门、国务院安全生产监
应急救援预案备 督管理部门和国务院有关主管部门备案;其所属单位 《生产安全事故应急预
安全生产规章制度至少应包含下列内容:安全生产职
责、安全生产投入、文件和档案管理、隐患排查与治 理、安全教育培训、特种作业人员管理、设备设施安 全管理、建设项目安全设施“三同时”管理、生产设 备设施验收管理、生产设备设施报废管理、施工和检
药品质量管理制度文件模板

编号:QMS-001起草部门:质量管理部起草人:[起草人姓名]审阅人:[审阅人姓名]起草日期:[日期]批准日期:[日期]执行日期:[日期]一、总则为加强本企业药品质量管理,确保药品质量符合国家相关法规和标准,保障人民群众用药安全,特制定本制度。
二、适用范围本制度适用于本企业所有药品的生产、储存、销售、配送、使用等环节。
三、职责与权限1. 质量管理部:- 负责制定和实施药品质量管理制度;- 负责组织质量管理体系的建设和运行;- 负责对药品质量进行监督、检查和考核;- 负责对不合格药品进行处理。
2. 生产部门:- 负责按照GMP要求进行生产,确保生产过程符合药品质量标准;- 负责对生产设备进行定期维护和保养;- 负责对生产人员进行质量培训。
3. 储存部门:- 负责按照GSP要求进行药品储存,确保药品储存环境符合要求;- 负责对储存药品进行定期检查和维护;- 负责对过期、变质、失效的药品进行处理。
4. 销售部门:- 负责按照药品经营质量管理规范进行销售,确保销售药品质量;- 负责对销售人员进行质量培训;- 负责对销售药品进行追溯管理。
5. 其他部门:- 负责按照本制度要求,配合质量管理部做好药品质量管理相关工作。
四、质量管理要求1. 药品生产:- 严格执行GMP,确保生产过程符合药品质量标准;- 对生产设备和工艺进行定期验证和确认;- 对生产人员进行质量培训。
2. 药品储存:- 严格执行GSP,确保药品储存环境符合要求;- 对储存药品进行定期检查和维护;- 对过期、变质、失效的药品进行处理。
3. 药品销售:- 严格执行药品经营质量管理规范,确保销售药品质量;- 对销售人员进行质量培训;- 对销售药品进行追溯管理。
4. 药品使用:- 医疗机构应当严格按照药品说明书和处方使用药品;- 定期对医务人员进行药品使用培训。
五、监督检查1. 质量管理部门定期对各部门的药品质量管理进行监督检查;2. 对检查中发现的问题,及时提出整改措施,并跟踪整改效果;3. 对违反本制度的行为,依法进行处理。
G001企业标准化管理规定

Q/CS赤山集团有限公司企业标准企业标准化管理办法企业标准化管理规定赤山集团有限公司发布前言本标准按照GB/T 1.1-2000、GB/T 15496-2003和《企业标准化管理办法》的要求而制订的。
本标准的附录A、附录B为资料性附录。
本标准由赤山集团有限公司提出并起草。
本标准主要起草人:孙述良、周洪刚、赵学文。
本标准自发布之日起实施。
企业标准化管理办法企业标准化管理规定1 范围本标准规定了企业标准化工作的基本要求与任务,标准化机构、人员素质与职责、企业标准化规划与计划的管理、企业标准的制修订管理、企业标准体系总要求、贯彻实施各级标准的管理、标准实施监督检查的管理、标准及标准化信息资料的管理、企业标准化人员培训的管理、采用国际标准工作的管理、企业标准化成果的管理等规定。
本标准适用于赤山集团总公司及下属各公司的企业标准化工作管理。
2 规范性引用文件下列文件中的条款通过本标准的引用而成为本标准的条款。
凡是注日期的引用文件,其随后所有的修改单或修订版均不适用于本标准,凡是不注日期的引用文件,其最新版本适用于本标准。
GB/T 1.1 标准化工作导则第1部分:标准的结构和编写规则GB/T 15496-2003 企业标准体系要求GB/T 15497-2003 企业标准体系技术标准体系的构成和要求GB/T 15498-2003 企业标准体系管理标准工作标准体系的构成和要求GB/T 19273-2003 企业标准体系评价与改进Q/G CS 002 企业标准化管理办法企业标准体系表与企业标准体系的构成和编制要求Q/G CS 003 企业标准化管理办法企业技术标准体系与技术标准制修订管理标准Q/G CS 004 企业标准化管理办法管理标准体系与管理标准制修订管理标准Q/G CS 005 企业标准化管理办法工作标准体系与工作标准制修订管理标准Q/G CS 006 企业标准化管理办法企业标准体系自我评价与改进3 企业标准化工作的基本要求与任务3.1 企业标准化工作的基本要求企业标准化是企业科学管理的基础,每个企业的生产都与外部环境有着密切的联系,并存在许多影响企业生产经营管理的约束条件,而在企业内部各部门、各环节之间又是一个相互依存、相互制约有机整体。
药品经营许可证号九位编码

药品经营许可证号九位编码
摘要:
一、药品经营许可证的概述
二、药品经营许可证的九位编码含义
三、九位编码在日常经营中的应用
四、合规经营的重要性
正文:
一、药品经营许可证的概述
药品经营许可证是我国食品药品监督管理局对药品经营企业进行监管的重要手段。
药品经营企业必须依法取得药品经营许可证,才能从事药品经营活动。
许可证的颁发旨在保障公众用药安全,维护药品市场秩序。
二、药品经营许可证的九位编码含义
药品经营许可证号九位编码是药品经营许可证的一个重要组成部分,它由两部分组成:
1.企业许可证号:前四位代表企业所在地的行政区划代码,如“110105”代表北京市东城区。
2.企业登记号:后五位为企业登记号,它是药品经营企业在国家工商行政管理部门登记的唯一标识。
三、九位编码在日常经营中的应用
药品经营企业在日常经营中,应将药品经营许可证号九位编码置于企业经营场所显著位置,以便监管部门进行检查。
同时,企业在进行药品采购、销售
等业务操作时,也需要提供许可证号九位编码,以确保药品的合法流通。
四、合规经营的重要性
药品经营企业在经营过程中,应严格遵守国家法律法规,确保药品的质量和安全。
合规经营不仅有助于企业规避法律风险,还能为企业树立良好的口碑,促进业务的可持续发展。
总之,药品经营许可证号九位编码是药品经营企业合规经营的重要依据。
企业应了解其含义及应用,确保在日常经营中合规操作,为公众提供安全、有效的药品。
药品生产企业管理文件 SMP-QC-001-02 实验室安全、卫生行为管理规程

目录1.目的 (2)2.范围 (2)3.职责 (2)4.内容 (2)5.相关程序、记录,附件 (4)6.参考资料 (4)7. 历史和修订记载 (4)1.目的:明确实验室的安全、卫生管理办法及卫生要求和人员行为规范,防止事故的发生,保证实验室的管理处于可控状态,从而避免造成公司财产损失和人员伤害以及保证其质量检验工作的正常进行。
2.范围:适用于公司质量管理部所有实验室,包括仪器实验室、理化检验室、试剂间、留样室等。
3.职责:3.1质量管理部QC负责本规程的制定和执行;3.2质量管理部QA负责监督本规程的执行。
4.内容:4.1实验室安全管理4.1.1实验室、试剂间内严禁吸烟、禁止明火。
4.1.2实验操作室内不可存放大量的化学危险品,如较大量的低沸点试剂和易燃易爆溶剂。
4.1.3专门放置易燃易爆物品的房间内不能有煤气嘴、洒精灯以及有电火花产生的任何电气设备,室内应通风。
4.1.4使用易燃试剂或进行产生有毒有害气体的实验时必须在不燃结构的通风橱内进行。
严禁靠近火,以免发生危险。
4.1.5易挥发、有毒、有害试剂必须封好口,置凉暗处保存。
4.1.6试剂间内不准进行实验工作,不得穿带钉子的鞋入内。
4.1.7毒剧品应放在保险柜中,双人分别保管钥匙和密码。
4.1.8检查电器设备必须使用专用设备和电笔,不得用水和湿布洗擦电器设备。
4.1.9试剂间内必须避免产生电火花,所有电气开关、电插座必须密封,使电火花与外部空气隔绝。
4.1.10冰箱内不准存放无盖的试剂、试药。
4.1.11实验室内应备有救火用的消防器材。
4.1.12日光能直射进房间的实验室、留样室内等必须备有窗帘,日光能照射的区域内不宜放置加热时易着火的一切物质,也不要放置受热时易挥发的物质。
4.1.13灭火器等消防设施一般应装在实验室门口外附近处,便于取用。
4.1.14压力容器严禁带压操作。
操作过程中应专人看管,排压后方可开锅(门)。
4.1.15试剂应由专人保管,保管员须经常检查存放在试剂间的试剂情况,发现泄漏及时处理;废旧包装不得在房内堆放。
药品经营企业GSP认证问题解答[001]
![药品经营企业GSP认证问题解答[001]](https://img.taocdn.com/s3/m/6003536769eae009581bec35.png)
药品经营企业GSP认证问题解答1、《药品经营质量管理规范》的依据是什么?答:制定《规范》的依据是《中华人民共和国药品管理法》、《中华人民共和国药品管理法实施条件》。
2、《药品经营质量管理规范》的适用范围是什么?答:《规范》中第三条已明确,除药品经营企业外,药品生产企业销售药品、药品流通过程中其他涉及储存与运输药品的,也应符合《规范》要求。
3、企业的认证申请资料或现场检查中发现有弄虚作假的行为该如何处理?答:如发现企业存在虚假行为,可直接判定该企业不符合本规范的要求。
4、质量管理体系内审应多久进行一次?答:企业质量管理体系的内审一般分为定期内审(建议每年度进行一次)和有因内审(即关键要素发生重大变化,包括:重大政策出台、企业股权变动、仓库变更、增加经营范围、因药品质量原因发生质量事故等情况)。
企业应根据规范和企业有关制度要求开展内审。
5、企业的法定代表人、企业负责人、质量负责人能否由同一人担任?答:不能。
批发、零售连锁企业总部的法定代表人、企业负责人可为同一人,但质量负责人必须单独设置,不得兼职其他岗位,保证相互监督和制约。
6、质量负责人能否兼任质量管理部门负责人?答:批发、零售连锁企业总部的质量负责人不得兼任质量管理部门负责人。
7、企业的质量管理部门是否必须设置质量管理部门负责人、质管员、验收员这三个岗位?答:是的。
但小型企业的质量管理部门负责人可兼任质管员。
8、委托药品现代物流企业存储药品的企业,质量管理部门是否还需设验收员的岗位?答:如企业在经营过程中有发生直调行为的,必须由本企业验收员负责直调的验收工作或者委托验收。
9、具有特殊管理药品经营范围的企业,是否需设置两名验收员?答:特殊管理药品要求双人验收,故须设一名验收员,一名验收复核员。
10、在新规范中对质量管理员资格要求中“相关专业”指的是哪些专业?答:“相关专业”指的是条款中所叙述的“药学或者医学、生物、化学”等专业。
验收员、养护员、采购员的专业要求同上。
药品生产企业管理文件 SMP-WJ-001-03 GMP文件管理规程

目录1.目的 (2)2.范围 (2)3.职责 (2)4.内容 (2)4.1 定义及术语 (2)4.2 文件管理流程图: (2)4.3具体内容 (3)4.4注意事项 (8)5.相关程序、记录,附件 (8)6.参考资料 (13)7.历史和修订记载 (13)1.目的:明确公司所有GMP文件的管理。
2.范围:适用于公司的所有GMP文件的起草、修订、审核、批准、复制、发放、撤销、定期审核、收回、销毁、保管等工作。
3.职责:3.1 质量管理部:负责与质量管理相关文件的起草、修订及其他GMP文件审核、批准、复制发放、撤销、定期审核、收回、销毁、执行、保管等工作;3.2 其他各部门负责本部门GMP文件的起草、修订、审核、定期审核、现行文件执行、保管等工作;4.内容:4.1 定义及术语4.1.1 文件:是指一切涉及药品生产及销售管理的书面标准和实施中的记录结果。
文件管理:文件管理是指文件的设计、制订、审核、批准、复制、分发、培训、执行、归档、变更、保存和销毁的一系列过程的管理活动。
4.1.2 修订版本号:对文件的部分内容进行修订并用两位阿拉伯数字表示,新文件修订版本号为00,首次修订为01,以后修订依次为 02、03……99依次顺延;修订版本号4.2 文件管理流程图:职责流程派生记录相关人员相关人员相关人员相关人员文件管理QA各相关部门各相关部门4.3具体内容4.3.1文件的起草/修订、审核、批准、发放、生效管理4.3.1.1文件的起草/修订、审核、批准权限,文件由单人起草、多人审核(所涉及部门)、单人批准。
4.3.1.1.1管理文件的起草/修订、审核、批准权限机构与人员文件:由行政部指定专人起草,行政部负责人及质量保证部审核,总经理批准;厂房与设施文件:由生产部指定专人起草,生产部负责人审核后交质量管理部审核,生产负责人批准;设备文件:由生产部指定专人起草,生产部审核后交质量管理部审核,生产负责人批准;物料与产品文件:由仓储部指定专人起草,仓储部负责人审核后交质量保证部审核,由质量负责人批准;确认与验证文件:由质量保证部指定专人起草,生产部审核后交质量管理部审核,质量负责人批准;文件管理文件:由质量保证部指定专人起草,QA主管及质量管理部负责人共同审核,质量负责人批准;生产管理文件:由生产部指定专人起草,生产部审核后交质量管理部审核,生产负责人批准;质量管理文件:由质量保证部指定专人起草,QA主管及质量管理部负责人审核,质量负责人批准;质量保证文件:由质量保证部指定专人起草,QA主管及质量管理部负责人共同审核,质量负责人批准;质量控制文件:由质量控制部指定专人起草,QC主管及质量管理部共同审核,质量负责人批准;委托生产与委托检验文件:由质量保证部指定专人起草,QA主管及质量管理部负责人共同审核,质量负责人批准;产品发运与召回文件:由销售部或质量保证部指定专人起草,销售部、QA主管共同审核,质量负责人批准;4.3.1.1.2技术规程的起草/修订、审核、批准权限质量标准:由质量控制部指定专人起草,质量控制部、质量管理部共同审核,质量受权人批准;工艺规程:由生产部岗位指定专人起草,生产部、质量保证部共同审核,质量负责人批准;4.3.1.1.3操作规程的起草/修订、审核、批准权限操作规程(SOP)、记录、标签:各部门指定专人起草,部门负责人和质量管理部共同审核,生产部或质量管理部批准;4.3.1.1.4批记录的起草/修订、审核、批准权限批生产记录、批包装记录:车间起草,生产部、质量管理部共同审核,质量负责人批准;批检验记录:质量控制部起草,质量保证部、质量管理部负责共同审核,质量负责人批准。
《新药品管理法》考试试题及答案 试卷编号ypglf-001

《新药品管理法》考试试题试卷编号ypglf-001 姓名:岗位:评分:说明:本试卷满分为100分一、单选题(共9题,每题4分,共36分)1.新《药品管理法》实施时间是()。
A、2020.01.01B、2019.12.12C、2015.03.01D、2019.12.012.对假劣药违法行为责任人的资格罚由十年禁业提高到( ),对生产销售假药被吊销许可证的企业,十年内不受理相应申请。
A、终身禁业B、刑事处罚C、民事处罚D、三十年禁业3.《药品管理法》规定建立( )制度,持有人每年将药品生产销售、上市后研究、风险管理等情况按照规定向药品监督部门报告。
A、年度回顾B、年度评估C、年度报告D、药品上市许可持有人4.()依法对药品研制、生产、经营、使用全过程中药品的安全性、有效性和质量可控性负责。
A、药品生产企业B、药品经营企业C、药品上市许可持有人D、药品监督管理部门5.从事药品生产活动,应当经所在地省、自治区、直辖市人民政府药品监督管理部门批准,取得( )。
A、药品经营许可证B、药品注册证书C、GMP证书D、药品生产许可证6.对药品生产过程中的变更,按照其对药品安全性、有效性和质量可控性的风险和产生影响的程度,实行分类管理。
属于重大变更的,应当经( )批准。
A、国务院药品监督管理部门B、省药品监督管理部门C、市药品监督管理部门D、自治区药品监督管理部门7.违反《药品管理法》规定,构成犯罪的,依法追究( )责任。
A、行政责任B、民事责任C、刑事责任8.生产、销售假药的,没收违法生产、销售的药品和违法所得,责令停产停业整顿,吊销药品批准证明文件,并处违法生产、销售的药品货值金额( )的罚款;货值金额不足十万元的,按十万元计算;A、十五倍以上三十倍以下B、十倍以上二十倍以下C、一倍以上五倍以下D、三十万元以上三百万元以下9.生产、销售劣药的,没收违法生产、销售的药品和违法所得,并处违法生产、销售的药品货值金额( )的罚款;违法生产、批发的药品货值金额不足十万元的,按十万元计算,违法零售的药品货值金额不足一万元的,按一万元计算;A、十五倍以上三十倍以下B、十倍以上二十倍以下C、一倍以上五倍以下D、三十万元以上三百万元以下二、多选题(共18题,每题3分,共54分)1.国家对违反《药品管理法》的企业依法处罚时,同时对( )人员也予以处罚,包括没收违法行为发生期间其所获收入、罚款、一定期限甚至终身禁业等?A、企业法定代表人B、主要负责人C、直接负责的主管人员D、其他责任人员2.药品上市许可持有人是指( )A、取得药品注册证书的企业B、取得药品生产许可的企业C、取得药品注册证书的药品研发机构D、取得药品生产许可证的自然人3.制定药品管理法的目的( )A、加强药品管理B、保证药品质量C、保证药品疗效D、保障公众用药安全和合法权益E.保护和促进公众健康4.本法所称药品,是指用于预防、治疗、诊断人的疾病,有目的地调节人的生理机能并规定有适应症或者功能主治、用法和用量的物质,包括( ) A、中药材B、中药C、化学原料药及其制剂D、化学药E、生物制品5.药品应当符合国家药品标准。
药品经营企业(批发)经营医疗用毒性药品审批指南

114-001 药品经营企业(批发)经营医疗用毒性药品审批一、行政许可项目名称:药品经营企业(批发)经营医疗用毒性药品审批二、行政许可内容:药品经营企业(批发)经营医疗用毒性药品审批三、设定行政许可的法律依据:《医疗用毒性药品管理办法》四、行政许可数量及方式:无五、行政许可条件:符合法定条件六、申请材料目录:资料编号1、《广东省经营医疗用毒性药品申请表》(一式2份);资料编号2、书面申请报告(包括申请单位的基本情况,人员、场地、设施、设备、仓储及经营医疗用毒性药品必要性说明等);资料编号3、《药品经营许可证》正、副本原件及复印件,《营业执照》、《药品GSP 证书》复印件;资料编号4、医疗用毒性药品仓储设施(包括摄像监控系统和与公安联网的报警系统)及其布局图;资料编号5、完善的经营医疗用毒性药品管理制度(包括采购、销售、保管、养护、销毁、监督等);资料编号6、医疗用毒性药品管理人员名册及其学历、职称评定书、职称聘任书等证书复印件;资料编号7、企业自查报告;资料编号8、经办人身份证复印件;资料编号9、申报材料真实性的自我保证声明,并对材料作出如有虚假承担法律责任的承诺。
真实性自我保证声明应由申请企业法定代表人或负责人签字并加盖企业公章,并包括以下内容:(1)所提交的申请材料清单;(2)单位承担相应法律责任的承诺。
资料编号10、凡申请单位申报材料时,申请人不是法定代表人或负责人本人,单位应当提交《授权委托书》。
七、申请材料要求:1、申报材料按规定的资料项目序号编号2、使用A4幅面纸张,5号~4号宋体字打印3、除申请表外,每项资料项目单独装订并附封面4、封面依次打印如下项目:资料项目编号,资料项目名称,单位名称(加盖公章)及其地址、经办人姓名及联系电话、申请日期。
5、所有复印件均需注明“与原件相符”并加盖申请单位公章。
6、申请表中注明“签名”的项目必须相关人员的亲笔签名。
7、在递交书面申报材料前,申请人必须先登录“企业网上办事平台(http://219.135.157.143)”进行网上申报工作(网上申报操作指引.pdf),填报申请事项材料,凭申报成功后取得的预受理号方可到受理大厅办理后续工作。
福建省财政厅、福建省地方税务局关于下达福建省不征收营业税的收

乐税智库文档财税法规策划 乐税网福建省财政厅、福建省地方税务局关于下达福建省不征收营业税的收费项目名单(第二批)的通知【标 签】不征收营业税,不征收营业税收费,第二批【颁布单位】福建省财政厅,福建省地方税务局【文 号】闽财税政﹝1999﹞23号【发文日期】1999-07-26【实施时间】1999-07-26【 有效性 】全文有效【税 种】营业税各地、市、县(区)财政局、地方税务局: 根据财税[1997]5号、财税[1997]117号和闽财税政[1997]69号的有关规定,现将《福建省不征收营业税的收费项目名单(第二批)》印发给你们,并就有关行政事业性收费(基金)营业税问题进一步补充明确如下: 一、虽已列入不征收营业税项目名单,但按有关规定应纳入而未及时、足额纳入预算管理或财政专户管理的收费、基金,由各级财政部门向同级地方税务部门提供其应纳入未纳入的收费情况,地方税务部门对其未纳入部分征收营业税。
二、虽已列入不征收营业税项目名单,但擅自超过收费范围或提高收费标准的收费、基金,除按有关规定处理外,地方税务部门对其超过标准部分,征收营业税。
三、凡不属于中央、省人大法规、省政府下文和省财政厅、省物委联合下文批准的行政事业性收费、基金、无论其是否纳入预算管理或财政专户管理,除按有关规定处理外,还应对其全部收入征收营业税。
四、本通知自发布之日起执行。
附件:福建省不征收营业税的收费项目名单(第二批)序号 收费部门 收费项目 收费依据 备注1 农业 农业综合开发基金 省政府闽政(1991)综181号2 社保 机关事业单位人员退休养老保险基金 省政府闽政(1994)1号3 见义勇为基金会 见义勇为基金 闽银(1993)704号4 文联 省文学基金 闽委办(1993)45号5 残联 残疾人募捐基金 省政府闽政办(1987)303号6 土地 耕地开发专项基金 省政府闽政(1996)第5号令7 土地 基本农田开发基金 省人大常委会8 省卫生厅及地市人民 初级卫生保健基金 省政府闽政办(1996)113号 政府、省直有关单位9 建委、土地 城市基础设施配套费 省政府闽政(1989)113号10 经贸委三峡办、电力 三峡工程库区移民对口支援基金 省政府闽政(1994)139号11 广播电视 审看审听录像录音鉴定费 省物委(1990)闽价(涉)字第122号12 广播电视 音像管理费 省物委(1990)闽价(涉)字第122号13 计委 “农转非”指标卡工本费 省物委、省财政厅(1994)费字45号14 医药 药品生产经营企业合格论证收费 省物委、省财政厅(1995)费字001号15 医药 新项目新产品可行性论证费 省物委、财政厅闽价(1997)费字197号16 财政 注册资产评估执业资格考试收费 省财政厅、省物委闽财综(1995)106号17 财政 会计证培训班考务审批费 省物委、财政厅闽价(1992)费字384号18 财政 注册会计师考试考核收费 省物委、省财政厅闽价(1993)费字85号19 二轻 室内装饰装修评审费 省物委、省财政厅闽价(1993)费字112号20 林业 森林植被恢复费 省物委、省财政厅闽价(1993)费字78号21 轻工业 蘑菇栽培苗种生产许可证 省物委(1991)闽价费字374号22 政府外事 公务护照办证费 省政府闽政(1988)13号23 外事办 办理护照收费 省物委、财政厅闽价(1997)费字90号24 地矿 矿山企业、个体采矿登记费 省政府闽政(1988)13号25 建委 注册建筑师报名考务费(一、二级) 省物委、省财政厅闽价(1995)房字179号26 建委 房地产估价师报名考务费(每人150元) 省财政厅、省物委闽财综(1996)070号27 建委 监理工程师考务费 省财政厅、省物委闽财综(1997)003号28 建委 勘察设计技术开发费 省政府闽政(1989)27号29 人事 高中级职称外语考试费 省物委、财政厅闽价(1998)费字442号30 建设 造价工程师执业资格考务费 省财政厅、省物价委闽财综(1998)房字49号31 建设 一级注册结构师考务费 省物委、财政厅闽价(1998)房字496号32 劳动 劳动伤残鉴定收费 省物委、省财政厅闽价(1997)费字252号33 劳动 就业调节费 省政府闽政(1997)25号、省劳动厅34 劳动 电梯、起重机械等物种设备产品安全 省物委、财政厅闽价(1993)费字280号 性能监检费35 贸易 生猪定点屠宰管理费 省物委、省财政厅闽价(1992)费字382号36 技术监督 科技进步奖评审费 省物委闽价(1992)费字第189号37 技术监督 企业产品执行标准证书费 省物委、财政厅闽价(1993)费字136号38 技术监督 标准现行性确认费 省物委、财政厅闽价(1993)费字136号39 技术监督 国际标准产品注册证书费 省物委、财政厅闽价(1994)费字282号40 交通 公路路产损坏赔偿费 省财政厅、省物委闽财综(1995)113号41 交通 养路费免征工本费 省政府闽政(1994)6号42 交通 差路费补证费 省政府闽政(1994)6号43 交通 差路费年审工本费 省政府闽政(1994)6号44 旅游 服务员技术职称考评费 省物委、省财政厅闽价(1992)费字78号45 人民银行 《经营金融业务许可证》工本费 省政府闽政(1988)22号46 农业 种子“三证”及检验收费 省政府闽政(1988)22号47 农办 水土保持补偿费 省物委、财政厅闽价(1996)费字396号48 卫生 药厂药品注册登记费 省政府闽政(1988)13号49 卫生 医院制剂品种注册登记费 省政府闽政(1988)13号50 防空办 防空地下室易地建设费 省政府闽政(1996)5号51 公安 城市公共消防设施配套费 闽人大常委会(1996)10号52 公安 航行港澳船舶证书费 省政府闽政(1988)13号53 公安 暂住人口管理费 省政府(94)第15号省长令54 矿产储量委员会 非国家地质事业勘探地质报告审批费 省政府闽政(1988)13号55 检察院 法医、文检、痕检等收费 省政府闽政(1989)27号56 检察、法院 法医勘验鉴定费 省物委、财政厅闽价(1993)费字202号57 科委 技术合同认定登记费 省物委、财政厅闽价(1993)费字20号58 税务 增值税专用发票工本费 省物委闽价(1996)费字129号59 统计 统计证工本费 省财政厅、物委闽财综(1996)费字043号60 统计 统计登记证工本费 省财政厅、物委闽财综(1995)费字111号61 教育 普通高中(职中、中专)招生报名费 省物委、财政厅、教委闽教计(91)050号62 建材工业 水泥行检收费 省政府闽政(1989)27号63 环境保护 放射性废物(源)监测、分析收费 省政府闽政(1988)13号64 环境保护 环境监测收费 省政府闽政(1988)13号65 民政 涉外出具《夫妻关系证明书》收费 省政府闽政(1988)13号66 民政 涉侨、港澳出具《夫妻关系证明书》收费 省政府闽政(1988)13号67 人事 人事工作证表收费 省物委、财政厅闽价(1992)费字12号68 人事 公务员招干考试费 省物委、财政厅闽价(1993)费字219号69 人事 机关补充人员及招干考试费 省物委、财政厅闽价(1994)费字219号机关事业单位工人技术岗位等级培训70 人事 费考核收 省财政厅、物委闽财综(1996)费字207号71 人事 经济专业、国际商务专业资格考试费 省物委、财政厅闽价(1997)费字134号72 人事 执业药师、执业中药师资格考务费 省财政厅、物委闽财综(1997)费字30号73 编委 事业单位登记收费 省政府闽政(1996)文138号74 烟草专卖 函授生经费 省教委闽教计(1995)24号75 安全 安装电话保密防范设备费 省物委闽价(1992)费字59号76 工商 指定印制商标单位证书工本费 省物委、财政厅闽价(1999)函16号77 妇联 幼儿园管理费 省物委、财政厅、教委闽价(1996)费字284号78 专利 专利纠纷调处费 省物委、财政厅、省专利局闽科专(86)024号、 (88)闽科专001号79 专利 专利技术转让费 省科委、财政厅、省专利局闽科专(86)024号、 (88)闽科专001号80 机关事务 公文交换站管理费 省物委、财政厅闽价(1994)费字55号81 粮食 《粮食供应证》工本费 省物委、财政厅(91)闽价(涉)字第031号82 福州市 门牌、幢牌工本费 省物委、财政厅闽价(1998)费字第233号83 福州市 福州市机要公文交换站收费 省物委(1991)闽价(费)字第385号84 福清市 海堤维护管理费 省财政厅、物委闽财综(1996)034号85 三明市 金湖风景区资源保护费 省物委、财政厅闽价(1996)费字446号86 南平市 武夷山风景区资源保护费 省物委、财政厅闽价(1995)费字57号。
药学部首营企业、首营品种审核制度

首营企业、首营品种审核制度文件编号YJK-YK-001制订日期:年月修订日期:年月审批:为维护企业的经营利益和质量信誉,保证人民用药安全有效,制定本制度。
一.首营企业的审核1. 首营企业的概念:采购药品时与我院首次发生供需关系的药品生产或经营企业。
2. 首营企业的审核,包括生产、经营资格和质量保证能力的审核。
审核工作由采购员具体负责,药库负责人核对无误后,由药学部主任审核,报药事管理与药物治疗学委员会批准后方可做为合格供货方。
3. 首营企业审核应提供的材料:《药品生产许可证》或《药品经营许可证》复印件、《营业执照》复印件、首营企业质量体系调查表、企业法人签署的销售人员“授权委托书”原件、销售人员身份证复印件和国家规定必须通过GMP认证的车间(品种、剂型)的批准证书复印件。
以上材料的复印件必须加盖供货方公章。
4. 除审核有关材料外,必要时应实地考察。
二.首营品种的审核1. 首营品种的概念:我院首次向药品生产企业或药品经营企业首次购进的药品,包括药品的新剂型、新规格、新包装等。
2. 通过药事管理与药物治疗学委员会批准的药品方可进行首营品种的审核。
审核工作由药品采购员具体负责,经药库负责人核对,科主任审批后方可进行采购。
3. 首营品种审核,厂方应提供以下材料:该品种的生产批文、该品种所适用的法定质量标准、该品种的生产厂家的检验报告书、该品种包装、标签及说明书样本、进口药品的《进口药品注册证》(或《医药产品注册证》)、《进口药品检验报告书》、药品生产企业所在地省级物价部门批文或山东省物价局的价格登记表。
以上材料的复印件须加盖供货方的企业公章或质量检验机构的原印章。
三.审核材料的备案与保管1. 要求备案的审核材料必须完整、清晰、有效。
2. 对审核材料要及时整理、妥善保存、建档备查。
关于调整制定苄星青霉素等药品最高零售价格的通知

关于调整制定苄星青霉素等药品最高零售价格的通知二○一一年七月十四日粤价〔2011〕166号
各地级以上市物价局,深圳市发展改革委、市场监管局,佛山市顺德区发展规划和统计局,各有关医疗机构、药品生产经营企业:按照《国家发展改革委关于调整部分抗微生物类和循环系统类药品最高零售价格的通知》(发改价格〔2011〕440号)等文件规定,我局依据《药品政府定价办法》和《药品差比价规则(试行)》等规定,结合我省药品销售情况,决定调整制定苄星青霉素等药品最高零售价格,有关事项通知如下:
一、本文的药品价格是按照药品差比价规则计算的补充剂型规格的最高零售价格(详见附件1)。
附件中没有标注生产企业的,为统一最高零售价格;标注生产企业名称的,为国家发展改革委或我省已差别定价的同种药品补充规格的价格,仅限于该企业执行。
二、取消部分规格不规范以及国家正式注册批件未标注的统一定价药品价格(详见附件2)。
三、各医疗卫生机构、社会零售药店及其他药品生产经营单位销售相关药品的价格不得超过本次公布的价格。
四、各级价格主管部门要加强对药品价格执行情况的监督检查和药品市场购销价格监测工作,对药品生产经营单位违反本通知规定的价格行为,要依法严肃查处。
执行中遇到的问题应及时上报我局。
五、本通知规定的价格自2011年7月20日起执行。
此前我局公布的
与本文附件相同的药品价格同时废止。
附件:1. 苄星青霉素等药品最高零售价格表
2. 取消部分统一定价药品价格品种表
附
件
1:
苄星青霉素等药品最高零售价格表
金额单位:元
附件2:
取消部分统一定价药品价格品种表。
药品经营-质量方针与质量目标管理制度

目的:为明确本公司经营管理的总体质量宗旨和质量目标,促进公司质量体系不断完善,结合本公司经营实际,制定本制度。
依据:依据《中华人民共和国药品管理法》及实施条例、《药品经营质量管理规范》(总局令第28号)、《药品经营质量管理规范》现场检查指导原则等法律法规。
适用范围:本制度适用于公司质量方针的确定和年度质量目标的制定,以及对质量方针和质量目标管理的过程。
职责:公司各部门负责实施。
内容:1.相关术语:1.1 质量方针,是由企业负责人正式发布的企业总的质量宗旨和方向,是企业经营总方针的组成部分,是企业负责人为保证药品质量而确定的指导思想和做出的承诺。
企业负责人应当确定质量方针并形成文件。
1.2 本公司质量方针:是由公司总经理以文件形式正式发布的本公司的质量宗旨和方向,是组织建立质量目标的框架和基础。
是实施和改进企业质量体系的推动力。
1.3 质量目标:是指公司在质量方面的追求和质量方针的展开与落实。
是为了确保建立和评价的质量目标与质量方针保持一致,进而确保质量方针与宗旨相适应。
1.4 公司的质量方针与质量目标:公司制定“质量第一、规范管理”的质量方针。
每个员工都应坚持“质量第一”的原则,加强基础管理,完善质量体系,为客户提供质量合格的药品和文明满意的服务。
在质量方针指导下进行各项经营管理工作。
2.公司总的质量目标和要求如下:2.1.按照《药品经营质量管理规范》(总局令第28号)等法律法规的要求,不断完善质量体系管理。
2.2.1公司将依据质量方针和质量目标开展质量目标经营活动。
把总的质量目标分解到各部门、各岗位,贯彻到药品经营活动的全过程,实现全员参与质量管理。
3.公司每年组织一次GSP内部评审,作为目标管理一项内容;每次监督检查也作为企业的质量目标。
针对GSP内部评审和监督检查中的不足,做出整改方案,改进措施又将作为新的质量目标进行管理和考核。
4.质量方针目标实施流程:4.1.每年度的“质量方针和目标”应形成书面文件,由总经理签署发布,并具体落实到公司各部门。
编号QR—030通用名称商品名称...

信息联系处理单药品质量档案表文件修订申请表文件销毁审批记录质量事故报告处理记录质量分析记录药品拒收报告单质量管理制度执行情况检查考核记录表编号:QR—010问题改进和措施跟踪记录编号:QR 011说明:本表一式三份,由实施部门实施后反馈到下达改进任务部门和分管领导各一份,自留一份。
内部质量管理体系审核报告(可另附纸叙述)不符合报告GSP自查评审表职工登记表编号:QR—020编号:QR—021 填表日期:健康档案登记表编号:QR—023强制检定计量器具检定记录卡编号:QR—026 制卡日期年月日制卡人:供货方一览表合格供货方档案首营企业审批表首营品种审批表编号:QR—030电话订货记录(代合同)编号:QR—033 年月日照,质量标准,生产批文。
所供药品包装、标签、说明书符合有关规定,药品应附产品合格证,包装符合运输要求,如遇有假药、劣药供方承担一切法律责任。
药品拆零登记表编号:QR—039购进退出通知单经办人:药品停售通知单编号:QR—043年第号通用名称规格剂型产品批号有效期生产日期生产企业经手人复核人其它停售原因签名:年月日药品解除停售通知单编号:QR—044年第号如下药品质量复查结果合格,撤消年第号“药品停售通知单”,请恢复正常出库及销售使用,特此告知。
通用名称规格剂型产品批号有效期生产日期生产企业经手人复核人其它签名:年月日不合格药品报损审批表编号:QR—046 报告时间:年月日说明:本表应附拟报损品种清单不合格药品销毁记录注:本表应附销毁品种清单。
记录人:药品质量复查报告单销后退回通知单经办人:药品养护档案表编号:QR—055 建档日期:中药饮片质量检查记录养护设备检修维护记录编号:QR—058药品储存温湿度记录表编号:QR—059 库区表号时间:年月药品陈列环境温湿度记录表编号:QR—060 库区表号时间:年月效期药品催销表报告人签字:年月日质量部门:业务部门经理注:1.此报告单由仓库保管员填写2.此报告单自填报日起保存2年3.此报告单一式四份,仓库、质量、业务、主管经理各一份。
药品生产类许可事项审查工作细则[001]
![药品生产类许可事项审查工作细则[001]](https://img.taocdn.com/s3/m/dfdb6629c281e53a5802ffba.png)
个人资料整理,仅供个人学习使用漳州市食品药品监督管理局药品生产类许可事项审查工作细则(试行)第一章总则第一条为确保正确履行行政审批职能,促进药品生产监管行政职能转变,提高行政执行力和行政效率,根据《中华人民共和国行政许可法》、《中华人民共和国药品管理法》、《麻醉药品和精神药品管理条例》、《反兴奋条例》、《麻醉药品和精神药品运输管理办法》、《麻醉药品和精神药品邮寄管理办法》等法律、法规、规章、规范性文件规定,结合实际,制定本细则。
第二条本细则适用于由漳州市审改办公布的由漳州市食品药品监督管理局(以下简称“市食药监局”)实施的药品生产许可类事项(含医疗机构制剂调剂使用审批、非药品生产企业使用咖啡因审批、科研和教学使用麻醉药品和精神药品审批、经营蛋白同化制剂、肽类激素审批、麻醉药品和第一类精神药品运输证明核发、麻醉药品和精神药品邮寄证明核发)的审查工作。
第三条药品生产类许可事项审查工作应当坚持有法必依的原则。
第四条药品生产类许可事项审查工作应当坚持客观公正、实事求是的原则。
第五条药品生产类许可事项审查工作应当严格实行回避制度。
第六条药品生产类许可事项审查工作主体是市食药监局派驻漳州市行政服务中心窗口(以下简称“市食药监局窗口”)。
第二章审查标准第七条药品生产类许可事项审查,依据《中华人民共和国行政许可法》、《中华人民共和国药品管理法》、《麻醉药品和精神药品管理条例》、《反兴奋条例》、《麻醉药品和精神药品运输管理办法》、《麻醉药品和精神药品邮寄管理办法》确定的标准开展审查工作。
第八条申请人应当按照市食药监局制定的申请书格式文本提交申请,并按照相关法律、法规和规章的规定提交有关材料。
申请人应当如实向市食药监局窗口提交有关材料和反映真实情况,并对其申请材料实质内容的真实性负责。
第九条申请人所申请事项内容应当符合相应申请条件,所提交的申请材料应与窗口事项服务指南或福建省网上办事大厅、漳州市网上办事大厅、市食药监局门户网站上公布的事项材料清单要求相一致。
医疗用毒性药品定点经营批发企业名单
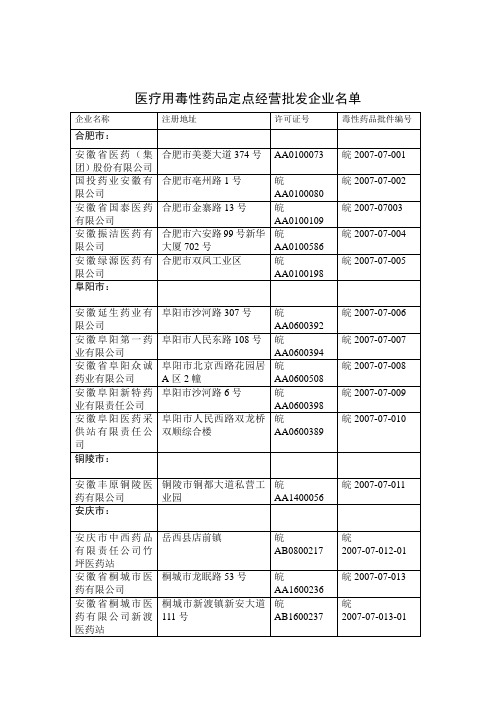
芜湖欣瑞医药有限责任公司
芜湖市芜宁路钱家山1号
皖AA1200527
皖2007-07-070
安徽省芜湖齐欣医药有限公司
南陵县工业园区
皖AA1200005
皖2007-07-071
杭州回音必集团芜湖医药有限公司
芜湖县芜湖南路9号
皖AA1200007
皖2007-07-072
安徽惠众医疗科技有限公司
芜湖市镜湖东路2号
金寨县医药有限责任公司青山医药站
金寨县青山镇
皖AB0900367
皖2007-07-056-01
安徽省弘济药业有限公司
六安市金安区宁平路2号
皖AB0900374
皖2007-07-057-01
霍邱县同济药业有限公司
城关东湖路5号
皖AA0900503
皖2007-07-058
霍邱县同济药业有限公司长集公司
霍邱县长集镇文昌路30号
皖2007-07-046
安徽省怀远县医药公司
怀远县新民路12号
皖AA0500204
皖2007-07-047
安徽省固镇县博济药业有限责任公司
固镇县胜利路52号
皖AA0500186
皖2007-07-048
安徽省蚌埠市吉坤医药有限公司
蚌埠市凤阳东路572号
皖AA0500194
皖2007-07-049
六安市:
宣城市昭亭路
皖AA1300055
皖2007-07-080
宿州市金茂商城4-36号
皖AA0400534
皖2007-07-019
宿州市中信药业有限公司
宿州市淮河中路36号
皖AA0400290
皖2007-07-020
常用的药品管理法律法规

常用的药品管理法律法规第一部分药品管理法一、无证经营药品第十四条开办药品批发企业,须经企业所在地省、自治区、直辖市人民政府药品监督管理部门批准并发给《药品经营许可证》;开办药品零售企业,须经企业所在地县级以上地方药品监督管理部门批准并发给《药品经营许可证》,凭《药品经营许可证》到工商行政管理部门办理登记注册。
无《药品经营许可证》的,不得经营药品。
第七十三条未取得《药品生产许可证》、《药品经营许可证》或者《医疗机构制剂许可证》生产药品、经营药品的,依法予以取缔,没收违法生产、销售的药品和违法所得,并处违法生产、销售的药品(包括已售出的和未售出的药品,下同)货值金额二倍以上五倍以下的罚款;构成犯罪的,依法追究刑事责任。
二、从非法渠道采购药品第三十四条药品生产企业、药品经营企业、医疗机构必须从具有药品生产、经营资格的企业购进药品;但是,购进没有实施批准文号管理的中药材除外。
第八十条药品的生产企业、经营企业或者医疗机构违反本法第三十四条的规定,从无《药品生产许可证》、《药品经营许可证》的企业购进药品的,责令改正,没收违法购进的药品,并处违法购进药品货值金额二倍以上五倍以下的罚款;有违法所得的,没收违法所得;情节严重的,吊销《药品生产许可证、《药品经营许可证》或者医疗机构执业许可证书。
三、生产销售假药第四十八条禁止生产(包括配制,下同)、销售假药。
有下列情形之一的,为假药:(一)药品所含成份与国家药品标准规定的成份不符的;(二)以非药品冒充药品或者以他种药品冒充此种药品的。
有下列情形之一的药品,按假药论处:(一)国务院药品监督管理部门规定禁止使用的;(二)依照本法必须批准而未经批准生产、进口,或者依照本法必须检验而未经检验即销售的;(三)变质的;(四)被污染的;(五)使用依照本法必须取得批准文号而未取得批准文号的原料药生产的;(六)所标明的适应症或者功能主治超出规定范围的。
第七十四条生产、销售假药的,没收违法生产、销售的药品和违法所得,并处违法生产、销售药品货值金额二倍以上五倍以下的罚款;有药品批准证明文件的予以撤销,并责令停产、停业整顿;情节严重的,吊销《药品生产许可证》、《药品经营许可证》或者《医疗机构制剂许可证》;构成犯罪的,依法追究刑事责任。
药品生产企业管理文件 SMP-QA-001-02 质量方针与质量目标管理规程

目录1.目的 (2)2.范围 (2)3.职责 (2)4.内容 (2)5.相关程序、记录,附件 (2)6.参考资料 (3)7.历史和修订记载 (3)1.目的:明确公司总体的质量方针和目标,统一全体员工的质量意识,结合公司实际制定本规程。
2.范围:适用于公司的所有与质量管理相关一切活动。
3.职责:3.1质量管理部:负责监督质量方针和质量目标的实施;3.2各部门:负责本部门质量方针和质量目标具体实施工作;4.内容:4.1定义及术语4.1.1质量方针:是指由企业最高管理者制定并发布的质量宗旨和方向,是实施和改进组织质量管理体系的推动力。
4.1.2质量目标:企业在质量方面所追求的目的。
质量目标是可测量的,并与质量方针保持一致。
4.2质量方针和质量目标4.2.1为实现“打造放心中药创造健康生活”的质量目标,确保顾客的需求和期望得到确定,并转化为公司的产品和服务要求,特确定本公司质量方针为“优秀为习惯、质量是生命”。
公司要将以最好的质量和最高的效率保持企业的生命力,诚信生产,保证供、消各方利益,以顾客为中心实现我们对顾客的承诺。
4.2.2企业质量方针由董事长根据企业内外部环境条件、发展目标等信息制定,并以文件形式正式发布。
4.2.3本方针为制订和评审质量目标提供了框架,公司与质量有关的各部门应在此基础上制定相应的质量目标。
4.2.4在质量管理部的指导下,各部门将企业总体质量目标进行分解为本部门具体工作目标,并制定出质量目标的实施方法。
4.2.5各级领导要将质量方针传达到作业层次,使全体员工正确理解并坚决执行。
4.2.6对质量方针的批准、发布、评审、修改都应实行控制,执行公司文件。
5.相关程序、记录,附件:5.1相关程序无5.2相关记录无5.3附件无6.参考资料:《药品生产质量管理规范》(2010年修订)《药品生产质量管理规范》(2010年修订)实施指南:质量管理体系(2质量管理体系概述)7.历史和修订记载:。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
盐酸环丙沙星胶囊
胶囊剂
250mg
12
12粒/盒
普通GMP药品
回音必集团浙江亚东制药有限公司
批件转移,生产企业由回音必集团浙江亚东制药有限公司(S0520)变更为回音必集团浙江齐齐制药有限公司(S3690),其他不变
101834
盐酸环丙沙星片
素片
250mg
12
12片/盒
普通GMP药品
回音必集团浙江亚东制药有限公司
各医疗机构、药品生产、经营企业:
根据企业提交的变更申请,对海南全星制药有限公司等企业的挂网信息进行调整,公示期3天,公示期内接受各方投诉质疑。
特此通知!
省公共资源交易中心
2017年5月27日
流水号
实际通用名
实际剂型
实际规格
转换系数
包装单位
申报企业注册号
申报企业
生产企业注册号
生产企业
调整情况
35046
进口产品总代变更,变更后总代为天津太平鸿业医药开发有限公司(j3175),其他不变
110134
贝米肝素钠注射液
注射液
0.2ml:3500IU(抗Xa)
1
支
J2506
辽宁天龙医药贸易有限公司
SJ477
Laboratorios Farmacéuticos ROVI,S.A.
进口产品总代变更,变更后总代为天津太平鸿业医药开发有限公司(j3175),其他不变
进口产品总代变更,变更后总代为华润广东医药有限公司(J0521),其他不变
112088
舒洛地特注射液
注射液
2ml:600LSU
10
盒
J2469
山东菏泽博晟利康医药有限公司
SJ424
ALFA WASSERMANN S.p.A.
进口产品总代变更,变更后总代为绿谷(上海)医药产业投资有限公司(J3040),其他不变
批件转移,生产企业由回音必集团浙江亚东制药有限公司(S0520)变更为回音必集团浙江齐齐制药有限公司(S3690),其他不变
20094
头孢拉定胶囊
胶囊剂
250mg
24
24粒/盒
普通GMP药品
回音必集团浙江亚东制药有限公司
批件转移,生产企业由回音必集团浙江亚东制药有限公司(S0520)变更为回音必集团浙江齐齐制药有限公司(S3690),其他不变
113847
注射用1,6-二磷酸果糖
粉针剂
5.0g
1
盒
J1441
四川兴科蓉药业有限责任公司
SJ059
意大利福斯卡玛生化制药公司
进口产品总代变更,变更后总代为广州保科力医药保健品进出口有限公司(J3061),其他不变
92123
苯丁酸氮芥片
薄膜衣片
2mg
25
盒
J1023
华润国康(广东)医药有限公司(原广东京卫医药有限公司)
批件转移,生产企业由回音必集团浙江亚东制药有限公司(S0520)变更为回音必集团浙江齐齐制药有限公司(S3690),其他不变
73651
西罗莫司片
糖衣片
1mg
10
盒
J1058
浙江瑞海医药有限公司
SJ076
辉瑞制药
进口产品总代变更,变更后总代为华润广东医药有限公司(J0521),其他不变
27632
注射用甲泼尼龙琥珀酸钠
回音必集团浙江亚东制药有限公司
批件转移,生产企业由回音必集团浙江亚东制药有限公司(S0520)变更为回音必集团浙江齐齐制药有限公司(S3690),其他不变
99001
健儿消食口服液
口服液
10ml
18
18支/盒
普通GMP药品
回音必集团浙江亚东制药有限公司
批件转移,生产企业由回音必集团浙江亚东制药有限公司(S0520)变更为回音必集团浙江齐齐制药有限公司(S3690),其他不变
27614
甲泼尼龙片
素片
4mg
30
盒
J1058
浙江瑞海医药有限公司
SJ076
辉瑞制药
进口产品总代变更,变更后总代为华润广东医药有限公司(J0521),其他不变
110114
贝米肝素钠注射液
注射液
0.2ml:2500IU(抗Xa)
1
支
J2506
辽宁天龙医药贸易有限公司
SJ477
Laboratorios Farmacéuticos ROVI,S.A.
76964
吡罗昔康贴片
贴剂
6.8cm×5.2cm,含吡罗昔康48mg
3
盒
J0316
上药控股有限公司(原上海医药分销控股有限公司)
SJ322
SK Chemicals Co. Ltd.
进口产品总代变更,变更后总代为北京科园信海医药经营有限公司(J0383),其他不变
原企业名称
变更后企业名称
浙江华立南湖制药有限公司
进口产品总代变更,变更后总代为华润广东医药有限公司(J0521),其他不变
76103
更昔洛韦分散片
分散片
250mg
12
12片/盒
片
海南长安国际制药有限公司
S0033
海南长安国际制药有限公司
批件转移,生产企业由海南长安国际制药有限公司(S0033)变更为海南全星制药有限公司(S0464),其他不变
23398
SJ364
Orion Corporation
进口产品总代变更,变更后总代为华润广东医药有限公司(J0521),其他不变
93252
恩他卡朋双多巴片(Ⅱ)
薄膜衣片
左旋多巴100mg,卡比多巴25mg,恩他卡朋200mg
30
盒
J0914
山德士(中国)制药有限公司
SJ364
Orion Corporation
SJ472
Aspen Pharmacare Australia Pty Ltd
进口产品总代变更,变更后总代为华润广东医药有限公司(J0521),其他不变
92121
硫唑嘌呤片(薄膜衣)
薄膜衣片
50mg
100
盒
J1023
华润国康(广东)医药有限公司(原广东京卫医药有限公司)
SJ472
Aspen Pharmacare Australia Pty Ltd
呼伦贝尔松鹿堂制药有限公司
呼伦贝尔松鹿制药有限公司
冻干粉针剂
500mg
1
瓶
J1058
浙江瑞海医药有限公司
SJ076
辉瑞制药
进口产品总代变更,变更后总代为华润广东医药有限公司(J0521),其他不变
27631
注射用甲泼尼龙琥珀酸钠
冻干粉针剂
40mg
1
瓶
J1058
浙江瑞海医药有限公司
SJ076
辉瑞制药
进口产品总代变更,变更后总代为华润广东医药有限公司(J0521),其他不变
贝克诺顿(浙江)制药有限公司
江苏豪森药业股份有限公司
江苏豪森药业集团有限公司
湖北海王医药有限公司
湖北海王医药集团有限公司
南漳天盛药业有限公司
襄阳华源天盛药业有限公司
河北百善医药贸易有限公司
河北百善医药科技有限公司
河南省新谊药业有限公司
上海凯宝新谊(新乡)药业有限公司
安徽众禾药业股份有限公司
精诚徽药药业股份有限公司
地奥司明片(薄膜衣)
薄膜衣片
500mg
24
盒
S0043
马应龙药业集团股份有限公司(原武汉马应龙药业集团股份有限公司)
S0043
马应龙药业集团股份有限公司(原武汉马应龙药业集团股份有限公司)
规格变更,变更后规格为0.45g,其他不变
45325
恩他卡朋片薄膜衣片2 Nhomakorabea0mg30
盒
J0914
山德士(中国)制药有限公司
98999
尼莫地平胶囊
胶囊剂
20mg
50
50粒/盒
普通GMP药品
回音必集团浙江亚东制药有限公司
批件转移,生产企业由回音必集团浙江亚东制药有限公司(S0520)变更为回音必集团浙江齐齐制药有限公司(S3690),其他不变
20093
头孢氨苄胶囊
胶囊剂
125mg
50
50粒/盒
普通GMP药品
回音必集团浙江亚东制药有限公司
柏洁洗剂
洗剂
150ml
1
盒
S0520
回音必集团浙江亚东制药有限公司
S0520
回音必集团浙江亚东制药有限公司
批件转移,生产企业由回音必集团浙江亚东制药有限公司(S0520)变更为回音必集团浙江齐齐制药有限公司(S3690),其他不变
89227
健儿消食口服液
口服液
10ml
10
10支/盒
支
盒
普通GMP药品
