第2节 离子峰的主要类型
质谱法基本知识(15)—离子类型(a分子离子峰)

质谱法基本知识(15)—离子类型(a分子离子峰)
分子离子峰
分子失去一个电子而生成的离子称为分子离子或母离子,相应的质谱峰称为分子离子峰或母峰。
特点:
分子离子峰通常出现在质荷比最高的位置,存在同位素峰时例外。
稳定性取决于分子结构,芳香族、共轭烯烃等强,脂肪醇、胺、硝基化合物很弱甚至不出现。
分子离子峰左边3-14原子质量单位范围内一般不可能出现峰,因为同时使一个分子失去三个氢原子几乎不可能,而能失去的最小基团通常是甲基,即(M-15)+峰。
凡是分子离子峰应符合“氮规则”。
氮规则表明相对分子质量为偶数的有机化合物一定含有偶数个氮原子或不含氮原子;相对分子质量为奇数的,则只能含奇数个氮原子。
主要用途是确定化合物相对分离质量
当分子离子峰不出现时,可以采用以下办法:
a.降低电子轰击的能量,可以减少分子离子进一步裂解的可能性,从而增强分子离子峰。
b.更换其它离子源。
c.采用化学衍生化的方法,使化合物(如醇)转变成稳定的衍生物(如酯)。
离子峰的主要类型

N规则 •含奇数N原子, 奇数(如CH3CN) +为偶数 •其他M
21:00:46
+为 M
四.亚稳离子峰
M1
+→
m2
++中性碎片
M1+→ m2 * +中性碎片
(m*= m22/ m1)
峰较钝而小,一般要 跨到2~5个质量单位; 质荷比通常不是整数
对氨基茴香醚产生亚稳离子的裂解
寻找和判断离子在裂解过程中的相互关系
正 己 烷
碎片离子峰
CH3
<
H3C CH2
< H3C
CH CH3
< H3C
43 57 29 15 71
正癸烷
C CH3 CH3
85 99 113 142 m/z
碎片离子峰
碎片离子峰
57
43
29 71
M =86 86 M
30 40 50 60 70 80
90 C C H 3 57
H 3C
C H 2 C H 2 C H2
H 3C
C H3
H 3 C C H2 C H2 H 3 C C H C H3 43
三、同位素离子峰
M+1, M+2,M+3。。。。;
例:CH4 M=16 12C+1H×4=16 M 分子离子峰 13C+1H×4=17 M+1 同 12C+2H+1H×3=17 M+1 位 素 13C+2H+1H×3=18 M+2 峰
第二节 离子峰的 主要类型
main types of ion peaks
一、分子离子峰 二、碎片离子峰 三、同位素离子 峰 四. 亚稳离子峰 五.多电子峰
MS(质谱图)PPT课件

NO2 NH2 183
69
精选
70
精选
71
三、碎片离子峰
一般有机化合物的电离能为7-13电子伏特,质谱中常用
的电离电压为70电子伏特,使结构裂解,产生各种“碎片”离
子。
烷正 己
15
29
43 57
71
H 3 C CH 2 CH 2 CH 2 CH 2 CH 3
71 57 43 29
15
7 1 H 3 C CH 2 CH 2 CH 2 CH 2
• GCMS中TIC图相当于色谱图 • EI源的TIC图 GC的FID检测器所得色谱图 • 每张MS图中所有离子的强度
精选
26
质谱图
精选
28
质谱术语
精选
29
有机质谱中的各种离子
– 、分子离子 – 、同位素离子 – 、碎片离子 – 、重排离子 – 、亚稳离子 – 、多电荷离子 – 、负离子 – 、准分子离子 如 MH+ 、 M Na+ 、 (M-H)– 、母离子与子离子 – 、奇电子离子和偶电子离子
精选
30 30
第二节 离子峰的主要类型
一、分子离子峰 二、同位素离子峰 三、碎片离子峰 四、奇电子离子峰 五、偶电子离子峰
一、分子离子峰
分子电离一个电子形成的离子所产生的峰。
分子离子的质量与化合物的分子量相等。 M+e-→ M ++2e
位于质谱图的右端,因为m/e最大
相对强度取决于分子离子相对于裂解产物的稳定性。
n=3 (a+b)3=a3+3a2b+3ab2+b3 a=3 b=1
=33+3× 32 × 1 + 3× 3 × 1 2+1
质谱分析-离子峰的主要类型

29 H3C CH2
CH2 CH2 CH2 CH3
15 CH3
CH2 CH2 CH2 CH2 CH3
13:07:34
碎片离子峰
CH3 < H3C CH2 < H3C CH CH3 < H3C C CH3
CH3
43
29 15
13:07:34
57 正癸烷
71 85 99 113 142
m/z
碎片离子峰
C7H4N O3 8.13 1.06
C8H11N2 O 9.61 0.61
C7H6N2 O2 8.50 0.72
C8H12N3 9.98 0.45
C7H8N3 O
13:07:34
8.88 0.55
C9H10 O2 9.96 0.84
三、碎片离子峰
fragment ion peaks
一般有机化合物的电离能为7-13电子伏特,质谱中常用
的电离电压为70电子伏特,使结构裂解,产生各种“碎片”离
子。
15 29 43 57
71
正 己
H3C CH2 CH2 CH2 CH2 CH3
71 57 43 29
15
烷
71 H3C CH2 CH2 CH2 CH2
CH3
57 H3C CH2 CH2 CH2
CH2 CH3
43 H3C CH2 CH2
CH2 CH2 CH3
C3 C C C4 20
6
C7CHO
2
C6COOH
0.5
C8NH2
0.5
C8OH
0.1
C7Cl
0.1
O C2 C C5 C4 O C4
O C6 C NH2
质谱

一、质谱的基本原理
质谱的原理=质谱仪器的原理,不同的仪器,原理略有 差异。质谱仪一般分一下几个部分:
进样系统
离子源
质量分析器
高真空系统
检测器
数据处理显示
8
进样系统
在不破坏真空条件下,将样品引入离子源
离子源
是样品电离,形成各种离子。离子源是各类质谱仪的 重要区别部件之一。常见的离子源有:电子轰击电离源 (electron impact ionization, EI) , 化 学 电 离 源 (chemical ionization, CI),场电离源(field ionization),快原子轰击电 离源(fast atom bombardment ionization),基质辅助激光 解吸电离源(matrix assisted laser desorption ionization), 电喷雾电离源(electrospray ionization)等
质谱分析法
(Mass Spectroscopy,MS)
1
第一节 质谱的基本原理
质谱是一种质量分析方法,类似于天平称量分析方法。但 不是直接称量,而是先将分子在一定的条件下电离形成气 态的离子,(例如分子失去1个电子后,形成分子离子; 还有可能分子被粉碎形成许多带电荷的碎片离子)。一般 情况下,这些离子都带1个正电荷,但质量却不相同,也 就是说,各种离子的质量/电荷比(简称质荷比m/z)不同。 可利用仪器(质谱分析器)将质荷比不同的离子分开,然 后利用离子检测器逐一检测。最后,通过计算机处理,给 出各种质荷比不同的离子的相对强度。
2
Sample
+ _
Ionizer
Mass Analyzer
Detector
分子离子峰和同位素离子峰之比

分子离子峰和同位素离子峰之比1.引言1.1 概述概述部分内容需要介绍文章的主题和背景。
在这篇文章中,我们将探讨分子离子峰和同位素离子峰之间的比较。
离子峰是质谱分析中常用的一个概念,它是质谱图中的一组信号峰,代表着不同的离子种类。
分子离子峰是由分子或分子片段所生成的离子所形成的峰状结构。
这些离子可能由化学反应生成,也可能经过分子解离而形成。
分子离子峰在质谱图上的位置和强度可以提供关于样品的结构和组成信息。
而同位素离子峰则是由同一分子的不同同位素所形成的离子峰。
同位素是指具有相同原子序数但质量数不同的同一元素的不同形式。
由于同位素的存在,分子中可能出现同位素替代,导致相应的同位素离子峰在质谱图上出现。
比较分子离子峰和同位素离子峰,可以帮助我们研究样品的同位素组成和分子结构。
通过观察这些离子峰的位置和强度变化,我们可以推测样品分子中的同位素分布情况,进而对其物理化学性质进行分析和解释。
本文将详细介绍分子离子峰和同位素离子峰的产生机制和特征,并通过相关案例和实验证据来支持我们的观点。
最后,通过比较分子离子峰和同位素离子峰的特点和应用,我们将得出一些结论和总结。
通过这篇文章,我们希望读者可以对分子离子峰和同位素离子峰之间的比较有一个全面的了解,并能够在质谱分析中灵活运用这些知识。
1.2文章结构文章结构是指文章的组织形式和呈现方式。
本文的主题是分子离子峰和同位素离子峰之比,为了清晰地阐述这个主题,本文将分为三个主要部分:引言、正文和结论。
引言部分将提供对主题的概述、文章的结构和目的进行介绍。
首先,我们将总结分子离子峰和同位素离子峰的含义、特点以及它们在化学和分析领域中的重要性。
然后,我们将概述本文的结构,包括各个部分的内容和目标。
最后,我们将明确本文的目的,即探讨和比较分子离子峰和同位素离子峰之间的关系和差异。
正文部分将详细介绍分子离子峰和同位素离子峰的概念和特征。
在2.1节中,我们将解释分子离子峰的定义、生成机制以及它们在质谱分析中的应用。
分子离子峰的特点
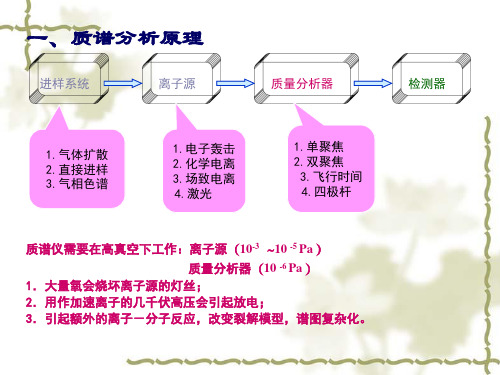
原理与结构 仪器原理图
电离室原理与 结构
质量分析器原理
加速后离子的动能 : (1/2)m 2= e V = [(2V)/(m/e)]1/2
在磁场存在下,带电离子按曲线轨迹飞行; 离心力 =向心力;m 2 / R= H0 e V
曲率半径: R= (m )/ e H0 质谱方程式:m/e = (H02 R2) / 2V 离子在磁场中的轨道半径R取决于: m/e 、 H0 、 V 改变加速电压V, 可以使不同m/e 的离子进入检测器。 质谱分辨率 = M / M (分辨率与选定分子质量有关)
B A CD
Separation
Mass Spectrometer (MS)
A B C D
Identification
第二节 离子峰的主要类型
一、分子离子峰 二、同位素离子峰 三、碎片离子峰
一、分子离子峰
分子电离一个电子形成的离子所产生的峰。 分子离子的质量与化合物的分子量相等。
有机化合物分子离子峰的稳定 性顺序: 芳香化合物>共轭链烯>烯烃> 脂环化合物>直链烷烃>酮>胺 >酯>醚>酸>支链烷烃>醇.
10
0
0 10 20 30 40 50 60 70
83 98(M )
80 90 100 110
二、芳烃的质谱图
三、醇和酚的质谱图
% OF BASE PEAK
100 90
o-Ethylphenol
80 122(M)
70
M-CH3M-H2O M
30
20
C6H5
10
0
0 10 20 30 40 50 60 70 80 90 100110120130140150
子和一个自由基阳离子
质谱图和主要离子峰类型教学提纲

33S/32S 0.8 34S /32S 4.4
37Cl/35Cl 32.5
81Br/79Br 97.9
减少,但分子离子峰的强度会增大,观察质荷比最大的峰是 否最后消失,最后消失的即为分子离子峰。
(二)同位素离子峰
一些同位素的天然丰度及丰度比
由于同位素的存在,
因此、分子离子峰的强度可以大致指示被测化合物的类型。
2、N律
由C、H、O组成的有机化合物,M一定是偶数。 由C、H、O、N组成的有机化合物,N奇数,M奇数。 由C、H、O、N组成的有机化合物,N偶数,M偶数。
如:醇、醚,CnH2n+2O CH3CH2OH,(CH3)2CHCH2OH 醛、酮,C2H2nO CH3COCH2CH3 CH3CHO 胺(1N),CnH2n+3N CH3NH2,CH3NHCH3,(CH3)3N 胺(2N),CnH2n+4N2 NH2CH2CH2NH2
同位素
可以看到比分子离子峰大
1H
一个质量单位的峰;有时
2H 12C
还可以观察到M+2,M+3
13C
等。
14N
15N
16O
17O
例如:CH4 M=16 12C+1H×4=16 M
13C+1H×4=17 M+1
12C+2H+1H×3=17 M+1
13C+2H+1H×3=18 M+2
18O
32S
分子离子峰
37Cl 79Br
这时碎片离子峰的强度都会
81Br
99.985 0.015 98.893 1.107 99.634 0.366 99.759 0.037 0.204 95.0 0.76 4.22 75.77 24.23 5 0.015 13C/12C 1.11
阳离子得裂解规律及分子离子峰

(一)分子离子峰的确认 分子离子峰一般位于质谱图中质荷比最高的位置,但 有时最高质荷比峰不一定是分子离子峰。因为: ①当出现M+n(n=1、2…)同位素时,同位素峰可能出 现在质荷比最高处; ②当样品不纯或仪器有污染时,杂质峰可能出现在最 高质荷比处; ③当样品分子的稳定性差时,分子离子峰很弱,甚至 不出现,此时最高质荷比的离子是碎片离子峰而非分 子离子峰。
ABCD+.
重排开裂
AD+.(重排离子)+BC(中性分子)
产生重排开裂的原因:重排离子具有更高的稳定性;能 够脱去稳定的中性分子;需要裂解的临界能较低;开裂 中心在易于移动的氢附近等。
重排开裂的类型:重排开裂的方式很多,其中较常见的有
(1)McLafferty重排(麦氏重排) (2)逆Diels-Alder重排(RDA重排)
④取代苯也能发生α裂解,产生m/z77的苯离子,进一步裂 解生成环丙烯离子m/z39及m/z51的环丁二烯离子:
⑤具有r氢的烷基取代苯,能发生McLafferty重排裂解, 产生m/z92(C7H8+.)重排离子:
综上所述,烷基取代苯的特征离子为 离子C7H7+ (m/z91)、C6H5+(m/z77)、 C5H5+ (m/z65 )、 ( m/z51 )及C3H3+(m/z39)等离子。
2.饱和脂肪醇: ①分子离子峰很弱,且随碳链的增长而减弱,以至消失 (约大于5个碳时)。如正丙醇为6%,正丁醇为1%,而 正戊醇0%或0.8%; ②易发生α裂解,生成一组 离子
③易发生脱水重排反应,产生M-18离子; ④直链伯醇会出现含羟基离子(m/z31、45、59…)、烷 基离子(m/z29、43、57…)及链烯离子(m/z27、41、 55…)3种系统的碎片离子,因此质谱峰较多。
质谱中分子离子峰的特点-概述说明以及解释

质谱中分子离子峰的特点-概述说明以及解释1.引言1.1 概述概述部分内容如下:在质谱分析领域中,分子离子峰是质谱图中的重要组成部分。
分子离子峰是由分子中的一个或多个原子失去或获得一个电子而形成的离子,具有其独特的特征。
通过分析质谱中的分子离子峰,能够揭示物质的组成成分、分子结构、分子量以及其他相关信息。
分子离子峰的特点主要包括其相对丰度、分子离子峰的相对位置和分子离子峰的形状。
相对丰度是指某个分子离子峰在质谱图中的峰高相对于其他分子离子峰的峰高的比例。
相对位置指的是不同分子离子峰之间的质荷比差异。
形状则是指分子离子峰的峰型,可以根据峰型的不同来推测分子中的官能团或基团的存在。
通过对质谱中分子离子峰特点的分析,可以帮助我们进行物质的鉴定和分析。
不同的物质在质谱图中的分子离子峰特征往往具有差异,这使得质谱分析成为一种有效的物质鉴定方法。
同时,分子离子峰的特点还可以为化学合成、分析方法的开发以及药物研发等领域提供有价值的参考。
本文将针对质谱中分子离子峰的特点进行详细的探讨和分析。
首先,我们将介绍分子离子峰的相对丰度和其在质谱图中的相对位置。
接着,我们将探讨分子离子峰的形状以及其与分子结构的关联。
最后,我们将总结本文的内容并展望分子离子峰特征在质谱分析领域的未来应用前景。
通过对质谱中分子离子峰的特点进行充分的理解和研究,不仅可以提高质谱分析的准确性和可靠性,还为化学科学的发展和实际应用提供了重要的支持和指导。
1.2文章结构文章结构部分的内容如下:本文主要分为引言、正文和结论三个部分。
引言部分主要概述了质谱中分子离子峰的特点,并介绍了文章的结构和目的。
正文部分将详细讨论分子离子峰的三个特征。
特征一将介绍分子离子峰的形态特点,包括峰的形状、峰的强度和峰的宽度等方面的内容。
特征二将探讨分子离子峰的质荷比及其在质谱图上的表现形式,以及质谱仪器中的质谱分辨率和质谱峰的分辨情况。
特征三将讨论分子离子峰的相对丰度和相对丰度的计算方法。
重排离子峰名词解释

重排离子峰名词解释
离子峰是指在质谱仪中观察到的质荷比与荷量相同的分子离子集中的状态。
离子峰是由分子在质谱仪中被离子化后形成的。
其是质谱仪中非常重要的组成部分之一。
离子峰的重排则是指在质谱仪中对已观察到的离子峰进行重新排列和编号。
以下是重排离子峰的一些常见的名词解释:
一、荷峰
荷峰是指质谱仪中观察到的离子峰中荷量最大的那个离子峰,它通常也是离子峰的主离子峰。
荷峰是界定离子峰的关键参数之一。
二、同位素峰
同位素峰是指具有相同原子数但原子量略有不同的分子离子,它们在质谱仪中会形成一组相邻的离子峰。
同位素峰之间的距离是由质量分辨率所决定的。
三、基线峰
基线峰是指在离子峰图谱中没有出现的质荷比范围内的信号,通常由仪器噪音和气体成分引起。
对离子峰分析和定量必须正确处理和减除
基线峰的干扰。
四、碎片离子
碎片离子是指分子离子在质谱仪中经过解离反应(如电子轰击、化学解离等)后形成的小分子离子。
这些离子往往是主离子峰的副产物,可以帮助分析化合物的结构。
五、挑选离子
挑选离子是指在质谱仪的离子源处选择特定的离子化方式和条件,通过挑选离子荷量或离子稳定性,得到特定的离子峰,用于更精确的物质鉴定和结构分析。
六、同分异构体离子峰
同分异构体离子峰是指化学品中具有相同化学结构但位置异构的同分异构体,在质谱仪中可能呈现出不同的离子峰。
这些离子峰通常需要通过对质谱图谱的结构分析才能进行鉴定。
以上是重排离子峰的一些常见的名词解释。
对于质谱分析人员来说,熟悉这些名词是非常重要的,有助于提高质谱分析的准确性和精度。
二_离子峰的主要类型

1、分子中含一个Cl,不含N,m/z=62 为分子离子峰; 不含Cl部分质量,62-35=27.
2、RI (M 1) 100 1.1x 4.8 RI (M )
x=4,不合理;所以x=2,y=3, 分子式:C2H3Cl,UN=1,合理.
2.同位素离子与同位素离子峰 在质谱中由重同位素组成,比分子离子或碎片离子的质
量高1、2、3、4、…等质量单位的离子称为同位素离子, 由它而形成的峰称为同位素离子峰。
例如:CH4 M=16 12C+1H×4=16 13C+1H×4=17 12C+2H+1H×3=17 13C+2H+1H×3=18
M M+1 M+1 M+2
(M+2)/M强度百分比为0.9%,M+2强度弱,说明不含Cl、
Br、S;查阅Beynon表,相对分子质量为150的化学式共有
29个,其中M+1峰的强度百分比在9%~11%的化学式共有
七种:
化学式 (M+1)/M % (M+2)/M %
① C7H10N4 ② C8H8NO2 ③ C8H10N2O ④ C8H12N3 ⑤ C9H10O2 ⑥ C9H12NO ⑦ C9H14N2
分子中含1 Cl, (a+b)1, M : M+2≈3 : 1
分子中含2 Cl, 分子中含1 Br,
(a+b)2, M : M+2 : M+4≈9 : 6 :1 (a+b)1, M : M+2≈1 : 1
分子中含2 Br, (a+b)2, M : M+2 : M+4≈1 : 2 :1 分子中含1Cl 和1Br (a+b) (c+d), M : M+2 : M+4≈3 : 4 : 1
第二节质谱中的主要离子

OH (M-15)
CH3 CH3
OH
(M-15) m/z 45来自由于碎片离子中的氧原子具有八偶体结构,其稳定性 大于分子离子。结果,促使生成的分子离子快速地裂解成 碎片离子,减少了分子离子的数值和生存时间,使得分子 离子峰的相对丰度减弱。
⑷ 结构中具有高度分支的化合物,其分子离子峰的相对 丰度也较小。这是因为在正碳离子中,稳定性的次序是叔 正离子>仲正离子>伯正离子,化合物结构中的支链多, 分子离子就容易通过裂解生成较稳定的碎片离子。
常见的失去离子类型有:
(3) 分子离子峰的质量应符合氮规则。 氮规则表述为:当化合物不含氮或含偶数个氮时,该化
合物分子量为偶数;当化合物含奇数个氮时,该化合物分 子量为奇数。
如果我们知道试样不含氮而最高质量端显示奇数质量 峰时,则该峰不是分子离子峰。 (4) M+峰和M+1┐+峰或M-1┐+峰的判别: 醚、酯、胺、酰胺、 腈化物、氨基酸酯、胺醇等可能有较强的M+1┐+峰,芳醛、 某些醇或某些化合物可能有较强的M-1┐+峰。 另:可据经验,结合裂解规律进行确认。
⑤基质辅助激光解析电离 (Matrix Assisted Laser Desorption Ionization, MALDI) 与前述的CI、FAB等软电离技术不同,该过程用的是试样与基质的 共结晶体,激光聚焦于试样表面,使试样由凝集相解吸而形成离子。
对于热敏感的化合物,如果对他们进行极快速的加热,可以避免 其加热分解。利用这个原理,采用脉冲式的激光,在一个微小的区域 内,在极短的时间间隔(纳秒数量级),激光可对靶物提供高的能量, 在极短的时间内穿越试样,对热敏感或不挥发的化合物可从固相直接 得到离子从而进行质谱分析
如甲苯的质谱图中m/z为91的碎片离子为基峰。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
二、同位素离子峰(M +1峰) 同位素离子峰( +1峰
由于同位素的存在, 由于同位素的存在,可以看到比分子离子峰大一个质量单 位的峰;有时还可以观察到 位的峰;有时还可以观察到M+2,M+3。。。。; , 。。。。;
例如: 例如:CH4 M=16 12C+1H×4=16 M 分子离子峰 × 同 13C+1H×4=17 M+1 × 位 素 12C+2H+1H×3=17 M+1 × 峰 13C+2H+1H×3=18 M+2 ×
分子离子峰的特点: 分子离子峰的特点:
一般质谱图上 质荷比最大的峰为 分子离子峰; 分子离子峰;有例 外。 形成分子离子 需要的能量最低, 需要的能量最低, 一般约10 10电子伏 一般约10电子伏 特。 质谱图上质荷比最大的峰一定为分子离子峰吗? 质谱图上质荷比最大的峰一定为分子离子峰吗? 一定为分子离子峰吗 如何确定分子离子峰? 如何确定分子离子峰?
N律
由C、H、O组成的有机化合物,M一定是偶数。 C、H、O组成的有机化合物, 一定是偶数。 组成的有机化合物 由C、H、O、N组成的有机化合物,N奇数,M奇数。 C、H、O、N组成的有机化合物,N奇数, 奇数。 组成的有机化合物,N奇数 由C、H、O、N组成的有机化合物,N偶数,M偶数。 C、H、O、N组成的有机化合物,N偶数, 偶数。 组成的有机化合物,N偶数 分子离子峰与相邻峰的质量差必须合理。 分子离子峰与相邻峰的质量差必须合理。
第十一章 质谱分析
第二节 离子峰的主要类型
一、分子离子峰 二、同位素离子峰 三、碎片离子峰
一、分子离子峰
分子电离一个电子形成的离子所产生的峰。 分子电离一个电子形成的离子所产生的峰。 分子离子的质量与化合物的相对摩尔质量相等。 分子离子的质量与化合物的相对摩尔质量相等。 有机化合物分子离子 峰的稳定性顺序: 峰的稳定性顺序: 芳香化合物>共轭链烯> 芳香化合物>共轭链烯> 烯烃>脂环化合物> 烯烃>脂环化合物>直链 烷烃> 烷烃>酮>胺>酯>醚> 支链烷烃> 酸>支链烷烃>醇。
43 C 2 H C 2 H
29 C 2 H
C 2 H C 2 H C 2 H C 2 H
C 2 H C 2 H C 2 H C 2 H
C 2 H
C 2 H
碎片离子峰
CH3
< H3C
43
CH2
< H3C CH
CH3
< H3C
C CH3 CH3
57 29 15
正癸烷
71
85 99 113 142 m/z
正 己 烷
15 HC 3 71 71 H C 3 57 H C 3 43 H C 3 29 2 H 57 C 2 H C 2 H C 2 H
57 C 2 H
71 C 2 H C 3 H 15 C 3 H C 2 H C 2 H C 2 H C 2 H C 3 H C 3 H C 3 H C 3 H
m/z 1 16 12 15 13 14 15 16 17 m/z
RA 3.1 1.0 3.9 9.2 85 100 1.1
三、碎片离子峰
一般有机化合物的电离能为7- 电子伏特 电子伏特, 一般有机化合物的电离能为 -13电子伏特,质谱中常用 的电离电压为70电子伏特,使结构裂解,产生各种“碎片” 的电离电压为 电子伏特,使结构裂解,产生各种“碎片”离 电子伏特 子。
内容选择: 内容选择:
• 第一节 基本原理与质谱仪 • 第二节 离子峰的主要类型 • 第三节 有机分子裂解类型 • 第四节 质谱图与结构解析
结束
