初中化学俗名与颜色
初三化学里的常见物质的化学式和俗称、还有常见的固体、液体的颜色

(一)、固体的颜色1、红色固体:铜,氧化铁2、绿色固体:碱式碳酸铜3、蓝色固体:氢氧化铜,硫酸铜晶体4、紫黑色固体:高锰酸钾5、淡黄色固体:硫磺6、无色固体:冰,干冰,金刚石7、银白色固体:银,铁,镁,铝,等金属8、黑色固体:铁粉,木炭,氧化铜,二氧化锰,四氧化三铁,(碳黑,活性炭)9、红褐色固体:氢氧化铁10、白色固体:氯化钠,碳酸钠,氢氧化钠,氢氧化钙,碳酸钙,氧化钙,硫酸铜,五氧化二磷,氧化镁(二)、液体的颜色11、无色液体:水,双氧水12、蓝色溶液:硫酸铜溶液,氯化铜溶液,硝酸铜溶液13、浅绿色溶液:硫酸亚铁溶液,氯化亚铁溶液,硝酸亚铁溶液14、黄色溶液:硫酸铁溶液,氯化铁溶液,硝酸铁溶液15、紫红色溶液:高锰酸钾溶液16、紫色溶液:石蕊溶液(三)、气体的颜色17、红棕色气体:二氧化氮18、黄绿色气体:氯气19、无色气体:氧气,氮气,氢气,二氧化碳,一氧化碳,二氧化硫,氯化氢气体等大多数气体。
鉴别,先看颜色,溶液中有颜色的就那几种,绿色是二价铁,黄棕是三价铁,蓝色是二价铜沉淀的颜色CU(OH)2,蓝色,FE(OH)3红褐色,剩下的都是白色,FE(OH)2也是白色的初中化学物质的检验(一)、气体的检验1、氧气:带火星的木条放入瓶中,若木条复燃,则是氧气.2、氢气:在玻璃尖嘴点燃气体,罩一干冷小烧杯,观察杯壁是否有水滴,往烧杯中倒入澄清的石灰水,若不变浑浊,则是氢气.3、二氧化碳:通入澄清的石灰水,若变浑浊则是二氧化碳.4、氨气:湿润的紫红色石蕊试纸,若试纸变蓝,则是氨气.5、水蒸气:通过无水硫酸铜,若白色固体变蓝,则含水蒸气.俗名学名化学式毒盐、硝盐(工业名称)亚硝酸钠NaNO2 酒精乙醇C2H5OH熟石灰、消石灰氢氧化钙Ca(OH)2 木酒精、木醇甲醇CH3OH生石灰氧化钙CaO 亚硫酸H2SO3醋酸(熔点16.6℃,固态称为冰醋酸)乙酸CH3COOH铜绿、孔雀石碱式碳酸铜Cu2(OH)2CO3 干冰CO2胆矾、蓝矾硫酸铜晶体CuSO4·5H2O 水银汞Hg盐镪水(工业名称)氢氯酸、盐酸HCl 金刚石、石墨C 纯碱、苏打、面碱碳酸钠Na2CO3 氢硫酸H2S纯碱晶体碳酸钠晶体Na2CO3·10H2O 氨水一水合氨NH3·H2O 酸式碳酸钠、小苏打碳酸氢钠NaHCO3苛性钠、火碱、烧碱氢氧化钠NaOH物质的检验(1)酸(H+)检验。
初中常见化学物质及其俗称

一、物质的学名、俗名及化学式⑴金刚石、石墨:C⑵水银、汞:Hg (3)生石灰、氧化钙:CaO(4)干冰(固体二氧化碳):CO2 (5)盐酸、氢氯酸:HCl(6)亚硫酸:H2SO3 (7)氢硫酸:H2S (8)熟石灰、消石灰:Ca(OH)2 (9)苛性钠、火碱、烧碱:NaOH (10)纯碱:Na2CO3 碳酸钠晶体、纯碱晶体:Na2CO3?10H2O (11)碳酸氢钠、酸式碳酸钠:NaHCO3 (也叫小苏打)(12)胆矾、蓝矾、硫酸铜晶体:CuSO4?5H2O (13)铜绿、孔雀石:Cu2(OH)2CO3(分解生成三种氧化物的物质)(14)甲醇:CH3OH 有毒、失明、死亡(15)酒精、乙醇:C2H5OH (16)醋酸、乙酸(16.6℃冰醋酸)CH3COOH (CH3COO- 醋酸根离子)具有酸的通性(17)氨气:NH3 (碱性气体)(18)氨水、一水合氨:NH3?H2O(为常见的碱,具有碱的通性,是一种不含金属离子的碱)(19)亚硝酸钠:NaNO2 (工业用盐、有毒)二、常见物质的颜色的状态1、白色固体:MgO、P2O5、CaO、NaOH、Ca(OH)2、KClO3、KCl、Na2CO3、NaCl、无水CuSO4;铁、镁为银白色(汞为银白色液态)2、黑色固体:石墨、炭粉、铁粉、CuO、MnO2、Fe3O4▲KMnO4为紫黑色3、红色固体:Cu、Fe2O3 、HgO、红磷▲硫:淡黄色▲ Cu2(OH)2CO3为绿色4、溶液的颜色:凡含Cu2+的溶液呈蓝色;凡含Fe2+的溶液呈浅绿色;凡含Fe3+的溶液呈棕黄色,其余溶液一般不无色。
(高锰酸钾溶液为紫红色)5、沉淀(即不溶于水的盐和碱):①盐:白色↓:CaCO3、BaCO3(溶于酸)AgCl、BaSO4(也不溶于稀HNO3) 等②碱:蓝色↓:Cu(OH)2 红褐色↓:Fe(OH)3白色↓:其余碱。
6、(1)具有刺激性气体的气体:NH3、SO2、HCl(皆为无色)(2)无色无味的气体:O2、H2、N2、CO2、CH4、CO(剧毒)▲注意:具有刺激性气味的液体:盐酸、硝酸、醋酸。
初中化学常见物质俗名、物质颜色

初中化学常见物质俗名、物质颜色初中化学常见物质俗名、物质颜色一、物质的学名、俗名及化学式⑴金刚石、石墨:C⑵水银、汞:Hg(3)生石灰、氧化钙:CaO(4)干冰(固体二氧化碳):CO2(5)盐酸、氢氯酸:HCl(6)亚硫酸:H2SO3(7)氢硫酸:H2S(8)熟石灰、消石灰:Ca(OH)2(9)苛性钠、火碱、烧碱:NaOH(10)纯碱:Na2CO3 碳酸钠晶体、纯碱晶体:Na2CO3?10H2O(11)碳酸氢钠、酸式碳酸钠:NaHCO3 (也叫小苏打)(12)胆矾、蓝矾、硫酸铜晶体:CuSO4?5H2O(13)铜绿、孔雀石:Cu2(OH)2CO3(分解生成三种氧化物的物质)(14)甲醇:CH3OH 有毒、失明、死亡(15)酒精、乙醇:C2H5OH(16)醋酸、乙酸(16.6℃冰醋酸)CH3COOH(CH3COO- 醋酸根离子) 具有酸的通性(17)氨气:NH3 (碱性气体)(18)氨水、一水合氨:NH3?H2O(为常见的碱,具有碱的通的粘稠状物质——波尔多液)三、物质的溶解性1、盐的溶解性含有钾、钠、硝酸根、铵根的物质都溶于水含Cl的化合物只有AgCl不溶于水,其他都溶于水; 含SO42- 的化合物只有BaSO4 不溶于水,其他都溶于水。
含CO32- 的物质只有K2CO3、Na2CO3、(NH4)2CO3溶于水,其他都不溶于水2、碱的溶解性溶于水的碱有:氢氧化钡、氢氧化钾、氢氧化钙、氢氧化钠和氨水,其他碱不溶于水。
难溶性碱中Fe(OH)3是红褐色沉淀,Cu(OH)2是蓝色沉淀,其他难溶性碱为白色。
(包括Fe(OH)2)注意:沉淀物中AgCl和BaSO4 不溶于稀硝酸,其他沉淀物能溶于酸。
如:Mg(OH)2 CaCO3 BaCO3 Ag2 CO3 等3、大部分酸及酸性氧化物能溶于水,(酸性氧化物+水→酸)大部分碱性氧化物不溶于水,能溶的有:氧化钡、氧化钾、氧化钙、氧化钠(碱性氧化物+水→碱)四、化学之最1、地壳中含量最多的金属元素是铝。
初中化学常见物质的颜色归纳总结

初中化学常见物质的颜色归纳总结初中化学常见物质的颜色归纳总结固体物质的颜色白色固体:氧化镁MgO、五氧化二磷P2O5、氧化钙CaO、氢氧化钙Ca(OH)2、碳酸钠Na2CO3、碳酸钙CaCO3、氯酸钾KClO3、氯化钾KCl、氢氧化钠NaOH、无水硫酸铜CuSO4等。
黄色固体:硫粉S。
红色固体:红磷P、氧化铁Fe2O3、铜Cu。
蓝色固体:胆矾CuSO4·5H2O。
黑色固体:木炭C、氧化铜CuO、二氧化锰MnO2、四氧化三铁Fe3O4、生铁Fe。
绿色固体:碱式碳酸铜Cu2(OH)2CO3.紫黑色固体:高锰酸钾KMnO4.无色固体:冰,干冰,金刚石。
银白色固体:银,铁,镁,铝,汞等金属。
生成沉淀的颜色白色沉淀:不溶于水也不溶于稀硝酸的氯化银AgCl和硫酸钡BaSO4.不溶于水但溶于稀硝酸或稀盐酸的氢氧化镁Mg(OH)2、碳酸钙CaCO3、碳酸钡BaCO3.红褐色沉淀:氢氧化铁Fe(OH)3.蓝色沉淀:氢氧化铜Cu(OH)2.溶液的颜色蓝色溶液Cu2+:硫酸铜CuSO4、硝酸铜Cu(NO3)2、氯化铜CuCl2等。
黄色溶液Fe3+:氯化铁FeCl3、硫酸铁Fe2(SO4)3、硝酸铁Fe(NO3)3等。
浅绿色溶液Fe2+:氯化亚铁FeCl2、硫酸亚铁FeSO4、硝酸亚铁Fe(NO3)2等。
无色液体:水,双氧水。
紫红色溶液:高锰酸钾溶液。
紫色溶液:石蕊溶液。
气体的颜色红棕色气体:二氧化氮。
黄绿色气体:氯气。
无色气体:氧气,氮气,氢气,二氧化碳,一氧化碳,二氧化硫,氯化氢气体等大多数气体。
常见物质的学名、俗名及化学式1.金刚石、石墨:C。
2.水银、汞:Hg。
3.生石灰、氧化钙:CaO。
4.干冰(固体二氧化碳):CO2.5.盐酸、氢氯酸:HCl。
6.亚硫酸:H2SO3.7.氢硫酸:H2S。
8.熟石灰、消石灰:Ca(OH)2.9.苛性钠、火碱、烧碱:NaOH。
10.纯碱、碳酸钠晶体、纯碱晶体:Na2CO3·10H2O。
初中常用的化学式-、俗名和化学方程式
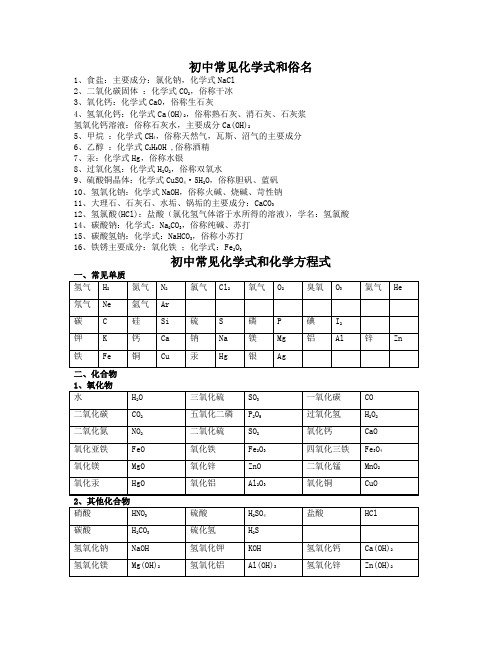
初中常见化学式和俗名1、食盐:主要成分:氯化钠,化学式NaCl2、二氧化碳固体:化学式CO2,俗称干冰3、氧化钙:化学式CaO,俗称生石灰4、氢氧化钙:化学式Ca(OH)2,俗称熟石灰、消石灰、石灰浆氢氧化钙溶液:俗称石灰水,主要成分Ca(OH)25、甲烷:化学式CH4,俗称天然气,瓦斯、沼气的主要成分6、乙醇:化学式C2H5OH ,俗称酒精7、汞:化学式Hg,俗称水银8、过氧化氢:化学式H2O2,俗称双氧水9、硫酸铜晶体:化学式CuSO4·5H2O,俗称胆矾、蓝矾10、氢氧化钠:化学式NaOH,俗称火碱、烧碱、苛性钠11、大理石、石灰石、水垢、锅垢的主要成分:CaCO312、氢氯酸(HCl):盐酸(氯化氢气体溶于水所得的溶液),学名:氢氯酸14、碳酸钠:化学式:Na2CO3,俗称纯碱、苏打15、碳酸氢钠:化学式:NaHCO3,俗称小苏打16、铁锈主要成分:氧化铁;化学式:Fe2O3初中常见化学式和化学方程式一、化合反应1.镁在空气中燃烧:2Mg + O2点燃 2Mg2. 铁在氧气中燃烧:3Fe + 2O2点燃 Fe3O43. 铜在空气中受热:2Cu + O2加热 2CuO4. 铝在空气中燃烧:4Al + 3O2点燃 2Al2O35. 氢气中空气中燃烧:2H2 + O2点燃 2H2O6. 红磷在空气中燃烧:4P + 5O2点燃 2P2O57. 硫粉在空气中燃烧: S + O2点燃 SO28. 碳在氧气中充分燃烧:C + O2点燃 CO29. 碳在氧气中不充分燃烧:2C + O2点燃 2CO10.一氧化碳在氧气中燃烧:2CO + O2点燃 2CO211.二氧化碳和水反应生成碳酸:CO2 + H2O= H2CO312.二氧化碳通过灼热的炭层:CO2+ C 2CO13.二氧化碳溶解于水:CO2 + H2O=H2CO314.生石灰溶于水:CaO + H2O = Ca(OH)215.三氧化硫溶于水:SO3 + H2O = H2SO416.无水硫酸铜作干燥剂:CuSO4 + 5H2O = CuSO4·5H2O二、分解反应高温17.2H 2O 通电2H 2↑+ O 2 ↑18. 过氧化氢分解:2O+O 2 ↑19.加热氯酸钾(有少量的二氧化锰):2KClO 2 ↑ 20.加热高锰酸钾:2KMnO 4 加热 K 2MnO 4 + MnO 2 + O 2↑ 21.碳酸不稳定而分解:H 2CO 3 === H 2O + CO 2↑ 22.高温煅烧石灰石:CaCO 3 高温 CaO + CO 2↑23.硫酸铜晶体受热分解:CuSO 4·5H 2O 加热 CuSO 4 + 5H 2O 三、置换反应24.氢气还原氧化铜:H 2 + CuO 加热 Cu + H 2O 25.木炭还原氧化铜:C+ 2CuO 高温 2Cu + CO 2↑ 26.焦炭还原氧化铁:3C+ 2Fe 2O 3 高温 4Fe + 3CO 2↑ 27.焦炭还原四氧化三铁:2C+ Fe 3O 4 高温 3Fe + 2CO 2↑ 金属单质 + 酸 -------- 盐 + 氢气 28.锌和稀硫酸Zn + H 2SO 4 = ZnSO 4 + H 2↑ 29.铁和稀硫酸Fe + H 2SO 4 = FeSO 4 + H 2↑ 30.镁和稀硫酸Mg + H 2SO 4 = MgSO 4 + H 2↑31.铝和稀硫酸2Al +3H 2SO 4 = Al 2(SO 4)3 +3H 2↑ 32.锌和稀盐酸Zn + 2HCl === ZnCl 2 + H 2↑ 33..铁和稀盐酸Fe + 2HCl === FeCl 2 + H 2↑34.镁和稀盐酸Mg+ 2HCl === MgCl 2 + H 2↑35.铝和稀盐酸2Al + 6HCl == 2AlCl 3 + 3H 2↑(2)金属单质 + 盐(溶液) ------- 另一种金属 + 另一种盐 36.铁和硫酸铜溶液反应:Fe + CuSO 4 === FeSO 4 + Cu 37.锌和硫酸铜溶液反应:Zn + CuSO 4 === ZnSO 4 + Cu38.铜和硝酸汞溶液反应:Cu + Hg(NO 3)2 === Cu(NO 3)2 + Hg 四、复分解反应(1)碱性氧化物 +酸 -------- 盐 + 水39.氧化铁和稀盐酸反应:Fe 2O 3 + 6HCl === 2FeCl 3 + 3H 2O 40.氧化铁和稀硫酸反应:Fe 2O 3 + 3H 2SO 4 === Fe 2(SO 4)3 + 3H 2O 41.氧化铜和稀盐酸反应:CuO + 2HCl ==== CuCl 2 + H 2O 42.氧化铜和稀硫酸反应:CuO + H 2SO 4 ==== CuSO 4 + H 2O 43.氧化镁和稀硫酸反应:MgO + H 2SO 4 ==== MgSO 4 + H 2O 44.氧化钙和稀盐酸反应:CaO + 2HCl ==== CaCl 2 + H 2O (2)酸 + 碱 -------- 盐 + 水45.硫酸和烧碱反应:H 2SO 4 + 2NaOH ==== Na 2SO 4 + 2H 2O 46.硫酸和氢氧化钾反应:H 2SO 4 + 2KOH ==== K 2SO 4 + 2H 2O47.硫酸和氢氧化铜反应:H2SO4+ Cu(OH)2==== CuSO4+ 2H2O48.硫酸和氢氧化铁反应:3H2SO4+ 2Fe(OH)3==== Fe2(SO4)3+ 6H2O49.盐酸和氢氧化钾反应:HCl + KOH ==== KCl +H2O50.盐酸和氢氧化铜反应:2HCl + Cu(OH)2 ==== CuCl2+ 2H2O51.盐酸和氢氧化钙反应:2HCl + Ca(OH)2 ==== CaCl2+ 2H2O52.盐酸和氢氧化铁反应:3HCl + Fe(OH)3 ==== FeCl3+ 3H2O53.氢氧化铝药物治疗胃酸过多:3HCl + Al(OH)3 ==== AlCl3+ 3H2O54.盐酸和烧碱起反应:HCl + NaOH ==== NaCl +H2O55.硝酸和烧碱反应:HNO3+ NaOH ==== NaNO3+H2O(3)酸 + 盐 -------- 另一种酸 + 另一种盐56.大理石与稀盐酸反应:CaCO3 + 2HCl === CaCl2+ H2O + CO2↑57.碳酸钠与稀盐酸反应: Na2CO3+ 2HCl === 2NaCl + H2O + CO2↑58.碳酸镁与稀盐酸反应: MgCO3 + 2HCl === MgCl2+ H2O + CO2↑59.盐酸和硝酸银溶液反应:HCl + AgNO3 === AgCl↓ + HNO360.硫酸和碳酸钠反应:Na2CO3+ H2SO4=== Na2SO4+ H2O + CO2↑61.硫酸和氯化钡溶液反应:H2SO4+ BaCl2==== BaSO4↓+ 2HCl(4)碱 + 盐 -------- 另一种碱 + 另一种盐62.氢氧化钠与硫酸铜:2NaOH + CuSO4 ==== Cu(OH)2↓ + Na2SO463.氢氧化钠与氯化铁:3NaOH + FeCl3 ==== Fe(OH)3↓ + 3NaCl64.氢氧化钠与氯化镁:2NaOH + MgCl2 ==== Mg(OH)2↓ + 2NaCl65.氢氧化钠与氯化铜:2NaOH + CuCl2 ==== Cu(OH)2↓ + 2NaCl66.氢氧化钙与碳酸钠:Ca(OH)2 + Na2CO3=== CaCO3↓+ 2NaOH(5)盐 + 盐 ----- 两种新盐67.氯化钠溶液和硝酸银溶液:NaCl + AgNO3 ==== AgCl↓ + NaNO368.硫酸钠和氯化钡:Na2SO4+ BaCl2==== BaSO4↓ + 2NaCl五、其他反应类型69.二氧化碳通入澄清石灰水中:CO2 + Ca(OH)2== CaCO3↓+ H2O70.消石灰吸收二氧化硫:Ca(OH)2 + SO2==== CaSO3↓+ H2O71.氢氧化钠溶液吸收二氧化硫:SO2 + 2NaOH==Na2SO3+ H2O72.氢氧化钠在空气中变质:CO2+ 2NaOH = Na2CO3+ H2O73.苛性钠吸收三氧化硫气体:2NaOH + SO3 ==== Na2SO4+ H2O74.一氧化碳还原氧化铜:CO + CuO Cu + CO275、酒精燃烧:C2H5OH + 3O22CO2+ 3H2O76、甲烷燃烧:CH4 + 2O2CO2+ 2H2O△点燃点燃。
初中化学常见物质的颜色归纳总结

初中化学常见物质的颜色归纳总结固体物质的颜色白色固体:氧化镁 MgO 、五氧化二磷 P2O5、氧化钙 CaO 、氢氧化钙Ca(OH)2、碳酸钠Na2CO3、碳酸钙CaCO3、氯酸钾KClO3、氯化钾KCl、氢氧化钠NaOH、无水硫酸铜CuSO4等。
黄色固体:硫粉S红色固体:红磷P、氧化铁Fe2O3、铜Cu蓝色固体:胆矾CuSO4·5H2O黑色固体:木炭C、氧化铜CuO、二氧化锰MnO2、四氧化三铁Fe3O4、生铁Fe绿色固体:碱式碳酸铜Cu2(OH)2CO3紫黑色固体:高锰酸钾KMnO4无色固体:冰,干冰,金刚石银白色固体:银,铁,镁,铝,汞等金属生成沉淀的颜色白色沉淀:不溶于水也不溶于稀硝酸:氯化银AgCl、硫酸钡BaSO4。
不溶于水但溶于稀硝酸或稀盐酸:氢氧化镁Mg(OH)2、碳酸钙CaCO3、碳酸钡BaCO3红褐色沉淀:氢氧化铁Fe(OH)3蓝色沉淀:氢氧化铜 Cu(OH)2溶液的颜色蓝色溶液Cu2+:硫酸铜CuSO4、硝酸铜Cu(NO3)2、氯化铜CuCl2等黄色溶液Fe3+:氯化铁FeCl3、硫酸铁Fe2(SO4)3、硝酸铁Fe(NO3)3等浅绿色溶液Fe2+:氯化亚铁FeCl2、硫酸亚铁FeSO4、硝酸亚铁Fe(NO3)2等无色液体:水,双氧水紫红色溶液:高锰酸钾溶液紫色溶液:石蕊溶液气体的颜色红棕色气体:二氧化氮黄绿色气体:氯气无色气体:氧气,氮气,氢气,二氧化碳,一氧化碳,二氧化硫,氯化氢气体等大多数气体。
常见物质的学名、俗名及化学式⑴金刚石、石墨:C⑵水银、汞:Hg(3)生石灰、氧化钙:CaO(4)干冰(固体二氧化碳):CO2(5)盐酸、氢氯酸:HCl(6)亚硫酸:H2SO3(7)氢硫酸:H2S(8)熟石灰、消石灰:Ca(OH)2(9)苛性钠、火碱、烧碱:NaOH(10)纯碱:Na2CO3碳酸钠晶体、纯碱晶体:Na2CO3·10H2O(11)碳酸氢钠、酸式碳酸钠:NaHCO3 (也叫小苏打)(12)胆矾、蓝矾、硫酸铜晶体:CuSO4·5H2O(13)铜绿、孔雀石:Cu2(OH)2CO3(分解生成三种氧化物的物质)(14)甲醇:CH3OH 有毒、失明、死亡(15)酒精、乙醇:C2H5OH(16)醋酸、乙酸(16.6℃冰醋酸)CH3COOH(CH3COO-醋酸根离子)具有酸的通性(17)氨气:NH3(碱性气体)(18)氨水、一水合氨:NH3·H2O(为常见的碱,具有碱的通性,是一种不含金属离子的碱)(19)亚硝酸钠:NaNO2(工业用盐、有毒)。
初中常用的化学式俗名和化学方程式
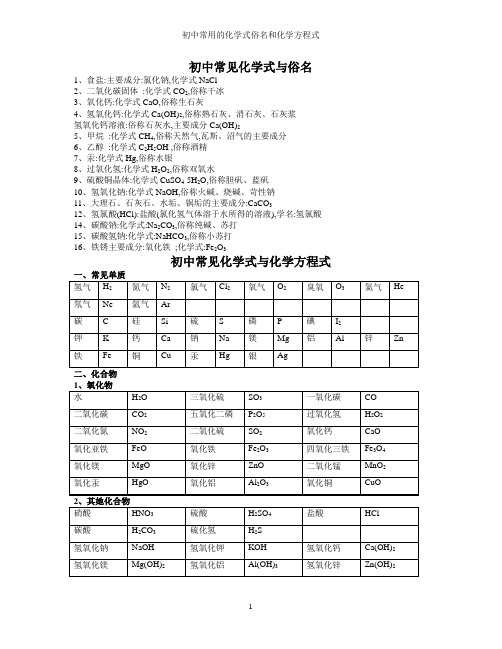
初中常见化学式与俗名1、食盐:主要成分:氯化钠,化学式NaCl2、二氧化碳固体:化学式CO2,俗称干冰3、氧化钙:化学式CaO,俗称生石灰4、氢氧化钙:化学式Ca(OH)2,俗称熟石灰、消石灰、石灰浆氢氧化钙溶液:俗称石灰水,主要成分Ca(OH)25、甲烷:化学式CH4,俗称天然气,瓦斯、沼气的主要成分6、乙醇:化学式C2H5OH ,俗称酒精7、汞:化学式Hg,俗称水银8、过氧化氢:化学式H2O2,俗称双氧水9、硫酸铜晶体:化学式CuSO4·5H2O,俗称胆矾、蓝矾10、氢氧化钠:化学式NaOH,俗称火碱、烧碱、苛性钠11、大理石、石灰石、水垢、锅垢的主要成分:CaCO312、氢氯酸(HCl):盐酸(氯化氢气体溶于水所得的溶液),学名:氢氯酸14、碳酸钠:化学式:Na2CO3,俗称纯碱、苏打15、碳酸氢钠:化学式:NaHCO3,俗称小苏打16、铁锈主要成分:氧化铁;化学式:Fe2O3初中常见化学式与化学方程式一、化合反应1.镁在空气中燃烧:2Mg + O2点燃2Mg2、铁在氧气中燃烧:3Fe + 2O2点燃Fe3O43、铜在空气中受热:2Cu + O2加热2CuO4、铝在空气中燃烧:4Al + 3O2点燃2Al2O35、氢气中空气中燃烧:2H2 + O2点燃2H2O6、红磷在空气中燃烧:4P + 5O2点燃2P2O57、硫粉在空气中燃烧: S + O2点燃SO28、碳在氧气中充分燃烧:C + O2点燃CO29、碳在氧气中不充分燃烧:2C + O2点燃2CO10、一氧化碳在氧气中燃烧:2CO + O2点燃2CO211、二氧化碳与水反应生成碳酸:CO2 + H2O= H2CO3高温12、二氧化碳通过灼热的炭层:CO2 + C 2CO13、二氧化碳溶解于水:CO2 + H2O=H2CO314、生石灰溶于水:CaO + H2O = Ca(OH)215、三氧化硫溶于水:SO3 + H2O = H2SO416、无水硫酸铜作干燥剂:CuSO4 + 5H2O = CuSO4·5H2O二、分解反应172O 通电2H 2↑+ O 2 ↑18、 过氧化氢分解:2H 22O+O 2 ↑19、加热氯酸钾(有少量的二氧化锰):2KClO 3 2 ↑ 20、加热高锰酸钾:2KMnO 4 加热 K 2MnO 4 + MnO 2 + O 2↑ 21、碳酸不稳定而分解:H 2CO 3 === H 2O + CO 2↑ 22、高温煅烧石灰石:CaCO 3 高温 CaO + CO 2↑23、硫酸铜晶体受热分解:CuSO 4·5H 2O 加热 CuSO 4 + 5H 2O 三、置换反应24、氢气还原氧化铜:H 2 + CuO 加热 Cu + H 2O 25、木炭还原氧化铜:C+ 2CuO 高温 2Cu + CO 2↑ 26、焦炭还原氧化铁:3C+ 2Fe 2O 3 高温 4Fe + 3CO 2↑ 27、焦炭还原四氧化三铁:2C+ Fe 3O 4 高温 3Fe + 2CO 2↑ 金属单质 + 酸 -------- 盐 + 氢气28、锌与稀硫酸Zn + H 2SO 4 = ZnSO 4 + H 2↑ 29、铁与稀硫酸Fe + H 2SO 4 = FeSO 4 + H 2↑ 30、镁与稀硫酸Mg + H 2SO 4 = MgSO 4 + H 2↑ 31、铝与稀硫酸2Al +3H 2SO 4 = Al 2(SO 4)3 +3H 2↑ 32、锌与稀盐酸Zn + 2HCl === ZnCl 2 + H 2↑ 33、、铁与稀盐酸Fe + 2HCl === FeCl 2 + H 2↑ 34、镁与稀盐酸Mg+ 2HCl === MgCl 2 + H 2↑ 35、铝与稀盐酸2Al + 6HCl == 2AlCl 3 + 3H 2↑(2)金属单质 + 盐(溶液) ------- 另一种金属 + 另一种盐 36、铁与硫酸铜溶液反应:Fe + CuSO 4 === FeSO 4 + Cu 37、锌与硫酸铜溶液反应:Zn + CuSO 4 === ZnSO 4 + Cu38、铜与硝酸汞溶液反应:Cu + Hg(NO 3)2 === Cu(NO 3)2 + Hg 四、复分解反应(1)碱性氧化物 +酸 -------- 盐 + 水39、氧化铁与稀盐酸反应:Fe 2O 3 + 6HCl === 2FeCl 3 + 3H 2O 40、氧化铁与稀硫酸反应:Fe 2O 3 + 3H 2SO 4 === Fe 2(SO 4)3 + 3H 2O 41、氧化铜与稀盐酸反应:CuO + 2HCl ==== CuCl 2 + H 2O 42、氧化铜与稀硫酸反应:CuO + H 2SO 4 ==== CuSO 4 + H 2O 43、氧化镁与稀硫酸反应:MgO + H 2SO 4 ==== MgSO 4 + H 2O 44、氧化钙与稀盐酸反应:CaO + 2HCl ==== CaCl 2 + H 2O (2)酸 + 碱 -------- 盐 + 水45、硫酸与烧碱反应:H 2SO 4 + 2NaOH ==== Na 2SO 4 + 2H 2O 46、硫酸与氢氧化钾反应:H 2SO 4 + 2KOH ==== K 2SO 4 + 2H 2O47、硫酸与氢氧化铜反应:H 2SO 4 + Cu(OH)2 ==== CuSO 4 + 2H 2O 48、硫酸与氢氧化铁反应:3H 2SO 4 + 2Fe(OH)3==== Fe 2(SO 4)3 + 6H 2O 49、盐酸与氢氧化钾反应:HCl + KOH ==== KCl +H 2O50、盐酸与氢氧化铜反应:2HCl + Cu(OH)2 ==== CuCl 2 + 2H 2O 51、盐酸与氢氧化钙反应:2HCl + Ca(OH)2 ==== CaCl 2 + 2H 2O 52、盐酸与氢氧化铁反应:3HCl + Fe(OH)3 ==== FeCl 3 + 3H 2O53、氢氧化铝药物治疗胃酸过多:3HCl + Al(OH)3 ==== AlCl 3 + 3H 2O 54、盐酸与烧碱起反应:HCl + NaOH ==== NaCl +H 2O 55、硝酸与烧碱反应:HNO 3+ NaOH ==== NaNO 3 +H 2O (3)酸 + 盐 -------- 另一种酸 + 另一种盐56、大理石与稀盐酸反应:CaCO 3 + 2HCl === CaCl 2 + H 2O + CO 2↑ 57、碳酸钠与稀盐酸反应: Na 2CO 3 + 2HCl === 2NaCl + H 2O + CO 2↑ 58、碳酸镁与稀盐酸反应: MgCO 3 + 2HCl === MgCl 2 + H 2O + CO 2↑ 59、盐酸与硝酸银溶液反应:HCl + AgNO 3 === AgCl ↓ + HNO 3 60、硫酸与碳酸钠反应:Na 2CO 3 + H 2SO 4 === Na 2SO 4 + H 2O + CO 2↑ 61、硫酸与氯化钡溶液反应:H 2SO 4 + BaCl 2 ==== BaSO 4 ↓+ 2HCl (4)碱 + 盐 -------- 另一种碱 + 另一种盐62、氢氧化钠与硫酸铜:2NaOH + CuSO 4 ==== Cu(OH)2↓ + Na 2SO 4 63、氢氧化钠与氯化铁:3NaOH + FeCl 3 ==== Fe(OH)3↓ + 3NaCl 64、氢氧化钠与氯化镁:2NaOH + MgCl 2 ==== Mg(OH)2↓ + 2NaCl 65、氢氧化钠与氯化铜:2NaOH + CuCl 2 ==== Cu(OH)2↓ + 2NaCl 66、氢氧化钙与碳酸钠:Ca(OH)2 + Na 2CO 3 === CaCO 3↓+ 2NaOH (5)盐 + 盐 ----- 两种新盐67、氯化钠溶液与硝酸银溶液:NaCl + AgNO 3 ==== AgCl ↓ + NaNO 3 68、硫酸钠与氯化钡:Na 2SO 4 + BaCl 2 ==== BaSO 4↓ + 2NaCl 五、其她反应类型69、二氧化碳通入澄清石灰水中:CO 2 + Ca(OH)2 == CaCO 3↓+ H 2O 70、消石灰吸收二氧化硫:Ca(OH)2 + SO 2 ==== CaSO 3 ↓+ H 2O 71、氢氧化钠溶液吸收二氧化硫:SO 2 + 2NaOH ==Na 2SO 3+ H 2O 72、氢氧化钠在空气中变质:CO 2+ 2NaOH = Na 2CO 3 + H 2O73、苛性钠吸收三氧化硫气体:2NaOH + SO 3 ==== Na 2SO 4 + H 2O74、一氧化碳还原氧化铜:CO + CuO Cu + CO 275、酒精燃烧:C 2H 5OH + 3O 2 2CO 2 + 3H 2O 76、甲烷燃烧:CH 4 + 2O 2 CO 2 + 2H 2O△点燃点燃。
俗称大全

初中常见化学物质俗称大全初中化学常见沉淀物质红褐色絮状沉淀------Fe(OH)3浅绿色沉淀------------Fe(OH)2蓝色絮状沉淀----- ---Cu(OH)2白色沉淀-------- ------CaCO3,BaCO3,AgCl,BaSO4,(其中BaSO4、AgCl是不溶于HNO3的白色沉淀,CaCO3 BaCO3是溶于HNO3的白色沉淀),Mg(OH)2.淡黄色沉淀(水溶液中)----S 微溶于水----- -- -----Ca(OH)2,CaSO4初中化学知识总结一、物质的学名、俗名及化学式⑴金刚石、石墨:C ⑵水银、汞:Hg (3)生石灰、氧化钙:CaO (4)干冰(固体二氧化碳):CO2(5)盐酸、氢氯酸:HCl (6)亚硫酸:H2SO3(7)氢硫酸:H2S (8)熟石灰、消石灰:Ca(OH)2(9)苛性钠、火碱、烧碱:NaOH (10)纯碱:Na2CO3碳酸钠晶体、纯碱晶体:Na2CO3·10H2O(11)碳酸氢钠、酸式碳酸钠:NaHCO3 (也叫小苏打) (12)胆矾、蓝矾、硫酸铜晶体:CuSO4·5H2O(13)铜绿、孔雀石:Cu2(OH)2CO3(分解生成三种氧化物的物质) (14)甲醇:CH3OH 有毒、失明、死亡(15)酒精、乙醇:C2H5OH (16)醋酸、乙酸(16.6℃冰醋酸)CH3COOH(CH3COO-醋酸根离子)具有酸的通性(17)氨气:NH3(碱性气体)(18)氨水、一水合氨:NH3·H2O(为常见的碱,具有碱的通性,是一种不含金属离子的碱)(19)亚硝酸钠:NaNO2(工业用盐、有毒)二、常见物质的颜色的状态1、白色固体:MgO、P2O5、CaO、 NaOH、Ca(OH)2、KClO3、KCl、Na2CO3、NaCl、无水CuSO4;铁、镁为银白色(汞为银白色液态)2、黑色固体:石墨、炭粉、铁粉、CuO、MnO2、Fe3O4▲KMnO4为紫黑色3、红色固体:Cu、Fe2O3、HgO、红磷▲硫:淡黄色▲ Cu2(OH)2CO3为绿色4、溶液的颜色:凡含Cu2+的溶液呈蓝色;凡含Fe2+的溶液呈浅绿色;凡含Fe3+的溶液呈棕黄色,其余溶液一般不无色。
初中化学常见物质的学名、俗名及化学式

初中化学常见物质的学名、俗名及化学式一、物质的学名、俗名及化学式⑴金刚石、石墨:C⑵水银、汞:Hg(3)生石灰、氧化钙:CaO(4)干冰(固体二氧化碳):CO2(5)盐酸、氢氯酸:HCl(6)亚硫酸:H2SO3(7)氢硫酸:H2S(8)熟石灰、消石灰:Ca(OH)2 (9)苛性钠、火碱、烧碱:NaOH(10)纯碱:Na2CO3碳酸钠晶体、纯碱晶体:Na2CO310H2O(11)碳酸氢钠、酸式碳酸钠:NaHCO3(也叫小苏打)(12)胆矾、蓝矾、硫酸铜晶体:CuSO45H2O(13)铜绿、孔雀石:Cu2(OH)2CO3(分解生成三种氧化物的物质)(14)甲醇:CH3OH有毒、失明、死亡(15)酒精、乙醇:C2H5 OH(16)醋酸、乙酸(16.6℃冰醋酸)CH3COOH(CH3COO- 醋酸根离子)具有酸的通性(17)氨气:NH3(碱性气体)(18)氨水、一水合氨:NH3H2O(为常见的碱,具有碱的通性,是一种不含金属离子的碱)(19)亚硝酸钠:NaNO2(工业用盐、有毒)二、常见物质的颜色的状态1、白色固体:MgO、P2O5、CaO、NaOH、Ca(OH)2、KClO3、KCl、Na2CO3、NaCl、无水CuSO4;铁、镁为银白色(汞为银白色液态)2、黑色固体:石墨、炭粉、铁粉、CuO、MnO2、Fe3O4▲KMnO4为紫黑色3、红色固体:Cu、Fe2O3、HgO、红磷▲硫:淡黄色▲Cu2(OH)2CO3为绿色4、溶液的颜色:凡含Cu2+的溶液呈蓝色;凡含Fe2+的溶液呈浅绿色;凡含Fe3+的溶液呈棕黄色,其余溶液一般不无色。
(高锰酸钾溶液为紫红色)5、沉淀(即不溶于水的盐和碱):①盐:白色↓:CaCO3、BaCO3(溶于酸)AgCl、BaSO4(也不溶于稀HNO3) 等②碱:蓝色↓:Cu(OH)2红褐色↓:Fe(OH)3白色↓:其余碱。
6、(1)具有刺激性气体的气体:NH3、SO2、HCl(皆为无色)(2)无色无味的气体:O2、H2、N2、CO2、CH4、CO(剧毒)▲注意:具有刺激性气味的液体:盐酸、硝酸、醋酸。
(中考复习)初中化学常见物质颜色及溶解性

初中化学知识总结(识记部分)百度文库专供中考资料:巅峰丶晓亮一、物质的学名、俗名及化学式(1)金刚石、石墨:C(2)水银、汞:Hg(3)生石灰、氧化钙:CaO(4)干冰(固体二氧化碳):CO2(5)盐酸、氢氯酸:HCl(6)亚硫酸:H2SO3(7)氢硫酸:H2S(8)熟石灰、消石灰:Ca(OH)2(9)苛性钠、火碱、烧碱:NaOH(10)纯碱:Na2CO3碳酸钠晶体、纯碱晶体:Na2CO3·10H2O(11)碳酸氢钠、酸式碳酸钠:NaHCO3 (也叫小苏打)(12)胆矾、蓝矾、硫酸铜晶体:CuSO4·5H2O(13)铜绿、孔雀石:Cu2(OH)2CO3(分解生成三种氧化物的物质)(14)甲醇:CH3OH 有毒、失明、死亡(15)酒精、乙醇:C2H5OH(16)醋酸、乙酸(16.6℃冰醋酸)CH3COOH (CH3COO- 醋酸根离子)具有酸的通性(17)氨气:NH3(碱性气体)(18)氨水、一水合氨:NH3·H2O(为常见的碱,具有碱的通性,是一种不含金属离子的碱)(19)亚硝酸钠:NaNO2(工业用盐、有毒)二、常见物质的颜色的状态1、白色固体:MgO、P2O5、CaO、NaOH、Ca(OH)2、KClO3、KCl、Na2CO3、NaCl、无水CuSO4;铁、镁为银白色(汞为银白色液态)2、黑色固体:石墨、炭粉、铁粉、CuO、MnO2、Fe3O4、KMnO4为紫黑色3、红色固体:Cu、Fe2O3、HgO、红磷、硫:淡黄色、Cu2(OH)2CO3为绿色4、溶液的颜色:凡含Cu2+的溶液呈蓝色;凡含Fe2+的溶液呈浅绿色;凡含Fe3+的溶液呈棕黄色,其余溶液一般不无色。
(高锰酸钾溶液为紫红色)5、沉淀(即不溶于水的盐和碱):①盐:白色↓:CaCO3、BaCO3(溶于酸)AgCl、BaSO4(也不溶于稀HNO3) 等②碱:蓝色↓:Cu(OH)2红褐色↓:Fe(OH)3白色↓:其余碱。
初中化学知识大全

初中化学知识大全一、物质的学名、俗名及化学式(1)金刚石、石墨:C(2)水银、汞:Hg(3)生石灰、氧化钙:CaO(4)干冰(固体二氧化碳):CO2(5)盐酸、氢氯酸:HCl(6)亚硫酸:H2SO3(7)氢硫酸:H2S(8)熟石灰、消石灰:Ca(OH)2(9)苛性钠、火碱、烧碱:NaOH(10)纯碱:Na2CO3碳酸钠晶体、纯碱晶体:Na2CO3·10H2O(11)碳酸氢钠、酸式碳酸钠:NaHCO3 (也叫小苏打)(12)胆矾、蓝矾、硫酸铜晶体:CuSO4·5H2O(13)铜绿、孔雀石:Cu2(OH)2CO3(分解生成三种氧化物的物质)(14)甲醇:CH3OH 有毒、失明、死亡(15)酒精、乙醇:C2H5OH(16)醋酸、乙酸(16.6℃冰醋酸)CH3COOH(CH3COO- 醋酸根离子)具有酸的通性(17)氨气:NH3(碱性气体)(18)氨水、一水合氨:NH3·H2O(为常见的碱,具有碱的通性,是一种不含金属离子的碱)(19)亚硝酸钠:NaNO2(工业用盐、有毒)二、常见物质的颜色的状态1、白色固体:MgO、P2O5、CaO、NaOH、Ca(OH)2、KClO3、KCl、Na2CO3、NaCl、无水CuSO4;铁、镁为银白色(汞为银白色液态)2、黑色固体:石墨、炭粉、铁粉、CuO、MnO2、Fe3O4▲KMnO4为紫黑色3、红色固体:Cu、Fe2O3、HgO、红磷▲硫:淡黄色▲ Cu2(OH)2CO3为绿色4、溶液的颜色:凡含Cu2+的溶液呈蓝色;凡含Fe2+的溶液呈浅绿色;凡含Fe3+的溶液呈棕黄色,其余溶液一般不无色。
(高锰酸钾溶液为紫红色)5、沉淀(即不溶于水的盐和碱):①盐:白色↓:CaCO3、BaCO3(溶于酸)AgCl、BaSO4(也不溶于稀HNO3) 等②碱:蓝色↓:Cu(OH)2红褐色↓:Fe(OH)3白色↓:其余碱。
6、(1)具有刺激性气体的气体:NH3、SO2、HCl(皆为无色)(2)无色无味的气体:O2、H2、N2、CO2、CH4、CO(剧毒)▲注意:具有刺激性气味的液体:盐酸、硝酸、醋酸。
初中化学名称和俗名对照表

初中化学名称和俗名对照表初中化学常见物质化学名称与俗称:1、金刚石/石墨:C金刚石俗称“金刚钻”。
也就是钻石的原身,它是一种由碳元素组成的矿物,是碳元素的同素异形体。
金刚石是自然界中天然存在的最坚硬的物质。
石墨可以在高温、高压下形成人造金刚石。
2、水银/汞:Hg汞俗称水银。
还有“白澒、姹女、澒、神胶、元水、铅精、流珠、元珠、赤汞、砂汞、灵液、活宝、子明”等别称。
是常温常压下唯一以液态存在的金属。
3、生石灰/氧化钙:CaO氧化钙是一种无机化合物,俗名生石灰。
物理性质是表面白色粉末,不纯者为灰白色,含有杂质时呈淡黄色或灰色,具有吸湿性。
4、二氧化碳:CO2二氧化碳(carbon dioxide),一种碳氧化合物,化学式为CO2,化学式量为44.0095,常温常压下是一种无色无味或无色无嗅(嗅不出味道)而略有酸味的气体。
5、盐酸/氢氯酸:HCl盐酸是氯化氢(HCl)的水溶液,属于一元无机强酸,工业用途广泛。
盐酸的性状为无色透明的液体,有强烈的刺鼻气味,具有较高的腐蚀性。
6、亚硫酸:H2SO3无色透明液体,具有二氧化硫的窒息气味,易分解;溶于水;主要用途:用作分析试剂、还原剂及防腐剂。
7、氢硫酸:H2S氢硫酸它是无色液体,有刺激气味,(有酸的特性),不直接腐蚀皮肤,作用于皮下血管,痛由皮下产生。
8、熟石灰/消石灰:Ca(OH)2氢氧化钙,无机化合物,是一种白色粉末状固体,加入水后,呈上下两层。
9、纯碱:Na2CO3碳酸钠分类属于盐,不属于碱。
国际贸易中又名苏打或碱灰。
它是一种重要的有机化工原料,主要用于平板玻璃、玻璃制品和陶瓷釉的生产。
初中化学物质俗称大全

物质俗称大全
1、食盐:主要成分:氯化钠,化学式NaCl
2、二氧化碳固体:化学式CO2,俗称干冰
3、氧化钙:化学式CaO,俗称生石灰
4、氢氧化钙:化学式Ca(OH)2,俗称熟石灰、消石灰
氢氧化钙溶液:俗称石灰水,主要成分Ca(OH)2
5、甲烷:化学式CH4,俗称天然气,瓦斯气、沼气的主要成分
6、乙醇:化学式C2H5OH ,俗称酒精
7、汞:化学式Hg,俗称水银
8、过氧化氢:化学式H2O2,俗称双氧水
9、硫酸铜晶体:化学式CuSO4•5H2O,俗称胆矾、蓝矾
10、氢氧化钠:化学式NaOH,俗称火碱、烧碱、苛性钠
11、大理石、石灰石的主要成分:CaCO3
12、氢氯酸(HCl):盐酸(氯化氢气体溶于水所得的溶液),学名:氢氯酸
13、天然气、沼气、瓦斯气的主要成分:甲烷 (CH4)
14、碳酸钠:化学式:Na2CO3,俗称纯碱、苏打
15、碳酸氢钠:化学式:NaHCO3,俗称小苏打。
初中化学常见物质俗名物质颜色吸放热的反应的类型

初中常见化学物质的俗名、颜色及其化学式一、常见物质的俗名⑴金刚石、石墨:C⑵水银、汞:Hg(3)生石灰、氧化钙:CaO(4)干冰(固体二氧化碳):CO2(5)盐酸、氢氯酸:HCl(6)亚硫酸:H2SO3(7)氢硫酸:H2S(8)熟石灰、消石灰、石灰乳:Ca(OH)2 (9)苛性钠、火碱、烧碱:NaOH(10)纯碱(碱面、口碱)、苏打:Na2CO3碳酸钠晶体、纯碱晶体:Na2CO3·10H2O(11)碳酸氢钠、酸式碳酸钠:NaHCO3(也叫小苏打)(12)胆矾、蓝矾、硫酸铜晶体:CuSO4·5H2O(13)铜绿、孔雀石:Cu2(OH)2CO3(分解生成三种氧化物的物质)(14)甲醇、木精(工业酒精):CH3OH 有毒、失明、死亡(15)酒精、乙醇:C2H5 OH(16)醋酸、乙酸(16、6℃冰醋酸)CH3COOH(CH3COO- 醋酸根离子) 具有酸的通性(17)氨气:NH3(碱性气体)(18)氨水、一水合氨:NH3·H2O(为常见的碱,具有碱的通性,就是一种不含金属离子的碱)(19)亚硝酸钠:NaNO2(工业用盐、有毒)(20)钡餐,重晶石: BaSO4(21)磁铁矿石: Fe3O 4(22)赤铁矿石:Fe2O 3(23)大理石(方解石、石灰石)、白垩:CaCO3 (24)天然气(沼气):CH4(25)尿素: CO(NH2) 2(26)葡萄糖:C6H12O6(27)淀粉: (C6H10O5)n二、常见物质的颜色的状态1、白色固体:MgO、P2O5、CaO、NaOH、Ca(OH)2、KClO3、KCl、Na2CO3、NaCl、无水CuSO4;铁、镁为银白色(汞为银白色液态)2、黑色固体:石墨、炭粉、铁粉、CuO、MnO2、Fe3O4▲KMnO4为紫黑色3、红色固体:Cu、Fe2O3、HgO、红磷▲硫:淡黄色▲ Cu2(OH)2CO3为绿色4、溶液的颜色:凡含Cu2+的溶液呈蓝色;凡含Fe2+的溶液呈浅绿色;凡含Fe3+ 的溶液呈棕黄色,其余溶液一般不无色。
初中化学物质的俗名3

化学中有很多物质,在生活中人们对它有另外的一种称呼,就是它的俗名了。
记住下面这些俗名,可以帮助你的中考额~~~
化钠;食盐NaCL氯化镁;盐卤MgCL2*6H2O
碳酸钠;苏打.纯碱Na2CO3
碳酸氢钠;小苏打NaHCO3
氢氧化钠;烧碱.苛性钠NaOH
氢氧化钾;苛性钾KOH
氢氧化钙;熟石灰Ca(OH)2
高锰酸钾;灰锰氧KMnO4
氟化钙;萤石.氟石CaF2
二硫化亚铁;黄铁矿.硫铁矿FeS2
硫酸铜晶体;胆矾.蓝矾CuSO4*5H2O
硫酸锌晶体;皓矾ZnSO4*7H2O
硫酸亚铁晶体;绿矾FeSO4*7H2O
硫酸铝晶体;明矾kAL(SO4)2*12H2O
硫酸钙晶体;(生)石膏CaSO4*2H2O
硫酸钙晶体;熟石膏.烧石膏(CaSO4)2*H2O
硫酸钡晶体;重晶体BaSO4
硫酸钠晶体;芒硝NaSO4*10H2O
硫酸镁晶体;泻盐MgSO4*7H2O
硫代硫酸钠;大苏打.海波Na2S2O3。
初中化学常见物质颜色及溶解性

初中化学知识总结(识记部分)一、物质的学名、俗名及化学式(1)金刚石、石墨:C(2)水银、汞:Hg(3)生石灰、氧化钙:CaO(4)干冰(固体二氧化碳):CO2(5)盐酸、氢氯酸:HCl(6)亚硫酸:H2SO3(7)氢硫酸:H2S(8)熟石灰、消石灰:Ca(OH)2(9)苛性钠、火碱、烧碱:NaOH(10)纯碱:Na2CO3碳酸钠晶体、纯碱晶体:Na2CO3·10H2O(11)碳酸氢钠、酸式碳酸钠:NaHCO3 (也叫小苏打)(12)胆矾、蓝矾、硫酸铜晶体:CuSO4·5H2O(13)铜绿、孔雀石:Cu2(OH)2CO3(分解生成三种氧化物的物质)(14)甲醇:CH3OH 有毒、失明、死亡(15)酒精、乙醇:C2H5OH(16)醋酸、乙酸(16.6℃冰醋酸)CH3COOH (CH3COO- 醋酸根离子)具有酸的通性(17)氨气:NH3(碱性气体)(18)氨水、一水合氨:NH3·H2O(为常见的碱,具有碱的通性,是一种不含金属离子的碱)(19)亚硝酸钠:NaNO2(工业用盐、有毒)二、常见物质的颜色的状态1、白色固体:MgO、P2O5、CaO、 NaOH、Ca(OH)2、KClO3、KCl、Na2CO3、NaCl、无水CuSO4;铁、镁为银白色(汞为银白色液态)2、黑色固体:石墨、炭粉、铁粉、CuO、MnO2、Fe3O4、KMnO4为紫黑色3、红色固体:Cu、Fe2O3、HgO、红磷、硫:淡黄色、Cu2(OH)2CO3为绿色4、溶液的颜色:凡含Cu2+的溶液呈蓝色;凡含Fe2+的溶液呈浅绿色;凡含Fe3+的溶液呈棕黄色,其余溶液一般不无色。
(高锰酸钾溶液为紫红色)5、沉淀(即不溶于水的盐和碱):①盐:白色↓:CaCO3、BaCO3(溶于酸) AgCl、BaSO4(也不溶于稀HNO3) 等②碱:蓝色↓:Cu(OH)2红褐色↓:Fe(OH)3白色↓:其余碱。
6、(1)具有刺激性气体的气体:NH3、SO2、HCl(皆为无色)(2)无色无味的气体:O2、H2、N2、CO2、CH4、CO(剧毒)▲注意:具有刺激性气味的液体:盐酸、硝酸、醋酸。
初中化学俗名

初中化学俗名合集无机部分:纯碱、苏打、口碱:Na2CO3小苏打:NaHCO3大苏打:Na2S2O3石膏(生石膏):CaSO4.2H2O熟石膏:2CaSO4·。
H2O莹石:CaF2重晶石、钡餐:BaSO4(无毒)碳铵:NH4HCO3石灰石、大理石:CaCO3生石灰:CaO熟石灰、消石灰:Ca(OH)2烧碱、火碱、苛性钠:NaOH绿矾:FaSO4·7H2O干冰:CO2明矾:KAl (SO4)2·12H2O漂白粉:Ca (ClO)2、CaCl2(混和物)胆矾、蓝矾:CuSO4·5H2O双氧水:H2O2皓矾:ZnSO4·7H2O硅石、石英:SiO2刚玉:Al2O3水玻璃、泡花碱:Na2SiO3铁红:Fe2O3磁铁矿:Fe3O4黄铁矿、硫铁矿:FeS2铜绿、孔雀石:Cu2(OH)2CO3赤铜矿:Cu2O波尔多液:Ca (OH)2和CuSO4天然气、沼气、坑气(主要成分):CH4水煤气:CO和H2王水:浓HNO3与浓HCl按体积比1:3混合而成。
尿素:CO(NH2)2有机部分:酒精、乙醇:C2H5OH醋酸、冰醋酸、食醋的主要成分CH3COOH焦炉气成分(煤干馏):H2、CH4、乙烯、CO等。
蚁醛、甲醛HCHO福尔马林:35%—40%的甲醛水溶液蚁酸甲酸HCOOH葡萄糖:C6H12O6果糖:C6H12O6蔗糖:C12H22O11麦芽糖:C12H22O11淀粉:(C6H10O5)n草酸、乙二酸:HOOC—COOH 强酸性,受热分解成CO2和水,使KMnO4酸性溶液褪色。
初中化学俗名总结

初中化学俗名总结work Information Technology Company.2020YEAR初中化学俗名(1)无机部分:纯碱、苏打、天然碱、口碱:Na2CO3 小苏打:NaHCO3 大苏打:Na2S2O3 石膏(生石膏):CaSO4.2H2O 熟石膏:2CaSO4•.H2O 莹石:CaF2 重晶石:BaSO4(无毒)碳铵:NH4HCO3 石灰石、大理石:CaCO3 生石灰:CaO 食盐:NaCl 熟石灰、消石灰:Ca(OH)2 芒硝:Na2SO4•7H2O (缓泻剂) 烧碱、火碱、苛性钠:NaOH 绿矾:FaSO4•7H2O干冰:CO2 明矾:KAl (SO4)2•12H2O漂白粉:Ca (ClO)2 、CaCl2(混和物)泻盐:MgSO4•7H2O胆矾、蓝矾:CuSO4•5H2O 双氧水:H2O2 皓矾:ZnSO4•7H2O硅石、石英:SiO2 刚玉:Al2O3 水玻璃、泡花碱、矿物胶:Na2SiO3 铁红、铁矿:Fe2O3 磁铁矿:Fe3O4 黄铁矿、硫铁矿:FeS2 铜绿、孔雀石:Cu2(OH)2CO3 菱铁矿:FeCO3 赤铜矿:Cu2O 波尔多液:Ca (OH)2和CuSO4 石硫合剂:Ca (OH)2和S 玻璃的主要成分:Na2SiO3、CaSiO3、SiO2 过磷酸钙(主要成分):Ca (H2PO4)2和CaSO4 重过磷酸钙(主要成分):Ca (H2PO4)2 天然气、沼气、坑气(主要成分):CH4 水煤气:CO和H2 硫酸亚铁铵(淡蓝绿色):Fe (NH4)2 (SO4)2 溶于水后呈淡绿色光化学烟雾:NO2在光照下产生的一种有毒气体王水:浓HNO3:浓HCl按体积比1:3混合而成。
铝热剂:Al + Fe2O3或其它氧化物。
尿素:CO(NH2) 2(2)有机部分:氯仿:CHCl3 电石:CaC2 电石气:C2H2 (乙炔) TNT:三硝基甲苯氟氯烃:是良好的制冷剂,有毒,但破坏O3层。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
初中化学常见物质的俗名与颜色
一、俗名
纯净物俗名 化学名称 化学式
备注
干冰 二氧化碳 (固体) 2CO
白色固体,易升华,
升华时吸收大量的热,可用于人工降雨 生石灰 氧化钙 CaO
与水反应放热,常用作食品干燥剂 熟石灰、消石灰 氢氧化钙 ()2Ca OH 微溶于水,溶解度随温度的升高而减小, 常用作建筑材料。
火碱、烧碱、 苛性钠 氢氧化钠 NaOH
强碱,溶于水放热,在空气中易潮解。
小苏打 碳酸氢钠 3NaHCO
白色细小晶体,制糕点所用的发酵粉, 医疗上能治疗胃酸过多
纯碱、苏打 碳酸钠 23Na CO 白色粉末,其水溶液呈碱性,
用于玻璃、造纸、纺织、洗涤、食品工业等 石碱、口碱 十水碳酸钠 23210Na CO H O ⋅
碳酸钠的晶体 胆矾、蓝矾 五水硫酸铜、 硫酸铜晶体 425CuSO H O ⋅ 蓝色晶体 氨水 一水合氨 32NH H O ⋅
弱碱溶液
水银 汞 Hg
常温下呈液态的金属,温度计常用的。
硫磺 硫 S
淡黄色粉末或晶块,在空气中燃烧发出 淡蓝色火焰,在纯氧中为蓝紫色 金刚石 C 天然最硬的物质之一
石墨 C
能导电,作润滑剂,制铅笔芯等
酒精 乙醇 25C H OH
无色有特殊香味的透明液体,易挥发,易燃, 燃烧发出淡蓝色火焰 醋酸 冰醋酸 乙酸 3CH COOH
具有酸的通性
毒盐、硝盐 亚硝酸钠 NaNO 2 食品添加剂,有毒,致癌 福尔马林 甲醛 HCHO 可用于防腐
葡萄糖 C 6H 12O 6 为人体组织提供营养,维持体温等 蔗糖
C 12H 22O 11 常用的食品甜味剂
淀粉(混合物)
(C 6H 12O 5)n
大米、麦、马铃薯等的主要成分
溶液的颜色 颜色所对应的离子
备注
蓝色 Cu 2+
可溶性铜盐溶液,如CuCl 2、CuSO 4、Cu(NO 3)2 黄色 Fe 3+ 可溶性铁盐溶液,如 FeCl 3、Fe 2(SO 4)3、Fe(NO 3)3 浅绿色 Fe 2+ 可溶性亚铁盐溶液,如 FeCl 2、FeSO 4、Fe(NO 3)2 紫红色
MnO 4
—
KMnO 4溶液
注:其他一般为无色透明溶液,酸碱指示剂的颜色变化要熟记。
混合物俗名
主要成分的化学式
备注
煤 C 用作燃料
木炭、 活性炭、 炭黑、 C
用作燃料,制火药等;
具有吸附性,可用来制防毒面具; 制油墨、颜料等 生铁、钢 Fe
铁碳合金
赤铁矿 23Fe O 纯净的氧化铁是一种红棕色粉末, 磁铁矿 34Fe O 黑色固体 铁锈
232Fe O xH O ⋅
红棕色 铜绿、铜锈、孔雀石 ()232Cu OH CO
绿色粉状物
石灰石、大理石 3CaCO
纯净的碳酸钙为白色固体, 常用作建筑材料
食盐 NaCl 烹饪中最常用的调味料,作防腐剂, 制生理盐水等 盐酸 HCl
胃酸的主要成分
水煤气 CO 、2H
水蒸气和C 高温下制得, 燃烧火焰呈蓝色
天然气、沼气 4CH 甲烷是一种无色无味的气体, 燃烧火焰呈蓝色 双氧水
22H O
无色透明液体,用于消毒
二、常见物质的颜色、状态
表一
火焰颜色 可燃物 化学方程式
蓝色 CO 、2H 、4CH 、25C H OH 、S
蓝紫色 S (在氧气中燃烧) 黄白色 P (在空气中燃烧) 白光
P (在空气中燃烧) Mg (在空气中燃烧) C (在氧气中燃烧)
常见固体颜色
名称
化学式
红色
铜 紫红色 Cu
氧化铁 红棕色 23Fe O
红磷 紫红色
P 黄色 硫
S
蓝色 硫酸铜晶体(五水硫酸铜) 425CuSO H O ⋅
绿色 碱式碳酸铜 ()232Cu OH CO
紫黑色 高锰酸钾 4KMnO
黑色
氧化铜 CuO 铁粉 Fe 木炭粉 C
二氧化锰 2MnO 四氧化三铁
34Fe O 白色
碳酸钙 3CaCO
氧化钙 CaO
氢氧化钙 2()Ca OH
氧化镁 MgO
氢氧化镁 ()2Mg OH 氢氧化钠 NaOH 氯化钠 NaCl
碳酸钠 23Na CO 氯酸钾 3KClO
氯化钾 KCl
无水硫酸铜 4CuSO
五氧化二磷
25P O
白磷(白色或浅黄色蜡性固体) P
氧化铝
23Al O
银白色
镁、铝、汞、铁(块状)…
Al Hg Ag Fe...Mg 、、、、
沉淀颜色名称化学式备注
白色氯化银
AgCl
不溶于水也不溶于酸
硫酸钡
4
BaSO
碳酸钙
3
CaCO
不溶于水能溶于酸产生气泡
(二氧化碳)
碳酸钡
3
BaCO
氢氧化镁()
2
Mg OH
不溶于水能溶于酸无气泡产生氢氧化亚铁
2
()
Fe OH
氢氧化铝()
3
Al OH
蓝色氢氧化铜()
2
Cu OH
红褐色氢氧化铁()
3
Fe OH
离子的检验
检验检验的方法
CO32—、SO42—先加足量稀硝酸检验并除尽CO32—,再加Ba(NO3)2溶液检验SO42—CO32—、Cl—先加足量稀硝酸检验并除尽CO32—,再加AgNO3溶液检验Cl—
SO42—、Cl—先加足量Ba(NO3)2溶液检验SO42—,过滤取滤液,再加AgNO3溶液
和稀硝酸检验Cl—
CO32—、SO42—、Cl—先加足量稀硝酸检验并除尽CO32—,再加足量Ba(NO3)2溶液检验并除
尽SO42—,过滤取滤液,再加AgNO3溶液检验Cl—
OH—、CO32—先加足量CaCl2溶液检验并除尽CO32—,过滤取滤液,再加酚酞试液
液检验OH—
物质的溶解性
1、盐的溶解性
含有钾、钠、硝酸根、铵根的物质都溶于水
含Cl的化合物只有AgCl不溶于水,其他都溶于水;
含SO42-的化合物只有BaSO4不溶于水,其他都溶于水。
含CO32-的物质只有K2CO3、Na2CO3、(NH4)2CO3溶于水,其他都不溶于水
2、碱的溶解性
溶于水的碱有:氢氧化钡、氢氧化钾、氢氧化钙、氢氧化钠和氨水,其他碱不溶于水。
难溶性碱中Fe(OH)3是红褐色沉淀,Cu(OH)2是蓝色沉淀,其他难溶性碱为白色。
(包括Fe(OH)2)注意:沉淀物中AgCl和BaSO4不溶于稀硝酸,
其他沉淀物能溶于酸。
如:Mg(OH)2 CaCO3 BaCO3 Ag2 CO3等
3、大部分酸及酸性氧化物能溶于水,(酸性氧化物+水→酸)大部分碱性氧化物不溶于水,能溶的有:氧化钡、氧化钾、氧化钙、氧化钠(碱性氧化物+水→碱)
化学之最
1、地壳中含量最多的金属元素是铝。
2、地壳中含量最多的非金属元素是氧。
3、空气中含量最多的物质是氮气。
4、天然存在最硬的物质是金刚石。
5、最简单的有机物是甲烷。
6、金属活动顺序表中活动性最强的金属是钾。
7、相对分子质量最小的氧化物是水。
最简单的有机化合物CH4
8、相同条件下密度最小的气体是氢气。
9、导电性最强的金属是银。
10、相对原子质量最小的原子是氢。
11、熔点最小的金属是汞。
12、人体中含量最多的元素是氧。
13、组成化合物种类最多的元素是碳。
14、日常生活中应用最广泛的金属是铁。
15、最早利用天然气的是中国;。
