工科化学问题详解第五章氧化还原反应与电化学
氧化还原反应和电化学

氧化还原反应和电化学氧化还原反应和电化学是化学领域中重要的研究方向,它们在生产、能源、环境保护等各个领域都具有重要的应用价值。
本文将从氧化还原反应的基础知识入手,介绍氧化还原反应的定义、特征以及电化学的相关概念和应用。
一、氧化还原反应的基本概念和特征1.1 氧化还原反应的定义氧化还原反应是指化学反应中,电子从一种物质转移到另一种物质的过程。
在氧化还原反应中,发生氧化的物质失去电子,而发生还原的物质则获得电子。
整个过程涉及到电子的转移和能量的释放。
1.2 氧化还原反应的特征氧化还原反应的特征可以总结为以下几个方面:1)电子的转移:氧化还原反应中,电子从一个物质转移到另一个物质,导致物质的氧化或还原。
2)氧化和还原:氧化是指物质失去电子,还原是指物质获得电子。
3)氧化剂和还原剂:氧化剂是指能接受电子的物质,还原剂是指能提供电子的物质。
4)氧化态和还原态:在氧化还原反应中,物质的氧化态和还原态发生变化。
二、电化学的基本概念和应用2.1 电化学的基本概念电化学是研究电能与化学能之间相互转化的学科。
它涉及到电解、电池等重要概念。
2.2 电化学的应用电化学在许多领域都有广泛的应用。
以下是电化学的几个应用方面:1)电解:通过电解,可以将化合物分解为原子或离子,使得某些实验或工业过程得以实现。
2)电池:电化学电池是将化学能转化为电能的装置,广泛应用于电子产品、交通工具等领域。
3)腐蚀和防腐:电化学腐蚀是指金属在电解质中发生的一种化学腐蚀过程,而电化学防腐则是通过电化学方法来保护金属材料。
4)电解池:电解池是用于电解过程的装置,广泛应用于化学实验、电镀、电解精炼等领域。
三、氧化还原反应与电化学的关系氧化还原反应和电化学有着密切的关系。
氧化还原反应中的电子转移过程是电化学研究的基础。
通过电化学的方法,我们可以控制和利用氧化还原反应,实现能量的转化和化学反应的控制。
例如,电化学电池就是通过氧化还原反应来产生电能的装置。
工科化学与实验(金继红)第5章-习题及思考题答案

思考题1.氧化还原反应的特征是什么?什么是氧化剂和还原剂?什么是氧化反应和还原反应?氧化还原反应的特征是有电子的转移或偏移。
在氧化还原的过程中,得电子的物质为氧化剂,失电子的物质为还原剂。
氧化数升高的过程称为氧化,氧化数降低的过程称为还原。
2.如何用离子-电子法配平氧化还原方程式?配平原则:(1)反应过程中氧化剂所夺得的电子数必须等于还原剂失去的电子数。
(2)反应前后各元素的原子总数相等。
配平步骤:将反应式改写成两个半反应式,先将两个半反应式配平,然后将这些反应加合起来,消去电子而完成。
3.什么是氧化还原电对?同一元素原子的氧化型物质及对应的还原型物质称为氧化还原电对。
氧化还原电对通常写成: 氧化型/还原型(Ox/Red),如: Cu2+/Cu;Zn2+/Zn4.如何用图式表示原电池?为简单起见,通常用符号表示原电池。
图式中“∣”表示相界面;“‖”表示盐桥;(—)和(+)分别表示原电池的负极和正极。
一般进行氧化反应的负极写在左边,进行还原反应的正极写在右边。
要注明电池反应的温度和压力,如不写明,一般是指在298.15K和标准压力下。
对气体要注明压力,对溶液要注明浓度,当溶液浓度为1mol/L时可以不写。
当电极无金属导体时,需要增加只起导电作用而不参加反应的惰性电极Pt 或C;若参加电极反应的物质中有纯气体,液体或固体时,则应写在惰性导体的一边。
5. 原电池的两个电极符号是如何规定的?如何计算电池的电动势?(—)和(+)分别表示原电池的负极和正极。
电池电动势 E = E + - E -E +和 E - 分别代表正,负极的电极电势。
6. 电对的电极电势值是否与电极反应式的写法有关?电对的电极电势值是强度性质,与电极反应式的写法无关。
7. 原电池的电动势与离子浓度的关系是什么?从能斯特方程中可反映出影响电极电势的因素有哪些?原电池的电动势与正极和负极的电极电势有关,等于两者之差。
而电极电势与离子浓度之间的关系,可由能斯特方程表达。
第五章 氧化还原与电化学

电子做有规则的定向流动
2. 原电池的组成:
(1)半电池和电极
锌半电池:锌片,锌盐-负极
铜半电池:铜片,铜盐-正极
正、负极也可以是惰性电极, 如:Pt、石墨等,只起导电作用。
(2)外电路 用金属导线把一个灵敏电流计 与两个半电池中的电极串连起来。 电子由锌 → 铜,电流由铜 → 锌。 (3)盐桥(是一种电解质溶液: 饱和KCl和琼胶) 加入盐桥,才能使电流完整,产生电流。 作用:沟通电路,使溶液中体系保持中性,使电极反 应得以继续进行。
液写离子; 4) 不同相用竖线“∣”隔开,同相用“,”
隔开,两个半电池用双竖线“‖”隔开 .
写出下列电池反应所对应的电池符号: Cu2+ + Zn ←→ Cu + Zn2+
( - ) Zn | Zn2+ (c1) || Cu2+(c2) | Cu ( + )
Cl2+2Fe2+ ←→ 2Fe3+ +2Cl( - )C | Fe2+(c1),Fe3+ (c2)||Cl-(c3)|Cl2(p)|C ( + )
2MnO4- +16H++ 10e 5SO32- + 5H2O
2MnO4- + 5SO32- + 6H+
2Mn2++8H2O 5SO42- +10H++10e +)
2Mn2+ + 5SO42- +3H2O
5)检查原子个数、电荷数,使之相等并还原 为分子反应式 。
2KMnO4 + 5K2SO3+ 3H2SO4 2MnSO4+ 6K2SO4 +3H2O
氧化还原反应、电化学
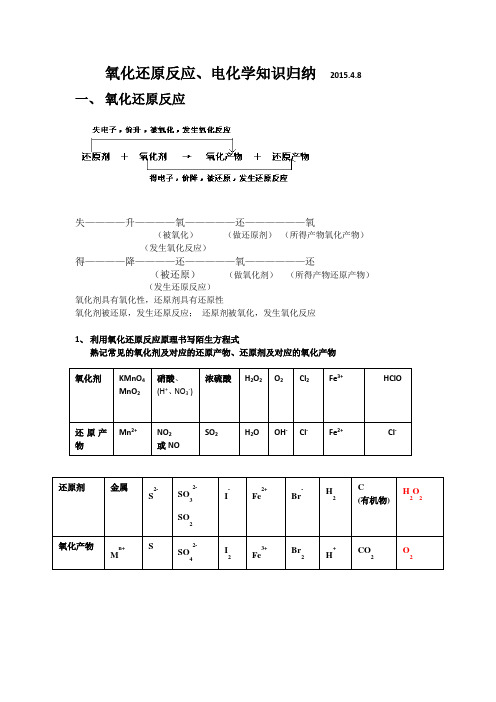
氧化还原反应、电化学知识归纳 2015.4.8一、 氧化还原反应失————升————氧—————还——————氧(被氧化) (做还原剂) (所得产物氧化产物)(发生氧化反应)得————降————还—————氧——————还(被还原) (做氧化剂) (所得产物还原产物) (发生还原反应)氧化剂具有氧化性,还原剂具有还原性氧化剂被还原,发生还原反应; 还原剂被氧化,发生氧化反应1、 利用氧化还原反应原理书写陌生方程式熟记常见的氧化剂及对应的还原产物、还原剂及对应的氧化产物氧化剂 KMnO 4 MnO 2 硝酸、 (H +、NO 3-) 浓硫酸 H 2O 2 O 2Cl 2 Fe 3+ HClO还原产物Mn 2+ NO 2 或NO SO 2 H 2O OH - Cl - Fe 2+ Cl - 还原剂 金属S 2- SO 32- SO 2I - Fe 2+ Br - H 2 C (有机物) H 2O 2氧化产物M n+ S SO 42- I 2 Fe 3+ Br 2 H + CO 2 O 22、建立氧化还原反应方程式的书写模型二、电化学(一)原电池1、原电池正负极的判断:① 、据电极材料:较活泼的电极材料——负极;较不活泼的电极材料——正极(一般规律)②、据电极发生的反应:失电子——负极;负——失——氧(氧化反应)得电子——正极;正——得——还(还原反应)③、根据电流方向或电子流向:电流(外电路),由正极流向负极;电子则由负极经内电路流向原电池的正极。
④ 、、据内电路离子的迁移方向:阳离子流向电池正极.阴离子流向原电池负极。
2、电极反应式的书写(1)根据总反应或者题目的提示,找出氧化剂、还原剂以及对应的产物(2)正极发生还原反应,氧化剂+ n e-==还原产物负极发生氧化反应,还原剂—n e-== 氧化产物(3)利用化合价升降守恒推出正确的转移电子数(4)反应式两端添加电解质中存在的离子,使反应式电荷守恒(5)利用元素守恒写出完整的电极反应式(二)、电解池1、电解池阴阳极的判断:① 、据电源的正负极判断:阳极——与电源的正极相连;阴极——与电源的负极相连②、据电极发生的反应:失电子——阳极;阳(极)——失——氧(氧化反应)得电子——阴极;阴(极)——得——还(还原反应)③、据内电路离子的迁移方向:阳离子流向电解池阴极.阴离子流向电解池阳极。
《无机化学》第五章 氧化还原反应和电化学基础

二、氧化还原反应方程式的配平
1. 氧化值法
配平原则:氧化剂中元素氧化值降低的总数等 于还原剂中元素氧化值升高的总数。
配平步骤: (1)写出反应方程式,标出氧化值有变化 的元素,求元素氧化值的变化值。
(2)根据元素氧化值升高总数和降低总数相等 的原则,调整系数,使氧化值变化数相等。
(3)用观察法使方程式两边的各种原子总数相 等。
酸表。
(4)E是电极处于平衡状态时表现出来的特
征,与反应速率无关。
(5)E仅适用于水溶液。
5.饱和甘汞电极:
Hg | Hg2Cl2(s) |KCl (饱和)
Hg2Cl2 (s) + 2e
2Hg(l) +2Cl-
E (Hg2Cl2/Hg)=0.245V
三、 影响电极电势的因素
1.影响 因素
(1)电极的本性:即电对中氧化型或还 原型物质的本性。
还原型:在电极反应中同一元素低氧化值的物质。)
电对:氧化型/还原型
例:MnO2 +4H+ + 2e
Mn2+ +2H2O
电对:MnO2 / Mn2+
(2)E与电极反应中的化学计量系数无关。
例:Cl2 + 2e 1/2Cl2 + e
2Cl- E(Cl2/Cl-)=1.358V Cl-
(3)电极反应中有OH- 时查碱表,其余状况查
(3)分别配平两个半反应,使等号两边的原子 数和电荷数相等。
(4)根据得失电子数相等的原则,给两个半 反应乘以相应的系数,然后合并成配平的离子 方程式。
(5)将离子方程式写成分子方程式。
离子电子法配平时涉及氧原子数的增加和减 少的法则:
氧化还原反应与电化学

氧化还原反应与电化学氧化还原反应是化学中最基本的反应类型之一,其与电化学的关系密不可分。
本文将探讨氧化还原反应与电化学之间的联系,并介绍其在实际应用中的意义。
一、氧化还原反应的基本概念氧化还原反应是指物质中电子的转移过程,其中一种物质被氧化(失去电子),另一种物质被还原(获得电子)。
在氧化还原反应中,氧化剂接受电子而被还原,还原剂失去电子而被氧化。
二、氧化还原反应的判别方法为了判断一个反应是否为氧化还原反应,我们可以根据以下几点进行分析:1. 电荷变化:氧化反应中,氧化剂的电荷减少,还原剂的电荷增加。
2. 氧化态的改变:化学物质的氧化态改变可以作为氧化还原反应的标志。
三、电化学的基本概念电化学是研究电与化学反应之间相互转化的科学,主要包括电解和电池两个方面。
1. 电解:将电能转化为化学能的过程称为电解。
电解涉及到正负电极、电解质和电解液等因素。
2. 电池:将化学能转化为电能的装置称为电池。
电池由两个半电池组成,每个半电池都包含一个电解质和一个电极。
四、氧化还原反应与电化学的联系氧化还原反应与电化学密切相关,电子的转移正是氧化还原反应中的核心过程。
氧化剂与还原剂之间的电子转移导致了电流的流动。
1. 电解过程中的氧化还原反应:在电解中,当外加电压大于一定值时,电解液中的化学物质发生氧化还原反应,从而实现电流的通过。
2. 电池中的氧化还原反应:在电池中,化学反应导致了电子的转移和电势的变化。
正极发生氧化反应,负极发生还原反应,电子在电解质中流动,产生了电势差。
五、氧化还原反应与电化学的应用氧化还原反应与电化学在各个领域中都有重要的应用,下面简要介绍其中几个方面:1. 电解产生金属:通过电解可以将金属离子还原为金属,实现金属的提取和纯化。
2. 电池的应用:电池作为一种便携式的能源装置,广泛应用于生活中的电子产品、交通工具和能源储备等方面。
3. 化学分析:电化学分析技术可以用于测定物质的含量、离子浓度和pH值等参数,具有快速、准确、灵敏的特点。
化学氧化还原反应与电化学

化学氧化还原反应与电化学化学氧化还原反应与电化学是化学学科中非常重要的两个概念和分支。
氧化还原反应是指物质在化学反应中,电子的转移导致氧化态和还原态的变化,而电化学则研究了电荷在体系中的传递和转化过程。
本文将分别讨论化学氧化还原反应和电化学的基本概念、应用以及二者之间的联系。
一、化学氧化还原反应化学氧化还原反应是指在化学反应中,物质的氧化态和还原态发生变化的过程。
氧化是指物质失去电子,增加氧化态的现象,而还原则是指物质获得电子,减少氧化态的现象。
在氧化还原反应中,氧化剂接受电子而被还原,还原剂失去电子而被氧化。
氧化还原反应在生活和工业生产中具有广泛的应用。
例如,在生物体内的呼吸过程中,有机物被氧化成二氧化碳和水,同时释放能量。
这是一个复杂的氧化还原反应链,是人体获得能量的重要途径。
此外,氧化还原反应也应用于电池、电解、腐蚀等方面。
二、电化学电化学研究了电荷在体系中的传递和转化过程。
它是诸多学科交叉的产物,涉及物理学、化学以及材料科学等领域。
在电化学中,电化学反应是指通过外加电势来引发的氧化还原反应。
在电化学实验中,常用的设备是电化学池,包括阳极、阴极和电解质溶液。
阳极是指发生氧化反应的电极,而阴极是指发生还原反应的电极。
电解质溶液则提供了离子来维持电解质平衡。
通过外部电源的施加,电流流经电化学池中的电解质溶液,从而引发氧化还原反应。
电化学的应用十分广泛。
电池就是典型的电化学装置,将化学能转化为电能。
从小型的纽扣电池到大型的汽车电池,电池在我们的日常生活中无处不在。
此外,电解也是电化学的应用之一,通过电解可以实现金属的电镀、水的电解制氢等。
电化学还广泛应用于能源储存、催化剂研究等领域。
三、化学氧化还原反应与电化学的联系化学氧化还原反应与电化学是密切相关的两个概念。
事实上,电化学反应中的氧化还原反应是化学氧化还原反应的一种特殊形式。
在电化学中,通过外部电源施加电势,可以实现将氧化还原反应引发和控制。
第五章氧化还原与电化学

{c( Ag )}{ c(Cl )} = Ksp (AgCl)
若c(Cl ) = 1.0mol L 时 , c( Ag ) = Ksp (AgCl)
1
Ag (aq ) e =
=
Ag(s)
( Ag / Ag)
( Ag / Ag) 0.0592V lg {c( Ag )} ( Ag / Ag) 0.0592V lg Ksp ( AgCl)
已知 298K , A (O2 /H2O) = 1.229V, 例: 求: ⑴ 若 p(O2 ) = p ,pH = 14 时, (O2 /H2O) = ? ⑵ B (O2 /OH ) = ?
2H2O(l) 解:⑴ O2 (g) 4H (aq) 4e 14 1 pH = 14,即 c(H ) = 1.0× 10 mol L
影响电极电势的因素(外因) ① 氧化型或还原型的浓度或分压 电极反应:氧化型 n e
还原型
=
2.303RT c(氧化型) lg nF c(还原型)
c (氧化型 ) , c (还原型 ) , 或 c (氧化型) c (还原型)
,
则:
② 介质的酸碱性
例: 已知 A (ClO /Cl ) = 1.45V 求:当c(ClO ) = c(Cl ) = 1.0mol L ,
H+/H
2
2H++2e =H2
电极符号:Pt|H2(p)|H+(c )
标准电极电势值
φΘ(H+/H2 )=0.000 V
是电极电势的符号,上标“Θ”表示标准态,
下标为该电极的电对 。
氧化还原反应和电化学

氧化还原反应和电化学氧化还原反应(简称“氧化还原反应”)是化学反应中一种非常重要的类型。
在氧化还原反应中,物质的电荷状态发生变化,原子失去或获得电子,从而形成离子,以完成化学反应。
电化学则是研究电能与化学能之间转化的学科。
一、氧化还原反应1. 概念和基本原理氧化还原反应是指在化学反应中,原子、离子或分子中的电子的互相转移过程。
氧化是指物质失去电子,而还原则是指物质获得电子。
在氧化还原反应中,存在着氧化剂和还原剂的概念。
氧化剂接受电子,自身被还原,而还原剂则失去电子,自身被氧化。
2. 氧化还原反应的应用氧化还原反应广泛应用于生活和工业领域。
例如,在电池中,氧化还原反应产生电能;在腐蚀过程中,金属发生氧化还原反应,导致金属的破坏;在生物体内,呼吸作用中的氧化还原反应产生能量。
二、电化学1. 电化学基本概念电化学是研究电能与化学能之间相互转化的学科。
它涉及到电解、电极反应、电池和电解质溶液等概念。
电化学通常分为两个分支:电解学和电池学。
2. 电化学实验电化学实验是研究电化学现象的重要手段。
在实验中,常见的电化学装置包括电解槽、电极、电解质溶液等。
通过实验可以观察到电流的流动和电极上发生的反应,从而揭示电化学过程的本质。
三、氧化还原反应与电化学的联系氧化还原反应与电化学紧密相关。
在电池中,氧化还原反应产生电能,而在电解槽中,电能则用于促使氧化还原反应发生。
此外,电极反应是电化学研究的重点之一,它涉及到氧化还原反应中电子的转移过程。
结论氧化还原反应是化学反应中重要的类型,通过氧化和还原的相互转化,实现能量的转化。
电化学则是研究电能与化学能之间相互转化的学科,它与氧化还原反应密切相关。
两者的研究和应用对于能源、环保等领域具有重要意义。
通过深入理解氧化还原反应和电化学,我们可以更好地应用于实际生活和工业中,促进科学技术的发展和进步。
这篇文章介绍了氧化还原反应和电化学的基本概念、原理和应用,并强调了两者之间的联系。
第五章 氧化还原反应和电化学

O.N.:
MnO4- Mn2+
+7
+2
change = -5
+7 to +2: Mn 被还原
半反应
半反应式:分别表示氧化反应和还原反应的 方程式
氧化型 + ne 还原型 氧化还原反应是两个(或两个以上)氧化还 原电对共同作用的结果 氧化态 I + 还原态 II 还原态 I + 氧化态 II
即与半反应式中的化学计量数无关 一些电对的 与介质的酸碱性有关, 因此有
酸表(A表, pH=0)和碱表(B表, pH=14)
代数值越大,表示在标准条件下该电对 中氧化态物质的氧化能力越强,或还原态 物质的还原能力越弱。
代数值越小,表示在标准条件下该电对 中还原态物质的还原能力越强,或氧化态 物质的氧化能力越弱。
氧化态和还原态
氧化态(物质):半反应中高氧化值(价 态)物质,作为氧化剂,获得电子
还原态(物质):半反应另一端的低氧化 值(价态)物质,作为还原剂,给出电子
同一半反应中的氧化态物质和还原态物质 构成氧化还原电对
氧化态/还原态
Zn2+/Zn
Cu2+/Cu
H+/H2
Cl2/Cl-
氧化半反应
氧化过程 = 失去电子
或液体)时,温度为25C(298K)时的电极
电势为标准电极电势,用符号 (电极)表
示,单位为V(伏特)
标准氢电极
由覆盖有极细而蓬松的铂粉的铂片和含有氢离子的
溶液所组成的气体电极。1953年IUPAC建议采用
标准氢电极的条件规定:
(1)通入的氢气压力为 100kPa
(2)溶液中 C(H+) = 1mol·L-1
氧化还原反应和电化学

氧化还原反应和电化学氧化还原反应是化学反应中常见的一种反应类型,也是电化学研究的基础。
它涉及到物质的电子转移过程,包括氧化和还原两个半反应。
在氧化还原反应中,物质会失去或者获得电子,产生不同的氧化态。
本文将介绍氧化还原反应的基本概念及其在电化学中的应用。
一、氧化还原反应的概念氧化还原反应是指物质中的原子或离子发生电子转移的过程。
在氧化还原反应中,一个物质被氧化,失去电子,而另一个物质被还原,获得电子。
氧化还原反应的关键是电子的转移,可以通过半反应来描述。
在一个氧化还原反应中,通常会有氧化剂和还原剂。
氧化剂是指能够接受电子的物质,它在反应中被还原。
还原剂是指能够捐赠电子的物质,它在反应中被氧化。
氧化还原反应中,物质的氧化态会发生改变。
原子或离子失去电子后,氧化态变大;反之,获得电子后,氧化态变小。
氧化态的改变可以通过氧化数的变化来表示。
二、电化学中的氧化还原反应电化学是研究电与化学反应相互关系的学科。
氧化还原反应在电化学中具有重要的意义,电解和电池就是基于氧化还原反应而发展起来的。
1. 电解电解是指在外加电势的作用下,使溶液中发生氧化还原反应的过程。
在电解中,通过外加电势提供能量,促使物质发生电子转移。
正极受电子,发生还原反应;负极释放电子,发生氧化反应。
电解可以将电能转化为化学能,促使化学反应进行。
电解的应用十分广泛,例如铜的电镀、水的电解等。
2. 电池电池是将化学能转换为电能的装置,它利用氧化还原反应来产生电流。
电池由两个半电池组成,分别是氧化半反应和还原半反应。
在电池中,氧化半反应发生在负极(阴极),还原半反应发生在正极(阳极)。
通过电解质溶液或离子传导体,电子会从负极流向正极,形成电流。
电池的种类有很多,例如干电池、蓄电池、燃料电池等。
它们都利用氧化还原反应的电子转移特性来产生电流,满足人们对电能的需求。
三、电化学的应用电化学在生活和工业中有着广泛的应用,涉及到电解、电池、电镀等领域。
1. 电解用于金属提取和电解制氢电解在金属提取中起着重要的作用,例如铝的电解、锌的电解等。
化学氧化还原反应与电化学反应

化学氧化还原反应与电化学反应化学氧化还原反应与电化学反应是化学领域中两个重要的研究方向。
两者都涉及原子或分子的电子转移过程,但相应的反应机制和应用领域有所不同。
本文将从基本概念、反应机制和应用领域等方面对这两种反应进行分析和比较。
一、基本概念1.化学氧化还原反应化学氧化还原反应是指物质中的原子或分子通过转移电子而产生的化学反应。
在氧化还原反应中,发生氧化反应的物质叫做还原剂,接受电子的物质叫做氧化剂。
氧化还原反应可以通过氧化态的变化来判断。
还原剂的氧化态在反应前较高,在反应后较低;氧化剂的氧化态在反应前较低,在反应后较高。
2.电化学反应电化学反应是指以电解质溶液或电解质固体为介质,通过电流传递来引起的化学反应。
在电化学反应中,正极吸收电子,发生氧化反应,称为氧化反应;负极放出电子,发生还原反应,称为还原反应。
电化学反应可以分为两类,即电解反应和电池反应。
电解反应是通过外加电压将化学物质分解成离子,而电池反应则是通过电催化反应产生电流。
二、反应机制1.化学氧化还原反应机制化学氧化还原反应的机制与反应物之间的电子转移有关。
还原剂从反应物中吸收电子,氧化剂则释放电子给反应物。
在反应过程中,发生氧化反应的物质将电子从其他物质转移给自身,形成较低的氧化态;而发生还原反应的物质则将电子给予其他物质,形成较高的氧化态。
2.电化学反应机制电化学反应的机制与电解质溶液中离子的运动和电子的传递有关。
正极的氧化反应是在电流作用下离子接受电子的过程,负极的还原反应是在电流作用下离子失去电子的过程。
当两极之间的电压足够大时,离子会从正极移动到负极,而在此过程中发生氧化还原反应。
三、应用领域1.化学氧化还原反应的应用化学氧化还原反应在许多化学领域中广泛应用。
例如,在有机合成中,氧化还原反应可以用于生成新的化合物或改变化合物的结构;在环境保护中,氧化还原反应可以用于废水处理和空气净化;在能源领域,氧化还原反应可以用于燃料电池和太阳能电池的电化学反应。
第五章 氧化还原反应与电化学基础

0 Ni 2 + / Ni
= – 0.23 V ;
E
0 Cu
2+
/ Cu
2、电极电势的应用 、
(2)判断氧化还原反应方向 )
根据 ∆ r G m = − zFE MF 可知:
E MF >0,∆ r G m< 0, 反应正向进行 E MF <0,∆ r G m >0, 反应逆向进行
E MF = 0, r G m= 0, 反应处于平衡状态 ∆
② 将氯气通入热的氢氧化钠溶液中,生成氯 化钠和氯酸钠,配平此反应方程式。
在碱性介质中,配平半反应时,少氧的一边加OH- , 多氧的一边加H2O ,绝不能出现H+。
三、电极电势及其利用 1、原电池和电极电势
(1)原电池的组成
借助于自发的氧化还原反应产生电流的装置称 ① 原电池: 为原电池。 在原电池中,两个半电池中发生的反应叫 做电极反应。 与电解质溶液发生氧化还原反应的位置 叫电极,分正极(发生还原反应)和负极(发生氧化反应)。
② 电极的类型:
金属-金属离子电极: Zn(s) | Zn2+(c) 气体-离子电极: Pt | H2(g,P) | H+(c) 金属-金属难溶盐电极: Ag-AgCl(s) | Cl-(c)
Pt “氧化还原”电极: | Fe3+(c1),Fe2+(c2)
(1)原电池的组成
③ 电池符号:将负极写在左边,正极写在右边,
在25℃时的标准状态下能否向右进行? (2)实验室中为什么能用MnO2(s)与浓HCl(12mol/L) 反应制取Cl2(g)?
例8、判断H2O2与Fe2+ 混合时能否发生氧化还 原反应?若能反应写出反应的产物。(已知: E0(O2/H2O2)=0.682V,E0(H2O2/H2O)=1.77V, E0(Fe2+/Fe)=-0.44V,E0(Fe3+/Fe2+)=0.771V)
氧化还原反应及电化学

伏安法
总结词
伏安法是通过测量电流随电压变化的过程来分析物质的氧化还原性质。
详细描述
伏安法是一种常用的电化学分析方法,通过在电极上施加一系列电压并测量相应的电流来分析物质的氧化还原性 质。这种方法可以提供关于物质氧化还原反应的动力学信息和机理信息,有助于深入了解物质的性质和行为。
极谱法
要点一
总结词
电池的能量转换效率
1
电池的能量转换效率是指电池输出的电能或化学 能与其输入的能量的比值,是评价电池性能的重 要指标之一。
2
提高电池的能量转换效率不仅可以减少能源浪费, 还可以降低电池的充电时间和重量,提高电池的 续航能力。
3
提高电池能量转换效率的方法包括优化电极材料、 改进电池结构、提高电解质的离子电导率等。
氧化还原反应及电化学
• 氧化还原反应概述 • 电化学基础 • 氧化还原反应在电化学中的应用 • 氧化还原反应的电化学检测方法 • 氧化还原反应的电化学应用实例
01
氧化还原反应概述
定义与特点
定义
氧化还原反应是一种化学反应,其中电子在反应过程中从一个原子或分子转移到另一个原子或分子。
特点
氧化和还原是同时发生的,且反应过程中有电子转移。
极谱法是通过测量电解过程中的电流随电压变化的过程来 分析物质的氧化还原性质。
要点二
详细描述
极谱法是一种常用的电化学分析方法,通过在电极上施加 一系列电压并测量相应的电流来分析物质的氧化还原性质 。极谱法通常使用滴汞电极作为工作电极,通过测量电解 过程中的电流随电压变化的过程来分析物质的性质和行为 。极谱法可以提供关于物质氧化还原反应的动力学信息和 机理信息,有助于深入了解物质的性质和行为。
02
氧化还原反应与电化学

氧化还原反应与电化学氧化还原反应(Redox)是化学反应中最为常见和重要的一种类型,它涉及到电子的转移和原子的价态变化。
与氧化还原反应密切相关的是电化学,它是研究电子在化学反应中的转移过程以及与化学反应的关系的学科。
一、氧化还原反应的基本概念和应用领域氧化还原反应是指在化学反应中,原子失去或获得电子的过程。
其中,原子失去电子的过程称为氧化,原子获得电子的过程称为还原。
氧化还原反应广泛应用于化学、生物和环境等领域。
比如在电池中,通过氧化还原反应将化学能转化为电能;在腐蚀过程中,金属的氧化还原反应导致金属的破坏;在生物体内,氧化还原反应参与能量产生和维持生命活动等。
二、氧化还原反应的基本原理1. 电子转移:在氧化还原反应中,电子的转移是关键步骤。
氧化剂接受电子,还原剂失去电子,电子从一个物质转移到另一个物质。
例如,在金属与酸反应的过程中,金属原子失去电子成为阳离子,酸接受电子而被还原。
2. 原子的价态变化:氧化还原反应中的原子价态发生改变。
氧化剂使原子的价态增加,还原剂使原子的价态降低。
根据原子价态的变化可以确定氧化还原反应中发生的电子转移。
三、电化学的基本原理和应用电化学研究电荷的转移和电化学反应的关系。
它包括两大分支:电解和电池。
1. 电解:电解是在外加电流的作用下,使电解质溶液中的正负离子离开电极,并在电极上发生氧化还原反应。
电解广泛应用于电镀、电解谱、化学分析等领域。
2. 电池:电池是利用氧化还原反应产生电能的装置。
它由两个导电电极和电解质组成。
其中,一个电极发生氧化反应,释放出电子;另一个电极发生还原反应,吸收电子。
电池广泛应用于电力储存、电子设备、交通工具等领域。
四、氧化还原反应与环境氧化还原反应在环境中起着重要作用。
例如,大气中二氧化硫与氧气发生氧化还原反应形成硫酸,造成酸雨现象;土壤中有机物的氧化还原反应导致土壤质量变化;废水处理中,利用氧化还原反应去除有机物等。
结论:氧化还原反应是广泛存在于化学、生物和环境等各个领域中的重要反应类型,它涉及电子的转移和原子的价态变化。
《氧化还原反应》氧化还原与电化学

《氧化还原反应》氧化还原与电化学在化学的世界里,氧化还原反应是一类极为重要的化学反应。
它不仅在实验室的瓶瓶罐罐中频繁发生,更是与我们的日常生活息息相关,从金属的腐蚀到电池的工作原理,从生物体内的新陈代谢到工业生产中的各种过程,都有着氧化还原反应的身影。
要理解氧化还原反应,首先得搞清楚什么是氧化和还原。
简单来说,氧化就是物质失去电子的过程,而还原则是物质得到电子的过程。
这两个过程总是同时发生,就像硬币的两面,缺一不可。
比如说,铁在空气中生锈,这就是一个氧化过程。
铁原子失去电子,变成了带正电荷的铁离子,与空气中的氧气和水结合,形成了铁锈。
而在氢气还原氧化铜的反应中,氢气得到电子,氧化铜失去电子,氢气被氧化成了水,氧化铜被还原成了铜。
氧化还原反应的本质是电子的转移。
在化学反应中,电子从一个原子或离子转移到另一个原子或离子,导致了化合价的变化。
化合价升高的物质被氧化,化合价降低的物质被还原。
那么,氧化还原反应与电化学又有什么关系呢?电化学,简单来讲,就是研究电能和化学能相互转化的科学。
而氧化还原反应正是实现这种转化的关键。
电池就是一个很好的例子。
在电池中,通过氧化还原反应,化学能被转化为电能。
比如常见的干电池,里面的锌筒发生氧化反应,失去电子成为锌离子,而石墨棒周围的二氧化锰发生还原反应,得到电子。
电子从锌筒通过导线流向石墨棒,从而形成了电流,为我们的各种电器设备提供了电能。
反过来,电解池则是将电能转化为化学能。
通过外加电源,强制让氧化还原反应朝着非自发的方向进行。
比如电解水,在直流电的作用下,水发生分解,生成氢气和氧气。
在工业生产中,电化学也有着广泛的应用。
例如电解精炼铜,粗铜作为阳极发生氧化反应,纯铜作为阴极发生还原反应,从而得到纯度更高的铜。
氧化还原反应和电化学在生物体内也起着至关重要的作用。
我们的呼吸过程,其实就是一系列复杂的氧化还原反应。
食物中的有机物在细胞内被氧化分解,释放出能量,供我们的身体进行各种生命活动。
【北京交大 工科化学】第5章 氧化还原反应与电化学

氧化数降低
氧化: 氧化数升高 (失去电子)的过程。 还原: 氧化数降低的过程。 还原剂:反应过程中氧化数升高(失去电子)的物质。 氧化剂:氧化数降低(得电子)的物质。
北化京学交系通大学 理学院 化学系 5
工科化学
工科化学
氧化数降低
Cl2 + H2O = HCl + HClO
氧化数升高
在氧化还原反应中,氧化数的升高和氧化数的 降低是同一物质的同一元素,则将此反应称为 歧化反应。
例题7 由 Fe3+/Fe2+ 、Pt/MnO4-,Mn2+,H+组成原电池 ()Pt Fe3+ (c1), Fe2+ (c2 ) MnO4 (c3), Mn2+ (c4 ), H + Pt(+)
北化京学交系通大学 理学院 化学系 27
工科化学
工科化学
根据原电池的图示,写出氧化还原反应。
(-)Zn|Zn2+(c) ‖ Cu2+(c′)|Cu(+)
电荷数。
③在大多数化合物中,氢的氧化数为 +1;在金属氢 化物中氢的氧化数为-1。
④通常,氧在化合物中的氧化数为-2;在过氧化物中, 氧的氧化数为-1,在氟的氧化物中,如OF2和O2F2 中,氧的氧化数分别为+2和+1。
⑤中性分子中,各元素原子的氧化数的代数和为零, 复杂离子的电荷等于各元素氧化数的代数和。
() Pt Fe2+ 1.0mol L1 , Fe3+ 0.1mol L1 ‖ Cl 2.0mol L1 Cl2 101325Pa |,Pt (+)
北化京学交系通大学 理学院 化学系 26
工科化学
工科化学
工科化学问题详解第五章氧化还原反应与电化学

第五章氧化还原反应与电化学教学容1. 氧化数;2.原电池与原电池电动势;3. 金属的腐蚀与防护;4.电解的基本原理及应用。
教学要求了解氧化数的概念及确定方法;掌握原电池的组成、结构、符号表示、电极反应及电池反应的表示方法;了解电极电势的产生原因和测求方法;掌握浓度对电极电势的影响及Nernst方程的有关计算;了解电解池的结构特点;理解理论分解电压、实际分解电压的概念及产生原因;了解电解的应用;熟悉金属电化学腐蚀的产生原因及析氢腐蚀、吸氧腐蚀的主要特点;了解电化学腐蚀的主要防护方法。
知识点与考核点1.氧化数某元素的一个原子在化合状态时的形式电荷数.....(可以为分数)。
2.电对同一元素氧化数高的状态(氧化态)与其氧化数低的状态(还原态)构成一个电对。
通常表述为氧化态/还原态,例如,Cu2+/Cu、Zn2+/Zn、 Fe3+/Fe2+、Fe2+/Fe、O2/H2O2、H2O2/OH–等。
3.原电池借助氧化还原反应直接..产生电流的装置。
4.原电池装置的符号表示:(以铜锌原电池为例)(-)Zn | Zn2+(c1)|| Cu2+(c2)| Cu(+)负极反应:Zn(s)→Zn2+(aq)+2e–正极反应: Cu2+(aq)+2e–→Cu(s)电池总反应: Cu2+(aq)+ Zn(s)= Cu(s) + Zn2+(aq)5.原电池装置的符号表示书写规则(1)负极在左侧,正极在右侧,(2)两个半电池的中间用盐桥“||”连接,(3)盐桥两侧分别是正、负极的离子“Zn2+(c1)||Cu2+(c2)”,溶液需标出离子的浓度。
例:将下列氧化还原反应组成原电池,写出电极反应。
(1)Sn2+(aq)+2Fe3+(aq)= Sn4+(aq)+2Fe2+ (aq)解:原电池符号表示式为(-)Pt | Sn2+ (c1), Sn4+ (c2) || Fe3+ (c3), Fe2+ (c4) | Pt(+)负极反应:Sn2+(aq)→ Sn4+(aq)+2e–正极反应:2Fe3+(aq)+ 2e–→2Fe2+(aq)说明:① 反应物中氧化剂的还原反应为正极反应,还原剂的氧化反应为负极反应。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第五章氧化还原反应与电化学教学容1. 氧化数;2.原电池与原电池电动势;3. 金属的腐蚀与防护;4.电解的基本原理及应用。
教学要求了解氧化数的概念及确定方法;掌握原电池的组成、结构、符号表示、电极反应及电池反应的表示方法;了解电极电势的产生原因和测求方法;掌握浓度对电极电势的影响及Nernst方程的有关计算;了解电解池的结构特点;理解理论分解电压、实际分解电压的概念及产生原因;了解电解的应用;熟悉金属电化学腐蚀的产生原因及析氢腐蚀、吸氧腐蚀的主要特点;了解电化学腐蚀的主要防护方法。
知识点与考核点1.氧化数某元素的一个原子在化合状态时的形式电荷数.....(可以为分数)。
2.电对同一元素氧化数高的状态(氧化态)与其氧化数低的状态(还原态)构成一个电对。
通常表述为氧化态/还原态,例如,Cu2+/Cu、Zn2+/Zn、 Fe3+/Fe2+、Fe2+/Fe、O2/H2O2、H2O2/OH–等。
3.原电池借助氧化还原反应直接..产生电流的装置。
4.原电池装置的符号表示:(以铜锌原电池为例)(-)Zn | Zn2+(c1)|| Cu2+(c2)| Cu(+)负极反应:Zn(s)→Zn2+(aq)+2e–正极反应: Cu2+(aq)+2e–→Cu(s)电池总反应: Cu2+(aq)+ Zn(s)= Cu(s) + Zn2+(aq)5.原电池装置的符号表示书写规则(1)负极在左侧,正极在右侧,(2)两个半电池的中间用盐桥“||”连接,(3)盐桥两侧分别是正、负极的离子“Zn2+(c1)||Cu2+(c2)”,溶液需标出离子的浓度。
例:将下列氧化还原反应组成原电池,写出电极反应。
(1)Sn2+(aq)+2Fe3+(aq)= Sn4+(aq)+2Fe2+ (aq)解:原电池符号表示式为(-)Pt | Sn2+ (c1), Sn4+ (c2) || Fe3+ (c3), Fe2+ (c4) | Pt(+)负极反应:Sn2+(aq)→ Sn4+(aq)+2e–正极反应:2Fe3+(aq)+ 2e–→2Fe2+(aq)说明:① 反应物中氧化剂的还原反应为正极反应,还原剂的氧化反应为负极反应。
② 没有金属作为电极,故选用不参与反应、只起导电作用的Pt 或石墨等惰性电机作为辅助电极。
(2)2HCl (aq ) + Zn (s )= H 2(g )+ ZnCl 2(aq )解:原电池符号表示式为(-)Zn| Zn 2+(c 1) || H +(c 2) | H 2(p ),(Pt)(+) 正极反应:2H +(aq ) + 2e –→ H 2 g ) 负极反应:Zn (s )→ Zn 2+(aq )+ 2e –(3)2MnO –4(aq)+16H +(aq)+10Cl –(aq)+10Hg(l ) = 2Mn 2+(aq )+5Hg 2Cl 2(s) +8H 2O解:原电池符号表示式为(-)Pt ,Hg (l )| Hg 2Cl 2(s ),Cl –(c 1) || Mn 2+(c 2), H +(c 3),MnO –4(c 4)| Pt (+)正极反应:2MnO –4(aq )+ 16H +(aq )+10e–= 2Mn 2+(aq )+ 8H 2O负极反应:10Cl –(aq )+ 10Hg (l )= 5Hg 2Cl 2(s )+10e –6.电极电势(ϕ)的概念金属(或非金属)与溶液中自身离子达到平衡时双电层的电势差。
每 个电对都有电极电势,电极电势是强度性质。
因电极电势的绝对值无法测得,为比较方便,人为规定标准氢电极的电极电势V 0)/H (H 2=+Θϕ7.参比电极作为对比参考的电极,其电极电势要求相对稳定。
例如甘汞电极: (Pt )Hg(l ) | Hg 2Cl 2(s), KCl(c )电极反应式为 (g)Cl )Hg(2e 2(s)Cl Hg 222+=+-l 25℃, c (KCl)=1mol •L –1时,V 268.0/Hg)Cl (Hg 22=Θϕ25℃, c (KCl)为饱和浓度时,V 242.0/Hg)Cl (Hg 22=Θϕ8.原电池电动势-+-=ϕϕE (Θ-Θ+Θ-=ϕϕE )9.浓度(分压)对电极电势的影响(Nernst 方程) 对电极反应 a 氧化态 + ze – = b 还原态J lg 0z0.059-=ϕϕ (298.15K )J 为半反应的“浓度商”,abJ ][][氧化态还原态=z 为反应转移的电子数。
例如:--=+Cl 2e 2Cl 2 Θ-Θ-=pp c /)](Cl [lg 20.0592Cl 2ϕϕ --=+Cl e Cl 212 21Cl )/()](Cl [lg 10.0592Θ-Θ-=p p c ϕϕ可以看出:Nernst 方程表达式与化学方程书写方式有关..,但是计算结果与方程书写方式无.关.,因同一反应写法不同,z 也不同。
这也表现出ϕ之强度性质的特性。
例:写出下列电池半反应的Nernst 方程表达式 (1)Cu e 2Cu 2=+-+;答:)(Cu 1lg2+Θ-=c z0.059ϕϕ (2)MnO 2 + 4H ++ 2e – = Mn 2++ 2H 2O ;答: 42)(H )(Mn lg 2++Θ-=c c 0.059ϕϕ 利用上式可求出不同c (H +)和c (Mn 2+)时的电极电势值。
(3)参比甘汞电极--+=+Cl Hg 2e 2Cl Hg 22;答:2)(Cl lg 2059.0-Θ-=c ϕϕ; 例: 计算半反应 O 2 + 2H 2O + 4e – = 4OH –的电极电势(25℃)已知 5O 10013.12⨯=p Pa ,c (OH –) = 0.010mol ·L –1,40.0OH O2=Θ-ϕ(V )解 -OH O2ϕ = 0.40 +459.0)1.0(10013.1/10013.1lg 4059.0455=⨯⨯(V) 例: 求电对MnO -4/Mn 2+在下述条件下的电极电势(25℃), 已知:Θ+-24MnMnO ϕ=1.51V ,pH=2.0,c (Mn 2+)=c (MnO -4)=1.0 mol ·L –1解 此电极反应为MnO -4+ 8H + + 5e – = Mn 2++ 4H 2O)](Mn [)](H )][(MnO [lg 5059.0284++-Θ+=c c c ϕϕ = 1.51 + 0.1)100.1(0.1lg 5059.082-⨯⨯= 1.51 – 0.19 = 1.32(V)10.电极电势的应用(1)判断氧化剂、还原剂的相对强弱电极电势大的氧化态物质的氧化能力强; 电极电势小的还原态物质的还原能力强。
例如:CuCu 2+ϕ > ZnZn 2+ϕ 所以其氧化性Cu 2+ > Zn 2+; 还原性 Zn > Cu(2)判断氧化还原反应进行的方向判据:电极电势大的氧化态和电极电势小的还原态能自发反应∵CuCu 2+ϕ > ZnZn 2+ϕ ∴自发反应为 +2Cu +Zn → Cu ++2Zn(3)判断氧化还原反应进行的程度059.0lg ΘΘ=E Kz (z 为总.反应转移的电子数) 例:(1)判断MnO 2 + 4HCl = MnCl 2 + Cl 2 + 2H 2O 在标准状态下反应自发进行的方向; (2)判断c (HCl) =10 mol •L –1,c (Mn 2+)=1.0mol •L –1,p (Cl 2)=Θp 时的反应方向;(3)写出该条件下的电池符号,并求其反应的标准平衡常数。
解:(1)查表 Θ-ClCl2ϕ= 1.36 V > Θ+22Mn MnOϕ = 1.23 V∴标准条件下反应自发向左进行(2)用浓HCl (10mol ·L –1)(其它物质的浓度或压强为标准态)+22Mn MnOϕ= Θ+22Mn MnO ϕ+)](Mn [)](H [lg2059.024++c c = 1.23 + 0.1100.1lg 2059.04⨯ = 1.34 (V) =-ClCl2ϕΘ-Cl Cl2ϕ+2Cl )])(lg 2059.02-(Cl [c Θp p = 1.36 +2100.11lg 2059.0⨯= 1.30(V) ∵+22Mn MnOϕ> -Cl Cl2ϕ,∴反应自发向右进行,实验室可以用浓盐酸与二氧化锰反应制备氯气。
(3)原电池符号表示式为(–)Pt,Cl 2(Θp )|Cl –(10 mol •L –1)||Mn 2+(1mol •L –1),H +(10mol •L –1)|MnO 2(s),Pt (+)059.0)]/Cl (Cl )/Mn (MnO [lg 222-+-=ΘΘΘϕϕz K=059.0)36.123.1(2-⨯4.4-=;=ΘK 4.410- = 3.9×10–5 (其平衡常数很小,所以不能在标准状态下制取氯气)例:反应MnO -4+ 8H + + 5Fe 2+ = Mn 2+ + 4H 2O + 5Fe 3+(1)判断标准状态时,反应进行的方向。
(2)上述反应进行的限度(或ΘK )。
(3)用符号表示相应的原电池。
解 (1)查表Θ+-24MnMnO ϕ=1.51V, Θ++23Fe Fe ϕ= 0.77V 。
ϕ大的氧化态能与ϕ小的还原态自发反应, 所以标准状态下自发向右进行。
(2)059.0lg Θ=E K z =7.62059.0)77.051.1(5=-⨯; K 值非常大,反应很完全。
(3)(–)Pt | Fe 3+(c Θ),Fe 2+(c Θ)|| H +(c Θ),Mn 2+(c Θ),MnO -4(c Θ) | Pt(+)11.原电池电动势与吉布斯函数变nFE G -=∆ (ΘΘ-=∆nFE G )F (法拉第常数)= 96485C ·mol –1,其意义是1mol 电子的电量。
例 :计算(–)Zn|Zn 2+(1mol ·L –1)||H +(1mol ·L –1)|H 2(100kPa )Pt (+)的吉布斯函数变(25℃)。
解:/Zn)(Zn )/H (H 22+Θ+ΘΘ-=ϕϕE= 0 – (– 0.7618) = 0.7618(V)ΘΔG = – ΘzFE = –2×96485 C ·mol –1 ×0.7618V –1= –147004 (J ·mol –1) 显见该反应的推动力较大。
12.化学腐蚀金属与干燥气体或非电解质直接发生反应而引起的腐蚀。
13.电化学腐蚀金属在水溶液或潮湿的空气中发生氧化还原反应引起的腐蚀。
(腐蚀电流为 短路、杂散电流,不可利用)14.析氢腐蚀在酸性介质中,由阴极以反应 2H e 2H 2=+-+ 引起的腐蚀。
