水的粘度与温度的关系对照表
海水粘度密度与温度对照表

海水粘度密度与温度对照表
密度、粘度是流体(液体或气体)的特性,会随着温度和压力的变化而变化。
对于海水,其密度和粘度也会随着温度的变化而变化。
以下是一份可能存在的海水粘度与密度与温度的关系对照表,但请注意这并非绝对准确的,因为海水的粘度和密度还会受到其他因
请注意,以上的数据是基于一般规律,实际上海水的密度和粘度可能受到更多其他因素的影响,例如盐度、压力、风力、地理位置等。
对于更精确的数据,您可能需要查阅专门的海水数据库或者咨询海洋科学专家。
水的粘度计算表
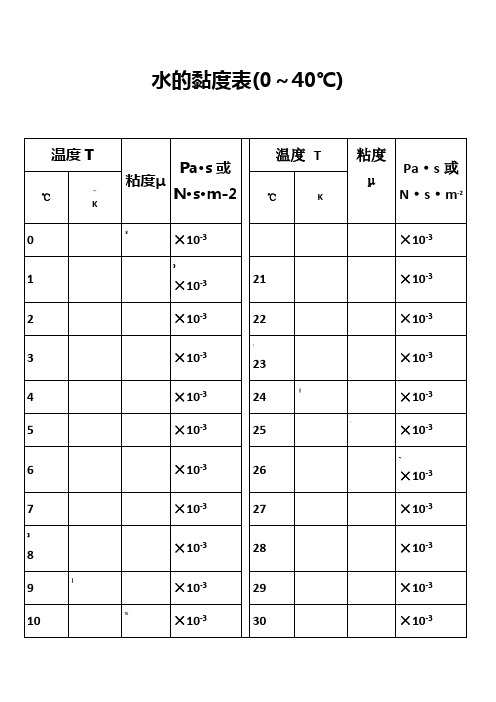
水的黏度表(0~40℃)水的物理性质F3 Viscosity decreases with pressure(at temperatures below 33°C)Viscous flow occurs by molecules moving through the voids that exist between them. As the pressure increases, the volume decreases and the volume of these voidsreduces, so normally increasing pressure increases the viscosity. 340350360109 370264Water's pressure-viscosity behavior [534] can be explained by the increased pressure (up to about 150 MPa) causing deformation, so reducing the strength of the hydrogen-bonded network, which is also partially responsible for the viscosity. This reduction in cohesivity more than compensates for the reduced void volume. It is thus a direct consequence of the balance between hydrogen bonding effects and the van der Waals dispersion forces [558] in water; hydrogen bonding prevailing at lower temperatures and pressures. At higher pressures (and densities), the balance between hydrogen bonding effects and the van der Waals dispersion forces is tipped in favor of the dispersion forces and the remaining hydrogen bonds are stronger due to the closer proximity of the contributing oxygen atoms [655]. Viscosity, then, increases with pressure. The dashed line (opposite) indicates the viscosity minima.The variation of viscosity with pressure and temperature has been used as evidence that the viscosity is determined more by the extent of hydrogen bonding rather than hydrogen bonding strength.Self-diffusion is also affected by pressure where (at low temperatures) both the translational and rotational motion of water anomalously increase as the pressure increases.。
水的粘度随温度的对照表
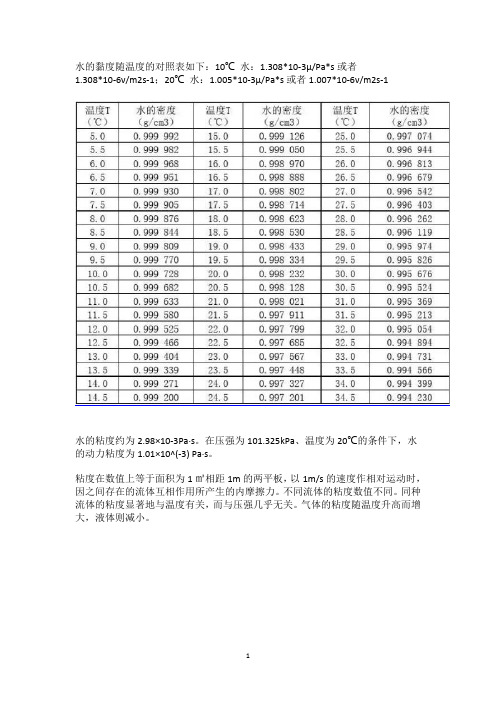
水的黏度随温度的对照表如下:10℃水:1.308*10-3μ/Pa*s或者
1.308*10-6ν/m2s-1;20℃水:1.005*10-3μ/Pa*s或者1.007*10-6ν/m2s-1
水的粘度约为2.98×10-3Pa·s。
在压强为101.325kPa、温度为20℃的条件下,水的动力粘度为1.01×10^(-3) Pa·s。
粘度在数值上等于面积为1㎡相距1m的两平板,以1m/s的速度作相对运动时,因之间存在的流体互相作用所产生的内摩擦力。
不同流体的粘度数值不同。
同种流体的粘度显著地与温度有关,而与压强几乎无关。
气体的粘度随温度升高而增大,液体则减小。
水的密度异乎寻常。
通常,在冷却过程中,液体密度会越来越大。
然而,水在4摄氏度时达到最大密度。
在这个温度以下,水的密度反而会下降。
所以,冰的密度比水小。
因此,冰会漂浮在水面,而水的冷冻是自上而下的。
水的表面张力非常高。
除水银外,它在所有液体中具有最高的表面张力。
因此,水蜘蛛能够站立在水上。
此外,水的沸点也高得异乎寻常。
还有,相较于其它液体,水能够溶解许多化学物质这点也很奇特。
不同温度下水的粘滞系数

不同温度下水的粘滞系数
水的粘滞系数是指水在一定温度下,单位速度梯度下单位体积流体所具有的粘性阻力,通常用η表示。
粘滞系数是流体力学中的一个重要参数,它反映了流体在运动时的内部阻力,与流体的种类、温度和压力等因素有关。
在常温下,水的粘滞系数约为1×10^-3帕秒(Pas)或1×10^-3 kg/(m·s),但这会随着温度的变化而变化。
水的粘滞系数随着温度的升高而减小,这意味着在高温下,水流会变得更顺畅,而低温下水流会受到更大的阻力。
以下是一些不同温度下水的粘滞系数的近似值:
●0摄氏度(32华氏度):1.796×10^-3 Pas
●20摄氏度(68华氏度):1.005×10^-3 Pas
●40摄氏度(104华氏度):6.79×10^-4 Pas
●60摄氏度(149华氏度):4.42×10^-4 Pas
●80摄氏度(176华氏度):2.94×10^-4 Pas
●100摄氏度(212华氏度):2.13×10^-4 Pas
这些数值可以帮助我们了解在不同温度下水的粘滞性如何变化。
例如,当我们在热水中游泳或洗澡时,由于水的粘滞系数较低,水流会更加顺畅,而不会受到过多的阻力。
而在冷水中游泳或洗澡时,由于水的粘滞系数较高,水流会受到较大的阻力,感觉更加粘稠。
需要注意的是,这些数值是近似值,实际的水粘滞系数可能会因为压力、水质和其他因素的影响而略有不同。
如果需要更精确的值,可以参考相关的流体动力学手册或实验数据。
水的粘度对照表

水的粘度对照表水的粘度是指水流动时所表现出的阻力大小,也就是水的黏度。
水的黏度值与温度有关,在不同温度下的水黏度值也是不同的。
以下是水的粘度对照表,列出了不同温度下水的粘度值。
一、水在0℃以下的黏度:水在0℃以下始终处于冰冻状态,此时无法测量其粘度值。
二、水在0℃~5℃的黏度:水在0℃~5℃范围内属于冷水,虽然温度较低但黏度并不高,粘度值约为0.00153 Pa·s。
三、水在5℃~10℃的黏度:水在5℃~10℃的温度下,黏度值开始升高,约为0.00131 Pa·s。
四、水在10℃~15℃的黏度:水在10℃~15℃的温度下,黏度值约为0.00114 Pa·s。
五、水在15℃~20℃的黏度:水在15℃~20℃的温度下,黏度值逐渐升高,约为0.001 Pa·s。
六、水在20℃~25℃的黏度:水在20℃~25℃的温度下,黏度值约为0.00089 Pa·s。
七、水在25℃~30℃的黏度:水在25℃~30℃的温度下,黏度值约为0.00081 Pa·s。
八、水在30℃~35℃的黏度:水在30℃~35℃的温度下,黏度值逐渐升高,约为0.00075 Pa·s。
九、水在35℃~40℃的黏度:水在35℃~40℃的温度下,黏度值约为0.0007 Pa·s。
十、水在40℃以上的黏度:水在40℃以上的温度下,黏度值不断升高,约为0.00064 Pa·s。
总结来说,水的黏度随着温度的升高而升高,但这种变化趋势并不是线性的,大致呈现出曲线形态。
在一定温度范围内,水的黏度值并不会随着温度的升高而在同样的比例增加,因为水的黏度受到温度、压力、浓度等多方面的影响,因此需要对不同条件下的水进行具体的测试才能得到精确的黏度值。
水的粘度计算表

水的粘度计算表 Revised as of 23 November 2020水的黏度表(0~40℃)水的物理性质F3 Viscosity decreases with pressure(at temperatures below 33°C)Viscous flow occurs by molecules moving through the voids that exist between them. As the pressure increases, the volume decreases and the volume of thesevoids reduces, so normally increasing pressure increases the viscosity.Water's pressure-viscosity behavior [] can be explained by the increased pressure (up to about 150 MPa) causing deformation, so reducing the strength of the hydrogen-bonded network, which is also partially responsible for the viscosity. This reduction in cohesivity more than compensates for the reduced void volume. It is thus a direct consequence of the between hydrogen bonding effects and the van der Waals dispersion forces [] in water; hydrogen bonding prevailing at lower temperatures and pressures. At higher pressures (and densities), the between hydrogen bonding effects and the van der Waals dispersion forces is tipped in favor of the dispersion forces and the remaining are stronger due to the closer proximity of the contributing oxygen atoms []. Viscosity, then, increases with pressure. The dashed line (opposite) indicates the viscosity minima.The variation of viscosity with pressure and temperature has been used as evidence that the viscosity is determined more by the extent of hydrogen bonding rather than hydrogen bonding strength.Self-diffusion is also affected by pressure where (at low temperatures) both the translational and rotational motion of water anomalously increase as the pressure increases.。
水的粘度计算表
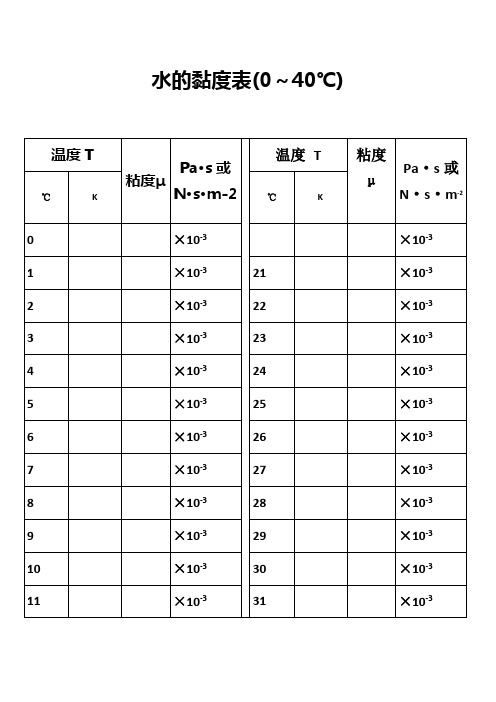
水的黏度表(0~40℃)水的物理性质370264F3 Viscosity decreases with pressure(at temperatures below 33°C)Viscous flow occurs by molecules moving through the voids that exist between them.As the pressure increases, the volume decreases and the volume of these voidsreduces, so normally increasing pressure increases the viscosity.Water's pressure-viscosity behavior [534] can be explained by the increased pressure(up to about 150 MPa) causing deformation, so reducing the strength of thehydrogen-bonded network, which is also partially responsible for the viscosity. Thisreduction in cohesivity more than compensates for the reduced void volume. It isthus a direct consequence of the balance between hydrogen bonding effects and thevan der Waals dispersion forces [558] in water; hydrogen bonding prevailing at lowertemperatures and pressures. At higher pressures (and densities), the balancebetween hydrogen bonding effects and the van der Waals dispersion forces is tippedin favor of the dispersion forces and the remaining hydrogen bonds are stronger dueto the closer proximity of the contributing oxygen atoms [655]. Viscosity, then, increases with pressure. The dashed line (opposite) indicates the viscosity minima.The variation of viscosity with pressure and temperature has been used as evidence that the viscosity is determined more by the extent of hydrogen bonding rather than hydrogen bonding strength.Self-diffusion is also affected by pressure where (at low temperatures) both the translational and rotational motion of water anomalously increase as the pressure increases.。
水的动力粘度与温度对照表

水的动力粘度与温度对照表表:水的动力粘度与温度对照① 0℃时:动力粘度为:1.7989×10-3 PXa.s② 15℃时:动力粘度为:1.0037×10-3 PXa.s③ 30℃时:动力粘度为:0.588×10-3 PXa.s④ 50℃时:动力粘度为:0.334×10-3 PXa.s⑤ 70℃时:动力粘度为:0.1956×10-3 PXa.s⑥ 90℃时:动力粘度为:0.1144×10-3 PXa.s水是自然界最常用的液体物质,在生物的各个过程中起着至关重要的作用。
动力粘度是温度对水流动粘度的表现,对于农业水利、机械工程、液压传动及温度传递设备等工业部门都有很重要的意义。
以下是水的动力粘度与温度间的对照表:以0℃为基准,其动力粘度为1.7989×10-3 PXa.s;水的温度升高到15℃时,其动力粘度会变成1.0037×10-3 PXa.s;当水的温度升高到30℃时,动力粘度变成0.588×10-3 PXa.s;随着水的温度继续上升到50℃时,其动力粘度变成0.334×10-3 PXa.s;继续往上加温至70℃时,动力粘度会变成0.1956×10-3 PXa.s;最后在90℃时,动力粘度变成0.1144×10-3 PXa.s。
根据此表可知,随着温度的升高,水的动力粘度呈现出逐渐减弱的趋势,其中升高每10℃温度所引起的动力粘度变化差值可以逐步趋于0.66X×10-3 PXa.s。
因此,水的动力粘度的变化受温度的大幅影响,只有准确地测量了水的温度,才能够准确测量出水的动力粘度。
而温度这一因素也是一些水利建设及机械设备运行过程中必不可少程度的一种因素。
因此,为了更好地推进水利建设、机械设备发展,以及各类水流体运行过程,研究者们必须更精确准确地测量及分析水的温度及动力粘度间的关系。
水的粘度计算表

313.16
0.6560
0.6560×10-3
水的物理性质
温度t/℃
饱和蒸气压p/kPa
密度ρ/kg·m-3
焓
H/kJ·kg-1
比定压热容cp/kJ·kg-1·K-1
导热系数λ/10-2W·m-1·K-1
粘度μ/10-5Pa·s
体积膨胀系数α/10-4K-1
表面张力σ/10-3N·m-1
普兰德数Pr
(at temperatures below33°C)
Viscous flow occurs by molecules moving through the voids that exist between them. As the pressure increases, the volume decreases and the volume of these voids reduces, so normally increasing pressure increases the viscosity.
290
7443.29
732.3
1289.95
5.485
55.82
9.42
26.2
17.2
0.93
300
8592.94
712.5
1344.80
5.736
53.96
9.12
29.2
14.7
0.97
310
9877.96
691.1
1402.16
6.071
52.34
8.83
32.9
12.3
1.02
320
11300.3
934.8
546.38
4.266
水的粘度计算表
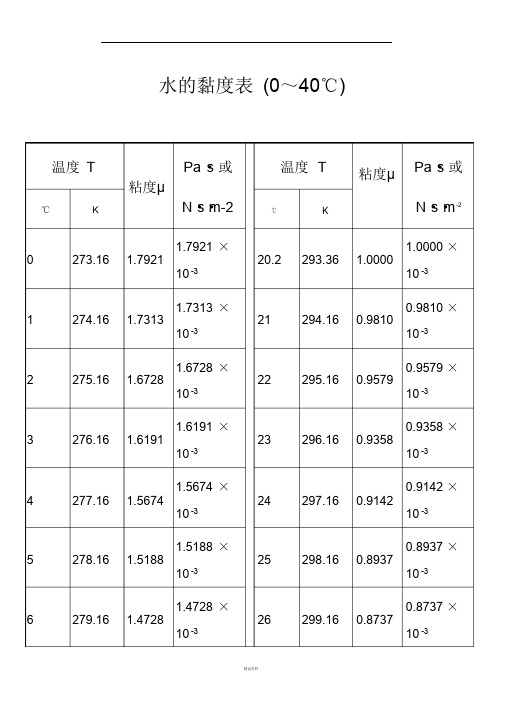
水的黏度表(0~40℃)温度T Pa ·s 或粘度μ温度T 粘度μPa·s 或℃KN·s·m-2 ℃K N·s·m-20 273.16 1.79211.7921 ×10 -3 20.2 293.36 1.00001.0000 ×10 -31 274.16 1.73131.7313 ×10 -3 21 294.16 0.98100.9810 ×10 -32 275.16 1.67281.6728 ×10 -3 22 295.16 0.95790.9579 ×10 -33 276.16 1.61911.6191 ×10 -3 23 296.16 0.93580.9358 ×10 -34 277.16 1.56741.5674 ×10 -3 24 297.16 0.91420.9142 ×10 -35 278.16 1.51881.5188 ×10 -3 25 298.16 0.89370.8937 ×10 -36 279.16 1.47281.4728 ×10 -3 26 299.16 0.87370.8737 ×10 -37 280.16 1.42841.4284 ×10 -3 27 300.16 0.85450.8545 ×10 -38 281.16 1.38601.3860 ×10 -3 28 301.16 0.83600.8360 ×10 -39 282.16 1.34621.3462 ×10 -3 29 302.16 0.81800.8180 ×10 -310 283.16 1.3077 1.3077 ×10 -330 303.16 0.80070.8007 ×10 -311 284.16 1.27131.2713 ×10 -3 31 304.16 0.78400.7840 ×10 -312 285.16 1.23631.2363 ×10 -3 32 305.16 0.76790.7679 ×10 -313 286.16 1.2028 1.2028 ×10 -333 306.16 0.75230.7523 ×10 -314 287.16 1.17091.1709 ×10 -3 34 307.16 0.73710.7371 ×10 -315 288.16 1.1404 1.1404 ×35 308.16 0.72250.7225 ×10 -3 10 -316 289.16 1.1111 1.1111 ×36 309.16 0.7085 0.7085 ×10 -3 10 -317 290.16 1.08281.0828 ×10 -3 37 310.16 0.69470.6947 ×10 -318 291.16 1.05591.0559 ×10 -3 38 311.16 0.68140.6814 ×10 -319 292.16 1.02991.0299 ×10 -3 39 312.16 0.66850.6685 ×10 -320 293.16 1.00501.0050 ×10 -3 40 313.16 0.65600.6560 ×10 -3水的物理性质温度t/℃饱和蒸气压p/kPa密度ρ/kg ·m-3焓H/kJ ·kg-1比定压热容c p /kJ·kg -1·K -1导热系数λ/10 -2 W·m-1 ·K-1粘度μ/10 -5 Pa ·s体积膨胀系数α/10 -4K -1表面张力σ/10 -3 N·m-1普兰德数Pr0 0.6082 999.9 0 4.212 55.13 179.21 0.63 75.6 13.66 10 1.2262 999.7 42.04 4.197 57.45 130.77 0.70 74.1 9.52 20 2.3346 998.2 83.90 4.183 59.89 100.50 1.82 72.6 7.0130 4.2474 995.7 125.69 4.174 61.76 80.07 3.21 71.2 5.42 40 7.3766 992.2 165.71 4.174 63.38 65.60 3.87 69.6 4.32 50 12.31 988.1 209.30 4.174 64.78 54.94 4.49 67.7 3.54 60 19.932 983.2 251.12 4.178 65.94 46.88 5.11 66.2 2.98 70 31.164 977.8 292.99 4.178 66.76 40.61 5.70 64.3 2.54 80 47.379 971.8 334.94 4.195 67.45 35.65 6.32 62.6 2.22 90 70.136 965.3 376.98 4.208 67.98 31.65 6.95 60.7 1.96 100 101.33 958.4 419.10 4.220 68.04 28.38 7.52 58.8 1.76 110 143.31 951.0 461.34 4.238 68.27 25.89 8.08 56.9 1.61 120 198.64 943.1 503.67 4.250 68.50 23.73 8.64 54.8 1.47 130 270.25 934.8 546.38 4.266 68.50 21.77 9.17 52.8 1.36 140 361.47 926.1 589.08 4.287 68.27 20.10 9.72 50.7 1.26 150 476.24 917.0 632.20 4.312 68.38 18.63 10.3 48.6 1.18 160 618.28 907.4 675.33 4.346 68.27 17.36 10.7 46.6 1.11 170 792.59 897.3 719.29 4.379 67.92 16.28 11.3 45.3 1.05 180 1003.5 886.9 763.25 4.417 67.45 15.30 11.9 42.3 1.00 190 1255.6 876.0 807.63 4.460 66.99 14.42 12.6 40.8 0.96200 1554.77 863.0 852.43 4.505 66.29 13.63 13.3 38.4 0.93 210 1917.72 852.8 897.65 4.555 65.48 13.04 14.1 36.1 0.91 220 2320.88 840.3 943.70 4.614 64.55 12.46 14.8 33.8 0.89 230 2798.59 827.3 990.18 4.681 63.73 11.97 15.9 31.6 0.88 240 3347.91 813.6 1037.49 4.756 62.80 11.47 16.8 29.1 0.87 250 3977.67 799.0 1085.64 4.844 61.76 10.98 18.1 26.7 0.86 260 4693.75 784.0 1135.04 4.949 60.84 10.59 19.7 24.2 0.87 270 5503.99 767.9 1185.28 5.070 59.96 10.20 21.6 21.9 0.88 280 6417.24 750.7 1236.28 5.229 57.45 9.81 23.7 19.5 0.89 290 7443.29 732.3 1289.95 5.485 55.82 9.42 26.2 17.2 0.93 300 8592.94 712.5 1344.80 5.736 53.96 9.12 29.2 14.7 0.97 310 9877.96 691.1 1402.16 6.071 52.34 8.83 32.9 12.3 1.02 320 11300.3 667.1 1462.03 6.573 50.59 8.53 38.2 10.0 1.11 330 12879.6 640.2 1526.19 7.243 48.73 8.14 43.3 7.82 1.22 340 14615.9 610.1 1594.75 8.164 45.71 7.75 53.4 5.78 1.38 350 16538.5 574.4 1671.37 9.504 43.03 7.26 66.8 3.89 1.60 360 18667.1 528.0 1761.39 13.984 39.54 6.67 109 2.06 2.36370 21040.9 450.5 1892.43 40.319 33.73 5.69 264 0.48 6.80 F3 Viscosity decreases with pressure(at temperatures below 33 °C)Viscous flow occurs by molecules moving through the voids that exist betweenthem. As the pressure increases, the volume decreases and the volume ofthese voids reduces, so normally increasing pressure increases the viscosity.Water's pressure-viscosity behavior [534] can be explained by the increased pressure (up to about 150 MPa) causing deformation, so reducing the strength of the hydrogen-bonded network, which is also partially responsible for the viscosity. This reduction in cohesivity more than compensates for the reduced void volume. It is thus a direct consequence of the balance between hydrogen bonding effects and the van der Waals dispersion forces [558] in water; hydrogen bonding prevailing at lower temperatures and pressures. At higher pressures (and densities), the balance between hydrogen bonding effects and the van der Waals dispersion forces is tipped in favor of the dispersion forces and the remaining hydrogen bonds are stronger due to the closer proximity of the contributing oxygen atoms [655]. Viscosity, then, increases with pressure. The dashed line (opposite) indicates the viscosity minima.The variation of viscosity with pressure and temperature has been used as evidence that the viscosity is determined more by the extent of hydrogen bonding rather than hydrogen bonding strength.Self-diffusion is also affected by pressure where (at low temperatures) both the translational and rotational motion of water anomalously increase as the pressure increases.Welcome To Download !!!欢迎您的下载,资料仅供参考!。
水的粘度0-40℃

水的粘度0-40℃水的粘度 0 40℃在我们日常生活和众多的工业领域中,水是一种极为常见且至关重要的物质。
而水的粘度这一特性,虽然不常被我们直接提及,但却在许多方面默默地发挥着重要作用。
今天,咱们就来深入探讨一下水在 0 40℃这个温度范围内的粘度变化。
首先,咱们得明白啥是粘度。
简单来说,粘度就是液体内部抵抗流动的一种性质。
想象一下,蜂蜜和水倒出来时的不同状态,蜂蜜流动得很慢,这就是因为它的粘度比较大;水则能很快地流出来,说明水的粘度相对较小。
当温度在 0℃时,水处于冰水混合的状态。
此时,水的粘度相对较高。
这是因为在接近冰点时,水分子的运动变得相对迟缓,它们之间的相互作用增强,导致液体内部的阻力增大,从而使得粘度上升。
随着温度逐渐升高,比如说升到5℃左右,水的粘度开始逐渐降低。
这是因为温度的升高给了水分子更多的能量,让它们能够更加自由地运动。
分子运动速度加快,相互之间的束缚减小,水流动起来就更容易了,表现出来就是粘度的降低。
当温度继续上升到 20℃时,这是一个比较常见且舒适的室温环境。
在这个温度下,水的粘度进一步降低,水的流动性能变得更好。
此时的水在许多应用场景中都表现出了较为理想的流动性,比如在一些管道输送、工业生产过程中的液体处理等方面。
再把温度升到 30℃,水的粘度继续降低,但降低的幅度相比之前会逐渐变小。
此时,水分子的热运动更加剧烈,它们之间的相互作用进一步减弱。
而当温度达到 40℃时,水的粘度已经处于一个相对较低的水平。
不过,需要注意的是,虽然温度越高水的粘度越低,但这种降低并不是无限的。
那么,了解水在 0 40℃的粘度变化到底有啥用呢?其实,这在很多领域都有着重要的意义。
在工业生产中,比如化工行业,许多反应和工艺流程都涉及到水的输送和处理。
如果能准确掌握水在不同温度下的粘度,就能更好地设计管道、优化泵送系统,提高生产效率,降低能耗。
在食品加工行业,水的粘度也会影响到一些产品的质量和生产工艺。
水的运动粘度与温度对照表

水的运动粘度与温度对照表水是地球上最重要的物质之一,它支撑着我们的生活。
水的性质受到温度的影响,而水的运动粘度又是如何受到温度的影响的呢?下面通过一张对照表来比较水的运动粘度与温度之间的关系。
温度(°C)t运动粘度(mPas)-20t4.016-10t1.7950t1.00210t0.71820t0.55530t0.45040t0.37650t0.32660t0.29070t0.262t从上面的表格中可以看出,随着温度的升高,水的运动粘度明显降低。
因此,当温度上升时,水的分子间的相互作用就会变弱,水的分子与周围的空气和其他物质的碰撞增加,这就导致水的运动粘度降低。
反之亦然,当温度降低,水的分子间的相互作用就会增强,水分子与周围空气和其他物质的碰撞减少,水的运动粘度也就增加了。
运动粘度是水分子间相互作用的一种量化描述,表明水分子穿梭时施加的摩擦力。
水运动粘度的大小决定了它的流动速度,粘度越大,流动速度越慢;粘度越小,流动速度越快。
因此,水的运动粘度的变化不仅会影响它的流动性能,还会影响水及其他悬浮物的渗透性能。
此外,水的运动粘度不仅受温度的影响,也受其它因素的影响,如浓度、酸碱度等因素。
例如,当浓度增加时,粘度也会随之增加;当酸碱度增加时,粘度会降低。
这些因素可以使水的运动粘度产生更大的变化。
水是生命之源,水的质量、流动性和渗透性等性质相当重要。
因此,了解水的运动粘度与温度之间的关系,对于掌握水质、保护水环境具有重要意义。
本文通过一张对照表揭示了水的运动粘度与温度之间的关系,并对其它影响因素进行了描述,为深入研究水的物理特性提供了一些指标参考。
水的粘度0-40℃

水的粘度0-40℃水的粘度 0 40℃水,这一地球上最为常见且至关重要的物质,其性质在众多领域都有着深远的影响。
而水的粘度就是其中一个重要的特性。
在 0 40℃这个温度范围内,水的粘度会发生显著的变化。
粘度,简单来说,就是液体内部阻碍其流动的一种力量。
想象一下,把水比作一群人在拥挤的通道中移动,有的人走得快,有的人走得慢,相互之间的牵扯和阻碍就使得整体的移动变得不那么顺畅,这种不顺畅的程度就类似于液体的粘度。
在 0℃时,水处于冰水混合物的状态,即将结冰。
此时,水分子的运动相对缓慢,它们之间的相互作用力较强,导致水的粘度较大。
这就好像在寒冷的冬天,人们行动变得迟缓,彼此之间的联系也更加紧密,行动受到的阻碍更大。
随着温度的逐渐升高,当达到 4℃时,水的粘度会出现一个特殊的现象。
在这个温度下,水的密度达到最大值,而粘度相对较低。
这是因为水分子在 4℃时形成了一种特殊的排列结构,使得它们之间的阻碍相对减小,从而水能够更顺畅地流动。
继续升温,到 10℃左右,水的粘度进一步降低。
水分子获得了更多的能量,运动更加活跃,彼此之间的牵制减少,就像在春天里,人们脱去了厚重的棉衣,行动更加自如。
当温度达到 20℃时,水的粘度处于一个相对较低且较为稳定的状态。
这也是我们日常生活中常见的室温范围,在这个温度下,水的流动性能较好,无论是在工业生产中的管道输送,还是在日常生活中的用水场景,都能较为轻松地实现水的流动和利用。
而当温度接近 40℃时,水的粘度继续降低。
此时的水分子仿佛在夏日的高温下狂欢,极度活跃,快速地穿梭和流动,相互之间的阻碍变得更小。
水的粘度在 0 40℃的变化,对于许多领域都有着重要的意义。
在工业生产中,例如化工、制药等行业,准确了解水在不同温度下的粘度对于优化工艺流程、提高生产效率至关重要。
比如在管道输送液体时,如果不考虑粘度的变化,可能会导致管道堵塞、压力失衡等问题,从而影响生产的正常进行。
在环境科学领域,水的粘度变化也有着不可忽视的作用。
水的粘度0-40℃

水的粘度0-40℃水的粘度 0 40℃水,这一地球上最常见且至关重要的物质,其性质的研究在众多领域都具有重要意义。
其中,水的粘度就是一个关键的特性。
在 0 40℃的温度范围内,水的粘度会发生显著的变化。
首先,让我们来理解一下什么是粘度。
简单来说,粘度就是液体内部阻碍其流动的一种性质。
想象一下,蜂蜜和水同时从一个容器中倒出,蜂蜜流动得很慢,而水则相对快速,这就是因为蜂蜜的粘度比水大得多。
在 0℃时,水的粘度相对较高。
这是因为在低温下,水分子的运动速度减慢,它们之间的相互作用力增强。
水分子更倾向于形成较为稳定的结构,导致液体的流动阻力增大。
当温度逐渐升高到 40℃时,水的粘度会逐渐降低。
这是因为随着温度的上升,水分子获得了更多的能量,运动变得更加活跃,它们之间的相互束缚减小,从而使得水更容易流动。
那么,水的粘度在 0 40℃范围内的变化对于我们的日常生活和各种工业应用有着怎样的影响呢?在日常生活中,比如在冬季,水温较低时,水的粘度增加,管道中的水流速度可能会变慢。
如果管道没有良好的保暖措施,甚至可能会出现冻结和堵塞的情况。
而在夏季,水温较高,水的粘度降低,水流更加顺畅,例如在水龙头中流出的水感觉更加“有力”。
在工业领域,水的粘度变化也有着重要的意义。
在化工生产中,许多反应需要在特定的温度下进行,以控制反应物和产物在溶液中的扩散速度,而水的粘度变化会直接影响这一扩散过程。
例如,在某些化学反应中,如果需要加快反应速率,可能会选择在水的粘度较低的温度条件下进行。
在食品加工行业,水的粘度变化也会影响生产过程和产品质量。
比如在制作冰淇淋时,需要控制水的温度来调节混合物的粘度,以达到理想的口感和质地。
在医学领域,血液的粘度与水的粘度有一定的相似性。
研究水在不同温度下的粘度变化,可以为理解血液在人体中的流动和相关疾病的诊断提供一定的参考。
此外,在环境科学中,了解水的粘度变化对于研究水体中污染物的扩散和迁移也具有重要意义。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
水的粘度与温度的关系对照表
水的粘度是它分子间的相互作用力以及分子间距离的影响。
随着温度的升高,水分子之间的作用力减弱,分子间的距离变大,这会导致水的粘度减小。
下表的数据显示了粘度和温度之间的相关性:| 水的温度 | 水的粘度 |
| :---: | :---: |
| 0℃ | 1.794mPa|s |
| 10℃ | 1.002mPa|s |
| 15℃ | 0.890mPa|s |
| 20℃ | 0.794mPa|s |
| 25℃ | 0.711mPa|s |
从上表中可以看出,随着温度的升高,水的粘度逐渐降低,这是由于水分子在高温下逐渐分散,相互之间的作用力变弱,水分子之间的距离变大,因此水的粘度减小了。
粘度在普通条件下水的粘度是 1.794mPa|s,当水的温度升到10℃时,水的粘度降低到1.002mPa|s,水的粘度还会继续降低,到15℃和20℃,它的粘度减少到0.890mPa|s和0.794mPa|s;再到25℃时,水的粘度还会再次减少到0.711mPa|s。
因此,我们清楚地可以看到,随着温度的升高,水的粘度也会随之降低,这是由于水的分子在高温下,会减弱它们之间的作用力和距离,从而导致水的粘度也会变得更低。
