20180214关于规范使用“通过一致性评价”标识的通知
170825总局关于仿制药质量和疗效一致性评价工作有关事项的公告(2017年第100号)

总局关于仿制药质量和疗效一致性评价工作有关事项的公告(2017年第100号)颁布时间:20170825为做好仿制药质量和疗效一致性评价工作(以下简称一致性评价),现就有关事宜公告如下:一、为便于企业选择参比制剂,国家食品药品监督管理总局将把《关于落实〈国务院办公厅关于开展仿制药质量和疗效一致性评价的意见〉有关事项的公告》(2016年第106号)所附289个品种的原研企业药品列出清单并向社会公布,供企业选择参比制剂时参考。
清单分为已在中国境内上市和未在中国境内上市两类。
建议企业按以下顺序选择其一作为参比制剂备案:(一)原研药品:进口原研药品、经审核确定的原研企业在中国境内生产上市的药品、未进口原研药品;(二)在原研企业停止生产的情况下,可选择美国、日本或欧盟获准上市并获得参比制剂地位的药品。
对国家食品药品监督管理总局已公布的参比制剂,建议企业按照公布的参比制剂开展研究,未备案的无需再备案;对已公布的参比制剂存疑的,可向国家食品药品监督管理总局药品审评中心提出异议并说明理由,国家食品药品监督管理总局召开专家咨询委员会会议公开审议,并公开审议结果。
二、企业报国家食品药品监督管理总局备案的参比制剂全部向社会公开。
对国家食品药品监督管理总局未公布参比制剂的品种,由国家食品药品监督管理总局组织专家咨询委员会讨论后区别情况提出如下指导性意见:(一)可以确认符合参比制剂条件的;(二)存疑的;(三)明显不符合条件的。
对于(二)(三)两种情况是否继续进行研究或重新选择参比制剂,由企业自主决定并承担相应的责任。
三、企业自行从境外采购的参比制剂产品,在提交一致性评价资料时需提供购买凭证、产品包装及说明书等材料,或以其他适当方法证明所用参比制剂是标明企业的产品。
企业发现所使用的参比制剂产品为假冒产品的,应终止正在进行的研究工作,已申报的,应及时向国家食品药品监督管理总局药品审评中心报告并撤回一致性评价申请,视情况免于责任;监管部门发现企业使用的参比制剂产品为假冒产品的,应及时通报相关企业,终止审评审批;已批准上市的要撤销批准文件并向社会公开信息,责成企业作出解释并根据情况立案调查。
国家认监委关于发布2018年第一批认证认可行业标准的通知-国认科〔2018〕21号

国家认监委关于发布2018年第一批认证认可行业标准的通知正文:----------------------------------------------------------------------------------------------------------------------------------------------------国家认监委关于发布2018年第一批认证认可行业标准的通知国认科〔2018〕21号研究所、认可中心、认证认可协会,各相关认证机构、检验检测机构:经审查,现将《有机产品认证目录评估准则》等23项认证认可行业标准予以发布。
国家认监委2018年3月23日2018年第一批认证认可行业标准目录序号标准编号标准名称实施日期1RB/T164-2018有机产品认证目录评估准则2018-10-12RB/T165.1-2018有机产品产地环境适宜性评价技术规范第1部分:植物类产品2018-10-13RB/T165.2-2018有机产品产地环境适宜性评价技术规范第2部分:畜禽养殖2018-10-14RB/T165.3-2018有机产品产地环境适宜性评价技术规范第3部分:淡水水产养殖2018-10-15RB/T166-2018有机羊毛地毯认证技术规范2018-10-16RB/T167-2018有机葡萄酒加工技术规范2018-10-17RB/T168-2018有机液态乳加工技术规范2018-10-18RB/T169-2018有机产品(植物类)认证风险评估管理通用规范2018-10-19RB/T170-2018区域特色有机产品生产优势产地评价技术指南2018-10-110RB/T171-2018实验室测量审核结果评价指南2018-10-111RB/T172-2018实验动物机构标识系统要求2018-10-112RB/T173-2018实验动物人道终点评审指南2018-10-113RB/T174-2018司法鉴定/法庭科学机构能力认可专业要求2018-10-114RB/T175-2018生物质能可持续性认证要求2018-10-115RB/T220-2018检验检测机构资质认定能力评价信息安全检验检测机构要求2018-10-116RB/T251-2018钢铁企业温室气体排放核查技术规范2018-10-117RB/T252-2018化工企业温室气体排放核查技术规范2018-10-118RB/T253-2018电网企业温室气体排放核查技术规范2018-10-119RB/T254-2018发电企业温室气体排放核查技术规范2018-10-120RB/T255-2018电石企业温室气体排放核查技术规范2018-10-121RB/T256-2018合成氨企业温室气体排放核查技术规范2018-10-122RB/T257-2018甲醇企业温室气体排放核查技术规范2018-10-123RB/T258-2018乙烯企业温室气体排放核查技术规范2018-10-1——结束——。
CNCA-C18-04 -2014 强制性产品认证实施规则 消防装备产品

消防装备产品消防认证办理取证:13868763740(微信同号)周老师QQ124234871,专业认证办理服务
0 引言 本规则遵循法律法规对消防产品市场准入的基本要求,基于消防装备
产品的安全风险和认证风险制定,规定了消防装备产品实施强制性产品认 证的基本原则和要求。
本规则与国家认监委发布的《强制性产品认证实施规则 生产企业分 类管理、认证模式选择与确定》、《强制性产品认证实施规则 生产企业检 测资源及其他认证结果的利用》、《强制性产品认证实施规则 工厂检查通 用要求》等通用实施规则配套使用。
目录
0 引言 ................................................................................................................................. 1 1 适用范围 .......................................................................................................................... 1 2 认证依据标准 .................................................................................................................... 1 3 认证模式........................................................................................................................... 1 4 认证单元划
关于做好通过仿制药质量和疗效一致性评价药品供应保障工作的通知(1)

附件2青海省药品集中采购工作领导小组办公室关于做好通过仿制药质量和疗效一致性评价药品供应保障工作的通知青药采办〔2018〕5号各市、自治州卫生计生委,委属各医院,行业医院,省政府行政服务和公共资源交易中心:为贯彻落实国务院办公厅《关于开展仿制药质量和疗效一致性评价的意见》精神,保证人民群众用上质量优良、价格合理的药品,鼓励医疗机构采购和使用通过一致性评价品种,现就做好通过仿制药质量和疗效一致性评价品种供应保障工作通知如下:一、做好通过一致性评价品种挂网采购工作经国家食品药品监督管理总局批准通过仿制药质量和疗效一致性评价的药品和视同通过一致性评价的药品,参加我省药品集中采购时,与原研药同等对待。
对省级挂网目录内暂未纳入的通过一致性评价的药品,由省政府行政服务和公共资源交易中心将生产企业及药品品种公布后,医疗机构根据省药品集中采购工作领导小组办公室的相关要求,与生产企业进行议价采购。
二、优先使用通过一致性评价的药品对通过一致性评价的药品,各医疗机构要将其纳入与原研药可相互替代药品目录,优先采购和使用,采购未通过一致性评价国产同类品种的,其实际采购价格不得高于通过一致性评价品种。
同时加强原研药品和通过一致性评价品种的价格监测,确保价格趋向更加合理。
鼓励有条件的医疗机构开展通过一致性评价的品种的临床综合评价工作,推进一致性评价品种的合理使用。
同品种药品通过仿制药质量和疗效一致性评价的生产企业达到3家以上的,医疗机构药品集中采购不再选用未通过仿制药质量和疗效一致性评价的品种。
附件:通过仿制药质量和疗效一致性评价品种和视同通过一致性评价的药品挂网目录青海省药品集中采购工作领导小组办公室2018年4月11日(信息公开形式:主动公开)青海省卫生计生委办公室2018年4月11日印发校对:张勇2附件已通过仿制药质量和疗效一致性评价和视同通过一致性评价的药品挂网目录3。
国家食品药品监管总局公告2016年第105号――关于发布仿制药质量和

国家食品药品监管总局公告2016年第105号――关于发布仿制药质量和疗效一致性评价工作程序的公告【法规类别】药品管理【发文字号】国家食品药品监管总局公告2016年第105号【发布部门】国家食品药品监督管理总局【发布日期】2016.05.25【实施日期】2016.05.25【时效性】现行有效【效力级别】部门规范性文件国家食品药品监管总局公告(2016年第105号)关于发布仿制药质量和疗效一致性评价工作程序的公告为规范仿制药质量和疗效一致性评价工作,根据《国务院办公厅关于开展仿制药质量和疗效一致性评价的意见》(国办发〔2016〕8号)的有关要求,国家食品药品监督管理总局组织制定了《仿制药质量和疗效一致性评价工作程序》,现予发布。
特此公告。
附件:仿制药质量和疗效一致性评价工作程序国家食品药品监管总局2016年5月25日附件仿制药质量和疗效一致性评价工作程序为贯彻落实国务院办公厅《关于开展仿制药质量和疗效一致性评价的意见》(国办发〔2016〕8号),规范仿制药质量和疗效一致性评价工作申报流程,特制定本工作程序。
一、评价品种名单的发布国家食品药品监督管理总局发布开展仿制药质量和疗效一致性评价(以下简称一致性评价)的品种名单。
药品生产企业按照国家食品药品监督管理总局发布的品种名单,对所生产的仿制药品开展一致性评价研究。
二、企业开展一致性评价研究药品生产企业是开展一致性评价的主体。
对仿制药品(包括进口仿制药品),应参照《普通口服固体制剂参比制剂选择和确定指导原则》(国家食品药品监督管理总局公告2016年第61号),选择参比制剂,以参比制剂为对照药品全面深入地开展比对研究。
参比制剂需履行备案程序的,按照《仿制药质量和疗效一致性评价参比制剂备案与推荐程序》(国家食品药品监督管理总局公告2016年第99号)执行。
仿制药品需开展生物等效性研究的,按照《关于化学药生物等效性试验实行备案管理的公告》(。
国家药品监督管理局公告第

国家药品监督管理局公告第集团文件版本号:(M928-T898-M248-WU2669-I2896-DQ586-M1988)国家药品监督管理局公告2018年第4号关于批准发布YY/T0127.13—2018《口腔医疗器械生物学评价第13部分:口腔黏膜刺激试验》等8项医疗器械行业标准和2项修改单的公告YY/T0127.13-2018《口腔医疗器械生物学评价第13部分:口腔黏膜刺激试验》等8项医疗器械行业标准和YY0581.2-2011《输液连接件第2部分:无针连接件》第1号修改单、YY0598-2015《血液透析及相关治疗用浓缩物》第1号修改单已经审定通过,现予以公布。
标准自2019年5月1日起实施,修改单自发布之日起实施。
标准适用范围及修改单内容见附件。
特此公告。
附件:1.YY/T0127.13-2018《口腔医疗器械生物学评价第13部分:口腔黏膜刺激试验》等8项医疗器械行业标准适用范围2.YY0581.2-2011《输液连接件第2部分:无针连接件》第1号修改单3.YY0598-2015《血液透析及相关治疗用浓缩物》第1号修改单国家药品监督管理局2018年4月11日序号标准编号标准名称代替标准号发布日期实施日期1YY/T0127.13-2018口腔医疗器械生物学评价第13部分:口腔黏膜刺激试验YY/T0127.13-20092018-04-112019-05-012YY/T0127.15-2018口腔医疗器械生物学评价第15部分:亚急性和亚慢性全身毒性试验:经口途径YY/T0127.15-20092018-04-112019-05-013YY/T0497-2018一次性使用无菌胰岛素注射器YY0497-20052018-04-112019-05-014YY/T0521-2018牙科学种植体骨内牙种植体动态疲劳试验YY/T0521-20092018-04-112019-05-015YY/T0587-2018一次性使用无菌牙科注射针YY0587-20052018-04-112019-05-016YY/T1589-2018雌二醇测定试剂盒(化学发光免疫分析法)2018-04-112019-05-017YY/T1594-2018人抗甲状腺球蛋白抗体测定试剂盒2018-04-112019-05-018YY/T1598-2018组织工程医疗器械产品骨用于脊柱融合的外科植入物的骨修复或再生评价试验指南2018-04-112019-05-01。
289种药品列入一致性评价目录

289种药品列入一致性评价目录289种药品列入一致性评价目录CFDA今日发布关于落实《国务院办公厅关于开展仿制药质量和疗效一致性评价的意见》有关事项的公告(2016年第106号),指出289种化学药品仿制药口服固体制剂原则上应在2018年底前完成一至性评价。
以下全文:为贯彻落实《国务院办公厅关于开展仿制药质量和疗效一致性评价的意见》(国办发〔2016〕8号),提高仿制药质量,现将有关事项公告如下: 一、评价对象和实施阶段(一)化学药品新注册分类实施前批准上市的仿制药,包括国产仿制药、进口仿制药和原研药品地产化品种,均须开展一致性评价。
(二)凡2007年10月1日前批准上市的列入国家基本药物目录(2012年版)中的化学药品仿制药口服固体制剂(附件),原则上应在2018年底前完成一致性评价。
(三)上述第(二)款以外的化学药品仿制药口服固体制剂,企业可以自行组织一致性评价;自第一家品种通过一致性评价后,三年后不再受理其他药品生产企业相同品种的一致性评价申请。
二、参比制剂的选择和确定(四)药品生产企业对拟进行一致性评价的品种,参照《普通口服固体制剂参比制剂选择和确定指导原则》(食品药品监管总局公告2016年第61号)要求选择参比制剂。
(五)药品生产企业按照《仿制药质量和疗效一致性评价参比制剂备案与推荐程序》(食品药品监管总局公告2016年第99号),将选择的参比制剂向食品药品监管总局仿制药质量一致性评价办公室(以下简称一致性评价办公室)备案。
行业协会可向一致性评价办公室推荐参比制剂,原研药品生产企业、国际公认的同种药物生产企业可向一致性评价办公室申报参比制剂。
一致性评价办公室主动对参比制剂的备案、推荐和申报信息向社会公开。
食品药品监管总局及时公布推荐和确定的参比制剂信息,药品生产企业原则上应选择公布的参比制剂开展一致性评价。
(六)企业找不到且无法确定参比制剂的,由药品生产企业开展临床有效性试验。
三、一致性评价的研究内容(七)在开展一致性评价过程中,药品生产企业须以参比制剂为对照,全面深入地开展比对研究。
CNCA-C18-04 -2014 强制性产品认证实施规则 消防装备产品

编号:CNCA-C18-04:2014
强制性产品认证实施规则
消防装备产品
2014-05-30 发布
2014-09-01 实施
中国国家认证认可监督管理委员会发布
消防装备产品消防认证办理取证:13868763740(微信同号)周老师QQ124234871,专业认证办理服务
目录
0 引言 ................................................................................................................................. 1 1 适用范围 .......................................................................................................................... 1 2 认证依据标准 .................................................................................................................... 1 3 认证模式........................................................................................................................... 1 4 认证单元划分 .............................................
一致性评价相关法规汇总(更新至20180308)

关于2018年底前须仿制药质量和疗效完成一致性评价品种批准文号信息 总局关于发布化学药品仿制药口服固体制剂质量和疗效一致性评价申报资料要求(试行)的通告(2016年第120 号) 总局办公厅公开征求仿制药质量和疗效一致性评价改规格药品评价一般考虑的意见 总局办公厅公开征求仿制药质量和疗效一致性评价临床有效性试验一般考虑的意见 推进仿制药一致性评价提升行业发展水平——仿制药质量和疗效一致性评价有关政策解读 总局办公厅公开征求仿制药质量和疗效一致性评价工作中改盐基药品评价一般考虑的意见 总局办公厅公开征求仿制药质量和疗效一致性评价工作中改剂型药品(普通口服固体制剂)评价一般考虑的意见 仿制药质量和疗效一致性评价工作政策问答 总局办公厅公开征求仿制药质量和疗效一致性评价品种分类的指导意见的意见 总局办公厅公开征求进一步规范仿制药质量和疗效一致性评价参比制剂选择等相关事宜的指导意见的意见 总局办公厅公开征求仿制药质量和疗效一致性评价研究现场核查等指导原则的意见 总局关于发布仿制药质量和疗效一致性评价临床有效性试验一般考虑的通告(2017年第18号)
2018年需完成一致性评价的289个品种文号信息 通告附件 征求意见稿 征求意见稿 政策解读 征求意见稿 征求意见稿 政策解答 征求意见稿 征求意见稿 征求意见稿 通告附件 1.仿制药质量和疗效一致性评价工作中改规格药品(口服固 体制剂)评价一般考虑 2.仿制药质量和疗效一致性评价工作中改剂型药品(口服固 体制剂)评价一般考虑 3.仿制药质量和疗效一致性评价工作中改盐基药品评价一般 考虑 培训资料 名单 名单 通告附件 征求意见稿 名单 名单 1.仿制药质量和疗效一致性评价研制现场核查指导原则 2.仿制药质量和疗效一致性评价生产现场检查指导原则 3.仿制药质量和疗效一致性评价临床试验数据核查指导原则 4.仿制药质量和疗效一致性评价有因检查指导原则 征求意见稿 征求意见稿 征求意见稿 名单 名单 名单 正式通知已出(2017.8.25) 正式通知已出(2017.9.5) 正式通知已出(2017.5.18) 正式通知已出(2017.4.5) 正式通知已出(2017.2.17) 正式通知已出(2017.2.17) 正式通知已出(2017.2.17) 正式通知已出(2017.2.7)
CCCF-CPRZ-14:2018 电气火灾监控产品及可燃气体报警产品

5.2 认证时限............................................................................................................... 3 6. 获证前的认证要求 .................................................................................................3
3.1 认证的基本模式.................................................................................................... 2
3.2 认证模式的具体细化 ............................................................................................ 2 4. 认证单元划分 ........................................................................................................3 5. 认证基本流程及时限..............................................................................................3
刚刚CFDI发布仿制药一致性评价现场检查企业指南

刚刚!!发布仿制药一致性评价现场检查-企业指南为规范仿制药一致性评价现场检查工作,持续提高检查工作质量和效率,在原国家食品药品监督管理总局仿制药质量和疗效一致性评价相关文件的框架下,核查中心组织起草了《企业指南:质量和疗效一致性评价仿制药品药学研制现场检查要求》和《企业指南:质量和疗效一致性评价仿制药品生产现场检查要求》,现向社会公开征求意见。
请于2018年5月3日前将有关意见或建议以电子邮件形式反馈至核查中心。
真诚感谢一直以来对我中心工作的支持。
原国家食品药品监督管理总局食品药品审核查验中心(暂)2018年4月2日企业指南:质量和疗效一致性评价仿制药品药学研制现场检查要求(草案)一、前言为保证开展质量和疗效一致性评价的仿制药品药学研制现场检查工作的质量和效率,特制定本要求,本指南仅代表食品药品审核查验中心目前对相关事宜的考虑,将根据对检查工作的政策要求适时进行调整。
本指南所提及的仿制药具体指:化学药品新注册分类实施前批准上市的需开展一致性评价的仿制药。
本指南所指的检查要求主要包括:申请人在接受现场检查时,需提前准备的与产品注册、研制现场相关的资料和人员要求。
二、资料要求(一)首次会议企业汇报资料首次会议需要生产企业以幻灯片的形式介绍如下内容:药品研制基本情况(如属委托,应说明被委托研究单位基本情况)。
研制所涉及的批次(含批)批量用途,研制批次(含批)生产的地址、生产线、时间地点、使用量和剩余量等。
研制批次(含批)所用处方生产工艺、原辅料包装材料来源及标准、生产线(设备设施)、产品质量标准(含中间控制标准)等是否与已上市/拟上市商业化生产规模的批次一致。
参比制剂的来源、采购和使用情况。
药品和参比制剂体外研究的对比研究情况,研究时间、批号和研究结果药品关键质量属性(含稳定性)研究情况。
(二)检查时需事先准备的文件(尽可能提供原始文件)接受现场检查品种仿制药质量和疗效一致性评价全套注册申报资料。
委托研究协议和质量协议,如有。
国家药监局关于发布《化妆品功效宣称评价规范》的公告-国家药品监督管理局公告2021年第50号

国家药监局关于发布《化妆品功效宣称评价规范》的公告正文:----------------------------------------------------------------------------------------------------------------------------------------------------国家药品监督管理局公告2021年第50号国家药监局关于发布《化妆品功效宣称评价规范》的公告为贯彻落实《化妆品监督管理条例》,规范和指导化妆品功效宣称评价工作,国家药监局组织起草了《化妆品功效宣称评价规范》(以下称《规范》),现予公布,自2021年5月1日起施行。
现就实施有关问题公告如下:一、自2022年1月1日起,化妆品注册人、备案人申请特殊化妆品注册或者进行普通化妆品备案的,应当依据《规范》的要求对化妆品的功效宣称进行评价,并在国家药监局指定的专门网站上传产品功效宣称依据的摘要。
二、 2021年5月1日前已取得注册或者完成备案的化妆品,化妆品注册人、备案人应当于2023年5月1日前,按照《规范》要求,对化妆品的功效宣称进行评价,并上传产品功效宣称依据的摘要。
三、 2021年5月1日至2021年12月31日期间取得注册或者完成备案的化妆品,化妆品注册人、备案人应当于2022年5月1日前,按照《规范》要求,对化妆品的功效宣称进行评价,并上传产品功效宣称依据的摘要。
特此公告。
附件:化妆品功效宣称评价规范国家药监局2021年4月8日附件化妆品功效宣称评价规范第一条为规范化妆品功效宣称评价工作,保证功效宣称评价结果的科学性、准确性和可靠性,维护消费者合法权益,推动社会共治和化妆品行业健康发展,根据《化妆品监督管理条例》等有关法律法规要求,制定本规范。
第二条在中华人民共和国境内生产经营的化妆品,应当按照本规范进行功效宣称评价。
第三条本规范所称化妆品功效宣称评价,是指通过文献资料调研、研究数据分析或者化妆品功效宣称评价试验等手段,对化妆品在正常使用条件下的功效宣称内容进行科学测试和合理评价,并作出相应评价结论的过程。
国务院办公厅关于开展仿制药质量和疗效一致性评价的意见

国务院办公厅关于开展仿制药质量和疗效一致性评价的意见文章属性•【制定机关】国务院办公厅•【公布日期】2016.02.06•【文号】国办发〔2016〕8号•【施行日期】2016.02.06•【效力等级】国务院规范性文件•【时效性】现行有效•【主题分类】药政管理正文国务院办公厅关于开展仿制药质量和疗效一致性评价的意见国办发〔2016〕8号各省、自治区、直辖市人民政府,国务院各部委、各直属机构:开展仿制药质量和疗效一致性评价(以下简称一致性评价)工作,对提升我国制药行业整体水平,保障药品安全性和有效性,促进医药产业升级和结构调整,增强国际竞争能力,都具有十分重要的意义。
根据《国务院关于改革药品医疗器械审评审批制度的意见》(国发〔2015〕44号),经国务院同意,现就开展一致性评价工作提出如下意见:一、明确评价对象和时限。
化学药品新注册分类实施前批准上市的仿制药,凡未按照与原研药品质量和疗效一致原则审批的,均须开展一致性评价。
国家基本药物目录(2012年版)中2007年10月1日前批准上市的化学药品仿制药口服固体制剂,应在2018年底前完成一致性评价,其中需开展临床有效性试验和存在特殊情形的品种,应在2021年底前完成一致性评价;逾期未完成的,不予再注册。
化学药品新注册分类实施前批准上市的其他仿制药,自首家品种通过一致性评价后,其他药品生产企业的相同品种原则上应在3年内完成一致性评价;逾期未完成的,不予再注册。
二、确定参比制剂遴选原则。
参比制剂原则上首选原研药品,也可以选用国际公认的同种药品。
药品生产企业可自行选择参比制剂,报食品药品监管总局备案;食品药品监管总局在规定期限内未提出异议的,药品生产企业即可开展相关研究工作。
行业协会可组织同品种药品生产企业提出参比制剂选择意见,报食品药品监管总局审核确定。
对参比制剂存有争议的,由食品药品监管总局组织专家公开论证后确定。
食品药品监管总局负责及时公布参比制剂信息,药品生产企业原则上应选择公布的参比制剂开展一致性评价工作。
国家食品药品监督管理局关于开展仿制药质量一致性评价工作的通知-国食药监注[2013]34号
![国家食品药品监督管理局关于开展仿制药质量一致性评价工作的通知-国食药监注[2013]34号](https://img.taocdn.com/s3/m/63312d77b94ae45c3b3567ec102de2bd9605de6e.png)
国家食品药品监督管理局关于开展仿制药质量一致性评价工作的通知正文:---------------------------------------------------------------------------------------------------------------------------------------------------- 国家食品药品监督管理局关于开展仿制药质量一致性评价工作的通知(国食药监注[2013]34号)各省、自治区、直辖市食品药品监督管理局(药品监督管理局),新疆生产建设兵团食品药品监督管理局:开展仿制药质量一致性评价,全面提高仿制药质量是《国家药品安全“十二五”规划》的重要任务,是持续提高药品质量的有效手段,对提升制药行业整体水平,保障公众用药安全具有重要意义。
为此,国家食品药品监督管理局决定,对2007年修订的《药品注册管理办法》实施前批准的基本药物和临床常用仿制药,分期分批进行质量一致性评价。
现将有关事宜通知如下:一、充分认识重要意义。
各省级药品监督管理部门务必高度重视仿制药质量一致性评价工作,充分认识该项工作的重要性、复杂性和长期性,充分认识开展仿制药质量一致性评价对确保药品质量安全,促进医药经济结构调整和产业升级,进一步增强我国医药产业国际竞争能力的重要意义。
应将仿制药质量一致性评价工作纳入“十二五”期间药品监管工作重点,加强组织领导,落实工作责任,按照国家食品药品监督管理局工作部署,结合本行政区域实际情况,制定具体实施方案,确保各项工作落到实处。
二、积极宣传有关政策。
国家食品药品监督管理局制定了《仿制药质量一致性评价工作方案》(以下简称《工作方案》,附件),明确了质量一致性评价的工作目标、原则、内容和程序,对工作进行了总体部署。
国家食品药品监督管理局还将陆续下发相关技术指导原则,规范质量一致性评价的研究和技术审查。
各省级药品监督管理部门要积极落实《工作方案》,做好质量一致性评价工作的宣贯和培训,及时传达有关政策,使药品生产企业深刻认识质量一致性评价的重要性和必要性,引导药品生产企业积极开展研究,合理安排工作进度、主动作为。
仿制药质量一致性评价发布政策法规汇总
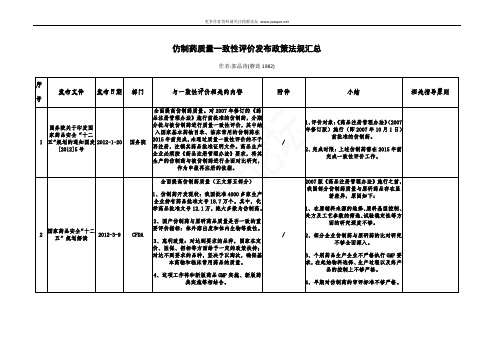
导原则(征求意见稿)
荐使用不少于 3 种 pH 值的溶出介质)及
通口服固体制剂参
2015-10-3
10 比制剂选择和确定
CFDA
0
3.仿制药质量一致性评价人体生物等效性研
体积选择(500ml、900ml 或 1000ml)3、 1-4
溶出曲线时间点选择 4、条件优化(在截
1-3
指导原则等意见的
究技术指导原则(征求意见稿)
局。
7、拟定了由中检院组织专家委员会在审 查一致性评价资料时一并审查处方、工艺 变更的工作流程。药审中心将参加专家委
员会,一并负责相关技术审查工作。
8、省局进行生产现场核查,连续抽取三 批样品送指定的药检所复核。
9、省局收到药检所复核结果后,将研究 资料及检验报告一并报专项办公室。
更多作者资料请关注药群论坛
国家食品药品监督 管理总局公开征求 6 仿制药质量一致性 2014-1-29 评价有关指导原则
等意见
CFDA CFDA
根据《国家食品药品监督管理局关于开展仿制 2013 年度仿制药
药质量一致性评价工作的通知》(国食药监注 质量一致性评价 涉及 75 个化学仿制药,制定评价方法的
〔2013〕34 号)要求,对 2013 年度仿制药质量 品种名单和方法 任务分发给中国食品药品检定研究院、其
2、对注册分类调整前受理的药品注册申请, 继续按照原规定进行审评审批,
国务院关于改革药
3、开展药品上市许可持有人制度试点。
品医疗器械审评审
ห้องสมุดไป่ตู้
4、改进药品临床试验审批。
批制度的意见 国发
9
2015-8-18 国务院
〔2015〕44 号
5、落实申请人主体责任。
《医疗器械说明书和标签管理规定》

二、规章条款详解
第一条 为规范医疗器械说明书和标签,保证医疗器械使用 的安全,根据《医疗器械监督管理条例》,制定本规定。 原办法《医疗器械说明书、标签和包装标识管理规定》, “包装标识”删除。 1.与国际接轨。从国际上看,普遍是采用Labeling一词,即 标签,并没有包装标识的概念。 2.与《医疗器械监督管理条例》 一致。条例中并未出现包装标识一词。 3.有利于概念的统一和 规范。修订过程中对于包装标识和标 签的定义进行了反复论 证,但难以形成一个清晰明确界限的定义。
一、规章修订概况和背景情况
第四十二条 进口的医疗器械应当是依照本条例第二章 的规定已注册或者已备案的医疗器械。 进口的医疗器械 应当有中文说明书、中文标签。说明书、标签应当符合 本条例规定以及相关强制性标准的要求,并在说明书中 载明医疗器械的原产 地以及代理人的名称、地址、联系 方式。没有中文说明书、中文标签或者说明书、标签不 符合本条规定的,不得进口。
一、规章修订概况和背景情况
第三十六条 医疗器械使用单位对需要定期检查、检验、 校准、保养、维护的医疗器械,应当按照产品说明书的要 求进行检查、检验、校准、保养、 维护并予以记录,及时 进行分析、评估,确保医疗器械处于良好状态,保障使用 质量;对使用期限长的大型医疗器械,应当逐台建立使用 档案,记录其 使用、维护、转让、实际使用时间等事项。 记录保存期限不得少于医疗器械规定使用期限终止后5年。 对经营和使用单位提出了要求。同时在第六十七条、 六十八条2条罚则中明确了各单位应承担的相应责任。
一、规章修订概况和背景情况
(七)安装和使用说明或者图示; (八)维护和保养方法,特殊储存条件、方法; (九)产品技术要求规定应当标明的其他内容。 第二类、第三类医疗器械还应当标明医疗器械注册证 编号和医疗器械注册人的名称、地址及联系方式。 由消费者个人自行使用的医疗器械还应当具有安全使 用的特别说明。 提出了医疗器械的说明书、标签的基本要求。
国家药品监督管理局办公室关于中药饮片标签标识有关问题的复函

国家药品监督管理局办公室关于中药饮片标签标识有
关问题的复函
文章属性
•【制定机关】国家药品监督管理局
•【公布日期】2018.08.30
•【文号】药监办函〔2018〕200号
•【施行日期】2018.08.30
•【效力等级】部门规范性文件
•【时效性】现行有效
•【主题分类】药政管理
正文
国家药品监督管理局办公室关于中药饮片标签标识有关问题
的复函
药监办函〔2018〕200号湖北省食品药品监督管理局:
你局《关于中药饮片标签标识有关问题的请示》(鄂食药监文〔2018〕41号)收悉。
经研究,现函复如下:
根据《中华人民共和国药品管理法》,中药饮片标签标识上标明的适应症或者功能主治应当符合国家药品标准的规定。
中药饮片标签标识超出国家药品标准规定的适应症或者功能主治范围的,属于《中华人民共和国药品管理法》第四十八条第三款第(六)项规定的"所标明的适应症或者功能主治超出规定范围的"情形,应当按假药论处。
国家药品监督管理局办公室
2018年8月30日。
