高中化学知识点复习PPT:常见的盐和化肥
合集下载
盐和化肥复习PPT课件
Ba(NO3)2溶 液和稀HNO3
HCl、NaCl、 AgNO3溶液 KCl、CaCl2 和稀HNO3
产生白色沉淀 白色沉淀不消失
产生白色沉淀 白色沉淀不消失
Na2CO3、 稀盐酸和澄 有无色气泡产 CaCO3、 清石灰水 生 澄清石灰水
K2CO3
变浑浊
有刺激性气味的气体
NH4HCO3 碱溶液(如NaOH) 产生气体,能使湿润的
碳酸钙
NaCl
食盐的主 要成分
作调味品,腌渍食品。医疗上 用来配制生理盐水,农业上来 选种。消除积雪。
Na2CO3
纯碱、苏打
用于生产玻璃、造纸、纺织、 洗涤剂。
NaHCO3 小苏打
发酵粉的主要成分,治疗胃 酸过多的药剂
CaCO3
大理石 石灰石主要 可用作建筑材料、补钙剂 成分
第2页/共28页
粗盐提纯
第21页/共28页
一看
<1>. N、P 、 K肥的区别 二闻
<2>. 几种氮肥的区别
第22页/共28页
三溶
CO(NH2)2 NH4Cl (NH4)2SO4 NH4NO3
Cl-、SO42- 、 CO32-、 NH4+的检验方法
离子 常见的物质 检验试剂
实验现象
SO42Cl-
CO32NH4+
H2SO4、 Na2SO4、 K2SO4
第26页/共28页
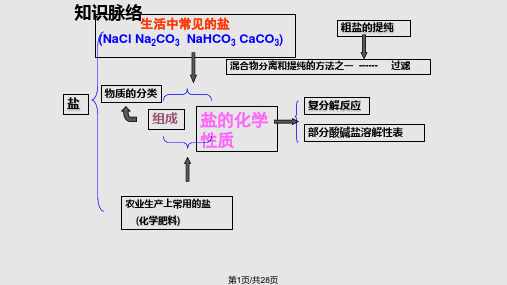
知识结构透视
常见的盐
NaCl
碳酸盐
粗盐的提纯 Na2CO3 NaHCO3 CaCO3
CO32-的检验
含金属离子(包括NH4+)和酸根离子的化合物
盐
复分解反应
概念 发生条件
生活中常见的盐及化学肥料 PPT教学课件 人教版

试根据相关信息计算:
⑴碳酸氢铵组成中有__4__种元素
⑵碳酸氢铵的相对分
子质量为__7_9__
⑶这种氮肥的纯度
是9__4_.8__%_
碳酸氢铵 (NH4HCO3)
净重:50kg 含氮量:16.8%
×××化学工业公司
5、⑴某学生家乡出现水稻倒伏现象,他通过 调查研究,发现主要原因是缺少 钾 肥,建议 农民适量施用草木灰或 KCl或K2SO(4 填化学式) ⑵大棚种植蔬菜在冬季需补充二氧化碳。某同学 在自家大棚内设计了补充二氧化碳的方法:将工 业废硫酸用水稀释后,盛放在塑料桶内,悬挂在 高处。每天向桶内加适量的碳酸氢铵,它和硫酸 反应生成硫酸铵、二氧化碳水。 ①写出该反应的化学方程式:
•
10、有些事想开了,你就会明白,在世上,你就是你,你痛痛你自己,你累累你自己,就算有人同情你,那又怎样,最后收拾残局的还是要靠你自己。
•
11、人生的某些障碍,你是逃不掉的。与其费尽周折绕过去,不如勇敢地攀登,或许这会铸就你人生的高点。
•
12、有些压力总是得自己扛过去,说出来就成了充满负能量的抱怨。寻求安慰也无济于事,还徒增了别人的烦恼。
•
13、认识到我们的所见所闻都是假象,认识到此生都是虚幻,我们才能真正认识到佛法的真相。钱多了会压死你,你承受得了吗?带,带不走,放,放不下。时时刻刻发悲心,饶益众生为他人。
•
14、梦想总是跑在我的前面。努力追寻它们,为了那一瞬间的同步,这就是动人的生命奇迹。
•
15、懒惰不会让你一下子跌倒,但会在不知不觉中减少你的收获;勤奋也不会让你一夜成功,但会在不知不觉中积累你的成果。人生需要挑战,更需要坚持和勤奋!
•
20、生活不会按你想要的方式进行,它会给你一段时间,让你孤独、迷茫又沉默忧郁。但如果靠这段时间跟自己独处,多看一本书,去做可以做的事,放下过去的人,等你度过低潮,那些独处的时光必定能照亮你的路,也是这些不堪陪你成熟。所以,现在没那么糟,看似生活对你的亏欠 ,其实都是祝愿。
《生活中常见的盐》盐化肥PPT课件(第2课时)

C.2KMnO4 D.2Na+2H2O
K2MnO4+MnO2+O2↑ 2NaOH+H2↑
5.要除去氯化钠溶液中少量的碳酸钠,可加入适量的
(
)。
A.石灰水 B.氯化钾溶液 C.盐酸 D.氯化钙溶液
6.(2017成都)能用于鉴别氢氧化钠溶液和氢氧化钙溶液的物
质是( )
A.HCl B.KNO3 C.K2CO3 D.FeCl3
___________________。
2.碳酸钠与氢氧化钙反应:
反应的化学方程式为
,工业上用该反
应制取烧碱。
3.复分解反应:两种 应,叫做复分解反应。
互相交换成分,生成另外两种
的反
4.(2017内江)下列反应属于复分解反应的是(
)
A.CO2+H2O
H2CO3
B.2HCl+Ca(OH)2
CaCl2+2H2O
+
+
AB + CD → AD + CB
思考:什么条件下复分解反应才能发生呢???
讲授新课
化合反应
化学基本反应类型的比较
分解反应
置换反应
定 义
类讲授新课
小结
盐的化学性质
1.盐溶液的酸碱性不确定。(如NaCl溶液呈中性,
Na2CO3溶液呈碱性,NH4Cl溶液呈酸性) 金属______________________
3.与盐溶液反应 【实验11-2】向盛有少量碳酸钠溶液 的试管中滴入氯化钡,观察现象。 现象: 分析:
硝酸银溶液
氯化钠 溶液
讲授新课
观察与思考
(1)CaCO3 +2HCl==CaCl2 + (2)Na2CO3 + 2HCl==2NaCl
盐化肥复习课PPT课件

盐化肥生产技术的发展与创新
传统盐化肥生产技术
传统盐化肥生产技术主要采用天然资源作为原料,通过化学反应制备而成。这种生产技术 具有原料丰富、工艺成熟等优点,但也存在能耗高、污染重等缺点。
新型盐化肥生产技术
新型盐化肥生产技术主要采用高新技术和环保理念,通过生物发酵、酶催化等手段制备而 成。这种生产技术具有能耗低、污染小、原料可再生等优点,但同时也存在成本高、技术 难度大等缺点。
02 盐化肥的应用
盐化肥在农业生产中的应用
盐化肥在农业生产中主要用于提高土壤肥力和促进作物生长 。通过施用盐化肥,可以增加土壤中的养分含量,提高土壤 的保水能力和通气性,促进作物根系发育和养分吸收,从而 提高作物的产量和品质。
盐化肥在农业生产中需要注意适量施用,避免过量使用导致 土壤盐碱化、水体富营养化等问题。同时,需要根据不同作 物和土壤类型选择合适的盐化肥品种和施用方法,以达到最 佳的施肥效果。
04 盐化肥的施用技术
盐化肥的施用方法与用量
施用方法
根据盐化肥的种类和土壤条件选择合适的施用方法,如撒施、条施、穴施等。
用量控制
根据作物种类、土壤肥力、气候条件等因素,合理确定盐化肥的施用量,避免过 量施用或不足。
盐化肥的配施原则与注意事项
配施原则
根据作物营养需求和土壤肥力状况, 合理搭配氮、磷、钾等营养元素,实 现平衡施肥。
注意事项
确保包装完好,防止泄漏、损坏。
运输过程中要保持干燥、防晒、密封,防止受潮、雨淋。
注意安全,遵守交通规则,防止发生交通事故。
盐化肥的安全管理措施
01
02
03
04
建立健全安全管理制度, 明确责任人。
对员工进行安全培训, 提高安全意识。
专题六 盐 化学肥料.ppt

5、初步认识复分解反应及发生的条件;
复分解反应的条件
生成物: 有气体、沉淀或水生成 反应物: 反应物中若没有酸,则两种
反应物均需可溶于水
能相互反应的离子
H+ + OH- = H2O 2 H+ + CO3 2- = H2O + CO2↑ OH- + NH4+ = NH3 ↑ + H2O 3 OH- + Fe3+ = Fe(OH)3↓ 2 OH- + Cu2+ = Cu (OH)2↓ 2 OH- + Mg2+ = Mg (OH)2↓ CO3 2- + Ca2+ = CaCO3 ↓ CO3 2- + Ba2+ = BaCO3 ↓ SO4 2- + Ba2+ = BaSO4 ↓ Cl - + Ag + = AgCl ↓
盐的命名:
正盐:无氧酸盐命名为“某化某”或“某 化亚某”如氯化钠(NaCl)、氯化亚铁 (FeCl2)。含氧酸盐命名为“某酸某”或 “某酸亚某”如硫酸铁[Fe2(SO4)3]、硫酸 亚铁(FeSO4)。
酸式盐:命名为“某酸氢某”如碳酸氢钠 (NaHCO3)、磷酸二氢铵(NH4H2PO4)。
碱式盐:命名为“碱式某酸某”如碱式碳 酸铜[Cu2(OH)2CO3]。
口诀
钾、钠、硝酸、铵盐溶 盐酸盐不溶氯化银 硫酸盐不溶硫酸钡 碳酸盐只溶钾、钠、铵 钾、钠、钙、钡的碱能溶 常见五酸都易溶 另外:AgCl、BaSO4不仅不溶于水,
而且还不溶于稀硝酸
2、了解食盐、纯碱、小苏打、碳酸钙等 在日常生活中的用途;
常见 盐
食盐
碳酸钙
纯碱 小打 硫酸铜 苏
盐、化肥复习PPT课件

③ HCl + K2CO3—— ④KNO3 + NaOH—— X
2、找出哪些离子不共存
①SO42-. ②Cl-. ③H+
④Cu2+. ⑤Ag+
⑥ Ba2+. ⑦.CO32-. ⑧Fe3+ ⑨OH-
①⑥ ⑥⑦ ②⑤ ③⑨ ④⑨ ⑧⑨
③⑦
3、为鉴别碳酸氢铵、氯化铵和尿素三种化肥,分别取三种样品编号为A、 B、C,并进行下列实验
分 特点 成分交换、化合价不变
解 反
反应物条件 有酸酸必溶,无酸两相溶
应 条件 生成物条件 生成物必须有气体或沉淀或水
应用 ①判断复分解反应能否进行 ②判断离子是否共存
氮肥:白色晶体,易溶于水,与熟石灰研磨有氨味
种 类 化 肥
钾肥:白色晶体,易溶于水。 磷肥 :灰色粉状,难溶于水。 复合肥:KNO3
防止滤纸破损
加快过滤速率和防止液滴飞溅
① 溶解中玻璃棒的作用:
搅拌,加快溶解的速度。
玻 璃 棒 的 ② 过滤中玻璃棒的作用 : 作 用玻璃棒引流。 用
③ 蒸发中玻璃棒的作用 :
搅拌滤液,以防液滴飞溅。
归纳总结
盐的组成 氯化钠 :———粗盐提纯
碳酸钠: 常见的盐 碳酸氢钠: CO32- 的检验方法
与盐反应:盐+盐=新盐+新盐
自学指导(2)
1、复习内容:阅读课本P75-76、的复分解反应 P79-84的化学肥料
2、复习方法:快速阅读,独立思考
3、复习时间:10分钟
4、复习要求:复习后,完成下列检测题
复习检测(2)
1、判断下列复分解反应能否发生,能反应的写出反应方程式
①H2SO4 + NaNO3—X— ② Na2SO4 + BaCl2——
生活中常见的盐及化学肥料PPT课件 人教版

CO2的密度比空气大, 便于植物叶面吸收 。 ②将塑料桶悬挂在高处的原因:
2NH4HCO3+H2SO4=(NH4)2SO4+2H2O+2CO2↑
③反应后生成的硫酸铵在农村还可用作 化肥 。
6、小明学习化学后,在家里想 用化学方法来鉴别碱面(主要成分 是碳酸钠)和食盐,你认为下列方法 可行的是 A、观察它们的颜色 B、分别倒入水中观察是否溶解 C、取少量分别倒入食醋 D、分别闻它们的气味 答案:( C )
4、氮肥能促使作物的茎叶生长茂盛,叶色 浓绿。某同学发现她家花盆中的花草生长 迟缓,便施用了一种氮肥。 下图为该氮肥包装袋上的部分文字说明。 试根据相关信息计算: 4 种元素 ⑴碳酸氢铵组成中有____ ⑵碳酸氢铵的相对分 碳酸氢铵 子质量为_____ 79 (NH4HCO3) ⑶这种氮肥的纯度 净重:50kg 是94.8% ______ 含氮量:16.8%
×××化学工业公司
5、⑴某学生家乡出现水稻倒伏现象,他通过 调查研究,发现主要原因是缺少 钾 肥,建议 4 农民适量施用草木灰或 KCl或K2SO (填化学式) ⑵大棚种植蔬菜在冬季需补充二氧化碳。某同学 在自家大棚内设计了补充二氧化碳的方法:将工 业废硫酸用水稀释后,盛放在塑料桶内,悬挂在 高处。每天向桶内加适量的碳酸氢铵,它和硫酸 反应生成硫酸铵、二氧化碳和水。 ①写出该反应的化学方程式:
第十一单元
盐
化肥
生活中常见的盐及化学肥料
1、了解食盐、纯碱、小苏打、碳酸钙 等盐在日常生活中的用途 2、知道一些化肥的名称和作用
氯化钠:俗称 食盐 碳酸钠:俗称 纯碱、苏打 面碱、口碱 碳酸氢钠:俗称 小苏打 碳酸钙:主要以大理石和 石灰石的形式存 在于自然界中
化肥的种类:
2NH4HCO3+H2SO4=(NH4)2SO4+2H2O+2CO2↑
③反应后生成的硫酸铵在农村还可用作 化肥 。
6、小明学习化学后,在家里想 用化学方法来鉴别碱面(主要成分 是碳酸钠)和食盐,你认为下列方法 可行的是 A、观察它们的颜色 B、分别倒入水中观察是否溶解 C、取少量分别倒入食醋 D、分别闻它们的气味 答案:( C )
4、氮肥能促使作物的茎叶生长茂盛,叶色 浓绿。某同学发现她家花盆中的花草生长 迟缓,便施用了一种氮肥。 下图为该氮肥包装袋上的部分文字说明。 试根据相关信息计算: 4 种元素 ⑴碳酸氢铵组成中有____ ⑵碳酸氢铵的相对分 碳酸氢铵 子质量为_____ 79 (NH4HCO3) ⑶这种氮肥的纯度 净重:50kg 是94.8% ______ 含氮量:16.8%
×××化学工业公司
5、⑴某学生家乡出现水稻倒伏现象,他通过 调查研究,发现主要原因是缺少 钾 肥,建议 4 农民适量施用草木灰或 KCl或K2SO (填化学式) ⑵大棚种植蔬菜在冬季需补充二氧化碳。某同学 在自家大棚内设计了补充二氧化碳的方法:将工 业废硫酸用水稀释后,盛放在塑料桶内,悬挂在 高处。每天向桶内加适量的碳酸氢铵,它和硫酸 反应生成硫酸铵、二氧化碳和水。 ①写出该反应的化学方程式:
第十一单元
盐
化肥
生活中常见的盐及化学肥料
1、了解食盐、纯碱、小苏打、碳酸钙 等盐在日常生活中的用途 2、知道一些化肥的名称和作用
氯化钠:俗称 食盐 碳酸钠:俗称 纯碱、苏打 面碱、口碱 碳酸氢钠:俗称 小苏打 碳酸钙:主要以大理石和 石灰石的形式存 在于自然界中
化肥的种类:
常见的盐和化肥PPT课件讲义

碳酸氢铵 碳碳铵铵
17.7%
硝酸铵 硫酸铵 氯化铵 硝 硝铵 铵 肥 肥田 田粉 粉
35% 21.2% 26.2%
讨论:
• 为什么铵态氮肥不能与熟石灰、草木灰等 碱性物质混合使用?
• 怎样在实验室用简单方法检验铵盐?
铵根的检验:
1、把少量待测物和熟石灰粉末放在一起研磨, 若产生刺激性臭味的气体,则有铵根存在。 2、把少量待测溶液和氢氧化钠溶液混合加热, 若产生能使湿润的红色石蕊试纸变蓝的气体, 则有铵根存在。
或用玻璃棒沾浓氨水置于试管口(有大量的白烟) 干燥:碱石灰
不能用无水CaCl2、P2O5、浓硫酸干燥。
课外拓展:
2、有机氮肥——尿素:CO(NH2 )2 白色晶体
含氮量高,肥效持久,对土壤没有不良影响, 是一种优质氮肥。
3、氮肥、磷肥、钾肥的区别
氮肥
钾肥
看外观
白色晶体
加水
全部溶于水
加熟石灰 放出有刺激性气 无刺激
2)装置 固+固加热型(同O2)
3)收集:向下排空气法 4) 检验:湿润的红色石蕊试纸 (变蓝)或用玻璃棒沾浓氨水置于试管口(有量的白烟) 5) 干燥:碱石灰
不能用无水CaCl2、P2O5、浓硫酸干燥。
注意:消石灰不能用KOH、NaOH代替
• 问题想1:一如想何鉴: 别下列4种物质
NH4NO3、Na2SO4、 (NH4)2SO4、NaNO3
农家肥料
常含多种营养元素, 营养元素含量较小。
一般易溶于水, 易于被作物吸收,
肥效较快。
便于工业生产,成本较高。
有些品种化肥如长期 大量施用能使土壤板结。
一般较难溶于水,经腐熟 后逐步转化为可溶于水、 能被作物吸收的物质,肥
常见的盐和化肥ppt课件

1、俗称:食盐 (生活中的盐与化学中的盐) 2、存在:海水、盐湖、井盐、盐矿;
3、制取:晾晒海水,煮井盐水、盐湖水,开 采盐矿;
4、用途:调味、腌渍食品、生理盐水、化工 原料(制取碳酸钠、氢氧化钠、和盐酸等)
选种、化雪盐。
NaCl + NH3 + CO2 +H2O = NaHCO3↓+ NH4Cl
通电
玻璃棒 的作用
搅拌、引流、搅拌
加速溶解
防止受热不均匀使 液体溅出
烧 伤 病 人 的 治疗通 常是取 烧伤病 人的健 康皮肤 进行自 体移植 ,但对 于大面 积烧伤 病人来 讲,健 康皮肤 很有限 ,请同 学们想 一想如 何来治 疗该病 人
过滤后滤液仍浑浊的原因:
⑴过滤时滤纸破损。 ⑵倾倒液体时,液面超过滤纸边缘。 ⑶仪器不干净
的气体
不燃烧, 跳动或有
爆炸声
无明显变 化
磷肥
灰白色粉末 大多不溶或部
分溶于水 无明显变化
无明显变化
使湿润的红色石蕊试纸变蓝
烧 伤 病 人 的 治疗通 常是取 烧伤病 人的健 康皮肤 进行自 体移植 ,但对 于大面 积烧伤来治 疗该病 人
三、其它常见的盐
1、硫酸铜(CuSO4) 白色固体,溶于水得到蓝色溶液,无水硫酸铜 在实验中常用来检验水的存在。
CuSO4·5H2O 俗名:胆矾、蓝矾 CuSO4 +2NaOH = Cu(OH)2↓ + Na2SO4
CuSO4 + BaCl2 = CuCl2 + BaSO4↓
用途:有毒,农业上与熟石灰配制波尔多液杀 虫剂,游泳池常用其做消毒剂,精炼铜 的原料。
按金属元素分类:钠盐、钾盐、亚铁盐
按酸根分类:碳酸盐、盐酸盐、硫酸盐
3、制取:晾晒海水,煮井盐水、盐湖水,开 采盐矿;
4、用途:调味、腌渍食品、生理盐水、化工 原料(制取碳酸钠、氢氧化钠、和盐酸等)
选种、化雪盐。
NaCl + NH3 + CO2 +H2O = NaHCO3↓+ NH4Cl
通电
玻璃棒 的作用
搅拌、引流、搅拌
加速溶解
防止受热不均匀使 液体溅出
烧 伤 病 人 的 治疗通 常是取 烧伤病 人的健 康皮肤 进行自 体移植 ,但对 于大面 积烧伤 病人来 讲,健 康皮肤 很有限 ,请同 学们想 一想如 何来治 疗该病 人
过滤后滤液仍浑浊的原因:
⑴过滤时滤纸破损。 ⑵倾倒液体时,液面超过滤纸边缘。 ⑶仪器不干净
的气体
不燃烧, 跳动或有
爆炸声
无明显变 化
磷肥
灰白色粉末 大多不溶或部
分溶于水 无明显变化
无明显变化
使湿润的红色石蕊试纸变蓝
烧 伤 病 人 的 治疗通 常是取 烧伤病 人的健 康皮肤 进行自 体移植 ,但对 于大面 积烧伤来治 疗该病 人
三、其它常见的盐
1、硫酸铜(CuSO4) 白色固体,溶于水得到蓝色溶液,无水硫酸铜 在实验中常用来检验水的存在。
CuSO4·5H2O 俗名:胆矾、蓝矾 CuSO4 +2NaOH = Cu(OH)2↓ + Na2SO4
CuSO4 + BaCl2 = CuCl2 + BaSO4↓
用途:有毒,农业上与熟石灰配制波尔多液杀 虫剂,游泳池常用其做消毒剂,精炼铜 的原料。
按金属元素分类:钠盐、钾盐、亚铁盐
按酸根分类:碳酸盐、盐酸盐、硫酸盐
中考化学:第9课《常见的盐和化肥》ppt复习课件

盐的化学性质
写化学方程式
(1)盐与金属反应 Fe+CuSO4==Cu+FeSO4 反应条件: 必须是活 Cu+2AgNO3 泼金属与不活泼金属的 盐溶液反应(K、CaC、u(NO3=)=2__+__2_A_g_________ Na等除外)
考盐点的化梳学性理质
写化学方程式
(2)盐与酸反应
CaCO3+2HCl==CaCl2+H2O+CO2↑
边,则表示( D )
A.右盘重,砝码轻
B.右盘轻,样品重
C.左盘重,样品轻
D.左盘轻,砝码重
中考预测
(2)第②步实验过程中用到的玻璃仪器有
,
Hale Waihona Puke ; 烧杯玻璃棒(3)第③步实验操作的目的是除去样品中的
;发生N反a应2S的O化4 学方程式是 ; Na2SO4 + BaCl2 = BaSO4↓ + 2NaCl
(4)第④步操作发生反应的化学方程式是
。 2NaOH + MgCl2 = Mg(OH)2↓ + 2NaCl
中考预测
(5)第⑤步实验操作的目的是除去BaCl2 和 CaCl2 ;反
应的化学方程式是 Na2CO3+BaCl2 =BaCO3↓+2Na;Cl
Na2CO3+CaCl2=CaCO3↓ + 2NaCl
反应条件: 生成物中有
沉淀或气体或水等2生N成aCl
N=+=a_2HC_2O_O3_+_+2_H_CC_lO_2_↑_________
(3)盐与碱反应
Na2CO3+Ca(OH)2
反应条件: 反应物都可 ==CaCO3↓+2NaOH
《化学肥料》常见的酸、碱、盐PPT课件(第1课时)

对比化学肥料和农家肥料的一些特点
化学肥料
农家肥料
所含营养元素种类少,但营养 元素的含量大
一般易溶于水,易于被作物吸 收,肥效较快
常含多种营养元素,营养元素含 量较少
一般较难溶于水,经腐熟后逐步 转化为可溶于水、能被作物吸收 的物质,肥效较慢但较长
便于工业生产,成本较高
便于就地取材,成本低廉
有些品种化肥如长期大量施用 能使土壤板结
能改良土壤结构
1.氮肥
常见氮肥
性状
[CO尿(N素H2)2]白色或淡黄色晶体,易溶于水
含氮量
主要作用
缺乏时的 症状
不超过 46.67%
(碳NH酸4H氢C铵O3)又会受称潮碳,铵易,分白解色晶体,易溶于水,低于17%
氮肥有促 植物缺少 进植物茎、氮元素,
叶生长茂 表现为植
硝酸铵 (NH4NO3)
又高温称或硝受铵猛,烈白撞色击晶时体易,爆易炸溶于水,低于35%
Fe
C u
Z n
S
Mg
N a
B
M o
M n
其中C、O、H元素从空气和水中摄取。
农作物最需要补 充的是N、P、K
植物生长需要养分,土壤所能提供的养分是有限的,因此要 靠施肥来补充。施肥是使农业增产的重要手段。
庄稼一枝花, 全靠肥当家
常用化肥
肥料 简单 分类
肥料
氮肥
化学肥料
磷肥 钾肥 复合肥料
农家肥料:人畜粪便、植物体等 沤制的天然有机肥料等。
溶于水,易结 病虫害和抗倒伏 尖端发黄,并
块
等功能
逐渐枯萎
植物缺钾时的表现
茎秆软弱,易倒伏
叶尖及叶缘呈黄色, 甚至焦枯
3.复合肥
《生活中常见的盐》盐化肥PPT课件

酸
白色固体溶解,放出使澄清石灰
现 象 水变浑浊的无色气体
碳酸钠(或碳酸氢钠)与盐酸
分 析 反应生成了CO2气体
【练习】请同学们写出上述有关化学方程式。
Na2CO3+2HCl=2NaCl+H2CO3 CO2↑+H2O
NaHCO3+HCl=NaCl+H2CO3 CO2↑+H2O
Na2CO3+2HCl=2NaCl+CO2↑+H2O NaHCO3+HCl=NaCl+CO2↑+H2O
×
(2)K2CO3+CaCl2 K2CO3+CaCl2=CaCO3↓+2KCl
(3)Cu+HCl
×
(4)Na2SO4+BaCl2 Na2SO4+BaCl2=BaSO4↓+2NaCl
(5)BaSO4+Na2CO3
×
(6)Ba(OH)2+CuCl2 Ba(OH)2+CuCl2=Cu(OH)2↓+BaCl2
碱:最后两个字母是OH(氢氧化某)
盐:其他的为盐(某酸某,某化某) 指出下列物质中那些是酸?那些是碱?那些是盐?
NaHCO3 KOH HNO3 K2CO3 NaNO3 H2 CO3 Mg(OH)2 酸:HNO3 、H2CO3 碱:KOH 、 Mg(OH)2
盐:NaHCO3 、 K2CO3 、NaNO3
(3)能与某些盐反应 Na2CO3+ CaCl2==CaCO3 ↓+ 2NaCl
【讨论】1.酸和碱作用生成盐和水的反 应是否也属于复分解反应?为什么?
2.分析、归纳上述几个酸、碱、盐之间 的复分解反应,它们的生成物有什么特 点?
二、复分解反应
两种化合物互相交换成分,生成另外两 种化合物的反应
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
A.甲:熟石灰
乙:稀盐酸
B.甲:水
乙:氢氧化钠溶液
C.甲:氢氧化钠溶液 乙:水
D.甲:稀盐酸
乙:氯化钠溶液
第14讲 常见的盐和化肥
重难点突破
【思路点拔】 根据NH4HCO3、NH4Cl、KCl三种物质的 性质分析。根据图示:NH4HCO3、NH4Cl、KCl三种物 质加入试剂甲后,NH4HCO3、NH4Cl放出氨气,根据铵 盐遇碱会放出氨气的性质,可判断甲是一种碱; NH4HCO3、NH4Cl加入试剂乙,NH4HCO3产生气泡说明加 入的是一种酸,利用这些知识解决。
茎秆软ห้องสมุดไป่ตู้, 容易倒伏
第14讲 常见的盐和化肥
知识梳理
2.化学肥料的简易鉴别
项目 看外
观
氮肥
钾肥
白色晶体
加水
全部溶于水
加熟 石灰
产生具有刺 激性气味的 氨气(尿素除 外)
不产生具有 刺激性气味 的氨气
磷肥 灰白色粉未 大多不溶于水 或部分溶于水
——
第14讲 常见的盐和化肥
3.氮肥的简易鉴别
知识梳理
解反应的条件,铵盐与碱反应有氨气生成)
如:NH4NO3+NaOH __N_H_4_N__O_3_+__N_a__O_H_______N_H__3_↑_+__H_2_O_+__N__a_N_O__3____。
4.盐1+盐2→新盐1+新盐2(反应物需都可溶且满足
复分解反应的条件)
如:Na2CO3+CaCl2 __C_a_C__l2_+__N_a_2_C__O_3______C__a_C_O__3_↓_+__2_N_a_C__l ________。
溶液的pH>7,显 碱性。碳酸钠中 因含CO,易发生 复分解反应。
业上
第14讲 常见的盐和化肥
知识梳理
物质 化学式、俗名
用途
碳酸 氢钠
N__a_H_小C_O_苏_3,打__俗__名_
焙制糕点、治疗 胃酸过多等
备注
患有胃溃疡患者, 不能服用含有碳酸 氢钠的胃药。
实验室中常用石
灰石(或大理石)和
碳酸 钙
2.盐+酸 →新盐+新酸(满足复分解反应的条件)
如:Na2CO3+2HCl __N__a_2_C_O__3_+__2_H_C__l _____2_N__a_C_l_+__H_2_O_+__C__O_2_↑________。
第14讲 常见的盐和化肥
知识梳理
3.盐+碱→新盐+新碱(反应物需都可溶且满足复分
离子符号); (2)B中反应的现象是__有__气__泡__产__生_____;
(3)写出C反应的化学方程式 __3_N_a_O__H_+__F__e_C_l_3______F_e_(_O_H__)_3↓_+__3_N__a_C_l________;
(4)D中反应能发生反应的原因是 __交__换__成__分__有__沉__淀__生__成____。
第三分部
身边的化学物质 第14讲 常见的盐和化肥
第14讲 常见的盐和化肥
第14讲 常见的盐和化肥
1 …考…情…分…析….. 2 …知…识…梳…理….. 3 …重…难…点…突…破.. 4 …中…考…特…训…..
第14讲 常见的盐和化肥
考情分析
直击 重点
1.食盐、纯碱、小苏打、碳酸钙等盐在日常生活中的 用途(认识) 2.一些常用化肥的名称和作用(知道)
第14讲 常见的盐和化肥
重难点突破
①HCl和Na2CO3反应时其实是分步进行的,即: Na2CO3+HCl===NaCl+NaHCO3(先),NaHCO3+ HCl===NaCl+H2O+CO2↑(后)。 ②NaHCO3溶液与足量澄清石灰水混合会变浑浊。 ③Ca(HCO3)2溶于水 请回答: (1)NaHCO3俗称_小__苏__打_____; (2)NaHCO3在医疗上是治疗__胃__酸__过__多__的药剂之一。
第14讲 常见的盐和化肥
重难点突破
【思路点拔】 (1)根据溶液的酸碱度与溶液的酸碱 性、碳酸氢钠的用途分析回答; (2)①根据装置的特点分析在实验结束时操作上要 注意的问题;②根据实验的现象分析、比较碳酸钠 和碳酸氢钠的热稳定性。
第14讲 常见的盐和化肥
重难点突破
3.(2018·贵港) 某化学兴趣小组同学学习海水“制 碱”知识后,到实验室做实验,小华实验:先取2 mL Na2CO3溶液于试管中,再用胶头滴管滴入少量稀盐酸, 无明显现象;小红实验:先取2 mL稀盐酸于试管中, 再用胶头滴管滴入少量Na2CO3溶液,却马上观察到有气 泡产生,两人实验所用的Na2CO3溶液、稀盐酸均相同, 却观察到不同的实验现象,他们为了查明原因,查阅 资料:
第14讲 常见的盐和化肥
知识梳理
高频方程式小练:
1.稀盐酸与硝酸银反应: __A__g_N_O_3+__H__C_l______A_g_C__l↓_+__H__N_O__3________________
2.氯化钡溶液与硫酸钠溶液反应: __B_a_C_l_2+__N__a_2_S_O__4 ______B_a_S_O__4_↓_+__2_N_a_C__l___________
一、几种常见的盐
物质 氯化 钠
碳酸 钠
化学式、俗名
用途
备注
生活的盐指NaCl
做调味剂和防腐 (食盐),若将工业
NaCl
剂;配制生理盐 用盐如NaNO2(亚 水;重要的化工 硝酸钠)当做食盐
原料
食用,会造成中
毒。
制烧碱;泡沫灭
_N_a_2_C纯_O_碱3_,__俗__名_
火器中制取二氧 化碳;重要的化 工产品,广泛应 用于玻璃、造纸、 纺织、洗涤等工
知识梳理
1.复合肥料:含N、P、K元素中的两种或三种的肥 料。 2.草木灰的主要成分为K2CO3,水溶液呈碱性。 3.铵态氮肥(如硫酸铵、氯化铵等)能否与碱性肥 料(如草木灰)混合使用? __铵__态__氮__肥__能__与__碱__性__肥__料__发__生__反__应__,__产__生__氨__气__,__降__ __低__肥__效______________________。
第14讲 常见的盐和化肥
知识梳理
三、化学肥料 1.化学肥料的作用
化学肥料 氮肥
作用
促进植物茎 和叶生长茂 盛、叶色浓
绿(促苗)
缺少出现 症状
叶片发黄
磷肥
钾肥
促进根系发 促使作物生
达,穗粒增 长健壮、茎
多、饱满, 叶粗硬、增
增强作物抗 强作物抗病
寒、抗旱能 虫害、抗倒
力(催果) 伏能力(壮秆)
籽粒不饱满
【查阅资料】
20 ℃ 8% Na2CO3溶液 8% NaHCO3溶液
pH
10.6
8.0
现有20℃时溶质质量分数为8%的Na2CO3和 NaHCO3溶液, 由数据可知两种溶液都显___碱__性_____(选填“酸性”、
“碱性”或“中性”);这两种物质中常用作治疗胃酸 过多的药剂是____N__a_H_C__O_3___。
第14讲 常见的盐和化肥
重难点突破
【提出问题】 小华实验后溶液中的溶质是什么? 【猜想与假设】 猜想①NaCl;②NaCl、NaHCO3;③ NaCl、Na2CO3;④NaCl、Na2CO3、NaHCO3 【提出质疑】 小红认为猜想____③_____一定不正确。 【实验探究】
实验操作
实验现象 结论
CaCO3,石灰 稀盐酸来制取 石或大理石的主 CO2。工业上煅
要成分 烧石灰石来获得
不溶于水,珍珠、 贝壳的主要成分, 常用的补钙剂。
生石灰,是重要
的建筑材料
第14讲 常见的盐和化肥
知识梳理
二、 盐的化学性质
1.盐+金属→新盐+新金属(“前金”换“后金”,盐
可溶,钾钙钠除外)
如:Fe+CuSO4 _F__e_+__C_u_S__O_4______F_e_S__O_4_+__C_u____________________。
第14讲 常见的盐和化肥
重难点突破
(2)碳酸钠溶液与过量稀盐酸混合后的化学反应方程 式为_N_a_2_C_O_3_+__2_H_C_l_____2_N_a_C_l_+__H_2_O_+__C_O_2_↑__,实际参 加反应的微粒是__碳__酸__根__离__子__和__氢__离__子_______。
3.熟石灰与纯碱反应制取氢氧化钠: __C_a_(_O_H_)_2+__N__a_2_C_O__3_____C__a_C_O__3_↓_+__2_N_a_O__H_________
4.湿法炼铜的反应: __F_e_+__C_u_S__O_4______F__e_S_O__4+__C__u___________________
第14讲 常见的盐和化肥
重难点突破
一、盐的性质
(2019·陕西模拟) 如图是李龙同学实验某些盐
的化学性质的四个实验,分析后请回答问题:
编号
A
反应物类别 盐和金属
B 盐和酸
C 盐和碱
D 盐和盐
实验内容
第14讲 常见的盐和化肥
重难点突破
(1)A中反应后溶液中的阳离子一定有____F_e_2+____ (填
第14讲 常见的盐和化肥
重难点突破
1.物质由微粒构成。化学反应过程 中某些微粒会发生改变,而有些微 粒则不会发生改变。 (1)以下是氢氧化钠和盐酸的反应的微观 示意图,发生的化学反应方程式为 __H_C_l_+__N__a_O_H_______N__a_C_l_+__H_2_O_____,从微观示意图可知,该 反应中发生变化的微粒是_氢__离__子__和__氢__氧__根__离__子___,它们是该反 应的“参与者”;未发生变化的微粒是_钠__离__子__和__氯__离__子___,它 们是该反应的“旁观者”。
