材料科学基础:二元相图
合集下载
材料科学基础---二元相图

微分整理,得: 微分整理,
dG = −SdT +VdP + ∑µidni
µi =
∂G ∂ni T,P,r
(代表体系内物质传输的驱动力; 代表体系内物质传输的驱动力; 等温、 等温、等压及其它组元数量不变 的情况下,每增加单位摩尔i 的情况下,每增加单位摩尔 组 体系自由能的变化) 元,体系自由能的变化)
组织结构 相图 加工处理 特性 性能
相图热力学的基本要点
— 相平衡条件
设有一多元系,含组元 为 摩尔,组元2为 摩尔, 设有一多元系,含组元1为n1 摩尔,组元 为n2 摩尔 ……,则体系 , 吉布斯自由能 :
G = G(T, P, n1, n2,...)
(温度T、压力 、各组元物质量 i 的函数) 温度 、压力P、各组元物质量n 的函数)
相图提供的信息
某一成分的合金, 一定温度下 所处的状态、 某一成分的合金,在一定温度下,所处的状态、相组成 状态 合金在冷却过程中 发生了哪些反应或转变, 合金在冷却过程中,发生了哪些反应或转变,以及其开始与终了温度 冷却过程 一定成分的合金,在室温下具有什么样的平衡组织, 一定成分的合金,在室温下具有什么样的平衡组织,可以根据组织与 平衡组织 性能的关系,预测材料的性能 性能的关系,预测材料的性能 相图与材料的加工工艺性能 如流动性) 相图与材料的加工工艺性能(如流动性)存在一定的对应关系 新材料研发、材料加工过程中 过程中, 在新材料研发、材料加工过程中,都起着十分重要的作用
相图热力学的基本要点
— 吉布斯相律 Gibbs phase rule
相律:在平衡条件下,一个系统的组元数、相数、 相律:在平衡条件下,一个系统的组元数、相数、自由度数之
间的关系规律,相律的数学表达式: 间的关系规律,相律的数学表达式:
材料科学基础-6二元相图

2
Ω=0,>0,G-x曲线也有一最小值;
Ω>0, G-x曲线也有2个最小值,拐点内<0。
6.3.2 多相平衡的公切线原理
6.3.3 混合物的自由能和杠杆法则
6.3.4 从自由能—成分曲线推测相图
6.3.5 二元相图的几何规律
★相图中所有的相界线代表相变的温度和平衡相 成分,即平衡相成分沿着相界线随温度变化而变 化; ★两单相区之间必定有这两相的两相区-相区接 触法则; ★二元相图的三相平衡区为一水平线,其与三个 单相区的交点确定平衡相的浓度; ★两相区与单相区的分界线与三相等温线相交, 分界线的延长线进入另一两相区。
(1)单相区:3个, L、 α 、β (2)两相区: 3个, L+α 、L+β 、α +β 相区:1个, L+α+β (3)三
5.与匀晶和共晶相图的区别
(1)相同处
PDC线以上区域; PDC线以下、DF以右区域的
分析方法以及结晶过程与匀晶相同;
BPDF以内区域,与共晶线MEN线以下区域相同,
按照固ห้องสมุดไป่ตู้度线分析。 (2)不同处 包晶线PDC及包晶反应:L+α→β
6.10 铁碳合金相图 6.11 二元合金的凝固理论
第6章 二元合金相图及合金凝固
由一种元素或化合物构成的晶体称为单组元晶体或纯晶体,
该体系称为单元系。两个组元的为二元系,n个组元都是独立
的体系称为n元系。对于纯晶体材料而言,随着温度和压力的 变化,材料的组成相会发生变化。
从一种相到另一种相的转变称为相变。由不同固相之间的
2.非平衡共晶组织
a
非平衡共晶组织(成分位于a点稍左)一般分布在初晶α 的相界上,或者在枝晶间。可以通过扩散退火来消除,最终得
材料科学基础-8-二元相图(2)
第二节 二元相图
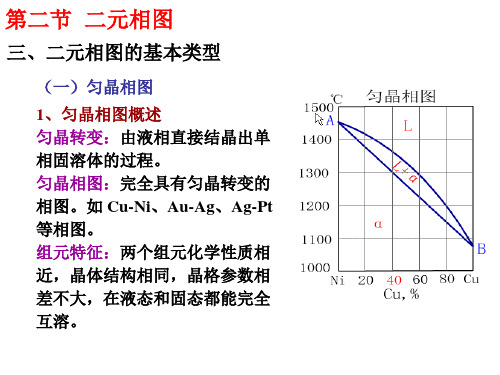
(一)匀晶相图
2、固溶体的平衡凝固
(3)固溶体的结晶规律
c.固溶体的凝固过程与纯金
属一样,也包括形核与长大
两个阶段
e. 平衡凝固得到的固溶体显
微组织和纯金属相同,除了
晶界外,晶粒之间和晶粒内
部的成分却是相同的。
d.合金结晶形核时需要能量
起伏和成分起伏
a. 固溶体的结晶与纯金属不同,它不在
(2)压力加工性:压力加工合金通常是相图上单相固溶体
成分范围内的单相合金或含有少量第二相的合金。
——单相固溶体合金切削加工性能
不够好,而具有两相组织的合金切
削加工性一般比较好。
(4)热处理性:
相图上无固态相变或固溶度变化的
合金不能进行热处理。
孔等缺陷。
——我国20世纪60年代开始研制Pt-Ag合金,但至今无法批量
稳定发展
——国内外通过添加Pd(钯)制成Pt-Pd-Ag三元合金,虽综合
性能不如Pt-Ag合金,但加工性能得以改善。
第二节 二元相图
(三)包晶相图
2、包晶合金的凝固及其平衡组织
(1)ω (Ag)为42.4%的Pt-Ag合金(合金I)
′
% =
× %
第二节 二元相图
1186℃
A
LP+αC ↔ βD
(三)包晶相图
f=2-3+1=0
包晶点
• 1、包晶相图
• 包晶转变:由一个固相与
液相作用生成另一个固相
的过程。
• 包晶相图:两组元在液态
无限互溶,固态下有限互
溶,并发生包晶反应的二
元系相图。
第二节 二元相图
2、包晶合金的凝固及其平衡组织
材料科学基础4 二元相图PPT课件

由于结晶成树枝状晶---枝晶偏析。 液、固相线距离越大,则偏析越 严重。 冷速越快,偏析越严重。
第四章:二元相图
4.2.1匀晶相图 3.固溶体合金的非平衡结晶及组织。 (1)晶内偏析: ②枝晶偏析对性能影响
力学性能降低,尤其是塑性、韧性↓↓ 耐蚀性 ↓ 压力加工性↓ ③消除枝晶偏析方法。
高温扩散退火(均匀化退火):
将铸件加热至固相线下100--200℃长期保温, 使溶质、溶剂原子相互扩散。
第四章:二元相图 3.固溶体合金的非平衡结晶及组织。 (2)区域偏析
实际铸件表面与心部化学成分不均匀现象→宏 观偏析。 以K 0 <1为例 (图示) 先结晶溶质含量低(表面),后结晶溶质含量 高(心部)。
Ko <1
第四章:二元相图 3.固溶体合金的非平衡结晶及组织。 (3)区域提纯
第四章:二元相图 复习合金、组元、相、相结构(固溶体、化物)
纯金属结晶→单相。
相图: 以温度为纵坐标,成分为横坐标,反映不同成分
的合金在任意温度下所处的平衡相状态的图解。 相图→状态图,平衡状态图 。
第四章:二元相图 平衡:
合金从液态(高温)到室温是在极其缓慢的条 件下完成的。 相图用途:
①帮助认识相的变化规律 ②计算任意合金在不同温度下相和组织含量。 ③ 帮助制定热加工工艺:
第四章:二元相图 4.1.3相律及杠杆定律 2.杠杆定律: 问题提出:
①当二元合金(成分已知)由两相组成时两相的 相对重量是多少?
例:45钢(含C=0.45%),铁素体(F)和Fe3C 两相各占多少?
②当二元合金两相相对重量已知时,合金成分是 多少?
例:金相观察:F:95%; Fe3C:5%;求钢的含 碳量?
液相平衡成分为L2点,α相平衡成分为α2 点。
第四章:二元相图
4.2.1匀晶相图 3.固溶体合金的非平衡结晶及组织。 (1)晶内偏析: ②枝晶偏析对性能影响
力学性能降低,尤其是塑性、韧性↓↓ 耐蚀性 ↓ 压力加工性↓ ③消除枝晶偏析方法。
高温扩散退火(均匀化退火):
将铸件加热至固相线下100--200℃长期保温, 使溶质、溶剂原子相互扩散。
第四章:二元相图 3.固溶体合金的非平衡结晶及组织。 (2)区域偏析
实际铸件表面与心部化学成分不均匀现象→宏 观偏析。 以K 0 <1为例 (图示) 先结晶溶质含量低(表面),后结晶溶质含量 高(心部)。
Ko <1
第四章:二元相图 3.固溶体合金的非平衡结晶及组织。 (3)区域提纯
第四章:二元相图 复习合金、组元、相、相结构(固溶体、化物)
纯金属结晶→单相。
相图: 以温度为纵坐标,成分为横坐标,反映不同成分
的合金在任意温度下所处的平衡相状态的图解。 相图→状态图,平衡状态图 。
第四章:二元相图 平衡:
合金从液态(高温)到室温是在极其缓慢的条 件下完成的。 相图用途:
①帮助认识相的变化规律 ②计算任意合金在不同温度下相和组织含量。 ③ 帮助制定热加工工艺:
第四章:二元相图 4.1.3相律及杠杆定律 2.杠杆定律: 问题提出:
①当二元合金(成分已知)由两相组成时两相的 相对重量是多少?
例:45钢(含C=0.45%),铁素体(F)和Fe3C 两相各占多少?
②当二元合金两相相对重量已知时,合金成分是 多少?
例:金相观察:F:95%; Fe3C:5%;求钢的含 碳量?
液相平衡成分为L2点,α相平衡成分为α2 点。
材料科学基础4-2二元相图及其类型

合金2 :
2016
液相线:
2020
组成
2017
凝固过程:
2021
后退
2018
合金1:
下页
01
04
02
03
如图所示
后退
下页
伪共晶 在非共晶成分处获得100%的共晶组织,只能在非平衡条件下得到。
不平衡凝固
后退 下页
不平衡共晶
m点以左,n点以右合金不平衡凝固时出现的共晶组织 。
01.
后退
02.
后退
下页
(2)共晶转变 在三相共存水平线men上,两条液相线汇交于e点。e点以上是液相区,e点下方是α+β两相共存区。这说明,相当于e点成分的液相,当冷至三相共存线men时会同时结晶出成分为m的α相与成分为n的β相。
三个单相区:
三个两相区:
后退
下页
共晶反应:
固相线:
2019
水的状态示意图
P
T
水
冰
气
其中f为系统的自由度数,C为组元数,P为自由度数等于组元数与相数之差再加上2。所谓自由度,即指独立可变的因
素,包括各组成相的成分、数量及温度、压力等。在金属及合金的制造和应用过程中,一般都是在常压下进行的,因此常把压力看成一个常数,相律的表达式可写成
相图基本知识
利用相图可以获取的信息 不同成分的材料在不同温度下存在哪些变化 各稳定相的相对量是多少 成分与温度变化时所可能发生的变化
第二节 二元相图及其类型
了解相图的分析和使用方法后,就可以了解合金的组织状态,进而预测合金的性能。另外,可以根据相图来制订合金的锻造和热处理工艺。
组元——组成材料最基本的、独立的物质。
2016
液相线:
2020
组成
2017
凝固过程:
2021
后退
2018
合金1:
下页
01
04
02
03
如图所示
后退
下页
伪共晶 在非共晶成分处获得100%的共晶组织,只能在非平衡条件下得到。
不平衡凝固
后退 下页
不平衡共晶
m点以左,n点以右合金不平衡凝固时出现的共晶组织 。
01.
后退
02.
后退
下页
(2)共晶转变 在三相共存水平线men上,两条液相线汇交于e点。e点以上是液相区,e点下方是α+β两相共存区。这说明,相当于e点成分的液相,当冷至三相共存线men时会同时结晶出成分为m的α相与成分为n的β相。
三个单相区:
三个两相区:
后退
下页
共晶反应:
固相线:
2019
水的状态示意图
P
T
水
冰
气
其中f为系统的自由度数,C为组元数,P为自由度数等于组元数与相数之差再加上2。所谓自由度,即指独立可变的因
素,包括各组成相的成分、数量及温度、压力等。在金属及合金的制造和应用过程中,一般都是在常压下进行的,因此常把压力看成一个常数,相律的表达式可写成
相图基本知识
利用相图可以获取的信息 不同成分的材料在不同温度下存在哪些变化 各稳定相的相对量是多少 成分与温度变化时所可能发生的变化
第二节 二元相图及其类型
了解相图的分析和使用方法后,就可以了解合金的组织状态,进而预测合金的性能。另外,可以根据相图来制订合金的锻造和热处理工艺。
组元——组成材料最基本的、独立的物质。
二元相图【材料科学基础】

相区: 液相区(L)、固相区 (α)、固液两相共存 区(L+α)。
13
¾ α相: Cu-Ni合金形成的置换固溶体。 ¾ 在两相区中: 9 f =C-P+1=2-2+1= 1,两个相的成分和温度
变量中只有一个可以独立变化,其中一个固定后, 另一个也随之固定。 9 例如,温度一定,在此温度下两个平衡相成分固 定,由该温度水平线与该两相区边界线相交的两点 决定(杠杆定律)。
33
• 共晶反应:在一定的温度下,由一定成分的液相同 时结晶出成分一定且不相同的两个固相的转变过 程,也称共晶转变。其反应式为:
共晶温度
• 发生共晶反应时,根据相律 f = C – P + 1 = 2-3+1=0,所以三个相的成分不能变化,温度也 不能变化,因此共晶线为水平线,三个相在此线上 有确定的成分点。
以Cu-40%Ni合金为例
16
t0
●
t1
●
t2
●
t3
●
● ●
●
●
17
平衡结晶过程
形核和核长大
¾ 形核:过冷、结构起伏、能量起伏、成分起伏(微 小区域内成分偏离平均成分的现象)。
¾ 长大:建立平衡 界面前沿液相中溶质原子扩散 破坏平衡 晶体长大 恢复平衡 重
新建立平衡。
18
19
20
结晶特点: ¾ 结晶在一个温度范围内进行,f =1,平衡结晶过
共晶区如此。 • 组成共晶体的两相均为金属
型液固界面,两个相的长大 速度与过冷度关系的差别不 大,伪共晶区对称地扩大。
53
9 (2)伪共晶区偏向一边扩大
• 两个组元熔点差别大,共晶点偏向低熔点组元,伪共晶 区偏向高熔点组元。
13
¾ α相: Cu-Ni合金形成的置换固溶体。 ¾ 在两相区中: 9 f =C-P+1=2-2+1= 1,两个相的成分和温度
变量中只有一个可以独立变化,其中一个固定后, 另一个也随之固定。 9 例如,温度一定,在此温度下两个平衡相成分固 定,由该温度水平线与该两相区边界线相交的两点 决定(杠杆定律)。
33
• 共晶反应:在一定的温度下,由一定成分的液相同 时结晶出成分一定且不相同的两个固相的转变过 程,也称共晶转变。其反应式为:
共晶温度
• 发生共晶反应时,根据相律 f = C – P + 1 = 2-3+1=0,所以三个相的成分不能变化,温度也 不能变化,因此共晶线为水平线,三个相在此线上 有确定的成分点。
以Cu-40%Ni合金为例
16
t0
●
t1
●
t2
●
t3
●
● ●
●
●
17
平衡结晶过程
形核和核长大
¾ 形核:过冷、结构起伏、能量起伏、成分起伏(微 小区域内成分偏离平均成分的现象)。
¾ 长大:建立平衡 界面前沿液相中溶质原子扩散 破坏平衡 晶体长大 恢复平衡 重
新建立平衡。
18
19
20
结晶特点: ¾ 结晶在一个温度范围内进行,f =1,平衡结晶过
共晶区如此。 • 组成共晶体的两相均为金属
型液固界面,两个相的长大 速度与过冷度关系的差别不 大,伪共晶区对称地扩大。
53
9 (2)伪共晶区偏向一边扩大
• 两个组元熔点差别大,共晶点偏向低熔点组元,伪共晶 区偏向高熔点组元。
材料科学基础-二元相图

LE→( αC + βD)
相图的构成:
LE→( αC + βD)
相图的构成:线
AE和BE为两液相线; AC和BD为两固相线; CG和DH:(固溶度曲线) 固溶体α、β的溶解度线; CED:水平共晶线。
三个单相区: L、α、β; 三个双相区:L+α、L+β、
α+β 一个三相区:L+α+β,
CED共晶线。 29
连接转变开始点 和终了点
冷却过程中,不同相的热容量不同,冷却曲线上的斜率 不同, 曲线的转折点对应温度就是相变温度。
相图的测定: 二元相图:4000个(81%)(4950); 三元相图:8000(5%)(161700)。工作量巨大。 四元相图:1000(0.1%)(3921225) 问题:成分难控制,高熔点,难以达到相平衡
室温组织:α+βII +(α+β)
(α+β)%=L%=c2/ce, (α+βII)%=e2/ce
α%=c’g/fg× e2/ce,
βII%=fc’/fg × e2/ce
41
相: α+β
α初 :暗黑色粗大树枝状, βII :白色颗粒。
(α+β)
亚共晶组织:
α+βII +(α+β)
④合金Ⅳ:过共晶合金 L→L+β→β+(α+β)→β+αII+ (α+β)
4. 偏晶转变相图 fdc Ld→αf +Lc
偏晶转变:
L36→Cu +L87
72
5、具有合晶转变的相图
Lc+Ld→f
6、熔晶转变相图
→ +L
♣ 6.3.5 二元相图的几何规律
相图的构成:
LE→( αC + βD)
相图的构成:线
AE和BE为两液相线; AC和BD为两固相线; CG和DH:(固溶度曲线) 固溶体α、β的溶解度线; CED:水平共晶线。
三个单相区: L、α、β; 三个双相区:L+α、L+β、
α+β 一个三相区:L+α+β,
CED共晶线。 29
连接转变开始点 和终了点
冷却过程中,不同相的热容量不同,冷却曲线上的斜率 不同, 曲线的转折点对应温度就是相变温度。
相图的测定: 二元相图:4000个(81%)(4950); 三元相图:8000(5%)(161700)。工作量巨大。 四元相图:1000(0.1%)(3921225) 问题:成分难控制,高熔点,难以达到相平衡
室温组织:α+βII +(α+β)
(α+β)%=L%=c2/ce, (α+βII)%=e2/ce
α%=c’g/fg× e2/ce,
βII%=fc’/fg × e2/ce
41
相: α+β
α初 :暗黑色粗大树枝状, βII :白色颗粒。
(α+β)
亚共晶组织:
α+βII +(α+β)
④合金Ⅳ:过共晶合金 L→L+β→β+(α+β)→β+αII+ (α+β)
4. 偏晶转变相图 fdc Ld→αf +Lc
偏晶转变:
L36→Cu +L87
72
5、具有合晶转变的相图
Lc+Ld→f
6、熔晶转变相图
→ +L
♣ 6.3.5 二元相图的几何规律
材料科学基础5-二元相图

第四节 二元包晶相图及合金凝固
2 平衡结晶过程及其组织
(2)成分在d-p之间合金的结晶
结晶过程:α剩余 ( 量的计算 ) ;
室温组织:α+β+αⅡ+βⅡ。
第四节 二元包晶相图及合金凝固
2 平衡结晶过程及其组织
第二节 二元匀晶相图
第二节 二元匀晶相图
第三节 二元共晶相图及合金凝固
共晶转变:由一定成分的液相同时结晶出两个一定 成分固相的转变。 共晶相图:具有共晶转变特征的相图(液态无限互 溶、固态有限互溶或完全不溶,且发生共晶反应)。 共晶组织:共晶转变产物。(是两相混合物)
第三节 二元共晶相图及合金凝固
第二节 二元匀晶相图
5 成分过冷及对生长形态的影响 (3)成分过冷形成的条件和影响 因素 条件:G/R<mC0(1-k0)/Dk0 合金固有参数: m( 液相线斜率 ), k0; 实 验 可 控 参 数 : G( 温 度 梯 度 ), R(凝固速度)。 (4)成分过冷对生长形态的影响 (正温度梯度下)G越小,成分 过冷 越大-生长形态:平面状 -胞状-树枝状。
2 合金的平衡结晶及其组 织(以Pb-Sn相图为例) (3)共晶合金 ① 凝固过程(冷却曲线、 相变、组织示意图)。 ② 共晶线上两相的相对 量计算。 ③ 室温组织 (α+β+αⅡ+βⅡ)及其 相对量计算。
第三节 二元共晶相图及合金凝固
2 合金的平衡结晶及其组 织(以Pb-Sn相图为例) (4)亚共晶合金 ① 凝固过程(冷却曲线、 相变、组织示意图)。 ② 共晶线上两相的相对 量计算。 ③ 室温组织 (α+βⅡ+α+β)及其相 对量计算。
b. 冷却速度非常慢→有扩散和对流→固相不混合、液 相完全混合。 c. 冷却速度很大→仅有扩散→固相不混合、液相完全 不混合。
材料科学基础I 5-3 二元匀晶相图

四、匀晶合金的非平衡结晶
匀晶合金在平衡条件下结晶,冷却速 度极其缓慢,先后结晶的固相虽然成分 不同,但是有足够的时间进行均匀化扩 散。所以,室温下的组织是均匀的固溶 体,在光学显微镜下观察,与纯金属十 分相似。
匀晶合金平衡组织示意图
但是,在实际生产中合金的冷却速度很快,远远达不到平衡 的条件。因此,固、液二相中的扩散来不及充分进行,先后结 晶出来的固相中较大的成分差别被保留下来。这种成分差别的 存在,还造成结晶时固相以树枝状形态生长。因此,这种成分 上的不均匀性被称为“树枝状偏析”或枝晶偏析。 采用均匀化热处理(Homogenizing heat treatment)可以消除枝 晶偏析。
为了计算简便,一般取合金总量Q =1。 因上述结果与物理学中的杠杆定律的表达式相似,所以这里 也称为杠杆定律。
三、典型合金冷却过程分析
各种成分的Cu-Ni合金都属于匀晶合金。下面以Cu-53%Ni合 金为例,分别对合金结晶过程中液、固二相的成分变化规律, 二相相对量的计算和微观组织的形成进行分析讨论。
§5-3 二元匀晶相图
二元匀晶(Isomorphous)相图是二元合金相图中图形最简单的
相图。 具有匀晶相图的二元合金系统有Cu-Ni, Fe-Cr, Ag-Au, Nb-Ti,
Cr-Mo, W-Mo等。
右图所示Cu-Ni相图是最常 见的二元匀晶相图,以此相图 为例进行讨论,其它匀晶相图 与此类似。
二元合金在平衡状态下两相共存,如结晶时,可以利用杠杆 定律(Lever rule)计算出某一温度下两相的相对量。 设合金的平均成分为x,合 金的总量为Q,在温度T1时液、 固两相平衡,液相的成分为xL、 质量为QL,固相的成分为xS、 质量为QS。则有:
Q QL QS Q x QL xL QS xS
材料科学基础_第5章_二元相图

不大时,它们不仅可以在液态或熔融状态完全互溶,而且 在固态也完全互溶,形成成分可变的连续固溶体,称为无 限固溶体或连续固溶体,它们形成的相图即为匀晶相图或 互溶相图。 ➢ 由液相结晶出单相固溶体的过程称为匀晶转变。液固态完 全互溶的体系不多,但是包含匀晶转变部分的相图却不少 ,几乎所有的二元系统都含有匀晶转变部分。
Cu
18 20
30 40
66 60 80
Ni 相对质量为1/4。溶体合金的平衡凝固及组织
➢ 平衡凝固是指凝固过程中每个阶段都能达到平衡,因此 平衡凝固是在极其缓慢的冷速下实现的。现以30%Ni和 70%Cu的铜镍合金为例来说明固溶体的平衡冷却过程及其 组织的。
11
冷却曲线 t Ⅱ
23
X2合金结晶过程分析
L
(共晶合金)
T,C
183
L
L+
L+
c
d
e
+
T,C
(+ )
围内凝固,具有变温凝固的特征 ②还需要成分起伏
15
5.3.2 二元共晶相图 两组元在液态无限互溶,固态有限溶解,通过共晶反
应形成两相机械混合物的二元合金称为二元共晶相图。共 晶反应是液相在冷却过程中同时结晶出两个结构不同的固
相的过程。 L
16
Ta,tb分别是Pb,Sn的熔点 M:锡在铅中的最大溶解度。N:铅在锡中的最大溶解度 E:为共晶点,具有该点成分的合金在恒温183℃发生共 晶转变LE→aM+ΒN,共晶转变是具有一定成分的液相在恒 温下同时转变为两个具有一定成分和结构的固相的过程。 F:室温时锡在铅中的溶解度;G:室温时铅在锡中的溶 解度
之间一定是由这两个相组成的两相区。如铁区(线)区(
Cu
18 20
30 40
66 60 80
Ni 相对质量为1/4。溶体合金的平衡凝固及组织
➢ 平衡凝固是指凝固过程中每个阶段都能达到平衡,因此 平衡凝固是在极其缓慢的冷速下实现的。现以30%Ni和 70%Cu的铜镍合金为例来说明固溶体的平衡冷却过程及其 组织的。
11
冷却曲线 t Ⅱ
23
X2合金结晶过程分析
L
(共晶合金)
T,C
183
L
L+
L+
c
d
e
+
T,C
(+ )
围内凝固,具有变温凝固的特征 ②还需要成分起伏
15
5.3.2 二元共晶相图 两组元在液态无限互溶,固态有限溶解,通过共晶反
应形成两相机械混合物的二元合金称为二元共晶相图。共 晶反应是液相在冷却过程中同时结晶出两个结构不同的固
相的过程。 L
16
Ta,tb分别是Pb,Sn的熔点 M:锡在铅中的最大溶解度。N:铅在锡中的最大溶解度 E:为共晶点,具有该点成分的合金在恒温183℃发生共 晶转变LE→aM+ΒN,共晶转变是具有一定成分的液相在恒 温下同时转变为两个具有一定成分和结构的固相的过程。 F:室温时锡在铅中的溶解度;G:室温时铅在锡中的溶 解度
之间一定是由这两个相组成的两相区。如铁区(线)区(
材料科学基础.第四章
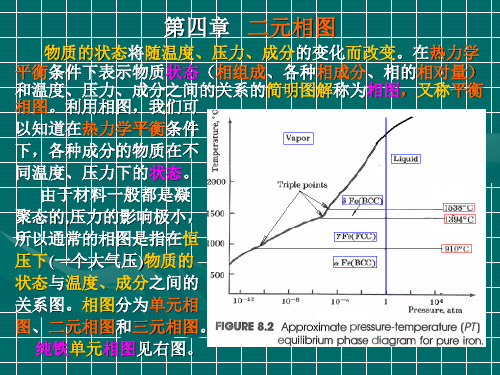
向凝固问题。合金K0 <1, 凝固自左向右进行。
(1)平衡凝固溶质分布 冷却时固相的溶质分布
这种情况下,冷速极其缓慢, 固体、液体中溶质原子充
分扩散。凝固结束时,各部分成分都为Co,无偏析产生,如图
中的Co水平线。
(2)实际凝固(正常凝固)溶质分布 溶质分布及表达式见图。 ①液体中溶质完全混合--偏析严重,左端纯化; ②液体中溶质完全不混合—比较符合实际凝固; ③液体中溶质部分混合。
f=c-p+1(←f=c-p+2,温度、压力) 自由度数是指在木改变系统平衡相的数目的条件厂,可独立改变
的,不影响(影响/决定体系状态)合金状态的因素(如温度、压 力、平衡相成分)的数目。
自由度数的最小值为零,f =0时发生恒温转变,例如纯金属结 晶、二元合金的三相平衡转变、三元合金的四相平衡转变等。
1
4( 3
h2 hk k 2 a2
)(
l c
)2
六方系
对复杂点阵(体心立方,面心立方等),要考虑晶面层数的增加。 体心立方(001)面之间还有一同类的晶面(002),因此间距减半。
1.2.4 晶体的极射赤面投影
通过投影图可将立体图表现于平面上。晶体投影方法很多, 包括球面投影和极射赤面投影。
不平衡凝固的冷速越快,平均成分线的偏离越大。合金内部成分
不均匀现象称为偏析,晶粒内部成分不均匀称为“晶内偏析”, 树
枝晶内的偏析称为“枝晶偏析”。生产中用扩散退火(均匀化退 火)
4.固溶体合金凝固时的溶质量分布 合金凝固时的溶质重新分布,导致宏观偏析和微观偏析并对 晶体的生长形态产生很大影响。 匀晶合金冷却时,固相浓度CS与液相浓度CL的比值K0= CS/CL, 称为平衡分配系数,如图示。 讨论图4.7水平放置的圆 棒容器中,合金液体的定
(1)平衡凝固溶质分布 冷却时固相的溶质分布
这种情况下,冷速极其缓慢, 固体、液体中溶质原子充
分扩散。凝固结束时,各部分成分都为Co,无偏析产生,如图
中的Co水平线。
(2)实际凝固(正常凝固)溶质分布 溶质分布及表达式见图。 ①液体中溶质完全混合--偏析严重,左端纯化; ②液体中溶质完全不混合—比较符合实际凝固; ③液体中溶质部分混合。
f=c-p+1(←f=c-p+2,温度、压力) 自由度数是指在木改变系统平衡相的数目的条件厂,可独立改变
的,不影响(影响/决定体系状态)合金状态的因素(如温度、压 力、平衡相成分)的数目。
自由度数的最小值为零,f =0时发生恒温转变,例如纯金属结 晶、二元合金的三相平衡转变、三元合金的四相平衡转变等。
1
4( 3
h2 hk k 2 a2
)(
l c
)2
六方系
对复杂点阵(体心立方,面心立方等),要考虑晶面层数的增加。 体心立方(001)面之间还有一同类的晶面(002),因此间距减半。
1.2.4 晶体的极射赤面投影
通过投影图可将立体图表现于平面上。晶体投影方法很多, 包括球面投影和极射赤面投影。
不平衡凝固的冷速越快,平均成分线的偏离越大。合金内部成分
不均匀现象称为偏析,晶粒内部成分不均匀称为“晶内偏析”, 树
枝晶内的偏析称为“枝晶偏析”。生产中用扩散退火(均匀化退 火)
4.固溶体合金凝固时的溶质量分布 合金凝固时的溶质重新分布,导致宏观偏析和微观偏析并对 晶体的生长形态产生很大影响。 匀晶合金冷却时,固相浓度CS与液相浓度CL的比值K0= CS/CL, 称为平衡分配系数,如图示。 讨论图4.7水平放置的圆 棒容器中,合金液体的定
材料科学基础-二元系相图及其合金凝固1.3-二元包晶相图

αⅡ+
(4)包晶点(P)以右合金III的平衡凝固
1
L+
D
P2
42.4
1
L+2
1 2
3
室温组织为:单相组织
(5) 包晶点(P)以左合金I的平衡凝固
1 1
L+
D
2
P2
H 42.4
L+
液态合金冷却到1-2点时,发生匀 晶转变,液相中先结晶出初晶α相。
α相成分沿AD变化,液相成分沿 AC变化。 当温度达到2点时,液相成分相当 于C点成分, α相成分相当于D点成 分,合金处于LC+αD两相平衡状态。
以后,随着温度继续下降,在4点 以下温度范围,从β相中析出次生相 α,β→αⅡ。此时,合金处于α和β两 相平衡,直至室温。 合金在室温处于α和β两相平衡,室 温组织为β+αⅡ。
(3) 包晶点(P)以右合金II的平衡凝固
1
L+
D
P2
42.4
1 L+2
3
在0~1点温度范围,合金为液相。
根据这两个特点,在工业上可有 下述应用。 (1). 在轴承合金中的应用 (2). 包晶转变的细化晶粒作用
4、包晶转变的实际应用
(1). 在轴承合金中的应用
滑动轴承是一种重要的机器零件。 由于价格昂贵,更换困难,所以希望 轴在工作中所受的磨损最小。
为此,希望轴承材料的组织由具有 足够塑性和韧性的基体及均匀分布的 硬质点所组成。
对于成分为PC范围的合金,在平衡 冷却条件下,包晶转变产物中不存在α 相。
但是,在非平衡冷却条件下,由于 包晶转变不完全,使得包围在β相中的 α相在包晶转变后仍有残留,通常把这 种组织称为核心(或包心)组织。
1
Hale Waihona Puke L+DP2
(4)包晶点(P)以右合金III的平衡凝固
1
L+
D
P2
42.4
1
L+2
1 2
3
室温组织为:单相组织
(5) 包晶点(P)以左合金I的平衡凝固
1 1
L+
D
2
P2
H 42.4
L+
液态合金冷却到1-2点时,发生匀 晶转变,液相中先结晶出初晶α相。
α相成分沿AD变化,液相成分沿 AC变化。 当温度达到2点时,液相成分相当 于C点成分, α相成分相当于D点成 分,合金处于LC+αD两相平衡状态。
以后,随着温度继续下降,在4点 以下温度范围,从β相中析出次生相 α,β→αⅡ。此时,合金处于α和β两 相平衡,直至室温。 合金在室温处于α和β两相平衡,室 温组织为β+αⅡ。
(3) 包晶点(P)以右合金II的平衡凝固
1
L+
D
P2
42.4
1 L+2
3
在0~1点温度范围,合金为液相。
根据这两个特点,在工业上可有 下述应用。 (1). 在轴承合金中的应用 (2). 包晶转变的细化晶粒作用
4、包晶转变的实际应用
(1). 在轴承合金中的应用
滑动轴承是一种重要的机器零件。 由于价格昂贵,更换困难,所以希望 轴在工作中所受的磨损最小。
为此,希望轴承材料的组织由具有 足够塑性和韧性的基体及均匀分布的 硬质点所组成。
对于成分为PC范围的合金,在平衡 冷却条件下,包晶转变产物中不存在α 相。
但是,在非平衡冷却条件下,由于 包晶转变不完全,使得包围在β相中的 α相在包晶转变后仍有残留,通常把这 种组织称为核心(或包心)组织。
1
Hale Waihona Puke L+DP2
材料科学基础 第7章 其他类型的二元相图

其他类型的二元相图
1. 具有化合物的二元相图 2. 具有偏晶转变的相图 3. 具有合晶转变的相图 4. 具有熔晶转变的相图 5. 具有固态转变的二元相图
1. 具有化合物的二元相图
在某些二元系中,可形成一个或多个化合 物,化合物一般处于相图的中间位置,又称 为中间相(intermediate phase)。根据两 组元间形成化合物的稳定性,可分为:
复杂二元相图的分析方法
分析复杂二元相图的步骤和方法如下:
(1) 首先看相图中是否存在化合物,如有稳定化合物,则以这 些稳定化合物为界(把化合物视为组元),把相图分成几个区域 (基本相图)进行分析。(2)Biblioteka 根据相区接触法则,认清各相区的组成相。
组成二元相图的基本单元有单相区、两相区和三相水平线。这 些单元根据相区接触法则组合在一起。
(4) 应用相图分析典型合金的组晶过程和组织变化规 律。
单相区;相成分、质量与原合金相同。
双相区;在不同温度下两相成分沿相界线变化,各相 的相对量可由杠杆法则求得。
三相共存(平衡)时,三个相的成分固定不变,可用杠 杆法则求出恒温转变前、后相组成的相对量。
二元相图恒温转变类型
恒温转变类型
反应式
转变特征:是在一定温度下从一 个液相中同时分解出一个固相和 另一成分的液相的过程,且固相 的相对量总是偏多。 即:
L1→A+L2
3.具有合晶转变的相图
合晶转变(syntectic reaction)相图(图7.41)特点:二元 组在液态下有限溶解,存在不熔合线,不熔合线以下的两液相 L1和L2。
Mg-Si合金, 就能形成稳定化合物Mg2Si。Mg-Si合金相图 属于含有稳定化合物的相图。
在分析将整个Mg-Si相图可分为Mg-Mg2Si和Mg2Si-Si两个相图来进行分析
1. 具有化合物的二元相图 2. 具有偏晶转变的相图 3. 具有合晶转变的相图 4. 具有熔晶转变的相图 5. 具有固态转变的二元相图
1. 具有化合物的二元相图
在某些二元系中,可形成一个或多个化合 物,化合物一般处于相图的中间位置,又称 为中间相(intermediate phase)。根据两 组元间形成化合物的稳定性,可分为:
复杂二元相图的分析方法
分析复杂二元相图的步骤和方法如下:
(1) 首先看相图中是否存在化合物,如有稳定化合物,则以这 些稳定化合物为界(把化合物视为组元),把相图分成几个区域 (基本相图)进行分析。(2)Biblioteka 根据相区接触法则,认清各相区的组成相。
组成二元相图的基本单元有单相区、两相区和三相水平线。这 些单元根据相区接触法则组合在一起。
(4) 应用相图分析典型合金的组晶过程和组织变化规 律。
单相区;相成分、质量与原合金相同。
双相区;在不同温度下两相成分沿相界线变化,各相 的相对量可由杠杆法则求得。
三相共存(平衡)时,三个相的成分固定不变,可用杠 杆法则求出恒温转变前、后相组成的相对量。
二元相图恒温转变类型
恒温转变类型
反应式
转变特征:是在一定温度下从一 个液相中同时分解出一个固相和 另一成分的液相的过程,且固相 的相对量总是偏多。 即:
L1→A+L2
3.具有合晶转变的相图
合晶转变(syntectic reaction)相图(图7.41)特点:二元 组在液态下有限溶解,存在不熔合线,不熔合线以下的两液相 L1和L2。
Mg-Si合金, 就能形成稳定化合物Mg2Si。Mg-Si合金相图 属于含有稳定化合物的相图。
在分析将整个Mg-Si相图可分为Mg-Mg2Si和Mg2Si-Si两个相图来进行分析
材料科学基础——二元系相图

3. 间隙相与间隙化合物
由原子半径比较大的过渡族金属(M)与原子半径 比较小的非金属(X=H,B,C,N,O)组成,非金属 占间隙位置。
RX/RM=0.23, 占四面体间隙CN=4
RX/RM=0.41~0.59,占据八面体间隙CN=6
RX/RM>0.59,如硼化物与硅化物(Cr,Mn,Fe,Al的 碳化物),则会形成复杂的结构
1. 正常价化合物
结合一般是离子键,具有稳定的电子层结构。 NaCl型结构,fcc: HfC, HfN, VC, TiC, ZrC, PbS, PbSe。e2B, Be2C, Mg2Si, Mg2Si。 闪锌矿ZnS结构,立方: AlSb, CdS, β-SiC。
0
20
40
60
80
100 wt% Ni
47
Effect of Temperature & Composition (Co)
• Changing T can change # of phases: path A to B. • Changing Co can change # of phases: path B to D.
T(°C) 1600 1500 1400 L (liquid) B D
Cu-Ni system
1300 1200 1100 1000 Cu 0 20 A 40 a (FCC solid solution)
60
80
100
wt% Ni
48
合金相结构总结
置换固溶体 固溶体 间隙固溶体
合金相
中间相/ 金属间 化合物
是有限固溶体。晶体结构相同并同时满足电负
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
Tb
Ta
8
③相区。在TaTb凸曲线以上为液相的单相区,用L表示;在 TaTb凹曲线以下为固相的单相区,用a表示;a是Cu-Ni互 溶形成的置换式无限固溶体。在TaTb凸曲线和在TaTb凹曲 线之间为液固两相平衡区用L+a表示。
④匀晶转变。由液相结晶出单相固溶体的过程被称为匀晶转变。 匀晶转变可用下式表示L →a
围内凝固,具有变温凝固的特征 ②还需要成分起伏
15
5.3.2 二元共晶相图 两组元在液态无限互溶,固态有限溶解,通过共晶反
应形成两相机械混合物的二元合金称为二元共晶相图。共 晶反应是液相在冷却过程中同时结晶出两个结构不同的固
相的过程。 L
16
Ta,tb分别是Pb,Sn的熔点 M:锡在铅中的最大溶解度。N:铅在锡中的最大溶解度 E:为共晶点,具有该点成分的合金在恒温183℃发生共 晶转变LE→aM+ΒN,共晶转变是具有一定成分的液相在恒 温下同时转变为两个具有一定成分和结构的固相的过程。 F:室温时锡在铅中的溶解度;G:室温时铅在锡中的溶 解度
Tb
Ta
9
例:求30%Ni合金在1280 时相的相对量
解:作成分线和
T,C
L
1500
1400 1300
a1 b1L+ c1
1200
1100a 1000
1083
1455 c 1280 C
温度线如图。
根据杠杆定律推 论, Q / Q = a1b1 /a1c1 =12/48=1/4 答:所求合金在
1280 时相的
不大时,它们不仅可以在液态或熔融状态完全互溶,而且 在固态也完全互溶,形成成分可变的连续固溶体,称为无 限固溶体或连续固溶体,它们形成的相图即为匀晶相图或 互溶相图。 ➢ 由液相结晶出单相固溶体的过程称为匀晶转变。液固态完 全互溶的体系不多,但是包含匀晶转变部分的相图却不少 ,几乎所有的二元系统都含有匀晶转变部分。
Cu
18 20
30 40
66 60 80
Ni 相对质量为1/4。
100
Ni%
10
5.3.1.2 固溶体合金的平衡凝固及组织
➢ 平衡凝固是指凝固过程中每个阶段都能达到平衡,因此 平衡凝固是在极其缓慢的冷速下实现的。现以30%Ni和 70%Cu的铜镍合金为例来说明固溶体的平衡冷却过程及其 组织的。
11
17
18
19
共晶合金相图的分类
20
共晶反应要点
• 共晶转变在恒温下进行。 • 转变结果是从一种液相中结晶出两个不同的固相。 • 存在一个确定的共晶点。在该点凝固温度最低。 • 成分在共晶线范围的合金都要经历共晶转变。
T,C
183
L
L+
L+
c
d
e
+
Pb
Sn
21
端部固溶体合金结晶过程分析 L
之间一定是由这两个相组成的两相区。如铁区(线)区(
和碳相图中
线)的共
同相为
线与PS线之间为
两相区。
4
➢ 4.当两相区与单相区的分界线与三相等温线相交,则分界 线的延长线应进入另一两相区,而不会进入单相区
两相区和单相区分界线走向
5
5.3 二元相图
二元匀晶相图 ➢ 当两个组元化学性质相近,晶体结构相同,晶格参数相差
冷却曲线 t Ⅱ
23
X2合金结晶过程分析
L
(共晶合金)
T,C
183
L
L+
L+
c
d
e
+T,Cຫໍສະໝຸດ (+ )T,C
T,C
1
L
2
L
L+
L
L+
L+
183 c
d
e
3
f4
Pb X1
+
g
Sn
+ Ⅱ
冷却曲线 t Ⅱ
22
端部固溶体合金结晶特点 L
1.没有共晶反应过程,
T,C
而是经过匀晶反应形成 单相固相。
L
L+
L
+ Ⅱ
2.要经过脱溶转变, 固溶体中析出另一 种固相的过程,产 物称为次生相和二 次相, Ⅱ
水平线与三个单相区的接触点确定了三个平衡相及相浓度。每条水平
线必与三个两相区相邻。铁碳相图中EC、PS水平线都是三相平衡线。
如PS水平线表示
三相区。a相成分由P点确定, r相成分由S点
确定,而Fe3C的成分由三相水平线与Fe3C (为一垂线,图中未画出)
的交点决定
3
➢ 3.如果两个恒温转变中有两个相同的相,则这两条水平线
13
14
➢ 固溶体平衡凝固时的成分变化为:随着温度的降低,固相 的成分沿固相线变化,相对量不断增加,液相的成分沿液 相线变化,相对量不断减少。——固溶体平衡凝固的重要 规律之一。
➢ 固溶体凝固过程与纯金属凝固的区别 相同点:过冷度、能量起伏、结构起伏 不同点:①纯金属在恒温下凝固,固溶体合金在一个温度范
➢ 在30%Ni处作垂线与液相交于B,与固相线交于H。由相图 可见t>t1时,合金为单一液相。在t1温度,表象点在液相 线上,这时液相LB与固相ac平衡,结晶即将开始。继续冷 却,发生匀晶转变(表象点进入L+a区),液相中析出固 相a。这时液相成分沿液相线变化,固相成分沿固相线变 化。
12
➢ 在t2温度,液相成分和固相成分分别为E,F点对应的成分。 这时,两相的重量百分数可由杠杆定理求出。继续冷却, 固相a不断析出。在t3温度,表象点落在固相线H上,液相 全部凝固为合金成分为30%的a相,匀晶转变结束。
6
1.相图分析
➢ 由液相结晶出单相固溶体的过程被称为匀晶转变。 匀晶转
变可用下式表示L
a
➢ 表示匀晶转变的相图称为匀晶相图。大多数合金的相图中 都包含匀晶转变部分。也有一些合金Cu-Ni,Si-Be 等只发 生匀晶转变。
➢ Cu-Ni合金是典型的匀晶系合金,其相图如图所示,匀晶
转变在L+a两相区内完成,自由度为1,结晶在一个温度范
材料科学基础
第5章 相 图 5.3 二元相图
1
二元相图的几何规律
1.两个单相区之间必定有一个由这两个相组成的两相区,而 不能以一条线接界。两个两相区必须以单相区或三相水平线 隔开。由此可以看出二元相图中相邻相区的相数差一个(点 接触除外)。这个规律被称为相区接触法则。
2
2.在二元相图中,若是三相平衡,则三相区必为一水平线,这条
围内完成。
7
图为Cu-Ni的二元匀晶相图,按相图中点线相区进行相图分析。 ①点:相图中的两端点Ta、Tb分别为纯组元Cu、Ni的熔点 ② 线:TaTb凸曲线为液相线,各不同成分的合金加热到该线以
上时全部转变为液相而冷却到该线以下时开始凝固出a固溶体; TaTb凹曲线为固相线,各不同成分的合金加热到该线时开始 熔化,而冷却到该线以下时全部转变为a固溶体。
Ta
8
③相区。在TaTb凸曲线以上为液相的单相区,用L表示;在 TaTb凹曲线以下为固相的单相区,用a表示;a是Cu-Ni互 溶形成的置换式无限固溶体。在TaTb凸曲线和在TaTb凹曲 线之间为液固两相平衡区用L+a表示。
④匀晶转变。由液相结晶出单相固溶体的过程被称为匀晶转变。 匀晶转变可用下式表示L →a
围内凝固,具有变温凝固的特征 ②还需要成分起伏
15
5.3.2 二元共晶相图 两组元在液态无限互溶,固态有限溶解,通过共晶反
应形成两相机械混合物的二元合金称为二元共晶相图。共 晶反应是液相在冷却过程中同时结晶出两个结构不同的固
相的过程。 L
16
Ta,tb分别是Pb,Sn的熔点 M:锡在铅中的最大溶解度。N:铅在锡中的最大溶解度 E:为共晶点,具有该点成分的合金在恒温183℃发生共 晶转变LE→aM+ΒN,共晶转变是具有一定成分的液相在恒 温下同时转变为两个具有一定成分和结构的固相的过程。 F:室温时锡在铅中的溶解度;G:室温时铅在锡中的溶 解度
Tb
Ta
9
例:求30%Ni合金在1280 时相的相对量
解:作成分线和
T,C
L
1500
1400 1300
a1 b1L+ c1
1200
1100a 1000
1083
1455 c 1280 C
温度线如图。
根据杠杆定律推 论, Q / Q = a1b1 /a1c1 =12/48=1/4 答:所求合金在
1280 时相的
不大时,它们不仅可以在液态或熔融状态完全互溶,而且 在固态也完全互溶,形成成分可变的连续固溶体,称为无 限固溶体或连续固溶体,它们形成的相图即为匀晶相图或 互溶相图。 ➢ 由液相结晶出单相固溶体的过程称为匀晶转变。液固态完 全互溶的体系不多,但是包含匀晶转变部分的相图却不少 ,几乎所有的二元系统都含有匀晶转变部分。
Cu
18 20
30 40
66 60 80
Ni 相对质量为1/4。
100
Ni%
10
5.3.1.2 固溶体合金的平衡凝固及组织
➢ 平衡凝固是指凝固过程中每个阶段都能达到平衡,因此 平衡凝固是在极其缓慢的冷速下实现的。现以30%Ni和 70%Cu的铜镍合金为例来说明固溶体的平衡冷却过程及其 组织的。
11
17
18
19
共晶合金相图的分类
20
共晶反应要点
• 共晶转变在恒温下进行。 • 转变结果是从一种液相中结晶出两个不同的固相。 • 存在一个确定的共晶点。在该点凝固温度最低。 • 成分在共晶线范围的合金都要经历共晶转变。
T,C
183
L
L+
L+
c
d
e
+
Pb
Sn
21
端部固溶体合金结晶过程分析 L
之间一定是由这两个相组成的两相区。如铁区(线)区(
和碳相图中
线)的共
同相为
线与PS线之间为
两相区。
4
➢ 4.当两相区与单相区的分界线与三相等温线相交,则分界 线的延长线应进入另一两相区,而不会进入单相区
两相区和单相区分界线走向
5
5.3 二元相图
二元匀晶相图 ➢ 当两个组元化学性质相近,晶体结构相同,晶格参数相差
冷却曲线 t Ⅱ
23
X2合金结晶过程分析
L
(共晶合金)
T,C
183
L
L+
L+
c
d
e
+T,Cຫໍສະໝຸດ (+ )T,C
T,C
1
L
2
L
L+
L
L+
L+
183 c
d
e
3
f4
Pb X1
+
g
Sn
+ Ⅱ
冷却曲线 t Ⅱ
22
端部固溶体合金结晶特点 L
1.没有共晶反应过程,
T,C
而是经过匀晶反应形成 单相固相。
L
L+
L
+ Ⅱ
2.要经过脱溶转变, 固溶体中析出另一 种固相的过程,产 物称为次生相和二 次相, Ⅱ
水平线与三个单相区的接触点确定了三个平衡相及相浓度。每条水平
线必与三个两相区相邻。铁碳相图中EC、PS水平线都是三相平衡线。
如PS水平线表示
三相区。a相成分由P点确定, r相成分由S点
确定,而Fe3C的成分由三相水平线与Fe3C (为一垂线,图中未画出)
的交点决定
3
➢ 3.如果两个恒温转变中有两个相同的相,则这两条水平线
13
14
➢ 固溶体平衡凝固时的成分变化为:随着温度的降低,固相 的成分沿固相线变化,相对量不断增加,液相的成分沿液 相线变化,相对量不断减少。——固溶体平衡凝固的重要 规律之一。
➢ 固溶体凝固过程与纯金属凝固的区别 相同点:过冷度、能量起伏、结构起伏 不同点:①纯金属在恒温下凝固,固溶体合金在一个温度范
➢ 在30%Ni处作垂线与液相交于B,与固相线交于H。由相图 可见t>t1时,合金为单一液相。在t1温度,表象点在液相 线上,这时液相LB与固相ac平衡,结晶即将开始。继续冷 却,发生匀晶转变(表象点进入L+a区),液相中析出固 相a。这时液相成分沿液相线变化,固相成分沿固相线变 化。
12
➢ 在t2温度,液相成分和固相成分分别为E,F点对应的成分。 这时,两相的重量百分数可由杠杆定理求出。继续冷却, 固相a不断析出。在t3温度,表象点落在固相线H上,液相 全部凝固为合金成分为30%的a相,匀晶转变结束。
6
1.相图分析
➢ 由液相结晶出单相固溶体的过程被称为匀晶转变。 匀晶转
变可用下式表示L
a
➢ 表示匀晶转变的相图称为匀晶相图。大多数合金的相图中 都包含匀晶转变部分。也有一些合金Cu-Ni,Si-Be 等只发 生匀晶转变。
➢ Cu-Ni合金是典型的匀晶系合金,其相图如图所示,匀晶
转变在L+a两相区内完成,自由度为1,结晶在一个温度范
材料科学基础
第5章 相 图 5.3 二元相图
1
二元相图的几何规律
1.两个单相区之间必定有一个由这两个相组成的两相区,而 不能以一条线接界。两个两相区必须以单相区或三相水平线 隔开。由此可以看出二元相图中相邻相区的相数差一个(点 接触除外)。这个规律被称为相区接触法则。
2
2.在二元相图中,若是三相平衡,则三相区必为一水平线,这条
围内完成。
7
图为Cu-Ni的二元匀晶相图,按相图中点线相区进行相图分析。 ①点:相图中的两端点Ta、Tb分别为纯组元Cu、Ni的熔点 ② 线:TaTb凸曲线为液相线,各不同成分的合金加热到该线以
上时全部转变为液相而冷却到该线以下时开始凝固出a固溶体; TaTb凹曲线为固相线,各不同成分的合金加热到该线时开始 熔化,而冷却到该线以下时全部转变为a固溶体。
