吸光度-资料
紫外分光光度法吸光度范围

紫外分光光度法-吸光度范围自吸泵参数范围-上海阳光泵业自吸泵参数范围-上海阳光泵业上海阳光泵业作为国内一家著名的集研制、开发、生产、销售、服务于一体的大型多元化企业,上海阳光泵业制造有限公司一直坚持“以质量求生存、以品质求发展”的宗旨为广大客户提供优质服务!同时,上海阳光泵业一直专注于自身实力的提升以及对产品质量的严格把关,为此,目前不但拥有国内最高水准的水泵性能测试中心、完善的一体化服务体系、经验丰富的水泵专家,同时经过多年的发展,产品以优越的性能、精良的品质、良好的服务口碑获得各项专业认证证书和客户认可。
经过团队的不懈努力,上海阳光泵业在国内水泵行业已经取得了很大成就。
这样一家诚信为本、责任重于天的水泵行业佼佼者,对于水泵的维修、保养等各大方面都有自己独特的方法,下面就一起来看看吧!一、S型立式中开泵概述:S型系立式单级双吸垂直中开的离心泵,适应于工厂、城市、矿山、电站、农田水利工程等领域。
该型泵用于输送不含固体颗粒的清水或物理、化学性质类似于水的其它液体,被输送的介质温度为0℃~80℃,允许最大进口压力。
二、S型立式中开泵参数范围:流量Q 200~3770m3/s扬程H ~142m三、S型立式双吸泵型号说明:10SLZ-910-吸入口径被25除(即进口直径为250mm)SLZ-立式单级双吸轴向中开式直联离心泵9-比转数被10除化整的约数四、S型立式中开泵结构型式:泵为立式安装,吸入口和吐出口均在水平方向,中开泵的分开面在轴中心线上垂直分开,检修时不需拆卸进水、出回管路以及电机,即可揭开泵盖,取出转子部件。
泵的上轴采用滚动轴承,油脂润滑,在轴承体上没有冷却腔。
泵的下轴承为导轴承,由泵本身水进行润滑冷却。
轴封采用软填料密封和机械密封两种形式。
五、S型立式中开泵的旋转方向:从电机端向泵看,泵为逆时针方向旋转,即面向泵的可拆泵盖面右为进水口,左为出水口。
光密度及吸光度吸光度量符号的正确表示方法’汪勤俭刘洪娥冷怀明来嘉张大春《第三军医大学学报》编辑部400038重庆沙坪坝区高滩岩,E-mail:wanggj@mail.tmmu.com.cn收稿日期二20050-2-23修回日期:20050-70-1摘要针对目前各科技期刊对吸光度的童符号的不同认识和不恰当表示方法,分析了吸光度的含义,根据《量和单位》国家标准的规定,提出了吸光度量符号的正确表示方法,以期为广大同仁提供参考,为正确执行《量和单位》国家标准提供依据。
分子吸收光谱

分子吸收光谱首页资讯法规技术质量检验标准资料仪器图库商城人才英语课堂专题网刊网址论坛当前位置:首页>>检验技术>>食品理化检验>>仪器分析>>正文分子吸收光谱一. 分子吸收光谱的产生(一)分子能级与电磁波谱分子中包含有原子和电子,分子、原子、电子都是运动着的物质,都具有能量,且都是量子化的。
在一定的条件下,分子处于一定的运动状态,物质分子内部运动状态有三种形式:①电子运动:电子绕原子核作相对运动;②原子运动:分子中原子或原子团在其平衡位置上作相对振动;③分子转动:整个分子绕其重心作旋转运动。
所以:分子的能量总和为E分子= Ee +Ev +Ej +⋯ (E0 +E平) (3)分子中各种不同运动状态都具有一定的能级。
三种能级:电子能级E(基态E1 与激发态E2)振动能级V= 0,1,2,3 ⋯转动能级J = 0,1,2,3 ⋯当分子吸收一个具有一定能量的光量子时,就有较低的能级基态能级E1 跃迁到较高的能级及激发态能级E2,被吸收光子的能量必须与分子跃迁前后的能量差∆E 恰好相等,否则不能被吸收。
图1 双原子分子的三种能级跃迁示意图对多数分子对应光子波长光谱∆E 约为1~20eV 1.25 ~ 0.06㎛ 紫外、可见区(电子)∆E 约为0.5~1eV 25 ~ 1.25㎛ (中)红外区(振动)∆E约为10-4~0.05eV 1.25cm~ 25㎛ (远)红外区(转动)分子的能级跃迁是分子总能量的改变。
当发生电子能级跃迁时,则同时伴随有振动能级和转动能级的改变,即“电子光谱”——均改变。
因此,分子的“电子光谱”是由许多线光谱聚集在一起的带光谱组成的谱带,称为“带状光谱”。
吸光度(光密度)量符号的正确表示方法’

按 G 30 6 9 , brBe . 3Lm e-e 定律应写作 : B1 一 2 a t r
D二一 g gAP 1 7二1P ,二kb t c
摘 要
针对目 前各科技期刊对吸光度( 光密度) 的童符号的不同 认识和不恰当表示方法, 分析了吸光度( 光密度) 的含义,
根据《 量和单位》 标准的规定, 国家 提出了 吸光度( 度) 光密 量符号的正确表示方法, 期为广大同 以 仁提供参考, 为正确执行《 量
和单位》 国家标准提供依据。
关键词 量和单位 吸光度 光密度
吸光度( 光密度) 量符号的正确表示方法’
汪勤俭 刘洪娥 冷怀明 来嘉 张大春
《 第三军医大学学报》 编辑部 403 重庆沙坪坝区 008 高滩岩, -a: g mitm . c Emiwn j a. uc . l a @ lm o n g m
收稿日 20- - 期二 5 2 3 00 2 修回日 20- - 期: 5 7 1 0 00
或O 4二有的 D 2 , 用正体, 9 。 有的用斜体; 也有的标注为D 。 a笔
者查阅了一些资料, 报告如下。
1 光密度(pc dnt 的含义 ota esy il i)
光密度(pc es , 也称吸光度(b r ne la dnt O ) o il i D y a o ec, sb A, )通俗地理解即吸收了多少光。一定的物质会吸收一定波 长的光, 从而显示一定的色彩; 而在灰度或黑白图像中则表 现为灰度的改变。 D ( O =g人射光灰度/ 1 透射光灰度)人射 , 光的灰度有的软件中用背景的灰度值来表示, 即玻片中空白 部分的图 像灰度; 严格的光密度分析需要进行系统的光密度 标定, 方法是将一套标准的光密度吸光片, 通过显微摄像系 统输入图像分析软件, 绘制线性图, 然后根据标准直线作出 校准。光密度越大, 表示某种物质的含量越高, 在病理图像
紫外可见吸收光谱分析

(2) 介质不均匀性引起的偏离 朗伯-比尔定律在均匀、非散射时可成立,当介质不均匀,或有胶体、乳浊、悬浮体存
在时,入射光除了被吸收外,还有反射、折射损失,故所测A值比实际吸收要大许多,导 致偏离比尔定律。
引起工作曲线弯曲的原因还有一些,如:溶质的性质变化、操作不当等等。
§ 2.3 影响显色反应的若干因素 (一) 吸光光度法对显色反应的要求
2、分子吸收光谱
①电子光谱 在多原子分子中,分子轨道中有许多电子能级,平时各电子都尽先进入低能级,处于基态。当
有光波照射这些分子时,轨道中的电子会吸收光波中的某些波长的光,使这束光中缺少某些波长的 光。电子本身将从低能级跃迁到高能级上。
象这样的情况下,被吸收的光往往波长较短,在紫外和可见光范围。本章主要讨论这一部分内 容。
红色), 1﹕3(pH 8~11.5 黄色,最稳定)三种不同颜色的络合物生成。
3、温度的影响:一般在室温.有些需加热. 4、显色时间的影响
5、溶剂的影响:可提高显色反应的灵敏度. 6、共存离子的影响:
§ 2.4 光度测量误差和测量条件的选择
一、 仪器测量误差
在吸光光度分析中,除了各种化学条件所引起的误差外,仪器测量不准确也是误差的主要来源。 任何光度计都有一定的测量误差,这种误差可能来源于光电池不灵敏、光电流测量不准和光源不稳
§ 2 光度分析法的基本原理
一、光度分析法的特点 1、适用范围:常用于测定试样中1%~10-3 %的微量组分,甚至可测定低至10-4 %~10-5 %的痕量组份。目 前,随着仪器和方法的改进,有的已达10-9 %。一般情况下,相对误差为2~5 %,这在微量分析中已是十 分精确的了。 2、特点:灵敏、快速、准确、简便。
cF2e
半自动生化分析仪吸光度示值误差测量结果不确定度分析

冯丽娟 孔繁 森 ( 邯郸市计量测试所)
摘要 : 半 自动 生 化 分 析 仪 是 通 过 测 量 吸 光度 , 用 未知 浓度 样 品 与 已知 浓度 的标 准 物 质 相 比较 来 进 行 定 量 分 析 的 。 本 文 使 用 中 国计 量
参 考文献 :
【 1 ] J J G 4 6 4 — 2 0 1 1 半 自动生化分析仪检定规 程.
【 2 】 李瑞昌等. 测 量 结 果 不确 定 度 分析 实例 . 河 北 省 计 量 协 会 内 部 资料 , 2 0 0 4 .
U= 0 . 0 0 6 A( k = 2 o ① 在相 同的测量条件下,用标称值为 0 . 5 A的标准物 确定 度 为 :
质进 行 1 0次测 量 , 所 得 数据如 下 ( 单位 : A) :
科 学 院 生 产 的标 准 物 质 进 行 吸 光 度 测 量 ,并 对 示值 误 差 测 量 结 果 的 不确 定 度 进 行 分析 评 定 。
S
关键词 : 半 自动 生 化 分析 仪
吸 光度
不确 定 度
— 0. 0 01|
1概 述 1 . 1 测量 方法
由于 实际测 量 中 , 要 求测量 三 次取平 均值 , 则 有
设 定 波长 为 3 4 0 n m, 吸收池 温度 为 3 7 q C, 吸液 量大 于
度 示值 误 差。 1 . 6 符 合上 述 条件 下 的 测量 结 果 , 一般 可 直 接使 用 本
不确 定 度 的评定 结 果。
u ( A ) l 测量重复 性 1 0 . o 0 1 } 1 1 0 . 0 0 1 u ( A s ) I 标准物质不确定度1 0 . 0 0 2 5 l一 1 l 0 . 0 0 2 5
医学检验主管检验师资格考试复习资料生物化学(11)临床化学常用分析技术

医学检验主管检验师资格考试复习资料生物化学(11)临床化学常用分析技术一、光谱分析(分光光度技术)利用各种化学物质所具有的发射、吸收或散射光谱谱系的特征,来确定其性质、结构或含量的技术,称为光谱分析技术。
特点:灵敏、快速、简便。
是生物化学分析中最常用的分析技术。
分类(一)可见及紫外分光光度法分光光度法的理论基础是朗伯-比尔定律。
mber-Beer定律:A=k·b·cA为吸光度k—吸光系数b—光径,单位:cmc—溶液浓度,单位:g/L2.摩尔吸光系数:在公式“A=k·b·c”中,当c=1mol/L,b=1cm时,则常数k可用ε表示。
3.比吸光系数:在公式“A=k·b·c”中,当c为百分浓度(w/v),b为cm时,则常数k可用E%表示,称为比吸光系数或百分吸光系数。
(二)原子吸收分光光度法原子吸收分光光度法是基于元素所产生的原子蒸气中待测元素的基态原子,对所发射的特征谱线的吸收作用进行定量分析的一种技术。
即在一定条件下,原子的吸光度同原子蒸气中待测元素基态原子的浓度成正比。
常用的定量方法有:标准曲线法、标准加入法、内标法。
1.标准曲线法:将一系列浓度不同的标准溶液按照一定操作过程分别进行测定,以吸光度为纵坐标,浓度为横坐标绘制标准曲线。
在相同条件下处理待测物质并测定其吸光度,即可从标准曲线上找出对应的浓度。
由于影响因素较多,每次实验都要重新制作标准曲线。
2.标准加入法:把待测样本分成体积相同的若干份,分别加入不同量的标准品,然后测定各溶液的吸光度,以吸光度为纵坐标,标准品加入量为横坐标,绘制标准曲线,用直线外推法使工作曲线延长交横轴,找出组分的对应浓度。
本法的优点是能够更好地消除样品基质效应的影响,较为常用。
3.内标法:在系列标准品和未知样品中加入一定量样本中不存在的元素(内标元素),分别进行测定。
以标准品与内标元素的比值为纵坐标,标准品浓度为横坐标绘制标准曲线,再根据未知样品与内标元素的比值依曲线计算出未知样品的浓度。
水质 铜、锌、铅、镉的测定--原子吸收分光光度法

资料范本本资料为word版本,可以直接编辑和打印,感谢您的下载水质铜、锌、铅、镉的测定--原子吸收分光光度法地点:__________________时间:__________________说明:本资料适用于约定双方经过谈判,协商而共同承认,共同遵守的责任与义务,仅供参考,文档可直接下载或修改,不需要的部分可直接删除,使用时请详细阅读内容1 适用范围本标准规定了测定水中铜、锌、铅、镉的火焰原子吸收分光光度法。
本标准分为两部分。
第一部分为直接法,适用于测定地下水、地面水和废水中的铜、锌、铅、镉;第二部分为螯合萃取法,适用于测定地下水和清洁地面水中低浓度的铜铅、镉。
2 定义2.1溶解的金属,未酸化的样品中能通过0.45um滤膜的金属成分。
2.2金属总量:未经过滤的样品经强烈消解后测得的金属浓度,或样品中溶解和悬浮的两部分金属浓度的总量。
3 试剂和材料除非另有说明,分析时均使用符合国家标准的分析纯试剂;实验用水,GB/T 6682,二级。
3.1 硝酸:ρ(HNO3)=1.42 g/mL,优级纯。
3.3 硝酸:ρ(HNO3)=1.42 g/mL,分析纯。
3.3 高氯酸:ρ(HClO4)=1.67 g/mL,优级纯。
3.4 燃料:乙炔,用钢瓶气或由乙炔发生器供给,纯度不低于99.6%。
3.5 氧化剂:空气,一般由气体压缩机供给,进入燃烧器以前应经过适当过滤,以除去其中的水、油和其他杂质。
3.6 硝酸溶液:1+1。
用硝酸(3.2)配制。
3.7 硝酸溶液:1+499。
用硝酸(3.1)配制。
3.8 金属储备液:1.000g/L。
称取1.000g光谱纯金属,准确到0.001g,用硝酸(3.1)溶解,必要时加热,直至溶解完全,然后用水稀释定容至1000mL。
3.9 中间标准溶液。
用硝酸溶液3.7稀释金属贮备液3.8配制,此溶液中铜、锌、铅、镉的浓度分别为50.00、10.00、100.00、10.00mg/L。
4 采样和样品4.1用聚乙烯塑料瓶采集样品。
吸光度、光学密度、吸收系数、吸收率之间的关系Word文档
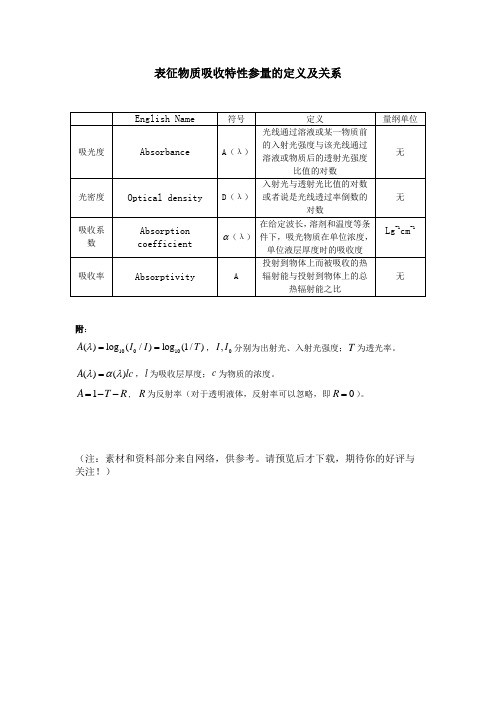
在给定波长,溶剂和温度等条件下,吸光物质在单位浓度,单位液层厚度时的吸收度
Lg-1cm-1
吸收率
Absorptivity
A
投射到物体上而被吸收的热辐射能与投射到物体上的总热辐射能之比
无
附:
, 分别为出射光、入射光强度; 为透光率。
, 为吸收层厚度; 为物质的浓度。
, 为反射率(对于透明液体,反射率可以忽略,即 )。
(注:素材和资料部分来自网络,供参考。请预览后才下载,期待你的好评与关注!)
表征物质吸收特性参量的定义及关系
English Name
符号
定义
量纲单位
吸光度
Absorbance
A(λ)
光线通过溶液或某一物质前的入射光强度与该光线通过溶液或物质后的透射光强度比值的对数
无
光密度
Opticaldensity
D(λ)
入射光与透射光比值的对数或者说是光线透过率倒数的对数
cient
吸光度-资料

吸光度-资料最近频繁用到酶标仪,对OD值和吸光度值(abs)的概念和其线性范围不甚理解,查了很多资料,包括园子里前辈的总结和我从其他网站上获得的,也包括我个人的理解,在此做更全面的总结(因为园子里的都是N年前的老帖子,且不是很全面,呵呵)希望能供战友们参考1、首先明白什么是朗伯比尔定律朗伯——比尔(Lambert-beer)光吸收定律:A=-lgT=εb cA——吸光度,又称光密度“O.D”。
T——透光度,T=I / I。
,I。
——为照射到吸收池上的光强,I——为透过吸收池的光强。
ε——摩尔吸光系数或克分子吸光系数(L?mol-1?cm-1)。
b——样品光程(cm),通常使用1.0cm 的吸收地,b=1cm。
C?——样品浓度(mol/L)。
由上式可以看出:吸光度A与物质的吸光系数“ε”和物质的浓度“C”成正比。
2、OD值定义OD值(optical density)表示某一物质在某一个特定波长下的吸光度;ABS是吸光值absorbance 的缩写. 在分析化学里,某一化学物质都可吸收一定波长的光,并且对光的吸收度与此化学物质的浓度成正比.因此可以利用吸光度的大小来测定某种物质的浓度.其中某物质在特定波长下对光的吸收度,就是OD值,一般用经过石英管后的光强比上照射到石英管前的光强来表示.3、吸光度值(abs/AU)定义吸光度,absorbance,是指光线通过溶液或某一物质前的入射光强度与该光线通过溶液或物质后的透射光强度比值的对数,影响它的因素有溶剂、浓度、温度等等。
吸光系数与入射光的波长以及被光通过的物质有关,只要光的波长被固定下来,同一种物质,吸光系数就不变。
当一束光通过一个吸光物质(通常为溶液)时,溶质吸收了光能,光的强度减弱。
吸光度就是用来衡量光被吸收程度的一个物理量。
吸光度用A表示。
A=abc,其中a为吸光系数,单位L/(g·cm),b为液层厚度(通常为比色皿的厚度),单位cm ,c为溶液浓度,单位g/L影响吸光度的因数是b和c。
红外吸收光谱法

1020
中强峰(m)
120
弱峰(w)
1
极弱峰(vw)
2、吸收强度的影响因素
(1)振动能级的跃迁几率: 振动能级的跃迁几率越大,吸收峰越强,从基 态到第一激发态的跃迁几率最大,因此基频吸收带 一般最强。 (2)振动过程中偶极矩的变化: 振动过程中只有发生偶极矩变化的跃迁,才有红外 活性,同时偶极矩变化越是大,对应的吸收峰强度 也越强,因此,化学键两端原子的电负性相差越大, 或分子的对称性越差,伸缩振动时偶极矩变化越大, 产生的吸收峰也越强。
2.多原子分子的振动类型及振动自由度
(1)分子的振动类型 绝大多数的分子是多原子分子,其振动方式显然 很复杂。但可依据简正振动形式的不同将其归结为 二类基本振动: 伸缩振动:化学键两端的原子沿键轴方向作来回 周期运动(键长发生变化)。 弯曲振动(变形振动):使化学键角发生周期性变化 的振动。
§1
红外吸收光谱图
红外吸收光谱基本原理
Principle of IR
吸收带在光谱图中的位置可用波长(μm)或波数(cm-1) 表示(横坐标)。光谱图的纵坐标,即吸收强度,可用百 分透光度或吸光度表示。
吸收峰出现的频率位置 吸收峰的个数 吸收峰的强度
决定因素?
一、 红外吸收光谱产生的条件
分子必须同时满足以下两个条件时,才能产生红外 吸收。 1、 能量必须匹配 即只有当照射分子的红外辐射频率与分子某种振动 方式的频率相同时,分子吸收能量后,从基态振动 能级跃迁到较高能量的振动能级,从而在图谱上出 现相应的吸收带。
1892年朱利叶斯(Julius)用岩盐棱镜及测热辐射计, 测得了 20几种有机化合物的红外光谱,这是一个具有开拓意义的研 究工作。
利用物质的分子对红外辐射吸收,得到与分子结构 相应的红外光谱图,从而来鉴别分子结构的方法, 称为红外吸收光谱法,简称红外光谱法。 λ : 0.78 ~ 1000µ m
紫外可见吸收光谱

§ 2 光度分析法的基本原理
一、光度分析法的特点 1、适用范围:常用于测定试样中1%~10-3 %的微量 组分,甚至可测定低至10-4 %~10-5 %的痕量组份。目 前,随着仪器和方法的改进,有的已达10-9 %。一般 情况下,相对误差为2~5 %,这在微量分析中已是十 分精确的了。 2、特点:灵敏、快速、准确、简便。
(二)控制适当的吸光度范围
从仪器测量误差的讨论中了解到,为使测量结果得 到较高的准确度,一般应控制标准溶液和被测试液 的吸光度在0.2~0.8范围内。为此,可以从下列两方 面来考虑。
1.控制溶液的浓度,如改变试样的称量和改变 溶液的稀释度等。
但是在实际绘制中却常常出现弯曲情况。如果标 准曲线弯曲,测定数据必带来很大的误差,故应 努力找出原因设法解决之。一般来说引起标准曲 线弯曲的主要原因有如下几种。
(一)比尔定律的局限性
比尔定律为:A=KC即A∝C
这是在溶液很稀的情况下,即各溶质质点互不 干扰时才成立。
当溶液较浓时,溶液中的有色配合物会互相吸 引、排斥,光线在质点之间发生反射,使出射光线 发生改变,从而使比尔定律失效。
▲跃迁:电子受激发,从低能级转移到高
能级的过程
2.分子吸收光谱的分类: 分子内运动涉及三种跃迁能级,所需能量大
小顺序 E电E振E转
E电1~20ev0.06~1.25m紫外 可见吸收 E振0.05~1ev25~1.25m红外吸收光 E转0.00~50.05ev25~025m远红外吸
3.紫外-可见吸收光谱的产生 由于分子吸收中每个电子能级上耦合有许多
一、 仪器测量误差
在吸光光度分析中,除了各种化学条件所引起的 误差外,仪器测量不准确也是误差的主要来源。
任何光度计都有一定的测量误差,这种误差可能 来源于光电池不灵敏、光电流测量不准和光源不 稳等。如果测量误差以光电流表示为Δi,相当于 光强的误差ΔI,由此引起透光率的误差为ΔT 。对 于同一光度仪器,ΔT基本上为一常数,一般为 0.01~0.02 。
(生物饵料培养学)实验资料

【注意事项】
1.用加热法消毒培养用水时,三角瓶内的水量不能超过瓶子的 2/3,瓶外面不能有水珠,瓶口用纸盖住,不要绑紧。
2.洗液在瓶子内转动时,注意瓶口不能对着自己,也不能对着 他人。
3.干热灭菌过程中,实验者不能离开,严防恒温调节的自动控 制失灵而造成安全事故。
4.烘箱内的温度需冷却至60℃以下,才能打开烘箱门取出工具、 容器。
【注意事项】
1.血球计数板计数时,藻液不能溢出盖玻片上方,若有溢出,需冲 洗干净,重新取样,注意控制藻液流入量,不能过多,也不能过少, 应充满计数板的部分,不能有气泡。 2.应注意摇匀后,再取样进行测定或计数。 3.如果藻细胞浓度太大,应稀释后才计数,计数结果应乘以稀释倍 数。 4.运动的藻类,应杀死后才能计数。(建议:稀释液中含有固定液)
YOUR SITE HERE
【实验用品】
一、实验器材
电子天平、电炉、容量瓶、烧杯、搅拌棒、试剂瓶、100ml量筒、吸管、10ml 移液管、耳球、微量注射器。 二、药品 NaNO3、(NH2)2CO、KH2PO4、FeSO4.7H2O、MnSO4、 EDTA-Na2、VB1、VB12、Na2SiO3 。
量。
【作业与思考】
1.单细胞藻类培养液配制的操作过程中应注意什么问题? 2.单细胞藻类的全培养液配方应包含哪些成分? 3.试述该配方中的N、P比是多少?
YOUR SITE HERE
Thank you!
YOUR SITE HERE
实验四 单细胞藻一级培养
【实验目的】
掌握单细胞藻一级培养的基本操作与管理,从而有可能做到有计划地培 养足够数量的符合质量的单细胞藻。
1ml水体的藻类细胞数目=计数平均值×稀释倍数×10000个(简记:万个 /ml)
环境监测复习资料

环境监测复习资料第一章1.环境监测的主要任务是什么?①对环境中各项要素进行经常性监测,掌握和评价环境质量状况及发展趋势;②对各个有关单位排放污染物的情况进行监视性监测;③为政府部门执行各项环境法规、标准,全面展开环境监测技术的发展的监测数据和资料;④开展环境监测技术研究,促进环境监测技术的发展。
2、根据环境污染的特点说明对近代环境监测提出哪些要求?①三高(灵敏度、准确度、分辨率高)②三化(自动化、标准化、计算机化)③多学科、边缘性、综合性、社会性3、环境监测有何特点?①环境监测的技术特点:生产性,综合性,连续性,追踪性②环境监测的政府行为属性:依法强制性,行为公正性,社会服务性③环境监测与环境管理4、是分析环境监测的地位与作用环境检测是科学管理和环境执法监督的基础,是环境保护必不可少的基础性工作;环境监测在正确认识环境质量,解决现存或潜在的环境问题,改善生活环境和生态环境,协调人类和环境的关系,最终实现人类的可持续发展中起着举足轻重的作用。
5、简述环境监测的目的与类型?目的:①评价环境质量②为监督管理控制污染服务③预测预报环境质量④制定环境法规标准规划类型:安环境对象分为水质监测、空气监测、土壤监测、固体废物检测、生物监测与生物污染监测、生态监测、物理污染监测;按监测目的分为政府授权的公益型环境监测和非政府组织的公共事务环境监测;按监测区域分为厂区监测和区域监测;按专业部门分为气象监测、卫生监测、资源监测等。
6、试分析我国环境标准体系的特点三级:国家环境标准、国家环境行业标准、地方环境标准六类:环境质量标准、污染物排放标准、环境基础标准、环境方法标准、环境标准物质标准、环保仪器设备标准7、制定环境标准的原则是什么?是否标准越严越好?原则:①以人为本②科学性、政策性③以环境基准为基础,与国家的技术水平、社会经济承受能力相适应④综合效益分析,实用性、可行性⑤因地制宜、区别对待⑥与有关标准、制度协调配套原则⑦采用国际标准,与国际标准接轨⑧便于实施与监督控制技术水平、经济条件和社会要求实际情况,并非越严越好8、环境优先检测有何原则?①对污染物做全面分析,从中选出影响面广,持续时间长,不易或不能被微生物所分解而能让动植物发生病变的物质做日常监测,具有生物累积性,三只物质、毒性大的、数量大的作优先监测②需要检测的项目必须有可靠的监测手段并保证能获得比较满意的效果③监测结果具有可比较的标准或能做正确的解释和判断,否则具有盲目性第二章1、什么叫滴定分析?有几种类型?滴定分析:将被测定的溶液置于锥形瓶内,同时在溶液中加入适当的指示剂,然后用一种已知准确浓度滴定,并摇动锥形瓶促其进行化学反应,直到指示剂变色停止滴定,据标准溶液的浓度和消耗的体积计算出待测物质的含量。
食品仪器分析原子吸收分光光度法参考答案

原子吸收分光光度法习题一、填空题1.原子吸收光谱分析是利用基态的待测原于蒸气对光源辐射的吸收进行分析的。
答:特征谱线2.原子吸收光谱分析主要分为类,一类由将试样分解成自由原子,称为分析,另一类依靠将试样气化及分解,称为分析。
b5E2RGbCAP答:两,火焰,火焰原子吸收,电加热的石墨管,石墨炉无火焰原子吸收。
3.一般原子吸收光谱仪分为、、、四个主要部分。
答:光源、原子化器,分光系统,检测系统。
4.空心阴极灯是原子吸收光谱仪的,其最主要部分是,它是由制成的。
整个灯熔封后充以或成为一个特殊形式的。
p1EanqFDPw答:光源,空心阴极灯,待测元素本身或其合金,低压氖,氢气,辉光放电管。
5.原子吸收光谱仪中的火焰原子化器是由、及三部分组成。
答:雾化器,雾化室,燃烧器。
6.原子吸收光谱仪中的分光系统也称,其作用是将光源发射的与分开。
答:单色器,待测元素共振线,其它发射线。
7.早期的原子吸收光谱仪使用棱镜为单色器,现在都使用单色器。
前者的色散原理是,后者为。
答:光栅,光的折射,光的衍射。
8.在原子吸收光谱仪中广泛使用做检测器,它的功能是将微弱的信号转换成信号,并有不同程度的。
答:光电倍增管,光,电,放大。
9.原子吸收光谱分析时工作条件的选择主要有的选择、的选择、的选择、的选择及的选择。
答:灯电流,燃烧器高度,助燃气和燃气流量比,吸收波长,单色器狭缝宽度。
10.原子吸收法测定固体或液体试样前,应对样品进行适当处理。
处理方法可用、、、等方法。
答:溶解,灰化,分离,富集。
11.原子吸收光谱分析时产生的干扰主要有干扰,干扰,干扰三种。
答:光谱干扰,物理干扰,化学干扰。
二、判断题1.原子吸收光谱分析定量测定的理论基础是朗伯一比尔定律。
< √)2.在原子吸收分析中,对光源要求辐射线的半宽度比吸收线的半宽度要宽的多。
< ×)3.原子吸收光谱仪和752型分光光度计一样,都是以氢弧灯做为光源的。
< ×)4.原子吸收法测定时,试样中有一定基体干扰时,要选用工作曲线法进行测定。
标准曲线的绘制吸光度标准曲线绘制

标准曲线的绘制-吸光度标准曲线绘制生物化学实验报告ALT与其吸光度的标准曲线绘制采集样本:广西医科大学口腔医学2016级13班四个组中7组生物化学实验数据采集时间:2016年11月15日2016~2016上学期第十一周周一下午采集人:何洁梅一、几组ALT与其吸光度的标准曲线数据记录ALT活力单位A520吴修团1组A520黎丁菱1组A520杨璇璇1组A520谢晓兰2组A520莫雪玲2组A520李文良3组A520文全海4组00000000二、各采集样本汇总图样本1测定得待测血清ALT活力单位为50U/L样本2测定得待测血清ALT活力单位为97U/L样本3测定得待测血清ALT活力单位为135U/L样本4测定得待测血清ALT活力单位为70U/L样本5测定得待测血清ALT活力单位为148U/L样本6测定得待测血清ALT活力单位为45U/L样本7测定得待测血清ALT活力单位为98U/L四、采集数据处理结果分析1.数据总结样本编号测定的ALT活力单位是否大于40U/L正常/非正常150是非正常297是非正常3135是非正常470是非正常5148是非正常645是非正常798是非正常平均值92均为“是”均为“非正常”2.针对数据处理结果的分析采集的7组数据经标准曲线测量后,得到的ALT活力单位值均大于40,即均为非正常值,综上,认为待测血清中ALT 含量超于正常值。
3.针对源数据的分析采集的7组数据中样本4、5、6的数据经画图后可基本分布呈过原点的线性关系,符合理论规律,但其他的数据误差较大。
另外,比较符合理想标准曲线的4、5、6样本的三个ALT活力单位值也存在较大的出入。
4.经分析,总结可能的误差来源如下配置丙酮酸标准溶液、底物溶液、磷酸缓冲液的混合溶液时,丙酮酸标准溶液的剂量都很小,容易造成误差。
加入2,4—二硝基苯肼的时间可能有误差,保温的时间,以及加入NaOH 以停止反应的时间都有可能有偏差,容易造成较大。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
最近频繁用到酶标仪,对OD值和吸光度值(abs)的概念和其线性范围不甚理解,查了很多资料,包括园子里前辈的总结和我从其他网站上获得的,也包括我个人的理解,在此做更全面的总结(因为园子里的都是N年前的老帖子,且不是很全面,呵呵)希望能供战友们参考1、首先明白什么是朗伯比尔定律朗伯——比尔(Lambert-beer)光吸收定律:A=-lgT=εb cA——吸光度,又称光密度“O.D”。
T——透光度,T=I / I。
,I。
——为照射到吸收池上的光强,I——为透过吸收池的光强。
ε——摩尔吸光系数或克分子吸光系数(L?mol-1?cm-1)。
b——样品光程(cm),通常使用1.0cm 的吸收地,b=1cm。
C?——样品浓度(mol/L)。
由上式可以看出:吸光度A与物质的吸光系数“ε”和物质的浓度“C”成正比。
2、OD值定义OD值(optical density)表示某一物质在某一个特定波长下的吸光度;ABS是吸光值absorbance 的缩写. 在分析化学里,某一化学物质都可吸收一定波长的光,并且对光的吸收度与此化学物质的浓度成正比.因此可以利用吸光度的大小来测定某种物质的浓度.其中某物质在特定波长下对光的吸收度,就是OD值,一般用经过石英管后的光强比上照射到石英管前的光强来表示.3、吸光度值(abs/AU)定义吸光度,absorbance,是指光线通过溶液或某一物质前的入射光强度与该光线通过溶液或物质后的透射光强度比值的对数,影响它的因素有溶剂、浓度、温度等等。
吸光系数与入射光的波长以及被光通过的物质有关,只要光的波长被固定下来,同一种物质,吸光系数就不变。
当一束光通过一个吸光物质(通常为溶液)时,溶质吸收了光能,光的强度减弱。
吸光度就是用来衡量光被吸收程度的一个物理量。
吸光度用A表示。
A=abc,其中a为吸光系数,单位L/(g·cm),b为液层厚度(通常为比色皿的厚度),单位cm ,c为溶液浓度,单位g/L影响吸光度的因数是b和c。
a是与溶质有关的一个常量。
此外,温度通过影响c,而影响A。
符号A,表示物质对光的吸收程度。
97801 式中I0是通过均匀的液体介质的一束平行光的入射光的强度;It是透射光强度;T是透射比。
A值越大,表示物质对光的吸收越大。
根据比尔定律,吸光度与吸光物质的量浓度c成正比,以A对c作图,可得到光度分析的校准曲线。
在多组分体系中,如果各组分的吸光质点彼此不发生作用,那么吸光度便等于各组分吸光度之和,这一规律称吸光度的加和性。
据此可以进行多组分同时测定及某些化学反应平衡常数的测定。
在吸光度测定中,为抵消吸收池对入射光的吸收、反射以及溶剂、试剂等对入射光的吸收、散射等因素,可选用双光束分光光度计,并选光学性质相同、厚度相等的吸收池分别盛待测溶液和参比溶液。
4、国外资料的权威总结"Optical density" can also refer to index of refraction.In spectroscopy, the absorbance A (also called optical density) is defined as: Aλ=log10(I0/I)where I is the intensity of light at a specified wavelength λ that has passed through a sample (transmitted light intensity) and I0 is the intensity of the light before it enters the sample or incident light intensity (or power). Absorbance measurements are often carried out in analytical chemistry, since the absorbance of a sample is proportional to the thickness of the sample and the concentration of the absorbing species in the sample, in contrast to the transmittance I / I0 of a sample, which varies logarithmically with thickness and concentration.Absorbance vs transmittanceAbsorbanceTransmittance (I / I0)Percent transmittance (100 * I / I0)0 1 1000.1 0.79 790.25 0.56 560.5 0.32 320.75 0.18 180.9 0.13 131 0.1 102 0.01 13 0.001 0.1Instrument measurement rangeAny real measuring instrument has a limited range over which it can accurately measure absorbance. An instrument must be calibrated and checked against known standards if the readings are to be trusted. Many instruments will become non-linear (fail to follow the Beer-Lambert law) starting at approximately 2 AU (~1% Transmission). It is also difficult to accurately measure very small absorbance values (below 10?4) with commercially available instruments for chemical analysis. In such cases, laser-based absorption techniques can be used, since they have demonstrated detection limits that supersede those obtained by conventional non-laser-based instruments by many orders of magnitude (detections have been demonstrated all the way down to 5 10?13). The theoretical best accuracy for most commercially available non-laser-based instruments is in the range near 1 AU. The path length or concentration should then, when possible, be adjusted to achieve readings near this range.5、再看看园子里的精华总结OD值1. 朗伯——比尔(Lambert-beer)光吸收定律:A=-lgT=εb cA——吸光度,又称光密度“O.D”。
T——透光度,T=I / I。
,I。
——为照射到吸收池上的光强,I——为透过吸收池的光强。
ε——摩尔吸光系数或克分子吸光系数(L?mol-1?cm-1)。
b——样品光程(cm),通常使用1.0cm 的吸收地,b=1cm。
C?——样品浓度(mol/L)。
由上式可以看出:吸光度A与物质的吸光系数“ε”和物质的浓度“C”成正比。
2. DNA和RNA的OD值2.1 原理嘌呤碱和嘧啶碱具有共轭双键,使碱基、核苷、核苷酸和核酸在240~290nm的紫外波段有一强烈的吸收峰,因此核酸具有紫外吸收特性。
DNA钠盐的紫外吸收在260nm附近有最大吸收值(图3-25),在230nm处为吸收低谷,其吸光率(absorbance)以A260表示,A260是核酸的重要性质,RNA钠盐的吸收曲线与DNA无明显区别,蛋白质在280nm处有最大的吸收峰,盐和小分子则集中在230nm处,对于纯的核酸溶液,测定A260,即可利用核酸的比吸光系数计算溶液中核酸的量,核酸的比吸光系数是指浓度为1μg/mL的核酸水溶液在260nm处的吸光率,天然状态的双链DNA的比吸光系数为0.020,变性DNA和RNA的比吸光系数为0.022。
据朗波-比尔光吸收定律A=-lgT=εbc知,c=A/εb,而b通常为1cm,所以,通常以1OD值相当于50μg/mL双螺旋DNA,或40μg/mL单螺旋DNA(或RNA),或20μg/mL寡核苷酸计算。
2.2 纯度DNA和RNA的纯度可以通过测定260nm,230nm和280nm的紫外吸收值来测定,纯的DNA OD260/280在1.8-1.9,OD260/230应大于2.0,纯的RNA OD260/280在1.9-2.0,如果DNA比值高于1.8-1.9,可能有RNA没有去除干净,如果DNA比值小于1.8-1.9,可能含有酚或者蛋白质(RNA中含有酚或者蛋白质比值也会降低),若OD260/230小于2.0说明有残存的盐或小分子杂质污染。
2.3 浓度DNA和RNA的量,据朗波-比尔光吸收定律A=-lgT=εbc知测量样品的浓度为c=A/εb,又知ε=0.020,在b=1cm的情况下,c=A/(0.020×1)=50×A,则未稀释的样品的浓度为50×A×稀释倍数(μg/mL)=50×A×稀释倍数/1000(mg/mL)2.4 注意事项:1) 比色杯应为石英杯,玻璃杯在此波长时读数不准。
2) 检测时应使OD260值在0.15 到1.0之间,数值比较准确。
3) 这种比值测定的方法仅仅适用于核酸浓度大于0.25ul/ml的时候,浓度小于0.25ul/ml 的时候测量误差较大。
4) 既含有RNA又含有蛋白质也可能使比值维持在1.8,这个时候要根据电泳情况鉴定是不是含有RNA,或者测定一下是不是含有蛋白质;5) A260/A280比值可提供DNA纯度的一个参考,但A260/A280 比值会受pH影响。
如果未调pH,比值可能与实际差别很大。
