CSCO肺癌诊疗指南2018
原发性肺癌诊疗规范(2018年版)

原发性肺癌诊疗规范(2018年版)一、概述原发性肺癌(primary lung cancer,PLC)是世界范围内最常见的恶性肿瘤。
从病理和治疗角度,肺癌大致可以分为非小细胞肺癌(non small cell lung cancer,NSCLC)和小细胞肺癌(small cell lung cancer,SCLC)两大类,其中非小细胞肺癌约占80%~85%,其余为小细胞肺癌。
由于小细胞肺癌独特的生物学行为,治疗上除了少数早期病例外,主要采用化疗和放疗结合的综合治疗。
如果没有特别说明,肺癌指代非小细胞肺癌。
肺癌是我国30年来发生率增长最快的恶性肿瘤,20世纪70年代中期开展的我国第一次死因回顾调查资料表明,当时我国肺癌死亡率为5.47/10万,在癌症死因中,排在胃癌、食管癌、肝癌和宫颈癌之后,居第5位,占全部癌死亡的7.43%。
我国第二次死因抽样调查结果显示,20世纪90年代肺癌死亡率已居癌症死因第3位,仅次于胃癌和食管癌。
在21世纪开展的第三次死因回顾调查则显示肺癌已居癌症死亡原因首位。
根据全国肿瘤登记中心的最新统计数据提示:我国2011年新增肺癌病例约65万例,有52万例死于肺癌,两者均排名恶性肿瘤的第一位。
全国肿瘤登记中心2016年发布数据显示,2015年我国新发肺癌病例73.33万(男性50.93万,女性22.40万),居恶性肿瘤首位(男性首位,女性第2位),占恶性肿瘤新发病例的17.09%(男性20.27%,女性12.59%)。
同期,我国肺癌死亡人数为61.02万(男性43.24万,女性17.78万),占恶性肿瘤死因的21.68%(男性23.89%,女性17.70%)。
地区分布上,我国城市肺癌死亡率均高于农村地区。
东、中部城市和农村肺癌死亡率明显高于西部。
发病年龄>40岁人群死亡率快速升高。
二、筛查和诊断(一)肺癌的危险因素由于我国工业化不断发展导致空气污染日益加重,加之烟草流行率全球最高以及老龄化等因素的影响,肺癌的发病率和死亡率越来越高。
2018版 肺癌治疗方案总结 诊疗规范 CSCO指南 NCCN指南
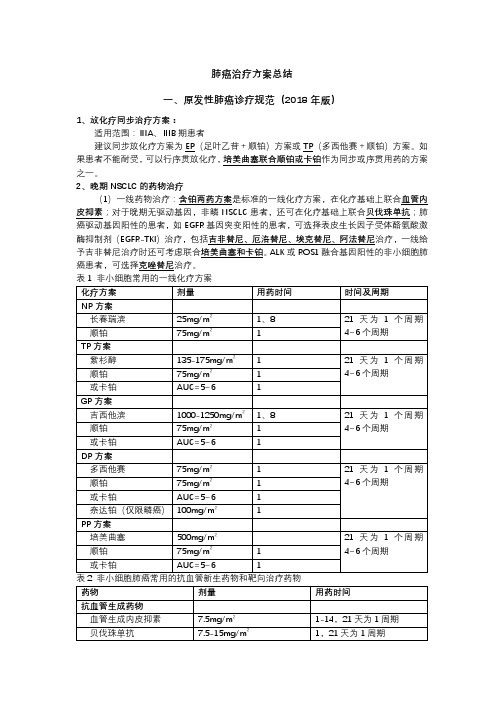
肺癌治疗方案总结一、原发性肺癌诊疗规范(2018年版)1、放化疗同步治疗方案:适用范围:ⅢA、ⅢB期患者建议同步放化疗方案为EP(足叶乙苷+顺铂)方案或TP(多西他赛+顺铂)方案。
如果患者不能耐受,可以行序贯放化疗,培美曲塞联合顺铂或卡铂作为同步或序贯用药的方案之一。
2、晚期NSCLC的药物治疗(1)一线药物治疗:含铂两药方案是标准的一线化疗方案,在化疗基础上联合血管内皮抑素;对于晚期无驱动基因,非鳞NSCLC患者,还可在化疗基础上联合贝伐珠单抗;肺癌驱动基因阳性的患者,如EGFR基因突变阳性的患者,可选择表皮生长因子受体酪氨酸激酶抑制剂(EGFR-TKI)治疗,包括吉非替尼、厄洛替尼、埃克替尼、阿法替尼治疗,一线给予吉非替尼治疗时还可考虑联合培美曲塞和卡铂。
ALK或ROS1融合基因阳性的非小细胞肺癌患者,可选择克唑替尼治疗。
对一线治疗达到疾病控制(完全缓解、部分缓解、稳定)的患者,可选择维持治疗。
目前同药维持治疗的循证医学证据支持的药物有培美曲塞(非鳞癌)、贝伐珠单抗(非鳞癌)和吉西他滨;有循证医学证据支持的换药维持治疗的药物有培美曲塞(非鳞癌),对于EGFR 基因敏感突变患者可以选择EGFR-TKI进行维持治疗。
(2)二线药物治疗:二线治疗可选择的药物包括多西紫杉醇、培美曲塞、纳武单抗、EGFR-TKI和克唑替尼。
肺癌驱动基因突变阳性的患者,如果一线维持治疗时没有应用相应的分子靶向药物,二线治疗时应优先应用分子靶向药物;一线EGFR-TKI治疗后耐药并且EGFR T790M突变阳性的患者,二线治疗时应优先使用奥希替尼。
对于ALK阳性,一线接受克唑替尼治疗后出现耐药的患者,二线治疗时可序贯使用塞瑞替尼。
对于一线接受EGFR-TKI或者克唑替尼治疗出现耐药,二线接受化疗治疗的患者,可根据患者的ECOG PS评分选择含铂双药或者单药治疗方案。
对于驱动基因阴性的患者,应优先考虑化疗,对于无驱动基因且组织学类型为鳞癌的患者,可选择使用阿法替尼(表3)。
2018 CSCO肺癌指南更新说明

原发肿瘤和转移灶都适于进行EGFR突变/ALK融合/ROS1融合分子 检测[13]
原发肿瘤和转移灶都适于进行EGFR突变/ALK融合分子 检测[11]
为了避免样本浪费和节约检测时间,对于晚期NSCLC活检样本,应 根据所选用的技术特点,一次性切出需要诊断组织学类型和进行
EGFR突变/ALK融合/ROS1融合检测的样本量,避免重复切片浪费 样本;如果样本不足进行分子检测,建议进行再次取材,确保分子
*(2B类证据)[23-29]
#新辅助治疗模式包括:单纯化疗、序贯化放疗、同步放化疗、化疗后同步放化疗等,最佳模式尚未确定[13-17]。 *术后病理N2可以考虑术后放疗(2B类证据)或加入术后放疗随机分组研究[23-29]。
3. 可手术IIIA期原发性NSCLC的治疗
总体推荐:临床IIIA期NSCLC (经PET/CT、EBUS或纵隔镜进行淋巴结分期)
ADJUVANT
吉非替尼 (n=111):中位28.7个月 长春瑞滨+顺铂 (n=111):中位18.0个月
100
HR=0.60
95%Cl 0.42,0.87
80
P=0.005
3年DFS率
60
34% vs 27%
EVAN
厄洛替尼 (n=46):中位42.41个月 长春瑞滨+顺铂(n=33):中位21.19个月
• T790M检测:对于EGFR TKIs耐药病例,建议二次组织活 检进行继发耐药EGFR T790M检测(ARMS或Super ARMS 法)[22]。EGFR-TKIs耐药后不能获取组织的患者,建议行血 液ctDNA EGFR T790M检测(ARMS或Super ARMS法) (1A类证据)[23-26]
2018CSCO肺癌指南更新说明

T790M突变是一代EGFR-TKI主要耐药机制之一,占比超过50%,三代
EGFR-TKI奥希替尼作用于该靶点,AURA3[23]已证实可有效治疗EGFR-TKI 治疗进展伴T790M突变患者,奥希替尼在中国已获CSFDA批准用于T790M 阳性的一代EGFR-TKI耐药患者。研究报道血浆ctDNA可用来检测T790M突 变[24],可作为二次活检组织标本不可获取的替代标本,同时也是对可以组织
原发肿瘤和转移灶都适于进行EGFR突变/ALK融合/ROS1融合分子 检测[13]
原发肿瘤和转移灶都适于进行EGFR突变/ALK融合分子 检测[11]
为了避免样本浪费和节约检测时间,对于晚期NSCLC活检样本,应 为了避免样本浪费和节约检测时间,对于晚期NSCLC活
根据所选用的技术特点,一次性切出需要诊断组织学类型和进行
• 通过NGS技术对血GFR突变, KRAS突变,HER-2突变,ALK融合,ROS-1融合, BRAF V600E突变,RET融合,MET扩增和MET14外 显子跳跃突变等。(2B类证据)[36-43]
EGFR-TKI术后辅助治疗使 EGFR突变型N1N2 非鳞NSCLC患者获益
ADJUVANT
吉非替尼 (n=111):中位28.7个月 长春瑞滨+顺铂 (n=111):中位18.0个月
100
HR=0.60
95%Cl 0.42,0.87
80
P=0.005
3年DFS率
60
34% vs 27%
EVAN
厄洛替尼 (n=46):中位42.41个月 长春瑞滨+顺铂(n=33):中位21.19个月
Zhong WZ, et al. Lancet Oncol. 2018 Jan;19(1):139-148. Yue D, et al. 2017 WCLC OA16.04.
原发性肺癌诊疗规范(2018年版)

原发性肺癌诊疗规范(2018年版)一、概述原发性肺癌(primary lung cancer,PLC)是世界范围内最常见的恶性肿瘤。
从病理和治疗角度,肺癌大致可以分为非小细胞肺癌(non small cell lung cancer,NSCLC)和小细胞肺癌(small cell lung cancer,SCLC)两大类,其中非小细胞肺癌约占80%~85%,其余为小细胞肺癌。
由于小细胞肺癌独特的生物学行为,治疗上除了少数早期病例外,主要采用化疗和放疗结合的综合治疗。
如果没有特别说明,肺癌指代非小细胞肺癌。
肺癌是我国30年来发生率增长最快的恶性肿瘤,20世纪70年代中期开展的我国第一次死因回顾调查资料表明,当时我国肺癌死亡率为5.47/10万,在癌症死因中,排在胃癌、食管癌、肝癌和宫颈癌之后,居第5位,占全部癌死亡的7.43%。
我国第二次死因抽样调查结果显示,20世纪90年代肺癌死亡率已居癌症死因第3位,仅次于胃癌和食管癌。
在21世纪开展的第三次死因回顾调查则显示肺癌已居癌症死亡原因首位。
根据全国肿瘤登记中心的最新统计数据提示:我国2011年新增肺癌病例约65万例,有52万例死于肺癌,两者均排名恶性肿瘤的第一位。
全国肿瘤登记中心2016年发布数据显示,2015年我国新发肺癌病例73.33万(男性50.93万,女性22.40万),居恶性肿瘤首位(男性首位,女性第2位),占恶性肿瘤新发病例的17.09%(男性20.27%,女性12.59%)。
同期,我国肺癌死亡人数为61.02万(男性43.24万,女性17.78万),占恶性肿瘤死因的21.68%(男性23.89%,女性17.70%)。
地区分布上,我国城市肺癌死亡率均高于农村地区。
东、中部城市和农村肺癌死亡率明显高于西部。
发病年龄>40岁人群死亡率快速升高。
二、筛查和诊断(一)肺癌的危险因素由于我国工业化不断发展导致空气污染日益加重,加之烟草流行率全球最高以及老龄化等因素的影响,肺癌的发病率和死亡率越来越高。
2018 版 CSCO 肺癌指南更新主要内容

2018版CSCO肺癌指南更新主要内容2018年4月21日,中国临床肿瘤学会(CSCO)指南会在南京召开。
原发性肺癌诊疗指南是CSCO发布的第一个指南,2016年首次发布,本次已迎来第2次更新。
整个指南凸显了精准医学的特点,旨在推进中国肿瘤治疗的规范化。
大会上,北京大学肿瘤医院的林冬梅教授、天津大学肿瘤医院的岳东升教授、中国医学科学院肿瘤医院的王志杰教授及广东省人民医院的周清教授分别对指南的更新进行了解读。
那么,2018版《CSCO原发性肺癌诊疗指南》中究竟更新了哪些内容?又是基于哪些证据呢?让我们一起来看一下。
分子分型部分的更新指南新增推荐相对早期(I〜IIIA期)非小细胞肺癌(NSCLC)进行分子检测(1B类证据),主要基于ADJUVANT和EVAN硏究中靶向药物辅助治疗获益的数据。
推荐对于I〜IIIA期NSCLC、N1/N2阳性的非鳞癌患者进行EGFR 突变检测(1B类证据)。
对于晚期NSCLC患者,除了过去推荐的EGFR和ALK检测,本次更新增加了ROS1重排的检测推荐。
EGFR突变的检测可采用ARMS或SuperARMS法(1类证据)。
ALK融合基因的检测可采用Ventana免疫组化、FISH或RT-PCR的方法(1类证据)。
ROS1融合基因的检测可采用RT-PCR或FISH的方法(1B类证据)随着EGFRTKIs继发性耐药和三代TKI的出现,推荐对EGFRTKIs耐药患者进行EGFRT790M检测。
组织学检测为金标准,在组织不可获取时,血液ctDNAEGFRT790M检测可作为有效补充(1A类证据)。
检测方法上,除了CFDA批准的试剂盒外,也可基于中国现有的检测平台使用Cobas、ddPCR、NGS等方法,并以血液检测作为组织检测的补充。
但是融合基因的血液检测技术尚不成熟,故仍应尽可能进行组织学检测。
而由于NGS的成本高,检测规范性、可靠性欠佳,指南将其列为可推荐但推荐级别不高。
基于病理类型、分期和分子分型的综合治疗部分的更新1.NSCLC治疗的更新(1)IA、IB期原发性NSCLC的治疗仍推荐进行解剖性肺叶切除(1类证据)+肺门纵隔淋巴结清扫术(2A类证据)。
中国原发性肺癌诊疗规范2018年版
中国原发性肺癌诊疗规范
(2018年版)
2019-04-12
目录
CONTENTS
一.概述 二.早期筛查 三.诊断与分期 四.手术治疗 五.放射治疗
六.化疗与靶向治疗 七.肺癌的分期治疗模式 八.诊疗流程与随访 .
Motic
概述
? 原发性肺癌(以下简称肺癌)是我国最常见的恶性肿瘤 之一
? 全国肿瘤登记中心 2016年发布数据显示, 2015年我国新 发肺癌病例 73.33万(男性50.93万,女性22.40万),居 恶性肿瘤首位(男性首位,女性第 2位),占恶性肿瘤新 发病例的17.09% (男性20.27%,女性12.59%)。
Motic
胸部CT检查
? 是目前肺癌诊断、分期、疗效评价及治疗后随诊中最重 要和最常用的影像手段。
? 肺癌初诊患者胸部 CT扫描范围应包括双侧肾上腺。 ? 对于难以定性诊断的胸部病变,可采用 CT引导下经皮肺
中国肺癌低剂量螺旋CT筛查指南(2018年版)

周清华和范亚光为共同第一作者 本研究受国家重大研发计划项目(No.2016YFE0103400)资助 作者单位:610041 成都,四川大学华西医院肺癌中心/肺癌研究所(周清华);300052 天津,天津医科大学总医院肺癌研究所(周清华,范亚 光,王颖,王新允,韦森);610041 成都,中国肺癌早诊早治专家组(周清华,范亚光,乔友林,王贵齐,黄云超,王新允,吴宁);100021 北京,中国医学科学院肿瘤医院/国家癌症中心(乔友林,王贵齐,吴宁,石远凯,孙燕);650105 昆明,云南省肿瘤医院(黄云超);200040 上海,上海华东医院(张国桢,郑向鹏);610041 成都,四川大学华西医院病理科(步宏);450008 郑州,河南省肿瘤医院(李印);100853 北京,中国人民解放军总医院(陈良安);410008 长沙,中南大学湘雅医院(胡成平)(通讯作者:周清华,E-mail: zhouqh135@;孙 燕,E-mail: suny@)
Cancer Institute, Tianjin Medical University General Hospital, Tianjin 300052, China; 3China National Expert Group of Early Diagnosis and Treatment of Lung Cancer, Chengdu 610041, China; 4Cancer Hospital, Chinese Academy of Medical Sciences/China National Cancer Center, Beijing 100021, China; 5Cancer Hospital of Yunnan Province, Kunming 650105, China; 6Shanghai Huadong Hospital, Shanghai 200040, China; 7Department of Pathology, West China Hospital, Sichuan University, Chengdu 610041, China; 8Cancer Hospital of Henan Province, Zhengzhou 450008, China; 9General Hospital of People’s Liberation Army, Beijing 100853,
2018肺癌诊疗指南

1 概述3.1 肺癌的危险因素3.1.1 吸烟20世纪50年代首先发现吸烟与肺癌的关系,并提出了"吸烟可导致肺癌"的重要推论。
大量调查结果表明,吸烟和许多癌症发生有密切关系,尤以肺癌为甚。
通常认为,吸烟与鳞状细胞癌和小细胞癌的关系相对更为密切。
肺癌发生的高峰期往往滞后于吸烟高峰期,开始吸烟年龄越小、每日吸烟量越大、持续时间越长,引起肺癌的相对危险度越高。
被动吸烟也会增加肺癌的发生。
3.1.2 环境污染广义的环境污染包括室外大环境污染和室内小环境污染。
各种农业、工业废气、粉尘、汽车尾气等可导致呼吸系统疾病上升及心肺疾病死亡率的上升。
室内污染也是导致肺癌发生不容忽视的原因,例如室内烹饪燃烧的烟煤释放的大量苯并芘,其可导致肺癌发病率升高。
3.1.3 职业暴露长期接触铀、镭等放射性物质和石棉、氡、砷及其化合物等高致癌物质者更易罹患肺癌。
对于发达国家的非吸烟人群而言,氡是仅次于被动吸烟的室内致肺癌发生因素;另外,经常接触柴油废气者的肺癌发病率也会升高。
3.1.4 肺癌家族史及既往肿瘤史这类人群往往可能携带有异常基因改变。
在目前尚无可靠的肺癌基因筛查系统和公认方法时,更应关注患者的肺癌家族史及既往罹患肿瘤史。
有证据表明,一级亲属被诊断肺鳞状细胞癌的个体患肺癌的风险度明显升高。
3.1.5 年龄在我国,45岁以下人群肺癌发病率相对较低,45岁及以上人群呈现明显增加趋势。
3.1.6 其他肺结核、慢性阻塞性肺疾病、尘肺等慢性肺部疾病患者肺癌发病率高于健康人。
肺支气管慢性炎症及肺纤维瘢痕病变在愈合过程中的鳞状上皮化生或增生可能发展成肺癌。
3.2 肺癌的临床表现周围型肺癌早期可无明显症状,随着病情的发展,可出现相应的呼吸道症状或转移相关症状。
3.2.1 原发肿瘤表现(1)咳嗽、咳痰:咳嗽是肺癌患者就诊时最常见的症状,早期常表现为刺激性咳嗽,如果肿瘤增大影响到痰液引流,可继发阻塞性肺炎。
(2)痰血与咯血:由于肿瘤组织血管常较为丰富,部分患者肿瘤坏死可出现痰血,如果肿瘤侵袭较大血管,可引起咯血。
中华医学会肺癌临床诊疗指南(2018版)

中华医学会肺癌临床诊疗指南(2018版)1 概述原发性支气管肺癌简称肺癌,起源于支气管黏膜上皮及肺泡,是我国及世界范围内发病率和死亡率最高的恶性肿瘤之一,严重危害人类健康。
在我国,随着工业化、城市化的进展所致的空气污染以及吸烟率的居高不下,肺癌的发病率和死亡率仍呈明显上升趋势。
据我国国家癌症中心统计,2014年我国肺癌发病率和死亡率均居首位,其中新发病例约78.1万,死亡病例约62.6万;男性高于女性,城市高于农村;发病率和死亡率亦存在区域差异,由高到低依次为东部、中部和西部。
早期肺癌多无明显症状,多数患者确诊时已属晚期,致肺癌整体5年生存率仅为16 %左右。
因此,在减少危险因素、发现高危人群、进行高危人群早期筛查、早期诊断以及对晚期肺癌进行除了病理检测以外的基因和分子分型的精准诊断和治疗等方面,制定诊疗指南是当务之急。
近年来,肺癌的诊断和治疗进展迅速。
对于早期肺癌,人们日益追求精细且创伤性更小的手术方式;对于晚期肺癌,靶向治疗深入人心,免疫治疗的出现给野生型肺癌患者带来了新的希望,肺癌患者的治疗选择较前显著增多。
为进一步提高我国肺癌的诊疗水平、改善患者的预后、给各级临床医师提供专业的循证医学意见,中华医学会组织全国的专家,整合近年来肺癌病理、基因检测、免疫分子标志物检测、新治疗手段等最新研究成果,并结合中国的国情,制定了此中国肺癌诊疗指南。
循证医学和精准医学是制定此指南的基本原则。
目前国际指南是基于当前国际上最新的研究结果和证据。
中国是一个发展中国家,必须考虑到药物和治疗措施的可及性。
欧美国家已批准上市的药物在我国可能一段时间内尚不可及,我国不同区域因发展的不平衡,在治疗的选择上存在差异,因此,结合国际指南和我国的国情,本专家组制定了中国肺癌临床诊疗指南。
根据循证医学级别进行了分类推荐,共分4个级别:1类推荐证据级别最高,为专家组一致推荐;2A类推荐证据级别稍低,为专家组一致推荐;2B类推荐证据级别低,为部分专家推荐;3类推荐证据为专家分歧较大。
CSCO肺癌指南更新说明ppt课件

EGFR突变/ALK融合的检测应在患者诊断为晚期NSCLC 时立即进行,早期患者演变为IV期时也应进行EGFR突 变/ALK融合的检测[11] 原发肿瘤和转移灶都适于进行EGFR突变/ALK融合分子 检测[11] 为了避免样本浪费和节约检测时间,对于晚期NSCLC活 检样本,应根据所选用的技术特点,一次性切出需要诊 断组织学类型和进行EGFR突变/ALK融合检测的样本量, 避免重复切片浪费样本;如果样本不足进行分子检测, 建议进行再次取材,确保分子检测有足够样本
EVAN
厄洛替尼 (n=46):中位42.41个月 长春瑞滨+顺铂(n=33):中位21.19个月 中位OS HR=0.327 95%Cl 0.160,0.669 P=0.002 2年DFS率 80.39% vs 47.54%
80
60 40
20
0
辅助2年的EGFR-TKI治疗较化疗显著延长DFS,显著降低疾病复发风险
• 对于血液ctDNA的检测方法除ARMS和Super ARMS法 之外,还包括cobas、微滴式数字PCR(ddPCR)和高通 量二代测序(NGS)。
• 通过NGS技术对血液或组织进行检测,可高效确定全 部具有临床意义的目标靶点变异如:EGFR突变, KRAS突变,HER-2突变,ALK融合,ROS-1融合, BRAF V600E突变,RET融合,MET扩增和MET14外 显子跳跃突变等。(2B类证据)[36-43]
中国临床肿瘤学会 (CSCO) 原发性肺癌诊疗指南 2018版:更新说明
更新的主要内容
分子分型
基于病理类型、分期和分子分型的综合治疗
随访
分子分型
• I~IIIA期NSCLC手术后采用组织进行分子检测,根据分子分型指导治疗 (1B类证据)
2018年肺癌诊疗指南解读(LF)

病率与死亡率亦存在区域差异,由高到低依次为东部、中部、西部。
早期肺癌多无明显症状,多数患者确诊时已属晚期,致肺癌整体5年生 存率仅为16%。
3、证据级别:
级别 1类推荐 2类推荐 A
B 3类推荐
推荐等级 证据级别最高,专家组一致推荐 级别稍低,专家组一致推荐 级别低,部分专家推荐 专家分歧较大
高、全身一次成像、不易漏诊的特点。
诊。
是肺癌诊断、分期与再分期、放疗靶区勾画、疗效和 预后评估的最佳方法之一。
对脑和脑膜转移敏感性相对 较差,对于需排除有无脑转 移的患者,建议与脑部增强 MRI联合,以提高诊断率。
三、肺癌的诊断
4、获取肺癌组织学或细胞学的检查方法:
痰液细胞学检查 胸腔穿刺术 浅表淋巴结及皮下转移结节活组织检查 经胸壁肺穿刺术 纤维支气管镜检查 经支气管针吸活组织检查术
癌胚抗原(CEA)
常
用 的
神经元特异性烯醇化酶(NSE)
肺
细胞角蛋白片段19
癌
(CYFRA21-1)
标
胃泌素释放肽前体
志
(ProGRP)
物
鳞状上皮细胞癌抗原
(SCC)
三、肺癌的诊断
5、肺癌的实验室血清学检查
辅助诊断: • 肺癌的诊断通常需要结合影像学和病理学检查。肺癌血清肿瘤标
志物上午灵敏度和特异度还不高,但肺癌患者血清肿瘤标志物的 升高可早于一些临床症状的出现,因此临床诊断时可根据需要检 测相关肿瘤标志物。 • 意义:标志物水平较高提示肿瘤处于发展期,其水平与肿瘤的大 小和分期有一定关联。首次诊断及开始治疗前升高的标志物水平 对于以后的监测治疗有重要意义。治疗后的标志物水平可为肿瘤 的疗效判断等提供信息,提示预后。
2018版CSCO恶性肿瘤诊疗指南公布

2018版CSCO恶性肿瘤诊疗指南公布南京——2018年4月21日,中国临床肿瘤学会(CSCO)于南京召开了CSCO指南会,近千名来自全国各肿瘤领域的临床工作者,参加了会议,交流研究结果,见证指南更新。
4月21日早上8点,CSCO召开了新闻发布会,CSCO理事长李进教授,学会领导秦叔逵教授、吴一龙教授、梁军教授、徐瑞华教授、王绿化教授、程颖教授,秘书长江泽飞教授、郭军教授,出席新闻发布会并回答记者提问。
为积极响应建设“健康中国”的伟大部署,配合国家医药、卫生行政部门和社会保障部门进一步做好肿瘤防治工作,推动全国临床肿瘤学科的规范化建设,帮助各级医务人员提高诊治和研究水平,CSCO 本着“兼顾地区发展不平衡、兼顾药物和治疗措施的可及性、兼顾肿瘤治疗价值”基本原则及核心思想,制定一系列常见恶性肿瘤诊疗指南。
2016年,CSCO首次发布肺癌诊疗指南,2017年,CSCO发布了包括结直肠癌、乳腺癌、胃癌和恶性黑色素瘤等4种常见恶性肿瘤诊疗指南,指南发布以来,受到专业人士和社会各界的广泛认可。
2018年,CSCO指南工作委员会将更新肺癌、乳腺癌、胃癌、结直肠癌指南,同时还将新发布肾癌、头颈肿瘤、甲状腺癌、肉瘤、胰腺癌、肝癌、血液肿瘤、食管癌等八个指南。
CSCO指南特点基于循证医学证据、兼顾诊疗产品的可及性、吸收精准医学新进展,制定中国常见癌症的诊断和治疗指南,是CSCO的基本任务之一。
近年来,国际指南的制定出现了一个新趋向,即更多地考虑诊疗资源的可及性,这尤其适合发展中国家和地区差异性显著的国家及地区,CSCO指南需要兼顾地区发展差异、药物和诊疗手段的可及性以及肿瘤治疗的社会价值三个方面。
CSCO指南的具体特点可以概括为:针对恶性肿瘤的诊疗问题,以前分为基本策略和可选策略,基本策略属于可及性好的普适性诊疗措施,可选策略属于在国际或国内已有高级别证据,但可及性差或效价比超出国人承受能力的药物或质量措施,或临床实用但证据等级不高的措施。
2018年版CSCO肺癌指引

2017版CSCO肺癌指南2017年4月22日,中国临床肿瘤学会(CSCO)指南发布会在广州举行。
CSCO副理事长、吉林省肿瘤医院院长程颖教授就《CSCO原发性肺癌诊疗指南》2017年更新版进行了解读。
那么,2017版《CSCO原发性肺癌诊疗指南》中究竟更新了哪些内容?又是基于哪些证据呢?让我们一起来看一下。
在影像和分期诊断部分、病理学诊断部分以及随访部分,内容没有变化。
分子分型部分的更新在基本策略中,非鳞癌除了EGFR 和ALK 融合基因检测外,新增加了耐药后行二次活检对继发耐药T790M 进行检测,不能行组织学检测的患者可行血液ctDNA T790M 检测(I类证据)。
可选策略中,增加了ROS1融合基因RT-PCR检测(从IIA类提到IB证据)。
更新ROS1检测方法,主要是基于吴一龙教授牵头的东亚ROS1 阳性患者的II 期研究,入组127例病人,其中中国患者74例,使用RT-PCR方法,阳性患者使用克唑替尼治疗。
其中CR 14例,PR 74例,ORR 69.3%, PFS 13.4个月,ROS1成为克唑替尼治疗有效的第二个分子类型。
基于病理类型,分期和分子分型的综合治疗部分的更新1.非小细胞肺癌(NSCLC)治疗的更新(1)不可手术的IIIA或IIIB期NSCLCPS 0-1 者新增加了同步放化疗证据。
证据来自于王绿化教授的III 期研究,比较依托泊甙/ 顺铂和紫杉醇/ 卡铂同步放化疗随机对照研究,3 年OS 率分别是41.4% 和26.0%,因此推荐依托泊甙/顺铂为IIIA或IIIB期不能手术患者的优选同步放化疗方案。
(2)IV期EGFR突变患者的一线治疗PS 0-3 分者,按照上市时间,在基本策略里推荐吉非替尼,埃克替尼,厄洛替尼和阿法替尼,其中阿法替尼是今年增加的证据。
可选策略里,PS 0-1分者增加了联合化疗循证医学依据。
此推荐基于JMIT研究,EGFR突变患者使用吉非替尼培美曲塞,PFS达到近16个月。
2018年肺癌诊疗指南解读(LF)

2B类推荐 1类推荐 2A类推荐
五、肺癌的治疗 (二)、III期NSCLC患者的综合治疗
1、可切除类III期NSCLC--手术原则
推荐 在完全切除肿瘤的基础上尽可能保留肺组织 在术前充分评估的基础上,根据肿瘤浸润范围可进行肺 叶、复合肺叶、袖状以及全肺切除,推荐到有条件的大 型医院进行此类手术 证据等级 1类推荐 2A类推荐
同期多原发癌:
五、肺癌的治疗 (二)、III期NSCLC患者的综合治疗
III期NSCLC是一类异质性明显的疾病,根据国际肺癌研究学会第8版III 期非小细胞肺癌分为IIIa、IIIb、IIIc期。
IIIb、IIIc
归为不可切除的III期NSCLC,治疗以根治性同步 放化疗为主要治疗方式(1类推荐证据)。
优点
最基本的影像学检查方法,包括胸部正、侧位片。价 格便宜。 可以有效检出早期周围性肺癌,进一步验证病变所在 部位和累计范围,可以帮助鉴别恶性程度,是目前肺 癌诊断、分期、疗效评价及治疗后随访中最重要和最 常见的影像学手段。 对椎体及骨转移灵敏度和特异度均较高 常用于检查腹部重要器官有无转移,也可检查有无胸 膜转移、胸腔积液及心包积液。
小细胞肺癌 临床表现
非小细胞肺癌
鳞状细胞癌 腺癌 大细胞肺癌 大细胞肺癌 小细胞肺癌 鳞状细胞癌 腺癌
神经内分泌肺癌
内分泌成分
非神经内分泌肺癌
三、肺癌的诊断
5、肺癌的实验室血清学检查
常 用 的 肺 癌 标 志 物
癌胚抗原(CEA)
神经元特异性烯醇化酶(NSE) 细胞角蛋白片段19(CYFRA21-1) 胃泌素释放肽前体(ProGRP)
IIIa期可手术的NSCLC术后推荐辅助含铂两药化疗
不常规推荐术后辅助放疗,建议进行多学科会诊,评估 术后辅助放疗对于N2患者的治疗获益与风险 对于术后发现驱动基因阳性的患者,可行术后辅助EGFRTKI靶向治疗
中国临床肿瘤学会CSCO原发性肺癌诊疗指引2018版更新说明

20
0
辅助2年的EGFR-TKI治疗较化疗显著延长DFS,显著降低疾病复发风险
Zhong WZ, et al. Lancet Oncol. 2018 Jan;19(1):139-148. Yue D, et al. 2017 WCLC OA16.04.
分子分型 总体推荐 – 注释部分的更新 (1)
• T790M检测:对于EGFR TKIs耐药病例,建议二次组织活 检进行继发耐药EGFR T790M检测(ARMS或Super ARMS 法)[22]。EGFR-TKIs耐药后不能获取组织的患者,建议行血 液ctDNA EGFR T790M检测(ARMS或Super ARMS法) (1A类证据)[23-26] • ALK融合Ventana免疫组化或FISH或RT-PCR检测 (1类证 据)[8-13,27-30] • ROS1融合RT-PCR或FISH法检测(1B类证据)[12,13,18,31-35 ]
尤其在标本量有限的情况下,可采用同时检测多个驱动 基因的技术,如PCR技术或NGS技术
EGFR突变/ALK融合的检测应在患者诊断为晚期NSCLC 时立即进行,早期患者演变为IV期时也应进行EGFR突 变/ALK融合的检测[11] 原发肿瘤和转移灶都适于进行EGFR突变/ALK融合分子 检测[11] 为了避免样本浪费和节约检测时间,对于晚期NSCLC活 检样本,应根据所选用的技术特点,一次性切出需要诊 断组织学类型和进行EGFR突变/ALK融合检测的样本量, 避免重复切片浪费样本;如果样本不足进行分子检测, 建议进行再次取材,确保分子检测有足够样本
*术后病理N2可以考虑术后放疗(2B类证据)或加入术后放疗随机分组研究[23-29]。
3. 可手术IIIA期原发性NSCLC的治疗
原发性肺癌诊疗规范(2018版)

31
三、肺癌的病理分型和分期
(一)世卫组织2015年肺癌组织学分型标准 8.免疫组化和特殊染色 腺鳞癌 肉瘤样癌 小涎腺来源的癌
精选可编辑ppt
32
三、肺癌的病理分型和分期
(二)肺癌的分期 •T分期(原发肿瘤) •N-区域淋巴结 •M-远处转移 •临床分期
精选可编辑ppt
33
四、肺癌的治疗
(二)肺癌的分期 •多学科综合治疗与个体化治疗相结合 •(一)外科治疗 •肺切除术是早中期肺癌的主要治疗手段,也是目前临床治愈肺癌 的重要方法。 完全性切除、不完全性切除和不确定性切除。
• (三)药物治疗 • 化疗(新辅助化疗、辅助化疗、姑息化疗) • 分子靶向治疗 • 免疫治疗
精选可编辑ppt
42
四、肺癌的治疗
• (三)药物治疗 • 1.晚期NSCLC的药物治疗 • 2.不能手术切除的NSCLC的药物治疗 • 3.NSCLC的围手术期药物治疗 • 4.SCLC的药物治疗 • 5.肺癌化疗的原则
精选可编辑ppt
34
四、肺癌的治疗
• (一)外科治疗 • 1.支气管和肺系统的外科解剖 • 2.肺癌手术适应症 • 3肺癌手术禁忌症 • 4.肺癌的完全切除概念 • 5.肺癌的淋巴结清扫
精选可编辑ppt
35
四、肺癌的治疗
•(一)外科治疗 •6.肺癌外科手术概述 完全切除手术(根治性切除术) 不完全切除手术(姑息性切除术) 7.肺癌外科并发症
精选可编辑ppt
19
• 影像学分型根据肺癌发生部位
• 中央型:鳞状细胞癌、小细胞癌 • 周围型:直径≤1cm的局限病变称为小结节, 1cm<直径≤3cm的
局限病变称为结节,而直径>3cm者称为肿物。
