厦门大学化学系考研解析
厦门大学839无机化学(海洋化学)2010年考研专业课真题答案解析

《厦门大学839无机化学历年考研真题及答案解析》15/52Ⅱ历年考研真题试卷答案解析厦门大学2010年招收攻读硕士学位研究生入学考试试题答案解析科目代码:839科目名称:无机化学招生专业:海洋化学考生须知:答案必须使用墨(蓝)色墨水(圆珠)笔;不得在试卷(草稿)纸上作答;凡未按规定作答均不予评阅、判分一、(18分)判断下列说法是否正确?说明理由。
(1)主量子数n 为3时有3s ,3p ,3d ,3f 四条轨道。
【考查重点】:这是原子结构内容,考查主量子数、角量子数等。
【答案解析】:这一说法是错误的,主量子数n 为3时有3s ,3p ,3d 共有9个轨道。
(2)氧原子数的2s 轨道的能量与碳原子的2s 轨道的能量相同。
【考查重点】:这是原子结构内容,考查主量子数、角量子数等。
【答案解析】:这一说法是错误的。
虽然都是2s 轨道,但是由于不同原子原子核中质子数是不相同的,核外电子也不相同,因此氧原子和碳原子的2s 轨道能量是不同的。
(3)中心原子的几个原子轨道杂化时,必形成数目的杂化轨道。
【考查重点】:这是分子结构的内容,考查杂化轨道理论。
【答案解析】:这一说法是正确的。
形成的杂化轨道数与参与杂化的原子轨道数目是一样的。
(4)在某温度下,密闭容器中反应222(g)+O (g)2(g)NO NO 达到平衡,当保持温度和体积不变充入惰性气体时,总压将增加,平衡向气体分子数减少即生成2NO 的方向移动。
【考查重点】:这是化学平衡内容,考查加入惰性气体对平衡移动的影响。
【答案解析】:这一说法是错误的。
T 、V 一定时,充入惰性气体,由于体积不变,反应体系中的物质。
厦门大学物化考研试题分析研究

厦门大学物理化学考研试题分析研究一、历年考题所考查各章节的分数分布情况:气体0热力学第一定律 6 热力学第二定律 6 多组分系统热力学 5 相平衡 18化学平衡15 统计热力学基础 4 电化学 34界面现象10化学动力学38胶体化学 2其他7二、2005-2011期间各章节所考查知识点的统计:⑴气体:范德华方程⑵热力学第一定律:绝热可逆膨胀过程、节流膨胀过程,对系统温度的影响;两者的P-T图的区别及在冷冻机的制冷过程中是如何应用的。
由生成焓求反应热;热量计算的综合知识运用;若已知臭氧催化分解主要是在冰晶或固体水合物表面进行,试根据有关热力学原理说明为什么南极上的臭氧层空洞较其他地方多。
节流膨胀过程中的转换温度;当温度与转换温度满足不同关系时,对节流膨胀过程温差正负的影响。
相变焓、相变过程中的熵变;两者能否应用于过程方向的判断。
三种获得低温的方法,比较优缺点;对确定过程的热力学函数变判断;热力学函数之间的计算;卡诺热机的应用-燃烧热转化为有用功的计算;⑶热力学第二定律:理想气体PVT过程焓变的计算,标准摩尔生成吉布斯自由能,标准摩尔生成焓变计算。
相变焓;等效过程设计;相变过程中的热力学函变;吉布斯判据;亥姆霍兹判据。
标准摩尔反应吉布斯自由能变与温度的关系图,及与反应方程式存在的对应关系;标准摩尔反应吉布斯自由能的计算;标准摩尔生成焓变、熵变的求法。
恒温条件下,可逆过程中系统对环境做最大功;最大功与吸收热的关系;体系经过一个不可逆过程对体系、环境熵的影响。
TdS=CvdT+T[δp/δT]dV;试问两物质应以什么比例,能获得最大混合熵;标准摩尔生成吉布斯自由能的求法;标准摩尔反应焓变的求法。
水在真空容器中汽化的热力学函变;热力学函变在生物化学中的应用。
对反应方向的判断;确定过程的热力学函数变计算。
⑷多组分系统热力学:稀溶液的依数性;活度,真实液态化合物的性质。
化学势;理想液体混合物;物质的量分数、质量分数与饱和蒸汽压的关系;拉乌尔定律;蒸气是理想气体与否,对溶剂标准吉布斯自由能变的影响。
《厦门大学827分析化学历年考研真题及答案解析》

(B) H3O+-OH-
(C) HPO42--PO43-
(D)NH3+CH2COOH-NH3+CH2COO-
4.卤化银对卤化物和各种吸附指示剂的吸附能力如下:二甲基二碘荧光黄>Br->曙
红>Cl->荧光黄。如用法扬司法分别测定 Br-和 Cl-时,应分别选择的指示剂是:( )
(A)二甲基二碘荧光黄和荧光黄 (B)二甲基二碘荧光黄和曙红
Ⅱ 历年考研真题试卷答案解析.............................................................................................37
厦门大学 2007 年招收攻读硕士学位研究生入学考试试题答案解析................................ 37 厦门大学 2008 年招收攻读硕士学位研究生入学考试试题答案解析................................ 45 厦门大学 2009 年招收攻读硕士学位研究生入学考试试题答案解析................................ 54 厦门大学 2010 年招收攻读硕士学位研究生入学考试试题答案解析................................ 61 厦门大学 2011 年招收攻读硕士学位研究生入学考试试题答案解析................................ 68 厦门大学 2012 年招收攻读硕士学位研究生入学考试试题答案解析................................ 75 厦门大学 2013 年招收攻读硕士学位研究生入学考试试题答案解析................................ 81 厦门大学 2014 年招收攻读硕士学位研究生入学考试试题答案解析................................ 95
厦大物理化学、有机化学考研经验

厦大物理化学、有机化学考研经验分享给学弟学妹考研结束,担子卸了,忽然觉得时间一下子多了,在家无事,便胡乱写一下自己在这半年来的心得体会,希望后来的学弟学妹能够有所借鉴。
对于自己为何选择厦大作为考研的学校,其实没有特别的原因。
不想转专业考研,太难太累人,也不喜欢有机实验室浓重的试剂气味,于是我便选了物理化学。
而厦大的物化还是很有名气的,而且比对了历年来厦大物化的考研收录比,大概3:1的样子,对于名校来说,是比较简单的了。
于是我便着手开始收集资料。
我的大部分资料都是在百度文库收集来的,上面你能够找到很多好心人发的资料,很全,像真题、物化题库、厦大的物化ppt等都能找到。
我是从7月份开始复习的,当时看了下物化的真题,觉得好难好难,潜意识里就产生了对它的恐惧心理。
其实从现在来看这种心理是恨不正确的。
厦大的物化有它自己的特色,题目很活,看上去很偏,很难,即使是南大那本教材的题目都能做,看到厦大的一些题目也会摸不着头脑。
这是因为厦大有它自己的出题方式,南大教材的课后习题是很经典的题目,而厦大的出题则会偏向于应用,我感觉13年的真题尤其是这样。
所以,在大概地看一遍南大的教材,打下基础之后,就要马上去看厦大的教材了。
厦大的两本教材很厚,内容也很多,很复杂,我在开始复习时翻了翻,觉得吃不消,就没怎么看,还是以南大的教材为主。
事实证明,厦大的教材需要尽早看,因为你在做厦大的课后习题时(建议大家一定要买那本与厦大教材配套的课后习题集,而且至少要做两遍,因为历年真题里很多题目就是从这里出的),会发现很多知识点都是南大那本教材没有涉及的,需要你去重新翻书,这样非常浪费时间,也不利于形成一个整体的知识框架。
我的建议是,尽早开始看厦大教材,看一章,做一章课后习题,有做笔记习惯的同学可以在看的过程中做下笔记,因为内容多,公式多,做了笔记之后再第二次看时能够省力一些。
第一次做题目时,有好些不会做,这是很正常的,不要烦躁,好在它有答案,根据自己的习惯在那些不会做的题目上做好记号,第二次做的时候再来解决。
新版厦门大学有机化学考研经验考研参考书考研真题

回首过去一年的各种疲惫,困顿,不安,怀疑,期待等等全部都可以告一段落了,我真的是如释重负,终于可以安稳的让自己休息一段时间了。
虽然时间如此之漫长,但是回想起来还是历历在目,这可真是血与泪坚坚实实一步步走来的。
相信所有跟我一样考研的朋友大概都有如此体会。
不过,这切实的果实也是最好的回报。
在我备考之初也是看尽了网上所有相关的资料讯息,如大海捞针一般去找寻对自己有用的资料,所幸的是遇到了几个比较靠谱的战友和前辈,大家共享了资料和经验。
他们这些家底对我来讲还是非常有帮助的。
而现如今,我也终于可以以一个前人的姿态,把自己的经验下下来,供大家翻阅,内心还是比较欣喜的。
首先当你下定决心准备备考的时候,要根据自己的实际情况、知识准备、心理准备、学习习惯做好学习计划,学习计划要细致到每日、每周、每日都要规划好,这样就可以很好的掌握自己的学习进度,稳扎稳打步步为营。
另外,复试备考计划融合在初试复习中。
在进入复习之后,自己也可以根据自己学习情况灵活调整我们的计划。
总之,定好计划之后,一定要坚持下去。
由于篇幅较长,还望各位同学能够耐心看完,在结尾处附上我的学习资料供大家下载。
厦门大学有机化学的初试科目为:(101)思想政治理论(201)英语一(619)有机化学(826)物理化学参考书目为:1、《有机合成》,黄培强等编著,高等教育出版社,北京:2004;2、《物理化学》(第四版),傅献彩、沈文霞、姚天扬编,高教出版社;3、《物理化学》,黄启巽、吴金添、魏光编著,厦门大学出版社,1996年;4、《物理化学》(第一版),韩德刚、高执棣、高盘良编,高教出版社,2002年5、《基础有机化学》,邢其毅等编著,高等教育出版社,北京:1993;6、《木糖英语真题手译》2021版先综合说一下英语的复习建议吧。
如何做阅读?做阅读题的时候我建议大家先看题干,了解一下这篇文章大致讲什么内容,然后对应题干去阅读文章,在阅读文章的过程中可以把你做出答题选择的依据标注出来,便于核对答案时看看自己的思路是否正确,毕竟重要的不是这道题你最后的答案正确与否,而是你答题的思路正确与否。
厦门大学839无机化学(海洋化学)2013年考研专业课真题答案解析

(1)[FeF6]3-(µ=5.9 B.M.);(2)[Mn(CN)6]4-(µ=1.8 B.M.); 【考查重点】: 这是配位化合物的内容,考查配位化合物的理论、中心价层轨道的杂化、配位化合物的 磁性。 【答案解析】:
物质的磁矩 与物质轨道中单电子数 n 之间满足:
n(n 2) B ,
其中, B 为磁矩单位,称为玻尔磁子。
厦门大学 2013 年招收攻读硕士学位研究生入学考试试题答案解析
科目代码:839 科目名称:无机化学 招生专业:海洋化学
考生须知:答案必须使用墨(蓝)色墨水(圆珠)笔;不得在试卷(草稿)纸上作答; 凡未按规定作答均不予评阅、判分
一、(18 分)判断下列说法是否正确?说明理由。
(1)过渡元素的原子填充电子时是先填 4s 然后填 3d,失去电子时是先失去 3d 再失去 4s;
决化学反应的方向和限度问题,并不涉及反应速率,因为热力学中的方程是在静态或准静态 条件下推导而来,而静态或准静态要求过程无限缓慢,并不考虑时间。氧化还原反应的电极 电势(能斯特方程)正是热力学的产物,因此,它不考虑反应速率问题。
《厦门大学 839 无机化学历年考研真题及答案解析》
厦门大学839无机化学(海洋化学)2014年考研专业课真题答案解析

(
2s
)2
(
2s
)2
(
2
px
)2
(
2
py
)2
(
2
pz
)2
(
* 2
py
)1
N2+:
(
1s
)
2
(
1s
)2
(
2
s
)2
(
2
s
)2
(
2
py
)2
(
2
pz
)2
(
2
px
)1
O2 的键级为 2,O2+的键级为 2.5,比 O2 的键级大,故 O2 电离生成 O2+后键长缩短;N2 的键级为 3,N2+的键级为 2.5,比 N2 的键级小,故 N2 电离生成 N2+后键长增长。
《厦门大学 839 无机化学历年考研真题及答案解析》
46 / 52
【答案解析】: 这一说是错误的,如 Cu(CN)43-的电荷数是-3,而中心离子的电荷数是+1。
二、(12 分)已知 M2+离子 3d 轨道中有 5 个电子,试推出:
(1)M 原子的核外电子排布; (2)M 原子的最外层和最高能级组中电子数; (3)M 元素在周期表中的位置(周期、族、分区)。 【考查重点】: 这是原子结构和元素周期律的内容,考查核外电子排布、最外层和最高能级组电子数、 元素在周期表中的位置。 【答案解析】: (1)该原子核外电子:1s22s22p63s23p63d54s2 (2)最外层电子数为 2,最高能级组中电子数为 7 (3)该元素在周期表中的第四周期,第ⅦB 族,d 区。
三、(16 分)
用分子轨道理论说明:(1)O2 分子有顺磁性;(2)N2 分子特别稳定;(3)O2 和 N2 分 别电离生成 O2+及 N2+时键长如何变化?
2007厦大考研有机化学真题及答案解析
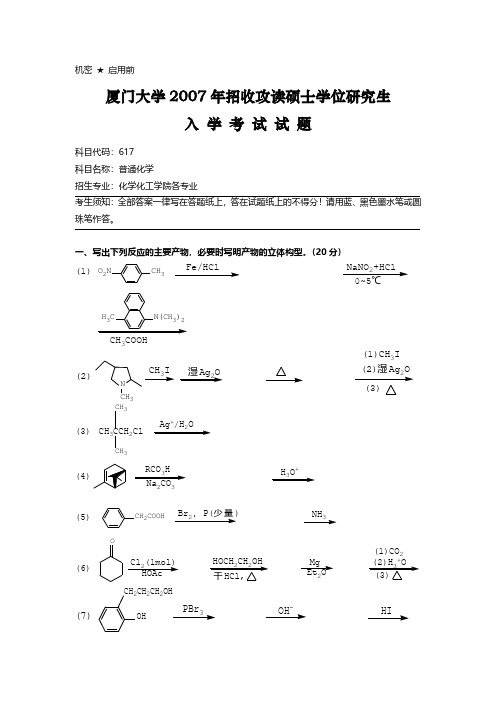
(5 分)
50ml
4. 简答题(1 分) 从茶叶中提取咖啡因的实验中,浓缩液中加入氧化钙的目的是什么?能否用氯化钙代
替?
2007 真题解析
一、写出下列反应的主要有机产物,必要时写明产物的立体构型。
NH2
N2+Cl-
N(CH3)2
N=NΒιβλιοθήκη CH3(1) CH3
CH3
CH3
本题考查硝基的还原,苯胺的重氮化反应及重氮盐的偶联反应。
本题考查羟醛缩合反应,酮的 α 氢不同时生成不同的缩合产物。
二、根据下列合成路线和有关波普数据,写出化合物 A-J 的结构式。
O
oo
O
o
O
1、(A)
O
(B)
o
o
o
o
o
(C)
o
o
oo
oo
NaO
ONa
(D)
o
o
(E)
本题考查的是红外、核磁共振氢谱,由分子式知道化合物 A 的不饱和度为 2,并且质谱
只有两组峰,说明分子中只有两种氢,根据三重峰及四重峰可以推测出分子中具有乙基结构
OH
CH3
OH2 CH3
CH2COOH
H3C O
CH3 OH
CH3
H3C O
H2O
CH2COOH
CH3
OH2 OH
-H+
CH3
CH2COOH
CH3 OH
OH CH3 CH2COOH O
HOOC
OH
OH
CH3 + H3C
CH3
OH
H+
-H+
O
CH3
-H2O
厦门大学基础化学考研试题分析研究

厦门大学有机化学考研真题分析一、考试题型分析:①中(英)文命名及考查化合物结构的题目常考点:环烷烃、立体异构、羧酸及羧酸衍生物、烯烃、卤代烷、烯炔、苯的取代物、胺醇、醚、酮、费歇尔结构式、酯、酰胺、胺、桥环;通常一个化合物中会涉及3个小点,注意费歇尔结构,立体异构(手性),官能团优先顺序等。
考查有机物结构的方式主要有:芳香性判断,对映体判别,光学活性有否判断,费歇尔结构的书写等。
②碱或酸性大小顺序排列:通常会涉及英文,有些甚至考查α-H酸活性的强弱。
要求对基团的吸电子效应、推电子效应比较熟悉,以及共轭效应、溶剂消应等掌握熟练。
考查的范围比较广,但应该不难做。
或化合物熔沸点高低的排序;反应速率比较或产率比较(如影响亲电、亲核反应的因素);结构稳定性比较(如酮式与烯醇式)或受热后的产物,或者物质在不同溶剂条件下的主要存在形式或酸碱水解产物、醇解产物;优势构象,紫外吸收波长的排序;③同种物质在不同条件下发生的特色反应(如烯烃、醛基),或以同一种物质为原料合成不同类型的化合物,或由不同物质经过不同的反应途径合成同一种物质,注意知识点如苯环上的定位效应。
④已知逆合成分析过程或已知反应试剂,完成合成路线;或者反应试剂、反应条件都告诉,要求写出反应产物(常考查其立体构型)。
主要考查对化学反应试剂、必要条件及产物结构等的掌握。
⑤对反应机理的认识考查,中间体的结构,电子或电子对转移方向。
能利用反应机理对反应结果作出解释或能根据反应结果推测可能的反应机理。
⑥化合物结构推测:要注意牢记掌握一些特色反应。
⑦有机物红外光谱、H-核磁共振图谱的应用,能根据图谱推测出结构式,牢记重要官能团伸缩振动峰的大致位置。
⑧实验题25分题型:单选,多选,简答,判断,填空,改错。
估计就只能多做题了。
⑨注意一些具有异曲同工之妙的方法总结,如将羰基还原成亚甲基的方法。
注意特色反应的归纳总结(如碘仿反应,与饱和亚硫酸钠的反应)。
⑩??芳香性大小排序。
厦门大学无机化学考研

厦门大学无机化学考研发布时间:2013-08-05浏览次数:111字号:大中小一、厦门大学无机化学考研方向有哪些?(01)原子团簇化学(包括团簇分离与分析、簇基光(02)功能配合物化学(03)无机生物材料(04)纳米催化和光催化(05)分子磁学二、厦门大学无机化学考研科目是什么?除了招生计划每年变动比较大以外,其他诸如初试要求、初试科目、奖学金等问题一般都不会变。
2014年硕士研究生招生目录要到九月份才能出来,所以14年报考的各位同学可以先参考2013的招生目录。
厦门大学无机化学考研初试科目:(101)思想政治理论、(201)英语一、(617)基础化学、(826)物理化学三、厦门大学无机化学招生情况如何?每年招生简章要到每年的9月份公布,在院校的招生简章公布后即可查看。
但每年招生简章变化不是很大,可以先参照2013年的。
厦门大学(101)化学系(070301)无机化学院系所:165,其中推免:66。
因而考生提前复习时可参考院校往年的招生专业目录中的信息进行复习,在新的招生专业目录公布后,对于变化的部分及时调整和补充。
四、厦门大学无机化学考研就业去向有哪些?毕业生主要在高等院校、科研部门、工矿企业、政府机关、贸易部门等相关专业的单位从事教学、科研、生产、检验管理;也可在环保、化工、医药、外贸、海关、卫生、质检、轻工、普教等相关单位从事应用研究开发、生产技术管理及产品营销工作。
五、无机化学考研院校都有哪些可以推荐?南京大学、吉林大学、北京大学、中国科学技术大学、南开大学、中山大学、复旦大学、厦门大学、山东大学、东北师范大学、北京师范大学、同济大学、武汉大学、兰州大学、苏州大学、福州大学。
2021年厦门大学619有机化学之基础有机化学考研精编资料

.2021 年厦门大学 61 9 有机化学之基础有机化学考研精编资料一、厦门大学 61 9 有机化学考研真题汇编及考研大纲1 .厦门大学 61 9 有机化学 1999-2006 、 2009 、 20011-2013 、 2015 年考研真题,暂无答案。
2. 厦门大学 619有机化学考研大纲①2018年厦门大学619有机化学考研大纲。
二、 2021 年厦门大学 61 9 有机化学考研资料3 .邢其毅《基础有机化学》考研相关资料①厦门大学 61 9 有机化学之邢其毅《基础有机化学》考研复习笔记。
②厦门大学 61 9 有机化学之邢其毅《基础有机化学》本科生课件。
③厦门大学 61 9 有机化学之邢其毅《基础有机化学》复习提纲。
4 .厦门大学 619 有机化学考研核心题库(含答案)①厦门大学 619 有机化学考研核心题库之选择题精编。
②厦门大学 619 有机化学考研核心题库之综合题精编。
5 .厦门大学 619 有机化学考研模拟题 [ 仿真 + 强化 + 冲刺 ]① 2021 年厦门大学 61 9 有机化学考研专业课六套仿真模拟题。
② 2021 年厦门大学 61 9 有机化学考研强化六套模拟题及详细答案解析。
③ 2021 年厦门大学 61 9 有机化学考研冲刺六套模拟题及详细答案解析。
三、V资料X获取:ky21985四、 2021 年研究生入学考试指定 / 推荐参考书目(资料不包括教材)6 .厦门大学 61 9 有机化学考研初试参考书黄培强《有机合成》;T.W. Graham Solomons 《 Organic Chemistry 》;邢其毅《基础有机化学》;胡宏纹《有机化学》五、 2021 年研究生入学考试招生适用院系 / 专业7 .厦门大学 61 9 有机化学适用院系 / 专业化学系;材料科学与工程系;公共卫生学院.。
厦门大学有机化学考研真题及答案(2012年)

机密★启用前和使用过程中厦门大学2012年招收攻读硕士学位研究生入学考试试题科目代码:617科目名称:有机化学招生专业:化学系、材料科学与工程系、能源研究院各相关专业考生须知:答题必须使用黑(蓝)色墨水(圆珠)笔;不得直接在试题(草稿)纸上作答;凡未按上述规定作答均不予评阅、判分,责任考生自负。
一、解答下列问题。
(50分)1. (6分)下列烷烃分别在光照条件下与氯气反应都只生成一种一氯代产物,请写出这些烷烃及其一氯代产物的结构简式。
(1) C5H10 (2) C8H18 (3) C5H122. (4分)4,4-二甲基-5-羟基-2-戊酮的红外光谱在1600至1800cm-1区域无吸收峰,而在3000至3400cm-1区域出现一个宽吸收峰,13C NMR在150ppm处无吸收峰,在110ppm处有吸收峰,请给出合理的解释。
3. (3分)分别比较下列各组化合物中哪个酸性较强?4. (3分)写出实现下列转化所需要的试剂:5. (7分)化合物A分别与下列试剂反应,主要有机产物是什么?6. (4分)写出下列各步合成反应中化合物2—5的立体结构式。
7. (3分)写出下列化合物发生硝化反应所得主要产物的结构简式:8. (16分)用反应式表示如何由1-甲基-4-氯苯制备下列化合物:9. (4分)如何用简单的化学方法鉴别下列各组化合物?(1)4-氯苯酚和1-甲基-4-氯苯(2)苯氧基乙烯和乙氧基苯二、写出下列反应的主要有机产物,必要时写明产物的立体构型。
(12分)三、写出下列反应的机理,用弯箭头“”表示电子对的转移,用鱼钩箭头“”表示单电子的转移,并写出各步可能的中间体。
(10分)四、综合题(35分)1. (30分)文献报道的天然产物Patriscabrol(化合物19)和Isopatriscabrol(化合物20)的合成方法如下:(1)(2分)分别用中、英文系统命名法命名化合物1;(2)(14分)写出步骤(A)—(N)所需的试剂及必要的反应条件;(3)(14分)用反应机理解释由化合物10到11的转变过程。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
厦门大学化学系考研解析
2019招生专业目录
无机化学
有机化学
物理化学
高分子化学与物理
纳米材料化学
化学生物学
分析化学
招生计划
历年报录比
考试范围
参考2019化学系考试范围
617无机化学:化学原理与无机元素化学
619有机化学:有机化合物的命名、结构与性质、有机化合物的结构分析、有机合成826物理化学:热力学定律(含多组分体系,电化学热力学),化学反应和平衡(含热化学、化学平衡和相平衡),化学动力学(含电化学动力学),胶体与界面
827分析化学(含仪器分析):酸碱反应、沉淀反应、络合反应、氧化还原反应、分子光谱、原子光谱、红外光谱、核磁共振、质谱、色谱、电化学分析、数据分析。
