高二化学氢键与物质性质
高二化学氢键与物质性质

3.氢键对物质性质的影响: 对物质熔沸点的影响
分子间氢键使物质熔点升高 分子内氢键使物质熔点降低
范德华力、氢键和共价键的对比
概念
存在 范围
范德华力 分子间普 遍存在的
作用力
分子之间
氢键
已经与电负性很强的原子形成 共价键的氢原子与另一分子中 电负性很强的原子之间的作用
力
分子间或分子内氢原子与电负 性很强的N、O、F之间
共价键 原子之间通过 共用电子对形
成的化学键
相邻原子之间
强度 微弱
对物 质的 影响
思考
1.通过图片上各族元素氢化物的熔、沸点的变化 规律,哪些物质的熔、沸点出现了反常? __________________ 通过对比,请你分析出现反常现象的原因是什么? ___________________
2. 分析碳族元素氢化物的变化规律是否也有反 常现象? ___________ 通过对比,请你分析出现反常现象的原因是什么? ___________
熔沸点
较弱 溶解性、熔沸点
很强
主要影响化学 性质
比较下列熔、沸点高低并且说明原因。
(1)H2O和H2S____原因________ (2) HF和HCl____原因________ (3) NH3和PH3____原因________ (4) CH4和CCl4____原因________
3.氢键对物质性质的影响
0 -25 NH3 -50
-75 -100 -125
高二化学氢键与物质性质3

[名词解释]后生动物 [单选]对确诊SLE和判断其活动性参考价值最大的抗体是()。A.抗核抗体B.抗dsDNA抗体C.抗Sm抗体D.抗rRNP抗体E.抗Ro抗体 [填空题]亮度对比是视场中()与()之比。 [填空题]液氨罐检修置换。顺序为开放空阀-打开人孔-()-排水-()-鼓风机吹扫-活动物试验-检测氨浓度-合格后交出检修。 [单选,A1型题]五倍子鞣质从结构上看属于()A.没食子鞣质B.逆没食子鞣质C.可水解鞣质低聚体D.咖啡鞣质E.缩合鞣质 [单选,A型题]胃泡与"左侧膈下游离气"鉴别点不包括()A.气体量多少B.边缘是否有黏膜C.与膈之间是否有分隔影D.气体是否可以游离到右侧膈下E.造影检查可以区别 [单选]多人采用走访形式提出共同的信访事项的,应当推选代表,代表人数不得超过()。A.3人B.5人C.8人D.10人 [单选]光和作用的原料是二氧化碳和()A.水B.空气C.钙元素D.氧气 [单选]甲公司的董事张某以公司的资产为本公司的股东林某的对外欠下的个人债务3万元提供了担保,且此个人债务的债权人对此并不知情,则此担保合同的效力是?()A.效力待定B.有效C.无效D.效力有瑕疵 [单选,A1型题]原子核发生电子俘获后()A.质子数减少2,质量数减少4,放出α射线B.质子数增加1,质量数不变,放出β射线和反中微子C.质子数减少1,质量数不变,放出β射线和中微子D.质子数减少1,质量数不变,放出中微子,同时释放出特征X射线和俄歇电子E.质子数和质 [单选]职业道德不仅有(),也有一定的历史继承性。A、价值观念B、技术延续C、法律色彩D、创造性 [单选]急性化脓性胃炎最常见的致病菌是()A.沙门菌B.嗜盐菌C.幽门螺杆菌D.金黄色葡萄球菌E.甲型溶血性链球菌 [填空题]客运经营者未报告原许
高中化学第二章分子结构与性质3.1键的极性和分子的极性范德华力和氢键及其对物质性质的影响课时评价含解

键的极性和分子的极性范德华力和氢键及其对物质性质的影响(30分钟50分)一、选择题(本题包括4小题,每小题5分,共20分)1。
(2020·太原高二检测)下列物质性质的变化规律与分子间作用力无关的是()A。
在相同条件下,N2在水中的溶解度小于O2B。
HF、HCl、HBr、HI的热稳定性依次减弱C.F2、Cl2、Br2、I2的熔、沸点逐渐升高D。
CH3CH3、CH3CH2CH3、(CH3)2CHCH3、CH3CH2CH2CH3的沸点逐渐升高【解析】选B。
A项中,N2和O2都是非极性分子,在水中的溶解度都不大,但在相同条件下,O2分子与水分子之间的作用力比N2分子与水分子之间的作用力大,故O2在水中的溶解度大于N2。
B项中,HF、HCl、HBr、HI的热稳定性与其分子中的氢卤键的强弱有关,而与分子间作用力无关.C项中,F2、Cl2、Br2、I2的组成和结构相似,分子间作用力随相对分子质量的增大而增大,故其熔、沸点逐渐升高。
D项中,烷烃分子之间的作用力随相对分子质量的增大而增大,故乙烷、丙烷、丁烷的沸点逐渐升高,在烷烃的同分异构体中,支链越多分子结构越对称,分子间作用力越小,熔、沸点越低,故异丁烷的沸点小于正丁烷。
【补偿训练】下列关于范德华力的叙述正确的是()A。
是一种较弱的化学键B。
分子间的范德华力越大,分子就越稳定C.相对分子质量相同的分子之间的范德华力也相同D.稀有气体的原子间存在范德华力【解析】选D。
范德华力是分子间存在的较弱的相互作用,它不是化学键,A错误;分子的稳定性是由形成分子的原子之间的化学键强弱决定的,与分子间作用力大小无关,B错误;相对分子质量相同,范德华力不一定相同,如CO与N2,相对分子质量相同,但分子间作用力CO大,C错误;稀有气体为单原子分子,分子之间靠范德华力相结合,D正确。
2.如图中每条折线表示周期表第ⅣA族~第ⅦA族中的某一族元素氢化物的沸点变化,每个小黑点代表一种氢化物,其中a点代表的是()A.HCl B。
2020年春高二化学下学期选修《物质结构与性质》学案3.4.1分子间作用力

专题三第四单元分子间作用力分子晶体第1课时分子间作用力【学习目标】1.熟知常见的分子间作用力(范德华力和氢键)的本质及其对物质性质的影响。
2.会比较判断范德华力的大小,会分析氢键的形成。
【新知导学】一、范德华力1.分析讨论,回答下列问题:(1)液态苯、汽油等发生汽化时,为何需要加热?(2)降低氯气的温度,为什么能使氯气转化为液态或固态?(3)卤素单质F2、Cl2、Br2、I2,按其相对分子质量增大的顺序,物理性质(如颜色、状态、熔点、沸点)有何变化规律?2.上述事实能够说明:(1)固体、液体和气体中分子之间的________叫范德华力。
(2)一般来说,相对分子质量________,范德华力越大。
(3)范德华力一般没有方向性和饱和性,只要分子周围空间允许,当气体分子凝聚时,它总是________________________________________________________________________。
3.范德华力对物质性质的影响(1)对物质熔、沸点的影响①组成和结构相似的分子,相对分子质量________,范德华力________,物质的熔、沸点就越高。
例如熔、沸点:CF4<CCl4<CBr4<CI4。
②组成相似且相对分子质量相近的物质,分子电荷分布越不均匀,范德华力越大,其熔、沸点就越高,如熔、沸点:CO>N2。
③在同分异构体中,一般来说,支链数________,熔、沸点就越低,如沸点:正戊烷>异戊烷>新戊烷。
(2)对物质溶解度的影响溶质分子与溶剂分子之间的范德华力越______,溶解度越大。
【归纳总结】1.范德华力普遍存在于________、________和________分子之间。
2.影响范德华力的因素:主要包括__________、________________以及分子中电荷分布是否均匀等。
3.范德华力______,物质的________越高,______越大。
第1课时 键的极性和分子的极性、范德华力、氢键及其对物质性质的影响

sp3 杂化,且有两对孤电子对,分子构型为V形,整个分子电荷
分布不对称,为极性分子。CO2分子中C采取sp杂化,分子构型 为直线形,分子为非极性分子,C原子位于2个O原子所连成的 直线的中央。 答案: C
工具
第二章 分子结构与性质
栏目导引
工具
第二章 分子结构与性质
栏目导引
1.范德华力对物质性质的影响 (1)对物质熔、沸点的影响 一般说来,组成和结构相似的物质,相对分子质量越大, 分子间作用力越大,物质的熔、沸点通常越高。如熔、沸点: I2>Br2>Cl2>F2,Rn>Xe>Kr>Ar>Ne>He。 (2)对物质溶解性的影响
分子 分子空间 类型 构型 A A2 — 键角 — 键的 极性 — 分子 极性 常见物质
非极性分子 He、Ne、Ar等
AB
AB2 A2B
直线形(对 非极 — 非极性分子 H2、O2、N2等 称) 性键 直线形(非 HX、CO、NO — 极性键 极性分子 对称) 等 直线形(对 180° 极性键 非极性分子 CO2、CS2等 称) 折线形(对 称) — 极性键 极性分子 H2O、H2S等
第二章 分子结构与性质
栏目导引
(3)根据中心原子最外层电子是否全部成键判断 中心原子即其他原子围绕它成键的原子。分子中的中心原 子最外层电子若全部成键,此分子一般为非极性分子;分子中
的中心原子最外层电子若未全部成键,此分子一般为极性分子。
CH4、BF3、CO2等分子中的中心原子的最外层电子均全部成键, 它们都是非极性分子。
第三节
分子的性质
工具
第二章 分子结构与性质
栏目导引
第1课时 键的极性和分子的极性、范德华 力、氢键及其对物质性质的影响
分子间作用力(范德华力、氢键) 高二化学课件(人教版2019选择性必修2)

O—H … N O—H … F N—H … O
F—H … O
4、特点: ①氢键具有方向性和饱和性
方向性:A—H…B—总是尽可能在同一直线上。 饱和性:每个裸露的氢原子核只能形成一个氢键
每个孤电子对也只能形成一个氢键。
②氢键比化学键的键能小1~2个数量级,不属于化学键,也是一
种分子间的作用力。以冰晶体为例:共价键>氢键 >范德华力
因氢键而相互缔合,形成所谓的缔合分子。
课堂练习3:下列有关水的叙述中,不能用氢键的知识来解释的是( D)
A、 0℃时,水的密度比冰大
B、水的熔沸点比硫化氢的高
C、测得H2O的相对分子质量大于18
D、水比硫化氢气体稳定
③氢键对溶解度的影响
与水分子间能形成氢键的物质在水中的溶解度增大
氨气极易溶于水、乙醇、乙醛、乙酸与水互溶而乙烷不溶于水
共价键的键能(KJ•mol-1) 范德华力(KJ•mol-1) 氢键(KJ•mol-1)
467
11
18.8
5、类别: ① 分子间氢键 分子间氢键存在于如HF、H2O、NH3 、C2H5OH、
CH3COOH 等同种分子之间,也存在于它们相互之间
② 分子内氢键
对羟基苯甲醛不能形
成分子内氢键
邻羟基苯甲醛
降温加压时气体会液化,降温时液体会凝固,这些事实表明,分子之间 存在着相互作用力 ——分子间作用力(包括范德华力和氢键)
一、 范德华力
1、概念:
把分子聚集在一起的作用力,称为范德华力
实质: 分子间的一种静电作用
2、特点:
①范德华力很弱,比化学键的键能小1~2数量级
分子
HCl HBr HI
范德华力(kJ/mol) 21.14 23.11 26.00
高中化学 氢键及其对物质性质的影响课后微练习3高二3化学试题

促敦市安顿阳光实验学校氢键及其对物质性质的影响1.下列说法中错误的是A.卤化氢中,以HF沸点最高,是由于HF分子间存在氢键B.H2O的沸点比HF的高,可能与氢键有关C.氨水中有分子间氢键D.氢键X—H…Y的三个原子总在一条直线上2.下列物质发生变化时,所克服的粒子间相互作用属同种类型的是()A.碘与干冰分别受热变为气体B.硝酸铵与硝酸分别受热变为气体C.氯化钠与氯化氢分别溶解在水中D.二氧化硅晶体与冰分别受热熔化3.在硼酸[B(OH)3]分子中,B原子与3个羟基相连,其晶体具有与石墨相似的层状结构。
则分子中B原子杂化轨道的类型及同层分子间的主要作用力分别是()A.sp,范德华力 B.sp2,范德华力 C.sp2,氢键 D.sp3,氢键4.下列物质中不存在氢键的是()A.冰醋酸中醋酸分子之间B.液态氟化氢中氟化氢分子之间C.一水合氨分子中的氨分子与水分子之间D.可燃冰(CH4·8H2O)中甲烷分子与水分子之间5.据元素周期表知识回答下列问题。
(1)PH3分子与NH3分子的构型关系________(填“相似”或“不相似”)。
(2)NH3与PH3相比,热稳性________更强。
(3)NH3、PH3在常温、常压下都是气体,但NH3比PH3易液化,其主要原因是________(填字母代号)。
A.键的极性:N—H比P—H强B.相对分子质量:PH3比NH3大C.NH3分子之间存在特殊的分子间作用力(氢键)6. CO2、CH4、BF3都是非极性分子,HF、H2O、NH 3都是极性分子,由此推测AB n 型分子是非极性分子的经验规律正确的是()A.所有原子在同一平面B.分子中不含有氢原子C.在AB n中A原子没有孤电子对D.A的相对原子质量小于B7.关于氢键,下列说法正确的是()A.每一个水分子中含有两个氢键B.冰、水、水蒸气中都含有氢键C.DNA中的碱基互补配对是通过氢键来实现的D.水是一种非常稳的化合物,这是由于氢键所致8.下列关于氢键的说法中正确的是()A.氢键属于共价键B .氢键只存在于分子之间C.氢键的形成使物质体系的能量降低D.氢键在物质内部一旦形成,就不会再断裂9.若不断地升高温度,实现“雪花→水→水蒸气→氧气和氢气”的变化。
氢键知识点归纳

氢键知识点归纳
(1)概念:已经与电负性很大的原子(如N、O、F) 形成共价键的氢原子与另一个电负性很大的原子(如 N、O、F)之问的作用力。
如水分子问的氢键如下图所示。
(2)表示方法:A—H…B一(A、B为N、O、F“一” 表示共价键,“…”表示形成的氢键)。
(3)分类(4)属性:氢键不属于化学键,它属于一一种较强的分子间作用力,其作用能大小介于范德华力和化学键之间。
(5)对物质性质的影响
①氢键对物质熔、沸点的影响。
分子问存在氧键时,破坏分子问的氢键,需要消耗更多的能量,所以存在氢键的物质具有较高的熔点和沸点。
例如:氮族、氧族、卤素中的N、O、F的氧化物的熔、沸点的反常现象。
②氢键对物质溶解度的影响:氢键的存在使物质的溶解性增大。
例如:NH3极易溶解于水,主要是由于氨分子和水分子之问形成了氢键,彼此互相缔合,因而加大了溶解。
再如乙醇、低级醛易溶于水,也是因为它们能与水分子形成氢键。
③氢键的存在会引起密度的变化。
水结冰时体积膨胀、密度减小的反常现象也可用氢键解释:在水蒸气中水以单个的水分子形式存在;在液态水中,通常是几个水分子通过氢键结合,形成(H2O)n小集团;在固态水(冰)中,水分子大范围地以氢键互相连接,成为疏松的晶体,因此在冰的结构中有许多空隙,造成体积膨胀,密度减小。
④分子内氢键与分子间氢键对物质性质的不同影响:氢键既可以存。
高二化学氢键与物质性质

3.氢键对物质性质的影响
氢键的键能一般小于40kJ/mol,强度介 于化学键和范徳华力之间.因此氢键不属于 化学键,而属于分子间作用力的范畴。同范 徳华力一样,氢键只对物质的物理性质有影 响,主要表现为物质的熔沸点升高,另外, 对物质的电离和溶解等也有影响。
3.氢键对物质性质的影响:
对物质熔沸点的影响 分子间氢键使物质熔点升高
存在 范围 强度 对物 质的 影响
微弱 熔沸点
很强 主要影响化学 性质
比较下列熔、沸点高低并且说明原因。 (1)H2O和H2S____原因________ (2) HF和HCl____原因________ (3) NH3和PH3____原因________ (4) CH4和CCl4____原因________
第四节
分子间的作用力与物质的性质
第O
25
0 -25 -50 -75 -100 -125 -150 H2S H2Se H2Te
2
3
4
5
周期
1.定义:当氢原子与电负性大的X原子以共价 键结合时,它们之间的共用电子对强烈地偏向 X,使H几乎成为“裸露”的质子,这样相对显 正电性的H与另一分子中相对显负电性的X(或Y) 原子相接近并产生静电相互作用和一定程度的 轨道的重叠作用,这种相互作用称氢键。 表示:氢键可以用X—H…Y表示。X和Y可以是 同种原子,也可以是不同种原子。表示式中的实 线表示共价键,虚线表示氢键。
在什么样的条件下才能形成氢键? 思考:
2. 氢键的形成 条件:X—H…Y中, X和Y都是电负性 较大、半径极小 的非金属原子 (一般就是N、 O、F)。
沸点/℃100 75
50 25 0 -25 -50 NH3 HF
H2O
氢键的相关知识点总结

氢键的相关知识点总结1. 氢键的概念和定义氢键是指两个或多个分子间的相互作用力,其作用力主要来源于氢原子与其他原子形成的非共价键。
在氢键中,氢原子通过与其他原子(通常是氧、氮或氟原子)形成共价键而与带负电性较强的原子形成氢键。
氢键通常被表示为“H···A”,其中H代表氢原子,A代表带负电性的原子。
氢键的形成是在电负性较强的原子上形成部分正电荷,使其与邻近原子的带负电性原子发生相互作用,从而形成了氢键。
氢键的作用力既包括电荷-电荷相互作用力,也包括范德华力等非共价相互作用力。
氢键的强度通常在5-40kj/mol之间,比范德华力强,但比共价键弱。
氢键是一种比较强的作用力,在化学和生物学中起到了非常重要的作用。
它不仅使得分子之间能够形成化学键,还能够在生物体内调控生物分子的结构和功能。
由于氢键的独特性质,使得它成为了一种非常重要的相互作用力,其研究在化学、生物学、物理化学等领域都有着重要的应用和意义。
2. 氢键的结构氢键的结构主要取决于参与形成氢键的分子的性质和构型。
一般而言,氢键的结构可以分为两种类型:线性氢键和非线性氢键。
线性氢键是指氢原子和带负电性原子以直线的方式相互作用形成的氢键。
在线性氢键中,氢原子和带负电性原子之间的键角约为180°,结构上呈现出一条直线状。
线性氢键通常具有较大的键能,且较为稳定。
非线性氢键是指氢原子和带负电性原子以非直线的方式相互作用形成的氢键。
在非线性氢键中,氢原子与带负电性原子之间的键角大约在160°-180°之间,结构上呈现出一定的弯曲状。
非线性氢键通常具有较小的键能,且较为不稳定。
氢键的结构相对复杂,同时也受到多种因素的影响。
分子的构型、成键原子的性质以及外界环境等都能够对氢键的结构产生一定程度的影响。
因此,氢键的结构十分复杂且多样化。
3. 氢键的性质氢键具有一系列独特的性质,使得它成为一种非常重要的相互作用力。
人教版高二化学选修3教学案:第二章 第三节 分子的性质含答案

1.了解共价键的极性及分子的极性及其产生的原因。
2.知道范德华力、氢键对物质性质的影响。
3.了解影响物质溶解性的因素及相似相溶原理。
4.了解手性分子在生命科学等方面的应用。
5.了解无机含氧酸分子酸性强弱的原因。
细读教材记主干1.共价键依据电子对是否偏移分为非极性键和极性键,依据电子云的重叠方式分为σ键和π键。
2.分子间作用力是化学键吗?其主要影响物质的物理性质还是化学性质?提示:不是,其主要影响物质的物理性质,如熔、沸点,溶解性等。
3.极性分子中一定有极性键,含极性键的分子不一定是极性分子。
非极性分子中可能有极性键,也可能含有非极性键。
4.分子的相对分子质量越大,范德华力越大,其熔、沸点越高。
若分子之间存在氢键,会使物质的熔、沸点升高。
5.非极性溶质一般能溶于非极性溶剂,极性溶质一般能溶于极性溶剂;溶质和溶剂之间形成氢键,可增大其溶解度。
6.无机含氧酸的通式(HO)m RO n,若成酸元素R相同,n值越大,酸性越强。
[新知探究]1.键的极性2.分子的极性3.键的极性和分子极性的关系(1)只含非极性键的分子一定是非极性分子。
(2)含有极性键的分子有没有极性,必须依据分子中极性键的极性的向量和是否等于零而定,等于零时是非极性分子。
[名师点拨]分子极性的判断方法只含非极性键→非极性分子(单质分子,如Cl2,N2,P4,I2)等[对点演练]1.(2016·桓台高二检测)下列含有极性键的非极性分子是( )①CCl4②NH3③CH4④CO2⑤N2⑥H2O ⑦HFA.②③④⑤B.①③④⑤C.①③④ D.以上均不对解析:选C ①CCl4中含有极性键,空间结构为正四面体,正负电荷的中心重合,属于非极性分子;②NH3中含有极性键,空间结构为三角锥形,正负电荷的中心不重合,属于极性分子;③CH4中含有极性键,空间结构为正四面体,正负电荷的中心重合,属于非极性分子;④CO2含有极性键,空间结构为直线型,属于非极性分子;⑤N2是由非极性键构成的非极性分子;⑥H2O中含有极性键,空间结构为V型,属于极性分子;⑦HF是极性键形成的极性分子;含有极性键的非极性分子是①③④,C项正确。
高二化学物质的聚集状态与物质的性质试题答案及解析

高二化学物质的聚集状态与物质的性质试题答案及解析1.关于氢键,下列说法正确的是()A.分子间形成的氢键使物质的熔点和沸点升高;B.冰中存在氢键,水中不存在氢键;C.每一个水分子内含有两个氢键;D.H2O是一种非常稳定的化合物,这是由于氢键所致【答案】A【解析】氢键不是化学键,一般影响物质的物理性质,而不能影响分子的稳定性,A正确,D不正确。
水分子间存在氢键,所以选项BC都是错误的,答案选A。
2.为了确定SbCl3、SbCl5、SnCl4是否为离子化合物,可以进行下列实验,其中合理、可靠的是()A.观察常温下的状态,SbCl5是苍黄色液体,SnCl4为无色液体。
结论:SbCl5和SnCl4都是离子化合物B.测定SbCl3、SbCl5、SnCl4的熔点依次为73.5℃、2.8℃、-33℃。
结论:SbCl3、SbCl5、SnCl4都不是离子化合物C.将SbCl3、SbCl5、SnCl4溶解于水中,滴入HNO3酸化的AgNO3溶液,产生白色沉淀。
结论:SbCl3、SbCl5、SnCl4都是离子化合物D.测定SbCl3、SbCl5、SnCl4的水溶液的导电性,发现它们都可以导电。
结论:SbCl3、SbCl5、SnCl4都是离子化合物【答案】B【解析】离子化合物形成的晶体都是离子晶体,熔沸点高,所以A不正确,B正确。
共价化合物溶于水也能发生电离,也可以导电,但熔融时只有离子化合物可以导电,所以CD都是错误错误的,答案选B。
3.下列现象与氢键有关的是:①H2O的熔、沸点比VIA族其他元素氢化物的高②小分子的醇、羧酸可以和水以任意比互溶③冰的密度比液态水的密度小④NH3在水中的溶解度很大⑤邻羟基苯甲酸的熔、沸点比对羟基苯甲酸的低⑥水分子高温下也很稳定:A.①②③④⑤⑥B.①②③④⑤C.①②③④D.①②③【答案】B【解析】氢键不是化学键,一般影响物质的物理性质。
水分子稳定和水分子中的化学键强弱有关系,与氢键是无关的,其余和氢键都有关系,所以正确的答案是B。
高二化学分子的性质3

思考与交流
1. NH3是极性分子,CH4为非极性分子,而水是极性分 子,根据“相似相溶”规律, NH3易溶于水,而CH4不 易溶于水。并且NH3与水分子之间还可以形成氢键,使 得NH3更易溶于水。
2. 油漆是非极性分子,有机溶剂如(乙酸乙酯)也是 非极性溶剂,而水为极性溶剂,根据“相似相溶”规 律,应当用有机溶剂溶解油漆而不能用水溶解油漆。 3. 实验表明碘在四氯化碳溶液中的溶解性较好。这是 因为碘和四氯化碳都是非极性分子,非极性溶质一般 能溶于非极性溶剂,而水是极性分子。
如:H3PO4 < H2SO4 < HClO4
高氯酸是非金属含氧酸中酸性最强的无机酸
2.在同一主族中,处于相同价态的不同元素, 其含氧酸的酸性随成酸元素的原子序数递 增,自上而下减弱。
如
HClO>HBrO>HIO HClO2>HBrO2>HIO2 HClO3>HBrO3>HIO3 HClO4>HBrO4>HIO4
第三节
分子的性质
(第三课时)
四、溶解性 1. “相似相溶”规律: 非极性 物质一般易溶于非 极性 溶剂,极性溶质一般易溶于极性溶剂。 2. 若存在氢键,溶质和溶剂之间的氢键作用力越 大 ,溶解性越 好 。 3. 若溶质遇水能反应将增加其在水中的溶解度。
4. “相似相溶”还适用于分子结构的相似性。 阅读 资料卡片
试一试:是否重合
五. 手性
1. 手性:镜像对称,在三维空间里组成和原子排列的一对分子,如同 左手与右手一样互为镜像,却在三维空间里不能重叠, 互称手性异构体。 3. 手性分子: 有手性异构体的分子叫做手性分子。
4. 手性碳原子 当碳原子结合的四个原子或原 子团各不相同时,该碳原子是手性 碳原子。
3.同一元素若能形成几种不同价态的含氧酸, 其酸性依化合价的递增而递增;
高二化学分子的性质1

嘴哆市安排阳光实验学校高二化学分子的性质知识精讲人教实验版一. 本周教学内容:分子的性质1. 键的极性和分子的极性2. 范德华力及其氢键对物质性质的影响3. 相似相溶原理4. 有机分子的手性和无机含氧酸分子的酸性二. 重点、难点1. 了解极性共价键和非极性共价键。
2. 结合常见物质分子立体结构,判断极性分子和非极性分子。
3. 了解范德华力、氢键及其对物质性质的影响,能举例说明化学键和分子间作用力的区别。
4. 从分子结构的角度,认识“相似相溶”规律。
5. 了解“手性分子”在生命科学等方面的应用。
6. 能用分子结构的知识解释无机含氧酸分子的酸性。
三. 教学过程(一)键的极性和分子的极性1、键的极性按共用电子对是否偏移,共价键分为极性键和非极性键。
(1)非极性共价键(非极性键):同种非金属元素原子间形成的共价键。
(2)极性共价键(极性键):不同种非金属元素原子之间形成的共价键。
(3)非极性键和极性键的比较:②当成键原子的电负性相同时,核间的电子云密集区域在两核的中间位置,两个原子核正电荷所形成的正电荷重心和成键电子对的负电荷重心恰好重合,这样的共价键称为非极性共价键。
如H2、O2分子。
③当成键原子的电负性不同时,核间的电子云密集区域偏向电负性较大的原子一端,使之带部分负电荷,而电负性较小的原子一端则带部分正电荷,键的正电荷重心与负电荷重心不重合,这样的共价键称为极性共价键。
如HCl分子。
④成键原子的电负性差值愈大,键的极性就愈大。
2、分子的极性(1)非极性分子:分子结构对称,整个分子内正负电荷重心重合的分子叫做非极性分子。
(2)极性分子:分子结构不对称、分子内正负电荷重心不重合的分子。
如:极性键构成的双原子化合物分子、结构不对称的多原子分子。
(3)键的极性和分子的极性的比较:研究对象不同,键的极性研究的是原子,而分子的极性研究的是分子本身;研究的方向不同,键的极性研究的是共用电子对的偏离与偏向,而分子的极性研究的是分子中电荷分布是否均匀。
氢键对物质性质的影响.ppt
性
练习:(04广东)下列关于氢键的说法中正 确的是( ) A、每个水分子内含有两个氢键 B、在所有的水蒸气、水、冰中都含有氢键 C、分子间能形成氢键,使物质的熔沸点升 高
D、HF稳定性很强,是因为其分子间能形成 氢键
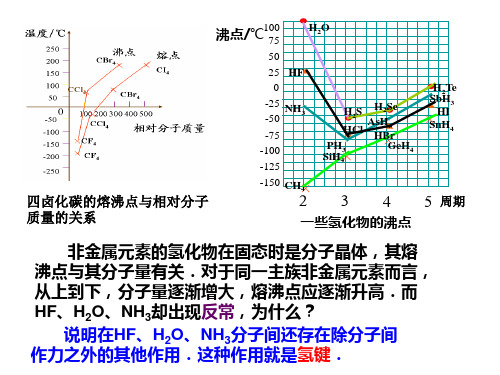
说明在HF、H2O、NH3分子间还存在除分子间 作力之外的其他作用.这种作用就是氢键.
三、氢键及其对物质性质的影响
1、氢键
氢键的概念:
氢键是一种特殊的分子间作用力,它是由已经与电负性很 强的原子(N、O、F)形成共价键的氢原子与另一分子 中电负性很强的原子之间的作用力.
氢键的本质:
是一种静电作用,是除范德华力之外的另一种分子 间作用力. 注意:只有分子充分接近时,氢键作用才明显, 如固体和液体中;而气体中往往忽略
2、氢键及其对物质性质的影响
氢键对物质熔沸点影响:
分子间氢键使物质熔沸点升高 分子内氢键使物质熔沸点降低
氢键对物质溶解度的影响:
极性溶剂里,溶质分子与溶剂分子间的氢键使溶质 溶解度增大,而当溶质分子形成分子内氢键时使溶 质溶解度减小。
课堂讨论
比较熔沸点: HF > HCl H2O > H2S 邻羟基苯甲醛 > 对羟基苯甲醛
另外的N、O、F原子之间。
如:HF、H2O、NH3 相互之间 C2H5OH、CH3COOH、H2O相互之间
分子内氢键 (不属于分子间作用力)
某些物质在分子内也可形成氢键,例如当苯酚在邻位上 有—CHO、—COOH、—OH和—NO2时,可形成分子内的氢键, 组成“螯合环”的特殊结构.
例如 (1)分子间氢键: (2)分子内氢键:
3.应用与拓展
• 为什么NH3极易溶于水?
• 冰的硬度比一般固体共价化合物大,为什么?
氢键课件高二化学人教版选择性必修4

3.互为同分异构体的分子,支链越多, 分子间范德华力越弱, 熔、沸点就越低,如沸点:正戊烷>异戊烷>新戊烷。
注意:键能大小影响分子的热稳定性, 范德华力的大小影响物质的熔、沸点。
二、氢键及其对物质性质的影响 1. 氢键概念:氢键是一种特殊的分子间作用力,它是由已经与电负性很强
油漆的主要成分是非极性或极性很小的有机分子,故易溶于非极性或极性很小 的有机溶剂中,如苯、甲苯、乙酸乙酯等,而不溶于水。
【思考与讨论】P59 视频:碘单质的溶解性
(3)在一个小试管里放入一小粒碘晶体,加入约5 mL蒸馏水,观察碘在水中的溶解性
(若有不溶的碘,可将碘水溶液倾倒在另一个试管里继续下面的实验)。在碘水溶液中
加入约1 ml CCl4,振荡试管,观察碘被CCl4萃取,形成紫红色的碘的CCl4溶液。再向试 管里加入1 ml 浓碘化钾(KI)水溶液,振荡试管,溶液紫色变浅,这是由于在水溶液里
可发生如下反应:I2+I-
I3-。实验表明碘在纯水还是在CCl4中溶解性较好?为什么?
→I2是非极性分子,所以在极性溶剂水中的溶解度很小,
而易溶于非极性溶剂CCl4 。
→碘水中加人浓的KI溶液后,由于发生反应:I2+I- I3-, 碘生成了无色的I3-,并溶解到水中,碘的浓度降低,所以 溶液紫色变浅。
【思考与交流】 分析下表,你能得到哪些规律,并加以解释
非 极 性 分 子 水是极性溶剂,根据“相似相溶”,非极性溶质在水中的溶解度不大。
5.范德华力的大小和特征
1.范德华力很弱,比化学键的键能小1~2个数量级
2.组成和结构相似的分子,相对分子质量越大,范德华力越大
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
[单选,A2型题]某早产女婴,出生后3天吃奶少,哭声低,全身冰凉,体温29°,四肢及躯干皮肤似硬橡皮样。错误的处理是()A.立即放入28℃温箱内逐渐复温B.热量供应从209.2kJ(50kcal)/(k·D.C.根据病原菌选用广谱抗生素预防感染D.可少量输血或血浆E.尽量母乳喂养和口服补液 [问答题,案例分析题]女性,30岁。主诉:发热伴咽痛2天急诊就诊。请针对该案例,说明问诊内容与技巧。 [多选]在《担保法》规定的五种担保方式中,既允许债务人用自己的财产也可以用第三人财产向债权人提供担保的有()。A.保证B.抵押C.动产质押D.权利质押E.定金 [填空题]人的心理活动包括___________与个性心理。 [单选,A2型题,A1/A2型题]关于1型糖尿病,下列错误的是()。A.对胰岛素不敏感B.有发生酮症酸中毒的倾向C.起病较急,症状明显D.大多消瘦E.发病年龄较早 [单选]TMN至用户终端的通信路经是().A.业务节点—-业务节点接口—-用户-网络接口B.用户—网络接口—-业务节点—-业务节点接口C.业务节点接口—-业务节点—-用户—网络接口 [单选]以下股利分配政策中,最有利于股价稳定的是()。A.剩余股利政策B.固定股利政策C.固定股利支付率政策D.低正常股利加额外股利政策 [单选,A1型题]下列各项,属于暑淫证临床表现的是()。A.头昏如裹B.胸闷脘痞C.肌肉酸痛D.头身疼痛E.卒然昏倒 [单选]()接口:承载BSS和PCF之间数据的传输。A8B.A9C.A10D.Z11 [单选,A1型题]原发性醛固酮增多症患者的尿液变化是()A.尿多,以白天尿多为主B.尿多,以夜尿多为主C.尿量无变化D.尿量减少E.尿少,以夜尿少为主 [问答题,简答题]ST型缓冲器的组成? [单选]下列不属于注册消防工程师职业道德原则特点的是()。A.稳定性B.普遍性C.本质性D.基准性 [填空题]电动机按它所耗用电能种类的不同可分为()电动机和()电动机。 [单选]某车祸病人,现场验伤时应注意检查有无()A.勃起功能障碍B.早泄C.阴茎异常勃起D.精索静脉曲张E.输精管道梗阻 [单选,A1型题]提示膀胱损伤的表现是()A.血尿B.假性尿失禁C.排尿障碍而膀胱空虚D.导尿管不易插入E.下腹部腹膜刺激征 [单选]Alifeboatisweighttestedbyloweringtonearthewaterandloadingtocapacitywithweightevenlydistributed.Itisthenloweredintothewaterandreleased.Thistestmustbedoneatleastonceevery().A.6monthsB.12monthsC.18monthsD.24month [单选,A型题]下列哪种片剂用药后可缓缓释药、维持疗效几周、几月甚至几年()A、多层片B、植入片C、包衣片D、肠溶衣片E、缓释片 [单选]糖尿病微血管病变特异改变是()A.眼底微血管瘤B.肾小球结节性硬化C.眼底动脉硬化D.毛细血管基底膜增厚E.动脉粥样硬化 [单选,A型题]破伤风痉挛毒素()A.抑制多种细胞的蛋白质合成B.阻断上下神经元之间的正常抑制性神经冲动传递C.抑制胆碱能运动神经释放乙酰胆碱D.激活肠粘膜腺苷环化酶,增高细胞内cAMP水平E.作用于呕吐中枢 [填空题]电力机车用辅助机组一般采用()电机。 [单选]在A1.3建筑物区架设的10-20kV的架空线路,其轴线与1.3建筑物不应小于电杆高度的()。A.1倍B.1.2倍C.1.5倍D.2倍 [多选]施工现场选择水源的基本原则是()。A.就近选用企业废水B.选用天然水源C.企业、工厂的正式供水管道D.就近选用海水E.利用附近居民区或正式供水管道 [多选]下列各项中,影响利润表“所得税费用”项目金额的有()。A.当期应交所得税B.递延所得税收益C.递延所得税费用D.代扣代交的个人所得税 [填空题]超声诊断胆囊内结石是在胆囊内显示出______。 [单选]甲公司一次性出资300万元购买大型生产设备,预计该固定资产投资项目投资当年可获净利40万元,第2年开始每年递增5万元,投资项目有效期6年,并按直线法折旧(不考虑净残值)。该投资项目的投资回收期为()年。A.3.14B.5C.3.45D.4.56 [单选]公路供配电线路构成中,下列选项中错误的是()。A.10kV高压线路可采用架空电线路或电缆线路B.10kV高压线路只能采用电缆线路C.低压配电线路一般采用电缆线路D.按电压等级可分为10kV高压线路、380/220V低压配电线路 [单选]上层建筑甲板上的空气管自甲板至水可能进入下面的那一点的高度至少为()。A、600mmB、760mmC、450mmD、380mm [单选]石油基本上由碳、氢、()等五种元素组成。A、硫、钠、氧B、硫、氮、氧C、硫、氮、镁D、氮、氧、钾 [单选]下列各项中哪项是食管癌最典型的临床症状()A.咽下疼痛B.食管反流C.进行性咽下困难D.上消化道出血E.消瘦、恶病质 [单选]在短时记忆中,把几个孤立的项目结合成一个有意义的单位来识记称为()A.组块B.编码C.项目D.容量 [单选]关于类风湿关节炎患者行关节镜手术治疗,叙述正确的是()。A.关节镜滑膜切除术适合在类风湿关节炎疾病晚期,伴有明显滑膜炎、关节狭窄的患者B.经积极药物治疗6个月后患者仍有关节积液和滑膜炎C.关节镜下滑膜切除术是治疗类风湿关节炎的根治手术D.通过关节镜手术可修补损伤 [判断题]海绵动物主要生活于海水中,全部营漂浮生活。()A.正确B.错误 [单选]以下关于石油库防火堤说法正确的是()。A.防火堤应采用非燃烧材料建造B.防火堤应能承受所容纳油品的静压力且不应泄漏C.立式油罐防火堤的计算高度应保证堤内有效容积需要D.防火堤的实高不应低于1mE.防火堤的实高不宜高于2.2m [单选]应隔离治疗的皮肤病是()A.带状疱疹B.盘状红斑狼疮C.疥疮D.药物性皮炎E.丘疹样荨麻疹 [单选]我国社会信用管理体制选择:()。A.以商业征信公司形成的管理体系B.以中央银行为主体建立的管理体系C.以行业信用自律管理为核心的体系D.在国家信用管理总局领导下的信用管理体制 [单选]决定深度知觉的主要线索是()A.生理线索B.运动透视C.两眼视差D.结构级差 [多选]根据劳动合同法律制度的规定,下列情形中,职工不能享受当年年休假的有()。A,依法享受寒暑假,其休假天数多于年休假天数的B.请事假累计20天以上,且单位按照规定不扣工资的C.累计工作满1年不满10年,请病假累计2个月以上的D.累计工作满20年以上,请病假累计满3个月的 [单选,A1型题]诊断慢性支气管炎的主要依据是()A.病史B.阳性体征C.胸部X线检查D.心电图改变E.肺功能检查 [单选,A1型题]以下哪个选项是阳和汤的主治病证()A.五更泻B.阴疽C.大头瘟D.丹毒E.喑痱 [单选]()是指企业的采购部门根据过去和许多供应商打交道的经验,选取供货企业,并订购过去采购的同类产业用品。A.修正重购B.直接重购C.新购D.间接重购
