重庆大学热力学第一定律习题答案(鞠治刚)
大学物理化学1-热力学第一定律课后习题及答案

热力学第一定律课后习题一、是非题下列各题中的叙述是否正确?正确的在题后括号内画“√”,错误的画“⨯”。
1.在定温定压下,CO2由饱和液体转变为饱和蒸气,因温度不变,CO2的热力学能和焓也不变。
( )2. d U = nC V,m d T这个公式对一定量的理想气体的任何pVT过程均适用。
( )3. 一个系统从始态到终态,只有进行可逆过程才有熵变。
( )4. 25℃时H2(g)的标准摩尔燃烧焓等于25℃时H2O(g)的标准摩尔生成焓。
( )5. 稳定态单质的∆f H(800 K) = 0。
( )二、选择题选择正确答案的编号,填在各题后的括号内:1. 理想气体定温自由膨胀过程为:()。
(A)Q > 0;(B)∆U < 0;(C)W <0;(D)∆H = 0。
2. 对封闭系统来说,当过程的始态和终态确定后,下列各项中没有确定的值的是:( )。
( A ) Q;( B ) Q+W;(C ) W( Q = 0 );( D ) Q( W = 0 )。
3. pVγ = 常数(γ = C p,m/C V,m)适用的条件是:( )(A)绝热过程;( B)理想气体绝热过程;( C )理想气体绝热可逆过程;(D)绝热可逆过程。
4. 在隔离系统内:( )。
( A ) 热力学能守恒,焓守恒;( B ) 热力学能不一定守恒,焓守恒;(C ) 热力学能守恒,焓不一定守恒;( D) 热力学能、焓均不一定守恒。
5. 从同一始态出发,理想气体经可逆与不可逆两种绝热过程:( )。
( A )可以到达同一终态;( B )不可能到达同一终态;( C )可以到达同一终态,但给环境留下不同影响。
6. 当理想气体反抗一定的压力作绝热膨胀时,则:( )。
( A )焓总是不变;(B )热力学能总是增加;( C )焓总是增加;(D )热力学能总是减少。
7. 已知反应H2(g) +12O2(g) ==== H2O(g)的标准摩尔反应焓为∆r H(T),下列说法中不正确的是:()。
大学物理化学1-热力学第一定律课后习题及答案

热力学第一定律课后习题一、是非题下列各题中的叙述是否正确?正确的在题后括号内画“√”,错误的画“⨯”。
1.在定温定压下,CO2由饱和液体转变为饱和蒸气,因温度不变,CO2的热力学能和焓也不变。
( )2. d U = nC V,m d T这个公式对一定量的理想气体的任何pVT过程均适用。
( )3. 一个系统从始态到终态,只有进行可逆过程才有熵变。
( )4. 25℃时H2(g)的标准摩尔燃烧焓等于25℃时H2O(g)的标准摩尔生成焓。
( )5. 稳定态单质的∆f H(800 K) = 0。
( )二、选择题选择正确答案的编号,填在各题后的括号内:1. 理想气体定温自由膨胀过程为:()。
(A)Q > 0;(B)∆U < 0;(C)W <0;(D)∆H = 0。
2. 对封闭系统来说,当过程的始态和终态确定后,下列各项中没有确定的值的是:( )。
( A ) Q;( B ) Q+W;(C ) W( Q = 0 );( D ) Q( W = 0 )。
3. pVγ = 常数(γ = C p,m/C V,m)适用的条件是:( )(A)绝热过程;( B)理想气体绝热过程;( C )理想气体绝热可逆过程;(D)绝热可逆过程。
4. 在隔离系统内:( )。
( A ) 热力学能守恒,焓守恒;( B ) 热力学能不一定守恒,焓守恒;(C ) 热力学能守恒,焓不一定守恒;( D) 热力学能、焓均不一定守恒。
5. 从同一始态出发,理想气体经可逆与不可逆两种绝热过程:( )。
( A )可以到达同一终态;( B )不可能到达同一终态;( C )可以到达同一终态,但给环境留下不同影响。
6. 当理想气体反抗一定的压力作绝热膨胀时,则:( )。
( A )焓总是不变;(B )热力学能总是增加;( C )焓总是增加;(D )热力学能总是减少。
7. 已知反应H2(g) +12O2(g) ==== H2O(g)的标准摩尔反应焓为∆r H(T),下列说法中不正确的是:()。
第一章习题解答

第一章热力学第一定律思考题答案一、是非题1.√2.×3.×4.×5.×6.×7.√8.√9.×10.×11.×12.×13.×14.×15.√二、选择题1.D 2.D 3.D 4.C 5.D 6.B 7.B 8.C 9.D 10.D 11.B 12.D 13.A 14.D 15.C 16.D习题解答1. 请指出下列公式的适用条件:(1) △H=Q p;(2) △U=Q V;(3)W=-nRlnV2/V1解:(1)封闭系统,恒压不做其他功。
(2)封闭系统,恒容不做其他功。
(3)封闭系统,理想气体恒温可逆过程。
2. 用热力学概念判断下列各过程中功、热、热力学能和焓的变化值:(1)理想气体自由膨胀;(2)van der Waals气体等温自由膨胀;(3)Zn(s)+2HCl(l)===ZnCl2(l)+H2(g)进行非绝热等压反应;(4)H2(g)+C12(g)===2HCl(g)在绝热钢瓶中进行;(5)常温、常压下水结成冰(273.15K,101.325kPa)。
解:(1)W=0,Q=0,△U=0,△H=0(2)W=0,Q>0,△U>0,△H不能确定。
(3)W<0,Q<0,△U<0,△H<0(4) W=0,Q=0,△U=0,△H>0(5) W>0,Q<0,△U<0,△H<03. 在相同的温度和压力下,一定量氢气和氧气从4种不同的途径生成相同终态的水;(1)氢气在氧气中燃烧;(2)爆鸣;(3)氢氧热爆炸;(4)氢氧燃料电池。
请问这4种变化途径的热力学能和焓的变化值是否相同?解:相同。
4. 一定量的水,从海洋蒸发变为云,云在高山上变为雨、雪,并凝结成冰。
冰、雪融化变成水流入江河,最后流入大海。
整个循环,水的热力学能和焓的变化是多少?解:零。
大学物理 热力学第一定律 习题(附答案)

A13 = Q13 = 1.25 × 10 4 ( J)
(5)由(1)有系统终态的体积为
hi
5 R , R = 8.31 J / mol ⋅ K 。 2
na
T V3 = V2 ( 2 ) γ−1 = 40 × 21. 5 = 113 ( l) T1 nRT3 2 × 8.31 × 300 p3 = = ÷ 1.013 × 10 5 = 0.44 ( atm) −3 V3 113 × 10
0 . 44
O
om
p (atm ) 1 2
3
三、计算题: 1.2 mol 初始温度为 27 � C ,初始体积为 20 L 的氦气,先等压过程膨胀到体积加倍, 然 后绝热过程膨胀回到初始温度。 (1)在 p-V 平面上画出过程图。 (2)在这一过程中系统总吸热是多少? (3)系统内能总的改变是多少? (4)氦气对外界做的总功是多少?其中绝热膨胀过程对外界做功是多少? (5)系统终态的体积是多少?
5 = 1 × R × 60 = 1.25 × 10 3 ( J) 2
γ
(B) p 0 γ (D) p 0 / 2
(γ = C
p
/ Cv )
p0
解:绝热自由膨胀过程中 Q = 0,A = 0,由热力学第一定律,有 ∆ E = 0 ,膨胀前后系统
[
]
(A) (B) (C) (D)
这是一个放热降压过程 这是一个吸热升压过程 这是一个吸热降压过程 这是一个绝热降压过程
将状态 a、b 分别与 o 点相连有
om
A
O
V1
V2
V
T B
C
Q
V
等压过程中吸收了相同的热量,则它们对外做功之比为 A 1: A 2 = (各量下角标 1 表示氢气,2 表示氦气)
第一章_热力学第一定律_习题答案

第一章热力学第一定律练习参考答案1. 一隔板将一刚性绝热容器分成左右两侧,左室气体的压力大于右室气体的压力。
现将隔板抽去,左、右气体的压力达到平衡。
若以全部气体作为体系,则ΔU、Q、W为正?为负?或为零?解:∵U=02. 试证明1mol理想气体在恒后下升温1K时,气体与环境交换的功等于摩尔气体常数R 。
解: 恒压下,W= - p外ΔV= - p外p TnR∆= - R(p外= p,n=1mol,ΔT=1 )3. 已知冰和水的密度分别为0.92×103 kg•m-3和1.0×103 kg•m-3,现有1mol 的水发生如下变化:(1) 在100℃、101.325kPa下蒸发为水蒸气,且水蒸气可视为理想气体;(2) 在0℃、101.325kPa下变为冰。
试求上述过程体系所作的体积功。
解: 恒压、相变过程,(1)W= -p外(V2 –V1) = - 101.325×103×⎪⎭⎫⎝⎛⨯⨯-⨯⨯⨯33100.1018.0110325.101373314.81=-3100 ( J )(2) W= - p外(V2 –V1) = - 101.325×103×⎪⎭⎫⎝⎛⨯⨯-⨯⨯33100.1018.011092.0018.01= -0.16 ( J )4. 若一封闭体系从某一始态变化到某一终态。
(1) Q、W、Q-W、ΔU是否已完全确定;(2) 若在绝热条件下,使体系从某一始态变化到某一终态,则(1)中的各量是否已完全确定?为什么?解:(1)Q+W、ΔU完全确定。
( Q+W=ΔU;Q、W与过程有关)(2) Q、W、Q+W、ΔU完全确定。
(Q=0,W = ΔU)5. 1mol理想气体从100℃、0.025m3经下述四个过程变为100℃、0.1m3:(1) 恒温可逆膨胀;(2) 向真空膨胀;(3) 恒外压为终态压力下膨胀;(4) 恒温下先以恒外压等于0.05m 3的压力膨胀至0.05m 3,再以恒外压等于终态压力下膨胀至0.1m 3。
大学物理化学1-热力学第一定律课后习题及答案

热力学第一定律课后习题一、是非题下列各题中的叙述是否正确?正确的在题后括号内画“√”,错误的画“⨯”。
1.在定温定压下,CO2由饱和液体转变为饱和蒸气,因温度不变,CO2的热力学能和焓也不变。
( )2. d U = nC V,m d T这个公式对一定量的理想气体的任何pVT过程均适用。
( )3. 一个系统从始态到终态,只有进行可逆过程才有熵变。
( )4. 25℃时H2(g)的标准摩尔燃烧焓等于25℃时H2O(g)的标准摩尔生成焓。
( )5. 稳定态单质的∆f H(800 K) = 0。
( )二、选择题选择正确答案的编号,填在各题后的括号内:1. 理想气体定温自由膨胀过程为:()。
(A)Q > 0;(B)∆U < 0;(C)W <0;(D)∆H = 0。
2. 对封闭系统来说,当过程的始态和终态确定后,下列各项中没有确定的值的是:( )。
( A ) Q;( B ) Q+W;(C ) W( Q = 0 );( D ) Q( W = 0 )。
3. pVγ = 常数(γ = C p,m/C V,m)适用的条件是:( )(A)绝热过程;( B)理想气体绝热过程;( C )理想气体绝热可逆过程;(D)绝热可逆过程。
4. 在隔离系统内:( )。
( A ) 热力学能守恒,焓守恒;( B ) 热力学能不一定守恒,焓守恒;(C ) 热力学能守恒,焓不一定守恒;( D) 热力学能、焓均不一定守恒。
5. 从同一始态出发,理想气体经可逆与不可逆两种绝热过程:( )。
( A )可以到达同一终态;( B )不可能到达同一终态;( C )可以到达同一终态,但给环境留下不同影响。
6. 当理想气体反抗一定的压力作绝热膨胀时,则:( )。
( A )焓总是不变;(B )热力学能总是增加;( C )焓总是增加;(D )热力学能总是减少。
7. 已知反应H2(g) +12O2(g) ==== H2O(g)的标准摩尔反应焓为∆r H(T),下列说法中不正确的是:()。
第一章 热力学第一定律 习题答案

第一章热力学第一定律练习参考答案1. 一隔板将一刚性绝热容器分成左右两侧,左室气体的压力大于右室气体的压力。
现将隔板抽去,左、右气体的压力达到平衡。
若以全部气体作为体系,则ΔU、Q、W为正?为负?或为零?解:∵U=02. 试证明1mol理想气体在恒后下升温1K时,气体与环境交换的功等于摩尔气体常数R 。
解: 恒压下,W= - p外ΔV= - p外p TnR∆= - R(p外= p,n=1mol,ΔT=1 )3. 已知冰和水的密度分别为0.92×103 kg•m-3和1.0×103 kg•m-3,现有1mol 的水发生如下变化:(1) 在100℃、101.325kPa下蒸发为水蒸气,且水蒸气可视为理想气体;(2) 在0℃、101.325kPa下变为冰。
试求上述过程体系所作的体积功。
解: 恒压、相变过程,(1)W= -p外(V2 –V1) = - 101.325×103×⎪⎭⎫⎝⎛⨯⨯-⨯⨯⨯33100.1018.0110325.101373314.81=-3100 ( J )(2) W= - p外(V2 –V1) = - 101.325×103×⎪⎭⎫⎝⎛⨯⨯-⨯⨯33100.1018.011092.0018.01= -0.16 ( J )4. 若一封闭体系从某一始态变化到某一终态。
(1) Q、W、Q-W、ΔU是否已完全确定;(2) 若在绝热条件下,使体系从某一始态变化到某一终态,则(1)中的各量是否已完全确定?为什么?解:(1)Q+W、ΔU完全确定。
( Q+W=ΔU;Q、W与过程有关)(2) Q、W、Q+W、ΔU完全确定。
(Q=0,W = ΔU)5. 1mol理想气体从100℃、0.025m3经下述四个过程变为100℃、0.1m3:(1) 恒温可逆膨胀;(2) 向真空膨胀;(3) 恒外压为终态压力下膨胀;(4) 恒温下先以恒外压等于0.05m 3的压力膨胀至0.05m 3,再以恒外压等于终态压力下膨胀至0.1m 3。
热力学第一定律习题及答案

热力学第一定律习题一、单选题1) 如图,在绝热盛水容器中,浸入电阻丝,通电一段时间,通电后水及电阻丝的温度均略有升高,今以电阻丝为体系有:( )A. W =0,Q <0,U <0B. W <0,Q <0,U >0C. W <0,Q <0,U >0D. W <0,Q =0,U >02) 如图,用隔板将刚性绝热壁容器分成两半,两边充入压力不等的空气(视为理想气体),已知p右> p左,将隔板抽去后: ( )A. Q=0, W =0, U =0B. Q=0, W <0, U >0C. Q >0, W <0, U >0D. U =0, Q=W03)对于理想气体,下列关系中哪个是不正确的:( )A. (∂U/∂T)V=0B. (∂U/∂V)T=0C. (∂H/∂p)T=0D. (∂U/∂p)T=04)凡是在孤立孤体系中进行的变化,其U 和H 的值一定是:( )A. U >0, H >0B. U =0, H=0C. U <0, H <0D. U =0,H 大于、小于或等于零不能确定。
5)在实际气体的节流膨胀过程中,哪一组描述是正确的: ( )A. Q >0, H=0, p < 0B. Q=0, H <0, p >0C. Q=0, H =0, p <0D. Q <0, H =0, p <06)如图,叙述不正确的是:( )A.曲线上任一点均表示对应浓度时积分溶解热大小B.H1表示无限稀释积分溶解热C.H2表示两浓度n1和n2之间的积分稀释热D.曲线上任一点的斜率均表示对应浓度时HCl的微分溶解热7)H=Q p此式适用于哪一个过程: ( )A.理想气体从101325Pa反抗恒定的10132.5Pa膨胀到10132.5sPaB.在0℃、101325Pa下,冰融化成水C.电解CuSO4的水溶液D.气体从(298K,101325Pa)可逆变化到(373K,10132.5Pa )8) 一定量的理想气体,从同一初态分别经历等温可逆膨胀、绝热可逆膨胀到具有相同压力的终态,终态体积分别为V1、V2。
第二章-热力学第一定律--题加答案
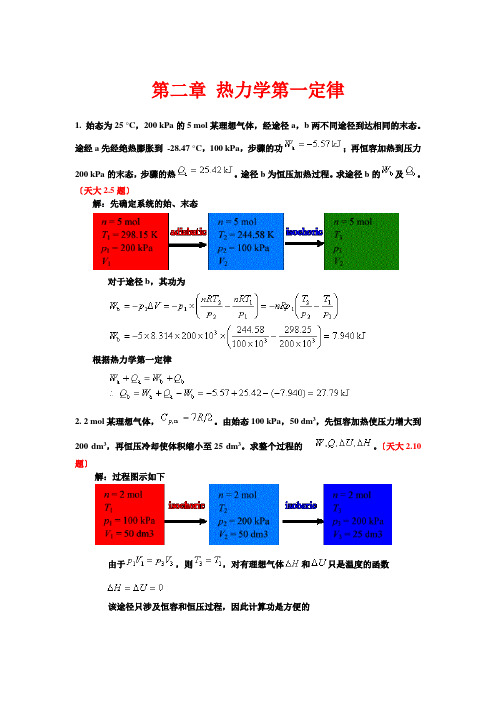
第二章热力学第一定律1. 始态为25 °C,200 kPa的5 mol某理想气体,经途径a,b两不同途径到达相同的末态。
途经a先经绝热膨胀到-28.47 °C,100 kPa,步骤的功;再恒容加热到压力200 kPa的末态,步骤的热。
途径b为恒压加热过程。
求途径b的及。
〔天大2.5题〕解:先确定系统的始、末态对于途径b,其功为根据热力学第一定律2. 2 mol某理想气体,。
由始态100 kPa,50 dm3,先恒容加热使压力增大到200 dm3,再恒压冷却使体积缩小至25 dm3。
求整个过程的。
〔天大2.10题〕解:过程图示如下由于,则,对有理想气体和只是温度的函数该途径只涉及恒容和恒压过程,因此计算功是方便的根据热力学第一定律3. 单原子理想气体A与双原子理想气体B的混合物共5 mol,摩尔分数,始态温度,压力。
今该混合气体绝热反抗恒外压膨胀到平衡态。
求末态温度及过程的。
〔天大2.18题〕解:过程图示如下分析:因为是绝热过程,过程热力学能的变化等于系统与环境间以功的形势所交换的能量。
因此,单原子分子,双原子分子由于对理想气体U和H均只是温度的函数,所以4. mol〔单原子分子〕理想气体,由、300K按以下两种不同的途径压缩到、300K,试计算并比较两途径的Q、W、ΔU及ΔH。
(1〕等压冷却,然后经过等容加热;(2)等容加热,然后经过等压冷却。
解:C p,m=2.5R, C V,m〔1〕、、、300K30.09858 dm30.09858 dm3Q=Q1+Q2××××(300-119.8)=-3745+2247=-1499(J)W=W1+W2×103×(0.09858-0.2470)+0=1499(J)ΔU=Q+W=0ΔH=ΔU+Δ(pV)××0.2470=0〔2〕、、、300K330.09858 dm3Q=Q1+Q2××××(300-751.6)=5632-9387=-3755(J)W=W1+W2×103×(0.09858-0.2470) =3755(J)ΔU=Q+W=0ΔH=ΔU+Δ(pV)××0.2470=0计算结果说明,Q、W与途径有关,而ΔU、ΔH与途径无关。
第一定律习题及解答

第二章习题及解答1. 如果一个系统从环境吸收了40J的热,而系统的热力学能却增加了200J,问系统从环境得到了多少功?如果该系统在膨胀过程中对环境作了10kJ的功,同时吸收了28kJ的热,求系统热力学能的变化值。
解Q1=40J ΔU1=200J W1=ΔU1- Q1=160JW2= -10kJ Q2=28kJ ΔU2= Q2+W2=18kJ2. 有10 mol的气体(设为理想气体),压力为1000 kPa,温度为300K,分别求出等温时下列过程的功:(1)在空气压力为100 kPa时,体积胀大1dm3;(2)在空气压力为100 kPa时,膨胀到气体压力也是100 kPa;(3)等温可逆膨胀到气体压力为100 kPa。
解(1)属于等外压膨胀过程W1=-p环ΔV=-100kP a×1dm3=-100J(2)也是等外压膨胀过程W2=-p环(V2-V1)=-nRT(1-p2/p1)=-10 mol×8.314 J·K-1·mol-1×300K(1-100/1000)=-22448J(3)等温可逆膨胀过程W3=-nRTln(p1/p2)=-10 mol×8.314 J·K-1·mol-1×300K×ln(1000/100)=-57431J4. 在291K和pӨ压力下,1mol Zn(s)溶于足量稀盐酸中,置换出1mol H2并放热152kJ。
若以Zn和盐酸为体系,求该反应所作的功及体系内能的变化。
解Zn(s)+2HCl(aq) = ZnCl2(aq)+H2(g)W = -pΔV = -p(V2-V1)≈-pV(H2) = -nRT= -(1mol)×(8.314J·K-1·mol-1)×(291K)= -2.42kJΔU = Q+W = (-152-2.42)kJ = -154.4kJ5. 在298K时,有2mol N2(g),始态体积为15dm3,保持温度不变,经下列三个过程膨胀到终态体积为50 dm3,计算各过程的ΔU、ΔH、W和Q的值。
热力学第一定律习题及答案

热力学第一定律习题 一、单选题1)如图,在绝热盛水容器中,浸入电阻丝,通电一段时间,通电后水及电阻丝的温度均略 有升高,今以电阻丝为体系有: ()绝热A. W =0, Q <0, U <0B. W <0, Q <0, U >0C. W <0, Q <0, U >0D. W <0, Q =0, U >0 2)如图,用隔板将刚性绝热壁容器分成两半,两边充入压力不等的空气 (视为理想气体), 已知P 右> P 左,将隔板抽去后:()n mol H 2O / 1 mol HC1曲线上任一点均表示对应浓度时积分溶解热大小 H I 表示无限稀释积分溶解热 H 2表示两浓度n i 和%之间的积分稀释热D.曲线上任一点的斜率均表示对应浓度时 HCI 的微分溶解热7) H = Q p 此式适用于哪一个过程:()A. 理想气体从101325Pa 反抗恒定的10132.5Pa 膨胀到10132.5sPaB. 在0C 、101325Pa 下,冰融化成水C. 电解CuS04的水溶液D. 气体从(298K , 101325Pa )可逆变化到(373K , 10132.5Pa )8) 一定量的理想气体,从同一初态分别经历等温可逆膨胀、绝热可逆膨胀到具有相同压力 的终态,终态体积分别为 匕、V 2。
() A. V 1 < V 2 B. V 1 = V 2 C. V 1 > V 2 D.无法确定 9) 某化学反应在恒压、 绝热和只作体积功的条件下进行, 体系温度由T i 升高到T 2,则此过A. B. C. D. 空气 %空气Q = 0, W = U = 0Q = 0, WU >0 Q >0, WU >0 U = 0, Q = W 0对于理想气体,下列关系中哪个是不正确的: ()(::U/ 汀)V = 0 B. (:U/::V )T = 0 C. C :H/_:P )T =0 D. ( :U/::p )T = 凡是在孤立孤体系中进行的变化,其 U 和 H 的值- U HU = H =U H <0U = 0, H 大于、小于或等于零不能确定。
物理化学热力学第一定律习题答案

第二章 热力学第一定律2-1 1mol 理想气体于恒定压力下升温1℃,试求过程中气体与环境交换的功W 。
解:体系压力保持恒定进行升温,即有P 外=P ,即反抗恒定外压进行膨胀,JT nR nRT nRT pV pV V V p W amb 314.8)(121212-=∆-=+-=+-=--= 2-2 系统由相同的始态经过不同途径达到相同的末态。
若途径a 的Q a =2.078kJ ,W a = -4.157kJ ;而途径b 的Q b = -0.692kJ 。
求W b 。
解:应用状态函数法。
因两条途径的始末态相同,故有△U a =△U b ,则 b b a a W Q W Q +=+ 所以有,kJ Q W Q W b a a b 387.1692.0157.4078.2-=+-=-+=2-3 4mol 某理想气体,温度升高20℃,求△H -△U 的值。
解: 方法一: 665.16J208.3144 )20()( 2020,,20,20,=⨯⨯=-+==-=-=∆-∆⎰⎰⎰⎰++++T K T nR nRdT dT C C n dT nC dT nC U H KT T K T T m V m p K T T m V KT Tm p方法二:可以用△H=△U+△(PV)进行计算。
2-4 某理想气体, 1.5V m C R =。
今有该气体5 mol 在恒容下温度升高50℃,求过程的W ,Q ,△H 和△U 。
解:恒容:W=0;根据热力学第一定律,:W=0,故有Q=△U=3.118kJ2-5 某理想气体, 2.5V m C R =。
今有该气体5 mol 在恒压下温度降低50℃,求过程的W ,Q ,△H 和△U 。
解: kJ J K nC T K T nC dT nC U m V m V KT T m V 196.55196503145.8255)50( )50(,,50,-=-=⨯⨯⨯-=-⨯=--==∆⎰-2-6 1mol 某理想气体,R C m P 27,=。
《热力学第一定律》习题及答案

《热力学第一定律》习题及答案选择题1.热力学第一定律ΔU=Q+W 只适用于()(A) 单纯状态变化 (B) 相变化 (C) 化学变化 (D) 封闭物系的任何变化答案:D2.关于热和功, 下面的说法中, 不正确的是(A) 功和热只出现于系统状态变化的过程中, 只存在于系统和环境间的界面上(B) 只有在封闭系统发生的过程中, 功和热才有明确的意义(C) 功和热不是能量, 而是能量传递的两种形式, 可称之为被交换的能量(D) 在封闭系统中发生的过程中, 如果内能不变, 则功和热对系统的影响必互相抵消答案:B2.关于焓的性质, 下列说法中正确的是()(A) 焓是系统内含的热能, 所以常称它为热焓 (B) 焓是能量, 它遵守热力学第一定律(C) 系统的焓值等于内能加体积功 (D) 焓的增量只与系统的始末态有关答案:D。
因焓是状态函数。
3.涉及焓的下列说法中正确的是()(A) 单质的焓值均等于零 (B) 在等温过程中焓变为零 (C) 在绝热可逆过程中焓变为零(D) 化学反应中系统的焓变不一定大于内能变化答案:D。
因为焓变ΔH=ΔU+Δ(pV),可以看出若Δ(pV)<0则ΔH<ΔU。
4.下列哪个封闭体系的内能和焓仅是温度的函数()(A) 理想溶液(B) 稀溶液(C) 所有气体(D) 理想气体答案:D5.与物质的生成热有关的下列表述中不正确的是()(A) 标准状态下单质的生成热都规定为零 (B) 化合物的生成热一定不为零 (C) 很多物质的生成热都不能用实验直接测量(D) 通常所使用的物质的标准生成热数据实际上都是相对值答案:A。
按规定,标准态下最稳定单质的生成热为零。
6.dU=CvdT及dUm=Cv,mdT适用的条件完整地说应当是()(A) 等容过程 (B)无化学反应和相变的等容过程 (C) 组成不变的均相系统的等容过程(D) 无化学反应和相变且不做非体积功的任何等容过程及无反应和相变而且系统内能只与温度有关的非等容过程答案:D7.下列过程中, 系统内能变化不为零的是()(A) 不可逆循环过程 (B) 可逆循环过程 (C) 两种理想气体的混合过程 (D) 纯液体的真空蒸发过程答案:D。
第一章热力学第一定律答案

第一章热力学第一定律答案第一章热力学练习题参考答案一、判断题解答:1.错。
对实际气体不适应。
2.错。
数量不同,温度可能不同。
3.错。
没有与环境交换能量,无热可言;天气预报的“热”不是热力学概念,它是指温度,天气很热,指气温很高。
4.错。
恒压(等压)过程是体系压力不变并与外压相等,恒外压过程是指外压不变化,体系压力并不一定与外压相等。
5.错。
一般吸收的热大于功的绝对值,多出部分增加分子势能(内能)。
6.错。
例如理想气体绝热压缩,升温但不吸热;理想气体恒温膨胀,温度不变但吸热。
7.第一句话对,第二句话错,如理想气体的等温过程ΔU = 0,ΔH = 0,U 、H 不变。
8.错,两个独立变数可确定系统的状态只对组成一定的均相组成不变系统才成立。
9.错,理想气体U = f (T ),U 与T 不是独立的。
描述一定量理想气体要两个独立变量。
10.第一个结论正确,第二个结论错,因Q+W =ΔU ,与途径无关。
11.错,Q V 、Q p 是过程变化的量、不是由状态决定的量,该式仅是数值相关而已。
在一定条件下,可以利用ΔU ,ΔH 来计算Q V 、Q p ,但不能改变其本性。
12.错,(1)未说明该过程的非体积功W '是否为零;(2)若W ' = 0,该过程的热也只等于系统的焓变,而不是体系的焓。
13.对。
因为理想气体热力学能、焓是温度的单值函数。
14.错,这是水的相变过程,不是理想气体的单纯状态变化,ΔU > 0。
15.错,该过程的p 环= 0,不是恒压过程,也不是可逆相变,吸的热,增加体系的热力学能。
吸的热少于30.87 kJ 。
16.错,在25℃到120℃中间,水发生相变,不能直接计算。
17.错,H = f (T ,p )只对组成不变的均相封闭系统成立,该题有相变。
18.错,Δ(pV )是状态函数的增量,与途径无关,不一定等于功。
19.错,环境并没有复原,卡诺循环不是原途径逆向返回的。
热力学第一定律习题解答

第七章 热力学第一定律一 选择题1. 图为质量一定的某理想气体由初态a 经两过程到达末状态c ,其中abc 为等温过程,则 ( )A . adc 也是一个等温过程B . adc 和abc 过程吸收的热量相等C . adc 过程和abc 过程做功相同D . abc过程和adc 过程气体内能变化相同解:热量和功均是过程量,内能是状态量。
故答案选D 。
2. 有两个相同的容器,容积不变,一个盛有氦气,另一个盛有氢气,(看成刚性分子),它们的压强和温度都相等,现将5J 的热量传给氢气,使氢气的温度升高,如果使氦气也升高同样的温度,则应向氦气传递热量是 ( )A . 6J B. 5J C. 3J D. 2J解:氦气是单原子分子,自由度为3,氢气是双原子分子,自由度为5。
根据理想气体的状态方程,两种气体的摩尔数相同。
容器容积不变,气体吸收的热量全部转化为内能。
再根据理想气体的内能公式,使氦气也升高同样的温度,应向氦气传递热量是3J 。
答案选C 。
3. 1mol 的单原子分子理想气体从状态A 变为状态B ,如果不知是什么气体,变化过程也不知道,但A 、B 两态的压强、体积和温度都知道,则可求出 ( )选择题1图A.气体所作的功B.气体内能的变化C.气体传给外界的热量D.气体的质量 解 答案:B4. 已知系统从状态A 经某一过程到达状态B ,过程吸热10J ,系统内能增量为5J 。
现系统沿原过程从状态B 返回状态A ,则系统对外作功是 ( ) A. -15J B. -5J C. 5J D. 15J解 热力学第一定律的表达式W U Q +∆=,系统从A 态经某一过程到达B 态时系统做的功为5510=-=∆-=U Q W J 。
因此当系统沿原过程从B 态返回A 态时,系统对外做功为-5J 。
因此答案选B 。
5. 用公式T C U V ∆=∆m ,ν计算理想气体内能增量时,此式 ( ) A. 只适用于准静态的等体过程 B. 只适用于一切等体过程 C. 只适用于一切准静态过程D. 适用于一切始末态为平衡态的过程解 答案选D6. 对于室温下的双原子分子理想气体,在等压膨胀的情况下,系统对外所作的功与从外界吸收的热量之比W / Q 等于( )A. 2/3B.1/2C.2/5D.2/7 解 答案选 D7. 理想气体初态的体积为V 1,经等压过程使体积膨胀到V 2,则在此过程中,气体对外界作 ( )A.正功,气体的内能增加B.正功,气体的内能减少C.负功,气体的内能增加D.负功,气体的内能减少解等压膨胀过程系统对外作正功,由于压强不变体积增加,所以温度升高,因此气体的内能增加。
热力学第一定律答案参考资料

第一章热力学第一定律习题参考答案选择题1.[答](B)2.[答](A)因为整个刚性绝热容器为体系,与环境无功和热的传递。
3.[答(D)4.[答](B)5.[答](A )6.[答](c)7.[答](B)8.[劄(B) 9.[答](D) 10.[答](D) 11.[答](B) 12.[答](B)13.[劄(C) 14.[答](C) 15.[答](B) 16.[答](D)17.[劄(D) △ U=Cv △ T=(3/2)R{(P 仃1/P 2)-T 1 18.[答](B)19.[劄(D)20.[答](C) 21.[答](A ) 填空题1. [答]一定大于(因为H = U + PV); 一定大于;因为△ H = △ U + ( △ n)RT,而△ n为正。
2. [答]△ U = 0 △ H = 03. [答]波义耳(Boyle's) 零4. [答](A ) = (b) = (c) > (d) >5. [答]0 ; P2V2- P 1V16. [答]Q v- Q p= △ nRT = -4988 J7. [答]△ r H m = Q p= Q v+ △ nRT_1△ c H m = (1/2) △ r H= -285.7 kJ.mol8. [答]△ r U m= -4816 kJ.mol -1△ r H m = -4826 kJ.mol -19. [答]△ G= ( E C P,B) (生成物)- (E C P,B) (反应物)10. [答]改变分子的能级;改变在分子能级上分布的分子数三.问答题:1. [答]只能看作绝热体系2. [答]前句不对。
(例:绝热膨胀,温度有变化但不吸热)后句也不对。
(例:相变过程,温度可以不变,但有热量变化)3. [答]错。
因为:(1) Q V为恒容条件下传递的能量,总是与过程伴随着的物理量。
(2) 当存在非体积功时,△ U = Q V- W f,△ U K Q V4. [答]不会沸腾。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
三、填空题 1、 , H U PV, , U 0, H U ( PV ) RTn 0 2、 , 3、 , , ( 因为H U ( PV ) VP 0 ), ( 因为Q 0 ) 4、 0,VP 5、 QV QP
n
( g ) RT
2 8.31451 300 4பைடு நூலகம்88.7 J
(g)
6、 r H m rU m RT
n
564 8.31451 298 ( 0 2 1 ) / 1000
571.43KJ, c H m ,H 2
1 r H m 285.72 KJ mol 1 2
r H m ( 298K ) 110.54 3 822.16 490.54 KJ / mol
B
C P ,m , B 3 (27.61 5.02 10 3 T ) 2 ( 14.1 29.7110 3 T )
3 R( T2 609.3 ) P外 ( V2 5 10 3 ) RT2 5 10 3 101.325 103 2 T2 390.0 K
2、解:Q 400103 0.5523 (850 25) (1 30%) 103 236937 KJ 236937 65.82KW h 3600 1000 1000 3、解:QP 24.48 (1083 25) 13560 63.54 63.54 1000 31.40 (1200 1083 ) 63.54 407615 213409 57819 678843 J 678.8 KJ
7、 rU m 602
1 4816KJ mol 1 0.125
1 ( g ) 4816 2 . 5 ( 7 11 ) 4826 KJ mol B
r H m rU m RT
8、
B
B
C p ,m ,B 0
9、 , , 10、 (因为H Q p 0), (因为H Q p 0) 11 、 两、物质的量
11 、O(Q 0,W U nCV ,m ( T1 T2 )
nR( T1 T2 ) p1V1 P2V2 ) 1 1
12、 (理想气体是这样的, 但是实际气体绝热自由 膨胀后温度会降低,分 子间有作用力) 13、 (公式表达式虽然一样 ,但是T的变化量并不一样) 14、 (热力学能的变化是由 Q和W共同作用的结果) 15、 (有其他功时H Q P) 16、 (反抗恒定外压绝热膨 胀属于绝热不可逆过程 ,过程S 0,末态熵增加) 17、 (概念混淆,压力不具 有加和性,属于强度性 质) 18、 (水汽化要吸热,所以 系统内能会增加) 19、 (向真空蒸发, w 0,Q U,而U H (P V) H nRT Q H nRT 30.87KJ 1 8.31451 353.1 / 1000 27.93KJ ,18题的说法错误也可由此 得证) 20、 (过程中有相变发生, 应该分段计算) 21 、 (应该是石墨) 22、O 23、O
-1 12、 350J mol (因为 H m C p,m T
7 7 5 7 RT RT U) 2 5 2 5
1 -1 13、 46.1KJ mol (因为 f H r H m m) 2
四、选择题
1 C
2 D
3 C
4 B
5 C
6 A
7 A
两途径的终态相同,因 为二者的T、V一样。 8、绝热系统。因为过程 对外做功。 9、错。系统的温度变化 可能会由功的交换引起 ,比如绝热压缩,无热 交换,但是系统温度升 高。 10、错。这只是说明无其 他功的定容过程 Q V可以用系统的U来度量,但是Q V依然为过程量。
11 、不会沸腾,内外温度 相等,没有传热。 12、前半部分对,后一句 话错,状态可能会发生 变化。比如理想气体绝 热自由膨胀, 不做功不吸热,但是状 态变化了,体积增大。 13、错。不可逆过程依然 可以逆向进行,只是系 统复原时环境不能同时 复原。 14、对。 15、对。前半部分叙述可 由热力学第一定律得证 :U 0, 而H U (P V) (P V),它并不守恒,比如 绝热钢瓶 中发生C CO 2 的反应,系统的焓会增 加VP。 (S) O 2 (g) (g) 16、不对,必须是理想气 体绝热可逆过程。 17、Q 0,W 0,U 0,H 0 18、不对,热力学能的变 化量可以通过功、热的 测定利用U Q - W计算,U 的绝对值是不知道的。
1) / 3 (4) 5、解: ( 2 (2) 6 (3)
r H m, 4 ( r H m,1 2 r H m, 2 6 r H m,3 ) / 3 (6.3 2 22.6 6 13.9) / 3 14.83KJ / m ol
55.85103 4、解( 1 )QP 30.30 (1000 298) 103 55.85 21271 KJ
1000 55.8510 (2)QP (14.10 29.7 103 T )dT 298 55.85 3
23434017 J 23434 KJ
9、解:Fe2O3( S )
f Hm 882.16
3C( S ) 0
2 Fe( S ) 0
3CO( g ) 110.54
a bT 91.55 201.67 10 3 T
14.1 29.7110 3 T 27.61 5.02 10 3 T
17.15 4.27 10 3 T
1 6、解:由SO2 ( g ) O2 ( g ) SO3 ( g ) 2 1 r H m f H m ( SO3 , g ) f H m ( SO2 , g ) f H m (O2 , g ) 2
1 f H ( SO , g ) H H ( SO , g ) H m 3 r m f m 2 f m (O2 , g ) 2 98.28 296.83 0 395.11KJ m ol1 由SO3 ( g ) H 2O(l ) H 2 SO4 (l )
热力学第一定律习题答 案 一、判断题
重庆大学热力学第一定律习题答案(鞠治刚)
1、 (状态改变,状态函数 不一定都发生变化) 2、 (水和水蒸气的比例不 能确定) 3、 (理想气体的热力学能 和温度并不相互独立) 4、 (由热力学第一定律知 道绝热压缩时系统温度 也会升高,考虑功的影 响) 5 (Q - W U,后者只要始终态分别 相同,则两种途径的变 化量U相同) 6、 (H Q P 适用于无其他功的等压 过程,比如对绝热系统 进行等压机械搅拌, Q 0,但是H 0)。 7、O(H U P V nRT) 8、 (因为相变属于复杂物 理变化,等T、P相变时的焓变即相变热 ,不等于0) 9、 (可逆循环需逆向进行 后系统和环境才会同时 复原) 10、 (这只是准静态过程, 不是可逆过程,可逆要 求此基础上无耗散效应 )
r H H ( H SO , l ) H ( SO , g ) H m f m 2 4 f m 3 f m ( H 2 O, l) f H ( H SO , l ) H H ( SO , g ) H m 2 4 r m f m 3 f m ( H 2 O, l)
19、 r H m ( B f H m ,B )P ( B f H m ,B )R
[ 1382 .8 2 ( 92.30 )] [ 2 ( 411.0 ) ( 811.3 )] 65.9 KJ m ol1
rU m r H m RT B ( g ) 65.9 8.31451 298 2 / 1000 60.94KJ m ol1
注:8、没有指明反应前后的温度,所以选D
11、J-T=-/Cp,所以选B
PV 1013.25 103 5 103 1、解:T1 609.3K R 8.31451 恒外压101.325KPa绝热膨胀:Q 0 W P外 ( V2 V1 ) 由热力学第一定律可知 :U Q W W P外 ( V2 V1 ) 3 U CV ,m ( T2 T1 ) R( T2 T1 ) 2 3 R( T2 609.3 ) P外 ( V2 5 10 3 ) 2 P2 P外 101.325 103 P外V2 RT2
130.29 395.11 285.83 811.23KJ m ol1
7、解:C (S) 2H 2 (g) CH 4 ( g ) f H m ,CH 4 , g C H m ,C , S 2 C H m , H 2 , g C H m ,CH 4 , g 3.93105 2 2.86 105 8.90 105 7.5 104 J / m ol 8、解: 2C (S) H 2 (g) C 2 H 2 ( g ) f H m ,C 2 H 2 , g 2 C H m ,C , S C H m , H 2 , g C H m ,C 2 H 2 , g 2 f H m ,CO2 , g f H m , H 2O ,l C H m ,C2 H 2 , g 2 3.93 105 285.85 1299.6 226.75KJ / m ol
8 D
9 B
10 A
11 B 21 A 31 D
12 C 22 C 32 B
13 B 23 B 33 C
14 D 24 A 34 B
15 D 25 A 35 D
