第二章 热力学第一定律(总复习题)
(完整word版)热力学第一定律复习题(13,10)

第二章 热力学第一定律:系统与环境间由于温差而交换的能量。
是物质分子无序运动的结果。
是过程量。
:除热以外的、在系统与环境间交换的所有其它形式的能量。
是物质分子有序运动的、恒压条件下,△H =Q p 。
系统状态变化时,计算系统与环境间交换的能量) 恒压反应热与恒容反应热的关系:Q p =Q V +∑νB (g)RT,21;()()p r p m r m r m m C H T H T dT ∆∆=∆+1. 当理想气体冲入一真空绝热容器后,其温度将(a) 升高(b) 降低(c) 不变(d) 难以确定(答案) c (△U=Q+W, ∵p外=0 , ∴W=0 ,又∵绝热,∴Q=0,所以△U=0)因为是真空故不做功,又因为是绝热故无热交换,故△U=0。
温度不变。
2. 当热力学第一定律写成d U = δQ–p d V时,它适用于(a). 理想气体的可逆过程(b). 封闭体系的任一过程(c). 封闭体系只做体积功过程(d). 封闭体系的定压过程(答案) c (W=W体+W非,当W非=0时,W体= -pdV)3.对热力学可逆过程,下列说法中正确的是(a) 过程进行的速度无限慢 (b) 没有功的损失(c) 系统和环境可同时复原 (d) 不需环境做功(答案) c可逆过程:体系经过某一过程从状态(1)变到状态(2)之后,如果能够使体系和环境都恢复到原来的状态而未留下任何永久性的变化,则该过程称为热力学可逆过程。
否则为不可逆过程特征:①状态变化时推动力与阻力相差无限小,体系与环境始终无限接近于平衡态;②过程中的任何一个中间态都可以从正、逆两个方向到达;③体系变化一个循环后,体系和环境均恢复原态,变化过程中无任何耗散效应;④等温可逆过程中,体系对环境作最大功,环境对体系作最小功。
⑤在可逆过程中,由于状态变化时推动力与阻力相差无限小,所以完成过程所需的时间为无限长。
4.对于封闭体系来说,当过程的始态与终态确定后,下列各项中哪一个无确定值(a) Q (b) Q + W(c) W (当Q = 0时) (d) Q (当W = 0时)(答案) a (△U=Q+W)5.对于孤立体系中发生的实际过程,下列关系中不正确的是(a) W = 0 (b) Q = 0(c) ΔU= 0 (d) ΔH = 0(答案) d (孤立体系?△U=Q+W)6.对于内能是体系状态的单值函数概念,错误理解是(a) 体系处于一定的状态,具有一定的内能(b) 对应于某一状态,内能只能有一数值不能有两个以上的数值(c) 状态发生变化,内能也一定跟着变化 (d) 对应于一个内能值,可以有多个状态(答案) c (理想气体等温过程,△U ,即内能不变; 绝热可逆过程△S=0)7.凡是在孤立体系中进行的变化,其ΔU 和ΔH 的值一定是 (a) ΔU > 0 , ΔH > 0 (b) ΔU = 0 , ΔH = 0(c) ΔU < 0 , ΔH < 0 (d) ΔU = 0 , ΔH 大于、小于或等于零不确定(答案) d8. 封闭体系从A 态变为B 态,可以沿两条等温途径:甲)可逆途径;乙)不可逆途径,则下列关系式⑴ ΔU 可逆> ΔU 不可逆 ⑵ ⎢W 可逆⎢ > ⎢W 不可逆 ⎢⑶ ⎢Q 可逆⎢< ⎢Q 不可逆⎢ ⑷ ( Q 可逆 - W 可逆) > ( Q 不可逆 - W 不可逆) 正确的是(a) (1),(2) (b) (2),(3) (c) (3),(4) (d) (1),(4)(答案) b (④等温可逆过程中,体系对环境作最大功,环境对体系作最小功。
大学物理化学上学期各章节复习题及答案(傅献彩版)

第二章热力学第一定律一、选择题1、下列叙述中不具状态函数特征的是:()(A)系统状态确定后,状态函数的值也确定(B)系统变化时,状态函数的改变值只由系统的初终态决定(C)经循环过程,状态函数的值不变(D)状态函数均有加和性2、下列叙述中,不具可逆过程特征的是:()(A)过程的每一步都接近平衡态,故进行得无限缓慢(B)沿原途径反向进行时,每一小步系统与环境均能复原(C)过程的初态与终态必定相同(D)过程中,若做功则做最大功,若耗功则耗最小功3、如图,将CuSO4水溶液置于绝热箱中,插入两个铜电极,以蓄电池为电源进行电解,可以看作封闭体系的是:()(A)绝热箱中所有物质(B)两个铜电极(C)蓄电池和铜电极(D) CuSO4水溶液5、在下列关于焓的描述中,正确的是()(A)因为ΔH=QP,所以焓是恒压热(B)气体的焓只是温度的函数(C)气体在节流膨胀中,它的焓不改变(D)因为ΔH=ΔU+Δ(PV),所以任何过程都有ΔH>0的结论6、在标准压力下,1mol石墨与氧气反应生成1mol二氧化碳的反应热为ΔrH ,下列哪种说法是错误的? ()(A) ΔH 是CO2(g)的标准生成热(B) ΔH =ΔU(C) ΔH 是石墨的燃烧热(D) ΔU <ΔH7、在标准状态下,反应C2H5OH(l)+3O2(g) →2CO2(g)+3H2O(g)的反应焓为Δr H mθ, ΔC p>0, 下列说法中正确的是()(A)Δr H mθ是C2H5OH(l)的标准摩尔燃烧焓(B)Δr H mθ〈0(C)Δr H mθ=ΔrUmθ(D)Δr H mθ不随温度变化而变化8、下面关于标准摩尔生成焓的描述中,不正确的是()(A)生成反应中的单质必须是稳定的相态单质(B)稳态单质的标准摩尔生成焓被定为零(C)生成反应的温度必须是298.15K(D)生成反应中各物质所达到的压力必须是100KPa9、在一个绝热钢瓶中,发生一个放热的分子数增加的化学反应,那么:()(A) Q > 0,W > 0,∆U > 0 (B)Q = 0,W = 0,∆U < 0(C) Q = 0,W = 0,∆U = 0 (D) Q < 0,W > 0,∆U < 010、非理想气体进行绝热自由膨胀时,下述答案中哪一个是错误的? ( )(A) Q=0 (B) W=0 (C) ΔU=0 (D) ΔH=011、下列表示式中正确的是( )(A)恒压过程ΔH=ΔU+pΔV (B)恒压过程ΔH=0(C)恒压过程ΔH=ΔU+VΔp (D)恒容过程ΔH=012、理想气体等温反抗恒外压膨胀,则( )(A)Q>W (B)Q<W (C)Q=W (D)Q=△U13、当理想气体其温度由298K升高到348K,经(1)绝热过程和(2)等压过程,则两过程的()(A)△H1>△H2W1<W2(B)△H1<△H2W1>W2(C)△H1=△H2W1<W2(D)△H1=△H2 W1>W214、当理想气体从298K,2×105Pa 经历(1)绝热可逆膨胀和(2)等温可逆膨胀到1×105Pa时,则( )(A)△H1<△H2W1>W2(B)△H1>△H2 W1<W2(C)△H1<△H2W1<W2(D)△H1>△H2 W1>W215、对于封闭体系,在指定始终态间的绝热可逆途径可以有:( )(A) 一条(B) 二条(C) 三条(D) 三条以上16、实际气体绝热恒外压膨胀时,其温度将:( )(A) 升高(B) 降低(C) 不变(D) 不确定17、功的计算公式为W=nC v,m(T2-T1),下列过程中不能用此式的是()(A)理想气体的可逆绝热过程(B)理想气体的绝热恒外压过程(C)实际气体的绝热过程(D)凝聚系统的绝热过程18、凡是在孤立体系中进行的变化,其ΔU和ΔH的值一定是:( )(A) ΔU> 0 , ΔH > 0 (B) ΔU= 0 , ΔH = 0(C) ΔU< 0 , ΔH < 0 (D) ΔU= 0 , ΔH大于、小于或等于零不确定19、一定量的理想气体从同一始态出发,分别经(1) 等温压缩,(2) 绝热压缩到具有相同压力的终态,以H1,H2分别表示两个终态的焓值,则有:( )(A) H1> H2 (B) H1= H2 (C) H1< H2 (D) H1>=H220、将H2(g)与O2以2:1的比例在绝热刚性密闭容器中完全反应,则该过程中应有()(A)ΔT=0 (B)Δp=0 (C)ΔU=0 (D)ΔH=021、刚性绝热箱内发生一化学反应,则反应体系为( )(A)孤立体系(B)敞开体系(C)封闭体系(D)绝热体系22、理想气体可逆绝热膨胀,则下列说法中正确的是( )(A)焓总是不变(B)内能总是增加(C)焓总是增加(D)内能总是减少23、关于等压摩尔热容和等容摩尔热容,下面的说法中不正确的是( )(A)C p,m与C v,m不相等,因等压过程比等容过程系统多作体积功(B)C p,m–C v,m=R既适用于理想气体体系,也适用于实际气体体系(C)C v,m=3/2R适用于单原子理想气体混合物(D)在可逆相变中C p,m和C v,m都为无限大24、下列哪个过程的dT≠0,dH=0?( )(A)理想气体等压过程(B)实际气体等压过程(C)理想气体等容过程(D)实际气体节流膨胀过程25、隔离系统内发生一变化过程,则系统的:(A)热力学能守恒,焓守恒(B)热力学能不一定守恒,焓守恒(C)热力学能守恒,焓不一定守恒(D)热力学能、焓均不一定守恒二、判断题1、体系在某过程中向环境放热,则体系的内能减少。
第二章 热力学第一定律(总复习题)

大学物理化学上学期各章节复习题及答案

第二章热力学第一定律一、选择题1、下列叙述中不具状态函数特征的是:()(A)系统状态确定后,状态函数的值也确定(B)系统变化时,状态函数的改变值只由系统的初终态决定(C)经循环过程,状态函数的值不变(D)状态函数均有加和性2、下列叙述中,不具可逆过程特征的是:()(A)过程的每一步都接近平衡态,故进行得无限缓慢(B)沿原途径反向进行时,每一小步系统与环境均能复原(C)过程的初态与终态必定相同(D)过程中,若做功则做最大功,若耗功则耗最小功3、如图,将CuSO4水溶液置于绝热箱中,插入两个铜电极,以蓄电池为电源进行电解,可以看作封闭体系的是:()(A)绝热箱中所有物质(B)两个铜电极(C)蓄电池和铜电极(D) CuSO4水溶液5、在下列关于焓的描述中,正确的是()(A)因为ΔH=QP,所以焓是恒压热(B)气体的焓只是温度的函数(C)气体在节流膨胀中,它的焓不改变(D)因为ΔH=ΔU+Δ(PV),所以任何过程都有ΔH>0的结论6、在标准压力下,1mol石墨与氧气反应生成1mol二氧化碳的反应热为Δr H ,下列哪种说法是错误的? ()(A) ΔH 是CO2(g)的标准生成热(B) ΔH =ΔU(C) ΔH 是石墨的燃烧热(D) ΔU <ΔH7、在标准状态下,反应C2H5OH(l)+3O2(g) →2CO2(g)+3H2O(g)的反应焓为Δr H mθ, ΔC p>0, 下列说法中正确的是()(A)Δr H mθ是C2H5OH(l)的标准摩尔燃烧焓(B)Δr H mθ〈0(C)Δr H mθ=ΔrUmθ(D)Δr H mθ不随温度变化而变化8、下面关于标准摩尔生成焓的描述中,不正确的是()(A)生成反应中的单质必须是稳定的相态单质(B)稳态单质的标准摩尔生成焓被定为零(C)生成反应的温度必须是298.15K(D)生成反应中各物质所达到的压力必须是100KPa9、在一个绝热钢瓶中,发生一个放热的分子数增加的化学反应,那么:()(A) Q > 0,W > 0,?U > 0 (B)Q = 0,W = 0,?U < 0(C) Q = 0,W = 0,?U = 0 (D) Q < 0,W > 0,?U < 010、非理想气体进行绝热自由膨胀时,下述答案中哪一个是错误的? ( )(A) Q=0 (B) W=0 (C) ΔU=0 (D) ΔH=011、下列表示式中正确的是( )(A)恒压过程ΔH=ΔU+pΔV (B)恒压过程ΔH=0(C)恒压过程ΔH=ΔU+VΔp (D)恒容过程ΔH=012、理想气体等温反抗恒外压膨胀,则( )(A)Q>W (B)Q<W (C)Q=W (D)Q=△U13、当理想气体其温度由298K升高到348K,经(1)绝热过程和(2)等压过程,则两过程的()(A)△H1>△H2W1<W2(B)△H1<△H21>W2(C)△H 1=△H21<W2(D)△H1=△H21>W214、当理想气体从298K,2×105Pa 经历(1)绝热可逆膨胀和(2)等温可逆膨胀到1×105Pa时,则( )(A)△H1<△H21>W2(B)△H1>△H21<W2(C)△H 1<△H21<W2(D)△H1>△H21>W215、对于封闭体系,在指定始终态间的绝热可逆途径可以有:( )(A) 一条(B) 二条(C) 三条(D) 三条以上16、实际气体绝热恒外压膨胀时,其温度将:( )(A) 升高(B) 降低(C) 不变(D) 不确定17、功的计算公式为W=nC v,m(T2-T1),下列过程中不能用此式的是()(A)理想气体的可逆绝热过程(B)理想气体的绝热恒外压过程(C)实际气体的绝热过程(D)凝聚系统的绝热过程18、凡是在孤立体系中进行的变化,其ΔU和ΔH的值一定是:( )(A) ΔU> 0 , ΔH > 0 (B) ΔU= 0 , ΔH = 0(C) ΔU< 0 , ΔH < 0 (D) ΔU= 0 , ΔH大于、小于或等于零不确定19、一定量的理想气体从同一始态出发,分别经(1) 等温压缩,(2) 绝热压缩到具有相同压力的终态,以H1,H2分别表示两个终态的焓值,则有:( )(A) H1> H2 (B) H1= H2 (C) H1< H2 (D) H1>=H220、将H2(g)与O2以2:1的比例在绝热刚性密闭容器中完全反应,则该过程中应有()(A)ΔT=0 (B)Δp=0 (C)ΔU=0 (D)ΔH=021、刚性绝热箱内发生一化学反应,则反应体系为( )(A)孤立体系(B)敞开体系(C)封闭体系(D)绝热体系22、理想气体可逆绝热膨胀,则下列说法中正确的是( )(A)焓总是不变(B)内能总是增加(C)焓总是增加(D)内能总是减少23、关于等压摩尔热容和等容摩尔热容,下面的说法中不正确的是( )(A)C p,m与C v,m不相等,因等压过程比等容过程系统多作体积功(B)C p,m–C v,m=R既适用于理想气体体系,也适用于实际气体体系(C)C v,m=3/2R适用于单原子理想气体混合物(D)在可逆相变中C p,m和C v,m都为无限大24、下列哪个过程的dT≠0,dH=0?( )(A)理想气体等压过程(B)实际气体等压过程(C)理想气体等容过程(D)实际气体节流膨胀过程25、隔离系统内发生一变化过程,则系统的:(A)热力学能守恒,焓守恒(B)热力学能不一定守恒,焓守恒(C)热力学能守恒,焓不一定守恒(D)热力学能、焓均不一定守恒二、判断题1、体系在某过程中向环境放热,则体系的内能减少。
第二章 热力学第一定律习题

第二章热力学第一定律选择题1.热力学第一定律ΔU=Q+W 只适用于(A) 单纯状态变化 (B) 相变化(C) 化学变化 (D) 封闭物系的任何变化答案:D2.关于热和功, 下面的说法中, 不正确的是(A) 功和热只出现于系统状态变化的过程中, 只存在于系统和环境间的界面上(B) 只有在封闭系统发生的过程中, 功和热才有明确的意义(C) 功和热不是能量, 而是能量传递的两种形式, 可称之为被交换的能量(D) 在封闭系统中发生的过程中, 如果内能不变, 则功和热对系统的影响必互相抵消答案:B3.关于焓的性质, 下列说法中正确的是(A) 焓是系统内含的热能, 所以常称它为热焓(B) 焓是能量, 它遵守热力学第一定律(C) 系统的焓值等于内能加体积功(D) 焓的增量只与系统的始末态有关答案:D。
因焓是状态函数。
4.涉及焓的下列说法中正确的是(A) 单质的焓值均等于零(B) 在等温过程中焓变为零(C) 在绝热可逆过程中焓变为零(D) 化学反应中系统的焓变不一定大于内能变化答案:D。
因为焓变ΔH=ΔU+Δ(pV),可以看出若Δ(pV)<0则ΔH<ΔU。
5.下列哪个封闭体系的内能和焓仅是温度的函数(A) 理想溶液 (B) 稀溶液 (C) 所有气体 (D) 理想气体答案:D6.与物质的生成热有关的下列表述中不正确的是(A) 标准状态下单质的生成热都规定为零(B) 化合物的生成热一定不为零(C) 很多物质的生成热都不能用实验直接测量(D) 通常所使用的物质的标准生成热数据实际上都是相对值答案:A。
按规定,标准态下最稳定单质的生成热为零。
7.dU=CvdT及dUm=Cv,mdT适用的条件完整地说应当是(A) 等容过程(B)无化学反应和相变的等容过程(C) 组成不变的均相系统的等容过程(D) 无化学反应和相变且不做非体积功的任何等容过程及无反应和相变而且系统内能只与温度有关的非等容过程答案:D8.下列过程中, 系统内能变化不为零的是(A) 不可逆循环过程 (B) 可逆循环过程(C) 两种理想气体的混合过程 (D) 纯液体的真空蒸发过程答案:D 。
(完整版)《物理化学》第二章热力学第一定律练习题(含答案)

(完整版)《物理化学》第⼆章热⼒学第⼀定律练习题(含答案)第⼆章练习题⼀、填空题1、根据体系和环境之间能量和物质的交换情况,可将体系分成、、。
2、强度性质表现体系的特征,与物质的数量⽆关。
容量性质表现体系的特征,与物质的数量有关,具有性。
3、热⼒学平衡状态同时达到四种平衡,分别是、、、。
4、体系状态发⽣变化的称为过程。
常见的过程有、、、、。
5、从统计热⼒学观点看,功的微观本质是,热的微观本质是。
6、⽓体各真空膨胀膨胀功W= 07、在绝热钢瓶中化学反应△U= 08、焓的定义式为。
⼆、判断题(说法对否):1、当体系的状态⼀定时,所有的状态函数都有⼀定的数值。
(√)2、当体系的状态发⽣变化时,所有的状态函数的数值也随之发⽣变化。
(χ)3.因= ΔH, = ΔU,所以与都是状态函数。
(χ)4、封闭系统在压⼒恒定的过程中吸收的热等于该系统的焓。
(χ)错。
只有封闭系统不做⾮膨胀功等压过程ΔH=Q P5、状态给定后,状态函数就有定值;状态函数确定后,状态也就确定了。
(√)6、热⼒学过程中W的值应由具体过程决定( √ )7、1mol理想⽓体从同⼀始态经过不同的循环途径后回到初始状态,其热⼒学能不变。
( √ )三、单选题1、体系的下列各组物理量中都是状态函数的是( C )A 、T、P、V、QB 、m、W、P、HC、T、P、V、n、D、T、P、U、W2、对于内能是体系的单值函数概念,错误理解是( C )A体系处于⼀定的状态,具有⼀定的内能B对应于某⼀状态,内能只能有⼀数值不能有两个以上的数值C状态发⽣变化,内能也⼀定跟着变化D对应于⼀个内能值,可以有多个状态3下列叙述中不具有状态函数特征的是(D )A体系状态确定后,状态函数的值也确定B体系变化时,状态函数的改变值只由体系的始终态决定C经循环过程,状态函数的值不变D状态函数均有加和性4、下列叙述中正确的是( A )A物体温度越⾼,说明其内能越⼤B物体温度越⾼,说明其所含热量越多C凡体系温度升⾼,就肯定是它吸收了热D凡体系温度不变,说明它既不吸热也不放热5、下列哪⼀种说法错误( D )A焓是定义的⼀种具有能量量纲的热⼒学量B只有在某些特定条件下,焓变△H才与体系吸热相等C焓是状态函数D焓是体系能与环境能进⾏热交换的能量6、热⼒学第⼀定律仅适⽤于什么途径(A)A同⼀过程的任何途径B同⼀过程的可逆途径C同⼀过程的不可逆途径D不同过程的任何途径7. 如图,将CuSO4⽔溶液置于绝热箱中,插⼊两个铜电极,以蓄电池为电源进⾏电解,可以看作封闭系统的是(A)(A) 绝热箱中所有物质; (B) 两个铜电极;(C) 蓄电池和铜电极;(D) CuSO4⽔溶液。
第 二 章 热力学第一定律练习题及解答

第 二 章 热力学第一定律一、思考题1. 判断下列说法是否正确,并简述判断的依据(1)状态给定后,状态函数就有定值,状态函数固定后,状态也就固定了。
答:是对的。
因为状态函数是状态的单值函数。
(2)状态改变后,状态函数一定都改变。
答:是错的。
因为只要有一个状态函数变了,状态也就变了,但并不是所有的状态函数都得变。
(3)因为ΔU=Q V ,ΔH=Q p ,所以Q V ,Q p 是特定条件下的状态函数? 这种说法对吗?答:是错的。
∆U ,∆H 本身不是状态函数,仅是状态函数的变量,只有在特定条件下与Q V ,Q p 的数值相等,所以Q V ,Q p 不是状态函数。
(4)根据热力学第一定律,因为能量不会无中生有,所以一个系统如要对外做功,必须从外界吸收热量。
答:是错的。
根据热力学第一定律U Q W ∆=+,它不仅说明热力学能(ΔU )、热(Q )和功(W )之间可以转化,有表述了它们转化是的定量关系,即能量守恒定律。
所以功的转化形式不仅有热,也可转化为热力学能系。
(5)在等压下,用机械搅拌某绝热容器中的液体,是液体的温度上升,这时ΔH=Q p =0答:是错的。
这虽然是一个等压过程,而此过程存在机械功,即W f ≠0,所以ΔH≠Q p 。
(6)某一化学反应在烧杯中进行,热效应为Q 1,焓变为ΔH 1。
如将化学反应安排成反应相同的可逆电池,使化学反应和电池反应的始态和终态形同,这时热效应为Q 2,焓变为ΔH 2,则ΔH 1=ΔH 2。
答:是对的。
Q 是非状态函数,由于经过的途径不同,则Q 值不同,焓(H )是状态函数,只要始终态相同,不考虑所经过的过程,则两焓变值∆H 1和∆H 2相等。
2 . 回答下列问题,并说明原因(1)可逆热机的效率最高,在其它条件相同的前提下,用可逆热机去牵引货车,能否使火车的速度加快? 答?不能。
热机效率hQ W -=η是指从高温热源所吸收的热最大的转换成对环境所做的功。
但可逆热机循环一周是一个缓慢的过程,所需时间是无限长。
第二章-热力学第一定律--题加答案
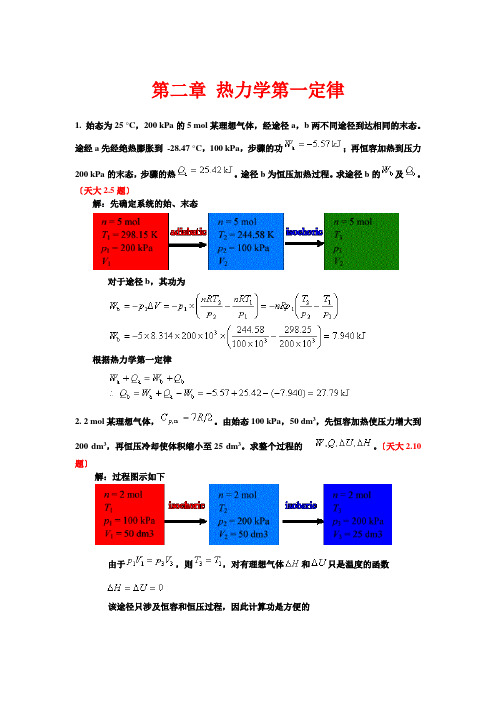
第二章热力学第一定律1. 始态为25 °C,200 kPa的5 mol某理想气体,经途径a,b两不同途径到达相同的末态。
途经a先经绝热膨胀到-28.47 °C,100 kPa,步骤的功;再恒容加热到压力200 kPa的末态,步骤的热。
途径b为恒压加热过程。
求途径b的及。
〔天大2.5题〕解:先确定系统的始、末态对于途径b,其功为根据热力学第一定律2. 2 mol某理想气体,。
由始态100 kPa,50 dm3,先恒容加热使压力增大到200 dm3,再恒压冷却使体积缩小至25 dm3。
求整个过程的。
〔天大2.10题〕解:过程图示如下由于,则,对有理想气体和只是温度的函数该途径只涉及恒容和恒压过程,因此计算功是方便的根据热力学第一定律3. 单原子理想气体A与双原子理想气体B的混合物共5 mol,摩尔分数,始态温度,压力。
今该混合气体绝热反抗恒外压膨胀到平衡态。
求末态温度及过程的。
〔天大2.18题〕解:过程图示如下分析:因为是绝热过程,过程热力学能的变化等于系统与环境间以功的形势所交换的能量。
因此,单原子分子,双原子分子由于对理想气体U和H均只是温度的函数,所以4. mol〔单原子分子〕理想气体,由、300K按以下两种不同的途径压缩到、300K,试计算并比较两途径的Q、W、ΔU及ΔH。
(1〕等压冷却,然后经过等容加热;(2)等容加热,然后经过等压冷却。
解:C p,m=2.5R, C V,m〔1〕、、、300K30.09858 dm30.09858 dm3Q=Q1+Q2××××(300-119.8)=-3745+2247=-1499(J)W=W1+W2×103×(0.09858-0.2470)+0=1499(J)ΔU=Q+W=0ΔH=ΔU+Δ(pV)××0.2470=0〔2〕、、、300K330.09858 dm3Q=Q1+Q2××××(300-751.6)=5632-9387=-3755(J)W=W1+W2×103×(0.09858-0.2470) =3755(J)ΔU=Q+W=0ΔH=ΔU+Δ(pV)××0.2470=0计算结果说明,Q、W与途径有关,而ΔU、ΔH与途径无关。
(完整版)物理化学课后答案-热力学第一定律

欢迎共阅第二章热力学第一定律【复习题】【1】判断下列说法是否正确。
(1)状态给定后,状态函数就有一定的值,反之亦然。
(2)状态函数改变后,状态一定改变。
(3)状态改变后,状态函数一定都改变。
(4)因为△ U=Q v, △H =Q p,所以Q v,Q p是特定条件下的状态函数。
(5)恒温过程一定是可逆过程。
(6)汽缸内有一定量的理想气体,反抗一定外压做绝热膨胀,则△H= Q p=0。
(7)根据热力学第一定律,因为能量不能无中生有,所以一个系统若要对外做功,必须从外界吸收热量。
(8)系统从状态Ⅰ变化到状态Ⅱ,若△T=0 ,则Q=0 ,无热量交换。
(9)在等压下,机械搅拌绝热容器中的液体,使其温度上升,则△H = Q p = 0。
(10)理想气体绝热变化过程中,W=△U,即W R=△U=C V△T,W IR=△U=C V△T,所以W R=W IR 。
(11)有一个封闭系统,当始态和终态确定后;(a)若经历一个绝热过程,则功有定值;(b)若经历一个等容过程,则Q 有定值(设不做非膨胀力);(c)若经历一个等温过程,则热力学能有定值;(d)若经历一个多方过程,则热和功的代数和有定值。
(12)某一化学反应在烧杯中进行,放热Q1,焓变为△ H 1,若安排成可逆电池,使终态和终态都相同,这时放热Q2,焓变为△ H2,则△ H1=△H 2。
【答】(1)正确,因为状态函数是体系的单质函数,体系确定后,体系的一系列状态函数就确定。
相反如果体系的一系列状态函数确定后,体系的状态也就被惟一确定。
(2)正确,根据状态函数的单值性,当体系的某一状态函数改变了,则状态函数必定发生改变。
(3)不正确,因为状态改变后,有些状态函数不一定改变,例如理想气体的等温变化,内能就不变。
(4)不正确,ΔH=Qp,只说明Qp 等于状态函数H 的变化值ΔH,仅是数值上相等,并不意味着Qp 具有状态函数的性质。
ΔH=Qp 只能说在恒压而不做非体积功的特定条件下,Qp 的数值等于体系状态函数H 的改变,而不能认为Qp 也是状态函数。
第二章热力学第一定律

系统与环境之间无物质交换,但有能量交换。
(3)隔离系统(isolated system) 系统与环境之间既无物质交换,又无能量交换。
二、状态和状态性质
1、状态
系统的物理性质和化学性质的综合表现称为系统的状态。
2、状态性质
描述系统状态的宏观物理量称为系统的状态性质。
可分为两类: ① 广度性质(extensive properties) 又称为容量性质,它的数值与系统的物质的量成正比, 如体积、质量、熵等。这种性质有加和性。
②强度性质(intensive
properties)
它的数值与系统的数量无关,不具有加和性,如温
度、压力等。两个广度性质相除,所得为强度性质 如:
m/V =ρ V/n = Vm
3、状态性质的特性 ①状态一定,状态性质的值一定。 ②状态性质的变化值仅取决于系统的始态和终态,而与 变化的途径无关。 ③周而复始,变化为零。
2
3
的关系是 p 2 ( )。2
(1)p1 p2 (2)p1 p2 (3)p1 p2 (4) 不能确定
第二章 热力学第一定律
热w Of Thermodynamics
§2-1 热力学的基本概念
一、系统和环境
dU QV
该式表明,等容且非体积功为零的过程中,系统吸收或放出的热等于其 热力学能的变化。
二、等压热及焓 等压且非体积功为零的过程中系统和环境交换的热称
为等压热。等压热的符号为Qp。
对于只作体积功的等压过程,因为 p1 = p2 = psu = p = 常数,因此
dU =Qp – pdV Qp = dU + pdV=dU+d(pV) Qp = d(U + pV)
《物理化学》第二章-热力学第一定律练习题(含标准答案)

《物理化学》第二章-热力学第一定律练习题(含答案)————————————————————————————————作者:————————————————————————————————日期:第二章练习题一、填空题1、根据体系和环境之间能量和物质的交换情况,可将体系分成、、。
2、强度性质表现体系的特征,与物质的数量无关。
容量性质表现体系的特征,与物质的数量有关,具有性。
3、热力学平衡状态同时达到四种平衡,分别是、、、。
4、体系状态发生变化的称为过程。
常见的过程有、、、、。
5、从统计热力学观点看,功的微观本质是,热的微观本质是。
6、气体各真空膨胀膨胀功W= 07、在绝热钢瓶中化学反应△U= 08、焓的定义式为。
二、判断题(说法对否):1、当体系的状态一定时,所有的状态函数都有一定的数值。
(√)2、当体系的状态发生变化时,所有的状态函数的数值也随之发生变化。
(χ)3.因= ΔH, = ΔU,所以与都是状态函数。
(χ)4、封闭系统在压力恒定的过程中吸收的热等于该系统的焓。
(χ)错。
只有封闭系统不做非膨胀功等压过程ΔH=Q P5、状态给定后,状态函数就有定值;状态函数确定后,状态也就确定了。
(√)6、热力学过程中W的值应由具体过程决定( √ )7、1mol理想气体从同一始态经过不同的循环途径后回到初始状态,其热力学能不变。
( √ )三、单选题1、体系的下列各组物理量中都是状态函数的是( C )A 、T、P、V、QB 、m、W、P、HC、T、P、V、n、D、T、P、U、W2、对于内能是体系的单值函数概念,错误理解是( C )A体系处于一定的状态,具有一定的内能B对应于某一状态,内能只能有一数值不能有两个以上的数值C状态发生变化,内能也一定跟着变化D对应于一个内能值,可以有多个状态3下列叙述中不具有状态函数特征的是(D )A体系状态确定后,状态函数的值也确定B体系变化时,状态函数的改变值只由体系的始终态决定C经循环过程,状态函数的值不变D状态函数均有加和性4、下列叙述中正确的是( A )A物体温度越高,说明其内能越大B物体温度越高,说明其所含热量越多C凡体系温度升高,就肯定是它吸收了热D凡体系温度不变,说明它既不吸热也不放热5、下列哪一种说法错误( D )A焓是定义的一种具有能量量纲的热力学量B只有在某些特定条件下,焓变△H才与体系吸热相等C焓是状态函数D焓是体系能与环境能进行热交换的能量6、热力学第一定律仅适用于什么途径(A)A同一过程的任何途径B同一过程的可逆途径C同一过程的不可逆途径D不同过程的任何途径7. 如图,将CuSO4水溶液置于绝热箱中,插入两个铜电极,以蓄电池为电源进行电解,可以看作封闭系统的是(A)(A) 绝热箱中所有物质; (B) 两个铜电极;(C) 蓄电池和铜电极;(D) CuSO4水溶液。
物化上册复习题

B ΔU>0,ΔH<0
C ΔU=0,ΔH≠0
D ΔU<0,ΔH<0
12. 有一温泉的温度为60ºC,周围在气温度为25ºC,假设一卡诺热机工作在上述两个热源之间,
从温泉吸热100KJ,则对环境作功( )
A 66.67kJ B 10.5kJ
C 11.74kJ
D 58.33kJ
13. 某化学反应在恒压. 绝热和只做体积功的条件下进行,体系的温度由T1升高至T2, 则此过程
A:ΔS1>ΔS2
B:ΔS1=ΔS2
C:ΔS1<ΔS2
D:ΔS1. ΔS2无必然联系
4. 一 列 火 车 在 我 国 铁 路 上 行 驶 , 在 下 述 哪 一 种 地 理 和 气 候 条 件 下 内 燃 机 的 热 效 率 最高
()
A;南方的夏天
B:北方的夏天
C:南方的冬季
三 填空题
1. 1mol实际气体做某一不可逆循环, 又回到始态, 则ΔH 0, ΔU 0. 2. 在恒温恒压下, 反应CH4(g)+2O2(g)→CO2(g)+2H2O(l)的Q 0, W 0, ΔH 0. 3. 理想气体由101.325kPa下, 受恒定外压1013.25kPa绝热压缩至平衡态, 则ΔU 0,
A 45.2
B 40.7
C 37.6
D 52.2
6. 体系经历一不可逆循环后,下列答案不正确的是( )
A:ΔU=0 B. ΔH=0 C. W=0 D. ΔCP=0
7. 1mol单原子理想气体从298K,202.65kPa经历①等温 ②绝热 ③等压 三条途径可逆膨胀使体
积增大到原来的2倍,所作的功分别为W1. W2. W3,三者的关系是( )
的焓变ΔH为
第二章热力学第一定律习题和答案

第二章热力学第一定律一选择题1.某绝热体系在接受了环境所做的功之后,其温度() AA.一定升高B.一定降低C.一定不变D.不一定改变2.当体系将热量传递给环境后,体系的焓() DA.必定减少B.必定增加C.没有变化D.不一定改变3.热力学状态和热力学状态函数的关系为() BA.状态函数一定,状态就单一的确定B.状态一定,状态函数就单值的确定C .A、B 都对 D. A、B 都不对4.系统的状态函数,定义为H=U+pV 若系统发生状态变化时,则焓的变化为△H=△U+△(pV),式中△(pV)的意思是() BA. △(pV) = △P△VB.△(pV) = p2V2-p1V1C. △(pV) = p△V+V△p5.在一个密闭绝热的房间里放置一台电冰箱,将冰箱门打开,接通电源使冰箱工作,过一段时间后,室内的平均气温将如何变化?()A.升高B.降低C.不变D.先升后降 A6.分子数增加的放热化学反应在一绝热钢瓶中进行,则() DA. B.C. D.7.1mol 单原子理想气体,从p1=202650Pa,T1=273K 经p/T=常数的途径加热使压力增加到p2=405300Pa,则体系做的功为() CA.大于零B.小于零C.零D.无法确定8. 氧气的燃烧热应为何值() DA.大于零B.小于零C.等于零D.不存在9.下述说法中,哪一个正确?() BA.水蒸气的生成热即是氢气的燃烧热B.水的生成热即是氢气的燃烧热C.水的生成热即是氧气的燃烧热D.水蒸气的生成热即是氧气的燃烧热9.298K 及101325Pa 条件下,1mol 过冷水蒸气变成1mol 的液态水则ΔG 为 ( )A.ΔG < 0B.ΔG > 0C.ΔG = 0D.不一定 A10.关于焓,下述说法不正确的是() AA.△H=Q 适用于封闭体系等压只做功的过程B.对于常压下的凝聚相,过程△H≈△UC.对理想气体的恒容过程△H=△U+V△PD 对于任何体系等压只做体积功的过程△H=△U-W11.将某理想气体从温度T1加热到T2,若此变化为非恒容途径,则其热力学能的变化△U 应() BA.= 0B.= Cv(T2-T1)C.不存在D.等于其他值12.对于封闭体系,当过程的始终态确定后,下列值中不能确定的是()A.恒容、无其它功过程的QB.可逆过程的WC.任意过程的Q+WD.绝热过程的W D13.化学反应在只做体积功的定温定压条件下,若从反应物开始进进行反应,由此过程为() CA.是热力学可逆过程B.是热力学不可逆过程C.是否过逆不能确定 C.是不能进行的过程14.下面陈述中,正确的是() C A.虽然Q 和W 是过程量,但由于Q v=△U,Q p=△H,而U 和H 是状态函数,所以Q v 和Q p 是状态函数B.热量是由于温度差而传递的能量,它总是倾向于从含热量较多的高温物体流向含热量较少的低温物体C.封闭系统与环境之间交换能量的形式非功即热D.两物体之间只有存在温差,才可传递能量,反过来系统与环境间发生热量传递后, 必然要引起系统温度变化15.物质的量为n 的纯理想气体,若该气体的哪一组物理量确定之后,其它状态函数方有定值。
(完整版)第二章热力学第一定律习题

第二章热力学第一定律选择题1.热力学第一定律ΔU=Q+W 只适用于(A) 单纯状态变化 (B) 相变化(C) 化学变化 (D) 封闭物系的任何变化答案:D2.关于热和功, 下面的说法中, 不正确的是(A) 功和热只出现于系统状态变化的过程中, 只存在于系统和环境间的界面上(B) 只有在封闭系统发生的过程中, 功和热才有明确的意义(C) 功和热不是能量, 而是能量传递的两种形式, 可称之为被交换的能量(D) 在封闭系统中发生的过程中, 如果内能不变, 则功和热对系统的影响必互相抵消答案:B3.关于焓的性质, 下列说法中正确的是(A) 焓是系统内含的热能, 所以常称它为热焓(B) 焓是能量, 它遵守热力学第一定律(C) 系统的焓值等于内能加体积功(D) 焓的增量只与系统的始末态有关答案:D。
因焓是状态函数。
4.涉及焓的下列说法中正确的是(A) 单质的焓值均等于零(B) 在等温过程中焓变为零(C) 在绝热可逆过程中焓变为零(D) 化学反应中系统的焓变不一定大于内能变化答案:D。
因为焓变ΔH=ΔU+Δ(pV),可以看出若Δ(pV)<0则ΔH<ΔU。
5.下列哪个封闭体系的内能和焓仅是温度的函数(A) 理想溶液 (B) 稀溶液 (C) 所有气体 (D) 理想气体答案:D6.与物质的生成热有关的下列表述中不正确的是(A) 标准状态下单质的生成热都规定为零(B) 化合物的生成热一定不为零(C) 很多物质的生成热都不能用实验直接测量(D) 通常所使用的物质的标准生成热数据实际上都是相对值答案:A。
按规定,标准态下最稳定单质的生成热为零。
7.dU=CvdT及dUm=Cv,mdT适用的条件完整地说应当是(A) 等容过程(B)无化学反应和相变的等容过程(C) 组成不变的均相系统的等容过程(D) 无化学反应和相变且不做非体积功的任何等容过程及无反应和相变而且系统内能只与温度有关的非等容过程答案:D8.下列过程中, 系统内能变化不为零的是(A) 不可逆循环过程 (B) 可逆循环过程(C) 两种理想气体的混合过程 (D) 纯液体的真空蒸发过程答案:D 。
热力学第一定律复习题

第二章 热力学第一定律热 功热力学能热力学第一定律数学表达式:△焓函数、恒压条件下,△H =Q p 。
系统状态变化时,计算系统与环境间交换的能量g 节流膨胀:Q =0;△H =0;J-T =(d T /d p )H =0 T 不变(例如理想气体) <0致热 >0 致冷 摩尔反应焓的定义:△r H m =△r H /△标准摩尔反应焓的计算:()H T ∆=∑!反应进度定义、标准摩尔生成焓和标准摩尔燃烧焓的定义。
m dT1. 当理想气体冲入一真空绝热容器后,其温度将(a) 升高 (b) 降低(c) 不变 (d) 难以确定(答案) c (△U=Q+W, ∵p外=0 , ∴W=0 ,又∵绝热,∴Q=0,所以△U=0)因为是真空故不做功,又因为是绝热故无热交换,故△U=0。
温度不变。
2. 当热力学第一定律写成d U = δQ–p d V时,它适用于(a). 理想气体的可逆过程 (b). 封闭体系的任一过程(c). 封闭体系只做体积功过程 (d). 封闭体系的定压过程(答案) c (W=W体+W非,当W非=0时,W体= -pdV)3.对热力学可逆过程,下列说法中正确的是(a) 过程进行的速度无限慢 (b) 没有功的损失(c) 系统和环境可同时复原 (d) 不需环境做功(答案) c可逆过程:体系经过某一过程从状态(1)变到状态(2)之后,如果能够使体系和环境都恢复到原来的状态而未留下任何永久性的变化,则该过程称为热力学可逆过程。
否则为不可逆过程特征:①状态变化时推动力与阻力相差无限小,体系与环境始终无限接近于平衡态;②过程中的任何一个中间态都可以从正、逆两个方向到达;③体系变化一个循环后,体系和环境均恢复原态,变化过程中无任何耗散效应;④等温可逆过程中,体系对环境作最大功,环境对体系作最小功。
⑤在可逆过程中,由于状态变化时推动力与阻力相差无限小,所以完成过程所需的时间为无限长。
4.对于封闭体系来说,当过程的始态与终态确定后,下列各项中哪一个无确定值(a) Q (b) Q + W(c) W (当Q = 0时) (d) Q (当W = 0时)(答案) a (△U=Q+W)5.对于孤立体系中发生的实际过程,下列关系中不正确的是(a) W = 0 (b) Q = 0(c) ΔU= 0 (d) ΔH = 0(答案) d (孤立体系△U=Q+W)6.对于内能是体系状态的单值函数概念,错误理解是(a) 体系处于一定的状态,具有一定的内能(b) 对应于某一状态,内能只能有一数值不能有两个以上的数值(c) 状态发生变化,内能也一定跟着变化 (d) 对应于一个内能值,可以有多个状态(答案) c (理想气体等温过程,△U ,即内能不变; 绝热可逆过程△S=0)7.凡是在孤立体系中进行的变化,其ΔU 和ΔH 的值一定是(a) ΔU > 0 , ΔH > 0 (b) ΔU = 0 , ΔH = 0(c) ΔU < 0 , ΔH < 0 (d) ΔU = 0 , ΔH 大于、小于或等于零不确定(答案) d8. 封闭体系从A 态变为B 态,可以沿两条等温途径:甲)可逆途径;乙)不可逆途径,则下列关系式⑴ ΔU 可逆> ΔU 不可逆 ⑵ W 可逆 > W 不可逆 ⑶ Q 可逆 Q 不可逆 ⑷ ( Q 可逆 - W 可逆) > ( Q 不可逆 - W 不可逆) 正确的是(a) (1),(2) (b) (2),(3) (c) (3),(4) (d) (1),(4)(答案) b (④等温可逆过程中,体系对环境作最大功,环境对体系作最小功。
第二章 热力学第一定律(总复习题)

第二章 热力学第一定律一、 选择题1、下列叙述中不具状态函数特征的是:( )(A)系统状态确定后,状态函数的值也确定(B)系统变化时,状态函数的改变值只由系统的初终态决定(C)经循环过程,状态函数的值不变(D)状态函数均有加和性2、下列叙述中,不具可逆过程特征的是:( )(A)过程的每一步都接近平衡态,故进行得无限缓慢(B)沿原途径反向进行时,每一小步系统与环境均能复原(C)过程的初态与终态必定相同(D)过程中,若做功则做最大功,若耗功则耗最小功3、如图,将CuSO4水溶液置于绝热箱中,插入两个铜电极,以蓄电池为电源进行电解,可以看作封闭体系的是:( )(A)绝热箱中所有物质 (B)两个铜电极(C)蓄电池和铜电极 (D) CuSO 4水溶液5、在下列关于焓的描述中,正确的是( )(A)因为ΔH=QP,所以焓是恒压热(B)气体的焓只是温度的函数(C)气体在节流膨胀中,它的焓不改变(D)因为ΔH=ΔU+Δ(PV),所以任何过程都有ΔH>0的结论6、在标准压力下,1mol 石墨与氧气反应生成1mol 二氧化碳的反应热为ΔrH ,下列哪种说法是错误的? ( )(A) ΔH 是CO2(g)的标准生成热 (B) ΔH =ΔU(C) ΔH 是石墨的燃烧热 (D) ΔU <ΔH7、在标准状态下,反应C 2H 5OH (l )+3O 2(g)→2CO 2(g)+3H 2O(g)的反应焓为Δr H m θ, ΔC p >0, 下列说法中正确的是( )(A)Δr H m θ是C 2H 5OH (l )的标准摩尔燃烧焓(B)Δr H m θ〈0 (C)Δr H m θ=Δr Um θ(D)Δr H m θ不随温度变化而变化8、下面关于标准摩尔生成焓的描述中,不正确的是( )(A)生成反应中的单质必须是稳定的相态单质(B)稳态单质的标准摩尔生成焓被定为零(C)生成反应的温度必须是298.15K(D)生成反应中各物质所达到的压力必须是100KPa9、在一个绝热钢瓶中,发生一个放热的分子数增加的化学反应,那么:( )(A) Q > 0,W > 0,∆U > 0 (B)Q = 0,W = 0,∆U < 0(C) Q = 0,W = 0,∆U = 0 (D) Q < 0,W > 0,∆U < 010、非理想气体进行绝热自由膨胀时,下述答案中哪一个是错误的? ( )(A) Q =0 (B) W =0 (C) ΔU =0 (D) ΔH =011、下列表示式中正确的是 ( )(A)恒压过程ΔH=ΔU+pΔV (B)恒压过程 ΔH=0(C)恒压过程ΔH=ΔU+VΔp (D)恒容过程 ΔH=0 12、理想气体等温反抗恒外压膨胀,则 ( )(A)Q>W (B)Q<W (C)Q=W (D)Q=△U13、当理想气体其温度由298K 升高到348K ,经(1)绝热过程和(2)等压过程,则两过程的 ( )(A)△H 1>△H 2 W 1<W 2 (B)△H 1<△H 2W 1>W 2(C)△H 1=△H 2W 1<W 2 (D)△H 1=△H 2 W 1>W 214、当理想气体从298K ,2×105Pa 经历(1)绝热可逆膨胀和(2)等温可逆膨胀到1×105Pa 时,则( )(A)△H 1<△H 2W 1>W 2 (B)△H 1>△H 2 W 1<W 2(C)△H 1<△H 2W 1<W 2 (D)△H 1>△H 2 W 1>W 215、对于封闭体系,在指定始终态间的绝热可逆途径可以有:( )(A) 一条 (B) 二条 (C) 三条 (D) 三条以上16、实际气体绝热恒外压膨胀时,其温度将: ( )(A) 升高 (B) 降低 (C) 不变 (D) 不确定17、功的计算公式为W=nC v,m (T 2-T 1),下列过程中不能用此式的是( )(A)理想气体的可逆绝热过程(B)理想气体的绝热恒外压过程(C)实际气体的绝热过程(D)凝聚系统的绝热过程18、凡是在孤立体系中进行的变化,其ΔU 和ΔH 的值一定是:( )(A) ΔU > 0 , ΔH > 0 (B) ΔU = 0 , ΔH = 0(C) ΔU < 0 , ΔH < 0 (D) ΔU = 0 , ΔH 大于、小于或等于零不确定19、 一定量的理想气体从同一始态出发,分别经 (1) 等温压缩,(2) 绝热压缩到具有相同压力的终态,以H 1,H 2分别表示两个终态的焓值,则有:( )(A) H 1> H 2 (B) H 1= H 2 (C) H 1< H 2 (D) H 1>=H 220、将H 2(g )与O 2以2:1的比例在绝热刚性密闭容器中完全反应,则该过程中应有( )(A)ΔT=0 (B)Δp=0 (C)ΔU=0 (D)ΔH=021、刚性绝热箱内发生一化学反应,则反应体系为 ( )(A)孤立体系 (B)敞开体系 (C)封闭体系 (D)绝热体系22、理想气体可逆绝热膨胀,则下列说法中正确的是( )(A)焓总是不变 (B)内能总是增加(C)焓总是增加 (D)内能总是减少23、关于等压摩尔热容和等容摩尔热容,下面的说法中不正确的是 ( )(A)C p,m 与C v,m 不相等,因等压过程比等容过程系统多作体积功(B)C p,m –C v,m =R 既适用于理想气体体系,也适用于实际气体体系(C)C v,m =3/2R 适用于单原子理想气体混合物(D)在可逆相变中C p,m 和C v,m 都为无限大24、下列哪个过程的 dT≠0,dH=0? ( )(A)理想气体等压过程(B)实际气体等压过程(C)理想气体等容过程(D)实际气体节流膨胀过程25、隔离系统内发生一变化过程,则系统的:(A)热力学能守恒,焓守恒(B)热力学能不一定守恒,焓守恒(C)热力学能守恒,焓不一定守恒(D)热力学能、焓均不一定守恒二、判断题1、体系在某过程中向环境放热,则体系的内能减少。
第二章 热力学第一定律

第二章热力学第一定律一.判断题1、理想气体的内能U与p和V均无关,所以U与pV也无关。
()2、对于同一热力学体系,其在p~V图上的两条绝热可逆过程线绝不可能相交。
()3、因为Q V= ∆U,Q p = ∆H,而∆U和∆H是状态函数的增量,所以Q V和Q p也只取决于系统的始末态,与过程的具体途径无关。
()4、理想气体恒温膨胀过程中∆U = 0,Q = -W,即膨胀过程中系统所吸收的热全部变成了膨胀功,这是热力学第一定律的必然结果,但却违反了热力学第二定律。
( )二.选择题1、2000K时反应CO(g)+1/2O2(g)=CO2(g)的K p为 6.443,则在同温度下反应为2CO2(g)=2CO(g)+O2(g)的K p应为()A、1/6.443B、(6.443)1/2 C.、(1/6.443)2 D.、1/(6.443)1/22、A和B能形成理想溶液。
已知在100℃时纯液体A的饱和蒸汽压为133.3kPa, 纯液体B 的饱和蒸汽压为66.7 kPa, 当A和B的二元溶液中A的摩尔分数为0.5时,与溶液平衡的蒸气中A的摩尔分数是()A、1B、0.75C、0.667D、0.53、理想气体的真空自由膨胀,哪个函数不变()A。
、ΔS=0 B、V=0 C、ΔG=0 D、ΔH=04、一体积的氢气在0℃,101.3kPa下等温膨胀至原来体积的3倍,其内能变化是多少?(设氢气是理想气体) ()A、0.4JB、0JC、6JD、0.04J5、已知反应CO(g)+1/2O2(g)=CO2(g)的ΔH,下列说法中何者不正确()A.、ΔH是CO2(g)的生成热B.、ΔH是CO(g)的燃烧热C、ΔH是负值D、ΔH与反应ΔU的数值不等6、已知下列反应的平衡常数:()H2(g) + S(s)= H2S(g) K1 ;S(s) + O2(g) = SO2(g) K2;则反应H2S(g) + O2(g)= H2(g) + SO2(g) 的平衡常数为A、K2/K1B、K1—K2 C.、K1×K2D、K1/K27、对于N2和H2混合气体的绝热可逆压缩(没有生产NH3),则()A.、ΔU=0 B 、 ΔH=0 C 、 ΔS=0 D 、 ΔG=08.、298K 时反应Zn+Fe 2+=Zn 2++Fe 的E 0为0.323V ,则其平衡常数为( )A 、 2.89×105 B.、8.34×1010 C 、 5.53×104 D 、 2.35×1029、将H 2O(l)变成同温同压的H 2O(g),则体系的( )A 、内能不变B 、内能可能减少,也可能增加C 、内能增大D 、内能减少10、今有①T ②P ③U ④U m ⑤H ⑥H m ⑦Cp ⑧Cpm,对于理想气体上述量中随物质的量而改变的量有( )A.、①②③ B 、②④⑥ C 、③⑤⑦ D 、③④11、有关CO 2(g)的标准生成热△f H m 有以下说法①C(金刚石)+O 2(g) → CO 2(g) △r H m =△f Hm②CO(g)+0.5O 22(g) △r H m =△f H m③C(无定形)+O 2(g) → CO 2(g) △r H m =△f H m④C(石墨)+O 2(g) →CO 2(g) △r H m =△fH⑤CO(g)+0.5O 2(g) → CO 2(g) C(石墨)+0.5O 2(g)→ CO(g)可通过此二式的标准反应热效应,计算出CO 2(g)的△f Hm ,其中正确的是( )A 、①②B 、②③C 、④⑤D 、③④ 12 、查得298K 时Fe 3O 4,Fe 2O 3,FeO 的标准生成自由能分别为-1014,-741,-257(KJ.mol -1)则在298K101.3KPa 的空气中最稳定的物质是( )A.、Fe 3O 4B.、Fe 2O 3 C 、FeO D 、无法判断13、理想气体经历绝热不可逆过程从状态1(P 1,V 1,T 1)变化到状态2(P 2,V 2,T 2),所做的功为 ( )A 、P 2 V 2 - P 1 V 1B 、P 2(V 2 - V 1)C 、[])/1/1()1/(111222----γγγγV V V P D 、(P 2 V 2 - P 1 V 1)/(1-γ)14、在458K -475K 间,反应:2C 2H 5OH (g)=CH 3COOC 2H 5(g)+2H 2(g)的平衡常数与T 的关系为lgKp=-2100/T+4.66,已知△ f H m (C 2H 5OH,g,473K)=-235.34KJ.mol -1,则 △ f H m (CH 3COOC 2H 5,g,473K)等于:( )A 、-4.305×105J.mol -1B 、-1.951×105J.mol -1 o oC 、5.109×105J.mol -1D 、 2.756×105J.mol -115、反应C(s)+2H 2(g)→CH 4(g)在873K 时△r H m =-85 kJ ⋅mol -1,为获得CH 4的更大平衡产率,问温度和压力怎样选择?( )A 、降低温度,减少压力B 、升高温度,减少压力C 、升高温度,增加压力D 、降低温度,增加压力16、对于反应3H 2(g)+N 2(g)=2NH 3(g),当其中N 2因反应消耗了0.3 mol 时,反应进度ξ等于:( )A 、1.8 molB 、0.9 molC 、0.6 molD 、0.3 mol17、物质能以液体形式存在的最高温度是:( )A 、沸腾温度T bB 、临界温度T cC 、对比温度T rD 、熔融温度T m18、自发过程(即天然过程)的基本特征是 ( )A 、系统能够对外界作功B 、过程进行时不需要外界作功C 、过程发生后, 系统和环境不可能同时恢复原态D 、系统和环境间一定有功和热的交换19、下列说法不正确的是 ( )A 、热力学和统计热力学的研究对象都是大量粒子的集合体;B 、热力学和统计热力学的研究方法都是宏观的方法;C 、1900年,普朗克提出了量子论,引入了能量量子化的概念;D 、吉布斯创立了统计系综的方法,建立了系综理论;20、关于粒子配分函数的概念,不正确的说法是 ( )A 、分函数是无量纲量;B 、配分函数是对体系中所有粒子的所有可能状态的玻兹曼因子求和,故又称状态和;C 、配分函数中任意两项之比等于在该两能级上最概然分布的粒子数之比;D 、配分函数中任意一项与配分函数本身的比值等于粒子分配在该任意能级上的分数;21、对于O 2和N 2混合气体的可逆绝热压缩过程 ( )A 、0=∆UB 、0=∆FC 、0=∆SD 、0=∆G22、1mol 物质A 与1mol 物质B 形成的理想溶液(即理想液态混合物),在压力p 下达气-液两相平衡,已知**B A p p >,则 ( )A 、A A y x =B 、B A y y =C 、A A y x <D 、A A y x >23、100g 的2Cl 与一定量的8S 按反应式628SCl 8Cl 24S =+反应,当2Cl 全部转变成6SCl 时的反应进度ξ (单位:mo1)是 ( )A 、0.0587B 、0.470C 、0.587D 、0.04724、在2000K 时反应)(CO )(1/2O CO(g)22g g =+的标准平衡常数(θK )为6.443,则在同温度下反应)(O C O (g )2)(CO 222gg +=的标准平衡常数为 ( )A 、443.6/1B 、443.6C 、2)443.6/1(D 、443.6/125反应)(CH )(2H C(s)42g g →+在873K 时185-⋅-=∆mol kJ H m r θ,为提高CH 4的平衡产率,温度和压力应如何选择 ( )A 、降低温度,减少压力B 、升高温度,减少压力C 、升高温度,增加压力D 、降低温度,增加压力26、在配制理想溶液(即理想液态混合物)时,下列效应正确的是 ( )A 、∆H mix = 0B 、∆S mix = 0C 、∆G mix > 0D 、∆V mix < 027、 封闭体系,当状态从Ⅰ到Ⅱ发生变化时经历二条任意的不同途径,则 ( )A 、21Q Q =B 、21W W =C 、2211W Q W Q +=+D 、0=∆U28、热力学第一定律ΔU=Q+W 只适用于()(A) 单纯状态变化(B) 相变化(C) 化学变化(D) 封闭物系的任何变化29、关于热和功, 下面的说法中, 不正确的是()(A) 功和热只出现于系统状态变化的过程中, 只存在于系统和环境间的界面上(B) 只有在封闭系统发生的过程中, 功和热才有明确的意义(C) 功和热不是能量, 而是能量传递的两种形式, 可称之为被交换的能量(D) 在封闭系统中发生的过程中, 如果内能不变, 则功和热对系统的影响必互相抵消30、关于焓的性质, 下列说法中正确的是()(A) 焓是系统内含的热能, 所以常称它为热焓(B) 焓是能量, 它遵守热力学第一定律(C) 系统的焓值等于内能加体积功(D) 焓的增量只与系统的始末态有关31、涉及焓的下列说法中正确的是()(A) 单质的焓值均等于零(B) 在等温过程中焓变为零(C) 在绝热可逆过程中焓变为零(D) 化学反应中系统的焓变不一定大于内能变化32、下列哪个封闭体系的内能和焓仅是温度的函数()(A) 理想溶液(B) 稀溶液(C) 所有气体(D) 理想气体33、与物质的生成热有关的下列表述中不正确的是()(A) 标准状态下单质的生成热都规定为零(B) 化合物的生成热一定不为零(C) 很多物质的生成热都不能用实验直接测量(D) 通常所使用的物质的标准生成热数据实际上都是相对值34、dU=CvdT及dUm=Cv,mdT 适用的条件完整地说应当是()(A) 等容过程(B)无化学反应和相变的等容过程(C) 组成不变的均相系统的等容过程(D) 无化学反应和相变且不做非体积功的任何等容过程及无反应和相变而且系统内能只与温度有关的非等容过程35、下列过程中, 系统内能变化不为零的是()(A) 不可逆循环过程(B) 可逆循环过程(C) 两种理想气体的混合过程(D) 纯液体的真空蒸发过程36、第一类永动机不能制造成功的原因是()(A) 能量不能创造也不能消灭(B) 实际过程中功的损失无法避免(C) 能量传递的形式只有热和功(D) 热不能全部转换成功37、盖斯定律包含了两个重要问题, 即()(A) 热力学第一定律和热力学第三定律(B) 热力学第一定律及热的基本性质(C) 热力学第三定律及热的基本性质(D) 热力学第一定律及状态函数的基本特征38.当某化学反应ΔrCp,m<0,则该过程的随温度升高而()(A) 下降(B) 升高(C) 不变(D) 无规律39、在下面涉及盖斯定律的表述中, 不正确的是()(A) 对在等温等压且不做非体积功的条件下, 发生的各个化学反应过程和相变过程, 可使用盖斯定律(B) 对在等温等容且不做功的条件下, 发生的各个化学反应过程, 可使用盖斯定律(C) 同一物质在盖斯定律涉及的几个反应中都出现时, 只要无溶解等现象, 相态不同也可加减(D) 利用盖斯定律求某个反应的热效应时可引入一些别的反应,设想一些中间步骤, 无论实际反应是否按这些中间步骤进行都可以40、下面的说法符合热力学第一定律的是()(A) 在一完全绝热且边界为刚性的密闭容器中发生化学反应时,其内能一定变化(B) 在无功过程中, 内能变化等于过程热, 这表明内能增量不一定与热力学过程无关(C) 封闭系统在指定的两个平衡态之间经历绝热变化时, 系统所做的功与途径无关(D) 气体在绝热膨胀或绝热压缩过程中, 其内能的变化值与过程完成的方式无关41、关于热平衡, 下列说法中正确的是()(A) 系统处于热平衡时, 系统的温度一定等于环境的温度(B) 并不是所有热力学平衡系统都必须满足热平衡的条件(C) 若系统A与B成热平衡, B与C成热平衡, 则A与C直接接触时也一定成热平衡(D) 在等温过程中系统始终处于热平衡42、对于功, 下面的说法中不正确的是()(A) 在系统对环境做功或环境对系统做功时, 环境中一定会留下某种痕迹(B) 功的量值与系统的始末态有关(C) 无论做什么功都伴随着系统中某种物质微粒的定向运动(D) 广义功=广义力³广义位移。
第二章热力学第一定律复习题(最新整理)

热力学第一定律一、选择题1、有理想气体,温度由T 1变到T 2,压力由P 1变到P 2,则:( )a.;b.;T nC Hm p ∆=∆,T nC Q m p ∆=,c.;d.T nC Q m V ∆=,TnC T nC W m V m p ∆-∆=,,2、,式中W 代表:( )W Q U +=∆a.体积功; b.非体积功c.体积功和非体积功的和;d.体积功和非体积功的差。
3、对W 的规定是:( )a.环境对体系做功W 为正;b. 环境对体系做功W 为负c. 体系对环境做功W 为正;d. W 总为正4、焓的定义式是:( )a.; b. pV U H +=∆pV U H -=c. ;d. pV U H +=pV U H ∆+∆=∆5、反应 H 2(g) + 1/2O 2(g) = H 2O(l) 的 是:( )θm r H ∆a.H 2O(l)的标准生成焓; b.H 2(g)的标准燃烧焓;c.既是H 2O(l)的标准生成焓又是H 2(g)的标准燃烧焓;d.以上三种说法都对。
6、理想气体的 ( ),,/p m V m C C a.大于1; b.小于1;c.等于1;d.以上三者皆有可能。
7、某化学反应的,该化学反应的反应热:( )0=∆p r C a.不随温度而变; b.随温度升高而增大; c.随温度升高而减小; d.随温度降低而降低。
8、封闭物系 ( )a.不与环境交换功;b.不与环境交换热;c.不与环境交换物质;d.物系内物质种类不改变9、用公式 计算某反应在温度T 的反应焓变,要求:⎰∆+∆=∆Tp dT C H T H 298)298()(( )a.反应恒容;b.T >298K ;c.△C P ≠0;d. 298~T 间反应物和产物无相变10、气体标准态规定为 ( )a.298.15K ,100KPa 状态;b.100KPa ,298.15K 纯理想气体状态;c.100KPa 纯理想气体状态;d.298.15K ,101.325KPa 理想气体状态。
第二章 热力学第一定律--题加答案

第二章热力学第一定律1. 始态为25 °C,200 kPa的5 mol某理想气体,经途径a,b两不同途径到达相同的末态。
途经a先经绝热膨胀到-28.47 °C,100 kPa,步骤的功;再恒容加热到压力200 kPa的末态,步骤的热。
途径b为恒压加热过程。
求途径b的及。
(天大2.5题)解:先确定系统的始、末态对于途径b,其功为根据热力学第一定律2. 2 mol某理想气体,。
由始态100 kPa,50 dm3,先恒容加热使压力增大到200 dm3,再恒压冷却使体积缩小至25 dm3。
求整个过程的。
(天大2.10题)解:过程图示如下由于,则,对有理想气体和只是温度的函数该途径只涉及恒容和恒压过程,因此计算功是方便的根据热力学第一定律3. 单原子理想气体A与双原子理想气体B的混合物共5 mol,摩尔分数,始态温度,压力。
今该混合气体绝热反抗恒外压膨胀到平衡态。
求末态温度及过程的。
(天大2.18题)解:过程图示如下分析:因为是绝热过程,过程热力学能的变化等于系统与环境间以功的形势所交换的能量。
因此,单原子分子,双原子分子由于对理想气体U和H均只是温度的函数,所以4. 1.00mol(单原子分子)理想气体,由10.1kPa、300K按下列两种不同的途径压缩到25.3kPa、300K,试计算并比较两途径的Q、W、ΔU及ΔH。
(1)等压冷却,然后经过等容加热;(2)等容加热,然后经过等压冷却。
解:C p,m=2.5R, C V,m=1.5R(1)10.1kPa、300K 10.1kPa、119.8 25.3kPa、300K0.2470dm30.09858 dm30.09858 dm3Q=Q1+Q2=1.00×2.5R×(119.8-300)+ 1.00×1.5R×(300-119.8)=-3745+2247=-1499(J)W=W1+W2=-10.1×103×(0.09858-0.2470)+0=1499(J)ΔU=Q+W=0ΔH=ΔU+Δ(pV)=0+25.3×0.09858-10.1×0.2470=0(2)10.1kPa、300K 25.3kPa、751.6 25.3kPa、300K0.2470dm30.2470dm30.09858 dm3Q=Q1+Q2=1.00×1.5R×(751.6-300)+ 1.00×2.5R×(300-751.6)=5632-9387=-3755(J)W=W1+W2=0-25.3×103×(0.09858-0.2470) =3755(J)ΔU=Q+W=0ΔH=ΔU+Δ(pV)=0+25.3×0.09858-10.1×0.2470=0计算结果表明,Q、W与途径有关,而ΔU、ΔH与途径无关。
热力学第一定律物理化学考试题(卷)目

第二章热力学第一定律时间:2013-4-21 来源:匿名此新闻被浏览:2385 次1.热力学第一定律ΔU=Q+W 只适用于(A) 单纯状态变化 (B) 相变化(C) 化学变化 (D) 封闭物系的任何变化答案:D2.关于热和功, 下面的说法中, 不正确的是(A) 功和热只出现于系统状态变化的过程中, 只存在于系统和环境间的界面上(B) 只有在封闭系统发生的过程中, 功和热才有明确的意义(C) 功和热不是能量, 而是能量传递的两种形式, 可称之为被交换的能量(D) 在封闭系统中发生的过程中, 如果内能不变, 则功和热对系统的影响必互相抵消答案:B3.关于焓的性质, 下列说法中正确的是(A) 焓是系统内含的热能, 所以常称它为热焓(B) 焓是能量, 它遵守热力学第一定律(C) 系统的焓值等于内能加体积功(D) 焓的增量只与系统的始末态有关答案:D。
因焓是状态函数。
4.涉及焓的下列说法中正确的是(A) 单质的焓值均等于零(B) 在等温过程中焓变为零(C) 在绝热可逆过程中焓变为零(D) 化学反应中系统的焓变不一定大于内能变化答案:D。
因为焓变ΔH=ΔU+Δ(pV),可以看出若Δ(pV)<0则ΔH<ΔU。
5.下列哪个封闭体系的内能和焓仅是温度的函数(A) 理想溶液 (B) 稀溶液 (C) 所有气体 (D) 理想气体答案:D6.与物质的生成热有关的下列表述中不正确的是(A) 标准状态下单质的生成热都规定为零(B) 化合物的生成热一定不为零(C) 很多物质的生成热都不能用实验直接测量(D) 通常所使用的物质的标准生成热数据实际上都是相对值答案:A。
按规定,标准态下最稳定单质的生成热为零。
7.dU=CvdT及dUm=Cv,mdT适用的条件完整地说应当是(A) 等容过程(B)无化学反应和相变的等容过程(C) 组成不变的均相系统的等容过程(D) 无化学反应和相变且不做非体积功的任何等容过程及无反应和相变而且系统内能只与温度有关的非等容过程答案:D8.下列过程中, 系统内能变化不为零的是(A) 不可逆循环过程 (B) 可逆循环过程(C) 两种理想气体的混合过程(D) 纯液体的真空蒸发过程答案:D。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
1
第二章 热力学第一定律
一、 选择题
1、下列叙述中不具状态函数特征的是:( )
(A)系统状态确定后,状态函数的值也确定
(B)系统变化时,状态函数的改变值只由系统的初终态决定
(C)经循环过程,状态函数的值不变
(D)状态函数均有加和性
2、下列叙述中,不具可逆过程特征的是:( )
(A)过程的每一步都接近平衡态,故进行得无限缓慢
(B)沿原途径反向进行时,每一小步系统与环境均能复原
(C)过程的初态与终态必定相同
(D)过程中,若做功则做最大功,若耗功则耗最小功
3、如图,将CuSO4水溶液置于绝热箱中,插入两个铜电极,
以蓄电池为电源进行电解,可以看作封闭体系的是:( )
(A)绝热箱中所有物质 (B)两个铜电极
(C)蓄电池和铜电极 (D) CuSO 4水溶液
5、在下列关于焓的描述中,正确的是( )
(A)因为ΔH=QP,所以焓是恒压热
(B)气体的焓只是温度的函数
(C)气体在节流膨胀中,它的焓不改变
(D)因为ΔH=ΔU+Δ(PV),所以任何过程都有ΔH>0的结
论
6、在标准压力下,1mol 石墨与氧气反应生成1mol 二氧化碳的
反应热为Δr H ,下列哪种说法是错误的? ( )
(A) ΔH 是CO2(g)的标准生成热 (B) ΔH =ΔU
(C) ΔH 是石墨的燃烧热 (D) ΔU <ΔH
7、在标准状态下,反应C 2H 5OH (l )+3O 2(g)
→2CO 2(g)+3H 2O(g)的反应焓为Δr H m θ, ΔC p >0, 下列说法
中正确的是( )
(A)Δr H m θ是C 2H 5OH (l )的标准摩尔燃烧焓
(B)Δr H m θ〈0 (C)Δr H m θ=Δr Um θ
(D)Δr H m θ不随温度变化而变化
8、下面关于标准摩尔生成焓的描述中,不正确的是( )
(A)生成反应中的单质必须是稳定的相态单质
(B)稳态单质的标准摩尔生成焓被定为零
(C)生成反应的温度必须是298.15K
(D)生成反应中各物质所达到的压力必须是100Kpa
9、在一个绝热钢瓶中,发生一个放热的分子数增加的化学反应,
那么:( )
(A) Q > 0,W > 0,∆U > 0 (B)Q = 0,W = 0,∆U < 0
(C) Q = 0,W = 0,∆U = 0 (D) Q < 0,W > 0,∆U < 0
10、非理想气体进行绝热自由膨胀时,下述答案中哪一个是错误
的? ( )
(A) Q =0 (B) W =0 (C) ΔU =0 (D) ΔH =0
11、下列表示式中正确的是 ( )
(A)恒压过程ΔH=ΔU+pΔV (B)恒压过程 ΔH=0
(C)恒压过程ΔH=ΔU+VΔp (D)恒容过程 ΔH=0
12、理想气体等温反抗恒外压膨胀,则 ( )
(A)Q>W (B)Q<W (C)Q=W (D)Q=△U
13、当理想气体其温度由298K 升高到348K ,经(1)绝热过程和
(2)等压过程,则两过程的 ( )
(A)△H 1>△H 2 W 1<W 2 (B)△H 1<△H 2 W 1>W 2
(C)△H 1=△H 2 W 1<W 2 (D)△H 1=△H 2 W 1>W 2
14、当理想气体从298K ,2×105Pa 经历(1)绝热可逆膨胀
和(2)等温可逆膨胀到1×105Pa 时,则( )
(A)△H 1<△H 2 W 1>W 2 (B)△H 1>△H 2 W 1<W 2
(C)△H 1<△H 2 W 1<W 2 (D)△H 1>△H 2 W 1>W 2
15、对于封闭体系,在指定始终态间的绝热可逆途径可以有:
( )
(A) 一条 (B) 二条 (C) 三条 (D) 三条以上
16、实际气体绝热恒外压膨胀时,其温度将: ( )
(A) 升高 (B) 降低 (C) 不变 (D) 不确定
17、功的计算公式为W=nC v,m (T 2-T 1),下列过程中不能用此
式的是( )
(A)理想气体的可逆绝热过程
(B)理想气体的绝热恒外压过程
(C)实际气体的绝热过程
(D)凝聚系统的绝热过程
18、凡是在孤立体系中进行的变化,其ΔU 和ΔH 的值一定是:
( )
(A) ΔU > 0 , ΔH > 0 (B) ΔU = 0 , ΔH = 0
(C) ΔU < 0 , ΔH < 0
(D) ΔU = 0 , ΔH 大于、小于或等于零不确定
19、 一定量的理想气体从同一始态出发,分别经 (1) 等温压缩,
(2) 绝热压缩到具有相同压力的终态,以H 1,H 2分别表示两个
终态的焓值,则有:( )
(A) H 1> H 2 (B) H 1= H 2 (C) H 1< H 2 (D) H 1>=H 2
20、将H2(g)与O2以2:1的比例在绝热刚性密闭容器中完全反应,则该过程中应有()
(A)ΔT=0 (B)Δp=0 (C)ΔU=0 (D)ΔH=0
21、刚性绝热箱内发生一化学反应,则反应体系为( )
(A)孤立体系(B)敞开体系(C)封闭体系(D)绝热体系
22、理想气体可逆绝热膨胀,则下列说法中正确的是
( )
(A)焓总是不变(B)内能总是增加
(C)焓总是增加(D)内能总是减少
23、关于等压摩尔热容和等容摩尔热容,下面的说法中不
正确的是( )
(A)C p,m与C v,m不相等,因等压过程比等容过程系统多作
体积功
(B)C p,m–C v,m=R既适用于理想气体体系,也适用于实际气
体体系
(C)C v,m=3/2R适用于单原子理想气体混合物
(D)在可逆相变中C p,m和C v,m都为无限大
24、下列哪个过程的dT≠0,dH=0?( )
(A)理想气体等压过程(B)实际气体等压过程
(C)理想气体等容过程(D)实际气体节流膨胀过程
一、选择题
题号 1 2 3 5 6 7 8 9 10
答案 D C A C D B C C D
题号11 12 13 14 15 16 17 18 19 20
答案 A C C C A D C D C C
题号21 22 23 24 25
答案 A D B D C
二、判断题
1 2 3 4 5 6 7 8 9 10
××√√×√√××√25、隔离系统内发生一变化过程,则系统的:
(A)热力学能守恒,焓守恒
(B)热力学能不一定守恒,焓守恒
(C)热力学能守恒,焓不一定守恒
(D)热力学能、焓均不一定守恒
判断题
1、体系在某过程中向环境放热,则体系的内能减少。
( ) 2恒温过程的Q一定是零。
()
3、经历任意一个循环过程时,系统从环境吸收的热等于系统对外所做的功()
4尽管Q和W都是途径函数,但(Q+W)的数值与途径无关。
()
5、由于热力学能是状态函数,则理想气体的状态改变时,其热力学能一定跟着改变()
6、封闭体系经历一个不作其它功的等压过程,其热量只决定于体系的初终态()
7在绝热、密闭、坚固的容器中发生化学反应,△U一定为零,△H不一定为零。
()
8不可逆过程就是过程发生后,系统不能再复原的过程。
()
9、因△H = Q p所以只有等压过程才有△H。
()
10、理想气体,不管是恒压过程,还是恒容过程,公式
⎰=
∆dT
C
H
p
都适用。
()
2。
