有机化学课件第二章现代仪器分析方法及应用
《现代仪器分析》课件

现代仪器分析是一门前沿的科学技术,通过使用现代化的仪器设备,对样品 进行分析和测试,帮助我们更好地了解物质的组成和性质。
课程简介
介绍《现代仪器分析》课程的目标和内容,包括仪器使用的基本原理、实验操作技巧和数据分析方法。
现代仪器分析的基本概念
1 仪器选择
根据不同的分析需求选 择适合的仪器,如质谱 仪、色谱仪等。
环境样品测试
对环境中的污染物进行分析和 检测,保护环境和生态安全。
药物分析
对药物的质量和安全性进行分 析和评估,确保药物的有效性 和可靠性。
结论与总结
通过本课程的学习,我们深入了解了现代仪器分析的基本原理和实际应用,为今后的科学研究和实 践打下了坚实的物理和 化学原理,理解分析手 段和方法。
3 仪器操作
学习正确使用和操作仪 器,保证实验结果的准 确性和可靠性。
常见现代仪器分析技术
质谱技术
通过质谱设备,对样品中的 化合物进行定性和定量分析, 广泛应用于生物医药、环境 科学等领域。
光谱技术
利用不同波长的光与物质相 互作用的特性进行分析,如 紫外可见光谱、红外光谱等。
数据分析与处理
1
数据获取
通过仪器获得样品分析的原始数据,包括光谱图、质谱图等。
2
数据处理
对原始数据进行数据清洗、信号提取和数据变换等处理,以获得有用的信息。
3
数据解释
根据分析结果和相关背景知识,对数据进行解释和评估。
案例分析
化学分析
通过现代仪器对化学反应和反 应产物进行分析,帮助解决实 际问题。
色谱技术
通过分离样品中的化合物, 达到定性和定量分析的目的, 如气相色谱、液相色谱等。
《现代仪器分析方法》课件

结束语
仪器分析方法对科研和实际应用的意义
总结仪器分析方法在科研和实际应用中的重要 作用。
发展趋势预测
展望仪器分析方法的未来发展趋势和潜在的创 新方向。
第二章 原理与方法
1
紫外-可见分光光度法
2
详细阐述紫外-可见分光光度法的工作原
理和在生物化学和环境分析中的使用。
3
核磁共振波谱法
4
介绍核磁共振波谱法的工作原理和在有 机化学和生物医学研究中的重要性。
原子吸收光谱法
解释原子吸收光谱法的基本原理和在分 析金属元素中的应用。
荧光光谱法
探索荧光光谱法的基本概念以及在药物 分析和生物分子鉴定中的应用。
第三章 分析仪器
气相色谱仪
探索气相色谱仪的组成和原理,以及在药物分析和 食品安全领域中的应用。
高效液相色谱仪
详述高效液相色谱仪的基本结构和工作原理,并介 绍其在环境和生物样品分析中的应用。
离子色谱仪
讲解离子色谱仪的原理和在环境和食品质量检测中 的重要性。
质谱仪
解释质谱仪的原理和在化学分析和药物代谢研究中 的应用。
第五章 前沿技术
发光光谱法
探索发光光谱法的创新应用和在生命科学和材 料科学中的前沿研究。
原子荧光光谱法
讲解原子荧光光谱法的新兴应用和在环境污染 检测和矿产资源分析中的重要性。
电化学分析法
详细介绍电化学分析法的原理和在能源领域以 及环境监测中的应用。
能量色散X射线荧光光谱法
介绍能量色散X射现代仪器分析方法》 PPT课件
# 现代仪器分析方法PPT课件
第一章 概述
仪器分析方法定义
简单介绍仪器分析方法及其在科研和实际应用 中的重要性。
现代仪器分析方法及应用PPT74页

51、没有哪个社会可以制订一部永远 适用的 宪法, 甚至一 条永远 适用的 法律。 ——杰 斐逊 52、法律源于人的自卫本能。——英 格索尔
53、人们通常会发现,法律就是这样 一种的 网,触 犯法律 的人, 小的可 以穿网 而过, 大的可 以破网 而出, 只有中 等的才 会坠入 网中。 ——申 斯通 54、法律就是法律它是一座雄伟的大 夏,庇 护着我 们大家 ;它的 每一块 砖石都 垒在另 一块砖 石上。 ——高 尔斯华 绥 55、今天的法律未必明天仍是法律。 ——罗·伯顿
39、勿问成功的秘诀为何,且尽全力做你应该做的事吧。——美华纳
40、学而不思自己知道紧在哪里。——西班牙
37、我们唯一不会改正的缺点是软弱。——拉罗什福科
xiexie! 38、我这个人走得很慢,但是我从不后退。——亚伯拉罕·林肯
现代仪器分析ppt课件

热噪声(Thermal, or Johnson, noise)
属于白噪音(white noise),由元器件中电子或电荷 受热激发所产生的噪音信号。由于荷电粒子受激的随 机性和周期性,因而会导致电荷的不均一,进而使读 出的信号发生波动。只有在绝对零度时,该噪音才会 消失。
当电阻R,T,则N。(如UV二极管阵列检测器 在77K时,其噪音下降一半左右;此外,减少带宽,可 降低噪音,但同时也会延长响应时间,并降低测定的 可靠性。
现代仪器分析
主讲:
1
尹洪宗简介:
南开大学分析化学专业博士 教授,化学院副院长。 主要从事金纳米材料的光谱特性研究、散射光谱研究以及
稀土元素配合物及其荧光研究。 在《化学学报》、《分析化学》、 《Anal. Lett.》 、
《Talanta》等刊物发表论文30余篇,SCI收录16篇 办公室:文理大楼707 电话:8249248 E-mail: hzyin@
分析灵敏度 k / s
优点:当仪器信号放大时,k 值增加,灵敏度提高;
但此时 s 也相应增加,从而一定程度地保证了 灵敏度恒定;
缺点:s 与浓度有关,即灵敏度随浓度而变化!
21
2)检测限(Detection limit, DL)
检测限:在已知置信水平,可以检测到的待测物的最 小质量或浓度。它和分析信号(Signal)与 空白信号的波动(噪音, Noise)有关,或者 说与信噪比(S/N)有关。
化学分析
仪器分析
从原理看 根据化学反应计量 根据物质的物理或者物理化
关系
学性质、参数及变化规律
从仪器看 简单玻璃仪器
较复杂特殊的仪器
从操作看 从试样看 从应用看
多为手工操作、较 复杂
现代仪器分析课件ppt

校正方法: 用邻近非共振线校正背景 连续光源校正背景 塞曼 效应校正背景 自吸效应校正背景
在 整 堂 课 的 教学中 ,刘教 师总是 让学生 带着问 题来学 习,而 问题的 设置具 有一定 的梯度 ,由浅 入深, 所提出 的问题 也很明 确
在 整 堂 课 的 教学中 ,刘教 师总是 让学生 带着问 题来学 习,而 问题的 设置具 有一定 的梯度 ,由浅 入深, 所提出 的问题 也很明 确
贫燃火焰:指助燃气大于化学计量的火焰,它的温度 较低,有较强的氧化性,有利于测定易解离,易电离 元素,如碱金属。
在 整 堂 课 的 教学中 ,刘教 师总是 让学生 带着问 题来学 习,而 问题的 设置具 有一定 的梯度 ,由浅 入深, 所提出 的问题 也很明 确
2、非火焰原子化器(石墨炉原子化器)
Ni / N0 = gi / g0 exp(- Ei / kT)
统计权重 表示能级 的简并度
激发能
Boltzman 常数
热力学 温度
在 整 堂 课 的 教学中 ,刘教 师总是 让学生 带着问 题来学 习,而 问题的 设置具 有一定 的梯度 ,由浅 入深, 所提出 的问题 也很明 确
二、原子吸收光谱轮廓
消除办法:配制与被测试样组成相近的标准溶液 或采用标准加入法。若试样溶液的浓度高,还可采用 稀释法。
在 整 堂 课 的 教学中 ,刘教 师总是 让学生 带着问 题来学 习,而 问题的 设置具 有一定 的梯度 ,由浅 入深, 所提出 的问题 也很明 确
2.化学干扰
化学干扰是由于被测元素原子与共存组份发生化学反 应生成稳定的化合物,影响被测元素的原子化,而引起 的干扰。
现代仪器分析方法及应用

现代仪器分析方法及应用一、分光光度法分光光度法利用物质对光的吸收、散射、干涉、闪烁等现象进行分析。
常用的分光光度法有紫外可见分光光度法、红外吸收分光光度法、原子吸收分光光度法等。
分光光度法广泛应用于药物分析、环境分析、食品分析等领域。
二、电化学方法电化学方法通过测定电极上物质的电荷转移过程或与电极表面发生的电化学反应来进行分析。
常用的电化学方法有电位滴定法、电化学溶液分析法、恒定电流伏安法等。
电化学方法在药物分析、环境分析、金属离子检测等方面具有广泛应用。
三、质谱分析法质谱分析法通过测定样品中物质的质量与电荷比来进行分析。
常用的质谱分析法有质子化质谱法、电喷雾质谱法、时间飞行质谱法等。
质谱分析法在有机化合物的结构分析、食品中农药残留的检测以及毒性物质的鉴定等方面具有重要应用。
四、色谱分析法色谱分析法通过分离和测定化合物混合物中不同组分的相对含量来进行分析。
常用的色谱分析法有气相色谱法、液相色谱法、超高效液相色谱法等。
色谱分析法广泛应用于药物分析、食品分析、环境分析等领域。
五、核磁共振法核磁共振法利用原子核间的磁耦合和原子核的磁共振现象来进行分析。
常用的核磁共振法有氢核磁共振波谱法、碳核磁共振波谱法等。
核磁共振法在有机化合物结构鉴定、药物分析和生物分子结构研究等方面具有重要应用。
六、质量光谱法质量光谱法通过测定物质的质量与电荷比来进行定性和定量分析。
常用的质谱法有线性离子阱质谱法、四级杆质谱法等。
质谱法广泛应用于有机物质的结构分析、药物代谢研究以及环境污染物的检测等领域。
以上是现代仪器分析方法的几个主要方向,这些方法在现代化学分析中具有重要的地位和作用。
随着科学技术的不断发展,这些方法将进一步提高其灵敏度、准确性和快速性,为化学分析提供更多的选择和可能性。
同时,仪器分析方法的应用范围也将进一步拓展,为人类社会的发展与进步做出更大的贡献。
现代仪器分析PPT课件

• 1、作好笔记。 • 2、课后要复习。 • 3、按时完成作业。 • 4、做好实验。
第1页/共52页
第一章 绪论
第一节 概述 第二节 仪器分析方
法的主要评价指标
第2页/共52页
分析化学与仪器分析的关系?
• 分析化学是研究分析方法的科学或学科 • 是一门人们赖以获得 物质组成、结构和 形态 的信息的科学
第23页/共52页
分析仪器的微型化和智能化
随着分子计算机、DNA计算机、光子计算机、量子计算机等的不断推出, 计算机也将越来越微型化。计算机(电脑)与人脑的结合将不再是一个梦、带 有植入式电脑的人的智能将大大超过不带电脑的“自然人”。
第24页/共52页
分析仪器的大众化、个性化和日用品化,贵重仪器的网 络化
析化学由一门操作技术变成一门科学;
•
20世纪40年代前,化学分析占主导地位,仪器分析种类少和精度低;
第10页/共52页
阶段二:
20世纪40年代后,仪器分析的大发展时期。 仪器分析使分析速度加快,促进化学工业发展; 化学分析与仪器分析并重,仪器分析自动化程度低; 为什么出现在这一时期?一系列重大科学发现,为仪器分 析的建立和发展奠定基础。 (1)Bloch F 和Purcell E M;建立了核磁共振测定方法;诺 贝尔化学奖1952年; (2)Martin A J P 和Synge R L M;建立了气相色谱分析法 ;诺贝尔化学奖1952年; (3)Heyrovsky J,建立极谱分析法,诺贝尔化学奖1959年 仪器分析的发展引发了分析化学的第二次变革。
3. 过失误差
第40页/共52页
三、误差的减免
1. 系统误差的减免
(1) 方法误差—— 采用标准方法,对比实验 (2) 仪器误差—— 校正仪器 (3) 试剂误差—— 作空白实验
有机化学作业第二章现代仪器分析方法及应用
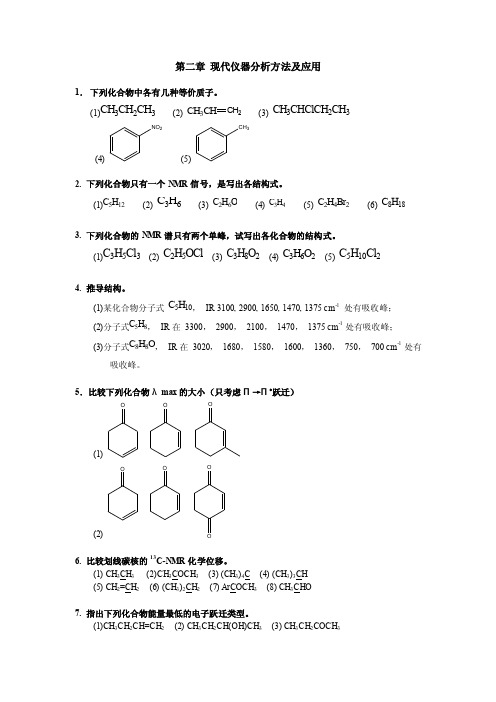
第二章现代仪器分析方法及应用1.下列化合物中各有几种等价质子。
(1)CH3CH2CH3(2) CH3CH CH2(3) CH3CHClCH2CH3(4) NO2(5)CH32.下列化合物只有一个NMR信号,是写出各结构式。
(1)C5H12(2) C3H6(3) C2H6O(4) C3H4(5) C2H4Br2(6) C8H18 3. 下列化合物的NMR谱只有两个单峰,试写出各化合物的结构式。
(1)C3H5Cl3(2) C2H5OCl(3) C3H8O2(4) C3H6O2(5) C5H10Cl24. 推导结构。
(1)某化合物分子式C5H10,IR 3100, 2900, 1650, 1470, 1375 cm-1处有吸收峰;(2)分子式C5H8,IR在3300,2900,2100,1470,1375 cm-1 处有吸收峰;(3)分子式C8H8O,IR在3020,1680,1580,1600,1360,750,700 cm-1 处有吸收峰。
5.比较下列化合物λmax的大小(只考虑П→П*跃迁)(1)O O O(2) O O OO6. 比较划线碳核的13C-NMR化学位移。
(1) CH3CH3(2)CH3COCH3(3) (CH3)4C (4) (CH3)3CH(5) CH2=CH2(6) (CH3)2CH2(7) ArCOCH3(8) CH3CHO7. 指出下列化合物能量最低的电子跃迁类型。
(1)CH3CH2CH=CH2(2) CH3CH2CH(OH)CH3(3) CH3CH2COCH3(4) CH3CH2OCH2CH3(5) CH2=CHCH=O8.解释:乙醇和乙二醇四氯化碳浓溶液的IR谱在3350cm-1处都有一个宽的O-H吸收带。
当用四氯化碳稀释这两种醇溶液时,乙二醇光谱的这个吸收带不变,而乙醇光谱的这个带被3600cm-1的一个尖峰替代。
9.下列化合物的1HNMR谱图中都只有一个单峰,试推测他们的结构。
《有机化学》NMR,IR,UV,MS

IR (Infrared Spectrum)
信号的强度: 极性键出峰较强 极性变化大的振动方式,出峰较强 定量分析
A=cl
信号的位置:
波数: =/c 单位:cm-1
官能团区
指纹区
与H结合的官能团 伸缩振动:
O-H,N-H,C-H,S-H
力常数大的键的伸缩振动: -CC-,-C N,-C=C=C-,-C=C=O, -N=C=O
3、 13C 同位素丰度较小
10 C 0-30 ppm (CH2)n n=4-7 22-27 ppm
20 C 25-45 ppm 苯环
128.5 ppm
30 C 30-60 ppm -CHO
175-205 ppm
40 C 35-70 ppm R-CO-R’
200-220 ppm
=C ~ 120 ppm -C=C-CO-R 180-210 ppm
信号的强度: 由样品性质决定 定量分析
A=cl
信号的位置: 由跃迁方式决定
* * n
n* * n* * * *
UV与分子结构的关系: 1、饱和化合物 2、不饱和化合物 非共轭 共轭 3、芳香族化合物
力常数较大的键: C=C,C=O,C=N,N=O
IR与结构的关系:
1、碳-碳伸缩振动 2、碳-氢伸缩振动 3、氢键的影响 4、共轭的影响
MS Mass Spectrum
UV Ultraviolet Spectrum
价电子跃迁吸收或放出的能量落于 紫外区
100-200 nm 远紫外(真空紫外) 200-400 nm 近紫外 400-800 nm 可见光谱
第二章 现代仪器分析方法及应用
电子课件仪器分析分析方法及应用

溶液的pH过高或过低会降低有色配合物 的稳定性
溶液酸度变化时,显色剂本身的颜色会发 生变化
pH过低可能会引起被测金属离子水解而 破坏了有色配合物而无法测定
电子课件仪器分析分析方法及应用
2.4.3 测量条件的选择
1、入射 光波长
的选择
2.4.6 应用
1 、配合物组成及 稳定常数的测定
• 摩尔比法 • 连续变化法
2、分光光度滴定
电子课件仪器分析分析方法及应用
摩尔比法测定配位比n
K稳=AaAb/(Aa-Ab)2cM
电子课件仪器分析分析方法及应用
连续变化法测定配位比n
A
K稳=AaAb/(Aa-Ab)2cM
n=V /V R M 电子课件仪器分析分析方法及应用
2、参比 溶液的 选择
测量条件 的选择
3、A值 范围的 选择
电子课件仪器分析分析方法及应用
2.4.4 定量方法的选择
单组分 样品的 测量
多组分 样品的 测量
高含量 组分的 测量
双波长 分光光 度法
电子课件仪器分析分析方法及应用
2.4.5 分析误差
溶液因素 误差
仪器因素 误差
电子课件仪器分析分析方法及应用
VR/(VR+VM)
2.5 目视比色法
方法原理
测定方法
特点
电子课件仪器分析分析方法及应用
2.6 紫外分光光度法
The Similarities
The Differences
电子课件仪器分析分析方法及应用
2.6.2 方法原理
电子课件仪器分析分析方法及应用
σ*反键
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
1660 cm-1
4、氢键的影响:(分子内、分子间氢键)对峰位,峰强产 生极明显影响,使伸缩振动频率向低波数方向 移动,峰变宽、变强。
分子间氢键对—OH伸缩吸收 峰影响:
游离伯醇: 3640 cm-1
双分子缔合: 3550-3450 cm-1
=C-H C-H O-H 氢键
O-H S-H P-H
N-H
C≡C
C=C
C=O C-C, C-N, C-X
N-O N-N C-F
C-X
C≡N
C=N
C-H, N-H, O-H
3500 3000 2500 2000 1500 1500 1000 500
特征区
指纹区
2.6 红外光谱与分子结构
1、碳-碳伸缩振动
20.0 7
-118 17
20
Acetone-d6 2.05 5 2.2
206.68 13 0.9
2.8
57 -94
29.92 7 19.4
Solvent
1H Chemical
HOD in 13C Chemical
Shift
JHD solvent
Shift
JCD B.P. M.P.
(Hz)
(Hz) (oC) (oC)
2.2 核磁共振的基本原理
600 MHz NMR
750 MHz NMR
800 MHz NMR
NMR仪器的基本组成
原子核的磁矩和磁共振
原子核的自旋运动和自旋量子数 I 相关。 核自旋量子数:I 原子核置于磁场中,将有:2I + 1 个取向
m = 1/2
m = -1/2 I = 1/2
m=1 m=0
CH = 2.8
CH = 2.8
2.3.2 信号的裂分:偶合常数
• 表示法: J 单位:Hz mJn m:表示两个偶合核之 间间隔键的数目 n: 其它信息
1)偶合的产生:自旋-自旋偶合
HA
HB +1/2
R1 CA CB R4 R2 R3
去屏蔽 B与外磁场平行
HA
HB -1/2
R1 CA CB R4 R2 R3
屏蔽 B与外磁场反平行
B不存在时,A的化学位移
偶合常数
2)裂分规律
• 相隔三根单键以上,一般J ≈ 0
O
CH3CH2 C CH3
• 等价质子(磁等价)互不裂分
CH4 CH3CH3 • 具有沿共价键的意味
CH3CH2Cl
CH3c
CH3d
• n + 1 规律
Ha
Hb
J ac ≠ Jad
n + 1 规律:一组化学等价的质子被一组数目为n的等 价质子裂分时,那么其吸收峰数目为n+1, 峰强比例符合二项式。
1H-NMR spectra for BS2PEP and re-oxidized BS2PEP recorded in 100% (v/v) [methyl-2H]methanol The spectra for BS2PEP oxidized in methanol (A) and BS2PEP reduced and oxidized in aqueous solution (B) are identical, indicating that both have the same structure and hence the same disulphide connectivity.
=2.12-3.10
CH2Cl2 =5.30
3.5
O-CH3
= 3.24-4.02
CHCl3 =7.27
例如:
CH3aCH2bCH2cCl
O CH3CH2 C CH2CH3
O CH3CH2 C OCH2CH3
H > H > H H> H 思考!
各向异性效应的影响:
CH2 = 4.5-5.9 H = 7.2
H0:外加磁场强度
△E = hH有效/2 H有效=H0-H感应
△E = hH有效/2 H有效=H0-H感应
处于不同化学环境中的质子外 层电子分布情况不同
产生的感应磁场也不同
2.3 1H-NMR(核磁共振氢谱)
信号的位置:化学位移 信号的裂分:偶合常数
信号的强度:积分曲线
2.3.1 信号的位置:化学位移
HOD in 13C Chemical
Shift
JHD solvent
Shift
JCD B.P. M.P.
(Hz)
(Hz) (oC) (oC)
(multiplicity)
(approx.) (multiplicity)
11.65 1 -Acetic Acid-d4
2.04 5 2.2
178.99 1 11.5
H被裂分为: (2+1)(3+1)重峰
注:s: 单重峰 d: 二重峰 t: 叁重峰 q: 四重峰 m: 多重峰
Jab = Jba
2.3.3 信号的强度:积分曲线
简单谱图分析:
提示1:测试NMR谱图时采用什么溶剂?
氘代试剂 D: I=0 注意未完全氘代的溶剂峰
Solvent
1H Chemical
1H,13C,31P, 15N, 19F
12C,
14N,18F
I=1/2 I=0
1H-NMR 13C-NMR 31P-NMR 15N-NMR 19F-NMR
问:跃迁(“核磁共振”)时所需要吸收的能量∆E为多少?
△E = hH0/2
核磁共振时
:磁旋比(为各种核的特征常数) h:plank常数
△E = hH0/2 = h
2.4 13C-NMR(核磁共振碳谱)
1、信息
()、J( 一般 )、积分曲线( )
2、化学位移 H 0-10 ppm ± 5 ppm C 0-250 ppm ± 100 ppm
3、 13C 同位素丰度较小
13C-NMR vs 1H-NMR
常见碳原子的化学位移
10 C 20 C
0-30 ppm (CH2)n n=4-7 25-45 ppm 苯环
200~400 nm
μ~15μ
400~800 nm
short
wavelength
NMR 1n~5n
long
第一部分 核磁共振谱(NMR) Nuclear Magnetic Resonance
2.2 核磁共振的基本原理 2.3 1H-NMR(核磁共振氢谱) 2.4 13C-NMR(核磁共振碳谱)
far-infrared infrared ultraviolet & visible microwave
各种光谱分析方法
X ray
Ultraviolet Visual Infrared
Micro Radio wave wave
RFID
Electron Spectroscopy Ultraviolet Visual Infrared
22-27 ppm 128.5 ppm
30 C 30-60 ppm -CHO
175-205 ppm
40 C 35-70 ppm R-CO-R’
200-220 ppm
=C
~ 120 ppm -C=C-CO-R
C
~ 70 ppm Ar-CO-R
180-210 ppm
裂分:
因每个碳原子周围有许多氢原子,裂分关系复杂; 同时C-H偶合常数大,易造成谱峰的交叉; 因此13C-NMR谱通常采用全去偶方式(即消除核之间的 相互偶合)。
原则2:不等价的质子化学位移不同
影响化学位移的因素: 原子核外电子云的分布:电负性 原子核所受的额外磁场:各向异性效应
电负性的影响:
△E = hH有效/2 H有效=H0-H感应
邻近基团电负性 质子上电子云密度 H感应 H有效
2.5
C-CH3
=0.77-1.88
CH3Cl =3.05
3.0
N-CH3
(multiplicity)
(approx.) (multiplicity)
Deuterium 4.80 1 -- 4.8
Oxide (DSS)
--
-- -- 101.4 3.8
8.03 1 -N,N-Dimethyl-
2.92 5 1.9 formamide
2.75 5 1.9
163.15 3 29.4 3.5 34.89 7 21.0 153 -61
信号的强度:
极性键出峰较强 C=O,O-H,C-H 等峰较强
C-C,C=C,C≡C 等峰较弱
极性变化大的振动方式,出峰较强
伸缩振动峰较强,弯曲振动峰较弱
峰强的表示方法
vs-很强 s-强 m-中 w-弱 v-可变
定量分析
A=cl
信号的位置:
简谐振动
+x -x
Hooke 定律
m
1
2
k
m1m2
m1 m2
HH
H
HCC
H
HH
外磁场方向
121
H被两个等价的H 裂分为叁重峰, 叁重峰的峰强比 为1:2:1
13 31
H被三个等价的H裂 分为四重峰,四重峰 的峰强比为1:3:3:1
如果一组化学等价的质子被两组数目分别为n和n’的等 价质子裂分时,那么其吸收峰数目为(n+1)(n’+1),
H2 BrH2C C CH3
相对于一个
基准物的相 低
对值
场
样品 - 标准 仪器
单位():ppm
高 场
零点:TMS
CH3
CH3 Si CH3
CH3
原则1:等价的质子化学位移相同
