非吸收性外科缝线产品技术要求派尔特0
非吸收外科缝线(带针不带针)产品技术要求瑞朗
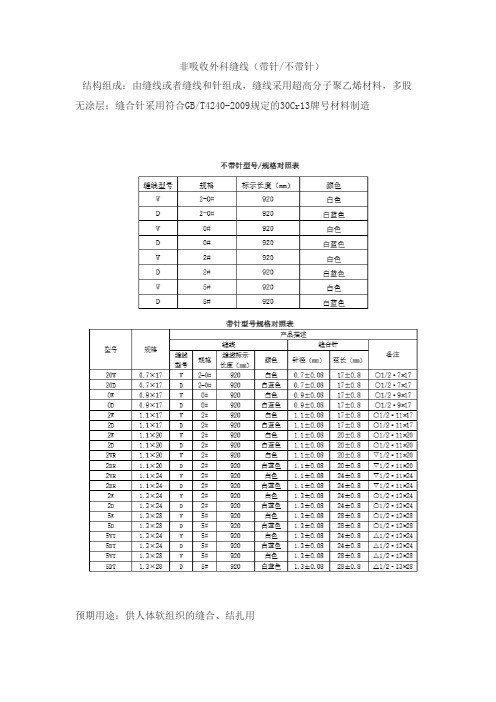
非吸收外科缝线(带针/不带针)结构组成:由缝线或者缝线和针组成,缝线采用超高分子聚乙烯材料,多股无涂层;缝合针采用符合GB/T4240-2009规定的30Cr13牌号材料制造预期用途:供人体软组织的缝合、结扎用2.1 缝线2.1.1 外观缝线表面应光滑,色泽一致,条干均匀,无污渍,无结头;2.1.2抗张强度应符合YY0167-2005表3中Ι类缝线对应的抗张强度要求;2.1.3线径缝线的线径应符YY0167-2005表2中相应型号缝线的规定;2.1.4长度缝线长度为920mm,尺寸误差应为±10mm;2.1.5褪色染色缝线的褪色试验应合格。
2.1.6缝线材质缝线红外光谱的主要吸收峰应与标准对照谱图(超高分子量聚乙烯)的特征吸收峰相吻合。
2.2 缝合针2.2.1外观2.2.1.1针体:缝合针表面应光洁、色泽均匀,针尖无弯钩,针孔和针槽应光洁居中,不得有毛刺或明显歪斜现象。
缝合针与缝合线衔接后,针尾应光洁,不得有毛刺;2.2.1.2三角刃口:三角刃口不得有卷刃、白刃或锯齿状;2.2.1.3表面粗糙度:表面粗糙度Ra之数值应不大于0.8µm。
2.2.2物理性能;2.2.2.1硬度:缝合针硬度不低于490HV0.22.2.2.2缝合针针体应有良好的弹性;2.2.2.3缝合针针体应有良好的韧性;2.2.2.4针尖强度:缝合针针尖应无虚尖,针尖经规定的加力速度加载顶压后不得有弯钩。
2.2.3使用性能2.2.3.1刺穿力:应符合YY/T0043-2016中4.3.1表2的规定;2.2.3.2切割力:应符合YY/T0043-2016中4.3.2表3的规定;2.2.3.3针线连接强度:应符合YY0167-2005中4.4表4的规定。
2.2.4材料针的材料符合GB/T4240-2009规定的30Cr13牌号材料。
2.2.5耐腐蚀性能针应有良好的耐腐蚀性能,其表面状态应不低于YY/T0149-2006中b级的要求。
非吸收外科缝线(带针 不带针)产品技术要求北京瑞朗泰科
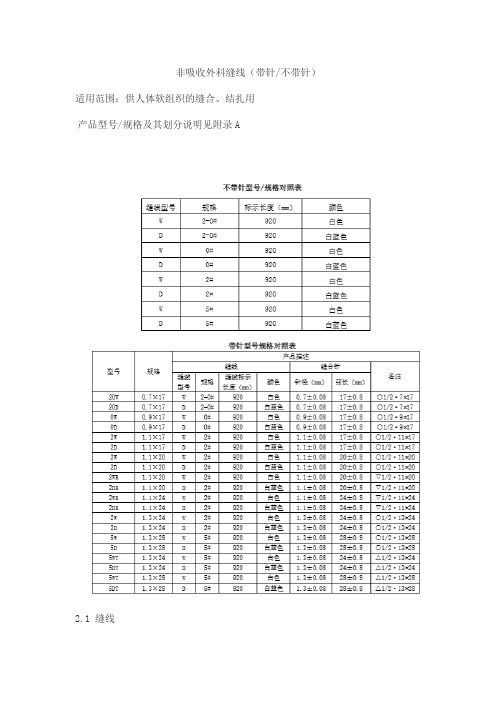
非吸收外科缝线(带针/不带针)适用范围:供人体软组织的缝合、结扎用产品型号/规格及其划分说明见附录A2.1 缝线2.1.1 外观缝线表面应光滑,色泽一致,条干均匀,无污渍,无结头;2.1.2抗张强度应符合YY0167-2005表3中Ι类缝线对应的抗张强度要求;2.1.3线径缝线的线径应符YY0167-2005表2中相应型号缝线的规定;2.1.4长度缝线长度为920mm,尺寸误差应为±10mm;2.1.5褪色染色缝线的褪色试验应合格。
2.1.6缝线材质缝线红外光谱的主要吸收峰应与标准对照谱图(超高分子量聚乙烯)的特征吸收峰相吻合。
2.2 缝合针2.2.1外观2.2.1.1针体:缝合针表面应光洁、色泽均匀,针尖无弯钩,针孔和针槽应光洁居中,不得有毛刺或明显歪斜现象。
缝合针与缝合线衔接后,针尾应光洁,不得有毛刺;2.2.1.2三角刃口:三角刃口不得有卷刃、白刃或锯齿状;2.2.1.3表面粗糙度:表面粗糙度Ra之数值应不大于0.8µm。
2.2.2物理性能2.2.2.1硬度:缝合针硬度不低于490HV;0.22.2.2.2缝合针针体应有良好的弹性;2.2.2.3缝合针针体应有良好的韧性;2.2.2.4针尖强度:缝合针针尖应无虚尖,针尖经规定的加力速度加载顶压后不得有弯钩。
2.2.3使用性能2.2.3.1刺穿力:应符合YY/T0043-2016中4.3.1表2的规定;2.2.3.2切割力:应符合YY/T0043-2016中4.3.2表3的规定;2.2.3.3针线连接强度:应符合YY0167-2005中4.4表4的规定。
2.2.4材料针的材料符合GB/T4240-2009规定的30Cr13牌号材料。
2.2.5耐腐蚀性能针应有良好的耐腐蚀性能,其表面状态应不低于YY/T0149-2006中b级的要求。
2.2.6尺寸针的尺寸应符合附录A的要求。
2.3环氧乙烷残留量采用环氧乙烷灭菌的产品,环氧乙烷残留量应≤10μg/g。
一次性使用吻合器组合包产品技术要求派尔特0

一次性使用吻合器组合包适用范围:适用于胃、肺等组织和消化道手术吻合用。
1.1产品型号规格WBF29VJ30 WBF29VJ45 WBF29VJ60 WBF32VJ30 WBF32VJ45 WBF32VJ60 WBF33VJ30 WBF33VJ45 WBF33VJ60 WBF34VJ30 WBF34VJ45 WBF34VJ60 WBF21VK30 WBF21VK45 WBF21VK60 WBF25VK30 WBF25VK45 WBF25VK60 WBF29VK30 WBF29VK45 WBF29VK60 WBF32VK30 WBF32VK45 WBF32VK60 WBF33VK30 WBF33VK45 WBF33VK60 WBF34VK30 WBF34VK45 WBF34VK60 WCF21VI30 WCF21VI45 WCF21VI60 WCF24VI30 WCF24VI45 WCF24VI60 WCF25VI30 WCF25VI45 WCF25VI60 WCF26VI30 WCF26VI45 WCF26VI60 WCF28VI30 WCF28VI45 WCF28VI60 WCF29VI30 WCF29VI45 WCF29VI60 WCF32VI30 WCF32VI45 WCF32VI60 WCF34VI30 WCF34VI45 WCF34VI60 WCF21VJ30 WCF21VJ45 WCF21VJ60 WCF24VJ30 WCF24VJ45 WCF24VJ60 WCF25VJ30 WCF25VJ45 WCF25VJ60 WCF26VJ30 WCF26VJ45 WCF26VJ60 WCF28VJ30 WCF28VJ45 WCF28VJ60 WCF29VJ30 WCF29VJ45 WCF29VJ60 WCF32VJ30 WCF32VJ45 WCF32VJ60 WCF34VJ30 WCF34VJ45 WCF34VJ60 WCF21VK30 WCF21VK45 WCF21VK60 WCF24VK30 WCF24VK45 WCF24VK60WCF26VK30 WCF26VK45 WCF26VK60 WCF28VK30 WCF28VK45 WCF28VK60 WCF29VK30 WCF29VK45 WCF29VK60 WCF32VK30 WCF32VK45 WCF32VK60 WCF34VK30 WCF34VK45 WCF34VK60 WDF21VI30 WDF21VI45 WDF21VI60 WDF24VI30 WDF24VI45 WDF24VI60 WDF26VI30 WDF26VI45 WDF26VI60 WDF28VI30 WDF28VI45 WDF28VI60 WDF29VI30 WDF29VI45 WDF29VI60 WDF32VI30 WDF32VI45 WDF32VI60 WDF34VI30 WDF34VI45 WDF34VI60 WDF21VJ30 WDF21VJ45 WDF21VJ60 WDF24VJ30 WDF24VJ45 WDF24VJ60 WDF26VJ30 WDF26VJ45 WDF26VJ60 WDF28VJ30 WDF28VJ45 WDF28VJ60 WDF29VJ30 WDF29VJ45 WDF29VJ60 WDF32VJ30 WDF32VJ45 WDF32VJ60 WDF34VJ30 WDF34VJ45 WDF34VJ60 WDF21VK30 WDF21VK45 WDF21VK60 WDF24VK30 WDF24VK45 WDF24VK60 WDF26VK30 WDF26VK45 WDF26VK60 WDF28VK30 WDF28VK45 WDF28VK60 WDF29VK30 WDF29VK45 WDF29VK60 WDF32VK30 WDF32VK45 WDF32VK60 WDF34VK30 WDF34VK45 WDF34VK60 WEF21VI30 WEF21VI45 WEF21VI60 WEF24VI30 WEF24VI45 WEF24VI60WEF28VI30 WEF28VI45 WEF28VI60 WEF29VI30 WEF29VI45 WEF29VI60 WEF32VI30 WEF32VI45 WEF32VI60 WEF34VI30 WEF34VI45 WEF34VI60 WEF21VJ30 WEF21VJ45 WEF21VJ60 WEF24VJ30 WEF24VJ45 WEF24VJ60 WEF26VJ30 WEF26VJ45 WEF26VJ60 WEF28VJ30 WEF28VJ45 WEF28VJ60 WEF29VJ30 WEF29VJ45 WEF29VJ60 WEF32VJ30 WEF32VJ45 WEF32VJ60 WEF34VJ30 WEF34VJ45 WEF34VJ60 WEF21VK30 WEF21VK45 WEF21VK60 WEF24VK30 WEF24VK45 WEF24VK60 WEF26VK30 WEF26VK45 WEF26VK60 WEF28VK30 WEF28VK45 WEF28VK60 WEF29VK30 WEF29VK45 WEF29VK60 WEF32VK30 WEF32VK45 WEF32VK60 WEF34VK30 WEF34VK45 WEF34VK60 WFF21VI30 WFF21VI45 WFF21VI60 WFF24VI30 WFF24VI45 WFF24VI60 WFF26VI30 WFF26VI45 WFF26VI60 WFF28VI30 WFF28VI45 WFF28VI60 WFF29VI30 WFF29VI45 WFF29VI60 WFF32VI30 WFF32VI45 WFF32VI60 WFF34VI30 WFF34VI45 WFF34VI60 WFF21VJ30 WFF21VJ45 WFF21VJ60 WFF24VJ30 WFF24VJ45 WFF24VJ60 WFF26VJ30 WFF26VJ45 WFF26VJ601.2型号划分说明1.2.1一次性使用吻合器组合包产品是将已取得注册证书的一次性使用管型吻合器(FCSLF 系列)、一次性使用管型吻合器(FCSMF 系列)、一次性使用管型吻合器(FCSSWF 系列)、一次性使用管型吻合器(FCSSMF 系列)产品及一次性使用腔镜下切割吻合器系列产品组合而成。
临床手术缝线选择标准及不可吸收缝线和可吸收缝线分类、用途、优缺点及用途

临床手术缝线选择标准及不可吸收缝线和可吸收缝线分类、用途、优缺点及用途手术缝线选择标准手术缝线是在外科手术中,是外伤处置当中,用于结扎止血、缝合止血以及组织缝合的特殊线。
用于组织缝合可以保证伤口闭合,支持其愈合,减少感染几率。
手术缝线选择应该尽量选择细而拉力大,对组织反应小的无菌单股可吸收线。
缝线常用 USP标准与 EP标准,对于USP标准:用 N/0 表示,N 值越大,表示缝线越细,但需注意,其不表示缝线具体直径的大小;对于 EP 标准:单位为 0.1 mm,数字越大,表示缝线直径越粗。
市面上手术缝线多采用USP标准,USP标准又和中国传统缝线规格有差异。
不可吸收缝线1. 丝质手术缝线:由蚕茧的连续性蛋白质纤维制成,为多股编制而成,分线团和线束两种包装。
优点:价格低廉,容易消毒,使用方便,打结结实;缺点:刺激组织产生炎性反应。
用途:主要用于缝合皮肤、皮下或体内结蹄组织、肌肉层等2、尼龙手术缝线:及聚酰胺纤维,简称 PA 线或锦纶线,分单丝尼龙线和多丝尼龙线,又分带针和不带针两种。
优点:张力强度高,植入体内后很少有组织反应,具有极佳弹性;缺点:在人体每年以15-20% 速率水解。
3. 聚丙烯缝线:单股合成缝线,是心血管外科首选缝线。
优点:被植入组织后保持永久的张力强度,手感顺滑,易于打结,很少有组织阻力感,可提供牢固的线结保障。
用途:心血管外科如血管吻合、神经吻合、冠状动脉远端吻合、换瓣手术等操作,可用于整形外科如皮肤缝合及皮内缝合等。
可吸收缝线1.天然吸收性缝线-肠线:以羊肠粘膜下层或牛肠浆膜为原料。
含 90% 胶原,经铬盐溶液处理后成为铬制肠线,可对抗体内各种酶的消化作用,可将吸收时间延长至 90 天以上。
2.聚乙醇酸缝线:为羟基乙酸的聚合物,属于多股编制缝线。
优点:特殊的涂层,柔软光滑,容易打结,无毒性、无胶原性、无抗原性、无致癌性,组织反应低。
2.聚乳酸羟基乙酸缝线:为多股编制,其又可分为快吸收类和保护类。
非吸收性外科缝线产品技术要求派尔特0

非吸收性外科缝线产品技术要求派尔特01.原材料要求:派尔特0非吸收性外科缝线所采用的原材料应符合医疗器械的相关标准和规定。
一般来说,派尔特0的原材料主要由聚丙烯或聚酯纤维制成。
这些原材料应具有一定的机械强度和耐久性,能够在手术过程中经受拉力,并保持一定的强度。
2.外观要求:派尔特0非吸收性外科缝线产品的外观应整齐、光滑、无明显的损伤、开裂、污染等现象。
其表面应无明显毛刺、纤维脱落等不完整现象。
此外,派尔特0产品的颜色应为统一的白色或深蓝色。
3.尺寸要求:派尔特0非吸收性外科缝线的尺寸应符合国际标准或行业标准,以确保其在手术中的适用性。
一般来说,派尔特0产品的线径应为0.2-4.0mm之间,长度应大于75cm。
4.强度要求:派尔特0非吸收性外科缝线在手术中经受拉力,需要具有一定的强度。
产品需要具有足够的强度,以确保在手术过程中不会出现线断裂等问题。
一般来说,派尔特0产品的抗拉强度应在45-55N之间。
5.生物相容性要求:派尔特0非吸收性外科缝线的使用不应对人体组织产生刺激或不良反应。
产品应符合相关的生物相容性标准和规定,经过生物相容性测试,确保其对人体组织的刺激性、过敏性等方面不会产生不良影响。
6.包装要求:派尔特0非吸收性外科缝线的包装应符合相关标准和规定,保证产品在运输过程中不受损坏。
包装应具有防潮、防污染等功能,确保产品质量和卫生安全。
7.质量控制要求:派尔特0非吸收性外科缝线产品的生产过程需要进行严格的质量控制,确保产品的一致性、可靠性和安全性。
生产厂商需要建立完善的质量管理体系,并持续进行相关的质量控制活动,监测产品的质量和性能。
总结起来,派尔特0非吸收性外科缝线产品的技术要求主要包括原材料要求、外观要求、尺寸要求、强度要求、生物相容性要求、包装要求和质量控制要求等。
这些要求的符合度,直接关系到产品的质量和性能,对于外科手术的成功进行至关重要。
因此,生产厂商应严格按照这些技术要求进行生产和监控,确保产品的质量和安全性。
非吸收性外科缝线线径测量不确定度的评定

{ +3 ( + x× )
() 2
5 不确 定 度分量 的评 定
测量的重复性系数 的不确定度 H ( ) 为:
( ) = = -0 0 0 .12
试验在 标准 规定 的条 件下 进 行 , 考 虑 温 度效 应 引 不
起的不确定度分量 , 非吸收性外科缝线 的线径测量结果 的不确定度主要来源于以下两个方面:
d n-) ( ̄ n d( ) r m
025 .2 0.3 0.3 0 2 l 0 2 8 . 3 0 2 6 0 2 5 23 2 3 . 4 .3 O 2 7 .3 .3 O.3 0.3 26 25
025 .2 0.3 0.3 0 2 l 0 2 8 0 2 7 O 2 6 23 2 4 . 4 .3 .3 .3 O.3 0.3 0.3 25 25 26
12 测试 原 理 : 量 承 载 负 荷 的 压 脚 与 基 准 面 之 间距 . 测
离。 13 环境 条件 : 度 (0— 5 o . 温 1 3 )C。
() 2 线径测 试仪 校准所 引入 的不 确定 度分 量 。 51 各分量 的标 准不确 定度 的评定 . () 1测量重 复性 引入 的不确定 分 量 影 响检测 结果 重复性 的因素主要 有测 量仪 器 的波动 性、 人员 操作 、 品不均匀 等 因素 。统计分 析在 重复 性测 样 量条件下 一 系列 测 量结 果 , 即可 得 到各 种 随 机 因 素合 并
黄葆 华等: 辞吸收挂"科缝线线径灏量不确 定度 的评定
非 吸 收 性 外 科 缝 线 线 径 测 量 不 确 定 度 的 评 定
E au t n o eMes rme tU cr it f ,teNo v lai ft a ue n n et ny o h n—a sra l o h a bob be
非吸收性外科缝线

非吸收性外科缝线1 范围本标准规定了非吸收性外科缝线的分类、要求、试验方法、型式检验、标签、说明书、包装、运输、贮存和有效期。
本标准适用于人体组织缝合、结扎的非吸收性外科缝线(以下简称缝线)。
本标准不适用于特殊设计的非吸收性外科缝线。
2 规范性引用文件下列文件对于本文件的应用是必不可少的。
凡是注日期的引用文件,仅注日期的版本适用于本文件。
凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。
GB/T 191 包装储运图示标志GB 4234 外科植入物用不锈钢GB/T 8170数值修约规则与极限数值的表示和判定GB/T 9737-2008化学试剂易碳化物质测定通则GB/T 9969工业产品使用说明书总则GB/T 14233.1-2008 医用输液、输血、注射器具检验方法第1部分:化学分析方法GB/T 16886(所有部分)医疗器械生物学评价YY/T 0466.1 医疗器械用于医疗器械标签、标记和提供信息的符号第1部分:通用要求YY/T 0816-2010 外科植入物缝合及其他外科用柔性金属丝中华人民共和国药典(2015年版)3 缝线的分类3.1 形式缝线有带缝合针与不带缝合针两种形式,均以无菌形式提供。
3.2 结构缝线的结构有单股和多股(捻股和编织)之分。
3.3 材料缝线的制造材料涉及天然纤维、合成纤维和金属材料(符合YY/T 0816-2010的第3章或GB 4234)。
注:天然纤维,如蚕丝。
合成纤维,如聚对苯二甲酸乙二酯、聚亚乙烯基二氟化物、聚酰胺6、聚酰胺6/6及聚丙烯。
金属材料,如不锈钢丝。
3.4 类别1缝线按制造材料、结构、染色和涂层影响分为三类(见表1),其中:A类缝线,由蚕丝或合成纤维制成,涂层不影响线径;B类缝线,由天然纤维或合成纤维制成,涂层影响线径;C类缝线,由金属制成。
表1 缝线的分类4 要求4.1 外观4.1.1 缝线应光滑,条干均匀,无污渍,无结头。
多股缝线表面应有涂层。
1.4.2不可吸收缝线的类别与使用

《宠物外产科病》不可吸收缝线的类别与使用掌握不可吸收缝线的种类与特点,掌握各种不可吸收缝线的使用范围.教学目标01教学重点02学习各种不可吸收缝线的来源,应用的优缺点。
教学难点03外科手术中如何灵活选择不同类型的缝线。
1、丝线4、不锈钢丝2、尼龙线3、聚丙烯线不可吸收缝线主要类别一、丝线•是用蚕茧的蛋白质纤维制成。
传统规格有:0、1、4、7、10号。
丝线为多股编制而成,分线团和线束两种包装。
•丝线可刺激组织产生炎症反应,主要用于缝合皮肤、皮下或体内结缔组织、肌肉层等。
由于其降解速度慢所以被归入不可吸收线,但理论上讲其在动物体内1年左右张力即会完全消失。
1.脱胶-除去蚕丝中易引起异物反应的蛋白质成分,2.编织-去胶后的纤维被精心编成丝线,使其抗张力强度增大;3.涂层-每股编织线的表面均封一层蜜蜡,使操作更顺利;4.包装-所有慕丝的丝线都采用实用的方法包装,使用方便。
5.消毒-所有慕丝线经辐射严格消毒。
美国强生公司生产的慕丝(musilk)带针手术丝线,采用下列加工程序制成:一、丝线•丝线在临床中的使用广泛。
•优点:廉价、易消毒、张力大、便于缝合、打结。
•缺点:缝合空隙器官时,易产生溃疡。
缝合膀胱、胆囊时,易形成结石。
一、丝线丝线线束丝线线团美国强生公司的慕丝线二、尼龙线•即聚酰胺纤维,简称PA线或锦纶线,无色,或染成黑色、深蓝色、紫色等。
分单丝尼龙线和多丝尼龙线,又分带针和不带针两种。
•尼龙线在动物体内每年以15%-20%的速率分解。
单丝尼龙缝线表面均匀平滑,张力强度高,植入体内后很少有组织反应,具有极佳弹性。
眼科或其他显微手术大多选用带针单丝尼龙线,称为无损伤缝线。
尼龙线三、聚丙烯缝线如美国强生公司生产的普里林(prolene)单股合成缝线,是心血管外科公认的首选缝线。
被植入组织后保持永久的张力强度(维持2年之久),且手感顺滑,易于打结,很少有组织阻力感,可提供牢固的线结保障。
聚丙烯线四、不锈钢丝•最常用的金属材料为不锈钢丝。
2 非吸收性外科缝线注册技术审查指导原则(征求意见稿)

非吸收性外科缝线注册技术审查指导原则(征求意见稿)本指导原则旨在为申请人进行非吸收性外科缝线的注册申报提供技术指导,帮助审评人员理解和掌握该类产品原理/机理、结构、性能、预期用途等内容,把握技术审评工作基本要求和尺度,对产品安全性、有效性做出系统评价。
本指导原则所确定的核心内容是在目前的科技认识水平和现有产品技术基础上形成的。
因此,审评人员应注意其适宜性,密切关注适用标准及相关技术的最新进展,考虑产品的更新和变化。
本指导原则不作为法规强制执行,不包括行政审批要求。
但是,审评人员需密切关注相关法规的变化,以确认申报产品是否符合法规要求。
一、适用范围本指导原则适用于第二类非吸收性外科缝线。
根据《总局关于发布医疗器械分类目录的公告(2017年第104号)》规定,非吸收性外科缝线管理类别为Ⅱ类,子目录为02无源手术器械,一级产品类别为13手术器械-吻(缝)合器械及材料,二级产品类别为07不可吸收缝合线。
本指导原则不适用于可吸收缝线、预期用于骨结合及其他有特殊要求的缝线(如主要用于肌腱和韧带缝合的超高分子量聚乙烯缝线、免打结式缝线、具有抗菌作用缝线等)。
二、注册申报资料要求(一)产品名称的要求产品名称应以产品的预期用途和适用范围为依据,一般应为不可吸收缝合线或非吸收性外科缝线。
产品名称中可体现缝线的材料(例如非吸收性聚丙烯外科缝线)。
(二)产品的结构组成非吸收性外科缝线通常是由天然材料或聚合材料制成的表面可有涂层的不可降解吸收的缝合线。
分为带针和不带针两种。
产品结构分为多股和单股。
根据产品材料、结构和有无涂层可以分为以下三类:表1 缝线的分类非吸收性外科缝线常见材质有蚕丝、聚酰胺、聚酯、聚丙烯、不锈钢等。
(三)产品工作原理非吸收性外科缝线在外科手术当中,或者是外伤处置当中,用于软组织、器官和/或皮肤的缝合。
(四)注册单元划分的原则和实例按照《医疗器械注册管理办法》(国家食品药品监督管理总局令第4号)第七十四条要求,“医疗器械注册或者备案单元原则上以产品技术原理、结构组成、性能指标和适用范围为划分依据”。
非吸收性外科缝线产品技术要求taikeman
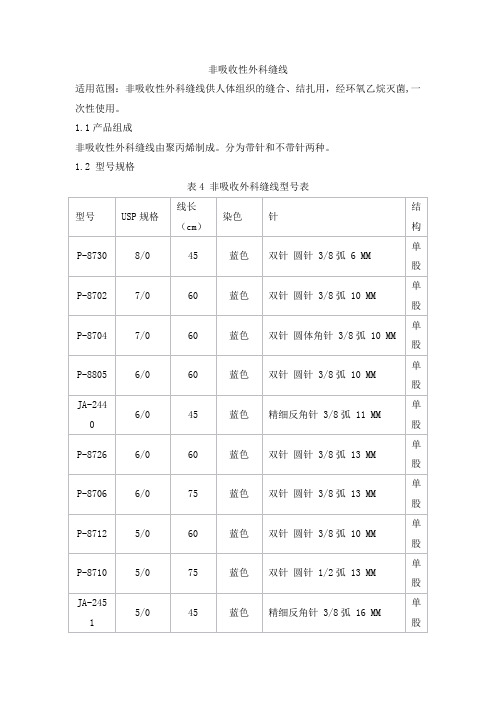
非吸收性外科缝线适用范围:非吸收性外科缝线供人体组织的缝合、结扎用,经环氧乙烷灭菌,一次性使用。
1.1产品组成非吸收性外科缝线由聚丙烯制成。
分为带针和不带针两种。
1.2 型号规格表4 非吸收外科缝线型号表1.3型号规格划分及说明:P ——表示材质为聚丙烯JA——表示反角针JC——表示圆针8——表示可用于心脏和血管外科1/2——表示用于缝皮手术1.4 缝合针的材质缝线分为带针和不带针两种。
带针缝线,按照YY0043-2005中3.2 材料的要求:缝合针以YB/T5219-1993中规定的材料制造。
YB/T5219-1993中6.1.1规定钢丝应选用GB1220-2007中规定的3Cr13和4Cr13牌号(等同于新牌号:30Cr13和40Cr13)。
钢的化学成分见下表5。
表5 钢的化学成分300型400型2.1外观要求:2.1.1缝线表面应光滑,色泽均匀一致,条干均匀,无污渍,无结头。
2.1.2缝合针与缝线衔接后针尾应光滑,不得有毛刺。
2.1.3针体中部表面应色泽均匀,表面粗糙度Ra数值应不大于0.8μm。
2.1.4 缝合针表面应光亮、色泽均匀,针孔和针槽应光滑居中,不得有毛刺或明显歪斜现象。
2.2线径:规格和线径见表1。
2.3 抗张强度:见表1。
表1 线径与抗张强度2.4线长:每根线的长度不得短于标示长度的95%。
线长见表4。
2.5缝合针与缝线连接应牢固,针线连接强度见表2。
表2 针线连接强度2.6如缝丝线染色,其萃取后的试验溶液颜色不应深于相应标准比色液的颜色。
2.7缝合针的使用性能和物理性能2.7.1缝合针针尖应无虚尖,针尖经规定的加力速度加载顶压后不得有弯钩。
2.7.2缝合针针尖应尖锐,其刺穿力应符合表3的规定。
表3 刺穿力2.7.3带刃口的缝合针刃口应锋利,不应有卷刃、白口及锯齿状。
2.7.4缝合针针体应经热处理,其硬度不低于490HV0.2(针体直径或宽度小于0.2mm不检验其硬度)。
2.7.5缝合针针体应有良好的弹性。
非吸收性外科缝线产品技术要求tianxingmaidi

非吸收性外科缝线适用范围:供人体组织的缝合、结扎用。
1. 产品型号规格及其划分说明1.1型号规格型号分为两种:UHS和UHT,规格如下:UHS规格:6-0、5-0、4-0、3-0、2-0/T、2-0、0、1、2、3、4、5、6、7、8、9、10;长度为:100mm-1000mm(每间隔50mm为一个规格)。
UHT规格:1mm、1.5mm、2mm、2.5mm、3mm、3.5mm、4mm、4.5mm、5mm;长度为:100mm-1000mm(每间隔50mm为一个规格)。
1.2产品划分说明根据缝线的结构,分为两种型号,分别为UHS和UHT,其中UH表示产品名称,S 表示圆型, T表示扁型。
根据UHS缝线的线径或UHT缝线宽度及厚度,缝线划分为不同的规格。
2.性能指标2.1 红外光谱缝线由超高分子量聚乙烯制成,其红外光谱应在2924cm-1、2853cm-1、1471cm-1、719cm-1附近有关键振动吸收峰。
2.2 外观缝线表面为白色或蓝白色,表面光滑,条干均匀,无污渍,无结头,表面无涂层。
2.3 规格尺寸2.3.1 长度缝线的长度应不小于标识长度的95%,单根缝线的长度应不大于3.5m。
2.3.2 线径UHS缝线的线径应符合YY0167-2005中3.2的规定。
具体见表1表1 UHS缝线的规格与线径范围UHT缝线的规格具体见表2表2 UHT缝线的规格表3 UHS缝线的抗张强度2.4抗张强度2.4.1 UHS缝线抗张强度应符合表3中的要求。
2.4.2 UHT缝线抗张强度见表4。
表4 UHT缝线抗张强度2.5 褪色染色缝线的褪色实验应合格。
2.6无菌该产品经环氧乙烷灭菌后,应无菌。
2.7 环氧乙烷残留量该产品的环氧乙烷残留量应不大于250μg/g。
非吸收性外科缝线产品技术要求yunyi

非吸收性外科缝线适用范围:用于人体组织的缝合、结扎。
1.1 产品型号/规格产品型号、规格见附录A。
1.3产品组成非吸收性外科缝线由超高分子量聚乙烯单丝或超高分子量聚乙烯单丝和聚酯丝线编织而成,分为带针和不带针两种。
缝合针采用符合标准GB/T4240-2009规定的12Cr18Ni9材料制成。
由超高分子量聚乙烯单丝和聚酯丝线编织而成的缝线表面涂覆有硅涂层。
1.4产品组件示意图见表1表1产品组件示意图2.1 外观缝线表面应光滑,条干均匀,无污渍,无结头。
由超高分子量聚乙烯和聚酯编织而成的缝线表面有涂层。
若缝线带针,针线连接处应光滑、无毛刺。
2.2 线径缝线的线径应符合表2的规定。
表2 线径2.3 抗张强度缝线的抗张强度应符合表3的规定。
表3 抗张强度2.4 针线连接强度若缝线带针,其针线连接强度见表4。
表4 针线连接强度2.5 长度缝线的长度应不小于标示长度的95%,单根缝线的长度应不大于3.5m。
2.6 缝针2.6.1 使用性能缝合针针尖应尖锐、无弯钩,其刺穿力应符合表5的规定。
表5 刺穿力2.6.2 物理性能2.6.2.1 硬度缝合针经处理,其硬度应不小于520HV。
0.22.6.2.2 弹性缝合针应有良好的弹性。
2.6.2.3 韧性缝合针应有良好的韧性。
2.6.2.4 针尖强度缝合针针尖应无虚尖,针尖经规定的加力速度加载荷顶压后,不得有弯钩。
2.6.3 外观2.6.3.1 针体缝合针表面应光亮,色泽均匀,针孔和针槽应光滑居中,不得有毛刺或明显歪斜现象。
2.6.3.2 表面粗糙度表面粗糙度Ra之数值应不大于0.8μm。
2.7 无菌产品经环氧乙烷灭菌后,应无菌。
2.8 环氧乙烷残留量环氧乙烷残留量应不大于250μg/g。
2.9 热原产品应无热原反应。
2.10 褪色染色缝线的褪色试验应合格。
2.11 耐腐蚀性能缝合针应有良好的耐腐蚀性能,其表面状态应不低于YY/T 0149-2006中5.4b级的规定。
非吸收性外科缝线产品技术要求泰科

非吸收性外科缝线结构组成:非吸收性外科缝线由聚酰胺材质制成,带针,缝线的颜色为黑色,所有缝线均为单股。
预期用途:用于软组织、器官和/或皮肤的缝合和/或结扎。
1. 产品型号/规格及其划分说明1.1 产品组成非吸收性外科缝线由聚酰胺制成,带针。
1.2 型号规格产品型号规格见附录A。
1.3 型号规格划分及说明:类别与结构:Ⅰ类单股AA ——表示线的颜色为黑色。
XXXX——数字为货号S ——表示长系列线长。
N ——表示短系列线长。
NC ——表示标准系列线长。
Z ——表示钻石针示例:AA-0635N:黑色,货号0635, N:短系列线长。
AA-1174SZ:黑色,货号1174,长系列线长,钻石针。
针的规格:依据YY/T 0043-2016,缝合针的形式、弧形、针孔和规格的标示。
1.4 缝合针的材质按照YY/T 0043-2016中3.4材料的要求,缝合针以GB/T 4240-2009规定中的12Cr18Ni9牌号材料制造。
钢的化学成分见表1。
表1 钢的化学成分2.1外观缝线表面应光滑,色泽均匀一致,条干均匀,无污渍,无结头。
2.2线径缝线规格与线径应符合表2的要求。
2.3 抗张强度缝线的抗张强度应符合表2的要求。
表2 缝线的规格、线径与抗张强度每根缝线的长度应不小于标示长度的95%,单根缝线的长度应不大于3.5m,缝线长度见附录A。
2.5 针线连接强度缝合针与缝线连接应牢固,针线连接强度见表3。
表3 针线连接强度如缝线染色,其萃取后的试验溶液颜色不应深于相应标准比色液的颜色,其中,标准比色液配制选择表5紫红色进行。
2.7缝合针性能2.7.1缝合针针体缝合针表面应光洁、色泽均匀,针尖无弯钩,针孔和针槽应光洁居中,不得有毛刺或明显歪斜现象。
缝合针与缝合线衔接后,针尾应光洁,不得有毛刺。
2.7.2 三角刃口三角针刃口不得有卷刃、白刃及锯齿状。
2.7.3 表面粗糙度表面粗糙度Ra之数值应不大于0.8μm。
2.7.4缝合针硬度应符合表4的规定。
非吸收性外科缝线产品技术要求泰科曼远东国际

非吸收性外科缝线适用范围:用于软组织、器官和/或皮肤的缝合和/或结扎。
1. 产品型号/规格及其划分说明1.1 产品组成非吸收性外科缝线由聚酰胺制成,带针。
1.2 型号规格产品型号规格见附录A。
1.3 型号规格划分及说明:类别与结构:Ⅰ类单股AA ——表示线的颜色为黑色。
XXXX——数字为货号S ——表示长系列线长。
N ——表示短系列线长。
NC ——表示标准系列线长。
Z ——表示钻石针示例:AA-0635N:黑色,货号0635, N:短系列线长。
AA-1174SZ:黑色,货号1174,长系列线长,钻石针。
针的规格:依据YY/T 0043-2016,缝合针的形式、弧形、针孔和规格的标示。
1.4 缝合针的材质按照YY/T 0043-2016中3.4材料的要求,缝合针以GB/T 4240-2009规定中的12Cr18Ni9牌号材料制造。
钢的化学成分见表1。
表1 钢的化学成分2. 性能指标2.1外观缝线表面应光滑,色泽均匀一致,条干均匀,无污渍,无结头。
2.2线径缝线规格与线径应符合表2的要求。
2.3 抗张强度缝线的抗张强度应符合表2的要求。
表2 缝线的规格、线径与抗张强度2.4缝线长度每根缝线的长度应不小于标示长度的95%,单根缝线的长度应不大于3.5m,缝线长度见附录A。
2.5 针线连接强度缝合针与缝线连接应牢固,针线连接强度见表3。
表3 针线连接强度2.6 褪色如缝线染色,其萃取后的试验溶液颜色不应深于相应标准比色液的颜色,其中,标准比色液配制选择表5紫红色进行。
2.7缝合针性能2.7.1缝合针针体缝合针表面应光洁、色泽均匀,针尖无弯钩,针孔和针槽应光洁居中,不得有毛刺或明显歪斜现象。
缝合针与缝合线衔接后,针尾应光洁,不得有毛刺。
2.7.2 三角刃口三角针刃口不得有卷刃、白刃及锯齿状。
2.7.3 表面粗糙度表面粗糙度Ra之数值应不大于0.8μm。
2.7.4缝合针硬度应符合表4的规定。
表4 缝合针硬度2.7.5弹性缝合针针体应有良好的弹性。
非吸收性外科缝线技术要求
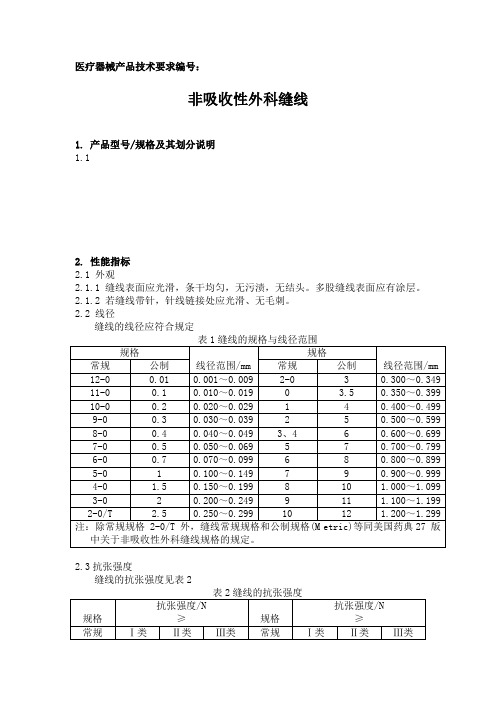
医疗器械产品技术要求编号:非吸收性外科缝线1.产品型号/规格及其划分说明1.12. 性能指标2.1 外观2.1.1 缝线表面应光滑,条干均匀,无污渍,无结头。
多股缝线表面应有涂层。
2.1.2 若缝线带针,针线链接处应光滑、无毛刺。
2.2 线径缝线的线径应符合规定2.3抗张强度缝线的抗张强度见表2若针线带针,其针线链接强度见表3染色缝线的褪色试验应合格。
2.6 长度缝线的长度应不小于标示长度的95%,单根缝线的长度应不大于3.5m。
2.7 缝针若缝线带针,缝针应符合YY0043 中使用性能、物理性能和外观(除弹机孔嵌线)的要求。
2.8 无菌缝线应无菌。
2.9 环氧乙烷残留量若缝线采用环氧乙烷灭菌时,环氧乙烷灭菌的残留量应不大于250ug/g。
2.10 生物学评价2.10.1 热原缝线应无热原。
2.10.2 血液相容性缝线的血液相容性试验,溶血率不大于5%。
2.10.3 细胞毒性反应不大于 1 级。
2.10.4 遗传毒性基因突变、染色体结构和数量以及对DNA(脱氧核糖核酸)的影响,不应有毒性变化反应。
2.10.5 植入炎性细胞反应程度和纤维囊腔形成程度应符合GB/T 16175-2008中12.9的规定。
2.10.6 致敏应无致敏。
3. 检验方法3.1 外观在正常光照下目测或借助5倍放大镜观察,应符合2.1.1,2.1.2的规定。
3.2 线径3.2.1 试验装置线径测量仪,最小分度值0.002mm,压脚与基准面的平整度在0.005mm之内,且互相平行,压脚直径为10mm~15mm之间,基准面的直径应不小于压脚的直径,压脚加在缝线上的负载在90g~210g之间。
3.2.2 试验程序3.2.2.1 从包装中取出缝线后,不经拉伸,应马上进行线径的测量。
若缝线用液体包装,试验必须在缝线从液体中取出后2min内完成。
3.2.2.2 把缝线的一端固定在线径测量仪上,同时,缝线的另一端应施加一定的张力。
张力的大小根据缝线的规格,取表2中Ⅰ类缝线抗张强度值的二分之一。
2 非吸收性外科缝线注册技术审查指导原则(征求意见稿)

非吸收性外科缝线注册技术审查指导原则(征求意见稿)本指导原则旨在为申请人进行非吸收性外科缝线的注册申报提供技术指导,帮助审评人员理解和掌握该类产品原理/机理、结构、性能、预期用途等内容,把握技术审评工作基本要求和尺度,对产品安全性、有效性做出系统评价。
本指导原则所确定的核心内容是在目前的科技认识水平和现有产品技术基础上形成的。
因此,审评人员应注意其适宜性,密切关注适用标准及相关技术的最新进展,考虑产品的更新和变化。
本指导原则不作为法规强制执行,不包括行政审批要求。
但是,审评人员需密切关注相关法规的变化,以确认申报产品是否符合法规要求。
一、适用范围本指导原则适用于第二类非吸收性外科缝线。
根据《总局关于发布医疗器械分类目录的公告(2017年第104号)》规定,非吸收性外科缝线管理类别为Ⅱ类,子目录为02无源手术器械,一级产品类别为13手术器械-吻(缝)合器械及材料,二级产品类别为07不可吸收缝合线。
本指导原则不适用于可吸收缝线、预期用于骨结合及其他有特殊要求的缝线(如主要用于肌腱和韧带缝合的超高分子量聚乙烯缝线、免打结式缝线、具有抗菌作用缝线等)。
二、注册申报资料要求(一)产品名称的要求产品名称应以产品的预期用途和适用范围为依据,一般应为不可吸收缝合线或非吸收性外科缝线。
产品名称中可体现缝线的材料(例如非吸收性聚丙烯外科缝线)。
(二)产品的结构组成非吸收性外科缝线通常是由天然材料或聚合材料制成的表面可有涂层的不可降解吸收的缝合线。
分为带针和不带针两种。
产品结构分为多股和单股。
根据产品材料、结构和有无涂层可以分为以下三类:表1 缝线的分类非吸收性外科缝线常见材质有蚕丝、聚酰胺、聚酯、聚丙烯、不锈钢等。
(三)产品工作原理非吸收性外科缝线在外科手术当中,或者是外伤处置当中,用于软组织、器官和/或皮肤的缝合。
(四)注册单元划分的原则和实例按照《医疗器械注册管理办法》(国家食品药品监督管理总局令第4号)第七十四条要求,“医疗器械注册或者备案单元原则上以产品技术原理、结构组成、性能指标和适用范围为划分依据”。
不可吸收性缝合线-卫生署医疗器材资料库

「不可吸收性縫合線」臨床前測試基準Guidance for Pre-clinical Testing of Non-absorbable Surgical Suture【說明】1.本測試基準係提供醫療器材廠商辦理產品查驗登記時,臨床前測試應檢附資料及進行項目之建議,未包含臨床試驗等其他資料之要求,醫療器材查驗登記申請案仍應符合相關法規。
廠商亦應依個案產品結構、材質及宣稱效能提出完整驗證評估(含臨床前測試及/或臨床試驗等)之資料。
2.本測試基準依據現行之參考資料制定,惟科技發展日新月異,法規更新未逮處,為確保國人健康安全,審查人員將視產品宣稱效能、結構與設計之安全性及功能性,要求廠商提供本測試基準所列項目外之驗證評估(含臨床前測試及/或臨床試驗)資料;另本測試基準將不定期更新。
3.臨床前測試資料應包括檢驗規格(含各測試項目之合格範圍及其制定依據)、方法、原始檢驗紀錄及檢驗成績書。
4.如製造廠未進行表列測試項目,應檢附相關文獻或科學性評估報告,以證實產品仍具有相等之安全及功能。
5.各項測試如本測試基準或表列之參考方法未訂有規格者,由各製造廠自行制定規格;如本測試基準或表列參考方法已訂有規格,惟製造廠另訂不同規格者,應檢附相關文獻或科學性評估報告以說明訂定規格之依據。
6.製造廠使用之測試方法如與本測試基準所列參考方法不同,但(1)具等同性者,應檢附製造廠測試方法供審核;(2)如不具等同性,應檢附製造廠測試方法及相關文獻或科學性評估報告以說明該測試方法制定之依據。
7.如表列參考資料有修訂、廢止或被其它標準取代,製造廠得參照新版標準進行測試。
一、本基準適用之醫療器材範圍(Scope):本基準適用於下列不可吸收性縫合線,包括附加及不附標準縫針者:不可吸收式聚乙烯縫合線(Nonabsorbable poly(ethylene terephthalate)surgical suture)、不可吸收式聚丙烯縫合線(Nonabsorbable polypropylene surgical suture)、不可吸收式聚醯胺縫合線(Nonabsorbable polyamide surgical suture)、不可吸收性絲縫合線(Natural nonabsorbable silk surgical suture)、不可吸收式已展開之聚四氟乙烯手術縫合線(Nonabsorbable expanded polytetrafluoroethylene surgical suture)、不銹鋼縫合線(Stainless steel suture)。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
非吸收性外科缝线
适用范围:供人体组织的缝合、结扎用。
1.1产品型号、规格及其划分说明
1.1.1根据缝合线的粗细分为9/0、8/0、7/0、6/0、5/0、4/0、3/0、2/0、0九种规格。
1.1.2根据缝合线的长度分为15cm、18cm、45cm、60cm、75cm、80cm、90cm、100cm、120cm和150cm十种规格。
1.1.3根据缝合线的颜色分为蓝色和白色。
1.1.4根据缝合针的针型不同分为圆针、圆体角针和角针,如图1、图2、图3。
图1 圆
针图2 圆体
角针图3 角针
1.1.5根据缝线与缝针连接型式分为单针和双针,双针连接型式为缝线两端各有一枚缝合针。
1.1.6型号划分说明如下:
1.1.7具体规格型号及尺寸见附录A。
1.2结构组成及材料
本产品由缝合线和缝合针组成,其中缝合线是由聚丙烯材料制成的单股缝线,表面涂覆有硅氧烷涂层,经酞氰-铜(Phthalocyanine-copper)染色,分为蓝色和白色(无染色)。
缝合针材质为30Cr13不锈钢。
按YY0167-2005中的分类规定属于Ⅱ类单股合成纤维缝线。
2.1缝线
2.1.1外观
2.1.1.1缝线表面应光滑,条干均匀,无污渍,无结头。
2.1.1.2针线连接处应光滑、无毛刺。
2.1.2 线径
缝线的线径应符合YY0167-2005中的规定,见表1。
表1缝线的规格与线径范围
2.1.3 抗张强度
缝线的抗张强度应符合YY0167-2005中的规定,见表2。
表2缝线的抗张强度
2.1.4 长度
缝线长度应不小于标识长度的95%,单根缝线的长度应不大于3.5m。
2.1.5褪色试验
若缝合线染色,褪色试验应合格。
2.2缝合针
2.2.1 使用性能
2.2.1.1刺穿力
缝合针针尖应尖锐、无弯钩,其刺穿力应符合YY0043-2005中的要求,见表3。
表3刺穿力
2.2.1.2切割力
三角针刃口应锋利,其切割力应符合YY0043-2005中的要求,见表4。
表4切割力
2.2.2 物理性能
应符合YY0043-2005中第4.2条的要求。
2.2.3 外观
应符合YY0043-2005中第4.3条(除4.3.4弹机孔嵌线)的要求。
2.3 针线连接强度
缝合线的针线连接强度应符合YY0167-2005中的要求,见表5。
表
5针线连接强度
2.4 环氧乙烷残留量
若缝线采用环氧乙烷灭菌时,环氧乙烷的残留量应不大于250μg/g。
2.5 无菌
缝合线和缝合针应无菌。
2.6 细菌内毒素
细菌内毒素限量应小于20EU/套。
