碳和硅形成的化合物
碳硅及其重要化合物间的转化关系

碳硅及其重要化合物间的转化关系全文共四篇示例,供读者参考第一篇示例:碳硅是一种重要的元素,它们在自然界中广泛存在并且具有许多重要的化合物。
碳和硅是两种非金属元素,它们在化学性质上有一些相似之处,因此在一些化学反应中可以相互转化。
在本文中,我们将探讨碳硅及其重要化合物之间的转化关系。
让我们来看一下碳的化合物。
碳是一种非金属元素,它在自然界中存在于多种形式中,如石墨、金刚石和全新炭等。
碳在化学反应中通常以四价的形式存在,它可以与氧、氢、氮等元素形成许多不同的化合物。
碳酸盐是碳循环中的一个重要环节,它在地壳中有着广泛的存在,并且可以通过各种化学反应转化为其他碳化合物,如石灰石、煤炭等。
硅是一种具有金属性质的元素,它在自然界中存在于硅石、石英和硅酸盐等形式中。
硅与氧形成的硅酸盐是地壳中的主要组成,它们可以通过地球内部的热液作用、熔融作用等过程来形成。
硅也可以与其他元素形成许多重要化合物,如硅烷、硅酸等。
碳硅在化学性质上有一些相似之处,因此它们在一些化学反应中可以相互转化。
碳可以与硅直接反应,生成碳硅化合物,如碳化硅。
碳化硅是一种重要的半导体材料,它具有优良的导电性能和热导率,被广泛应用于电子器件、太阳能电池等领域。
碳硅材料还可以通过不同的方法制备,如化学气相沉积、烧结等。
碳硅及其重要化合物之间存在着多种转化关系,它们在材料科学、化工等领域中有着广泛的应用前景。
通过深入研究碳硅化学性质及其相互转化关系,我们可以更好地利用这些重要元素和化合物,推动科学技术的发展,实现材料的创新和应用。
希望本文能够帮助读者更深入地了解碳硅及其重要化合物之间的转化关系,激发对这一领域的兴趣和热情。
希望碳硅化学的研究能够为人类社会的可持续发展做出更大的贡献。
【2000字】。
第二篇示例:碳硅是一种重要的元素,其在自然界中的存在形式有许多,包括石墨、金刚石等,而碳硅也是一种重要的金属loid,其在化学反应中具有独特的性质和作用。
碳硅及其重要化合物间的转化关系,既包括碳硅之间的相互转化,也包括碳硅与其他元素形成的化合物之间的转化关系。
有机硅新材料

有机硅新材料
有机硅是一种具有碳硅键的有机化合物,其分子结构中含有硅元素。
有机硅新材料是指以有机硅作为主要原料,通过化学合成或改性制备而成的新型材料。
有机硅新材料具有许多优良特性,被广泛应用于建筑、医药、化工、电子等领域。
首先,有机硅新材料具有优异的耐高温性能。
由于硅元素的特殊性质,有机硅新材料在高温环境下依然能够保持稳定的性能,不易熔化或变形,因此被广泛应用于航空航天、汽车制造等领域。
其次,有机硅新材料具有良好的耐腐蚀性能。
由于硅元素与氧气结合形成的二氧化硅具有很强的稳定性,因此有机硅新材料在酸碱等腐蚀性介质中表现出较好的耐蚀性,适用于化工设备、管道等领域。
此外,有机硅新材料还具有优异的绝缘性能和机械性能。
由于硅元素与有机基团的结合,使得有机硅新材料在电气绝缘和机械强度方面表现出色,广泛应用于电子电器、建筑材料等领域。
另外,有机硅新材料还具有良好的粘接性能和表面活性。
有机硅新材料可以通过改性制备成各种类型的胶水、润滑剂、表面处理剂等,被广泛应用于家居装饰、汽车制造、纺织印染等领域。
综上所述,有机硅新材料具有耐高温、耐腐蚀、绝缘、粘接等优异性能,被广泛应用于各个领域。
随着科学技术的不断发展,有机硅新材料的应用领域将会更加广泛,为人类社会的发展进步提供更多的可能性。
硅原子 碳原子 异同点

硅原子碳原子异同点
硅原子和碳原子是两种不同的元素,它们在周期表中分别位于第14和第6族。
虽然它们都属于同一元素周期,但在化学性质上存在显著的差异。
以下是它们的异同点:
相似点:
1.元素周期表中的位置:硅和碳都位于元素周期表的同一周期内,即第2周期。
2.能够形成共价键:硅和碳都是非金属元素,它们都能够通过共价键形成化合物。
3.在有机化学中的重要性:碳是有机化合物的基本组成元素,而硅也可以与碳形成类似的有机化合物,被称为硅有机化合物或硅氢化合物。
不同点:
1.原子结构:硅原子的电子排布为1s²2s²2p⁶3s²3p²,而碳原子的电子排布为1s²2s²2p²。
2.化学性质:由于电子结构的不同,硅和碳在化学性质上有很大差异。
碳原子形成的化合物通常具有较高的稳定性和多样性,包括形成链状、环状和立体构型的能力。
而硅原子形成的化合物通常较为稳定,但多数情况下较碳化合物更为简单且缺乏多样性。
3.生物学角度:碳是生命体中的基本元素,构成有机物质的基础,而硅在生命体中并不普遍存在,只在一些硅藻等特定生物中以硅质形式存在。
1 / 2
4.物理性质:硅是一种半金属,具有一些金属和非金属的特性,例如硅具有一定的导电性。
而碳则有多种同素异形体,包括钻石、石墨和纳米碳管等,具有不同的物理性质和用途。
总的来说,尽管硅和碳在周期表上相邻,但它们在化学性质、应用和生物学上有显著的不同。
2 / 2。
碳、硅及其重要化合物

碳、硅及其重要化合物一、碳、硅单质1.单质的结构、存在形态、物理性质和用途2.碳和硅的化学性质3.硅的工业制法及提纯石英砂――→①焦炭高温粗硅――→②氯气加热SiCl 4――→③氢气高温高纯硅反应①:□20SiO 2+C=====高温Si +2CO ↑。
反应②:□21Si +Cl 2=====△SiCl 4。
反应③:□22SiCl 4+2H 2=====高温Si +4HCl 。
二、碳、硅的氧化物 1.一氧化碳 (1)物理性质□01无色气体,□02有毒,□03难溶于水。
(2)化学性质 ①燃烧:2CO +O 2=====点燃2CO 2,□04淡蓝色火焰(空气中燃烧)。
②还原Fe 2O 3:□05Fe 2O 3+3CO=====高温2Fe +3CO 2(冶炼金属)。
2.二氧化碳和二氧化硅的比较续表三、硅酸、硅酸盐、无机非金属材料1.硅酸(H2SiO3)2.硅酸盐(1)硅酸盐是由硅、氧和金属元素组成的化合物的总称,是构成地壳岩石的重要成分。
(2)硅酸盐组成的表示方法通过用二氧化硅和金属氧化物的组合形式表示硅酸盐的组成,如硅酸钠(Na2SiO3)可表示为Na2O·SiO2,长石(KAlSi3O8)可表示为□06K2O·Al2O3·6SiO2。
(3)硅酸钠①白色、可溶于水的粉末状固体,其水溶液俗称□07水玻璃,有黏性,水溶液显碱性。
②与酸性较硅酸强的酸反应与CO2水溶液反应的化学方程式Na2SiO3+H2O+CO2===□08Na2CO3+H2SiO3↓。
(3)用途:黏合剂(矿物胶),耐火阻燃材料。
3.无机非金属材料(1)传统无机非金属材料①三种硅酸盐工业生产的比较②主要用途:陶瓷、玻璃、水泥是重要建筑材料,也广泛应用于生活中。
(2)新型无机非金属材料①高温结构陶瓷:如氮化硅陶瓷具有较高的硬度和耐磨性、较强的抗化学侵蚀性和电绝缘性等。
②生物陶瓷:对机体无排异反应,不会引起代谢作用异常。
高中化学碳和硅的知识点介绍

高中化学碳和硅的知识点介绍在高中的化学学习中,学生过会学习到很多的知识点,下面店铺的小编将为大家带来化学中关于碳和硅的知识点的介绍,希望能够帮助到大家。
高中化学碳和硅的知识点(一)碳族元素1、组成和结构特点(1)碳族元素包括碳、硅、锗、锡、铅五种元素,位于元素周期表的IVA族。
(2)碳族元素原子最外层有4个电子,在化学反应中不易得到或失去电子,易形成共价键。
主要化合价有+2和+4价,其中碳和硅有负价。
碳族元素在化合物中多以+4价稳定,而铅在化合物中则以+2价稳定。
碳族元素中碳元素形成的单质(金刚石)硬度最大;碳元素形成的化合物种类最多;在所有非金属形成的气态氢化物中,CH4中氢元素的质量分数最大;12C是元素相对原子质量的标准原子;硅在地壳中的含量仅次于氧,其单质晶体是一种良好的半导体材料。
2、性质的递变规律随着原子序数的增大,碳族元素的原子半径依次增大,由非金属元素逐渐转变为金属元素,即金属性逐渐增强,非金属性逐渐减弱;最高价氧化物对应水化物的酸性逐渐减弱,碱性逐渐增强;气态氢化物的稳定性逐渐减弱,还原性逐渐增强。
(二)碳及其化合物1、碳单质(1)碳的同素异形体(2)碳的化学性质常温下碳的性质稳定,在加热、高温或点燃时常表现出还原性,做还原剂,温度越高,还原性越强,高温时的氧化产物一般为一氧化碳。
溶解性不同:一般情况下,所有的钾盐、钠盐和铵盐是可溶的,所有的酸式盐是可溶的,正盐的溶解度小于酸式盐的溶解度,但碳酸钠的溶解度大于碳酸氢钠的溶解度。
热稳定性不同:一般情况下,难溶的正盐和酸式盐受热易分解,可溶性碳酸盐稳定不易分解。
与酸反应的剧烈程度不同:两者都能与强酸(H+)反应产生CO2,但反应的剧烈程度不同,根据反应的剧烈程度可鉴别两者。
可溶性盐的水解程度不同:相同浓度的正盐溶液的pH值大于酸式盐溶液的pH值。
与碱反应不同:弱酸的酸式盐可与碱反应生成正盐。
与盐反应不同:碳酸钠可与氯化钙或氯化钡反应生成难溶性碳酸盐,但碳酸氢钠不反应。
有机硅化合物

有机硅化合物
有机硅化合物是指与有机物结合的硅原子所构成的化合物,如硅醇、
硅醚、硅烷、硅酰胺、硅氧烷等。
它们是一类极重要的有机物,广泛应用
在生物化学、材料科学、农药、农业添加剂等领域。
硅醇是最常见的有机硅化合物,它是一种液态有机物,既可以是钠、钙、镁及其他离子的氢氧化物,也可以是羟基硅烷。
硅醇的大部分对水溶
液有极强的可溶性,可以与矿物质和氨基酸等多种化合物形成缓冲溶液,
用于维持多种有机反应的稳定性。
硅醚是有机硅化合物中的重要成分,它是将硅原子跟碳原子键连在一
起而形成的有机物质,具有重要的醚性质,是一种广泛应用的表面活性剂。
由于具有优良的稳定性、良好的溶解性和较大的分子量,它可以用于制造
润滑剂、润湿剂和各种除细泡剂和抗结垢剂等。
硅烷是有机硅化合物中的重要成分,它由一个硅原子与多个碳原子相
连而成,具有疏水性、易溶于有机溶剂的特性。
它们可以用于制造交联剂、发泡剂、着色助剂、黏合剂等,也可以用于制造涂料、塑料等。
此外,它
们也广泛用于制作农药和化妆品中。
碳及硅元素的性质及应用

摘要本文简单粗略地介绍了Ⅳ主族,即碳族元素的基本通性,并对其中的碳元素和硅元素进行展开,分析了它们的单质,各类化合物的性质与制备方法,并揭示了它们在现实生活、工业等各个领域的用途及应用前景。
最后对碳、硅元素之间的异同作了进一步的阐述。
希望通过本文能够更深入地了解有关碳元素、硅元素以及碳族元素的扩展知识。
关键词:金刚石、石墨、富勒烯、碳纳米管、超导材料、沸石分子筛、半导体、高温结构陶瓷、纤维一.碳族元素的通性碳族元素是Ⅳ族元素,包括碳(carbon C)、硅(silicon Si)、锗(germanium Ge)、锡(tin Sn)、铅(lead Pb)、五个元素。
碳和硅是非金属元素,其余三种是金属元素。
本族元素基态原子的价电子结构为ns2np2。
碳和硅主要形成共价化合物,常见的氧化态为+4。
由于C-C单键的键能比C-H、C-O的键能低,所以含C-C键的化合物大量存在。
碳原子还有较强的形成多重键的倾向。
与碳相比,硅生成多重键的倾向明显减弱,在绝大多数化合物中硅原子常以sp3杂化形成4个单键,由于Si-O键能比Si-Si键能多,所以硅是亲氧元素。
随着本族元素原子序数的递增,过渡到第六周期元素铅时,由于原子核中有充满的4f亚层,有集中增强的核电场,加强了6s电子的穿透性,使6s能级显著降低,6s电子较不易成键,这就是所谓的“惰性电子对”。
因此,在锗、锡、铅中,随着元素原子序数的增大,稳定氧化态由+4变为+2。
+2氧化态的锗有很强的还原性,而+2氧化态的锡和铅离子在极性溶液中存在,+4氧化态的铅为强氧化剂。
碳和硅在自然界中分布很广,其中硅在地壳中的含量仅次于氧,锗的分布很分散,锡和铅矿藏较集中,易提炼。
锡在自然界中主要的矿石是锡石SnO2,我国有丰富的铅资源。
铅的主要矿石是方铅矿PbS。
碳族元素的单质都有十分重要的应用。
例如,高纯度的硅和锗是良好的半导体材料,在电子工业中用来制造各种半导体元件,锡和铅可用于制造合金,铅还可以作核反应推的防护屏等。
碳化硅特性
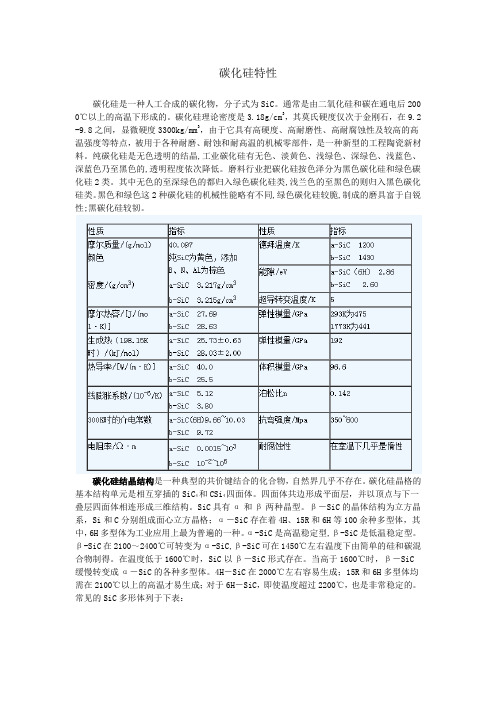
碳化硅特性碳化硅是一种人工合成的碳化物,分子式为SiC。
通常是由二氧化硅和碳在通电后200 0℃以上的高温下形成的。
碳化硅理论密度是3.18g/cm3,其莫氏硬度仅次于金刚石,在9.2 -9.8之间,显微硬度3300kg/mm3,由于它具有高硬度、高耐磨性、高耐腐蚀性及较高的高温强度等特点,被用于各种耐磨、耐蚀和耐高温的机械零部件,是一种新型的工程陶瓷新材料。
纯碳化硅是无色透明的结晶,工业碳化硅有无色、淡黄色、浅绿色、深绿色、浅蓝色、深蓝色乃至黑色的,透明程度依次降低。
磨料行业把碳化硅按色泽分为黑色碳化硅和绿色碳化硅2类。
其中无色的至深绿色的都归入绿色碳化硅类,浅兰色的至黑色的则归入黑色碳化硅类。
黑色和绿色这2种碳化硅的机械性能略有不同,绿色碳化硅较脆,制成的磨具富于自锐性;黑碳化硅较韧。
碳化硅结晶结构是一种典型的共价键结合的化合物,自然界几乎不存在。
碳化硅晶格的基本结构单元是相互穿插的SiC4和CSi4四面体。
四面体共边形成平面层,并以顶点与下一叠层四面体相连形成三维结构。
SiC具有α和β两种晶型。
β-SiC的晶体结构为立方晶系,Si和C分别组成面心立方晶格;α-SiC存在着4H、15R和6H等100余种多型体,其中,6H多型体为工业应用上最为普遍的一种。
α-SiC是高温稳定型,β-SiC是低温稳定型。
β-SiC在2100~2400℃可转变为α-SiC,β-SiC可在1450℃左右温度下由简单的硅和碳混合物制得。
在温度低于1600℃时,SiC以β-SiC形式存在。
当高于1600℃时,β-SiC 缓慢转变成α-SiC的各种多型体。
4H-SiC在2000℃左右容易生成;15R和6H多型体均需在2100℃以上的高温才易生成;对于6H-SiC,即使温度超过2200℃,也是非常稳定的。
常见的SiC多形体列于下表:碳化硅的基本性能包括化学性质、物理机械性能、电学性质以及其他性质(亲水性好,远红外辐射性等)。
碳和硅(1)

7.下列说法中摘自某科普杂志,你认为无科学性错误 的是( CD ) A.铅笔芯的原料是重金属铅,儿童在使用时不可用嘴 咬铅笔,以免引起铅中毒
B.一氧化碳有毒,生有煤炉的居室,可放置数盘清水, 这样可有效地吸收一氧化碳,防止煤气中毒
C.“汽水”浇灌植物有一定的道理,其中二氧化碳的 缓释 。有利于作物的光合作用 D.硅的提纯和应用,促进了半导体元件与集成芯片的 发展,可以说“硅是信息技术革命的催化剂”
CO2 无色无味的气体,无毒,微 溶于水,固态时叫干冰 CO2+H2O 不反应 CO2+ 2NaOH= Na2CO3+ H2O CO2+ CaO==CaCO3 CO2+ Na2CO3+ H2O = 2NaHCO3 CO2+C 2CO H2CO3
SiO2 硬度大,熔沸点高,常温 下为固体,不溶于水。 不反应 SiO2+4HF == SiF4↑+2H2O SiO2+ 2NaOH= Na2SiO3 + H2O
(3)用途
硅胶可作干燥剂、催化剂的载体
1. 无机酸一般易溶于水,而硅酸却难溶于水。
2. 碳酸酸性大于硅酸 水溶液中
CO2+ Na2SiO3+ H2O =H2SiO3↓+ Na2CO3 Na2SiO3 + CO2↑
高温条件下 SiO2+ Na2CO3
分析:在水溶液中,碳酸的酸性比硅酸强,因此发生了反应 生成了硅酸沉液,在高温重要条件下,生成的二氧化碳离 开了反应体系而使反应进行到底(化学平衡)。
(三)、其他新型无机非金属材料简介
(1)金刚石:金刚石是目前已知的最硬的材料,可以用来 切削和刻划其他物质,被用于钻探、磨削等行业
有机硅无机硅

有机硅与无机硅1. 引言有机硅和无机硅是化学领域中两种常见的物质类型。
它们在性质、结构和应用方面有着明显的差异。
本文将详细介绍有机硅和无机硅的定义、特点、制备方法以及主要应用领域。
2. 有机硅2.1 定义与特点有机硅是指含有碳-硅键的化合物,其中碳和硅之间共享电子对形成化学键。
由于碳-硅键的极性较小,有机硅具有较高的热稳定性、耐腐蚀性和绝缘性能。
此外,由于碳-硅键较长,有机硅分子通常具有柔软的链状结构。
2.2 制备方法2.2.1 直接合成法直接合成法是通过将含有碳-氢键的化合物与含有Si-H键的化合物反应得到。
这种方法通常需要催化剂存在,并在适当的温度下进行。
2.2.2 氧化还原法氧化还原法是通过将含有Si-OH基团的化合物与还原剂反应得到有机硅。
这种方法通常需要在惰性气体保护下进行,以防止氧化反应的发生。
2.3 应用领域2.3.1 塑料工业有机硅可以用作塑料添加剂,改善塑料的性能,如增加耐热性、耐候性和耐化学品腐蚀性。
2.3.2 医药领域有机硅可以用于制备药物载体,提高药物的溶解度和稳定性,并延长药物的释放时间。
2.3.3 电子工业有机硅可以用于制备半导体材料,如硅片和太阳能电池。
3. 无机硅3.1 定义与特点无机硅是指不含碳-硅键的化合物。
它们通常是由硅原子与其他原子(如氧、氢、铝等)形成化学键而构成。
无机硅具有较高的熔点、良好的导热性和电绝缘性。
3.2 制备方法3.2.1 硅石冶炼法硅石冶炼法是将含有二氧化硅(SiO₂)的原料与炭一起加热到高温,使二氧化硅还原为纯硅。
3.2.2 化学气相沉积法化学气相沉积法是将硅源物质(如三氯化硅)在高温下分解生成纯硅的方法。
3.3 应用领域3.3.1 玻璃工业无机硅是玻璃的主要成分,它赋予玻璃优良的透明性、耐高温性和化学稳定性。
3.3.2 陶瓷工业无机硅可以用于制备陶瓷材料,如陶器和耐火材料。
3.3.3 锂离子电池工业无机硅可以用作锂离子电池的负极材料,提高电池的容量和循环寿命。
有机硅合成

有机硅合成
有机硅合成是指通过化学反应将有机化合物与硅化合物结合形成新的有机硅化合物的过程。
有机硅化合物是一类含有碳-硅键的化合物,其具有特殊的化学和物理性质,广泛应用于化工、材料科学、医药和农业等领域。
有机硅合成的方法多种多样,常见的包括以下几种:
1. 反应硅烷与有机卤化物:将有机卤化物与硅烷在适当的反应条件下反应,通过取代反应形成碳-硅键,生成有机硅化合物。
2. 还原硅烷:将硅烷与还原剂反应,还原硅烷中的硅氢键,生成有机硅化合物。
3. 氧化硅烷:将硅烷与氧化剂反应,氧化硅烷中的碳-硅键,生成有机硅化合物。
4. 硅烷催化反应:利用硅烷作为催化剂,促进有机化合物之间的反应,从而形成有机硅化合物。
有机硅合成的关键是选择合适的反应条件和催化剂,以及控制反应的温度、压力和反应时间等因素。
此外,纯度和反应物的比例也会对合成产物的质量和收率产生影响。
总之,有机硅合成是一种通过化学反应将有机化合物和硅化合物结合
形成新的有机硅化合物的过程,其方法多种多样,需选择合适的反应条件和催化剂,并控制反应参数,以获得所需的有机硅化合物。
硅碳和石墨-概述说明以及解释

硅碳和石墨-概述说明以及解释1.引言1.1 概述概述部分:硅碳和石墨都是由碳元素组成的材料,具有许多相似的特性和应用领域。
硅碳是一种二元合金,其中硅和碳以不同的比例混合在一起,形成硅碳化合物。
这种合金具有高硬度、高热导性和耐腐蚀等特点,广泛应用于各种工业领域,如钢铁冶金、航空航天和化工等。
石墨是由碳元素形成的一种晶体结构材料,其分子结构中的碳原子以层状排列。
石墨具有良好的导电性、热稳定性和润滑性,广泛应用于电池、石墨烯制备、润滑剂和高温材料等领域。
本文将对硅碳和石墨的定义、性质以及各自的应用领域进行详细介绍。
通过对这两种材料的研究和分析,可以更好地理解它们的特点和优势,并探讨它们在未来的发展前景。
同时,本文还将总结硅碳和石墨的重要性,并展望它们在不同领域中的潜在应用和创新可能性。
1.2 文章结构文章结构部分的内容可以根据以下内容编写:文章结构部分旨在介绍本文的框架和组织,以帮助读者更好地理解文章内容。
本文共分为以下几个部分。
第一部分是引言。
该部分首先对硅碳和石墨进行简单介绍,包括它们的定义和基本性质。
接着,文章将说明本文的目的,即通过对硅碳和石墨的研究和分析,探讨它们在不同领域中的应用和未来发展的潜力。
第二部分是正文。
该部分将分别深入探讨硅碳和石墨。
对于硅碳,我们将详细介绍其定义和基本性质,例如硅碳的化学成分、晶体结构和物理特性等。
同时,我们还将探讨硅碳在各个领域的广泛应用,例如电子、能源、材料科学等,并重点介绍其在这些领域中的优势和潜在的挑战。
对于石墨,我们将同样展开讨论。
首先,我们将明确石墨的定义和基本性质,包括其有序的晶格结构和独特的导电性能。
然后,我们将介绍石墨在不同领域的应用,例如石墨烯在电子学和纳米技术中的应用,以及石墨在润滑剂、石墨电极和材料增强方面的应用。
第三部分是结论。
该部分将对硅碳和石墨进行总结,回顾之前的讨论,并强调它们的重要性和潜力。
同时,我们还将展望硅碳和石墨的未来发展,探讨可能的研究方向和应用领域。
sioc碳氧化硅

sioc碳氧化硅(原创版)目录1.SiOC 碳氧化硅的概述2.SiOC 碳氧化硅的特性与应用3.SiOC 碳氧化硅的发展前景正文【SiOC 碳氧化硅的概述】SiOC 碳氧化硅,也称为碳化硅氧化物,是一种由硅、碳和氧元素组成的无机化合物。
化学式为 SiOC,它具有高硬度、高热导率、低热膨胀系数等优异特性,因此在众多领域有着广泛的应用。
【SiOC 碳氧化硅的特性与应用】SiOC 碳氧化硅的特性主要体现在以下几个方面:1.高硬度:SiOC 碳氧化硅具有极高的硬度,其硬度仅次于金刚石,这使得它在工业领域具有广泛的应用,如切割、研磨等。
2.高热导率:SiOC 碳氧化硅的热导率很高,这意味着它能够在高温环境下保持良好的热稳定性,因此在高温设备中有着广泛的应用。
3.低热膨胀系数:SiOC 碳氧化硅的热膨胀系数较低,这意味着在温度变化时,其尺寸变化较小,因此在精密仪器和设备中有着广泛的应用。
4.化学稳定性:SiOC 碳氧化硅具有较好的化学稳定性,不易与大多数化学物质发生反应,因此在化学工业中有着广泛的应用。
5.高温抗氧化性:SiOC 碳氧化硅在高温下具有很好的抗氧化性,因此在航空航天、汽车尾气净化等领域有着重要的应用。
【SiOC 碳氧化硅的发展前景】随着科学技术的不断发展,SiOC 碳氧化硅在各个领域的应用也在不断拓展。
未来,SiOC 碳氧化硅的发展前景十分广阔,尤其在以下几个方面:1.新能源领域:SiOC 碳氧化硅在新能源领域,如太阳能电池、燃料电池等方面有着广泛的应用。
随着新能源技术的发展,SiOC 碳氧化硅的需求将会进一步增加。
2.航空航天领域:SiOC 碳氧化硅在航空航天领域有着重要的应用,如发动机部件、航空航天器结构材料等。
随着航空航天技术的不断发展,SiOC 碳氧化硅在该领域的应用将不断扩大。
3.汽车工业:SiOC 碳氧化硅在汽车尾气净化领域有着广泛的应用。
随着环保法规的不断严格,SiOC 碳氧化硅在汽车工业的需求将持续增长。
四甲基氢氧化铵 有机硅 平衡-概述说明以及解释

四甲基氢氧化铵有机硅平衡-概述说明以及解释1.引言1.1 概述概述部分的内容可以按以下方式编写:引言部分是文章的开头部分,用于向读者介绍文章的主题和背景。
在这里,我们将介绍四甲基氢氧化铵和有机硅两种化合物的概述。
四甲基氢氧化铵是一种季铵盐,化学式为(CH3)4NOH,它是一种无色无臭的结晶固体,在水中具有良好的溶解性。
四甲基氢氧化铵在许多领域都有广泛的应用。
它常用作离子液体、化学反应催化剂的溶剂和表面活性剂。
此外,四甲基氢氧化铵还可用作草坪草甘草素的溶剂和染料中间体的合成。
有机硅是一类化合物,其中碳和硅元素由共价键连接。
有机硅的结构和性质使得它在许多领域中具有广泛的应用。
有机硅可以大致分为有机硅化合物和无机硅氧烷两类。
有机硅化合物包括硅酮、硅烷、硅醇等,它们常用作液体橡胶、油剂、润滑剂和黏合剂等。
无机硅氧烷则包括硅烷氧基、硅醚以及其他含有硅氧键的化合物,它们常用作电子器件、涂料、塑料和防水材料等领域。
通过对四甲基氢氧化铵和有机硅的概述,我们可以更好地理解它们的物化性质、应用领域以及在科学研究和工业生产中的重要性。
本文将对这两种化合物进行详细的描述和分析,希望能为读者提供有关四甲基氢氧化铵和有机硅的全面了解。
(注意:以上内容仅为示例,可以根据实际情况和需要进行修改)1.2文章结构1.2 文章结构本文将分为引言、正文和结论三个部分。
具体的章节安排如下:2. 正文部分2.1 四甲基氢氧化铵2.1.1 物化性质2.1.2 应用领域2.2 有机硅2.2.1 结构和性质2.2.2 应用领域在正文部分,我们将首先介绍四甲基氢氧化铵的基本概念及其物化性质。
随后,我们将探讨四甲基氢氧化铵在各个应用领域中的具体应用情况,并深入了解其在医药、化学工业和科学研究等方面的重要性。
接下来,我们将重点讨论有机硅的结构和性质。
通过对有机硅的分子结构以及其在化学反应和材料制备中的特殊性质进行综合分析,加深对有机硅在化工、电子、光电子等技术领域的应用了解。
碳硅键和氧硅键

碳硅键和氧硅键
碳硅键和氧硅键是两种重要的化学键类型。
碳硅键是由碳和硅元素之间的共价键形成的,它们通常用于有机硅化合物的合成,例如硅烷和硅氧烷。
这些化合物在医药和农业领域中具有广泛的应用。
氧硅键是由硅和氧元素之间的共价键形成的,它们是硅酸盐矿物的主要成分。
这些矿物包括石英、长石、云母和辉石等,它们在地壳中广泛分布,并且是建筑材料、玻璃、电子器件和光学器件等的重要原材料。
碳硅键和氧硅键在化学反应中都具有重要的作用。
例如,在有机合成中,碳硅键可以作为稳定的化学键,允许化合物在高温、高压和强碱等条件下进行反应。
而氧硅键则可以通过碳硅键的还原反应制备硅烷和其他有机硅化合物。
总之,碳硅键和氧硅键是两种在化学和材料科学中非常重要的化学键类型,它们在各自领域中具有广泛的应用和重要的作用。
- 1 -。
硅烷沉积 硅碳

硅烷沉积硅碳1. 简介在材料科学领域中,硅烷沉积是一种常见的技术,用于在表面上形成硅碳薄膜。
该技术利用硅烷化合物在高温下分解并沉积在基底表面上,形成硅碳化合物的沉积层。
硅烷沉积硅碳具有许多优点,例如高纯度、较低的沉积温度和良好的薄膜均匀性,因此在半导体制造、光学涂层和防腐涂层等领域得到广泛应用。
2. 硅烷化合物硅烷沉积的关键是选取合适的硅烷化合物作为前体。
常用的硅烷化合物包括硅烷、硅烷烃和硅烷烷烃。
硅烷是一类化学式为SiH4的气体,具有较高的活性,易于分解并沉积在表面上。
硅烷烃是由硅烷和烃基团组成的化合物,其结构可以调整硅碳化合物的性质。
硅烷烷烃是由硅烷烃和烷烃基团组成的化合物,具有更复杂的结构,可用于制备复杂的硅碳化合物。
3. 硅烷沉积工艺硅烷沉积硅碳的工艺主要包括前体供应、沉积反应和沉积条件控制三个步骤。
3.1 前体供应在硅烷沉积过程中,硅烷化合物作为前体被输入到反应室中。
前体供应系统通常包括前体气体源、气体输送管道和控制阀。
硅烷化合物通常以气体形式存在,因此需要通过气体输送管道将其引入反应室。
3.2 沉积反应硅烷沉积硅碳的反应通常在高温下进行。
在反应室中,硅烷化合物会被加热并分解,产生活性的硅原子和氢气。
硅原子会与基底表面上的碳原子发生反应,形成硅碳化合物的沉积层。
同时,氢气会与反应产物发生反应,生成副产物并被排出反应室。
3.3 沉积条件控制为了获得高质量的硅碳薄膜,沉积条件需要进行精确控制。
主要的控制参数包括沉积温度、气体流量、压力和沉积时间等。
沉积温度决定了硅烷化合物的分解速率和反应速率,气体流量和压力控制了硅烷化合物的供应速率和反应物排除速率,沉积时间决定了沉积层的厚度。
4. 硅碳化合物的性质硅烷沉积硅碳形成的沉积层具有许多优良的性质,使其在各个领域得到广泛应用。
4.1 优良的化学稳定性硅烷沉积硅碳具有较高的化学稳定性,能够抵抗化学腐蚀和氧化。
这使得硅烷沉积硅碳在防腐涂层和光学涂层中得到广泛应用。
硅碳负极 硅烷气

硅碳负极硅烷气全文共四篇示例,供读者参考第一篇示例:硅碳负极硅烷气是一种重要的材料,具有广泛的应用领域和潜在的发展前景。
硅碳材料具有高能量密度、良好的循环性能和优异的导电性能,是锂离子电池等能源领域的理想材料之一。
硅烷气则是一种有机硅化合物,在半导体、光伏等领域有着重要的应用。
结合硅碳负极和硅烷气的特性,可以制备出高性能的硅碳负极硅烷气复合材料,为新型电池领域的发展提供了新的可能性。
硅碳负极材料是一种由硅和碳元素组成的复合材料,具有较高的容量和较低的电压平台,是目前研究的热点之一。
硅碳负极材料通过引入碳元素,可以缓解硅材料在循环过程中发生的体积膨胀问题,提高其循环稳定性和电化学性能。
而硅烷气则是一种有机硅化合物,具有较高的硅含量和良好的导电性能。
将硅烷气与硅碳负极材料结合,可以有效提高负极材料的导电性能和电化学性能,进而提升整个电池的性能和循环寿命。
硅碳负极硅烷气复合材料在锂离子电池等领域具有广阔的应用前景。
由于硅碳负极材料的高容量和硅烷气的良好导电性能,该复合材料可以显著提高电池的能量密度和功率密度,有效延长电池的循环寿命。
此外,硅碳负极硅烷气复合材料还具有较高的安全性和稳定性,有望成为下一代高性能电池的关键材料之一。
在制备硅碳负极硅烷气复合材料方面,研究人员正在不断探索新的合成方法和调控策略。
通过控制硅碳负极材料的结构和硅烷气的添加量,可以实现复合材料性能的进一步优化。
此外,还可以利用纳米技术和表面修饰等手段,进一步提高硅碳负极硅烷气复合材料的性能和稳定性。
未来,随着技术的不断进步和创新,硅碳负极硅烷气复合材料将在能源存储领域发挥重要作用。
综上所述,硅碳负极硅烷气复合材料具有广阔的应用前景和发展潜力。
通过合理设计和优化,可以制备出高性能的硅碳负极硅烷气复合材料,为新型电池领域的发展做出贡献。
未来,研究人员可以进一步探索该复合材料的制备和性能调控,推动其在能源领域的应用和推广,以实现可持续能源的发展和利用。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
碳和硅形成的化合物
碳和硅可以形成多种化合物,其中最常见的是硅化碳(silicon carbide,SiC)和硅氧烷(siloxane)。
硅化碳是一种重要的陶
瓷材料,具有高硬度、高熔点和良好的耐高温性能,常用于制造高温结构材料、陶瓷工艺品和刀具等。
硅氧烷是一类具有硅-氧键的有机化合物,通过在硅原子周围连接不同的有机基团,可以获得多种性质各异的硅氧烷化合物,如硅油、硅橡胶和硅树脂等。
硅氧烷具有良好的耐高温、耐化学腐蚀性和优异的绝缘性能,广泛应用于润滑剂、密封材料、涂料和电子器件等领域。
