生物化学第十四章-基因重组和基因工程
生物化学课件 基因重组和基因工程
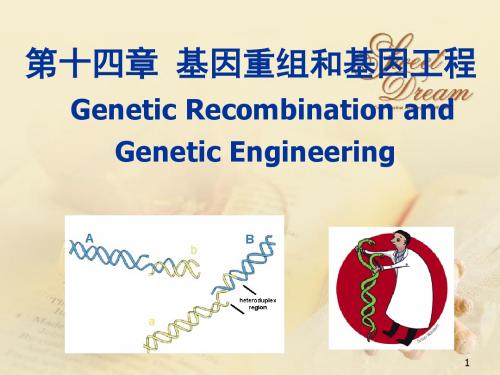
3´ 5´ 5´
内切酶
3´ (recBCD)
3´ 5´ 5´ 3´
5´ 3´ 3´ 5´
3´ 5´ 5´ 3´ 5 ´ 3´
DNA侵扰 (recA)
5´ 3´ 3´ 5´ 3´ 5´ 5´ 3´
分支迁移 (recA)
内切酶 (recBCD)
5´ 3´ 3´ 3´
3´ 5´ 5´ 3´
DNA 连接酶
5´ 3´ 3´ 5´
IR Transposase Gene IR
发生形式: 保守性转座(conservative transposition) 复制性转座(duplicative transposition)
15
插 入 序 列 的 复 制 性 转 座
16
(二)转座子转座
转座子(transposons) ——可从一个染色体位 点转移到另一位点的分散重复序列。 转座子组成:反向重复序列
使细胞或培养的受体细胞获得新的遗传表 型,称为转化作用 (transformation)。
8
例:溶菌时,裂解的DNA片段被另一细菌摄取。
9
10
(三)转导作用
当病毒从被感染的(供体)细胞释放出
来、再次感染另一(供体)细胞时,发生在
供体细胞与受体细胞之间的 DNA 转移及基因
重组即为转导作用(transduction)。
能否让细菌“吐出”蚕丝?
能否让微生物产生出人的胰岛素、干扰素等珍贵 的药物?
设想三
科学家于20世纪70年代创立了可以定向 改造生物的新技术——基因工程。
28
DNA重组技术是基因工程的核心技术
基因工程的 原理 操作环境 操作对象 操作水平 基本过程 基因重组
第十四章基因重组与基因工程.pptx

DNA利用菌体的酶系统,复制自身及 外壳蛋白,组装成大量新 噬菌体,并 将细菌涨破。
• 溶原 和裂 解可 以相 互转 变。
整合
转导
• 溶原菌中 DNA可以原样地切离出来, 也可以把邻近的宿主DNA在切离时带走 一部分。后者称转导。
酶有不止一个切口,需经过改造。 • 一个切口:插入型载体。 • 二个切口:置换型载体。
噬菌体载体
目的基因的来源
• 直接从染色体DNA中分离:原核生物 • 人工合成:简单的多肽 • 从NA后建库。
穿梭质粒
酵母
动 植 物 病 毒 、 组织培养细胞 昆虫载体 DNA 直 接 导 入 生 殖 细 胞
DNA重组体的筛选与鉴定
• 根据重组载体的表型进行筛选: 如质粒的抗药性、营养素的依赖型
• DNA限制酶切图谱分析: 提取经粗选后的宿主DNA,用限制性内 切酶切割后与原来载体比较。
• 利用核酸杂交和放射自显影进行鉴定: 用目的基因作探针监测宿主DNA是否重 组体。
分 切 接 转 筛
载体和目的基因
• 载体:vector 在宿主细胞内可独立复制的完整DNA分 子。但必须利用宿主的酶系统,才能有 进一步的基因表达能力。
• 常用的载体有: 质粒、 噬菌体 、 M13 噬菌体 逆转录病毒DNA、昆虫病毒DNA
• 载体与宿主共培育可大量生成,经纯化 后可用于基因工程。
转化
细菌的转化
转化
• 病毒癌基因 感染宿主细 胞后,可整 合到宿主染 色体上,从 而使宿主细 胞癌变。
细胞的转化
转染:噬菌体感染宿主菌后,核酸进入菌体 内的过程。
整合
• 整合: 噬菌体感染大肠杆菌的第一步 噬菌体粘附于细胞壁上,将自身的 DNA注入菌体中。 此 DNA可与细菌染 色体重组,成为细菌染色体的一部分。
沈同《生物化学》精要

沈同《生物化学》(第三版)精要速览第一章绪论第二章蛋白质的结构与功能第三章核酸的结构与功能第四章酶第五章糖代谢第七章生物氧化第八章氨基酸代谢第九章核苷酸代谢第十章DNA的生物合成第十一章RNA的生物合成第十二章蛋白质的生物合成第十三章基因表达调控第十四章基因重组和基因工程第一章绪论一、生物化学的的概念:生物化学(biochemistry)是利用化学的原理与方法去探讨生命的一门科学,它是介于化学、生物学及物理学之间的一门边缘学科。
二、生物化学的发展:1.叙述生物化学阶段:是生物化学发展的萌芽阶段,其主要的工作是分析和研究生物体的组成成分以及生物体的分泌物和排泄物。
2.动态生物化学阶段:是生物化学蓬勃发展的时期。
就在这一时期,人们基本上弄清了生物体内各种主要化学物质的代谢途径。
3.分子生物学阶段:这一阶段的主要研究工作就是探讨各种生物大分子的结构与其功能之间的关系。
三、生物化学研究的主要方面:1.生物体的物质组成:高等生物体主要由蛋白质、核酸、糖类、脂类以及水、无机盐等组成,此外还含有一些低分子物质。
2.物质代谢:物质代谢的基本过程主要包括三大步骤:消化、吸收→中间代谢→排泄。
其中,中间代谢过程是在细胞内进行的,最为复杂的化学变化过程,它包括合成代谢,分解代谢,物质互变,代谢调控,能量代谢几方面的内容。
3.细胞信号转导:细胞内存在多条信号转导途径,而这些途径之间通过一定的方式方式相互交织在一起,从而构成了非常复杂的信号转导网络,调控细胞的代谢、生理活动及生长分化。
4.生物分子的结构与功能:通过对生物大分子结构的理解,揭示结构与功能之间的关系。
5.遗传与繁殖:对生物体遗传与繁殖的分子机制的研究,也是现代生物化学与分子生物学研究的一个重要内容。
第二章蛋白质的结构与功能一、氨基酸:1.结构特点:氨基酸(amino acid)是蛋白质分子的基本组成单位。
构成天然蛋白质分子的氨基酸约有20种,除脯氨酸为α-亚氨基酸、甘氨酸不含手性碳原子外,其余氨基酸均为L-α-氨基酸。
高一生物必修课件基因重组和基因工程及其应用

两者区别
9字
基因重组是自然发生的,而 基因工程是人工操作的。
9字
基因重组的结果具有不确定 性,而基因工程可以精确设 计和控制。
9字
基因重组通常发生在同一物 种内,而基因工程可以跨物 种进行。
9字
基因重组不需要额外的工具 或技术,而基因工程需要依 赖特定的工具和技术,如限 制性内切酶、DNA连接酶等 。
高一生物必修课件基因重组和 基因工程及其应用
汇报人:XX
20XX-01-13
CONTENTS
• 基因重组 • 基因工程 • 基因工程应用 • 基因重组与基因工程关系 • 实验:基因重组和基因工程操
作实践
01
基因重组
基因重组概念
基因重组定义
基因重组是指在生物体进行有性生殖的过程中,控制不同性状的基因的重新组 合。
05
实验:基因重组和基因工程操作实践
实验目的与原理
目的
通过实验操作,了解基因重组和基因工程的基本原理,掌握相关实验技能,培养科学探究精神和实验能力。
原理
基因重组是生物体内基因重新组合的过程,包括同源重组和非同源重组两种方式。基因工程则是通过人工手段对 基因进行改造和重组,实现特定性状或功能的表达。本实验将通过模拟基因重组和基因工程操作,加深对相关原 理的理解。
重组DNA分子的导入
目的基因的检测与鉴定
将重组DNA分子导入受体细胞,使目的基 因在受体细胞中表达。
通过PCR、Southern杂交等方法检测目的 基因是否成功导入并表达。
03
基因工程应用
农业生产应用
转基因作物
通过基因工程手段,将外 源基因导入农作物中,使 其获得抗虫、抗病、抗除 草剂等优良性状,提高作
生物化学试题及答案(14

生物化学试题及答案〔14〕第十四章基因重组与基因工程[测试题]一、名词解释:1.基因工程〔geneticengineering〕。
2.接合作用(conjugation)。
3.转化作用(transforation)。
4.转导作用(transduction)。
5.转座(transposition)。
6.转座子(transposons)。
7.同源重组(homologousrecombination)。
8.全然重组(generalrecombination)。
9.DNA克隆〔DNAcloning〕。
10.复制子(replicon)。
11.限制性核酸内切酶(restrictionendonuclease)。
12.回文结构〔palindrome〕。
13.配伍末端〔compatibleend〕。
14.目的DNA〔targetDNA〕。
15.互补DNA(complementaryDNA;cDNA)。
16.克隆载体(cloningvector)。
17.表达载体(expressionvector)。
18.质粒(plasmid)。
19.α—互补(alphacomplementation)。
20.基因组DNA文库(genomicDNAlibrary)。
21.标志补救(markerrescue)。
22.转染〔transfection〕。
23.基因组DNA〔genomicDNA〕。
24.感受态细胞〔competentcell〕。
25.聚合酶链反响(polymerasechainreaction)。
26.cDNA文库(cDNAlibrary)。
27.保守性转座(conservativetransposition)。
28.复制性转座(duplicativetransposition)。
29.溶菌生长途径(lysispathway)。
30.溶源生长途径(lysogenicpathway)。
二、填空题:31.自然界的常见基因转移方式有____、____、____、____。
大学生物化学课件基因工程ppt

ቤተ መጻሕፍቲ ባይዱ
Bam HⅠ
GGATCC CCTAGG
GCCTAG+
GATCC G
切割DNA后产生含5’磷酸和3’羟基的末端
为深入学习习近平新时代中国特色社 会主义 思想和 党的十 九大精 神,贯彻 全国教 育大会 精神,充 分发挥 中小学 图书室 育人功 能
连接酶
重组体
转化 体外包装,转染
带重组体的宿主
筛选
表型筛选
酶切电泳鉴定
菌落原位杂交
以 质 粒 为 载 体 的
DNA 克 隆 过 程
扩增或表达
为深入学习习近平新时代中国特色社 会主义 思想和 党的十 九大精 神,贯彻 全国教 育大会 精神,充 分发挥 中小学 图书室 育人功 能
(六)克隆基因的表达
Ⅱ类酶识别序列特点—— 回文结构(palindrome)
GGATCC CCTAGG
切口 :平端切口、粘端切口
为深入学习习近平新时代中国特色社 会主义 思想和 党的十 九大精 神,贯彻 全国教 育大会 精神,充 分发挥 中小学 图书室 育人功 能
平端切口
HindⅡ
GTCGAC CAGCTG
GTC CAG
蛋白质而特意设计的载体称为表达载体。
载体的选择标准:
能在宿主细胞中自主复制; 具有两个以上的遗传标记物,便于重组体
的筛选和鉴定; 有克隆位点(外源DNA插入点),常具有
多个单一酶切位点,称为多克隆位点; 分子量小,以容纳较大的外源DNA。 作为表达载体,具有与宿主细胞相适应的
调控元件:启动子,增强子等。
为深入学习习近平新时代中国特色社 会主义 思想和 党的十 九大精 神,贯彻 全国教 育大会 精神,充 分发挥 中小学 图书室 育人功 能
生物化学教案:第十四章 基因重组与基因工程

转座子(transposon, Tn)
1950年麦克林托克(McClintock)在对玉米籽粒颜色遗传进行观察时所发现。转座子在移位过程中,导致DNA链的断裂/重接,或是某些基因启动/关闭。
(1)原核细胞转座子
其原型是E.coli的IS(insertion sequence,插入序列),一个细菌细胞常带少于10个IS序列。IS两端存在着反向重复序列IR(inverted repeat),IR长短不一。IS本身没有任何表型效应,只携带和它转座作用有关的基因,称转座酶基因。
1、同源重组的概念和机制。
最基本的DNA重组方式,同源重组是指发生在同源序列间的重组,它通过链的断裂和再连接,在两个DNA分子同源序列间进行单链或双链片段的交换,又称基因重组。
2、细菌的基因转移与重组
接合作用、转化作用、转化作用。
3、特异位点重组
λ噬菌体DNA的整合,细菌的特异位点重组,免疫球蛋白的基因重排。
B.人工接尾法:即同聚物加尾连接法。当载体和目的基因无法采用同一种限制酶进行切断,无法得到相同得粘性末端时,可采用此方法。此法首先使用单链核酸酶将粘性末端切平,再在末端核苷酸转移酶的催化下,将脱氧核糖核苷酸添加于载体或目的基因的3'-端,如载体上添加一段polyG,则可在目的基因上添加一段polyC,故二者即可通过碱基互补进行粘合,再由DNA连接酶连接。
授课章节
第三篇 基因信息传递·第十四章 基因重组与基因工程
授课对象
2007级本科
临床专业1、2、3班
学时
4
时间
2008.11.24/30
授课地点
5315、5506、2301教室
教材
《生物化学》·第六版·人民卫生出版社
基因重组与基因工程PPT课件

不易腐烂的番茄
2、动物植物的遗传改良
抗虫植物 化学农药
兔毛棉花在我国培育成功:用兔的一种角蛋白转化棉花,棉花纤维质量好,具有兔毛般的光泽。
3、人类基因治疗
(1)体细胞基因治疗
1990年9月14日美国政府首次批准了一项基因治疗临床研究计划:对一台患有腺苷脱氨酶(ADA)缺陷的重度联合免疫缺陷症(SCID)4岁女童进行基因治疗并获得成功。该患者今年已经10岁了。从而开创了医学界的新纪元。
(三)DNA序列的复制
(一)DNA克隆技术
2、PCR技术
10.3 基因工程
(一)基因工程的基本原理和方法
基因工程的实现主要分为三个步骤: 第一步:目的基因的分离或制备:人工分离生物基因组群中目的基因及内切酶定位切割或人工酶促合成 第二步:重组DNA:选择载体及目的基因与载体基因重组 第三步:导入与表达:重组DNA导入受体细胞,目的基因表达出目的效应和性状 实现以上三步需要进行以下工作: 1) 寻找目标基因 2) 取得目标基因 3) 基因的载体问题:现主要有质粒载体、病毒载体、脂质载体、原生质载体
(2)转基因生物的生产
转基因小鼠:导入人类基因,具有较强的学习能力。在迷宫实验中,转基因鼠觅食本领比普通鼠要高许多,同时对迷宫中食物存放地点记忆更清楚。
(二) 基因工程的应用
1、特殊蛋白质的大量生产
乳汁中分泌人凝血因子IX的转基因山羊
美国转基因猪,其体内含有人类的基因,乳汁含有人体蛋白fatorⅧ。只需300~600只这样的母猪就能满足全世界对这种蛋白的需求。
人胰岛素 从猪和牛的胰脏提取,获得100g胰岛素需800-1000kg的牛胰脏。现在用基因工程方法在大肠杆菌中表达产生。 人生长激素 具有物种特异性,只能用人的生长激素来治疗侏儒症。以前从尸体脑垂体中提取,来源非常有限,现在用基因工程方法在大肠杆菌中表达产生。 干扰素 体外培养人体细胞来生产,产量低,成本高,现用重组大肠杆菌生产。
第七版生物化学名词解释

第七版生物化学名词解释第一章蛋白质的结构与功能(1)肽键:蛋白质中前一氨基酸的α-羧基与后一氨基酸的α-(2)(3)肽键平面:肽键中的C-N键具有部分双键的性质,不能旋转,因此,肽键中的C、O、N、H(4)蛋白质分子的一级结构:蛋白质分子的一级结构是指构成蛋白质分子的氨基酸在多肽链中的排列顺序和连接方式(5)(6)蛋白质的等电点:在某-pH溶液中,蛋白质分子可游离成正电荷和负电荷相等的兼性离子,即蛋白质分子的净电荷等于零,此时溶液的pH⑺蛋白质变性:在某些理化因素作用下,蛋白质特定的空间构象被破坏,从而导致其理化性质改变和生物学活性的丧失的现象。
⑻协同效应:一个亚基与其配体结合后,能影响另一亚基与配体结合的能力。
(正、负)如血红素与氧结合后,铁原子就能进入卟啉环的小孔中,继而引起肽链位置的变动。
⑼变构效应:蛋白质分子因与某种小分子物质(效应剂)相互作用而致构象发生改变,从而改变其活性的现象。
⑽分子伴侣:分子伴侣是细胞中一类保守蛋白质,可识别肽链的非天然构象,促进各功能域和整体蛋白质的正确折叠。
细胞至少有两种分子伴侣家族——热休克蛋白和伴侣素。
第二章核酸的化学结构与功能(1)核酸变性:在某些理化因素的作用下,核酸双链间氢键断裂,双螺旋解开,变成无规则的线团,此(2)DNA的复性作用:变性的DNA在适当的条件下,两条彼此分开的多核苷酸链又可重新通过氢键连接,形成原来的双螺旋结构,并恢复其原有的理化性质,此即DNA的复性。
(3)杂交:两条不同来源的单链DNA,或一条单链DNA,一条RNA,只要它们有大部分互补的碱基顺序(4)增色效应:DNA变性时,A260(5)解链温度:在DNA热变性时,通常将DNA变性50%时的温度叫解链温度用Tm表示。
(6)DNA的一级结构:DNA的一级结构是指DNA链中,脱氧核糖核苷酸的组成,排列顺序第三章酶学(1)辅酶:与酶蛋白结合的较松,用透析等方法易于与酶分开。
辅基:与酶蛋白结合的比较(2)酶的活性中心:必需基团在酶分子表面的一定区域形成一定的空间结构,直接参与了将作用物转变为产物的反应过程,这个区域叫酶的活性中心。
《生物化学》分章重点总结

生物化学分章重点总结第一章蛋白质的结构与功能蛋白质的四级结构及维持的力(考到问答题)一级:多肽链中AA残基的排列顺序, 维持的力为肽键, 二硫键。
二级:Pr中某段肽链的局部空间结构, 即该段肽链主链骨架原子的相对空间位置, 不涉及AA碱基侧链的构象, 维持的力为氢键。
三级:整条多肽链全部AA残基的相对空间位置, 其形成和稳定主要靠次级键—疏水作用, 离子键(盐键), 氢键, 范德华力。
四级:Pr中各亚基的空间排布及亚基接触部位的布局和相互作用, 维持的力主要为疏水作用, 氢键、离子键(盐键)也参与其中。
第二章核酸的结构与功能DNA一级结构:DNA分子中脱氧核糖核苷酸的种类、数目、排列顺序及连接方式。
RNA的一级结构:RNA分子中核糖核苷酸的种类、数目、排列顺序及连接方式。
hnRNA:核内合成mRNA的初级产物, 比成熟mRNA分子大得多, 这种初级mRNA分子大小不一被称为核内不均一RNA。
基因:DNA分子中具有特定生物学功能的片段。
基因组:一个生物体的全部DNA序列称为基因组。
第三章酶酶抑制剂:使酶催化活性降低但不引起酶蛋白变性的物质。
酶激活剂:使酶从无活性到有活性或使酶活性增加的物质。
酶活性单位:衡量酶活力大小的尺度, 反映在规定条件下酶促反应在单位时间内生成一定量产物或消耗一定底物所需的酶量。
变构酶:体内一些代谢产物可与某些酶分子活性中心以外部位可逆结合, 使酶发生变构并改变其催化活性, 这种调节方式为变构调节, 受变构调节的酶为变构酶。
酶的共价修饰:酶蛋白肽链上一些基团可与某种化学基团发生可逆的共价结合从而改变酶活性的过程。
阻遏作用:转录水平上减少酶生物合成的物质称辅阻遏剂, 辅阻遏剂与无活性的阻遏蛋白结合影响基因的转录的过程第四章糖代谢糖代谢的基本概况葡萄糖在体内的一系列复杂的化学反应, 在不同类型细胞内的代谢途径有所不同, 分解代谢方式还在很大程度上受氧供状况的影响:有氧氧化彻底氧化成CO2和水、糖酵解生成乳酸。
生物化学(查锡良,人卫七版)

生物化学(查锡良,人卫七版)绪论 (2)第一章蛋白质的结构与功能 (3)第二章核酸的结构与功能 (5)第三章酶 (7)第四章糖代谢 (9)第五章脂类代谢 (12)第六章生物氧化 (16)第七章氨基酸代谢 (18)第八章核苷酸代谢 (21)第九章物质代谢的联系与调节 (22)第十章DNA的生物合成 (24)第十一章RNA的生物合成 (26)第十二章蛋白质的生物合成 (28)第十三章基因表达调控 (31)第十四章基因重组与基因工程 (34)第十五章细胞信号转导 (36)第十六章血液的生物化学 (39)第十七章肝的生物化学 (42)第十八章维生素与无机物 (43)第十九章糖蛋白、蛋白聚糖和细胞外基质 (45)第二十章癌基因、抑癌基因与生长因子 (46)第二十一章常用分子生物学技术的原理及应用 (48)绪论第一节生物化学发展简史一、叙述生物化学阶段二、动态生物化学阶段三、分子生物学时期1.DNA双螺旋结构被发现2.DNA克隆使基因操作无所不能3.基因组学及其他组学的研究四、我国科学家对生物化学发展的贡献1.协和-吴宪-血液化学分析-血滤液的制备、血糖测定法、蛋白质变性学说2.刘思职-免疫化学-定量分析法研究抗原抗体反应机制3.1965年-人工合成-牛胰岛素-解出三方二锌猪胰岛素的晶体结构4.有机合成+酶促→酵母丙氨酰tRNA第二节当代生物化学研究的主要内容1.生物分子的结构与功能2.物质代谢及调节3.基因信息传递及其调控第三节生物化学与医学一、生物化学已成为生物学各学科之间、医学各学科之间相互联系的共同语言二、生物化学为推动医学各学科发展做出了重要的贡献第一章蛋白质的结构与功能第一节蛋白质的分子组成一、组成人体蛋白质的20种氨基酸属于L-α-氨基酸二、氨基酸可根据侧链结构和理化性质进行分类三、20种氨基酸具有相同或特异的理化性质(一)氨基酸具有两性解离的性质(二)含共轭双键的氨基酸具有紫外吸收性质(三)氨基酸与茚三酮反应生成蓝紫色化合物四、蛋白质是由许多氨基酸残基组成的多肽链(一)氨基酸通过肽键连接而形成肽(二)体内存在多种重要的生物活性肽1.谷胱甘肽2.多肽类激素及神经肽第二节蛋白质的分子结构一、氨基酸的排列顺序决定蛋白质的一级结构二、多肽链的局部主链构象为蛋白质二级结构(一)参与肽键形成的6个原子在同一平面上(二)α-螺旋结构是常见的蛋白质二级结构(三)β-折叠使多肽链形成片层结构(四)β-转角和无规卷曲在蛋白质分子中普遍存在(五)模体是具有特殊功能的超二级结构(六)氨基酸残基的侧链对二级结构形成的影响三、在二级结构基础上多肽链进一步折叠形成蛋白质三级结构(一)三级结构是指整条肽链中全部氨基酸残基的相对空间位置(二)结构域是三级结构层次上的局部折叠区(三)分子伴侣参与蛋白质折叠分子伴侣可分为3类:①热休克蛋白70(Hsp70)②伴侣蛋白③核质蛋白四、含有两条以上多肽链的蛋白质具有四级结构五、蛋白质的分类六、蛋白质组学(一)蛋白质组学基本概念(二)蛋白质组学研究技术平台1.双向电泳分离样品蛋白质2.蛋白质点的定位、切取3.蛋白质点得质谱分析(三)蛋白质组学研究的科学意义第三节蛋白质结构与功能的关系一、蛋白质一级结构是高级结构与功能的基础(一)一级结构是空间构象的基础(二)一级结构相似的蛋白质具有相似的高级结构与功能(三)氨基酸序列提供重要的生物进化信息(四)重要蛋白质的氨基酸序列改变可引起疾病二、蛋白质的功能依赖特定空间结构(一)血红蛋白亚基与肌红蛋白结构相似(二)血红蛋白亚基构象变化可影响亚基与氧结合(三)蛋白质构象改变可引起疾病第四节蛋白质的理化性质一、蛋白质具有两性电离性质二、蛋白质具有胶体性质三、蛋白质空间结构破坏而引起变性四、蛋白质在紫外光谱区有特征性吸收峰五、应用蛋白质呈色反应可测定蛋白质溶液含量1.茚三酮反应2.双缩脲反应第五节蛋白质的分离、纯化与结构分析一、透析及超滤法可去除蛋白质溶液中的小分子化合物二、丙酮沉淀、盐析及免疫沉淀是常用的蛋白质沉淀方法三、利用荷电性质可用电泳法将蛋白质分离四、应用相分配或亲和原理可将蛋白质进行层析分离五、利用蛋白质颗粒沉降行为不同可进行超速离心分离六、应用化学或反向遗传学方法可分析多肽链的氨基酸序列七、应用物理学、生物信息学原理可进行蛋白质空间结构测定1.同源模建2.折叠识别3.从无到有表格&示意图1.表格-氨基酸分类(结构式、英文名、三字符、一字符)2.芳香族氨基酸的紫外吸收3.GSH与GSSH之间的转换4.超二级结构与蛋白质模体(αα、βαβ、ββ、锌指结构、钙结合蛋白之螺旋-转角-螺旋)5.β-巯基乙醇及尿素对核糖核酸酶的作用6.肌红蛋白与血红蛋白的氧解离曲线7.PrP c转变为PrP sc的过程8.离子交换层析分离蛋白质9.凝胶过滤分离蛋白质肽的氨基酸末端测定法第二章核酸的结构与功能第一节核酸的化学组成及一级结构一、核苷酸是构成核酸的基本组成单位二、DNA是脱氧核苷酸通过3’,5’-磷酸二酯键连接形成的大分子三、RNA也是具有3’,5’-磷酸二酯键的线性大分子四、核酸的一级结构是核苷酸的排列顺序第二节DNA的空间结构与功能一、DNA的二级结构是双螺旋结构(一)DNA双螺旋结构的研究背景(二)DNA双螺旋结构模型要点1.DNA是反向平行、右手螺旋的双链结构2.DNA双链之间形成了互补碱基对3.疏水作用力和氢键共同维持着DNA双螺旋结构(三)DNA双螺旋结构的多样性(四)DNA的多链螺旋结构二、DNA高级结构是超螺旋结构(一)原核生物DNA的环状超螺旋结构(二)真核生物DNA高度有序和高度致密的结构三、DNA是遗传信息的物质基础第三节RNA的结构与功能一、mRNA 是蛋白质合成的模板1.大部分真核细胞mRNA的5’-末端都以7-甲基鸟嘌呤-三磷酸核苷(m7GpppN)为起始结构2.在真核生物mRNA的3’-末端,有一段由80~250个腺苷酸连接而成的多聚腺苷酸结构,称为多聚腺苷酸尾或多聚A尾3.mRNA依照自身的碱基顺序指导蛋白质氨基酸顺序的合成,也就是为氨基酸的生物合成提供模板4.mRNA的成熟过程是hnRNA 的剪接过程二、t RNA是蛋白合成的氨基酸载体1.t RNA含有多种稀有碱基2.t RNA具有茎环结构3.t RNA的3’-末端连有氨基酸4.t RNA的反密码子能够识别mRNA的密码子三、以rRNA为组分的核糖体是蛋白质合成的场所四、snmRNA参与了基因表达的调控五、核酸在真核细胞和原核细胞中表现了不同的时空特异性第四节核酸的理化性质一、核酸分子具有强烈的紫外吸收二、DNA变性是双链解离为单链的过程三、变性的核酸可以复性或形成杂交双链第五节核酸酶结构&流程图1.构成核苷酸的嘌呤和嘧啶的化学结构式2.构成核苷酸的核糖和脱氧核糖的化学结构式3.核苷和脱氧核苷的化学结构式4.核苷酸的化学结构(包括3’,5’-cAMP)5.多聚腺苷酸的化学结构式6.DNA双螺旋结构示意图(数据)7.封闭的环状DNA分子(形成超螺旋)8.真核生物DNA形成核小体的示意图9.双链DNA经历折叠、盘绕形成高度有序和高度致密染色体的示意图10.表格-真核细胞内主要RNA的种类和功能(5+3)11.成熟的真核mRNA的结构示意图12.mRNA的甲基化位点(2点)13.真核生物mRNA的帽结构及加帽过程14.真核生物mRNA多聚A尾结构的形成过程15.鸡卵清蛋白mRNA的成熟过程16.t RNA分子中含有的稀有碱基17.t RNA的二级结构和三级结构18.t RNA的反密码子与m RNA的密码子相互识别示意图19.表格-核糖体的组成(原核、真核)20.由核糖体、mRNA和t RNA形成的复合体21.真核细胞和原核细胞基因表达的时空特异性22.DNA在解链过程中表现出得增色效应23.DNA解链温度曲线24.核酸分子复性和杂交的示意图第三章酶第一节酶的分子结构与功能一、酶的分子组成中常含有辅助因子二、酶的活性中心是酶分子中执行其催化功能的部位三、同工酶是催化相同化学反应但一级结构不同的一组酶第二节酶的工作原理一、酶反应特点(一)酶反应具有极高的效率(二)酶促反应具有高度的特异性1.绝对特异性2.相对特异性3.有些酶具有立体异构特异性(三)酶促反应具有可调节性二、酶通过促进底物形成过渡态而提高反应速率(一)酶比一般催化剂更有效地降低反应活化能(二)酶和底物的结合有利于底物形成过渡态1.诱导契合作用使酶与底物密切结合2.邻近效应与定向排列使诸底物正确定位于酶的活性中心3.表面效应使底物分子去溶剂化(三)酶的催化机制呈多元催化1.酸碱催化作用:酶是两性电离的蛋白质,活性中心可为质子供体,或质子受体,参与质子转移2.共价催化作用:酶的催化基团通过形成瞬间共价键而将底物激活3.亲核催化作用:中心基团属于亲核基团,可提供电子给带正电荷的过渡态中的中间物,加速产物生成第三节酶促反应动力学一、底物浓度对反应速率影响的作图呈矩形双曲线(一)米-曼氏方程式揭示单底物反应的动力学特性(二)Km与Vm是最有意义的酶促反应动力学参数1.Km值=酶促反应速率为最大速率一半时的底物浓度2.Km值愈小,酶对底物的亲和力愈大3.Km值是酶特性常数之一,只于酶的结构、底物和反应环境(T Ph 离子强度等)有关,与酶的浓度无关4.Vmax是酶完全被底物饱和时的反应速率,与酶的浓度呈正比(三)Km值和Vmax值可以通过作图法求取二、底物足够时酶浓度对反应速率的影响呈直线关系三、温度对反应速率的影响具有双重性四、P H通过改变酶和底物分子解离状态影响反应速率五、抑制剂可逆地或不可逆地降低酶促反应速率(一)不可逆性抑制剂主要与酶共价结合(二)可逆性抑制剂与酶和(或)酶-底物复合物非共价结合1.竞争性抑制作用的抑制剂与底物竞争结合酶的活性中心2.非竞争性抑制作用的抑制剂不改变酶对底物的亲和力3.反竞争性抑制作用的抑制剂仅与酶-底物复合物结合六、激活剂可加快酶促反应速率第四节酶的调节一、调节酶实现对酶促反应速率的快调节(一)变构酶通过变构调节酶的活性(二)酶的化学修饰调节是通过某些化学基团与酶共价结合与分离实现的(三)酶原的激活使无活性的酶原转变成有催化活性的酶二、酶含量的调节包括对酶合成与分解速率的调节(一)酶蛋白合成可被诱导或阻遏(二)酶的降解与一般蛋白质降解途径相同第五节酶的分类与命名一、酶可根据其催化的反应类型予以分类:1.氧化还原酶类2.转移酶类3.水解酶类4.裂解酶类(裂合酶类,synthase):合酶属此类5.异构酶类6.合成酶类(连接酶酶,ligases)二、每一种酶均有其系统名称和推荐名称第六节酶与医学的关系一、酶和疾病密切相关(一)酶的质、量与活性的异常均可引起某些疾病(二)酶的测定有助于对许多疾病的诊断1.酶活性测定和酶活性单位是定量酶的基础2.血清酶对某些疾病的诊断具有更重要的价值(三)酶和某些疾病的治疗关系密切二、酶在医学上的应用领域广泛(一)酶作为试剂用于临床检验和科学研究1.酶法分析是以酶作为工具对化合物和酶活性进行定量分析的一种方法2.酶标记测定法是酶学与免疫学相结合的一种测定方法3.工具酶广泛地应用于分子克隆领域(二)酶的分子工程是方兴未艾的酶工程学1.固定化酶是固相酶2.抗体酶是具有酶活性的抗体结构&流程示意图1.表格-某些辅酶(辅基)在催化中的作用2.表格-几种蛋白激酶的共有序列3.底物浓度对酶促反应速率的影响4.对氨基苯甲酸-磺胺类药物5.表格-各种可逆性抑制作用的比较第四章糖代谢第一节概述一、糖的主要生理功能是氧化供能二、糖的消化吸收主要是在小肠进行三、糖代谢的概况第二节糖的无氧代谢一、糖无氧氧化反应过程分为糖酵解途径和乳酸生成两个阶段(一)葡萄糖经糖酵解途径分解为两分子丙酮酸1.葡萄糖磷酸化为6-磷酸葡萄糖2.6-磷酸葡萄糖变为6-磷酸果糖3.6-磷酸果糖转变为1,6-二磷酸果糖4.磷酸己糖裂解为2分子磷酸丙糖5.磷酸二羟丙酮转变为3-磷酸甘油醛6.3-磷酸甘油醛氧化为1,3-二磷酸甘油酸7.1,3-二磷酸甘油酸转变为3-磷酸甘油酸8.3-磷酸甘油酸转变为2-磷酸甘油酸9.2-磷酸甘油酸脱水生成磷酸烯醇式丙酮酸10.磷酸烯醇式丙酮酸将高能磷酸基转移给ADP形成ATP和丙酮酸(二)丙酮酸被还原为乳酸二、糖酵解的调控是对3个关键酶活性的调节(一)6-磷酸果糖激酶-1对调节糖酵解途径的流量最重要(二)丙酮酸激酶是糖酵解的第二个重要调节点(三)己糖激酶受到反馈调节三、糖酵解的主要生理意义是机体缺氧的情况下快速功能第三节糖的有氧氧化一、糖有氧氧化的反应过程包括糖酵解途径、丙酮酸氧化脱羧、三羧酸循环及氧化磷酸化(一)葡萄糖循糖酵解途径分解为丙酮酸(二)丙酮酸进入线粒体氧化脱羧生成乙酰CoA1.丙酮酸脱羧形成羟乙基-TPP2.由二氢硫辛酰胺转乙酰酶E2→乙酰硫辛酰胺-E23.生成乙酰CoA,E2二硫键还原为两个巯基4.二氢硫辛酰胺脱氢酶E3,脱氢生成FADH2和硫辛酰胺5.FADH2→NADPH+H+二、三羧酸循环是以形成柠檬酸为起始物的循环反应系统(一)TCA循环由8步代谢反应组成1.乙酰CoA与草酰乙酸缩合成柠檬酸2.柠檬酸经顺乌头酸转变为异柠檬酸3.异柠檬酸氧化脱羧转变为α-酮戊二酸4.α-酮戊二酸氧化脱羧生成琥珀酰CoA5.琥珀酰CoA合成酶催化底物水平磷酸化反应6.琥珀酸脱氢生成延胡索酸7.延胡索酸加水生成苹果酸8.苹果酸脱氢生成草酰乙酸(二)TCA循环受底物、产物、关键酶活性的调节1.TCA循环中有3个关键酶2.TCA循环与上游和下游的反应相协调3.TCA循环是糖、脂肪、氨基酸代谢联系的枢纽三、糖有氧氧化是机体获得ATP的主要方式四、糖有氧氧化的调节是基于能量的需求五、巴斯德效应是指糖有氧氧化抑制糖酵解的现象第四节葡萄糖的其它代谢途径一、磷酸戊糖途径生成NADPH和磷酸戊糖(一)磷酸戊糖途径的反应过程分为两个阶段1.6-磷酸葡萄糖在氧化阶段生成磷酸戊糖和NADPH2.经过基团转移反应进入糖酵解途径(二)磷酸戊糖途径主要受NADPH/NADP+比值调节(三)磷酸戊糖途径的生理意义在于生成NADPH和5-磷酸核糖1.为核酸的生物合成提供核糖2.提供NADPH作为供氢体参与多种代谢反应二、糖醛酸途径可生成葡萄糖醛酸三、多元醇途径可生成木糖醇、山梨醇等第五节糖原的合成与分解一、糖原的合成代谢主要在肝和肌组织中进行二、糖原分解产物—葡萄糖可补充血糖三、糖原的合成与分解受到彼此相反的调节(一)糖原磷酸化酶是糖原分解的关键酶(二)糖原合酶是糖原合成的关键酶四、糖原累积症是由先天性没缺陷所致第六节糖异生一、糖异生途径不完全是糖酵解的逆反应(一)丙酮酸经丙酮酸羧化支路变为磷酸烯醇式丙酮(二)1,6-二磷酸果糖转变为6-磷酸果糖(三)6-磷酸葡萄糖水解为葡萄糖二、糖异生的调节是通过对两个底物循环的调节与糖酵解调节彼此协调(一)第一个底物循环:在6-磷酸果糖和1,6-二磷酸果糖之间进行(二)第二个底物循环:磷酸烯醇式丙酮酸和丙酮酸之间进行三、糖异生的生理意义主要在于维持血糖水平恒定(一)维持血糖水平的恒定是糖异生最主要的生理作用(二)糖异生是补充或恢复肝糖原储备的重要途径(三)肾糖异生增强有利于维持酸碱平衡四、肌中产生的乳酸运输至肝进行糖异生形成乳酸循环第七节其他单糖的代谢一、果糖被磷酸化后进入糖酵解途径二、半乳糖可转变为1-磷酸葡萄糖成为糖酵解的中间代谢产物三、甘露糖可转变为6-磷酸果糖进入糖酵解途径第八节血糖及其调节一、血糖的来源和去路是相对平衡的二、血糖水平的平衡主要是受激素调节(一)胰岛素是体内唯一降低血糖的激素(二)机体在不同状态下有相应的升高血糖的激素1.胰高血糖素2.糖皮质激素可引起血糖升高3.肾上腺素是强有力的升高血糖激素三、血糖水平异常及糖尿病是最常见的糖代谢紊乱(一)低血糖是指血糖浓度低于3.0mmol/L(二)高血糖是指空腹血糖高于6.9 mmol/L(三)糖尿病是最常见的糖代谢紊乱疾病结构&流程示意图:1.糖酵解的代谢途径2.2,6-二磷酸果糖激酶-1的活性调节3.丙酮酸脱氢酶复合体作用机制4.三羧酸循环5.表格-葡萄糖有氧氧化生成的ATP6.三羧酸循环的调控7.磷酸戊糖途径8.糖醛酸途径9.分支酶的作用10.脱支酶的作用11.糖原合成、分解的共价修饰调节12.糖异生途径13.乳酸循环14.半乳糖的代谢15.甘露糖的代谢第五章脂类代谢第一节不饱和脂酸的命名及分类一、脂酸的系统命名遵循有机酸命名的原则二、脂酸主要根据其碳链长度和饱和度分类(一)脂酸根据其碳链长度分为短链、中链、长链脂酸(二)脂酸根据其碳链是否存在双键分为饱和脂酸和不饱和脂酸1.饱和脂酸的碳链不含双键2.不饱和脂酸的碳链含有一个或一个以上双键第二节脂类的消化吸收一、脂类的消化发生在脂-水界面,需要胆汁酸盐参与二、饮食脂肪在小肠被吸收第三节甘油三酯代谢一、甘油三酯是甘油的脂酸酯(一)甘油三酯是脂酸的主要储存形式(二)甘油三酯的主要作用是为机体提供能量1.甘油三酯是机体重要的能量来源2.甘油三酯是机体主要能量储存形式二、甘油三酯的分解代谢主要是脂酸的氧化(一)脂肪动员是甘油三酯分解的起始步骤(二)甘油经糖代谢途径代谢(三)脂酸经β-氧化分解功能1.脂酸的活化形式为脂酰CoA2.脂酰CoA经肉碱转运入线粒体3.脂酸的β-氧化的终产物主要是乙酰CoA(1)脱氢(2)加水(3)再脱氢(4)硫解4.脂酸氧化是体内能量的重要来源(四)脂酸的其他氧化方式1.不饱和脂酸的氧化2.过氧化物酶体的β-氧化3.奇数碳原子脂酸的氧化(五)酮体的生成及利用1.酮体在肝细胞中生成(1)2个乙酰辅酶A→乙酰乙酰辅酶A(2)乙酰乙酰辅酶A+乙酰辅酶A→HMG CoA(3)HMGCoA 裂解为乙酰乙酸和乙酰辅酶A2.酮体在肝外组织中利用3.酮体生成的生理意义4.酮体生成的调节(1)饱食及饥饿的影响(2)肝细胞糖原含量及代谢影响(3)丙二酰CoA抑制脂酰CoA进入线粒体三、脂酸在脂酸合成酶系的催化下合成(一)软脂酸的合成1.合成部位2.合成原料3.脂酸合成酶系及反应过程(1)丙二酰CoA的合成(2)脂酸合成(二)脂酸碳链的加长1.脂酸碳链在内质网中的延长2.脂酸碳链在线粒体中的延长(三)不饱和脂酸的合成(四)脂酸合成的调节1.代谢物的调节作用2.激素的调节作用四、甘油和脂酸合成甘油三酯(一)合成部位(二)合成原料(三)合成基本过程1.甘油一酯途径2.甘油二酯途径五、几种多不饱和脂酸衍生物具有重要生理功能(一)前列腺素、血栓烷、白三烯的化学结构和命名(二)PG、TX、LT的合成1.前列腺素及血栓烷的合成2.白三烯的合成(三)PG、TX、LT的生理功能1.PG的主要生理功能2.TX的主要生理功能3.LT的主要生理功能第四节磷脂代谢一、含磷酸的脂类被称为磷脂(一)由甘油构成的磷脂统称为甘油磷脂(二)由鞘氨醇或二氢鞘氨醇构成的磷脂称为鞘磷脂二、磷脂在体内具有重要的生理功能(一)磷脂是构成生物膜的重要成分1.卵磷脂存在于细胞膜中2.心磷脂是线粒体膜的主要脂质(二)磷脂酰肌醇是第二信使的前体(三)缩醛磷脂存在于脑和心组织中(四)神经鞘磷脂和卵磷脂在神经髓鞘中含量较高三、甘油磷脂的合成与降解(一)甘油磷脂的合成1.合成部位2.合成的原料及辅因子3.合成的基本过程(1)甘油二酯合成途径(2)CDP-甘油二酯合成途径(二)甘油磷脂的降解四、鞘磷脂的代谢(一)鞘氨醇的合成1.合成部位2.合成原料3.合成过程(二)神经鞘磷脂的合成(三)神经鞘磷脂的降解第五节胆固醇代谢一、胆固醇的合成原料为乙酰CoA和NADPH(一)合成部位(二)合成原料(三)合成基本过程1.甲羟戊酸的合成2.鲨烯的合成3.胆固醇的合成(四)胆固醇合成受多种因素调节1.限速酶2.饥饿与饱食3.胆固醇4.激素二、转变为胆汁酸及类固醇激素是体内胆固醇的主要去路(一)胆固醇可转变为胆汁酸(二)胆固醇可转变为类固醇激素(三)胆固醇可转化为维生素D3前体第六节血浆脂蛋白代谢一、血脂是血浆所含脂类的统称二、不同血浆脂蛋白其组成、结构均不同(一)血浆脂蛋白的分类1.电泳法2.超速离心法(二)血浆脂蛋白的组成(三)载脂蛋白(四)脂蛋白结构三、血浆脂蛋白是血脂的运输形式,但代谢和功能各异(一)乳糜微粒(二)极低密度脂蛋白(三)低密度脂蛋白(四)高密度脂蛋白四、血浆脂蛋白代谢异常导致血脂异常或高脂血症(一)高脂血症(二)动脉粥样硬化1.LDL和VLDL具有致AS作用2.HDL具有抗AS作用(三)遗传缺陷结构&流程示意图1.常见的脂酸2.甘油一酯途径3.脂肪动员4.长链脂酰CoA进入线粒体5.脂酸的β-氧化6.酮体在干细胞中的生成7.酮体的氧化8.柠檬酸-丙酮酸循环9.软脂酸的生物合成10.表格-体内几种重要的甘油磷脂11.磷脂酶对磷脂的水解12.胆固醇的生物合成13.血浆脂蛋白琼脂糖凝胶电泳示意图14.超速离心分离血浆脂蛋白示意图15.血浆脂蛋白结构示意图16.脂蛋白代谢示意图第六章生物氧化第一节生成ATP的氧化磷酸化体系一、氧化呼吸链是一系列有电子传递功能的氧化还原组分(一)氧化呼吸链由4种具有传递电子能力的复合体组成1.复合体Ⅰ作用是将NADPH+H+中的电子传递给泛醌2.复合体Ⅱ作用是将电子从琥珀酸传递到泛醌3.复合体Ⅲ作用是将电子从还原型泛醌传递给细胞色素C4.复合体Ⅳ将电子从细胞色素C传递给氧(二)氧化呼吸链组分按氧化还原电位由低到高的顺序排列二、氧化磷酸化将氧化呼吸链释能与ADP磷酸化生成ATP偶联(一)氧化磷酸化偶联部位在复合体Ⅰ、Ⅲ、Ⅳ内1.P/O比值2.自由能变化(二)氧化磷酸化偶联机制是产生跨线粒体内膜的质子梯度(三)质子顺梯度回流释放能量被ATP合酶利用催化ATP合成三、氧化磷酸化作用可受某些内外源因素影响(一)有3类氧化磷酸化抑制剂1.呼吸链抑制剂阻断氧化磷酸化的电子传递过程2.解偶联剂破坏电子传递建立的跨膜质子电化学梯度3.ATP合酶抑制剂同时抑制电子传递和ATP的生成(二)ADP是调节正常人体氧化磷酸化速率的主要因素(三)甲状腺激素刺激机体耗氧量和产热同时增加(四)线粒体DNA突变可影响机体氧化磷酸化功能四、ATP在能量的生成、利用、转移和储存中起核心作用五、线粒体内膜对各种物质进行选择性转运(一)胞质中NADH通过穿梭机制进入线粒体氧化呼吸链1.α-磷酸甘油穿梭主要存在于脑和骨骼肌中2.苹果酸-天冬氨酸穿梭主要存在于肝和心肌中(二)ATP-ADP转位酶促进ADP进入和ATP移出紧密偶联第二节其他不生成ATP的氧化体系一、抗氧化酶体系有清除反应活性氧类的功能二、微粒体细胞色素P450单加氧酶催化底物分子羟基化结构&流程示意图1.表格-人线粒体呼吸链复合体2.电子传递链各复合体位置示意图3.化学渗透假说示意图4.ATP合酶结构和质子的跨内膜流动机制模式图5.ATP合酶的工作机制6.不同底物和抑制剂对线粒体氧耗的影响。
生物化学-考研-题库-答案学习资料

生物化学-考研-题库-答案学习资料目录第一章蛋白质的结构与功能 (2)第二章核酸的结构与功能 (16)第三章酶 (25)第四章糖代谢 (36)第五章脂类代谢 (49)第六章生物氧化 (62)第七章氨基酸代谢 (71)第八章核苷酸代谢 (80)第九章物质代谢的联系与调节 (86)第十章 DNA生物合成 ---- 复制 (93)第十一章 RNA的生物合成----转录 (103)第十二章蛋白质的生物合成---- 翻译 (110)第十三章基因表达调控 (119)第十四章基因重组与基因工程 (128)第十五章细胞信息转导 (136)第十六章肝的生物化学 (151)第十七章维生素与微量元素 (162)第十八章常用分子生物学技术的原理及其应用 (166) 第十九章水和电解质代谢 (171)第二十章酸碱平衡 (175)第一章蛋白质的结构与功能一. 单项选择题1. 下列不含有手性碳原子的氨基酸是A. GlyB. ArgC. MetD. Phe2. 那一类氨基酸在脱去氨基后与三羧酸循环关系最密切A. 碱性氨基酸B. 含硫氨基酸C. 分支氨基酸D. 酸性氨基酸E. 芳香族氨基酸3. 一个酸性氨基酸,其pH a1=2.19,pH R=4.25,pH a2=9.67,请问其等电点是A. 7.2B. 5.37C. 3.22D. 6.5E. 4.254. 下列蛋白质组分中,那一种在280nm具有最大的光吸收A. 酪氨酸的酚环B. 苯丙氨酸的苯环C. 半胱氨酸的巯基D. 二硫键E. 色氨酸的吲哚环5. 测定小肽氨基酸序列的最好办法是A. 2,4-二硝基氟苯法B. 二甲氨基萘磺酰氯法C. 氨肽酶法D. 苯异硫氰酸酯法E. 羧肽酶法6. 典型的α-螺旋含有几个氨基酸残基A. 3B. 2.6C. 3.6E. 4.47. 每分子血红蛋白所含铁离子数为A. 5B. 4C. 3D. 2E. 18. 血红蛋白的氧合曲线呈A. U形线B. 双曲线C. S形曲线D. 直线E. Z形线9. 蛋白质一级结构与功能关系的特点是A. 氨基酸组成不同的蛋白质,功能一定不同B. 一级结构相近的蛋白质,其功能类似可能性越大C. 一级结构中任何氨基酸的改变,其生物活性即消失D. 不同生物来源的同种蛋白质,其一级结构相同E. 以上都不对10. 在中性条件下,HbS与HbA相比,HbS的静电荷是A. 减少+2B. 增加+2C. 增加+1D. 减少+1E. 不变11. 一个蛋白质的相对分子量为11000,完全是α-螺旋构成的,其分子的长度是多少nmA. 11B. 110D. 15E. 110012. 下面不是空间构象病的是A. 人文状体脊髓变性病B. 老年痴呆症C. 亨丁顿舞蹈病D. 疯牛病E. 禽流感13. 谷胱甘肽发挥功能时,是在什么样的结构层次上进行的A. 一级结构B. 二级结构C. 三级结构D.四级结构E. 以上都不对14. 测得某一蛋白质样品的含氮量为0.40g,此样品约含蛋白质多少克A. 2.00gB. 2.50gC. 6.40gD. 3.00gE. 6.25g15. 在pH6.0的缓冲液中电泳,哪种氨基酸基本不动A. 精氨酸B. 丙氨酸C. 谷氨酸D. 天冬氨酸E. 赖氨酸16. 天然蛋白质不存在的氨基酸是A. 半胱氨酸B. 脯氨酸C. 丝氨酸D. 蛋氨酸E. 瓜氨酸17. 多肽链中主链骨架的组成是A. -NCCNNCCNNCCN-B. ―CHNOCHNOCHNO―C. ―CONHCONHCONH―D. ―CNOHCNOHCNOH―E. ―CNHOCCCNHOCC―18. 在20种基本氨基酸中,哪种氨基酸没有手性碳原子A. 谷氨酸B. 半胱氨酸C. 赖氨酸D. 组氨酸E.甘氨酸19. 下列哪种物质从组织提取液中沉淀蛋白质而不变性A. 硫酸B. 硫酸铵C. 氯化汞D. 丙酮E. 1N盐酸20. 蛋白质变性后表现为A. 粘度下降B. 溶解度增加C. 不易被蛋白酶水解D. 生物学活性丧失E. 易被盐析出现沉淀21. 对蛋白质沉淀、变性和凝固的关系的叙述,哪项是正确的A. 变性的蛋白质一定要凝固B. 变性的蛋白质一定要沉淀C. 沉淀的蛋白质必然变性D. 凝固的蛋白质一定变性E. 沉淀的蛋白质一定凝固22. 蛋白质溶液的稳定因素是A. 蛋白质溶液有分子扩散现象B. 蛋白质溶液有“布朗运动”C. 蛋白质分子表面带有水化膜和同种电荷D. 蛋白质的粘度大E. 蛋白质分子带有电荷23. 镰刀型贫血症患者,Hb中氨基酸的替换及位置是A. α-链第六位Val换成GluB. β-链第六位Val换成GluC.α-链第六位Glu换成ValD. β-链第六位Glu换成ValE. 以上都不对24. 下列蛋白质通过凝胶过滤层析柱时,最先被洗脱的是A.牛β乳球蛋白(分子量35000)B. 肌红蛋白(分子量16900)C. 牛胰岛素(分子量5700)D. 血清清蛋白(分子量68500)E. 超氧化物歧化酶(分子量32000)25.下列哪一种物质不属于生物活性肽A. 催产素B. 加压素C. 促肾上腺皮质激素D. 血红素E. 胰岛素26.下列不属于结合蛋白质的是A.核蛋白B. 糖蛋白C. 脂蛋白D. 清蛋白E.色蛋白27. 可用于裂解多肽链中蛋氨酸羧基侧形成的肽键的试剂是A. 甲酸B. 羟胺C. 溴化氰D.β-巯基乙醇E. 丹磺酰氯二. 多项选择题1. 下列氨基酸那些是蛋白质的组分A. HisB. TrpC. 瓜氨酸D. 胱氨酸2. 下列氨基酸中那些具有分支的碳氢侧链A. MetB. CysC. ValD. Leu3. 在生理pH值情况下,下列氨基酸中的那些氨基酸侧链带正电荷A. ArgB. GluC. LysD. Asp4.下列对于肽键的叙述正确的是A. 具有部分双键性质B. 具有部分单键性质C. 比双键键长长,比单键键长短D.比双键键长短,比单键键长长5. 对谷胱甘肽叙述正确的是A. 有一个γ-肽键B. 有一个功能性的基团-巯基C. 分别由谷氨酸胱氨酸和甘氨酸组成D. 对生物膜具有保护作用6. 下面那些是结合蛋白质A. 血红蛋白B. 牛胰核糖核酸酶C. 肌红蛋白D. 胰岛素7. 下列那些蛋白质具有四级结构A. 血红蛋白B. 牛胰核糖核酸酶C. 肌红蛋白D. 蛋白激酶A8. 含有卟啉环的蛋白质是A. 血红蛋白B. 过氧化氢酶C. 肌红蛋白D. 细胞色素9. 下列那些蛋白质含有铁离子A. 血红蛋白B. 牛胰核糖核酸酶C. 肌红蛋白D. 胰岛素10. 蛋白质变性是由于A. 氢键断裂B. 肽键破坏C. 破坏水化层和中和电荷D. 亚基解聚11. 镰刀型红细胞贫血症患者血红蛋白β-链上第六位的谷氨酸被缬氨酸所取代后,将产生那些变化A.在pH7.0电泳时增加了异常血红蛋白向阳极移动的速度B.导致异常脱氧血红蛋白的聚合作用C.增加了异常血红蛋白的溶解度D.一级结构发生改变12. 下面有哪些蛋白质或酶能协助蛋白质正确折叠A. 分子伴侣B. 牛胰核糖核酸酶C. 胰岛素D. 伴侣素13. 下列哪些肽分子一级组成极相近,而且属于寡肽A. 脑啡肽B.催产素C. 加压素D. 促肾上腺皮质激素14. 下面对氨基酸与蛋白质之间的关系叙述正确的是A. 氨基酸具有的性质蛋白质也一定具有B. 有些氨基酸的性质蛋白质也具有C.有些蛋白质的性质氨基酸不具有D.两者之间的性质关系并不紧密15. 肽键平面中能够旋转的键有A. C=OB. C-NC. Cα-ND. Cα-C16. 对血红蛋白的结构特点叙述正确的是A. 具有4个亚基B. 是一种结合蛋白质C. 每个亚基都具有三级结构D. 亚基键主要靠次级键连接三. 填空题1. 组成蛋白质的碱性氨基酸有、和。
(二)目的基因与载体的连接

P
5`
3`
3`
OH
5`
连接酶
5`
3`
3`
5`
3、逆转录酶
(一)概述 逆转录酶也称反转录酶或RNA依赖的DNA聚合酶 ( RNA dependent DNA polymerase,RDDP ) 。 是 由 Baltimove从鼠白血病病毒(murine leukemia virus,MLV)和 Mizutan从 劳氏 肉瘤 病 毒 (Rous sarcoma virus,RSV) 中, 于 1970 年 分 别 各 自 发 现 的 , 这 两 个 小 组 论 文 同 时 在 同 一 期 Nature上,可见其意义。该酶在逆转录病毒(retro virus)生 产循环中起主宰作用。
教学内容
1.工具酶 ①限制性核酸内切酶;②修饰酶(DNA聚合酶、逆转录酶、 T4DNA聚合酶、末端脱氧核苷酸转移酶。) 2.载体 ①常用的克隆载体(质粒、噬菌体、病毒);②表达载体 3.重组DNA技术的基本过程 ①目的基因的制备 ②载体的选择和制备 ③DNA的体外连接 ④将外源DNA导入宿生细胞 ⑤目的基因的筛选和鉴定 4.克隆基因的表达 ①克隆基因在大肠杆菌中的表达 ②克隆基因在哺乳动物细胞中的表达基Βιβλιοθήκη 基因工程因 有 关 的
分子杂交 聚合酶链反应 DNA序列测定
操
转基因动物
作
克隆动物
技
基因剔除技术
术
基因诊断和基因治疗
第一节 基因工程
重组DNA技术的发展史
1865年 G.J.Mendel的豌豆杂交试验 1944年 O.T.Avery的肺炎球菌转化实验 1973年 美国斯坦福大学的科学家构建第一个重组DNA分子 1977年 美国南旧金山由博耶和斯旺森建立世界上第一家遗传工
第十四章基因工程与蛋白质工程

限制性核酸内切酶
w 同裂酶:来源不同,但有相同的识别序列.或称 异源同工酶.
w 同切点酶:不仅识别序列相同,而且切点也相同.
w 同尾酶:酶的识别序列不完全相同,但切出的粘 性末端相同.
第十切酶的作用位点
第十四章基因工程与蛋白质工程
几种限制性内切酶的作用位点
第十四章基因工程与蛋白质工程
点,以便所要克隆的DNA片段能被插入载体.
第十四章基因工程与蛋白质工程
克隆载体
w 3、外源DNA片段插入载体后,不得使载体 的复制功能丧失.
w 4、具有某种明显的标志,例如抗药性标记, 以便利用这些标志筛选阳性克隆.
w 5、携带外源DNA的幅度较宽. w 6、生物防护是安全的.
第十四章基因工程与蛋白质工程
第十四章基因工程与蛋白质工程
限制性核酸内切酶
w 能识别DNA特定核苷酸序列的核酸内切 ➢ 酶分类:三类. 命名: EcoRI
➢ 分布:主要来源于原核生物。 ➢ 特点:特异性,即识别特定核苷酸序列,
切割特定切点。 ➢ 结果:产生黏性未端(碱基互补配对)或平
端。 ➢ 举例:大肠杆菌的一种限制酶能识别
GAATTC序列,并在G和A之间切开。
基团及其空间取向。 w 专一性设计:指功能性蛋白质在发挥其生理功能的时,
总是与其他分子发生专一性相互作用。 w 框架设计:是指对蛋白质分子的立体设计。 w (二)、定点突变技术 w 通过删除或置换DNA片段中的核苷酸,使基因发生改变,
从而产生新的蛋白质。 w 改变DNA核苷酸序列的几种方法: w 1.基因的化学合成. w 2.基因直接修饰法. w 3.盒式突变技术.
w 主要步骤: 1.带有目的基因的DNA片段的获得; 2、构建DNA重组分子; 3、重组DNA分子引入宿主细胞和筛选鉴定; 4、基因的表达.
第七版生物化学名词解释

第七版生物化学名词解释第一章蛋白质的结构与功能(1)肽键:蛋白质中前一氨基酸的α-羧基与后一氨基酸的α-氨基脱水形成的酰胺键。
(2)多肽链:由许多氨基酸借肽键连接而形成的链状化合物。
(3)肽键平面:肽键中的C-N键具有部分双键的性质,不能旋转,因此,肽键中的C、O、N、H 四个原子处于一个平面上,称为肽键平面。
(4)蛋白质分子的一级结构:蛋白质分子的一级结构是指构成蛋白质分子的氨基酸在多肽链中的排列顺序和连接方式。
(5)亚基:在蛋白质分子的四级结构中,每一个具有三级结构的多肽链单位,称为亚基。
(6)蛋白质的等电点:在某-pH溶液中,蛋白质分子可游离成正电荷和负电荷相等的兼性离子,即蛋白质分子的净电荷等于零,此时溶液的pH值称为该蛋白质的等电点。
⑺蛋白质变性:在某些理化因素作用下,蛋白质特定的空间构象被破坏,从而导致其理化性质改变和生物学活性的丧失的现象。
⑻协同效应: 一个亚基与其配体结合后,能影响另一亚基与配体结合的能力。
(正、负)如血红素与氧结合后,铁原子就能进入卟啉环的小孔中,继而引起肽链位置的变动。
⑼变构效应: 蛋白质分子因与某种小分子物质(效应剂)相互作用而致构象发生改变,从而改变其活性的现象。
⑽分子伴侣:分子伴侣是细胞中一类保守蛋白质,可识别肽链的非天然构象,促进各功能域和整体蛋白质的正确折叠。
细胞至少有两种分子伴侣家族——热休克蛋白和伴侣素。
第二章核酸的化学结构与功能(1) 核酸变性:在某些理化因素的作用下,核酸双链间氢键断裂,双螺旋解开,变成无规则的线团,此种作用称核酸的变性。
(2) DNA的复性作用:变性的DNA在适当的条件下,两条彼此分开的多核苷酸链又可重新通过氢键连接,形成原来的双螺旋结构,并恢复其原有的理化性质,此即DNA的复性。
(3) 杂交:两条不同来源的单链DNA,或一条单链DNA,一条RNA,只要它们有大部分互补的碱基顺序,也可以复性,形成一个杂合双链,此过程称杂交。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第十四章基因重组和基因工程
一、自然界的基因转移和重组:
基因重组(gene recombination)是指DNA片段在细胞内、细胞间,甚至在不同物种之间进行交换,交换后的片段仍然具有复制和表达的功能。
1.接合作用:当细胞与细胞相互接触时,DNA分子即从一个细胞向另一个细胞转移,这种遗传物质的转移方式称为接合作用(conjugation)。
2.转化和转染:由外来DNA引起生物体遗传性状改变的过程称为转化(transformation)。
噬菌体常常可感染细菌并将其DNA注入细菌体内,也可引起细菌遗传性状的改变。
通过感染方式将外来DNA引入宿主细胞,并导致宿主细胞遗传性状改变的过程称为转染(transfection)。
转染是转化的一种特殊形式。
3.整合和转导:外来DNA侵入宿主细胞,并与宿主细胞DNA进行重组,成为宿主细胞DNA的一部分,这一过程称为整合。
整合在宿主细胞染色体DNA中的外来DNA,可以被切离出来,同时也可带走一部分的宿主DNA,这一过程称为转导(transduction)。
来源于宿主DNA的基因称为转导基因。
4.转座:转座又称为转位(transposition),是指DNA的片段或基因从基因组的一个位置转移到另一个位
置的现象。
这些能够在基因组中自由游动的DNA片段包括插入序列和转座子两种类型。
⑴插入序列:典型的插入序列(insertion sequence,IS)是长750-1500bp的DNA片段,由两个分离的反向重复序列和一个转座酶基因。
当转座酶基因表达时,即可引起该序列的转座。
其转座方式主要有保守性转座和复制性转座。
⑵转座子:转座子(transposons)是可从一个染色体位点转移到另一个位点的分散的重复序列,含两个反向重复序列、一个转座酶基因和其他基因(如抗生素抗性基因)。
免疫球蛋白重链基因由一组可变区基因(VH)和一组恒定区基因(CH)构成,通过这些基因的选择性转座和重组,就可以转录表达出各种各样的免疫球蛋白重链,以对付不同的抗原。
5.基因重组的方式:
⑴位点特异性重组:在整合酶的催化下,两段DNA序列的特异的位点处发生整合并共价连接,称为位点特异性重组。
⑵同源重组:发生在同源DNA序列之间的重组称为同源重组(homologous recombination)。
这种重组方式要求两段DNA序列类似,并在特定的重组蛋白或酶的作用下完成。
二、重组DNA技术:
重组DNA技术又称为基因工程(genetic engineering)或分子克隆(molecular cloning),是指采用人工方法将不同来源的DNA进行重组,并将重组后的DNA引入宿主细胞中进行增殖或表达的过程。
1.载体和目的基因的分离(分):对载体DNA和目的基因分别进行分离纯化,得到其纯品。
⑴载体:常用的载体(vector)主要包括质粒(plasmid)、噬菌体(phage)和病毒(virus)三大类。
这些载体均需经人工构建,除去致病基因,并赋予一些新的功能,如有利于进行筛选的标志基因、单一的限制酶切点等。
①质粒:是存在于天然细菌体内的一种独立于细菌染色体之外的双链环状DNA,具有独立复制的能力,通常带有细菌的抗药基因。
②噬菌体:可通过转染方式将其DNA送入细菌体内进行增殖。
常用的为人工构建的λ噬菌体载体,当目的基因与噬菌体DNA进行重组时,可采用插入重组方式,也可采用置换重组方式。
③病毒:常用的为SV40,通过感染方式将其DNA送入哺乳动物细胞中进行增殖。
⑵目的基因:①直接从染色体DNA中分离:仅适用于原核生物基因的分离。
②人工合成:根据已知多肽链的氨基酸顺序,利用遗传密码表推定其核苷酸顺序再进行人工合成。
适应于编码小分子多肽的基因。
③从mRNA合成cDNA:采用一定的方法钓取特定基因的mRNA,再通过逆转录酶催化合成其互补DNA(cDNA),除去RNA链后,再用DNA聚合酶合成其互补DNA链,从而得到双链DNA。
④从基因文库中筛选:将某一种基因DNA用适当的限制酶切断后,与载体DNA重组,再全部转化宿主细胞,得到含全部基因组DNA的种群,称为G文库(genomic DNA library)。
将某种细胞的全部mRNA通过逆转合成cDNA,然后转化宿主细胞,得到含全部表达基因的种群,称为C-文库(cDNA library)。
C-文库具有组织细胞特异性。
⑤利用PCR合成:如已知目的基因两端的序列,则可采用聚合酶链反应
(polymerase chain reaction, PCR)技术,在体外合成目的基因。
2.载体和目的基因的切断(切):通常采用限制性核酸内切酶(restriction endonuclease),简称限制酶,分别对载体DNA和目的基因进行切断,以便于重组。
能够识别特定的碱基顺序并在特定的位点降解核酸的核酸内切酶称为限制酶。
限制酶所识别的顺序往往为4-8个碱基对,且有回文结构。
由限制酶切断后的末端可形成平端、3'-突出粘性末端和5'-突出粘性末端三种情况。
形成粘性末端(cohesive end)者较有利于载体DNA和目的基因的重组。
3.载体和目的基因的重组(接):即将带有切口的载体与所获得的目的基因连接起来,得到重新组合后的DNA分子。
⑴粘性末端连接法:载体与目的基因通过粘性末端进行互补粘合,再加入DNA连接酶,即可封闭其缺口,得到重组体。
⑵人工接尾法:即同聚物加尾连接法。
在末端核苷酸转移酶的催化下,将脱氧核糖核苷酸添加于载体或目的基因的3'-端,如载体上添加一段polyG,则可在目的基因上添加一段polyC,通过碱基互补进行粘合后,再由DNA连接酶连接。
⑶人工接头连接法:将人工连接器(即一段含有多种限制酶切点的DNA片段)连接到载体和目的基因上,即有可能使用同一种限制酶对载体和目的基因进行切断,得到可以互补的粘性末端。
4.重组DNA的转化和扩增(转):将重组DNA导入宿主细胞进行增殖或表达。
重组质粒可通过转化方式导入宿主细胞,λ噬菌体作为载体的重组体,则需通过转染方式将重组噬菌体DNA导入大肠杆菌等宿主细胞。
重组DNA导入宿主细胞后,即可在适当的培养条件下进行培养以扩增宿主细胞。
5.重组DNA的筛选和鉴定(筛):对含有重组体的宿主细胞进行筛选并作鉴定。
⑴根据重组体的表型进行筛选:对于带有抗药基因的质粒重组体,可采用插入灭活法进行筛选。
⑵根据标志互补进行筛选:当宿主细胞存在某种基因及其表达产物的缺陷时,可采用此方法筛选重组体。
即在载体DNA分子中插入相应的缺陷基因,如宿主细胞重新获得缺陷基因的表达产物,则说明该细胞中带有重组体。
⑶根据DNA限制酶谱进行分析:经过粗筛后的含重组体的细菌,还需进行限制酶谱分析进一步鉴定。
⑷用核酸杂交法进行分析鉴定:采用与目的基因部分互补的DNA片段作为探针,与含有重组体的细菌菌落进行杂交,以确定重组体中带目的基因。
获得带目的基因的细菌后,可将其不断进行增殖,从而得到大量的目的基因片段用于分析研究。
如在目的基因的上游带有启动子顺序,则目的基因还可转录表达合成蛋白质。
