《2018年度药品审评报告》附件3:2018年审评通过的优先审评药品名单
国家药品监督管理局2018年第6号公告附件

3.各级心力衰竭
对于症状性心衰病人,本品也适用于:提高生存率;延缓心衰的进展;减少因心衰而导致的住院。
4.预防症状性心衰
对于无症状性左心室功能不全病人,本品适用于:延缓症状性心衰的进展;减少因心衰而导致的住院。
5.预防左心室功能不全病人冠状动脉缺血事件,本品适用于:减少心肌梗死的发生率;减少不稳定型心绞痛所导致的住院。
南京正大天晴制药有限公司
国药准字H20057227
否
7
CYHB1750014
阿奇霉素片
Azithromycin Tablets
0.5 g
片剂
本品适用于敏感细菌所引起的下列感染:支气管炎、肺炎等下呼吸道感染;皮肤和软组织感染;急性中耳炎;鼻窦炎、咽炎、扁桃体炎等上呼吸道感染(青霉素是治疗化脓性链球菌咽炎的常用药,也是预防风湿热的常用药物。阿奇霉素可有效清除口咽部链球菌,但目前尚无阿奇霉素治疗和预防风湿热疗效的资料)。阿奇霉素可用于男女性传播疾病中由沙眼衣原体所致的单纯性生殖器感染。阿奇霉素亦可用于由非多重耐药淋球菌所致的单纯性生殖器感染及由杜克嗜血杆菌引起的软下疳(需排除梅毒螺旋体的合并感染)。
急性冠脉综合征的患者
非ST段抬高性急性冠脉综合征(包括不稳定性心绞痛或非Q波心肌梗死),包括经皮冠状动脉介入术后置入支架的患者,与阿司匹林合用。
用于ST段抬高性急性冠脉综合征患者,与阿司匹林联合,可合并在溶栓治疗中使用。
深圳信立泰药业股份有限公司
国药准字H20000542
是
4
CYHB1703441
马来酸依那普利片
1.溶血链球菌、肺炎链球菌、葡萄球菌或流感嗜血杆菌所致中耳炎、鼻窦炎、咽炎、扁桃体炎等上呼吸道感染。
2.大肠埃希菌、奇异变形杆菌或粪肠球菌所致的泌尿生殖道感染。
2018年FDA批准上市的505b2药物清单
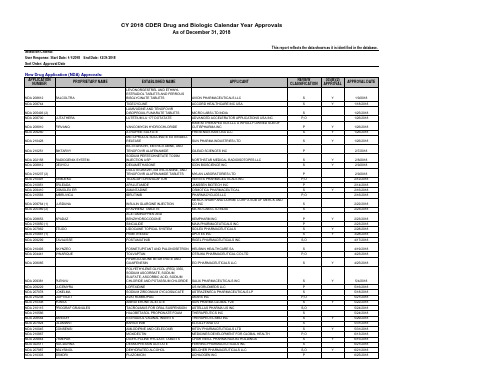
AKARX INC SUN PHARMA GLOBAL FZE ASTELLAS PHARMA US INC THERAPEUTICS INC THERAPEUTICSMD INC ELI LILLY AND CO KITOV PHARMACEUTICALS LTD
MOXIDECTIN DOXYCYCLINE HYCLATE TABLETS DESMOPRESSIN ACETATE
S
PIMAVANSERIN
ACADIA PHARMACEUTICALS INC
S
ARIPIPRAZOLE LAUROXIL
ALKERMES INC
S
FULVESTRANT
FRESENIUS KABI USA LLC
S
ATROPINE
RAFA LABORATORIES LTD
P
VANCOMYCIN HYDROCHLORIDE
S,O
Y
6/21/2018
P
6/25/2018
NDA 210365 NDA 210496 NDA 210498 NDA 210361 NDA 210793 NDA 209830 NDA 210326 (1) NDA 212319 NDA 209481 NDA 210997 NDA 208627
NDA 208313
NDA 207356 NDA 209863 NDA 209521 NDA 209816
ANNOVERA ONPATTRO
CEQUA
DIACOMIT DIACOMIT
INVELTYS ALTRENO XERAVA
LUTRATE DEPOT
PIFELTRO
DELSTRIGO TIGLUTIK CASSIPA XELPROS SEIZALAM COPIKTRA VIZIMPRO
医药年报:中国2018年通过仿制药质量和疗效一致性评价品种统计(十一)

243 盐酸西替利嗪片
lOmg 新华制药(高密)有限公司
国药准字H19990095
244 盐酸左西替利嗪片
5mg 重庆华邦制药有限公司
国药准字H20040249
245 盐酸左西替利嗪片
5mg 湖南九典制药股份有限公司
国药准字H20084566
246 盐酸左西替利嗪片
5mg 北京天衡药物研究院南阳天衡制药厂
255 吲达帕胺片
2.5mg 重庆药友制药有限责任公司
国药准字H50021320
256 吲达帕胺片
2.5mg 广东安诺药业股份有限公司
国药准字H44020885
257 注射用阿奇霉素
0.5g 海南普利制药股份有限公司
国25g 浙江京新药业股份有限公司
国药准字H20143177
中国2018年通过仿制药质量和疗效一致性评价品种统计(十一)
序号 药品名称
规格 企业名称
批准文号/注册证号
237 盐酸舍曲林片
50mg 浙江京新药业股份有限公司
国药准字H20051076
238 盐酸坦索罗辛缓释胶囊 0.2mg 江苏恒瑞医药股份有限公司
国药准字H20050392
239 盐酸特比萘芬片
国药准字H42021547
251 异烟肼片
0.1g 沈阳红旗制药有限公司
国药准字H21022350
252 异烟胼片
0.1g 宜昌人福药业有限责任公司
国药准字H42022005
253 异烟胼片
0.1g 广东华南药业集团有限公司
国药准字H44020699
254 异烟肼片
0.3g 沈阳红旗制药有限公司
国药准字H21022351
0.125g 齐鲁制药有限公司
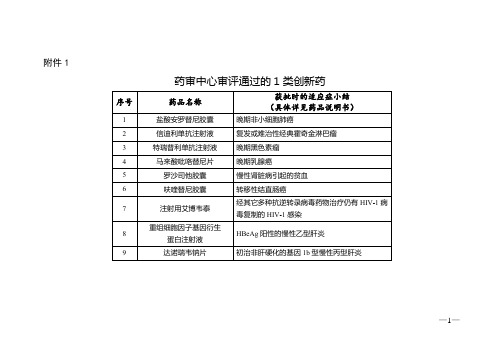
《2018年度药品审评报告》附件1:药审中心审评通过的1类创新药
8
重组细胞因子基因衍生
蛋白注射液
HBeAg阳性的慢性乙型肝炎
9
达诺瑞韦钠片
初治非肝硬化的基因1b型慢性丙型肝炎
附件1
药审中心审评通过的1类创新药
序号
药品名称
获批时的适应症小结
(具体详见药品说明书)
1
盐酸安罗替尼胶囊
晚期非小细胞肺癌
2
信迪利单抗注射液
复发或难治性经典霍奇金淋巴瘤
3
特瑞普利单抗注射液
晚期黑色素瘤
4
马来酸吡咯替尼片
晚期乳腺癌
5
罗沙司他胶囊
慢性肾7
注射用艾博韦泰
2018年,中国批准了这些重磅新药,抗癌药稳站C位!

2018年,中国批准了这些重磅新药,抗癌药稳站C位!2018年已接近尾声,一大波进口和国产新药借助优先审评快速获批上市,给我们带来一个又一个惊喜,也为广大国内患者带来新的选择与希望。
2018年国内到底有哪些重磅新药获批上市?汉鼎好医友为您梳理如下:5月盐酸安罗替尼胶囊:自主研发的1.1类抗癌新药商品名:福可维生产商:正大天晴适应症:非小细胞肺癌盐酸安罗替尼是在同类药物索拉非尼的基础上改构而成,通过抑制肿瘤新生血管生成和生长增殖信号通路发挥抗肿瘤作用。
这是一款100%原研新药,临床实验中明显提高了晚期非小细胞肺癌患者的总生存期。
据悉,该药是正大天晴药业迄今为止投入最大的一个产品,标志着“首仿之王”正大天晴迈出仿制药舒适圈的重要一步,同时也是该公司第一个按照国际研发流程和标准进行研发的创新小分子药。
安罗替尼的面世,将有效填补晚期非小细胞型肺癌三线治疗的空白。
6月纳武利尤单抗注射液:国内上市的首个以PD-1为靶点的单抗药物商品名:Opdivo生产商:百时美施贵宝适应性:二线治疗非小细胞肺癌Opdivo是全球首个上市的PD-1/PD-L1抑制剂,和传统的化疗和靶向治疗不同,主要是通过克服患者体内的免疫抑制,重新激活患者自身的免疫细胞来杀伤肿瘤,是一种全新的抗肿瘤治疗理念.该药于2014年首次获FDA批准用于治疗黑色素瘤,迄今已有包括黑色素瘤、非小细胞肺癌、结直肠癌、肝细胞癌在内的8个适应症获批。
江湖人称“O药”,被不少癌症患者誉为“抗癌神药”。
Opdivo在我国已被批准用于治疗表皮生长因子受体(EGFR)基因突变阴性和间变性淋巴瘤激酶(ALK)阴性、既往接受过含铂方案化疗后疾病进展或不可耐受的局部晚期或转移性非小细胞肺癌(NSCLC)成人患者。
7月艾博韦泰长效注射剂:我国首个自主研发抗艾新药商品名:艾可宁生产商:前沿生物适应症:抗HIV-1 病毒艾博卫泰,前沿生物药业自主研发的1类新药,同时也是全球第一个长效抗艾滋病药物。
医药年报:中国2018年批准新药统计(化学药品.中成药和生物制品)(四)

罗沙司他胶囊
H20180024
关黄母颗粒
Z20180001
金蓉颗粒
Z20180002
A群C群脑膜炎球菌多糖疫苗
S20180001
重组细胞因子基因衍生蛋白注射液
S20180002
重组人胰岛素注射液
S20180003
硫培非格司亭注射液
S20180004
狂犬病人免疫球蛋白
S20180005
四价流感病毒裂解疫苗
S20180013
Ⅰ型Ⅲ型脊髄灰质炎减毒活疫苗糖丸(人二倍体细胞)
S20180014
特瑞普利单抗注射液
S20180015
信迪利单抗注射液
S20180016
摘编自《中国医药统计年报2018·综合册》
学药品.中成药和生物制品)(四) 申请单位 四川海思科制药有限公司 四川海思科制药有限公司 珐博进(中国)医药技术开发有限公司 珐博进(中国)医药技术开发有限公司 通化万通药业股份有限公司 广州市康源药业有限公司 华兰生物疫苗有限公司 杰华生物技术(青岛)有限公司 合肥天麦生物科技发展有限公司 江苏恒瑞医药股份有限公司 河北大安制药有限公司 华兰生物疫苗有限公司 长春长生生物科技有限责任公司 北京凯因科技股份有限公司 北京民海生物科技有限公司 河北大安制药有限公司 艾美卫信生物药业(浙江)有限公司 中国医学科学院医学生物学研究所 中国医学科学院医学生物学研究所 中国医学科学院医学生物学研究所 苏州众合生物医药科技有限公司 信达生物制药(苏州)有限公司
S20180006
四价流感病毒裂解疫苗
S20180007
培集成干扰素α-2注射液
S20180008
23价肺炎球菌多糖疫苗
S20180009
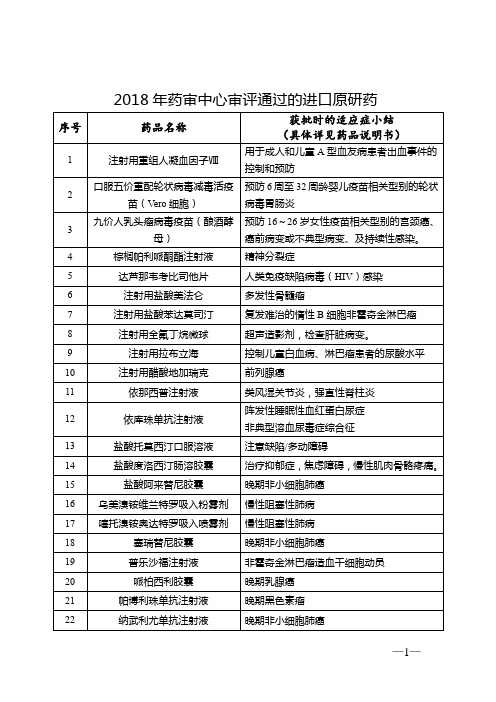
2018年药审中心审评通过的进口原研药
雷珠单抗注射液
脉络膜新生血管导致的视力损害
63
阿柏西普眼内注射溶液
新生血管性年龄相关性黄斑变性
64
注射用A型肉毒毒素
暂时性改善成人中度至重度鱼尾纹
65
盐酸莫西沙星片
轻至中度盆腔炎性疾病
66
多种维生素片(6)
用于维生素B1、维生素B6、维生素B12需求量增加,通过饮食摄入不能满足需求的患者
67
10%脂肪乳(OO)/5.5%氨基酸(15)/葡萄糖(20%)注射液
2018年药审中心审评通过的进口原研药
序号
药品名称
获批时的适应症小结
(具体详见药品说明书)
1
注射用重组人凝血因子Ⅷ
用于成人和儿童A型血友病患者出血事件的控制和预防
2
口服五价重配轮状病毒减毒活疫苗(Vero细胞)
预防6周至32周龄婴儿疫苗相关型别的轮状病毒胃肠炎
3Hale Waihona Puke 九价人乳头瘤病毒疫苗(酿酒酵母)
预防16~26岁女性疫苗相关型别的宫颈癌、癌前病变或不典型病变、及持续性感染。
早期特发性帕金森病
40
利那洛肽胶囊
成人便秘型肠易激综合征
41
拉莫三嗪分散片
癫痫
42
拉考沙胺片
癫痫
43
地诺孕素片
子宫内膜异位症
44
艾考恩丙替片
HIV-1感染
45
依达赛珠单抗注射液
快速逆转达比加群酯(泰毕全®)抗凝效果
46
左炔诺孕酮宫内节育系统(III)
避孕
47
小儿法罗培南钠颗粒
敏感细菌所致的儿童皮肤及皮肤组织感染、淋巴管炎、肺炎等感染性疾病。
4
棕榈帕利哌酮酯注射液
药监局2017年度药品审评报告
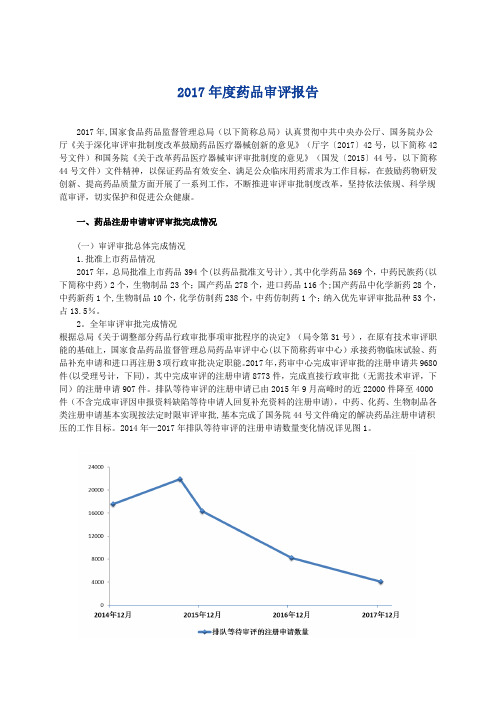
2017年度药品审评报告2017年,国家食品药品监督管理总局(以下简称总局)认真贯彻中共中央办公厅、国务院办公厅《关于深化审评审批制度改革鼓励药品医疗器械创新的意见》(厅字〔2017〕42号,以下简称42号文件)和国务院《关于改革药品医疗器械审评审批制度的意见》(国发〔2015〕44号,以下简称44号文件)文件精神,以保证药品有效安全、满足公众临床用药需求为工作目标,在鼓励药物研发创新、提高药品质量方面开展了一系列工作,不断推进审评审批制度改革,坚持依法依规、科学规范审评,切实保护和促进公众健康。
一、药品注册申请审评审批完成情况(一)审评审批总体完成情况1.批准上市药品情况2017年,总局批准上市药品394个(以药品批准文号计),其中化学药品369个,中药民族药(以下简称中药)2个,生物制品23个;国产药品278个,进口药品116个;国产药品中化学新药28个,中药新药1个,生物制品10个,化学仿制药238个,中药仿制药1个;纳入优先审评审批品种53个,占13.5%。
2。
全年审评审批完成情况根据总局《关于调整部分药品行政审批事项审批程序的决定》(局令第31号),在原有技术审评职能的基础上,国家食品药品监督管理总局药品审评中心(以下简称药审中心)承接药物临床试验、药品补充申请和进口再注册3项行政审批决定职能。
2017年,药审中心完成审评审批的注册申请共9680件(以受理号计,下同),其中完成审评的注册申请8773件,完成直接行政审批(无需技术审评,下同)的注册申请907件。
排队等待审评的注册申请已由2015年9月高峰时的近22000件降至4000件(不含完成审评因申报资料缺陷等待申请人回复补充资料的注册申请),中药、化药、生物制品各类注册申请基本实现按法定时限审评审批,基本完成了国务院44号文件确定的解决药品注册申请积压的工作目标。
2014年—2017年排队等待审评的注册申请数量变化情况详见图1。
图1 2014年—2017年排队等待审评的注册申请数量变化情况完成审评的申请中,化药注册申请为7729件,约占全部审评完成量的88%.各类药品注册申请审评完成情况详见图2。
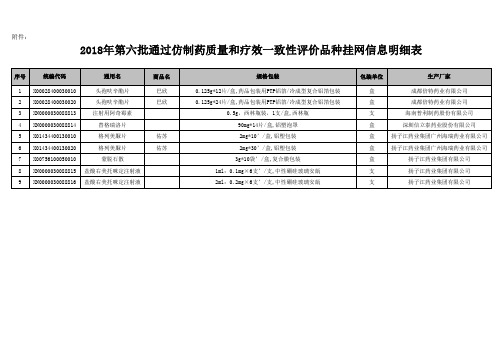
2018年第六批通过仿制药质量和疗效一致性评价品种挂网信息
附Байду номын сангаас:
2018年第六批通过仿制药质量和疗效一致性评价品种挂网信息明细表
序号 1 2 3 4 5 6 7 8 9 统编代码 X00028400030010 X00028400030020 XN0000030088813 XN0000030088814 X01434400130010 X01434400130020 X00756100050010 XN0000030088815 XN0000030088816 通用名 头孢呋辛酯片 头孢呋辛酯片 注射用阿奇霉素 替格瑞洛片 格列美脲片 格列美脲片 蒙脱石散 盐酸右美托咪定注射液 盐酸右美托咪定注射液 佑苏 佑苏 商品名 巴欣 巴欣 规格包装 0.125g*12片/盒,药品包装用PTP铝箔/冷成型复合铝箔包装 0.125g*24片/盒,药品包装用PTP铝箔/冷成型复合铝箔包装 0.5g,西林瓶装,1支/盒,西林瓶 90mg*14片/盒,铝塑泡罩 2mg*10’/盒,铝塑包装 2mg*30’/盒,铝塑包装 3g*10袋’/盒,复合膜包装 1ml:0.1mg×6支’/支,中性硼硅玻璃安瓿 2ml:0.2mg×6支’/支,中性硼硅玻璃安瓿 包装单位 盒 盒 支 盒 盒 盒 盒 支 支 生产厂家 成都倍特药业有限公司 成都倍特药业有限公司 海南普利制药股份有限公司 深圳信立泰药业股份有限公司 扬子江药业集团广州海瑞药业有限公司 扬子江药业集团广州海瑞药业有限公司 扬子江药业集团有限公司 扬子江药业集团有限公司 扬子江药业集团有限公司
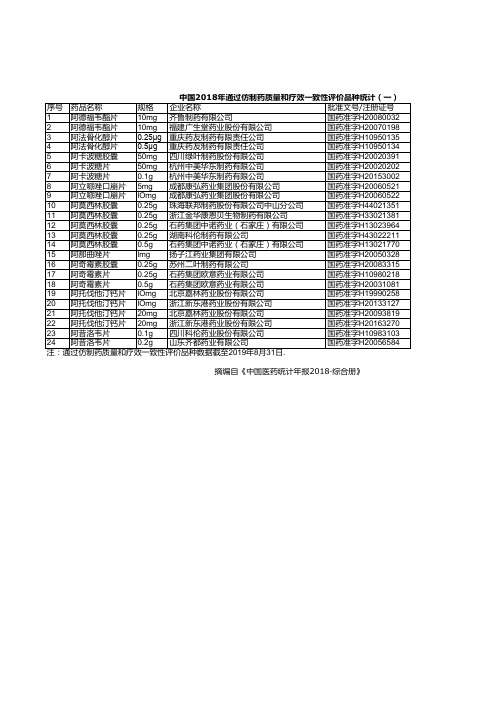
医药年报:中国2018年通过仿制药质量和疗效一致性评价品种统计(一)
国药准字H33021381
12 阿莫西林胶囊 0.25g 石药集团中诺药业(石家庄)有限公司
国药准字H13023964
13 阿莫西林胶囊 0.25g 湖南科伦制药有限公司
国药准字H43022211
14 阿莫西林胶囊 0.5g 石药集团中诺药业(石家庄)有限公司
国药准字H13021770
15 阿那曲唑片
国药准字H10983103
24 阿昔洛韦片
0.2g 山东齐都药业有限公司
国药准字H20056584
注:通过仿制药质量和疗效一致性评价品种数据截至2019年8月31日.
摘编自《中国医药统计年报2018·综合册》
统计(一)
是否289基药目录
否 否 是 是 是 是 否 是 是 是 是 是 是 否 否 是 是 否 否 否 否 否 否 是
国药准字H10950135
4 阿法骨化醇片 0.5μg 重庆药友制药有限责任公司
国药准字H10950134
5 阿卡波糖胶囊 50mg 四川绿叶制药股份有限公司
国药准字H20020391
6 阿卡波糖片
50mg 杭州中美华东制药有限公司
国药准字H20020202
7 阿卡波糖片
0.1g 杭州中美华东制药有限公司
中国2018年通过仿制药质量和疗效一致性评价品种统计(一)
序号 药品名称
规格 企业名称
批准文号/注册证号
1 阿德福韦酯片 10mg 齐鲁制药有限公司
国药准字H20080032
2 阿德福韦酯片 10mg 福建广生堂药业股份有限公司
国药准字H20070198
3 阿法骨化醇片 0.25μg 重庆药友制药有限责任公司
lmg 扬子江药业集团有限公司
医药年报:中国2018年通过仿制药质量和疗效一致性评价品种统计(七)

147 蒙脱石散
3g 浙江海力生制药有限公司
国药准字H19980050
148 米氮平片
15mg 哈尔滨三联药业股份有限公司
国药准字H20060702
149 米非司酮片
lOmg 华润紫竹药业有限公司
国药准字H20010633
150 米非司嗣片
25mg 华润紫竹药业有限公司
国药准字H10950003
151 奈韦拉平片
155 瑞格列奈片
lmg 江苏豪森药业集团有限公司
国药准字H20103637
156 瑞舒伐他汀钙片
5mg 浙江京新药业股份有限公司
ቤተ መጻሕፍቲ ባይዱ
国药准字H20080482
157 瑞舒伐他汀钙片
5mg 浙江海正药业股份有限公司
国药准字H20143337
158 瑞舒伐他汀钙片
5mg 鲁南贝特制药有限公司
国药准字H20080240
H20180008
167 碳酸氢钠片
0.5g 湖南汉森制药股份有限公司
国药准字H43020783
注:通过仿制药质量和疗效一致性评价品种数据截至2019年8月31日.
摘编自《中国医药统计年报2018·综合册》
种统计(七) 是否289基药目录
是 是 是 是 否 是 是 是 是 否 否 否 否 否 否 否 否 否 否 否 否 否 否 是
》
批准日期 2019.07.19 2019.07.19 2019.08.14 2019.08.30 2018.08.22 2018.12.28 2018.12.28 2018.05.14 2018.12.20 2019.01.16 2018.11.30 2018.12.13 2018.02.09 2018.07.06 2019.02.02 2019.03.05 2019.04.03 2017.12.27 2018.02.09 2018.07.06 2018.10.08 2019.02.02 2019.04.03 2019.03.21
2017年度药品审评报告

2017年度药品审评报告2018年03月22日发布2017年,国家食品药品监督管理总局(以下简称总局)认真贯彻中共中央办公厅、国务院办公厅《关于深化审评审批制度改革鼓励药品医疗器械创新的意见》(厅字〔2017〕42号,以下简称42号文件)和国务院《关于改革药品医疗器械审评审批制度的意见》(国发〔2015〕44号,以下简称44号文件)文件精神,以保证药品有效安全、满足公众临床用药需求为工作目标,在鼓励药物研发创新、提高药品质量方面开展了一系列工作,不断推进审评审批制度改革,坚持依法依规、科学规范审评,切实保护和促进公众健康。
一、药品注册申请审评审批完成情况(一)审评审批总体完成情况1.批准上市药品情况2017年,总局批准上市药品394个(以药品批准文号计),其中化学药品369个,中药民族药(以下简称中药)2个,生物制品23个;国产药品278个,进口药品116个;国产药品中化学新药28个,中药新药1个,生物制品10个,化学仿制药238个,中药仿制药1个;纳入优先审评审批品种53个,占13.5%。
2.全年审评审批完成情况根据总局《关于调整部分药品行政审批事项审批程序的决定》(局令第31号),在原有技术审评职能的基础上,国家食品药品监督管理总局药品审评中心(以下简称药审中心)承接药物临床试验、药品补充申请和进口再注册3项行政审批决定职能。
2017年,药审中心完成审评审批的注册申请共9680件(以受理号计,下同),其中完成审评的注册申请8773件,完成直接行政审批(无需技术审评,下同)的注册申请907件。
排队等待审评的注册申请已由2015年9月高峰时的近22000件降至4000件(不含完成审评因申报资料缺陷等待申请人回复补充资料的注册申请),中药、化药、生物制品各类注册申请基本实现按法定时限审评审批,基本完成了国务院44号文件确定的解决药品注册申请积压的工作目标。
2014年-2017年排队等待审评的注册申请数量变化情况详见图1。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
拉米夫定片
按与原研药质量和疗效一致的标准完善后重新申报
59
注射用替莫唑胺
按与原研药质量和疗效一致的标准完善后重新申报
60
利多卡因凝胶贴膏
首仿
61
磺达肝癸钠注射液
首仿
62
帕立骨化醇注射液
首仿
63
替格瑞洛片
首仿
64
盐酸普拉克索片
首仿
65
注射用醋酸西曲瑞克
首仿
66
奥氮平片
同步申报
67
伏立康唑片
同步申报
29
乌美溴铵维兰特罗吸入粉雾剂
具有明显临床价值的新药
30
信迪利单抗注射液
具有明显临床价值的新药
31
盐酸阿来替尼胶囊
具有明显临床价值的新药
32
盐酸安罗替尼胶囊
具有明显临床价值的新药
33
盐酸莫西沙星滴眼液
具有明显临床价值的新药
34
依达赛珠单抗注射液
具有明显临床价值的新药
35
依洛尤单抗注射液
具有明显临床价值的新药
53
口服I型+III型脊髓灰质炎减毒活疫苗(人二倍体细胞)
临床急需
54
注射用紫杉醇(白蛋白结合型)
临床急需
55
布洛芬注射液
按与原研药质量和疗效一致的标准完善后重新申报
56
氟比洛芬酯注射液
按与原研药质量和疗效一致的标准完善后重新申报
57
富马酸替诺福韦二吡呋酯片
按与原研药质量和疗效一致的标准完善后重新申报
22
帕博利珠单抗注射液
具有明显临床价值的新药
23
哌柏西利胶囊
具有明显临床价值的新药
24
培集成干扰素α-2注射液
具有明显临床价值的新药
25
塞瑞替尼胶囊
具有明显临床价值的新药
26
噻托溴铵奥达特罗吸入喷雾剂
具有明显临床价值的新药
27
索磷布韦维帕他韦片
具有明显临床价值的新药
28
特瑞普利单抗注射液
具有明显临床价值的新药
儿童用药
44
小儿法罗培南钠颗粒
儿童用药
45
盐酸托莫西汀口服溶液
儿童用药
46
依库珠单抗注射液
儿童用药
47
注射用拉布立海
儿童用药
48
注射用小儿多种维生素(13)
儿童用药
49
司来帕格片
罕见病
50
特立氟胺片
罕见病
51
注射用重组人凝血因子VIII
罕见病
52
I型III型脊髓灰质炎减毒活疫苗糖丸(人二倍体细胞)
临床急需
7
达诺瑞韦钠片
具有明显临床价值的新药
8
德拉马尼片
具有明显临床价值的新药
9
丁丙诺啡纳洛酮舌下片
具有明显临床价值的新药
10
呋喹替尼胶囊
具有明显临床价值的新药
11
富马酸丙酚替诺福韦片
具有明显临床价值的新药
12
枸橼酸伊沙佐米胶囊
具有明显临床价值的新药
13
甲磺酸仑伐替尼胶囊
具有明显临床价值的新药
14
九价人乳头瘤病毒疫苗(酿酒酵母)
36
注射用艾博韦泰
具有明显临床价值的新药
37
注射用全氟丁烷微球
具有明显临床价值的新药
38
注射用盐酸苯达莫司汀
具有明显临床价值的新药
39
注射用盐酸美法仑
具有明显临床价值的新药
40
艾美赛珠单抗注射液
儿童用药
41
口服五价重配轮状病毒减毒活疫苗(Vero细胞)
儿童用药
42
孟鲁司特钠颗粒
儿童用药
43
小儿多种维生素注射液(13)
80
安立生坦片
专利到期
81
琥珀酸普芦卡必利片
专利到期
82
琥珀酸索利那新片
专利到期
83
注射用米卡芬净钠
专利到期
具有明显临床价值的新药
15
拉考沙胺片
具有明显临床价值的新药
16
来迪派韦索磷布韦片
具有明显临床价值的新药
17
来那度胺胶囊
具有明显临床价值的新药
18
雷珠单抗注射液
具有明显临床价值的新药
19
罗沙司他胶囊
具有明显临床价值的新药
20
马来酸吡咯替尼片
具有明显临床价值的新药
21
纳武利尤单抗注射液
具有明显临床价值的新药
68
富马酸喹硫平缓释片
同步申报
69
克拉霉素缓释片
同步申报
70
克拉霉素片
同步申报
71
孟鲁司特钠咀嚼片
同步申报
72
孟鲁司特钠片
同步申报
73
吸入用地氟烷
同步申报
74
缬沙坦片
同步申报
75
盐酸多奈哌齐片
同步申报
76
盐酸二甲双胍片
同步申报
77
盐酸莫西沙星片
同步申报
78
注射用更昔洛韦钠
同步申报
79
左氧氟沙星片
同步申报
附件3
2018年审评通过的优先审评药品名单
序号
药品名称
纳入优先审评的理由
1
阿柏西普眼内注射溶液
具有明显临床价值的新药
2
艾尔巴韦格拉瑞韦片
具有明显临床价值的新药
3
奥达特罗吸入喷雾剂
具有明显临床价值的新药
4
奥拉帕利片
具有明显临床价值的新药
5
醋酸阿比特龙片
具有明显临床价值的新药
6
达芦那韦考比司他片
具有明显临床价值的新药
