化工原理大作业解答报告
化工原理作业答案解析

3.已知甲地区的平均大气压力为85.3 kPa,乙地区的平均大气压力为101.33 kPa,在甲地区的某真空设备上装有一个真空表,其读数为20 kPa。
若改在乙地区操作,真空表的读数为多少才能维持该设备的的绝对压力与甲地区操作时相同?解:(1)设备内绝对压力绝压=大气压-真空度=()kPa3.65Pa1020103.8533=⨯-⨯(2)真空表读数真空度=大气压-绝压=()kPa03.36Pa103.651033.10133=⨯-⨯5.如本题附图所示,流化床反应器上装有两个U管压差计。
读数分别为R1=500 mm,R2=80 mm,指示液为水银。
为防止水银蒸气向空间扩散,于右侧的U管与大气连通的玻璃管内灌入一段水,其高度R3=100 mm。
试求A、B两点的表压力。
解:(1)A点的压力()(表)Pa101.165Pa08.081.9136001.081.9100042汞3水A⨯=⨯⨯+⨯⨯=+=gRgRpρρ(2)B点的压力()(表)Pa107.836Pa5.081.91360010165.1441汞AB⨯=⨯⨯+⨯=+=gRppρ13.如本题附图所示,用泵2将储罐1中的有机混合液送至精馏塔3的中部进行分离。
已知储罐内液面维持恒定,其上方压力为1.0133⨯105 Pa。
流体密度为800 kg/m3。
精馏塔进口处的塔内压力为1.21⨯105 Pa,进料口高于储罐内的液面8 m,输送管道直径为φ68 mm ⨯4 mm,进料量为20 m3/h。
料液流经全部管道的能量损失为70 J/kg,求泵的有效功率。
解:在截面-A A'和截面-B B'之间列柏努利方程式,得2211221e2f22p u p ugZ W gZ hρρ+++=+++∑()sm966.1m004.02068.0414.33600204πkgJ70m0.8Pa1021.1Pa100133.1222f1125251=⨯-⨯====≈=-⨯=⨯=∑dVAVuhuZZpp;;;;()222121e 21f 2p p u u W g Z Z h ρ--=++-+∑()()768.9WW 173800360020kg J 175kg J 704.7893.146.2kgJ 700.88.92966.1800100133.121.1e s e 25=⨯⨯===+++=⎥⎦⎤⎢⎣⎡+⨯++⨯-=W w N W e19.用泵将2×104kg/h 的溶液自反应器送至高位槽(见本题附图)。
化工原理课后习题答案详解

《第一章 流体流动》习题解答1某敞口容器内盛有水与油。
如图。
已知水及油的密度分别为1000和860kg/m 3,解:h 1=600mm ,h 2=800mm ,问H 为多少mm ?m h h h m kg m kg mm h mm h 32.181.91080.081.91060.081.9860?,/860/10,800,6003333321=∴⨯=⨯⨯+⨯⨯===== 油水ρρ2.有一幢102层的高楼,每层高度为4m 。
若在高楼范围内气温维持20℃不变。
设大气静止,气体压强为变量。
地平面处大气压强为760mmHg 。
试计算楼顶的大气压强,以mmHg 为单位。
⎰⎰=∴-=⨯⨯⨯-=⨯⨯-=⎩⎨⎧---⨯=⨯⨯=----=---127.724,04763.040810190.181.9)760/(10190.181.910190.1)2.2938314/(29151408055P P p m mHg P p Ln dz pdp p p gdz d ②代入①,得②①解:ρρ3.某水池,水深4米,水面通大气,水池侧壁是铅垂向的。
问:水池侧壁平面每3米宽度承受水的压力是多少N ?外界大气压为1atm 。
Ndz gz P F 5423501045.12/481.9103410013.13)(3⨯=⨯⨯⨯+⨯⨯⨯=+=⎰水ρ4.4.外界大气压为1atm ,试按理想气体定律计算0.20at (表压)、20℃干空气的密度。
空气分子量按29计。
345/439.12.293831429)1081.020.010013.1(m Kg RT PM =⨯⨯⨯⨯+⨯==ρ解:5.5.有个外径为R 2、内径为R 1为的空心球,由密度为ρ’的材料制成。
若将该球完全淹没在某密度为ρ的液体中,若球能在任意位置停留,试求该球的外径与内径之比。
设球内空气重量可略。
3/1'1232'3132)/1(/)3/4())3/4(--=∴=-ρρρπρπR R g R g R R (解:6.6.为放大以U 形压差计测气体压强的读数,采用倾斜式U 形压差计。
化工原理课后习题解答

化工原理课后习题解答1. 习题一:物质平衡问题问题描述:一个化工过程中,有两个进料流A和B,分别进料流A中含有20%的物质X,进料流B中含有30%的物质X。
流出的产物中,物质X的浓度为50%。
求进料流A和B的流量比。
解答:首先,我们可以用公式表示物质的平衡关系:(物质X进料流A的质量流量 × 物质X进料流A的浓度) + (物质X进料流B的质量流量 × 物质X进料流B的浓度) = (物质X产物流的质量流量 × 物质X产物流的浓度)根据题目中的数据,我们可以得到以下等式:(20% × Qa) + (30% × Qb) = (50% × (Qa + Qb))其中,Qa和Qb分别表示进料流A和B的质量流量。
我们要求的是进料流A和B的流量比,可以假设进料流A的流量为1,即Qa = 1。
然后将上述等式进行变换得到:0.2 + 0.3Qb = 0.5(1 + Qb)通过解这个一元一次方程,可以得到 Qb = 1。
进料流A和B的流量比为1:1。
2. 习题二:能量平衡问题问题描述:一个化工过程中,进料流的温度为100℃,流出的产物温度为50℃。
进料流的流量为10 kg/min,产物的流量为8 kg/min。
进料流的焓为2000 kJ/kg,产物的焓为2400 kJ/kg/m。
求该过程的热效率。
解答:首先,我们可以用公式表示能量的平衡关系:(进料流的质量流量 × 进料流的焓) = (产物流的质量流量 × 产物流的焓)根据题目中的数据,我们可以得到以下等式:(10 kg/min × 2000 kJ/kg) = (8 kg/min × 2400 kJ/kg)通过解这个一元一次方程,可以得到8000 kJ/min = 19200 kJ/min。
我们可以计算出能量平衡的结果为:进料流的质量流量 × 进料流的焓 = 8000 kJ/min 产物流的质量流量 × 产物流的焓 = 19200 kJ/min根据热效率的定义,热效率 = (产物流的质量流量 × 产物流的焓) / (进料流的质量流量 × 进料流的焓)。
化工原理含实验报告(3篇)

第1篇一、实验目的1. 理解并掌握化工原理中的基本概念和原理。
2. 通过实验验证理论知识,提高实验技能。
3. 熟悉化工原理实验装置的操作方法,培养动手能力。
4. 学会运用实验数据进行分析,提高数据处理能力。
二、实验内容本次实验共分为三个部分:流体流动阻力实验、精馏实验和流化床干燥实验。
1. 流体流动阻力实验实验目的:测定流体在圆直等径管内流动时的摩擦系数与雷诺数Re的关系,将测得的~Re曲线与由经验公式描出的曲线比较;测定流体在不同流量流经全开闸阀时的局部阻力系数。
实验原理:流体在管道内流动时,由于摩擦作用,会产生阻力损失。
阻力损失的大小与流体的雷诺数Re、管道的粗糙度、管道直径等因素有关。
实验中通过测量不同流量下的压差,计算出摩擦系数和局部阻力系数。
实验步骤:1. 将水从高位水槽引入光滑管,调节流量,记录压差。
2. 将水从高位水槽引入粗糙管,调节流量,记录压差。
3. 改变流量,重复步骤1和2,得到一系列数据。
4. 根据数据计算摩擦系数和局部阻力系数。
实验结果与分析:通过实验数据绘制~Re曲线和局部阻力系数曲线,与理论公式进行比较,验证了流体流动阻力实验原理的正确性。
2. 精馏实验实验目的:1. 熟悉精馏的工艺流程,掌握精馏实验的操作方法。
2. 了解板式塔的结构,观察塔板上汽-液接触状况。
3. 测定全回流时的全塔效率及单板效率。
4. 测定部分回流时的全塔效率。
5. 测定全塔的浓度分布。
6. 测定塔釜再沸器的沸腾给热系数。
实验原理:精馏是利用混合物中各组分沸点不同,通过加热使混合物汽化,然后冷凝分离各组分的方法。
精馏塔是精馏操作的核心设备,其结构对精馏效率有很大影响。
实验步骤:1. 将混合物加入精馏塔,开启加热器,调节回流比。
2. 记录塔顶、塔釜及各层塔板的液相和气相温度、压力、流量等数据。
3. 根据数据计算理论塔板数、全塔效率、单板效率等指标。
4. 绘制浓度分布曲线。
实验结果与分析:通过实验数据,计算出了理论塔板数、全塔效率、单板效率等指标,并与理论值进行了比较。
化工分离化工原理作业解答
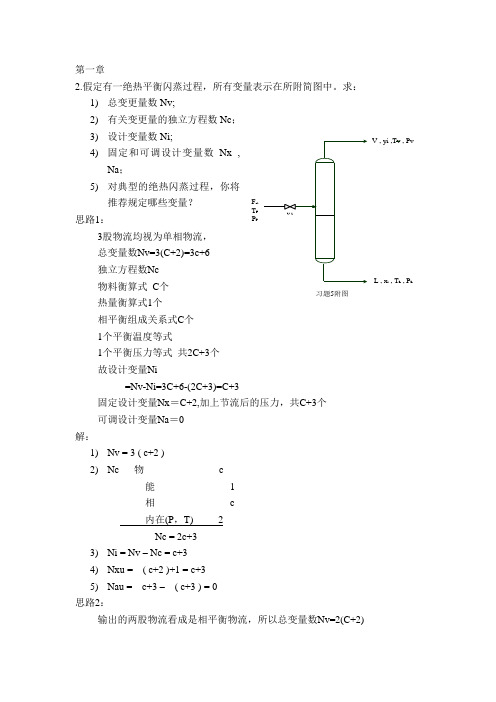
第一章2.假定有一绝热平衡闪蒸过程,所有变量表示在所附简图中。
求: 1) 总变更量数Nv;2) 有关变更量的独立方程数Nc ; 3) 设计变量数Ni;4) 固定和可调设计变量数Nx ,Na ;5) 对典型的绝热闪蒸过程,你将推荐规定哪些变量?思路1:3股物流均视为单相物流, 总变量数Nv=3(C+2)=3c+6 独立方程数Nc 物料衡算式 C 个 热量衡算式1个 相平衡组成关系式C 个 1个平衡温度等式1个平衡压力等式 共2C+3个 故设计变量Ni=Nv-Ni=3C+6-(2C+3)=C+3固定设计变量Nx =C+2,加上节流后的压力,共C+3个 可调设计变量Na =0 解:1) Nv = 3 ( c+2 )2) Nc 物 c 能 1 相 c 内在(P ,T) 2 Nc = 2c+3 3) Ni = Nv – Nc = c+3 4) Nxu = ( c+2 )+1 = c+3 5) Nau = c+3 – ( c+3 ) = 0 思路2:输出的两股物流看成是相平衡物流,所以总变量数Nv=2(C+2)F zi T F P FV , yi ,Tv , PvL , x i , T L , P L习题5附图独立方程数Nc :物料衡算式 C 个 ,热量衡算式1个 ,共 C+1个 设计变量数 Ni=Nv-Ni=2C+4-(C+1)=C+3固定设计变量Nx:有 C+2个加上节流后的压力共C+3个 可调设计变量Na :有0 第二章1.计算在0.1013MPa 和378.47K 下苯(1)-甲苯(2)-对二甲苯(3)三元系,当x 1=0.3125,x 2=0.2978,x 3=0.3897时的K 值。
汽相为理想气体,液相为非理想溶液。
并与完全理想系的K 值比较。
已知三个二元系的Wilson 方程参数。
83.977;33.103522121112=--=-λλλλ 15.4422223=-λλ ;05.4603323-=-λλ14.15101113=-λλ ; 81.16423313-=-λλ (单位:J/mol) 在T=378.47K 时液相摩尔体积为:m v L 3311091.100-⨯= ;321055.117-⨯=L v ;331069.136-⨯=L v 安托尼公式为:苯:()36.5251.27887936.20ln 1--=T P s ; 甲苯:()67.5352.30969065.20ln 2--=T P s ;对二甲苯:()84.5765.33469891.20ln 3--=T P s ;(K T Pa P s :;:) 解:由Wilson 参数方程()[]RT v v ii ij Li L j ij λλ--=Λexp()[]RT v v L L11121212exp λλ--=Λ()()[]47.378314.833.1035ex p 1091.1001055.11733⨯--⨯⨯=-- =1.619 ()[]RT v v L L22212121exp λλ--=Λ ()()[]47.378314.883.977ex p 1055.1171091.10033⨯-⨯⨯=-- =0.629同理:838.013=Λ ;244.131=Λ 010.123=Λ ;995.032=Λ由Wilson 方程∑∑∑ΛΛ-⎪⎪⎭⎫ ⎝⎛Λ-=k jjkj k ki j j ij i x x x ln 1ln γ: 9184.01=γ ;9718.02=γ ;9930.03=γ 根据安托尼方程:MPa P s 2075.01= ;Pa P s 4210693.8⨯= ;Pa P s 4310823.3⨯= 由式(2-38)计算得:88.11=K ;834.02=K ;375.03=K 如视为完全理想系,根据式(2-36)计算得: 048.21=K ;858.02=K ;377.03=K3.一液体混合物的组成为:苯0.50;甲苯0.25;对二甲苯0.25(摩尔分率)。
化工原理习题答案

化工原理习题答案问题一:质量守恒及干燥问题问题描述:一种含有30%水分的湿煤经过加热后,其水分含量降低到15%。
问:为了使1000kg湿煤的水分含量降到15%,需要排除多少千克水分?解答:根据质量守恒原则,该问题可以通过计算质量的变化来求解。
设湿煤的初始质量为m1,水分含量为w1,加热后的质量为m2,水分含量为w2。
根据题意可得到以下关系:m1 = m2 + m水分 w1 = (m水分 / m1) × 100% w2 = (m水分 / m2) × 100%根据题意可得到以下关系: w2 = 15% = 0.15 w1 = 30% = 0.30将以上关系代入计算,可得到: 0.15 = (m水分 / m2) × 100% 0.30 = (m水分 / m1) × 100%解得:m水分 = 0.15 × m2 = 0.30 × m1代入具体数值进行计算: m水分 = 0.15 × 1000kg = 150kg因此,需要排除150千克水分。
问题二:能量守恒问题问题描述:一个装有100升水的水箱,水温为20°C。
向该水箱中加热10000千卡的热量,水温升高到40°C。
问:热容量为1千卡/升·°C的水箱的温度升高了多少度?解答:根据能量守恒原理,可以通过计算热量的变化来求解。
热量的变化可表示为:Q = mcΔT其中,Q为热量的变化量,m为物体的质量,c为物体的比热容,ΔT为温度的变化。
根据题意可得到以下关系: Q = 10000千卡 = 10000 × 1000卡 m = 100升 = 100升 × 1千克/升 = 100 × 1千克 c = 1千卡/升·°C 代入公式计算温度的变化ΔT:10000 × 1000 = (100 × 1) × (ΔT) ΔT = (10000 × 1000) / (100 × 1) = 1000000 / 100 = 10000°C 因此,热容量为1千卡/升·°C的水箱的温度升高了10000度。
化工原理课后答案

化工原理课后答案
1. 甲烷的氧化反应方程式为:CH4 + 2O2 → CO2 + 2H2O。
2. 水的沸腾是因为液态水的分子具有一定的热运动能量,在特定的温度和压力下,水中的分子能克服水的表面张力,从而从液相转变为气相。
3. 化学反应速率可以通过测量反应物浓度的变化来确定。
一般情况下,反应速率与反应物浓度之间存在正比关系,即反应速率随着反应物浓度的增加而增加。
4. 标准气体体积的计量单位是摩尔,即每个摩尔的气体占据的体积为标准状况下的体积。
5. 配比是指化学反应中不同反应物之间的摩尔比例关系。
化学方程式中的系数即为反应物的配比关系。
6. 溶液的浓度可以通过溶质的质量或体积与溶液总质量或总体积的比例来计算得到。
常见的浓度单位包括摩尔浓度、质量浓度和体积浓度等。
7. 反应的热力学变化可以通过反应物和产物之间的化学键的形成和断裂来解释。
在化学反应中,反应物中的化学键断裂需要吸收能量,而产物中的化学键形成释放能量。
8. 氧化还原反应是指化学反应中电子的转移。
氧化剂接收电子,被还原;还原剂失去电子,被氧化。
9. 反应热是指在恒定压力下,化学反应发生时放出或吸收的能量。
反应热可通过测量反应物和产物的焓变来确定。
10. 反应平衡是指在特定的温度和压力下,反应物和产物之间的浓度或压力保持不变。
在平衡态下,反应物和产物之间的反应速率相等,且不再出现净反应。
化工原理课后习地的题目解析汇报汇报第一章
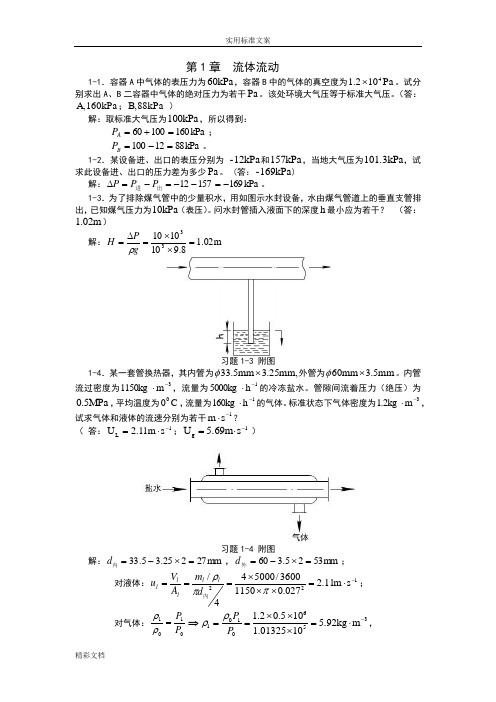
第1章 流体流动1-1.容器A 中气体的表压力为60kPa ,容器B 中的气体的真空度为Pa 102.14⨯。
试分别求出A 、B 二容器中气体的绝对压力为若干Pa 。
该处环境大气压等于标准大气压。
(答:A,160kPa ;B,88kPa )解:取标准大气压为kPa 100,所以得到:kPa 16010060=+=A P ;kPa 8812100=-=B P 。
1-2.某设备进、出口的表压分别为 12kPa -和157kPa ,当地大气压为101.3kPa ,试求此设备进、出口的压力差为多少Pa 。
(答:169kPa -) 解:kPa 16915712-=--=-=∆出进P P P 。
1-3.为了排除煤气管中的少量积水,用如图示水封设备,水由煤气管道上的垂直支管排出,已知煤气压力为10kPa (表压)。
问水封管插入液面下的深度h 最小应为若干? (答:m 02.1)解:m 02.18.910101033=⨯⨯=∆=g P H ρ习题1-3 附图1-4.某一套管换热器,其内管为mm,25.3mm 5.33⨯φ外管为mm 5.3mm 60⨯φ。
内管流过密度为3m 1150kg -⋅,流量为1h 5000kg -⋅的冷冻盐水。
管隙间流着压力(绝压)为MPa 5.0,平均温度为C 00,流量为1h 160kg -⋅的气体。
标准状态下气体密度为3m 1.2kg -⋅,试求气体和液体的流速分别为若干1s m -⋅?( 答:1L s m 11.2U -⋅=;1g s 5.69m U -⋅=)习题1-4 附图解:mm 27225.35.33=⨯-=内d ,m m 5325.360=⨯-=外d ;对液体:122s m 11.2027.011503600/500044/-⋅=⨯⨯⨯===ππρ内d m A V u l l l l l ; 对气体:0101P P =ρρ⇒3560101m kg 92.51001325.1105.02.1-⋅=⨯⨯⨯==P P ρρ,()224内外内外D d A A A g -=-=π()2322m 1032.10335.0053.04⨯=-=π,13s m 69.592.51032.13600/160/--⋅=⨯⨯===ggg gg g A m A V u ρ。
化工原理课后习题答案

第七章 吸收1,解:(1)(2) H,E 不变,则 (3)2,解:同理也可用液相浓度进行判断3,解:HCl 在空气中的扩散系数需估算。
现,故HCl 在水中的扩散系数.水的缔和参数分子量粘度 分子体积4,解:吸收速率方程1和2表示气膜的水侧和气侧,A 和B 表示氨和空气代入式x=0.000044m 得气膜厚度为0.44mm.5,解:查,008.0=*y 1047.018100017101710=+=x 764.001047.0008.0===*x y m Pa mp E 451074.710013.1764.0⨯=⨯⨯==Pa m kmol E C H ⋅⨯=⨯==3441017.71074.75.55KPa P 9.301=2563.0109.3011074.734⨯⨯==P E m 0195.0109.301109.533=⨯⨯=*y 01047.0=x 862.101047.00195.0===*x y m Pa mp E 531062.5109.301862.1⨯=⨯⨯==Pa m kmol E C H ⋅⨯=⨯==-35510875.91062.55.5509.0=y 05.0=x x y 97.0=*09.00485.005.097.0=<=⨯=*y y 吸收∴atm P 1=,293k T =,5.36=A M ,29=B M 5.215.1998.1=+=∑AV()()smD G 25217571071.11.205.2112915.36129310212121--⨯=+⨯+⨯=L D ,6.2=α,18=s M (),005.1293CP K =μmol cm V A 33.286.247.3=+=()()s m s cm D L 29256.081099.11099.13.28005.1293136.2104.721---⨯⨯=⨯⨯⨯⨯=或()()()12A A BM A P P P P RTx D N --=3107.53.10105.0m kN P A =⨯=2266.0m kN P A =212.96065.53.101m kN P B =-=226.10066.03.101m kN P B =-=()24.986.1002.9621m kN P BM =+=()()()07.566.04.983.101295314.81024.01043-⨯⨯-=--x s cm D C 2256.025=为水汽在空气中扩散系数下C 80cm s cm T T D D 25275.175.112121044.3344.029*******.0-⨯==⎪⎭⎫⎝⎛⨯=⎪⎪⎭⎫⎝⎛=水的蒸汽压为,时间 6,解:画图7,解:塔低:塔顶:2.5N 的NaOH 液含 2.5N 的NaOH 液的比重=1.1液体的平均分子量:通过塔的物料衡算,得到如果NaOH 溶液相当浓,可设溶液面上蒸汽压可以忽略,即气相阻力控制传递过程。
化工原理作业答案

化工原理作业答案Standardization of sany group #QS8QHH-HHGX8Q8-GNHHJ8-HHMHGN#3.已知甲地区的平均大气压力为 kPa ,乙地区的平均大气压力为 kPa ,在甲地区的某真空设备上装有一个真空表,其读数为20 kPa 。
若改在乙地区操作,真空表的读数为多少才能维持该设备的的绝对压力与甲地区操作时相同 解:(1)设备内绝对压力绝压=大气压-真空度= ()kPa 3.65Pa 1020103.8533=⨯-⨯(2)真空表读数真空度=大气压-绝压=()kPa 03.36Pa 103.651033.10133=⨯-⨯5.如本题附图所示,流化床反应器上装有两个U 管压差计。
读数分别为R 1=500mm ,R 2=80 mm ,指示液为水银。
为防止水银蒸气向空间扩散,于右侧的U 管与大气连通的玻璃管内灌入一段水,其高度R 3=100 mm 。
试求A 、B 两点的表压力。
解:(1)A 点的压力()(表)Pa 101.165Pa 08.081.9136001.081.9100042汞3水A ⨯=⨯⨯+⨯⨯=+=gR gR p ρρ(2)B 点的压力13.如本题附图所示,用泵2将储罐1中的有机混合液送至精馏塔3的中部进行分离。
已知储罐内液面维持恒定,其上方压力为⨯ Pa 。
流体密度为800 kg/m 3。
精馏塔进口处的塔内压力为⨯ Pa ,进料口高于储罐内的液面8 m ,输送管道直径为φ68 mm ⨯4 mm ,进料量为20 m 3/h 。
料液流经全部管道的能量损失为70 J/kg ,求泵的有效功率。
解:在截面-A A '和截面-B B '之间列柏努利方程式,得19.用泵将2×104 kg/h 的溶液自反应器送至高位槽(见本题附图)。
反应器液面上方保持×103 Pa 的真空度,高位槽液面上方为大气压。
管道为φ76 mm ×4 mm的钢管,总长为35 m ,管线上有两个全开的闸阀、一个孔板流量计(局部阻力系数为4)、五个标准弯头。
化工原理课后题答案

化工原理课后题答案1. 解:(1) 乙醛的饱和蒸汽压随温度的升高而增大,所以温度越高,收集到的甲醇的量就越多。
(2) 通过降低乙醛的饱和蒸汽压,如在装置中增加冷凝器,可以提高甲醇的回收率。
2. 解:(1) 乙烯的化学式为C2H4,分子量为28 g/mol。
(2) 对乙烯C2H4完全燃烧,需要的理论氧气量按照化学计量比为1:3,即每1 mol的乙烯需要3 mol的氧气。
(3) 所以,1 g乙烯需要$\dfrac{3 \times 32}{28}$ g的氧气进行完全燃烧。
3. 解:(1) 中和反应的化学方程式为:NaOH + HCl → NaCl + H2O。
(2) 摩尔质量:NaOH = 40 g/mol,HCl = 36.5 g/mol。
(3) 反应物NaOH与HCl摩尔比为1:1,所以1 g的NaOH可以与1 g的HCl完全反应。
(4) 根据化学方程式,1 mol的NaOH可以与1 mol的HCl完全反应,生成1 mol的NaCl。
(5) 所以,1 g的NaOH可以完全中和36.5 g的HCl,生成58.5 g的NaCl。
4. 解:(1) 化学反应的平衡常数K用来表示反应物浓度与产物浓度之间的比值。
(2) 如果K > 1,表示产物浓度远大于反应物浓度,反应是偏向产物一侧进行的。
(3) 如果K < 1,表示反应物浓度大于产物浓度,反应是偏向反应物一侧进行的。
(4) 如果K = 1,表示反应物浓度与产物浓度相等,反应处于平衡状态。
5. 解:(1) 工业上常用的高聚物有聚乙烯、聚丙烯、聚氯乙烯等。
(2) 高聚物的制备通常采用聚合反应,如聚乙烯的制备通常使用乙烯单体进行聚合反应。
(3) 聚合反应一般分为自由基聚合、阴离子聚合和阳离子聚合等不同机制。
6. 解:(1) 化学反应速率是指单位时间内反应物消耗或产物生成的量。
(2) 影响化学反应速率的因素包括反应物浓度、反应温度、催化剂和反应物物理状态等。
化工原理问答范文

化工原理问答范文1.什么是化工原理?化工原理是研究化学工程中的基本原理和基础知识的学科。
它涵盖了化学反应工程、物料平衡、能量平衡、传质、传热等方面的知识,通过对化工过程中的物质和能量转化、传递、调控的研究,来解决化工过程中的问题。
2.化工原理的重要性是什么?化工原理是化学工程的基础和核心,它对于化工工程师来说具有重要的指导和参考作用。
了解化工原理可以帮助工程师更好地设计和优化化工过程,提高生产效率,降低成本。
同时,化工原理对于研究新材料、新工艺以及处理环境污染等方面也具有重要的意义。
3.化工过程的物料平衡是什么?物料平衡是指在化工过程中,对物质进出量之间的平衡进行分析和计算。
它是化工工程设计和优化的基础。
通常通过简化的控制体积、物料输入输出的考虑,建立物质平衡方程来描述和解决物料平衡问题。
4.化工过程中的能量平衡是什么?能量平衡是指在化工过程中,对能量的进出量之间的平衡进行分析和计算。
它是化工工程设计和优化的重要内容。
通过考虑化工过程中各种能量输入和输出的关系以及其转化的热力学过程,建立能量平衡方程,解决能量平衡问题。
5.传质在化工过程中的作用是什么?传质是指物质在化工过程中由高浓度区向低浓度区传递的过程。
在化工过程中,传质过程是很常见的,对于溶质的扩散、渗透等进行研究有助于化工产品的分离和提纯,也有助于推动化学反应的进行。
6.传热在化工过程中的作用是什么?传热是指热量在物体之间由高温区向低温区传递的过程。
在化工过程中,传热是很重要的一个过程。
良好的传热设计可以提高化工设备的效率,降低能源消耗,并且对于一些过程来说,还可以控制反应速率和产物分布。
7.化学反应工程的研究内容是什么?化学反应工程主要研究化学反应的速率、产物分布、反应机理以及如何设计和优化反应过程。
它关注的是如何通过控制反应条件(温度、压力、反应物浓度等)和反应器的设计等手段,提高反应的效率和选择性,从而实现工业生产的目标。
8.化工原理在新材料研究中的应用是什么?化工原理在新材料研究中有着广泛的应用。
化工原理习题指导下册大题详细解答

化学工业出版社-化工原理习题指导大题详细解答5-26. 在25℃下,用CO 2浓度为0.01kmol/m 3和0.05kmol/m 3的CO 2水溶液分别与CO 2分压为50.65kPa 的混合气接触,操作条件下相平衡关系为p A *=1.66×105x (kPa),试说明上述两种情况下的传质方向,并用气相分压差和液相摩尔浓度差分别表示两种情况下的传质推动力。
解:4108.11000/1801.0-⨯=⨯==SSAM c x ρp A *=1.66×105×1.8×10-4=29.9(kPa)p A =50.65 kPa> p A * 所以传质方向为溶质由气相到液相(吸收过程)以气相分压差表示的传质推动力为kPa 8.209.2965.50*A A A =-=-=∆p p p与CO 2分压为50.65kPa 的气相呈相平衡的液相摩尔浓度35*kmol/m 017.01066.11865.501000=⨯⨯⨯==Ep M c AS S A ρ 以液相摩尔浓度差表示的传质推动力为3A *A A km ol/m 007.001.0017.0=-=-=∆c c c4''100.91000/1805.0-⨯=⨯==SSAM c x ρP ’A *=1.66×105×9.0×10-4=149.4(kPa)p A =50.65 kPa< p A * 所以传质方向为溶质由液相到气相(解吸过程)以气相分压差表示的传质推动力为kPa 8.9865.504.149A *A A =-=-=∆p p p以液相摩尔浓度差表示的传质推动力为3*A A A km ol/m 033.0017.005.0=-=-=∆c c c5-27.在一填料塔内用清水逆流吸收某二元混合气体中的溶质A 。
已知进塔气体中溶质的浓度为0.03(摩尔比,下同),出塔液体浓度为0.0003,总压为101kPa ,温度为 40℃,问: (1)压力不变,温度降为20℃时,塔底推动力(Y-Y *)变为原来的多少倍? (2)温度不变,压力达到202 kPa ,塔底推动力(Y-Y *)变为原来的多少倍? 已知:总压为101kPa ,温度为 40℃时,物系气液相平衡关系为Y *=50X 。
化工原理作业四套答案全

学员答案:A
本题得分:5
题号:5题型:单选题(请在以下几个选项中选择唯一正确答案)本题分数:5
内容:
对湿度一定的空气,以下各参数中哪一个与空气的温度无关。______
A、相对湿度
B、湿球温度
C、露点温度
D、绝热饱和温度
标准答案:C
学员答案:C
本题得分:5
题号:6题型:单选题(请在以下几个选项中选择唯一正确答案)本题分数:5
在stocks区颗粒的沉降速度正比于______。
A、密度差的1/2次方
B、黏度的零次方
C、颗粒直径的0.5次方
D、颗粒直径的平方
标准答案:D
学员答案:D
本题得分:5
题号:10题型:单选题(请在以下几个选项中选择唯一正确答案)本题分数:5
内容:
已知湿空气的下列哪两个参数,利用H—I图可以查得其他未知参数???????
标准答案:B
学员答案:B
本题得分:5
题号:4题型:单选题(请在以下几个选项中选择唯一正确答案)本题分数:5
内容:
对在蒸汽与空气间壁换热过程中,为强化传热,下列方案中的_____在工程上可行。
A、提高空气流速
B、提高蒸汽流速
C、采用过热蒸汽以提高蒸汽温度
D、在蒸汽一侧管壁上加装翅片,增加冷凝面积并及时导走冷凝液
内容:
多层等厚度平壁定态导热中,若某层材料的导热系数最小,则该层两侧的温差_____。
A、最大
B、最小
C、都相等
D、无法确定
标准答案:A
学员答案:A
本题得分:5
题号:14题型:单选题(请在以下几个选项中选择唯一正确答案)本题分数:5
内容:
化工原理作业参考答案-《化工原理》(上下册)天津科学技术出版社

《化工原理》作业参考答案教材:《化工原理》(上下册):天津大学化工原理教研室,天津科学技术出版社第一章 流体流动作业一【流体静力学基本方程式】:p.82 1,2,3,5【1-1】 某设备上真空表的读数为13.3×103Pa ,试计算设备内的绝对压强与表压强。
已知该地区大气压强为98.7×103Pa 。
解: 真空度=大气压-绝对压强∴绝对压强=大气压-真空度=98.7×103-13.3×103=85.4×103 Pa 表压强=-真空度=-13.3×103 Pa【1-2】 在本题附图所示的贮油罐中盛有密度为960kg/m 3的油品,油面高于罐底9.6m ,油面上方为常压。
在罐侧壁的下部有一直径为760mm 的圆孔,其中心距罐底800mm ,孔盖用14mm 的钢制螺钉紧固。
若螺钉材料的工作应力取为39.23×106Pa ,问至少需要几个螺钉?解:罐侧壁圆孔中心压强为)(P 108420.1)8.06.9(81.9960100133.1a 55绝压⨯=-⨯⨯+⨯=+=gh p p a ρ孔盖受到的压力:()()2551760.04100133.1 108420.1)(π⨯⨯⨯=-=-A p p P a螺钉受到的压力:()262014.041023.39πσ⨯⨯⨯==n S n P由力平衡,得21P P =,求得:n = 6.2, 取n = 7,即至少需要7个螺钉。
【1-3】 某流化床反应器上装有两个U 管压差计,如本题附图所示。
测得R 1=400mm ,R 2=50mm ,指示液为水银。
为防止水银蒸气向空间扩散,于右侧的U 管与大气连通的玻璃管内灌入一段水,其高度R 3=50mm 。
试求A 、B 两处的表压强。
解:A 处表压强为:(表压)mmHg 7.53Pa3.716105.081.91360005.081.910002Hg 3O H 2==⨯⨯+⨯⨯=+=gR gR p A ρρB 处表压强为: (表压)mmHg 7.453Pa1005.64.081.9136003.716141Hg =⨯=⨯⨯+=+=gR p p A B ρ【1-5】用本题附图中串联U 管压差计测量蒸汽锅炉水面上方的蒸汽压,U 管压差计的指示液为水银,两U 管间的连接管内充满水。
化工原理课后答案解析

3.在大气压力为101.3kPa 的地区,一操作中的吸收塔内表压为130 kPa 。
若在大气压力为75 kPa 的高原地区操作吸收塔,仍使该塔塔顶在相同的绝压下操作,则此时表压的读数应为多少?解:KPa.1563753.231KPa 3.2311303.101=-=-==+=+=a a p p p p p p 绝表表绝1-6 为测得某容器内的压力,采用如图所示的U 形压差计,指示液为水银。
已知该液体密度为900kg/m 3,h=0.8m,R=0.45m 。
试计算容器中液面上方的表压。
解:kPaPa gmρgR ρp ghρgh ρp 53529742.70632.600378.081.990045.081.9106.13300==-=⨯⨯-⨯⨯⨯=-==+1-10.硫酸流经由大小管组成的串联管路,其尺寸分别为φ76×4mm 和φ57×3.5mm 。
已知硫酸的密度为1831 kg/m 3,体积流量为9m 3/h,试分别计算硫酸在大管和小管中的(1)质量流量;(2)平均流速;(3)质量流速。
解: (1) 大管: mm 476⨯φh kg ρq m V s /1647918319=⨯=⋅= s m d q u V /69.0068.0785.03600/9785.0221=⨯==s m kg u G ⋅=⨯==211/4.1263183169.0ρ (2) 小管: mm 5.357⨯φ质量流量不变 h kg m s /164792=s m d q u V /27.105.0785.03600/9785.02222=⨯==或: s m d d u u /27.1)5068(69.0)(222112=== s m kg u G ⋅=⨯=⋅=222/4.2325183127.1ρ1-11. 如附图所示,用虹吸管从高位槽向反应器加料,高位槽与反应器均与大气相通,且高位槽中液面恒定。
现要求料液以1m/s 的流速在管内流动,设料液在管内流动时的能量损失为20J/kg (不包括出口),试确定高位槽中的液面应比虹吸管的出口高出的距离。
化工原理作业解析

吸收和分离
吸收和分离是化工生产中常用的分离技术,用于将混合物中的组分分离出来。
吸收是通过气体与液体之间的相互作用,将气体混合物中的一种或多种组分溶解在液体中, 从而实现混合物的分离。分离则包括过滤、离心、萃取等方法,用于将固体、液体或气体混 合物中的不同组分分离出来。
了解吸收和分离的原理、工艺条件和设备特点,有助于选择合适的工艺条件和设备,提高产 品的纯度和收率。
热电偶和温度传感器的原理及使用。
作业三:蒸发和结晶的解析
蒸发原理 蒸发过程的相变和热量需求。 多效蒸发和膜蒸发的比较与选择。
作业三:蒸发和结晶的解析
蒸发器的类型和设计要点。 结晶过程 结晶的原理和晶体生长机制。
作业三:蒸发和结晶的解析
结晶产品的分离和纯化方法。
结晶过程的控制因素和优化策略。
作业四:吸收和分离的解析
01
吸收原理
02
吸收剂的选择原则和吸收过程的动力学模型。
03
吸收塔的设计和操作要点。
作业四:吸收和分离的解析
吸收过程的强化措施和应 用实例。
蒸馏、萃取、膜分离等分 离技术的原理和应用范围。
分离技术
分离过程中的能耗和资源 回收利用。
作业五:蒸馏和萃取的解析
01
蒸馏原理
02
蒸馏的基本概念和分类。
03
多组分蒸馏的原理和操作方法。
作业五:蒸馏和萃取的解析
特殊蒸馏技术及其应用领域。 萃取过程
萃取剂的选择原则和萃取过程的动力学模型。
作业五:蒸馏和萃取的解析
萃取塔的设计和操作要点。
VS
萃取过程的强化措施和应用实例。
04 结论
作业总结
本次化工原理作业涉及了流 体流动、传热和传质等基本 原理的应用,通过计算和实 验数据的分析,加深了对化
化工原理课后习题答案

化工原理课后习题答案1. 题目题目:对于一个容器内的理想气体,假设质量为m,在压缩过程中体积由V1压缩至V2。
根据理想气体状态方程Pv = RT,求证在任意温度下,质量为m的理想气体在压缩过程中,做功的大小与压缩的速度无关。
1.1. 答案根据理想气体状态方程Pv = RT,我们可以推导出气体做功的表达式。
首先,设初始状态为(V1, T1),压缩后气体的状态为(V2, T2)。
设气体在压缩过程中的压强变化为dp,由状态方程可得:P1V1 = mRT1 (1)P2V2 = mRT2 (2)根据理想气体的压强定义 P = F/A,其中A为气体受力的面积,F = Δp A 表示单位时间内气体受到的压力作用力。
假设气体在压缩过程中受到的作用力为 F,即Δp A = F。
由于压缩过程中气体的体积减小了ΔV = V1 - V2,所以做功可以表示为:W = F * ΔV = A * Δp * ΔV由理想气体状态方程可得:Δp = P2 - P1 = mRT2/V2 - mRT1/V1将其代入做功公式中可得:W = A * (mRT2/V2 - mRT1/V1) * (V1 - V2)化简上述式子可得:W = A * (mRT1 - mRT2) * (1/V1 - 1/V2)我们可以看到,做功量与压力、温度、质量以及体积之间都有关系。
当温度恒定时,即 T1 = T2 = T,上式可以进一步化简为:W = A * mR * T * (1/V1 - 1/V2)这个式子表示了在恒温条件下,做功量与压缩速度(即体积的变化率)无关。
因此,根据以上推导,可证明在任意温度下,质量为m的理想气体在压缩过程中做功的大小与压缩速度无关。
2. 结论在任意温度下,质量为m的理想气体在压缩过程中做功的大小与压缩速度无关。
这是因为在恒温条件下,做功量仅与压强、质量、温度和体积之间相关,并与压缩速度无关。
这个结论可以应用于化工工程中的压缩过程分析和设计,可以通过调节温度、压强和体积的组合来实现对压缩过程的控制,无需考虑压缩速度的影响。
化工原理课后习题解答

目录第一章流体流动与输送设备 (2)第二章非均相物系分离 (26)第三章传热 (32)第四章蒸发 (44)第五章气体吸收 (48)第六章蒸馏 (68)第七章干燥 (84)第八章萃取 (92)第一章流体流动与输送机械1.燃烧重油所得的燃烧气,经分析知其中含%,%,276%, H 2O8% (体积%),试求此混合气体在温度500 C 、压力时的密度。
解:混合气体平均摩尔质量M m y i M i 0.085 44 0.075 320.76 28 0.08 18 28.86 10 3 kg/mol混合密度3 3101.3 10 28.86 108.31 (273 500)332.已知20C 下水和乙醇的密度分别为 kg/m 和789kg/m ,试计算50%(质量%)乙醇水溶液的密度。
又知其实测值为935 kg/m 3,计算相对误差。
解:乙醇水溶液的混合密度印 a 20.5 0.5 12998.27893m881.36kg/m相对误差:3.在大气压力为的地区,某真空蒸馏塔塔顶的真空表读数为 85kPa 。
若在大气压力为 90 kPa的地区,仍使该塔塔顶在相同的绝压下操作,则此时真空表的读数应为多少?解:P 绝 P a P 真 P a P 真P 真 P a (P a P 真)90 (101.3 85) 73.7kPa4 .如附图所示,密闭容器中存有密度为 900 kg/m 3的液体。
容器上方的压力表读数为 42kPa ,又在液面下装一压力表,表中心线在测压 口以上,其读数为 58 kPa 。
试计算液面到下方测压口的距离。
解:液面下测压口处压力PM m RT0.455kg /m 3100%1噱 100% Ep P0 g z P1 gh 题4附图3P1 gh P0 P1 P。
| (58 42) 10900 9.81h 0.55 2.36m5.如附图所示,敞口容器内盛有不互溶的油和水,油层和水层的厚度分别为在容器底部开孔与玻璃管相连。
化工原理大题答案

第一章蒸馏7.对习题6中的溶液,若原料液流量为100kmol/h,馏出液组成为0.95,釜液组成为0.04(以上均为易挥发组分的摩尔分率),回流比为2.5,试求产品的流量,精馏段的下降液体流量和提馏段的上升蒸汽流量。
假设塔内气液相均为恒摩尔流。
解:①产品的流量由物料衡算 Fx F = Wx W + Dx DD + W = F 代入数据得W = 60.44 kmol/h∴产品流量 D = 100 – 60.44 = 39.56 kmol/h②精馏段的下降液体流量LL = DR = 2.5×39.56 = 98.9 kmol/h③提馏段的上升蒸汽流量V'40℃进料q = 1.08V = V' + (1-q)F = D(1+R)= 138.46 kmol/h∴ V' = 146.46 kmol/h8.某连续精馏操作中,已知精馏段 y = 0.723x + 0.263;提馏段y = 1.25x – 0.0187若原料液于露点温度下进入精馏塔中,试求原料液,馏出液和釜残液的组成及回流比。
解:露点进料 q = 0 即精馏段 y = 0.723x + 0.263 过(x D,x D)∴x D = 0.949提馏段 y = 1.25x – 0.0187 过(x W ,x W)∴x W = 0.0748精馏段与y轴交于[0 ,x D/(R+1)] 即 x D/(R+1)= 0.263∴R = 2.61连立精馏段与提馏段操作线得到交点坐标为(0.5345 ,0.6490)∴ x F = 0.64911.用一连续精馏塔分离由组分A¸B组成的理想混合液。
原料液中含A 0.44,馏出液中含A 0.957(以上均为摩尔分率)。
已知溶液的平均相对挥发度为2.5,最回流比为1.63,试说明原料液的热状况,并求出q值。
解:在最回流比下,操作线与q线交点坐标(x q,y q)位于平衡线上;且q线过(x F,x F)可以计算出q线斜率即 q/(1-q),这样就可以得到q的值由式1-47 R min = [(x D/x q)-α(1-x D)/(1-x q)]/(α-1)代入数据得1.63 = [(0.957/x q)-2.5×(1-0.957)/(1-x q)]/(2.5-1)∴x q = 0.366 或x q = 1.07(舍去)即 x q = 0.366 根据平衡关系式y = 2.5x/(1 + 1.5x)得到y q = 0.591q线 y = qx/(q-1)- x F/(q-1)过(0.44,0.44),(0.366,0.591)q/(q-1)= (0.591-0.44)/(0.366-0.44)得 q = 0.67∵ 0 < q < 1 ∴原料液为气液混合物15.在连续操作的板式精馏塔中分离苯-甲苯的混合液。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
化工原理大作业解答报告
组长:王萌 组员:朱婧文 刘莉丹 谢白羿
用U 型管压差计测量一管路中某两个固定点之间的压差,在管路水平安装、倾斜安装和垂直安装三种情况下,压差计相应的显示值R1、 R2和R3的大小有何关系,它们是否一致?给出解释。
当关闭管路出口阀门后,管内流体处于静止,此时的三个显示值又如何?(三种情况下,两个测量点上、下游的管路没有发生变化)
解:R 值始终不变
设管路的倾斜角为 θ,管路内液体密度为ρ,
取等压面A 、B
11
202()A B
A B P P P gh P P g h R gR P ρρρ==+=-++
由上三式解得,12021()()P P gR g h h ρρρ-=-+- ①
对1、2列机械能衡算式
2
21122
1212
220e f
e P u P u gz w gz w u u w ρρ+++=+++==
则 1212()f P P g z z w ρ--+= ②
由图易知 1221()z z h h -=--
把①代入②得 01221()()()f gR g z z g h h w ρρρ--+
+-= 则有 0()f gR w ρρρ
-= 则 0()f w R g ρρρ=- ③
I 、当管内流体静止时 0f w =
由式 ② 得 0R =
即R 值与管无关
II 、当管内流体流动时,设流速为u 则 R e d u ρ
μ=
当 Re>4000 时 流体为湍流 0.23
2680.1()R e 2f d l u w d ε
λλ=+
= 为恒定量,故R 不变
当 Re<4000 时 流体为层流 264
R e
2
f l u w d λλ==
为恒定量,故R 不变
综上,不论何种情况,R 值与管无关。
