第三章习题答案
第三章 练习题答案

第三章练习题一、判断正误并解释1.所谓商品的效用,就是指商品的功能。
分析:这种说法是错误的。
商品的效用指商品满足人的欲望的能力,指消费者在消费商品时所感受到的满足程度2.不同的消费者对同一件商品的效用的大小可以进行比较。
分析:这种说法是错误的。
同一个消费者对不同商品的效用大小可以比较。
但由于效用是主观价值判断,所以同一商品对不同的消费者来说,其效用的大小是不可比的。
3.效用的大小,即使是对同一件商品来说,也会因人、因时、因地而异。
分析:这种说法是正确的。
同一商品给消费者的主观心理感受会随环境的改变而改变。
4.边际效用递减规律是指消费者消费某种消费品时,随着消费量的增加,其最后一单位消费品的效用递减。
分析:这种说法是错误的。
必须在某一特定的时间里,连续性增加。
5.预算线的移动表示消费者的货币收入发生变化。
分析:这种说法是错误的。
只有在收入变动,商品价格不变,预算线发生平移时,预算线的移动才表示消费者的收入发生了变化。
6.效应可以分解为替代效应和收入效应,并且替代效应与收入效应总是反向变化。
分析:这种说法是错误的。
正常物品的替代效应和收入效应是同向变化的。
二、选择1.当总效用增加时,边际效用应该:(A )A.为正值,但不断减少;B.为正值,且不断增加;C.为负值,且不断减少;D.以上都不对2.当某消费者对商品X的消费达到饱合点时,则边际效用MUχ为:(C )A.正值B.负值C.零D.不确定3.正常物品价格上升导致需求量减少的原因在于:(C )A.替代效应使需求量增加,收入效应使需求量减少;B.替代效应使需求量增加,收入效应使需求量增加;C.替代效应使需求量减少,收入效应使需求量减少;D.替代效应使需求量减少,收入效应使需求量增加。
4.无差异曲线的形状取决于(C )A.消费者收入;B.所购商品的价格;C.消费者偏好;D.商品效用水平的大小。
5.无差异曲线为斜率不变的直线时,表示相组合的两种商品是(B )A.可以替代的;B.完全替代的;C.互补的;D.互不相关的。
第三章-表示力学量算符-习题答案

第三章 量子力学中的力学量 1. 证明 厄米算符的平均值都是实数(在任意态)[证] 由厄米算符的定义**ˆˆ()F d F d ψψτψψτ=⎰⎰厄米算符ˆF的平均值 *ˆF Fd ψψτ=⎰ **ˆ[()]F d ψψτ=⎰ ***ˆ[]Fd ψψτ=⎰**ˆ[()]Fd ψψτ=⎰**ˆ[]F d ψψτ=⎰ *F =即厄米算符的平均值都是实数2. 判断下列等式是否正确(1)ˆˆˆHT U =+ (2)H T U =+(3)H E T U ==+[解]:(1)(2)正确 (3)错误因为动能,势能不同时确定,而它们的平均值却是同时确定 。
3. 设()x ψ归一化,{}k ϕ是ˆF的本征函数,且 ()()k kkx c x ψϕ=∑(1)试推导k C 表示式(2)求征力学量F 的()x ψ态平均值2k k kF c F =∑(3)说明2k c 的物理意义。
[解]:(1)给()x ψ左乘*()m x ϕ再对x 积分**()()()()mm k k k x x dx x c x dx ϕϕϕτϕ=⎰⎰*()()k m k kc x x dx ϕϕ=∑⎰因()x ψ是ˆF的本函,所以()x ψ具有正交归一性**()()()()mk m k k k kkx x dx c x x dx c mk c ϕψϕϕδ===∑∑⎰⎰ ()m k = *()()k m c x x dx ϕψ∴=⎰(2)k ϕ是ˆF 的本征函数,设其本征值为kF 则 ˆk k kF F ϕϕ= **ˆˆm k m k k kF F dx F c dx ψψψϕ==∑⎰⎰**()m mk k k kc x F c dx ϕϕ=∑∑⎰**m k kmkx mkc c F dϕϕ=∑⎰*m k k mk mkcc F δ=∑2k k kc F =∑即 2k k kF c F =∑(3)2k c 的物理意义;表示体系处在ψ态,在该态中测量力学量F ,得到本征值k F 的 几率为2k c 。
第三章习题解答

第三章习题解答一、判断下列说法是否正确,凡对的在括号内打“√”,否则打“×”。
(1)现测得两个共射放大电路空载时的电压放大倍数均为-100,将它们连成两级放大电路,其电压放大倍数应为10000。
( )(2)阻容耦合多级放大电路各级的Q点相互独立,( )它只能放大交流信号。
( )(3)直接耦合多级放大电路各级的Q点相互影响,( )它只能放大直流信号。
( )(4)只有直接耦合放大电路中晶休管的参数才随温度而变化。
( )(5)互补输出级应采用共集或共漏接法。
( )二、现有基本放大电路:A.共射电路B.共集电路C.共基电路D.共源电路E.共漏电路根据要求选择合适电路组成两级放大电路。
(1)要求输入电阻为1kΩ至2kΩ,电压放大倍数大于3000,第一级应采用,第二级应采用。
(2)要求输入电阻大于10MΩ,电压放大倍数大于300,第一级应采用,第二级应采用。
(3)要求输入电阻为100kΩ~200kΩ,电压放大倍数数值大于100,第一级应采用,第二级应采用。
(4)要求电压放大倍数的数值大于10,输入电阻大于10MΩ,输出电阻小于100Ω,第一级应采用,第二级应采用。
(5)设信号源为内阻很大的电压源,要求将输入电流转换成输出电压,且,输出电阻R o<100,第一级应采用,第二级应采用。
三、选择合适答案填入空内。
(1)直接耦合放大电路存在零点漂移的原因是。
A.电阻阻值有误差B.晶体管参数的分散性C.晶体管参数受温度影响D.电源电压不稳定(2)集成放大电路采用直接耦合方式的原因是。
A.便于设计B.放大交流信号C.不易制作大容量电容(3)选用差分放大电路的原因是。
A.克服温漂B. 提高输入电阻C.稳定放入倍数(4)差分放大电路的差模信号是两个输入端信号的,共模信号是两个输入端信号的。
A.差B.和C.平均值(5)用恒流源取代长尾式差分放大电路中的发射极电阻R e,将使电路的。
A.差模放大倍数数值增大B.抑制共模信号能力增强C.差模输入电阻增大(6)互补输出级采用共集形式是为了使。
(完整版)财务管理第三章习题及答案

(完整版)财务管理第三章习题及答案第三章财务分析⼀、单项选择题1、下列经济业务会使企业的速动⽐率提⾼的是( )。
A、销售库存商品B、收回应收账款C、购买短期债券D、⽤固定资产对外进⾏长期投资2、下列财务⽐率中,可以反映企业偿债能⼒的是( )。
A、平均收款期B、销售利润率C、市盈率D、已获利息倍数3、下列不属于偿债能⼒分析指标的是()。
A、资产负债率B、现⾦⽐率C、产权⽐率D、安全边际4、下列财务⽐率中综合性最强、最具有代表性的指标是()。
A 、资产周转率B、净值报酬率C 、资产负债率D 、资产净利率5、流动⽐率⼩于1时,赊购原材料若⼲,将会( )。
A、增⼤流动⽐率B、降低流动⽐率C、降低营运资⾦D、增⼤营运资⾦6、在计算速动⽐率时,要把存货从流动资产中剔除的原因,不包括( )A、可能存在部分存货已经损坏但尚未处理的情况B、部分存货已抵押给债权⼈C、可能存在成本与合理市价相差悬殊的存货估价问题D、存货可能采⽤不同的计价⽅法7、不影响应收账款周转率指标利⽤价值的因素是( )。
A、销售折让与折扣的波动B、季节性经营引起的销售额波动C、⼤量使⽤分期付款结算⽅式D、⼤量使⽤现⾦结算的销售8、ABC公司⽆优先股,去年每股盈余为4元,每股发放股利2元,保留盈余在过去⼀年中增加了500万元。
年底每股账⾯价值为30元,负债总额为5000万元,则该公司的资产负债率为( )。
A、30%B、33%C、40%D、44%9、在杜邦财务体系中,假设其他情况相同,下列说法中错误的是( )A、权益乘数⼤则财务风险⼤B、权益乘数⼤则权益净利率⼤C、权益乘数等于资产权益率的倒数D、权益乘数⼤则资产净利率⼤10、下列公式中不正确的是( )。
A、股利⽀付率+留存盈利⽐率=1B、股利⽀付率×股利保障倍数=1C、变动成本率+边际贡献率=1D、资产负债率×产权⽐率=111、市净率指标的计算不涉及的参数是( )。
A、年末普通股股数B、年末普通股权益C、年末普通股股本D、每股市价12、⼀般认为,流动⽐率保持在( )以上时,资产的流动性较好。
会计课后习题答案(第三章)

19 企业计提当年盈余公积的基数,不包括年初未分配利润。
答案: 正确
20 年度终了,“利润分配”账户所属的各明细账户中,除“未分配利润”明细账户可能有余额外,其他明细账户均无余额。
答案: 正确
21 得利与损失是与企业日常活动直接关联的经济利益总流入或总流出。
答案: 错误
8 下列支出不得列入成本费用的是 。
A: 支付给金融机构的手续费
答案: 制造费用
10 “应付职工薪酬”账户可设置 、 、 、 、 和“非货币性福利”等明细分类账户。
答案: 工资 社会保险费 职工福利 工会经费 职工教育经费
11 .直接生产工人的薪酬费用应计入 账户,车间技术及管理人员薪酬费用应计入 账户,销售机构人员的薪酬费用计入 账户,行政管理人员薪酬费用计入 账户。
答案: 正确
15 企业按职工工资总额一定比例计提的工会经费及职工教育经费应记入管理费用。
答案: 错误
16 企业专设销售机构的固定资产修理费用应计入销售费用。
答案: 正确
17 “生产成本”账户若有余额应在借方,反映期末自制半成品的实际生产成本。
答案: 错误
18 企业当年可供分配的利润包括当年实现的净利润和年初未分配利润。
B: 制造费用
C: 本年利润
D: 管理费用
E: 利润分配
答案: B, D
5 工业企业以下收入中应记入其他业务收入的有 。
A: 销售产品
B: 销售材料
C: 固定资产盘盈
D: 固定资产出租收入
E: 处置固定资产净收益
答案: B, D
6 工业企业以下各项应记入营业外支出的是 。
第三章习题解答

第3章 力学基本定律与守恒律 习题及答案1.作用在质量为10 kg 的物体上的力为i t F)210(+=N ,式中t 的单位是s ,(1)求4s 后,这物体的动量和速度的变化.(2)为了使这力的冲量为200 N ·s ,该力应在这物体上作用多久,试就一原来静止的物体和一个具有初速度j 6-m ·s -1的物体,回答这两个问题.解: (1)若物体原来静止,则i t i t t F p t 1401s m kg 56d )210(d -⋅⋅=+==∆⎰⎰,沿x 轴正向,ip I imp v111111s m kg 56s m 6.5--⋅⋅=∆=⋅=∆=∆ 若物体原来具有6-1s m -⋅初速,则⎰⎰+-=+-=-=t tt F v m t m F v m p v m p 000000d )d (,于是⎰∆==-=∆t p t F p p p 0102d,同理, 12v v ∆=∆,12I I=这说明,只要力函数不变,作用时间相同,则不管物体有无初动量,也不管初动量有多大,那么物体获得的动量的增量(亦即冲量)就一定相同,这就是动量定理. (2)同上理,两种情况中的作用时间相同,即⎰+=+=tt t t t I 0210d )210(亦即 0200102=-+t t 解得s 10=t ,(s 20='t 舍去)2.一颗子弹由枪口射出时速率为10s m -⋅v ,当子弹在枪筒内被加速时,它所受的合力为 F =(bt a -)N(b a ,为常数),其中t 以秒为单位:(1)假设子弹运行到枪口处合力刚好为零,试计算子弹走完枪筒全长所需时间;(2)求子弹所受的冲量.(3)求子弹的质量. 解: (1)由题意,子弹到枪口时,有0)(=-=bt a F ,得ba t =(2)子弹所受的冲量⎰-=-=tbt at t bt a I 0221d )(将bat =代入,得 ba I 22=(3)由动量定理可求得子弹的质量202bv a v I m == 3.如图所示,一质量为m 的球,在质量为M 半径为R 的1/4圆弧形滑槽中从静止滑下。
第三章习题参考答案

第三章习题参考答案一、填空题1、指令格式是由操作码和操作数所组成,也可能仅由操作码组成。
2、若用传送指令访问MCS-51的程序存储器,它的操作码助记符应为MOVC 。
3、若用传送指令访问MCS-51的片内数据存储器,它的操作码助记符应为MOV 。
4、若访问MCS-51的片外数据存储器,它的操作码助记符应为MOVX 。
5、累加器(A)=80H,执行完指令ADD A,#83H后,进位位C= 1 。
6、执行ANL A,#0FH指令后,累加器A的高4位= 0000 。
7、JZ rel的操作码地址为1000H,rel=20H,它的转移目的地址为1022H 。
8、JBC 00H,rel 操作码的地址为2000H,rel=70H,它的转移目的地址为2073H 。
9、累加器(A)=7EH,(20H)= #04H,MCS-51执行完ADD A,20H指令后PSW.0= 0 。
10、MOV PSW,#10H是将MCS-51的工作寄存器置为第 2 组。
11、指令LCALL 37B0H,首地址在2000H,所完成的操作是2003H 入栈,37B0H →PC。
12、MOVX A,@DPTR源操作数寻址方式为寄存器间接寻址。
13、ORL A,#0F0H是将A的高4位置1,而低4位保持不变。
14、SJMP rel的指令操作码地址为0050H,rel=65H,那么它的转移目标地址为 00B7H 。
15、设DPTR=2000H,(A)=80H,则MOVC A,@A+DPTR的操作数的实际地址为2080H 。
16、MOV C,20H源寻址方式为位寻址。
17、在直接寻址方式中,只能使用8 位二进制数作为直接地址,因此其寻址对象只限于片内RAM 。
18、在寄存器间接寻址方式中,其“间接”体现在指令中寄存器的内容不是操作数,而是操作数的地址。
19、在变址寻址方式中,以 A 作变址寄存器,以PC 或DPTR 作基址寄存器。
20、假定累加器A中的内容为30H,执行指令1000H:MOVC A,@A+PC后,把程序存储器1031H 单元的内容送入累加器A中。
第三章习题集答案

第三章习题集答案本章习题一、名词解释均衡产出或收入消费函数边际消费倾向平均消费倾向储蓄函数边际储蓄倾向平均储蓄倾向乘数投资乘数政府支出乘数税收乘数政府转移支出乘数平衡预算乘数对外贸易乘数相对收入消费理论生命周期消费理论永久收入消费理论二、判断题1.投资乘数起作用的关键因素是有确定的边际消费倾向值。
2.在一个没有政府的封闭经济中,经济均衡时一定是投资等于储蓄;在一个有政府的开放经济中情况仍是这样。
3.在均衡产出的情况下,企业的非意愿存货投资必然为零。
4.在045线上,消费支出和收入并不总是相等。
5.在经济学上,家庭储蓄是指可支配收入中未用于消费而放在银行的存款。
6.一般来说,高收入家庭消费倾向越高,低收入家庭消费倾向越低。
三、选择题1.收入超过支出,公司将减少生产,因为非计划存货量为( )A. 正;B. 负;C. 零;D.不确定。
2.消费函数为C=100+0.8(Y-T),政府支出乘数是( )A. 0.8B. 1.2C. 4D. 5。
3.消费函数的斜率取决于( )A. 边际消费倾向;B. 与可支配收入无关的消费总量;C. 平均消费倾向;D. 由于收入变化引起的投资量。
4.下列四种情况中,投资乘数最大的是( )A. 边际消费倾向为0.4 ; B . 边际储蓄倾向为0.1 ;C. 边际消费倾向为0.6 ;D. 边际储蓄倾向为0.35.在四部门经济中,其他条件不变,投资、储蓄、政府购买、税收、进口同时增加,则均衡收入( )A. 保持不变; B . 趋于增加; C. 趋于减少; D. 变化趋势不能确定。
6.在凯恩斯45°线图中,消费函数与45°线相交点的产出水平表示( )A. 净投资支出I大于零时的GNP水平;B. 均衡的GNP水平;C. 消费C和投资I相等;D. 没有任何意义,除非投资I恰好为零。
7.如果由于计划投资支出的减少而导致原来国民收入Y的均衡水平改变,可以预期( )A. Y将下降,但储蓄S不变;B. Y将下降,但储蓄S将上升;C. Y和储蓄S都将下降;D. Y不变,但储蓄S下降8.如果边际消费倾向为常数,那么消费函数将是( )A. 一条不通过原点的直线;B. 一条相对于横轴向上凸的曲线;C. 一条相对于横轴向下凹的曲线;D. 一条通过原点与横轴成45°的直线;E. 以上说法均不准确。
第三章习题解答及参考答案

(
)
①
2 式中 m 为整数。令 u = αr ,显然上式是 u 的周期函数,周期为 2π ,故可展开成傅里 ∞ 1 1 + sgn (cos u ) = ∑ Cn e inu 2 2 n = −∞
叶级数:
其中,
Cn =
1 2π
∫
π 2
−π 2
e −inu du =
sin (nπ 2) nπ
②
遂有:
∞ 1 1 sin (nπ 2 ) inαr 2 e + sgn cos αr 2 = ∑ 2 2 nπ n= −∞
②
σ ( f x ,0 ) 2λd i =1− f x = 1− f x f0 σ0 l
l l ≤ λd i f x ≤ (见附图3 - 4(b)) 4 2
2 1 l l σ ( f x ,0 ) = (l − λd i f x ) l − = − λd i l f x 2 2 2
λd ;两个一级分量与中央亮斑 L
附图 3-2
习题[3-2]图示
附图 3-3
归一化强度分布
[3-3]
将面积为 10 mm × 10 mm 的透射物体置于一傅里叶变换透镜的前焦面上作频谱分析。
用波长 λ = 0.5 µ m 的单色平面波垂直照明,要求在频谱面上测得的强度在频率 140 线/mm 以下能准确代表物体的功率谱。并要求频率为 140 线/mm 与 20 线/mm 在频谱面上的间隔为 30mm,问该透镜的焦距和口径各为多少? 解:取面积为10mm ×10mm 的透射物体的对角线方向为 x 轴。因要求在 140 线/mm 以下的 空间频率成分不受到有限孔径的渐晕效应的影响,故透镜的口径 D 应满足条件:
第三章习题参考答案
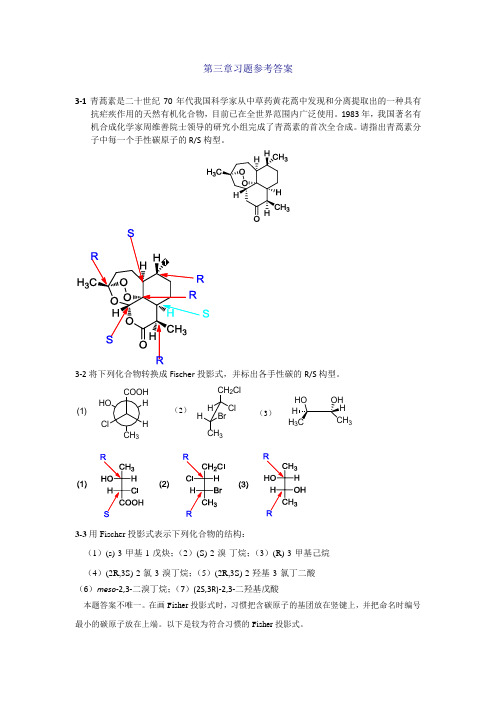
第三章习题参考答案3-1青蒿素是二十世纪70年代我国科学家从中草药黄花蒿中发现和分离提取出的一种具有抗疟疾作用的天然有机化合物,目前已在全世界范围内广泛使用。
1983年,我国著名有机合成化学家周维善院士领导的研究小组完成了青蒿素的首次全合成。
请指出青蒿素分子中每一个手性碳原子的R/S 构型。
3-2将下列化合物转换成Fischer 投影式,并标出各手性碳的R/S 构型。
(2)(3)3BrH3HClCH 2ClH 3H 3(1)3-3用Fischer 投影式表示下列化合物的结构:(1)(s)-3-甲基-1-戊炔;(2)(S)-2-溴-丁烷;(3)(R)-3-甲基己烷 (4)(2R,3S)-2-氯-3-溴丁烷;(5)(2R,3S)-2-羟基-3-氯丁二酸 (6)meso -2,3-二溴丁烷;(7)(2S,3R)-2,3-二羟基戊酸本题答案不唯一。
在画Fisher 投影式时,习惯把含碳原子的基团放在竖键上,并把命名时编号最小的碳原子放在上端。
以下是较为符合习惯的Fisher 投影式。
3-4下列化合物中哪些有手性?(1)、(3)、(5)、(7)、(9)无手性(2)、(4)、(6、)(8)、(10)有手性3-5长尾粉蚧壳虫信息素A是雌性长尾粉蚧壳虫(一种植物害虫)分泌的性激素,其外消旋体目前已被人工合成,并商业化用于农田害虫的控制和诱杀。
最近,化学家通过全合成途径确定了天然长尾粉蚧壳虫信息素的绝对构型(.Chem.2013,78,6281−6284)。
通过全合成方法分别得到了A的2种立体异构体,发现其中的(S)-(+)-异构体具有吸引雄性长尾粉蚧壳虫的活性,而它的对映体(R)-( )-A则无此生物活性。
此结果表明雌性长尾粉蚧壳虫分泌的天然长尾粉蚧壳虫信息素为(S)-A。
商业化使用的外消旋体与纯的(S)-对映体生物活性相似,说明(R)-A对(S)-A的生物活性无抑制作用。
写出(R)-A和(S)-A的结构式。
(R)-A(S)-A3-6山梗烷定是从印度烟叶中分离到的一种化合物,它没有旋光性,也不可被拆分。
第三章习题(含答案)

第三章会计等式与复式记账一、单项选择题1、总分类账户与明细分类账户平行登记四要点中的“依据相同”是指()。
A.总分类账要根据明细分类账进行登记B.明细分类账要根据总分类账进行登记C.根据同一会计凭证登记D.由同一人员进行登记2、某企业原材料总分类科目的本期借方发生额为25 000元,贷方发生额为24 000元,其所属的三个明细分类账中;甲材料本期借方发生额为8 000元,贷方发生额为6 000;乙材料借方发生额为13 000元,贷方发生额为16 000元;则丙材料的本期借、贷方发生额分别为()。
A.借方发生额为12 000元,贷方发生额为2 000元B.借方发生额为4 000元,贷方发生额为2 000元C.借方发生额为4 000元,贷方发生额为10 000元D.借方发生额为6 000元,贷方发生额为8 000元3、甲公司月末编制的试算平衡表中,全部科目的本月贷方发生额合计为120万元,除银行存款外的本月借方发生额合计104万元,则银行存款科目()。
A.本月借方余额为16万元B.本月贷方余额为16万元C.本月贷方发生额为16万元D.本月借方发生额为16万元4、下列记账错误中,不能通过试算平衡检查发现的是()。
A.将某一分录的借方发生额600元,误写成6 000元B.某一分录的借贷方向写反C.借方的金额误记到贷方D.漏记了借方的发生额5、下列关于试算平衡法的说法,正确的是()。
A.漏记某项经济业务影响试算平衡B.包括发生额试算平衡法和余额试算平衡法C.试算平衡了,账户记录一定正确D.发生额试算平衡法理论的依据是会计等式6、企业购入原材料10 000元,已开出支票支付6 000元,另4 000元暂欠。
下列会计分录正确的是()。
A.借:原材料10 000贷:银行存款10 000B.借:原材料10 000贷:应付账款10 000C.借:原材料10 000贷:银行存款6 000应付账款4 000D.借:原材料10 000贷:应付票据6 000应付账款4 0007、企业计算应交所得税时,正确的会计分录是()。
第三章 习题(带答案)

第三章判断题T 1 Linux操作系统的源代码是公开的,它是一种“自由软件”。
(判断)T 2 MATLAB是一种能用于数值计算的高级程序设计语言。
(判断)F 3 Windows系统中,不同文件夹中的文件不能同名(判断)F 4 Windows系统中,可以像删除子目录一样删除根目录。
(判断)F 5 Windows系统中,每一个物理硬盘只能建立一个根目录,不同的根目录在不同的物理硬盘中。
(判断)T 6 操作系统三个重要作用体现在:管理系统硬软件资源、为用户提供操作界面、为应用程序开发提供平台。
(判断)T 7 操作系统通过各种管理程序提供了“任务管理”、“存储管理”、“文件管理”、“设备管理”等多种功能。
(判断)T 8 计算机软件通常指的是用于指示计算机完成特定任务的,以电子格式存储的程序、数据和相关的文档。
(判断)T 9 软件产品是交付给用户使用的一整套程序、相关的文档和必要的数据。
(判断)T 10 软件是以二进位表示,且通常以电、磁、光等形式存储和传输的,因而很容易被复制。
T 11 为了延长软件的生命周期,常常要进行软件版本升级,其主要目的是减少错误、扩充功能、适应不断变化的环境。
(判断)T 12 在Windows系统中,按下Alt+PrintScreen键可以将桌面上当前窗口的图像复制到剪贴板中。
(判断)F [01]. 数据库管理系统是最接近计算机硬件的系统软件。
(判断)T [05]. 用Pentium4 的指令系统编写的可执行程序在PentiumⅢ中不一定能被执行;反之,用PentiumⅢ的指令系统编写的可执行程序在Pentium4 中一定能被执行。
(判断)F [07]. 所有存储在磁盘中的MP3音乐都是计算机软件。
(判断)F [09]. P3是世界著名的项目管理软件。
由于使用P3能管理一个大型工程系统的有关资源,因此,它应属于系统软件。
(判断)T [10]. 计算机软件包括软件开发和使用所涉及的资料。
(完整版)马克思主义基本原理概论第三章习题及答案

第三章人类社会及其发展规律一、单项选择题1.“手推磨产生的是封建主的社会,蒸汽磨产生的是工业资本家的社会”,这句话揭示了A. 生产工具是衡量生产力水平的重要尺度B. 科学技术是第一生产力C.社会形态的更替有其一定的顺序性D. 物质生产的发展需要建立相应的生产关系2.社会历史观的基本问题是A.生产力和生产关系的问题B.社会规律的客观性和主观能动性的关系问题C.社会存在和社会意识的关系问题D.自然和社会的关系问题3.划分生产关系类型的基本标志是A.产品的分配形式B.生产资料的所有制形式C.人们在生产中的地位D.生产关系与生产力的矛盾性质4.杰出人物的产生是A.纯粹是必然的B.纯粹是偶然的C.既是必然的,又是偶然的D.有些人是必然的,有些人是偶然的5.社会精神财富的源泉是A.客观的物质世界B.脑力劳动者的集体智慧C.思想家们的创造性思维D.人民群众的社会实践6.生产关系范畴反映的是A.人与自然之间的关系 B.人与人之间的政治关系C.人与人之间的经济关系 D.人与人之间的思想关系7.先进生产力的集中体现和主要标志是A.科学技术 B.劳动对象 C.劳动者 D.管理方式8.上层建筑的核心是A.社会意识形态B.政治法律思想C.国家政权D.政体9.我国社会主义初级阶段实行以公有制为主体、多种所有制经济共同发展的基本经济制度,促进了生产力的发展,说明实行这种制度遵循了A. 生产力决定生产关系的原理B. 经济基础决定上层建筑的原理C. 社会存在决定社会意识的原理D. 经济制度决定生产力状况的原理11.人类社会历史发展的决定力量是A.生产方式B.地理条件C.社会意识D.人口因素12.人类社会发展的一般规律是A.生产方式内部的矛盾规律B. 生产力和生产关系、经济基础和上层建筑之间的矛盾运动规律C.社会存在和社会意识的矛盾规律D.物质生产和精神生产的矛盾规律13. “任何英雄人物的历史作用都不能超出他们所处历史条件所许可的范围”这种看法是A、宿命论观点B、机械论观点C、历史循环论观点D、历史唯物主义观点参考答案:1-5 DCBCD 6-10 CACAA 11-13 ABD二、多项选择题1.社会存在包括A.社会生产的各种物质条件B. 社会生产的物质生产活动C.经济关系D. 全部社会关系2.生产关系的客观性是指A.人们不能自由选择生产关系B.人们不能随意创造或消灭某种生产关系C.生产关系是社会有机体中客观实在的组成部分D.生产关系是社会上层建筑的物质基础3. “历史不过是追求着自己目的的人的活动而已”,这一观点表明A.人们自己创造自己的历史B.历史不是神创造的C.历史是人们任意创造的D.历史是人思想发展史4.“时势造英雄”和“英雄造时势”A.是两种根本对立的观点B.这两种观点是相互补充的C.前者是历史唯物主义,后者是历史唯心主义D.前者是科学历史观,后者是唯心史观5.历史发展是“合力”作用的结果,这就是说A. 历史发展无规律可循B. 历史发展是无法认识的C. 历史发展的因素是复杂的D. 社会中的每个人是“合力”的一部分6. “如果资本主义的灭亡是由科学保证了的,为什么还要费那么大的力气去安排它的葬礼呢?”这种观点的错误在于A. 抹煞社会规律实现的特点B. 否认革命在社会质变中的作用C. 否认历史观上的决定论原则D. 否认科学是推动历史前进的革命力量7.上层建筑对经济基础的能动作用在于A.它为自己的经济基础服务B.它要促进自己经济基础的形成、巩固和发展C.它决定自己所服务的经济基础的性质D.它要排除自己经济基础的对立物参考答案:1.ABC2.ABCD3.AB4.ACD5.CD6.AB7.ABD三、简答题1.怎样理解生产力和生产关系的辩证关系?2.怎样理解经济基础和上层建筑的辩证关系?3.如何理解社会意识的相对独立性?4.如何理解社会存在和社会意识这两个概念?5.唯物史观的基本观点有哪些?6.什么是经济基础,如何理解经济基础这一概念的内涵?简答题1、2、3、4、6参见教科书。
第三章习题及答案

第三章练习题一、填空题1、从国际经济地理的分布上看,发达国家大都分布在北方,发展中国家大都分布在南方,因此,国际经济学界有时将这种发达国家与发展中国家的产业间贸易称作。
2、规模经济指企业的平均成本随着整个行业生产规模的不断扩大而下降。
3、不以要素禀赋差异为基础,而以规模经济和差异产品为基础的国际贸易是贸易。
4、外部规模经济下的国际分工与贸易模式是不可预测的,在很大程度上由因素决定。
5、从技术转移的角度探讨比较优势动态演变的贸易理论是技术差距理论和理论。
6、重叠需求理论认为,是影响一国需求结构的最主要因素。
7、1961年瑞典经济学家提出了重叠需求理论,从需求的角度探讨了国际贸易发生的原因。
8、国际贸易理论最新的发展方向之一是将技术作为贸易的内生变量来分析,既研究技术变化的原因,也研究作为生产和贸易结果的技术进步对与社会福利的影响。
9、在国内投资乘数理论的基础上,凯恩斯的追随们引申出理论。
10、战略性贸易理论的基本内容是利用关税分享外国企业的垄断利润和。
11、贸易政策有两大基本类型,即和保护贸易政策。
12、美国1988年在中修订过301条款。
13、就是以国内生产的工业品代替进口产品的政策。
14、指用工业制成品和半制成品的出口代替初级产品出口的政策。
15、除比较优势外,成为国际贸易的一个独立的基础和源泉。
16、某种商品的进口大国设置一定程度的关税会使贸易条件向有利于本国不利于外国的方向转化,使国内实际收入最大化,这种程度关税叫。
二、判断题1、如果厂商的生产具有规模报酬递增的特征,那么该厂商一定存在规模经济,但规模经济不一定要求规模报酬递增。
2、一个只存在外部规模经济的行业一般由大量较小的厂商构成。
3、外部规模经济下的国际分工与贸易格局在很大程度上由历史或偶然因素决定。
4、市场规模大的国家生产的差异化产品种类一般较多。
5、新制度经济学认为,所有交易集中在一个地方可以改进交易效率,只要交易效率改进带来的收益大于该地区地价上升产生的成本,行业还会进一步向该地区及其周边集中。
第三章习题参考答案

第三章 缓冲溶液习题参考答案1. 在1L 1.0×10-5mol ·L -1 NaOH 溶液中,加入0.001molNaOH 或HCl ,溶液的pH 怎样改变?解:ΔpH 1≈11-9=2;ΔpH 2≈3-9=-62. 设有下列三种由乳酸和乳酸钠组成的缓冲溶液,分别计算它们的pH 值(25℃时乳酸的K a = 1.4×10-4)。
(1)1L 溶液中含有0.1mol 乳酸和0.1mol 乳酸钠。
(2)1L 溶液中含0.1mol 乳酸和0.01mol 乳酸钠。
(3)1L 溶液中含0.01mol 乳酸和0.1mol 乳酸钠。
解:(1)85.31.01.0lg )104.1lg(lg p [HB]][B lg p pH 4HB B a a =+⨯-=+=+=--n n K K (2)85.21.001.0lg )104.1lg(lg [HB]][B lg p pH 4HB B a a =+⨯-=+=+=--n n pK K (3)85.401.01.0lg )104.1lg(lg [HB]][B lg p pH 4HB B a a =+⨯-=+=+=--n n pK K 3. 正常血浆中具有H 2PO 4--HPO 42-缓冲系,H 2PO 4-的p K a2 = 6.8(校正后),已知正常血浆中[HPO 42-]/[H 2PO 4-]为4/1,试求血浆的pH 值;尿中[HPO 42-]/[H 2PO 4-]为1/9,试求尿的pH 值。
解:血浆的pH 值:40.714lg 8.6[HB]][B lg p pH a =+=+=-K 尿液的pH 值:84.591lg 8.6[HB]][B lg p pH a =+=+=-K 4. 将0.15mol ·L -1 NaOH 溶液0.1mL 加于10mL pH 值为4.74的缓冲溶液中,溶液的pH 值变为4.79,试求此缓冲溶液的缓冲容量。
第三章练习题-答案

第三章练习题一、单选题1. ()是网上市场调研中最有效并经常使用的一种方法。
(A)(A)网上问卷调研(B)新闻组讨论(C)电子邮件(D)网上问答2. 以下()选项符合调研表问题设计要求?(C)(A)这种调料很润口吧(B)这种调料很辛辣吧(C)这种调料是润口还是辛辣呢(D)这种调料的口味是否很可口?3. 商家要开展电子商务活动,应该用( )作为其主要的生意平台。
(C)A.BBS B.电子邮件 C.在线商店 D.电话定购4. ()是商店生成系统的核心。
(D)(A)前台商务系统(B)后台数据系统(C)站点管理系统(D)店面管理系统5. 因为网络广告()的特征,使得公司在网络上许多位置放置公司的广告和相关产品介绍。
(C)(A)回馈快(B)效率高(C)成本低(D)交互强6. 在对竞争对手的研究的调研活动中,()发挥着重要作用。
(B)(A)网上直接调研(B)网上间接调研(C)E-mail问卷(D)Focus-Group7、网上市场调研可以充分利用Internet的开放性、()、平等性、广泛性和直接性等特点开展。
A.A.自由性B.规范性C.交叉性D.单一性8.()选项符合调研表问题设计要求。
C.A.这种调料很润口吧B.这种调料很辛辣吧C.这种调料是润口还是辛辣呢D.这种调料的口味是否很可口9.利用互联网进行市场调查所遵循的原则不包括()AA.公开被调查者的个人信息B.提高样本分布的均衡性C.在线调查表的设计便于结果表明处理D.开展定制化营销10.()策略多运用于高档消费。
D.A.抢先定位B.比附定位C.空隙定位D.品牌形象定位11.(A)是将工作的主要阶段按照阶段里程碑进行划分。
A、时间计划B、人力资源计划C、成本计划D、风险计划12.商店生成系统中最重要的模块是()。
BA.前台商务系统B.商家店面管理系统C.站点后台管理系统D.售后服务管理系统13.网上购物的一般流程是:进入网上商城-查找选购商品-查看-修改购物车-()-订单生成-订单跟踪。
第三章练习题(答案)

第三章练习题一、单选1、(A)是本—量—利分析最基本的假设,是本—量—利分析的出发点。
A、相关范围假设B、模型线性假设C、产销平衡假设D、品种结构不变假设2、在各种盈亏临界图中,(B)更符合变动成本法的思路。
A、传统式B、贡献毛益式C利量式D、单位式3、在单位盈亏临界图中,产品销售单价线与(A)的交点即为盈亏临界点。
A单位成本线B单位固定成本线C单位变动成本线D利润线4、已知A企业为生产和销售单一产品企业,A 企业计划年度销售量为1000件,销售单价为50元,单位变动成本30元,固定成本总额25000元,则销售量、单价、单位变动成本、固定成本各因素的敏感程度由高到低排列是(C)A、单价>销售量>单位变动成本>固定成本B、单价>单位变动成本>销售量>固定成本C、单价>单位变动成本>固定成本>销售量D、单价>销售量>固定成本>单位变动成本5、在利量式盈亏临界图中,若横轴代表销售额,则利润线的斜率代表(C)A、单位边际贡献B、变动成本率C、边际贡献率D、单位变动成本6、某企业只生产一种产品,单位变动成本为36元,固定成本总额4000元,产品单位售价56元,要使安全边际率达到50%,该企业的销售量应达到(A)件。
A、400B、222C、143D、5007、下列各式中,其计算结果不等于变动成本率的是(B)A 、1-边际贡献率B、1-达到盈亏临界点的作业率C、单位变动成本/单价×100%D、变动成本/销售收入×100%8、下列措施中只能提高安全边际而不能降低盈亏临界点的是(B)A、提高单价B、增加销售量C、降低单位变动成本D、压缩固定成本开支9某单位某产品的单价为40元,单位变动成本为30元,固定成本为20000元,目标净利润为26800元,所得税税率为33%,则实现目标净利润的销售量为(A)。
A、6000件B、5000件C、4680件D、5500件10、下列因素单独变动时,不会导致盈亏临界点随之变动的是(A)A、销售量B、单位变动成本C、固定成本D、单价11、下列各项指标中,其数值越小,说明企业经营的安全程度越大的是(D)A、安全边际率B、经营杠杆率C、边际贡献率D、达到盈亏临界点作业率12、某企业只经营一种销量不稳、单位边际贡献大于零、盈亏临界点销售量为1600件的产品。
第三章练习题及答案

(一) 填空题1.在高温热源T 1和低温热源T 2之间的卡诺循环, 其热温熵之和()1212Q Q T T +=。
循环过程的热机效率()η=。
2.任一不可逆循环过程的热温熵之和可以表示为()0Q T δ⎛⎫⎪⎝⎭⎰不可逆。
3.在绝热密闭的刚性容器中发生某一化学反应,此过程的()sys 0S ∆;()amb0S ∆。
4.系统经可逆循环后,S ∆( )0, 经不可逆循环后S ∆( )。
(填>,=,<)。
5.某一系统在与环境300K 大热源接触下经历一不可逆循环过程,系统从环境得到10kJ 的功,则系统与环境交换的热()Q =;()sysS∆=;()ambS∆=。
6.下列过程的△U 、△H 、△S 、△G 何者为零? ⑴ 理想气体自由膨胀( );⑵ H 2(g )和Cl 2(g )在绝热的刚性容器中反应生成HCl (g )的过程( ); ⑶ 在0 ℃、101.325 kPa 下水结成冰的相变过程( )。
⑷ 一定量真实气体绝热可逆膨胀过程( )。
⑸ 实际气体节流膨胀过程( )。
7.一定量理想气体与300K 大热源接触做等温膨胀,吸热Q =600kJ,对外所做功为可逆功的40%,则系统的熵变()S ∆=。
8. 1 mol O 2(p 1,V 1,T 1)和1 mol N 2(p 1,V 1,T 1)混合后,总压为2 p 1,总体积为V 1,温度为T 1,此过程的△S ( )0(填>,<或=,O 2和N 2均可看作理想气体)。
9.热力学第三定律用公式表示为:()()*m S =。
10. 根据 d G =-S d T+V d p 可知任一化学反应的 (1)r m ΔTG p ⎛⎫∂= ⎪∂⎝⎭( ); (2)r m ΔP G T ∂⎛⎫= ⎪∂⎝⎭( ); (3)r m ΔPV T ∂⎛⎫= ⎪∂⎝⎭( )。
11.某理想气体在500 K 、100 kPa 时,其m TS p ⎛⎫∂= ⎪∂⎝⎭ ( )(要求填入具体数值和单位)。
第三章习题(答案)

第三章辛亥革命与君主专制制度的终结一、单项选择题1. 1903年6月,()在上海《苏报》发表《驳康有为论革命书》,批驳康有为所谓“中国之可立宪,不可革命”的谬论A.陈天华B.邹容C.章炳麟D.梁启超2.1903年邹容写的()是中国近代史上第一部宣传革命和资产阶级共和国思想的著作A.《猛回头》B.《警世钟》C.《革命军》D.《驳康有为论革命书》3.中国近代第一个资产阶级革命政党是()A.强学会B.兴中会C.同盟会D.国民党4. 孙中山三民主义思想的核心是()A.驱除鞑虏B.恢复中华C.创立民国D.平均地权5.1905年11月,孙中山在《民报》发刊词中将中国同盟会的政治纲领概括为()A.创立民国、平均地权B.驱除鞑虏、恢复中华、创立合众政府C.民族主义、民权主义、民生主义D.联俄、联共、扶助农工6.武昌起义前同盟会领导的影响最大的武装起义是()A.广州起义B.萍浏醴起义C.镇南关起义D.黄花岗起义7.中国历史上第一部具有资产阶级共和国宪法性质的法典是()A.《钦定宪法大纲》B.《中华民国临时约法》C.《中华民国约法》D.《试训政纲领》8. 辛亥革命取得的最大成就是()A.推翻了封建帝制B.促进了资本主义的发展C.使人民获得了一些民主自由权利D.打击了帝国主义的殖民势力9. 南京临时政府的局限性表现为()A.承认清政府与列强所订的一切不平等条约和一切外债有效B.没有提出任何可以满足农民土地要求的政策和措施C.维护封建土地制度以及官僚、地主所占有的土地财产D.主体是资产阶级革命派10. 二次革命失败的最重要原因是()A.革命党人军队不足B.国民党力量涣散C.袁世凯军队强大D.袁世凯得到帝国主义的支持11.1915年,()在云南率先举起反袁护国的旗帜,发动护国战争A.黄兴B.段祺瑞C.蔡锷D.孙中山12.资产阶级革命派开展护国运动的主要原因是()A.袁世凯指使刺杀宋教仁B.袁世凯强迫国会选举他为正式大总统C.袁世凯解散国会D.袁世凯复辟帝制13. 袁世凯为复辟帝制不惜出卖主权,与日本签订了卖国的()A.中日共同防敌军事协定B.承认外蒙自治C.“二十一条”D.出让川汉、粤汉铁路14. 1917年孙中山针对()指出“以假共和之面孔,行真专制之手段”,并举起“护法”旗帜A.黎元洪B.张勋C.张作霖D.段祺瑞15.标志着整个中国民族资产阶级领导的旧民主主义革命终结的是()A.二次革命的失败B.护国运动的失败C.护法运动的失败D.保路风潮的失败16.20世纪初主张“实业救国”的著名实业家楷模是()A.张謇B.周学熙C.荣宗敬D.荣德生二、多项选择题1.《辛丑条约》的签订,标志着()。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第3章习题1 请解释为什么在大多数情况下固体间的反应都很慢?怎样才能加快反应速率?答:固相反应是复相反应,反应主要在界面间进行,反应速率由离子的相间扩散所决定,并且固体物质接触面积相对较小,混合不均匀,碰撞概率小,因而大多数情况下反应很慢。
通过充分破碎和研磨,或通过各种化学途径制备粒度细、比表面大、表面活性高的反应物原料,或提高反应温度等均可加快反应速率。
2 化学转移反应适合提纯具有什么特点的金属?你能举例说明吗?答:化学转移反应适合提纯熔点高,在高温下难以挥发的金属。
如金属钛的提纯。
钛的熔点高达1 933±10 K,沸点是3 560 K,高温下难挥发,但钛和碘在低温下能够形成TiI4,在高温下TiI4又容易分解,所以可以采用化学转移反应提纯钛。
3 低温合成适用哪类物质的合成?常用的制冷浴有哪些?答:用于低温合成的化合物主要是一些易挥发的化合物,例如,C3O2、CNCl、HCN、PH3、(CN)2、稀有气体化合物等。
常用的制冷浴有冰盐共熔体系、干冰浴和液氮。
4 高温合成包括哪些类型?答:高温合成主要包括以下类型:高温下的固相合成反应;高温下的固-气合成反应;高温下的化学转移反应;高温熔炼和合金制备;高温下的相变合成;高温熔盐电解;等离子体激光、聚焦等作用下的超高温合成;高温下的单晶生长和区域熔融提纯等。
5 彩色三基色稀土荧光粉是如何制备的?分别举例予以说明。
答:彩色电视机的显像屏是由红、蓝、绿(三基色)三种颜色的荧光粉组成的。
红粉Y2O2S:Eu的制备方法用稀HNO3或稀HCl溶解质量比为1:(0.062~0.07)的Y2O3和Eu2O3的混合稀土氧化物,用去离子水稀释到每1 mL含Y2O3大约10 mg,再用稀氨水调节pH值到2~3,并加热到80 ℃。
慢慢加入过量的草酸溶液,直至沉淀完毕,使沉淀静置几小时后抽滤,水洗至中性。
其反应过程如下:Y2O3+ Eu2O3+H+—→Y3++ Eu3++H2OY3++ Eu3++H2C2O4—→ (Y, Eu)2(C2O4)3·xH2O将草酸钇铕(Y, Eu)2(C2O4)3·xH2O于120 ℃下烘干脱水,再于800~1 000 ℃下灼烧1 h,便得到制备红粉的原料(Y, Eu)2O3:(Y, Eu)2(C2O4)3·xH2O —→ (Y, Eu)2O3+CO2↑+ CO↑+ xH2O↑然后,将质量比为100:30:30:5的(Y, Eu)2O3:S:Na2CO3:K3PO4(作助熔剂)混磨均匀,装入石英管中压紧,覆盖适量的硫磺及次料,加盖盖严,于1 150~1 250 ℃下恒温1~2 h,高温出炉,冷至室温。
在365 nm紫外光激发下选粉,用水或浓度为2~4 mol·L-1的HCl浸泡后再用热水洗至中性,抽滤、烘干、过筛,即得白色的Y2O2S:Eu红色发光粉。
反应为:Na2CO3+ S —→ Na2S+ Na2S x+ CO2↑(Y, Eu)2O3+ Na2S + Na2S x—→Y2O2S : Eu绿粉(Ce, Tb)MgAl11O19的制备方法按一定的比例将Al2O3(79 %)、MgCO3(5 %)、CeO2(9 %)、Tb4O7(5 %)、H3BO3(2 %,作助熔剂)混合研磨均匀后,装入石英坩埚,先在1 350 ℃灼烧2 h,取出粉碎磨匀,再装入刚玉坩埚于1 400 ℃灼烧1 h,粉碎,过200目筛即为产品。
蓝粉((Ba, Mg, Eu)3Al14O24)的制备按一定比例称取B2F2CO3、MgCO3、Mg(OH)2·5H2O、Eu2O3、Al2O3、H3BO3,混合磨匀,然后装入石英管中,并通入CO,在1 300 ℃灼烧还原1.5 h,出炉冷却后,粉碎,过200目筛,即为产品。
高温灼烧,是使物料发生高温固相反应生成晶体。
还原是使晶体中的Eu(Ⅲ)还原成Eu(Ⅱ),其还原剂是CO。
6 画出下列萃取剂的结构:162163 MIBK TBP N 263 P 204 HTTA解答:MIBK(甲基异丁基酮):TBP(磷酸三丁酯): N 263(氯化三烷基甲胺):[CH 3(CH 2)6~10CH 2]3N +Cl-P 204(二(2-乙基己基)磷酸):HTTA(噻吩甲酰基三氟丙酮)7 Xe(b.p.-109 ℃)、AsH 3(b.p.-62.5 ℃)和As 2H 4(b.p.100 ℃)的混合物通过蒸馏分离进入三个串联的冷阱里,在每一个冷阱处,你要采用哪种糊状浴或制冷剂?答:在第一处冷阱采用冰盐共熔体系,可以将As 2H 4冷凝下来;在第二处冷阱采用干冰浴,可以将AsH 3冷凝下来;在第三处冷阱采用液氮,可以将Xe 冷凝下来。
8 获得等离子体较实用的方法有哪些?答:较实用的获得等离子体的方法是放电法,如各种电弧放电、辉光放电、高频电感耦合放电、高频电容耦合放电和诱导放电等。
9 由氯化钾的电解氧化来制备氯酸钾,通1 A 电流2 h ,假设电流效率为50 %,可以得到多少克氯酸钾?解:电量Q =It =1 A ×(3 600×2) s =7 200 C氯化钾到氯酸钾的半反应为 Cl --6e =Cl 5+电解产生1 mol KClO 3(122.55 g)需要6×96 500 C 电量,因此7 200 C 电量应电解得到122.55× 7 200/(6×96 500)=1.52 g实际得到的氯酸钾为 1.52 × 50 % = 0.76 g10 说明为什么在汞阴极上还原钠离子是可能的,虽然水还原成氢是热力学上最有利的过程。
你应该怎样改变pH 值和温度去影响电流效率?答:虽然水还原成氢是热力学上最有利的过程,但如果采用汞为阴极,并且增高电流密度,由于H 2在汞上具有很高的过电位,因而能使Na +先在汞阴极上放电析出而变成钠汞齐。
为了提高电流效率,可以增大溶液pH 值(即降低H +浓度),适当提高温度。
11 用含氧酸盐煅烧制取氧化物时,常使用挥发性酸的盐,特别是碳酸盐,为什么?答:用含氧酸盐煅烧制取氧化物时,常使用挥发性酸的盐,这是因为分解时酸性氧化物容易逸出,这有利于平衡向右移动,分解更完全,产物比较纯。
之所以用碳酸盐,是因为它的分解温度更低。
12 为什么紫外-可见光谱能应用于金属配位化合物的鉴定?答:金属离子与配体反应生成配合物的颜色一般不同于游离金属离子(水合离子)和配体本身的颜色。
配合物的形成均可使最大吸收峰显著红移或紫移,摩尔吸光系数明显提高。
利用紫外-可见光谱可以研究配合物的电子跃迁、荷移吸收光谱和配体内电子跃迁,因而能够应用于金属配合物的鉴定。
13 有以下反应:CH 3CH 3CH CH 2C O CH 3C 4H 9OC 4H 9OC 4H 9OO CH 3(CH 2)32C 2H 5CH 3(CH 2)3CHCH 2C H O CF 3CH 3164A 是气体,相对分子质量为28,B 的红外光谱在1 880~2 000 cm -1处有三个吸收带,B 的核磁共振氢谱有四个相等强度的峰,B 为非电解质,C 为电解质,C 的红外光谱图在1 950~2 030 cm -1处有三个吸收带,其核磁共振氢谱只有一个峰,试推测B 和C 的结构。
解:由反应方程式和已知条件可知,B 的化学式为Mo(CO)3(C 7H 8),环庚三烯置换了三个CO ;C 的化学式为[Mo(CO)3(C 7H 7)]+BF 4-,环庚三烯中亚甲基上的氢以H -形式掉下并与Ph 3C +结合。
B和C 的结构分别如下所示:14 右图为MnCO 3在N 2中的热分析曲线。
试分析TGA曲线上每一阶段和DTA 曲线上每个峰对应的热分解过程,写出热分解反应方程式。
解:第一阶段:0~400℃,MnCO 3 —→ MnO 2 + CO第二阶段:400~550℃,MnO 2 —→ Mn 2O 3 + 1/2 O 2 第三阶段:550~900℃,Mn 2O 3 —→ Mn 3O 4 + 1/2 O 2 15 在高温合成反应中,为了降低烧结温度,提高材料的性能,常采取改善固相反应原料的手段,即前驱体法。
试以实例说明常用的几种前驱体方法。
答:常用的前驱体方法包括将反应物充分破碎和研磨,或通过各种化学途径制备成粒度细、比表面积大、表面具有活性的反应物原料,然后通过加压成片,甚至热压成型使反应物颗粒充分均匀接触;或通过化学方法使反应物组分事先共沉淀;或通过化学反应制成化合物前驱物。
其中共沉淀法是获得均匀反应前驱物的常用方法。
例如,合成ZnFe 2O 4尖晶石时使用的共沉淀法是用锌和铁的草酸盐作为反应物,以1 : 1的比例溶在水中,将溶液混合,加热蒸发,锌和铁的草酸盐一起产生共沉淀。
将沉淀过滤、焙烧得到产物。
由于混合的均匀程度很高,反应所需的温度可以降低很多。
溶胶-凝胶法也是一种常用的前驱体方法。
这是一种近期发展起来的能代替共沉淀法制备陶瓷、玻璃和许多固体材料的新方法。
例如超导氧化物膜YBa 2Cu 3O 7-x 的制备是以化学计量比的相关硝酸盐Y(NO 3)3·H 2O 、Ba(NO 3)2、Cu(NO 3)2·H 2O 作起始原料,将它们以一定的比例溶于乙二醇中生成均匀的混合溶液,然后在一定的温度下(如130~180 ℃)反应,蒸发出溶剂,生成的凝胶在高温(950 ℃)氧气氛下进行灼烧即可获纯的正交型YBa 2Cu 3O 7-x 。
A Ph 3CBF 4(惰性溶剂中)MoC 10H 7O 3BF 4(C)MoC H 8O 3(B)Mo(CO)+Ph 3CH (第14题) Mo CO COCO [BF 4]-。
