大肠菌群MPN检索表 国标
食品中大肠菌群检测及注意事项

食品中大肠菌群检测及注意事项大肠菌群(Coliform bacteria)是指一群能发酵乳糖、产酸产气、需氧和兼性厌氧的革兰氏阴性无芽胞杆菌。
该菌主要来源于人畜粪便,故以此作为粪便污染指标来评价食品的卫生质量,推断食品中是否有污染肠道致病菌的可能。
大肠菌群分布较广,在温血动物粪便和自然界中广泛存在。
检测方法MPN检索表使用GB/T 4789.3-2023检索表中阳性管数是以1mL(g)×3、0.1mL(g)×3和0.01mL(g)×3的梯度进行表示,GB 4789.3-2023阳性管数是以0.10、0.01和0.001的梯度表示,均根据稀释倍数推算结果,结果相同。
推算方法以GB 4789.3-2023为例,改用1g(mL)、0.1g(mL)和0.01g(mL)时,表内数字应相应降低10倍;如改用0.01g(mL)、0.001g(mL)和0.0001g(mL)时,则表内数字应相应增高10倍,其余类推即可。
常用标准常见问题及解答1、如何选择检测方法?答:你要依据产品的执行标准去选择检测方法,不是说你喜爱那种就可以用那种。
2、03版的结果能不能和10版的结果进行换算和比较?答:其实换算是不行的,这个两个不同的标准。
假如只是进行比较两个结果是可以的,但是不建议。
3、同一批产品,检测的两份结果不一样,是不是那里出问题?答:其实不是出问题,这个是正常的,同一批产品不代表他们的微生物检测结果是一模一样的,假如是这样也没必要做五份去验证产品合格了吧?假如说同一份样品(制成一份样)消失结果差好远的话,这里就要去分析那里出问题。
样品采集怎样采样,才能使样品具有代表性?这里将样品分为两类:预包装食品和散装食品或现场制作食品1、对于预包装食品① 应采集相同批次、独立包装、适量件数的食品样品,每件样品的采样量应满意微生物项目检验的要求。
② 独立包装小于、等于1000g 的固态食品或小于、等于1000mL 的液态食品,取相同批次的包装。
食品中大肠菌群的测定含MPN检索表

⾷品中⼤肠菌群的测定含MPN检索表实验六⾷品中⼤肠菌群的测定⼀、概述(⼀)⼤肠菌群的定义及范围根据国家1994年颁布的⾷品卫⽣检验⽅法微⽣物学部分,⼤肠菌群(coliform bacteria)系指⼀群在37℃、24h能发酵乳糖,产酸、产⽓,需氧和兼性厌氧的⾰兰⽒阴性⽆芽胞杆菌。
⼤肠菌群主要是由肠杆菌科中四个菌属内的⼀些细菌所组成,即艾希⽒菌届、拘橼酸杆菌属、克雷伯⽒菌属及肠杆菌属,其⽣化特性分类见表5-4。
表5-4 ⼤肠菌群⽣化特性分类表注:+,表⽰阳性;—,表⽰阴性;+/-,表⽰多数阳性,少数阴性。
由上表可以看出,⼤肠菌群中⼤肠艾希⽒菌I型和Ⅲ型的特点是,对靛基质、甲基红、v-P和拘橼酸盐利⽤四个⽣化反应分别为“⼗⼗⼀⼀”,通常称为典型⼤肠杆菌;⽽其他类⼤肠杆菌则披称为⾮典型⼤肠杆菌。
(⼆)⼤肠菌群的测定意义1、粪便污染的指标细菌早在1892年,沙尔丁格(Schardinger)⽒⾸先提出⼤肠杆菌作为⽔源中病原菌污染的指标菌的意见,因为⼤肠杆菌是存在于⼈和动物的肠道内的常见细菌。
⼀年后,塞乌博⽿德“斯密斯(Theobold.Smith)⽒指出,⼤肠杆菌因普遍存在于肠道内,若在肠道以外的环境中发现,就可以认为这是由于⼈或动物的粪便污染造成的;从此,就开始应⽤⼤肠杆菌作为⽔源中粪便污染的指标菌。
据研究发现,成⼈粪便中的⼤肠菌群的含量为:108个/g⼀109个/g。
若⽔中或⾷品中发现有⼤肠菌群,即可证实已被粪便污染,有粪便污染也就有可能有肠道病原菌存在。
根据这个理由,就可以认为这种含有⼤肠菌群的⽔或⾷品供⾷⽤是不安全的。
所以⽬前为评定⾷品的卫⽣质量⽽进⾏检验时,也都采⽤⼤肠菌群或⼤肠杆菌作为粪便污染的指标细菌。
当然,有粪便污染,不⼀定就有肠道病原菌存在,但即使⽆病原菌,只要被粪便污染的⽔或⾷品,也是不卫⽣的,不受⼈喜欢的。
2.粪便污染指标菌的选择作为理想的粪便污染的指标菌应具备以下⼏个特性,才能起到⽐较正确的指标作⽤。
gb7101标准中大肠菌群标准

gb7101标准中大肠菌群标准1目的规范食品中大肠菌群计数测定的标准操作规程。
2范围本标准规定了食品中大肠菌群(Coliforms)计数的方法。
本标准适用于食品中大肠菌群的计数。
3术语和定义3.1 大肠菌群coliforms在一定培养条件下能发酵乳糖、产酸产气的需氧和兼性厌氧革兰氏阴性无芽胞杆菌。
3.2 最可能数most probable number,MPN基于泊松分布的一种间接计数方法。
4责任质量部组织制订、化验室负责实施。
5内容5.1 设备和材料除微生物实验室常规灭菌及培养设备外,其他设备和材料如下:5.1.1 恒温培养箱:36 ℃±1 ℃。
5.1.2 冰箱:2 ℃~5 ℃。
5.1.3 恒温水浴箱:46 ℃±1 ℃。
5.1.4 天平:感量0.1 g。
5.1.5 均质器。
5.1.6 振荡器。
5.1.7 无菌吸管:1 mL(具0.01 mL 刻度)、10 mL(具0.1 mL 刻度)或微量移液器及吸头。
5.1.8 无菌锥形瓶:容量500 mL。
5.1.9 无菌培养皿:直径90 mm。
5.1.10 pH 计或pH 比色管或精密pH 试纸。
5.1.11 菌落计数器。
5.2培养基和试剂5.2.1 月桂基硫酸盐胰蛋白胨(Lauryl Sulfate Tryptose,LST)肉汤:见附录A 中A.1。
5.2.2 煌绿乳糖胆盐(Brilliant Green Lactose Bile,BGLB)肉汤:见附录A 中A.2。
5.2.3 结晶紫中性红胆盐琼脂(Violet Red Bile Agar,VRBA):见附录A 中A.3。
5.2.4 磷酸盐缓冲液:见附录A 中A.4。
5.2.5 无菌生理盐水:见附录A 中A.5。
5.2.6 无菌1 mol/L NaOH:见附录A 中A.6。
5.2.7 无菌1 mol/L HCl:见附录A 中A.7。
5.3大肠菌群MPN 计数法5.3.1 检验程序大肠菌群MPN计数的检验程序见图1。
关于新国标大肠菌群MPN表的理解问题

关于新国标大肠菌群MPN表的理解问题MPN, 国标, 大肠菌群刚才翻看论坛微生物板块,看到有多个贴子都在讨论新国标大肠菌群的MPN表问题,感觉大家的理解千差万别。
我也曾经做过几年微生物检测,把我的理解整理一下,也许对大家有些用处。
1、新国标的MPN表的基准问题。
新国标的MPN表采用了3个稀释度,分别是十倍-百倍-千倍,加样量是3管,每管1毫升,意味着加入样品的量为0.333克。
在样品加入量为0.333克的情况下,使用新国标MPN表,得到MPN/克的数值。
2、改变加样量的问题。
在实际操作中,因为一些原因需要改变加样量,一般是10倍增加或者降低,同样使用本表,得到的数值需要做10倍调整。
比如:加样量为3.33克(这样的情况一般是十倍稀释液用3管,每管10毫升,需要用双料管。
十倍百倍稀释液,各用三管,每管1毫升)。
这样查表得到的数值,应该降低10倍。
加样量为3.33克,阳性管为2-1-0,查表为15,这样的话,结果应该为 MPN 1.5/克,或者MPN 15/10克,或者MPN 150/100克。
再比如:加样量为0.0333克(这样的情况是,不使用十倍稀释液,而使用百倍-千倍-万倍稀释液,各用三管,每管1毫升)。
这样查表得到的数值,应该增高10倍。
加样量为0.0333克,阳性管为2-1-0,查表为15,这样的话,结果应该为 MPN 150/克,或者MPN 1500/10克,或者MPN 15000/100克。
3、关于和产品标准对应的问题。
大家应该注意到,这个问题其实是一个稀释度的选择问题。
另外,这个问题也可以回答是否可以直接换算的问题。
比如:某产品要求MPN<30 /100克。
在这种情况下,我们如果使用加样量0.333,如果全部是阴性0-0-0,得到的结果为<3/克,或者是<30/10克,或者是<300/100克。
很明显,在这种加样量情况下是不能做出是否符合结果的判定的。
这样的话,就需要增加加样量,变成加样量为3.33克,如果全部是阴性0-0-0,得到结果为<0.3/克,或者是<3/10克,或者是<30/100克。
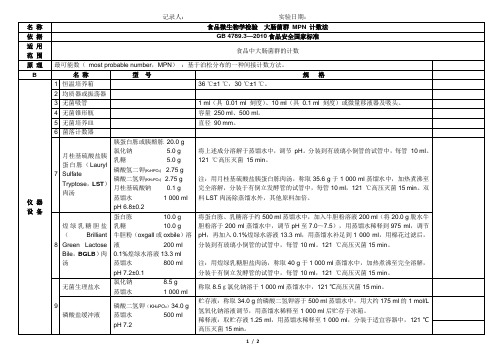
食品微生物学检验 大肠菌群 MPN 计数法
9
无菌生理盐水
氯化钠8.5 g
蒸馏水1 000ml
称取8.5g氯化钠溶于1 000ml蒸馏水中,121 ℃高压灭菌15 min。
磷酸盐缓冲液
磷酸二氢钾(KH2PO4)34.0 g
磷酸氢二钾(K2HPO4)2.75 g
磷酸二氢钾(KH2PO4)2.75 g
月桂基硫酸钠0.1 g
蒸馏水1 000ml
pH 6.8±0.2
将上述成分溶解于蒸馏水中,调节pH。分装到有玻璃小倒管的试管中,每管10ml。121℃高压灭菌15 min。
注:用月桂基硫酸盐胰蛋白胨肉汤,称取35.6 g于1 000ml蒸馏水中,加热煮沸至完全溶解,分装于有倒立发酵管的试管中,每管10ml,121℃高压灭菌15 min。双料LST肉汤除蒸馏水外,其他原料加倍。
蒸馏水500ml
pH 7.2
贮存液:称取34.0 g的磷酸二氢钾溶于500ml蒸馏水中,用大约175ml的1 mol/L氢氧化钠溶液调节,用蒸馏水稀释至1 000ml后贮存于冰箱。
稀释液:取贮存液1.25ml,用蒸馏水稀释至1 000ml,分装于适宜容器中,121 ℃高压灭菌15 min。
10
1 mol/L NaOH
如未产气则继续培养至48 h±2 h,产气者进行复发酵试验。
未产气者为大肠菌群阴性。
3
复发酵试验
用接种环从产气的LST肉汤管中分别取培养物1环,移种BGLB管中,36℃±1℃培养48 h±2 h,观察产气情况。
产气者,计为大肠菌群阳性管。
4
大肠菌群最可能数(MPN)的报告
大肠菌群检测(MPN法)

大肠菌群 (Coliforms)
一群在36℃培养48h可发酵乳糖产酸产气、需氧或兼性 厌氧的革兰氏阴性无芽孢杆菌。
该菌主要来源自人畜粪便,作为粪便污染指标评价食品 的卫生状况,推断食品中肠道致病菌污染的可能。
并非分类学概念,在生化及血清学方面并非完全一致。 一般认为包括大肠埃希氏菌、柠檬酸杆菌、肺炎克雷伯 氏菌和阴沟肠杆菌等。
大肠菌群计数MPN法流程图
GB 4789.3-2016(第一法)
检样
稀释
月桂基硫酸盐胰蛋白胨肉汤(LST)36±1℃,24~48±2h
不产气
产气 煌绿乳糖胆盐肉汤(BGLB) 36±1℃,24~48±2h
不产气 大肠菌群阴性
产气 大肠菌群阳性
报告
初发酵 复发酵
大肠菌群计数MPN法示意图
25g
移1ml
O26等) 侵袭性大肠杆菌(EIEC)——杆菌性痢疾 粘附性大肠杆菌(EAEC)——急慢性腹泻
大肠菌群、粪大肠菌群、大肠杆菌的关系
EIEC
ETEC
EHEC
O157:H7;O104:H4等
食品卫生学意义
是评价卫生质量的重要指标,作为食品中的粪便污染指标。 食品中检出大肠菌群,表明该食品有粪便污染,粪便中既有正常肠道菌,也可能
注意事项
归纳总结
目前很多产品大肠菌群标准要求单位为MPN/100mL(g),同2010版检测结果单位 MPN/100mL(g)不一致。中华人民共和国卫生部公告 2009第16号正式公告:现行食品标准 中规定的大肠菌群指标以“MPN/100克或MPN/100毫升”为单位的,适用《食品卫生微生物学 检验大肠菌群测定》(GB/T 4789.3-2003)进行检测;以“MPN/克或MPN/毫升”、“CFU/ 克或CFU/毫升”为单位的,适用《食品卫生微生物学检验大肠菌群计数》(GB/T 4789.3-2008) 进行检测。
食品安全国家标准——食品微生物学检验大肠菌群计数.pdf

食品安全国家标准食品微生物学检验 大肠菌群计数1 范围本标准规定了食品中大肠菌群(Coliforms)计数的方法。
本标准适用于食品中大肠菌群的计数。
2 术语和定义2.1 大肠菌群coliforms在一定培养条件下能发酵乳糖、产酸产气的需氧和兼性厌氧革兰氏阴性无芽胞杆菌。
2.2 最可能数most probable number,MPN基于泊松分布的一种间接计数方法。
3 设备和材料除微生物实验室常规灭菌及培养设备外,其他设备和材料如下:3.1 恒温培养箱:36 ℃±1 ℃。
3.2 冰箱:2 ℃~5 ℃。
℃℃。
3.3 恒温水浴箱:46 ±13.4 天平:感量0.1 g。
3.5 均质器。
3.6 振荡器。
3.7 无菌吸管:1 mL(具0.01 mL刻度)、10 mL(具0.1 mL刻度)或微量移液器及吸头。
3.8 无菌锥形瓶:容量500 mL。
3.9 无菌培养皿:直径90 mm。
3.10 pH计或pH比色管或精密pH试纸。
3.11 菌落计数器。
4 培养基和试剂4.1 月桂基硫酸盐胰蛋白胨(Lauryl Sulfate Tryptose,LST)肉汤:见附录A中A.1。
4.2 煌绿乳糖胆盐(Brilliant Green Lactose Bile,BGLB)肉汤:见附录A中A.2。
4.3 结晶紫中性红胆盐琼脂(Violet Red Bile Agar,VRBA):见附录A中A.3。
4.4 磷酸盐缓冲液:见附录A中A.4。
4.5 无菌生理盐水:见附录A中A.5。
4.6 无菌1 mol/L NaOH:见附录A中A.6。
4.7 无菌1 mol/L HCl:见附录A中A.7。
第一法 大肠菌群MPN计数法5 检验程序大肠菌群MPN计数的检验程序见图1。
图1 大肠菌群MPN计数法检验程序6 操作步骤6.1 样品的稀释6.1.1 固体和半固体样品:称取25 g样品,放入盛有225 mL磷酸盐缓冲液或生理盐水的无菌均质杯内, 8000 r/min~10000 r/min均质1 min~2 min,或放入盛有225 mL磷酸盐缓冲液或生理盐水的无菌均质袋中,用拍击式均质器拍打1 min~2 min,制成1:10的样品匀液。
大肠菌群最可能数(MPN)检索表
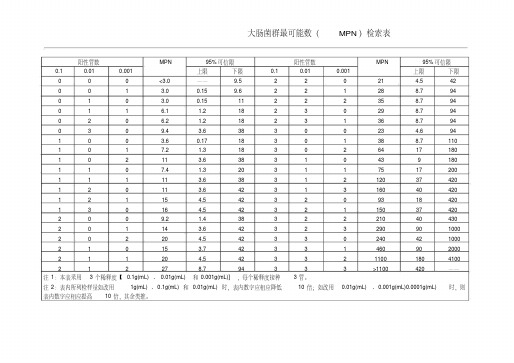
阳性管数MPN95%可信限阳性管数MPN95%可信限0.10.010.001上限下限0.10.010.001上限下限000<3.0——9.522021 4.542 001 3.00.159.6221288.794 010 3.00.1511222358.794 011 6.1 1.218230298.794 020 6.2 1.218231368.794 0309.4 3.63830023 4.694 100 3.60.1718301388.7110 1017.2 1.3183026417180 10211 3.638310439180 1107.4 1.3203117517200 11111 3.63831212037420 12011 3.64231316040420 12115 4.5423209318420 13016 4.54232115037420 2009.2 1.43832221040430 20114 3.642323********* 20220 4.542330********* 21015 3.742331460902000 21120 4.54233211001804100 212278.794333>1100420——注 1:本表采用 3 个稀释度【 0.1g(mL) 、 0.01g(mL)注 2:表内所列检样量如改用1g(mL) 、0.1g(mL) 和表内数字应相应提高10 倍,其余类推。
和 0.001g(mL)] ,每个稀释度接种0.01g(mL) 时,表内数字应相应降低3 管。
10 倍;如改用0.01g(mL)、0.001g(mL)0.0001g(mL)时,则一种微生物活菌数快速检测方法,其特征在于包括以下步骤:a)样品的选择:检测样品分为固体样品和液体样品;b)采样样品的制备:通过无菌操作取一定量溶液样品进行离心处理后,取上清液,再以更高的速度离心处理,弃去上清液,用移液器取出底部少量溶液;c)微生物活菌数的检测:将移液器取出的底部溶液,涂在载玻片上,经干燥固定,用美兰染色,冲洗后用生物显微镜镜检,记录被美兰染色且呈现空心状态的图像的个数来计数微生物数量。
