过敏原特异性IgE抗体检测试剂盒(化学发光免疫分析法)产品技术要求xinhualian
过敏原检测试剂盒说明书

过敏原检测试剂盒说明书本试剂盒采用管式酶免(ELISA)分析法,对人血清或血浆中的过敏原特异性IgE 抗体进行定性/半定量检测。
[概述]美国CORTEZ IgE抗体存在于具有过敏体质个体的血清中,这些个体在接触到特异性过敏原时主要出现速发型过敏反应的症状。
对血清中总IgE抗体水平的检测,可为判定机体对过敏的易感性提供有价值的信息。
而对血清中特异性过敏原检测可对患者进行脱敏治疗提供有力的依据。
皮试是常用的一种简单,低成本的体内过敏原检测方法,但皮试存在准确性低,结果不易判断以及危险性较大等缺点。
体外检测中的放射过敏吸附试验(RAST),荧光酶标法(FEIA)和酶标法(ELISA)已被用于定量检测来源于不同过敏原的IgE抗体。
过敏的临床症状主要包括过敏反应、花粉热、气喘、过敏性湿疹、皮炎、呼吸不畅和鼻炎。
通过检测大部分常见的过敏原或总IgE抗体来诊断过敏反应,就能更好地预防和治疗。
本试剂盒是一种体外定性/半定量的酶免法,可同时独立地检测各种常见的过敏反应,并估计人血清或血浆中IgE 的总水平。
这种独特的装置由一只反应管组成,反应管中含有一系列塑料段,在这些塑料段的表面包被有单一过敏原或过敏原混合物或单克隆抗体,这样,患者血清中的IgE抗体就可以与它们分别反应形成免疫复合物而沉淀下来。
由于过敏原的选择不同,本试剂盒检测的具体内容有多种形式。
每个反应管均带有阳性、阴性对照,有助于结果的分析。
[原理]当具有过敏抗原固化于表面的载体与病人血清培养在一起后,血清中特异性IgE(一抗)就会特异地结合到抗原上,此特异结合的抗体可被酶联的二抗所识别,加入显色剂后,二抗所联的酶使显色剂由黄色变成紫色。
显色的深度与血清中特异性IgE成正比;能半定量地检测血清中特异性IgE的浓度。
[贮存] 收到试剂盒后,应将试剂盒贮存在2-8℃。
[标本收集] 患者无需特殊的准备,也无需禁食。
使用血清或血浆。
标本不需稀释,反应管内吸入标本量约600l。
过敏原特异性抗体igeelisa检测试剂盒说明书

过敏原特异性抗体IgE ELISA 检测试剂盒说明书【用途】定性和定量检测过敏原特异性人IgE。
过敏反应是一种特殊的病理性免疫反应,是人体对一种或多种原本无害的物质产生不正常的反应。
其主要原因是患者吸入或食入含有过敏性物体刺激机体,触发细胞大量分泌药理活性物质,引起一系列过敏症状,例如过敏性哮喘,过敏性鼻炎,湿疹、发痒、流泪、皮炎以及肠胃道过敏症等。
同时产生相当量的E型免疫球蛋白(Immunoglobulin E 即Ig E),引起人类过敏反应的过敏原种类繁多,如能从中查到引起机体过敏的物质,就能很好地预防和治疗过敏反应。
本检测盒是一种用酶联免疫法(ELISA)快速、精确测定体内引起过敏反应的特异E型免疫球蛋白的体外诊断工具。
它可定性和定量地测定人体抗特种过敏原的E型免疫球蛋白在血清中的水平,从而帮助医生正确地诊断引起病人过敏反应的过敏原。
本过敏原检测盒适合于广泛的过敏原检测,特别适用于少儿患者,同时也非常适用于湿疹以及其他皮肤病患者和对皮试过敏的患者。
【检测原理】本试剂盒采用酶免ELISA法。
当具有过敏抗原固化于表面的载体与病人血清培养在一起后,血清中特异性IgE(一抗)就会特异地结合到抗原上,此特异结合的抗体可被酶联的二抗所识别,加入显色剂后,二抗所联的酶使显色剂呈蓝色,加终止液后呈黄色。
显色的深度与血清中特异性IgE成正比;能定性/半定量地检测血清中特异性IgE的浓度。
【检测盒组成】过敏原包被微孔酶标板(Coated Wells) 96wells HRP酶联二抗12 ml浓缩洗涤液(15X)(Washing Conc.) 40ml×1 TMB单组分显色液12 ml硫酸终止液(Stop Solution) 12ml 样本稀释液(Sample Diluent) 12 ml【检测动态范围】0.35 ~100 IU/ml (0.84ng ~ 240 ng/ml)。
【重现性】CV 10%~15%【重现性】0.30IU/ml (0.72ng/ml)【注意事项】1.严格按照规定的时间和温度进行温育以保证准确结果。
过敏原特异性IgE抗体检测试剂技术审查指导原则

附件2过敏原特异性IgE抗体检测试剂技巧审查指点原则本指点原则旨在指点注册申请人对过敏原特异性IgE抗体(Allergenspecific IgE)检测试剂注册申报材料的预备及撰写,同时也为技巧审评部分审评注册申报材料供给参考.本指点原则是对过敏原特异性IgE抗体(Allergenspecific IgE)检测试剂的一般请求,申请人应根据产品的具体特点肯定个中内容是否实用,若不实用,需具体阐述来由及响应的科学根据,并根据产品的具体特点对注册申报材料的内容进行充实和细化.如申请人以为有须要增长本指点原则不包含的研讨内容,可自行填补.本指点原则是供申请人和审查人员的指点文件,不涉及注册审批等行政事项,亦不作为律例强迫履行,若有可以或许知足律例请求的其他办法,也可以采取,但应供给具体的研讨材料和验证材料.应在遵守相干律例的前提下运用本指点原则.本指点原则是在现行律例.尺度系统及当前认知程度下制订的,跟着律例.尺度的不竭完美和科学技巧的不竭成长,本指点原则相干内容也将合时进行调剂.一.规模I型过敏反响性疾病相当广泛,人群总发病率高达10%~30%,是当宿世界性的重大卫生学问题,被世界卫生组织(WHO)列为二十一世纪重点防治的三大疾病之一.过敏性疾病是患者吸入.食入或者注入含有致敏成分的物资(称为过敏原或变应原,Allergen)后触发机体的B细胞产生特异性免疫球蛋白E(Immunoglobulin E, IgE),IgE以其Fc 段与肥大细胞或嗜碱性粒细胞的概况响应的FcεRI联合,使机体处于对该过敏原的致敏状况.当雷同过敏原再次或多次进入致敏机体时,可与肥大细胞或嗜碱性粒细胞概况的IgE产生特异性联合,当过敏原与致敏细胞概况的两个或两个以上相邻的IgE结应时,产生FcεRI 交联,使肥大细胞和嗜碱性粒细胞活化,导致细胞脱颗粒并释放储消失细胞浆颗粒里的炎性介质——组胺,并经由过程花生四烯酸门路合成新介质——白三烯.免疫反响性前列腺素和IL4.IL5等细胞因子及趋化因子,从而激发过敏反响(或称反常反响,Allergy)的疾病及相干症状,如过敏性哮喘.枯草热.荨麻疹.过敏性鼻炎.湿疹.结膜炎及胃肠道I型过敏性疾病及轻微过敏反响等.上述过敏性疾病的产生,IgE抗体起症结感化.I型过敏反响性疾病的特点是患者体内轮回血液中的过敏原特异性IgE抗体浓度较正常状况下高,且特异性IgE抗体浓度越高,诊断过敏性疾病的概率越高.本指点原则实用于过敏原特异性IgE抗体检测试剂,包含总IgE 和特异性IgE,同时实用于不合的检测办法(道理).本指点原则实用于申请产品注册和相干允许事项变动的产品.二.根本请求(一)综述材料综述材料重要包含产品预期用处.产品描写.有关生物安然性的解释.有关产品重要研讨成果的总结和评价以及同类产品在国表里同意上市的情形介绍等内容,个中同类产品上市情形介绍部分应侧重从重要原材料.检出限.阳性断定值或者参考区间等方面写明拟申报产品与今朝市场上已获同意的同类产品之间的重要差别,同时应对申报的每一个过敏原具体项目进行详尽的阐述,分离阐述每个过敏原的具体特色及相干信息.综述材料的撰写应该相符《体外诊断试剂注册治理办法》(国度食物药品监视治理总局令第5号)(以下简称《办法》)和《关于颁布体外诊断试剂注册申报材料要乞降同意证实文件格局的通知布告》(国度食物药品监视治理总局通知布告第44号)(以下简称44号通知布告)的相干请求.(二)重要原材料的研讨材料若重要原材料为申请人本身临盆,其临盆工艺必须稳固;如重要原材料源于外购,应供给的材料包含:供货方供给的质量尺度.出厂检定陈述以及申请人对到货后重要原材料的质量磨练材料.除上述内容外,建议申请人按照以下请求提交研讨材料:1.企业内部参考品的制备.定值进程.具体阐述参考品中过敏原特异性IgE抗体的剖断办法和浓度确认办法,剖断办法应科学合理并采取国际公认的办法.金尺度办法或临床诊断等办法分解进行确认.浓度确认应采取国度或国际尺度品进行溯源.应分离对每一个过敏原项目进行研讨.2.质控品的制备.定值进程应参照企业内部参考品的制备办法进行.3.过敏原重要原材料的研讨材料.(1)无论是自然提取抗原,照样基因工程重组抗原,均应对原料进行具体剖析研讨,至少包含重要过敏原(致敏)蛋白的特异性.分子量.纯度.致敏蛋白含量.反响性:生物活性,效价(克制实验)等内容.(2)对于以上请求的指标应给出具体的研讨计划.研讨办法.实验进程.实验数据.相干图谱等内容.(3)如为克己抗原,还需供给具体的抗原剖断.提取.制备.临盆等的研讨材料.(4)如为外购原材料,还需供给过敏原等重要原材料的出厂陈述及进货磨练陈述.(5)对于其他重要原材料,如二抗.对象酶.包被板等原材料,应供给重要原材料的选择.制备及质量尺度等内容的具体研讨材料及实验数据.(三)重要临盆工艺及反响系统的研讨材料1.重要临盆工艺介绍,可用流程图方法暗示,并扼要解释重要临盆工艺的肯定根据.2.产品根本反响道理介绍.3.重要临盆工艺进程的研讨材料.每一步临盆工艺的确认材料及实验数据.4.重要反响系统的研讨材料.每一步反响系统的确认材料及实验数据.(四)剖析机能评估材料申请人应提交在产品研制或成品验证阶段对试剂盒所有的剖析机能进行研讨的材料,对于每项剖析机能的研讨都应包含具体研讨目标.实验设计.研讨办法.可接收尺度.实验数据.统计办法等具体材料.有关剖析机能研讨的布景信息也应在注册申报资估中有所表现,包含研讨地点(实验室).实用仪器.试剂规格.批号.临床样原根源等.剖析机能研讨的实验办法,可以参考国内或国际有关体外诊断产品机能评估的指点原则.对于总IgE抗体的检测,不建议进行定性检测,应采取定量及半定量检测,所有剖析机能也应根据定量或半定量检测试剂的请求进行评估.对于过敏原IgE抗体检测试剂,建议侧重对以下剖析机能进行研讨.1.供给参考品(国度参考品.企业参考品)的验证材料.最低检出限的肯定及验证应采取恰当的参考品进行,最低检出限参考品应进行精确的浓度确认.对于定性检测产品,可采取每一浓度样本至少20次的检测情形对最低检出限进行研讨,拔取90%~95%检出率的浓度程度作为最低检出限;对于定量检测产品,可采取每一浓度样本至少10次的检测情形对最低检出限进行研讨,拔取CV值≤20%的浓度程度作为最低检出限.过敏原特异性IgE抗体的检测限建议不高于0.35IU/ml,总IgE抗体的检测限建议不高于3~5 IU/ml,可采取稀释或系列参考品的方法进行研讨,但应包管不合浓度的样本同时包含上述两个浓度及其临近的浓度,明白写明最低检出限临近浓度的检测情形,如过敏原特异性IgE 抗体浓度在0.30IU/ml程度的检测情形.总IgE抗体在阳性断定值临近浓度的检测情形.对于包被过敏原为混杂过敏原(非组合)的产品,应对可检测项目中的每一个过敏原项目进行最低检出限的评价及验证.对于定量或半定量检测的试剂,均应该进行线性规模的研讨.线性规模肯定的研讨应运用高值临床样本(由可溯源至国度参考品/国际参考品的办法定量)进行梯度稀释,稀释液应运用经确以为响应过敏原项目检测成果为阴性的混杂人血清或血浆,建议应包含许多于9个浓度(应包含接近最低检测限的临界值浓度,同时知足国度或国际分级尺度的请求),经由过程评价必定规模内的线性关系及各程度的精确度肯定该产品的线性规模.瞄精确度的评价,可采取与国度/国际参考品的误差.收受接管实验或者办法学比对等办法进行,申请人可根据现实情形选择合理办法进行研讨.具体描写评价办法中样本的制备进程.评价计划.实验进程.实验数据.统计办法.研讨结论等内容.除上述材料之外,对于过敏原特异性IgE抗体检测试剂,建议供给至少50例与临床诊断成果比对的研讨材料,对于极为罕有的过敏原特异性IgE抗体检测项目,可供给至少30例与临床诊断成果比对的研讨材料.周详度的评价办法并没有同一的尺度可依,可根据不合产品特点或申请人的研讨习惯进行,前提是必须包管研讨的科学合理性,具体实验办法可以参考相干的美国临床实验室尺度化协会同意指南(CLSIEP)或国内有关体外诊断产品机能评估的文件进行.申请人应对每项周详度指标的评价尺度做出合理请求,如尺度差或变异系数的规模等.针对本类产品的周详度评价重要包含以下请求:(1)至少应在产品检测阴性.最低检出限浓度.医学决议程度(Cutoff值)浓度进行周详度的评价.①阴性样本(质控品):应尽量采取高值阴性样本(质控品)进行(n≥20),如最低检出限浓度为0.35IU/ml,可选择0.30IU/ml浓度作为评价样本浓度.②最低检出限浓度样本(质控品):待测物浓度应接近产品的最低检出限(n≥20).③医学决议程度(Cutoff值)浓度样本(质控品):根据产品设计的Cutoff值肯定样本(质控品)的浓度(n≥20).(2)合理的周详度评价周期,例如:为期至少20天的持续检测,天天至少由2人完成许多于2次的完全检测,从而对批内/批间.日内/日间以及不合操纵者之间的周详度进行分解评价.若有前提,申请人应选择不合的实验室进行反复实验以对室间周详度进行评价.(1)交叉反响在进行交叉反响的研讨进程中,对于过敏原的选择建议斟酌以下内容:生物学分类的邻近性.基因组或构造的保守性和同源性.过敏原蛋白AA序列以及立体构造的类同性.IgE抗体联合表位在构象/拓扑学的兼容性.①应采取与被检过敏原蛋白在构成或构造上部分雷同或者具有邻近性的过敏原特异性IgE抗体阳性样本进行交叉反响研讨.②建议采取高浓度的过敏原特异性IgE抗体阳性样本进行交叉反响研讨,应明白抗体浓度.③申请人应对进行交叉反响研讨的过敏原特异性IgE抗体阳性样本的确认办法进行具体阐述,并供给具体的确认材料和数据,如:是否经由其他办法检测.经由金尺度的确认或经由临床诊断的确认等.④亦可采取抗原电泳剖析致敏蛋白的办法进行研讨.至少应对公认的可能具有交叉反响的过敏原项目进行验证,建议对于每种过敏原至少拔取2~3个可能产生交叉反响的过敏原进行研讨.(2)干扰物资①对样本中罕有的内源性干扰物资进行研讨,如血红蛋白.甘油三酯或胆固醇.胆红素.类风湿因子(RF).抗核抗体(ANA).抗线粒体抗体(AMA)等,肯定可接收的干扰物资极限浓度.建议采取被测物阴性及最低检出限浓度对每种干扰物资的干扰影响进行评价.②对高浓度的非特异性人IgA.IgG.IgM.IgD抗体阳性样本进行评价,建议采取被测物阴性及最低检出限浓度进行研讨.③对含有高浓度总IgE抗体的特异性IgE抗体阴性或弱阳性样本进行评价.干扰物资研讨的样本可采取临床或模仿添加样本进行验证,样本量选择应表现必定的统计学意义.7.钩状(HOOK)效应须采取高浓渡过敏原特异性IgE抗体阳性血清进行梯度稀释后由低浓度至高浓度开端检测,每个梯度的稀释液反复3~5份,对钩状效应进行合理的验证.应给出不会产生钩状效应的抗体最高浓度,并在产品解释书上明示对钩状效应的研讨成果.应提交具体的溯源性研讨材料,该类产品有国际尺度品,产品检测成果的量值必须溯源至国际尺度品.对于企业内部参考品.尺度品.质控品均应供给具体的溯源材料,包含溯源计划.溯源办法.溯源进程.溯源步调,溯源进程中每一步的不肯定度的盘算等内容.(五)阳性断定值或参考区间肯定材料对于过敏原特异性IgE抗体检测试剂,不合过敏原检测项目标阳性断定值可能不一致,是以应根据不合项目分离给出适于中国人群的阳性断定值,供给具体的研讨材料.如将阳性断定值肯定为0.35IU/ml或者按照国际或国度分级尺度的不合级别对阳性断定值进行设定,则应该解释白定或者设定的具体根据,并供给具体的验证材料.对于总IgE抗体检测试剂,应给出参考区间,应按照不合的年纪段分离进行参考区间的研讨,并供给具体的研讨材料.(六)稳固性研讨材料稳固性研讨材料重要涉及两部分内容,申报试剂的稳固性和实用样本的稳固性研讨.前者重要包含及时稳固性(有用期).运输稳固性.开瓶稳固性等研讨,申请人可根据现实须要选择合理的稳固性研讨计划.稳固性研讨材料应包含研讨办法的肯定根据.具体的实行计划.具体的研讨数据以及结论.对于及时稳固性研讨,应供给至少三批样品在现实储存前提下保管至成品有用期后的研讨材料.应对样本稳固性进行研讨,重要包含室温保管.冷藏和冷冻前提下的有用期验证,可以在合理的温度规模内选择温度点(温度规模),每距离必定的时光段即对储存样本进行全机能的剖析验证,从而确认不合类型样本的效期稳固性.适于冷冻保管的样本还应对冻融次数进行评价.试剂稳固性和样本稳固性两部分内容的研讨成果均应在解释书【储存前提及有用期】和【样本请求】两项中进行具体解释.(七)临床评价材料临床实验总体请求及材料内容应相符《体外诊断试剂临床实验技巧指点原则》.《办法》和44号通知布告的划定,以下仅根据过敏原检测试剂的特色对其临床实验中应重点存眷的内容进行阐述.对于该类试剂已有同类产品上市的,按照律例请求应选择境内已同意上市.临床广泛以为质量较好的同类产品作为比较试剂,采取实验用体外诊断试剂(以下称考察试剂)与之进行比较实验研讨,证实考察试剂与已上市产品等效.如无已上市同类产品的,应根据产品设计的具体用处进行临床实验.分解临床检测成果.病例临床材料.其他检测检讨成果(病史.皮肤实验.激发实验).患者治疗情形等多方面身分进行分解断定以评价产品检测成果是否精确.应充分斟酌地域性差别,因为过敏原检测项目许多,包含各类食物.吸入性.注入性等过敏原,并且过敏症状的产生计在季候性,所以应充分斟酌各类过敏原的地域性差别.发病时光的不合.风行病学的差别选择有代表性的单位进行临床实验,应尽量选择不合省分的临床单位.对于组合过敏原检测项目(套组,非混杂),每一个检测项目应分离进行统计,且应知足至少1000例的请求,对于每一个检测项目病例选择中应包含必定命量的交叉反响样本,以评价产品检测的特异性.对于每一过敏原检测(陈述)项目均应供给大于30~50例检测成果与临床诊断成果比对的临床材料,应随机选择病例,先选择高度疑惑的临床病例,再经由过程样本检测进行比对,比对病例应包管必定的阳性率,并供给具体的病例情形(包含病史.临床诊断办法.各类检测成果等),建议在反常反响科.呼吸科.消化科等临床专业科室进行临床实验.对于实用于对多个样本类型进行检测的产品,如不合样本类型之间具有可比性,应至少完成一个样本类型许多于1000例的临床研讨,同时再进行许多于 200例同一患者不合样本类型之间的比较研讨.如样本类型中包含指尖全血或静脉全血等全血样本,应至少进行300例同一患者全血样本与血清或者血浆样本的比对临床材料.对于定性检测试剂至少应盘算阳性相符率.阴性相符率.总相符率,并以四格表的情势进行列表,并对定性成果进行Kappa磨练以验证检测成果的一致性.对于定量和半定量检测试剂除盘算阳性相符率.阴性相符率.总相符率外,还应进行相干性剖析,给出相干系数,进行回归剖析给出回归方程和实验数据的散点图,并对相干系数和回归方程的斜率进行明显性剖析.对于半定量检测产品还应对检测的分级成果进行统计,明白分级消失差别的样本数目和分级差别情形,同时供给样本检测成果的频率散布图.对于两种试剂的检测成果有不一致(检测成果差别较大)的样本,应采取临床上公认较好的第三种同类试剂进行复核,同时联合患者的临床病情.临床材料对差别原因及可能成果进行剖析.对于半定量检测产品,在检测成果阴阳性剖断一致的情形下,如分级差别等于或大于2个级别,应采取第三种办法进行复核.对于选择的交叉反响样本应单独列出并单独进行统计,并对检测成果进行具体描写,并对可能产生交叉反响的原因进行详尽描写.7.临床实验成果应供给原始临床实验数据.8.对于在同一膜条上同时包含总IgE抗体和特异性IgE抗体检测项目标产品,应分离供给每个检测项目与定量检测试剂检测成果的比对研讨材料,每个项目应包含不合阳性强度的样本.(八)产品风险剖析材料根本请求应相符44号通知布告的请求,同时斟酌到过敏原特异性IgE抗体检测可能消失必定的交叉反响,并且过敏原特异性IgE抗体的浓度与患者的临床症状并没有绝对相干性,是以申请人应根据这些不肯定的身分剖析产品运用可能消失的风险.(九)产品技巧请求产品技巧请求应相符《办法》和44号通知布告的请求.申请人应该在原材料质量和临盆工艺稳固的前提下,根据产品研制.剖析机能评估等成果,根据国度尺度.行业尺度及有关文献,按照《医疗器械产品技巧请求编写指点原则》的有关请求,编写产品技巧请求.假如拟申报产品已有实用的国度/行业尺度宣布,则产品技巧请求的内容应不低于实用尺度.定性产品应进行参考品的检测,定量产品除进行参考品的检测外还应进行线性的评价.每个项目均须进行最低检出限和阳性参考品相符率的检测.机能指标及磨练办法中应明白写明阳性参考品所包含的检测项目.(十)产品注册磨练陈述根据《办法》及44号通知布告的请求,申请注册的第三类产品应在具有响应医疗器械磨练天资的医疗器械磨练机构进行持续3个临盆批次样品的注册磨练.今朝,过敏原IgE抗体检测试剂尚无实用的国度参考品,可采取企业参考品进行注册磨练,但企业参考品的具体信息应明白,如IgE抗体浓度.过敏原检测项目标肯定办法等.若有实用的国度参考品/尺度品宣布,则申请人应采取国度参考品/尺度品进行注册磨练,并在产品技巧请求中写明响应内容.(十一)产品解释书产品解释书承载了产品预期用处.磨练道理.磨练办法.磨练成果的解释以及留意事项等重要信息,是指点实验室工作人员精确操纵.临床大夫针对磨练成果给出合理医学解释的重要根据,是以,产品解释书是体外诊断试剂注册申报最重要的文件之一.产品解释书格局应相符《体外诊断试剂解释书编写指点原则》的请求,境外产品的中文解释书除格局请求外,其内容应尽量保持与原文解释书的一致性,翻译力图精确且相符中文表达习惯.产品解释书的所有内容均应与申请人提交的注册申报资估中的相干研讨成果保持一致,如某些内容引用自参考文献,则应以规范格局对此内容进行标注,并单独列明参考文献的相干信息.联合《体外诊断试剂解释书编写指点原则》的请求,下面临过敏原特异性IgE抗体(Allergenspecific IgE)检测试剂解释书的重点内容进行具体解释,以指点注册申请人更合理地编写产品解释书.1.【产品名称】可以根据拟申报产品的具体特色增长描写性说话,(吸入组1或2).(食物组1或2).(分解组1或2)等,如组合过敏原检测项目定名为“过敏原特异性IgE抗体检测试剂盒(吸入组1/化学发光法)”,以更好的区分不合的产品.2.【预期用处】应至少包含以下几部分内容:(1)试剂盒用于××检测人×××样本中的过敏原特异性IgE 抗体和/或总IgE抗体.个中,××应按照产品类型写明具体为定性.半定量照样定量检测,×××应写明实用的样本类型为血清.血浆照样全血,上述内容均应有响应的剖析机能评估材料和临床实验材料支撑.对于总IgE抗体检测试剂,不建议声称定性检测用处,对于过敏原特异性IgE抗体检测试剂,还应该逐项列明可以或许检测的具体过敏原项目.(2)应该解释该试剂不建议用于健康人群体检,检测成果阳性或者阴性仅代表响应的IgE抗体检测成果阳性或阴性,与患者是否患病的相干性不肯定,不得作为患者病情评价的独一指标,必须联合患者临床表示和其他实验室检测对病情进行分解剖析.(3)待测人群特点介绍:应分不合的年纪段.性别进行简略介绍,并对检测成果及患者临床症状之间的关系进行描写.(4)对过敏反响的机理进行简略的介绍.(5)临床用处:解释与预期用处相干的临床顺应症布景情形,解释相干的临床或实验室诊断办法,应对每个过敏原分离进行编写.3.【储存前提及有用期】解释试剂盒的效期稳固性.开封稳固性.运输稳固性等,应标明具体的储存前提及有用期.4.【阳性断定值或者参考区间】(1)明白产品的溯源情形,无论定量或是定性产品,其检测成果量值均须溯源至国际或国度尺度品,应以IU/ml作为单位或供给与国际单位的换算单位.(2)分离列出总IgE抗体(建议进行定量检测)和每个过敏原特异性IgE抗体的最低检出限(不大于0.35IU/ml)和参考区间,如两者一致可一同列出.(3)对于半定量或定量检测产品,可列消失行的国际或国度的定级尺度与特异性IgE抗体浓度之间的关系.(4)应明白检测旌旗灯号值与特异性IgE抗体浓度之间的关系及尺度曲线的制订办法(如实用).5.【磨练成果的解释】(1)应明白检测成果是否成立的剖断尺度,如阴.阳性对比品的检测请求(如实用).(2)如不合过敏原的检测成果消失差别,应对每一个过敏原特异。
食物特异性抗体IgG检测试剂盒(化学发光免疫分析法)产品技术要求xinhualian
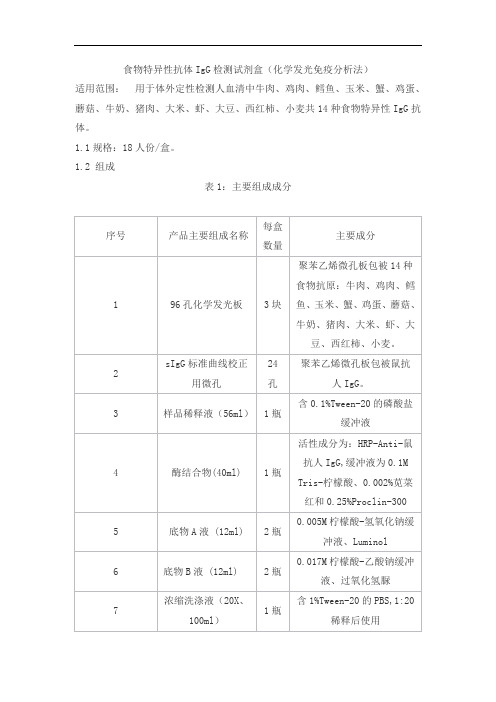
食物特异性抗体IgG检测试剂盒(化学发光免疫分析法)适用范围:用于体外定性检测人血清中牛肉、鸡肉、鳕鱼、玉米、蟹、鸡蛋、蘑菇、牛奶、猪肉、大米、虾、大豆、西红柿、小麦共14种食物特异性IgG抗体。
1.1规格:18人份/盒。
1.2 组成表1:主要组成成分表2:包被微孔布局注:空白对照和阳性对照包被鼠抗人IgG抗体2.1 外观外观应符合如下要求:•试剂盒各组分应齐全、完整,液体无渗漏;•中文包装标签应清晰,无破损。
2.2 溯源性根据GB/T 21415及有关规定提供校准品的来源、赋值过程及测量不确定度等内容,溯源至WHO人血清IgG,IgA, IgM国际标准品(WHO International Standard Immunoglobulins G,A and M,Human serum,100IU/ampoule)。
2.3 准确度2.3.1 相对偏差用WHO人血清IgG,IgA和IgM国际标准品(WHO International Standard Immunoglobulins G,A and M,Human serum.)标定的食物特异性IgG抗体阳性血清作为质控品进行检测,其测量结果的相对偏差应在±25%范围内。
2.3.2符合率a) 阳性符合率每种食物抗原用5份相应食物特异性IgG抗体阳性内部质控品检测,相应检测结果≥50 IU/mL,不得出现阴性。
b) 阴性符合率每种食物抗原用5份相应食物特异性IgG抗体阴性内部质控品检测,相应检测结果<50 IU/mL,不得出现阳性。
2.4最低检测限应不大于5 .0IU/mL。
2.5 线性在5 IU/mL~400 IU/mL线性范围内试剂盒的相关系数r应≥0.95。
2.6 重复性用阴性样本(<50IU/ml)和浓度分别为50 IU/mL±7.5 IU/mL、200IU/mL±30 IU/mL 的样本各重复检测5次,其变异系数(CV)应不大于15%。
吸入性过敏原特异性抗体IgE检测试剂盒

吸入性过敏原特异性抗体IgE检测试剂盒
产品用途:该产品用于定性检测人血清中过敏原特异性IgE水平主要技术参数和要求:
1.检测方法:免疫印迹法,血清检测
2.检测位点:10个位点
3.检测区间:≥0.35IU/ml
4.适用仪器:无需仪器
5.主要性能指标:最低检出量:用最低检出量质控品进行检测,
不高于0.35IU/ml。
阴性质控品符合率:阴性质控品结果判读为阴性结果,阴性质控
品符合率为100%。
阳性质控品符合率:阳性质控品结果判读符合阳性质控品性质,
阳性质控品符合率为100%。
精密度:以某一浓度的人IgE校准品重复测定(n=10),反应结果一致,显色度均一。
交叉反应:与5.0IU/ml人IgA、IgG、IgM无交叉反应;
由于两种或两种以上过敏原蛋白在结构上的相似,使
它们竞争IgE抗体的结合表位,引起交叉反应。
临床灵敏度:>95.0%
临床特异性:>98.0%
6.资质:国家食品药品监督管理局批准的三类体外诊断试剂证书。
吸入性 食物性过敏原特异性IgE抗体检测试剂盒(免疫印迹法)产品技术要求hejiechuangxin

吸入性/食物性过敏原特异性IgE抗体检测试剂盒(免疫印迹法)适用范围:用于定性检测人血清中的柳树/杨树/榆树、普通豚草、艾蒿、屋尘螨/粉尘螨、屋尘、猫毛、狗上皮、蟑螂、点青霉/分枝孢霉/烟曲霉/交链孢霉、葎草、鸡蛋白、牛奶、花生、黄豆、鳕鱼/龙虾/扇贝、虾、蟹过敏原特异性IgE 抗体。
1.1 试剂盒规格20人份/盒(7项、10项、17项)1.2 试剂盒型号吸入性/食物性过敏原特异性IgE抗体检测试剂盒(7项):鸡蛋白、牛奶、花生、黄豆、鳕鱼/龙虾/扇贝、虾、蟹;吸入性/食物性过敏原特异性IgE抗体检测试剂盒(10项):柳树/杨树/榆树、普通豚草、艾蒿、屋尘螨/粉尘螨、屋尘、猫毛、狗上皮、蟑螂、点青霉/分枝孢霉/烟曲霉/交链孢霉、葎草;吸入性/食物性过敏原特异性IgE抗体检测试剂盒(17项):柳树/杨树/榆树、普通豚草、艾蒿、屋尘螨/粉尘螨、屋尘、猫毛、狗上皮、蟑螂、点青霉/分枝孢霉/烟曲霉/交链孢霉、葎草、鸡蛋白、牛奶、花生、黄豆、鳕鱼/龙虾/扇贝、虾、蟹;1.3 试剂盒组成及规格见表1表1 试剂盒的组成及规格2.1 外观2.1.1 产品包装完整、标签清晰。
液体试剂中,样品稀释液、底物液和酶标二抗为淡黄色,其它试剂为无色,均无混浊,无未溶物。
2.1.2 检测膜条干净、无污渍、无破损。
2.2 膜条尺寸宽度: 2±0.5mm2.3 装量及组件数量检查见1.3,其中装量应不少于标示值。
2.4 阴性符合率用N1-N10总计10份阴性参考品进行检测,各项检测指标检测结果均为阴性。
2.5阳性符合率用P26-P45总计20份企业阳性参考品进行检测,各项检测指标检测结果应符合企业阳性参考品结果。
2.6最低检出限应小于或等于0.35IU/mL。
2.7分析特异性用N11-N15总计5份分析特异性企业参考品进行检测,各项检测指标检测结果均为阴性。
其中,N11为花生特异性IgG抗体阳性,N12为黄豆特异性IgG抗体阳性,N13为虾特异性IgG抗体阳性,N14葎草特异性IgG抗体阳性,N15为屋尘螨/粉尘螨特异性IgG抗体阳性。
过敏原特异性IgE抗体检测试剂盒(胶体金免疫层析法)产品技术要求xhl

过敏原特异性IgE抗体检测试剂盒(胶体金免疫层析法)产品技术要求xhl过敏原特异性IgE抗体检测试剂盒(胶体金免疫层析法)适用范围:该产品用于体外定性检测人血清中针对蒿属花粉/豚草花粉、户尘螨/粉尘螨、猫毛皮屑、狗毛皮屑、大豆、鸡蛋、牛奶、杨树/柳树/榆树花粉变应原的特异性IgE抗体。
1.1 包装规格:25人份/盒。
1.2 主要组成成分:2.1 外观检查外观应符合如下要求:2.1.1试剂盒各组分应齐全、完整,密封包装无漏气、破损;2.1.2包装、标签无破损,文字清晰。
2.1.3铝箔袋内检测卡外观平整,物料贴附牢固,内容齐全。
2.2 物理检查试纸条的宽度应不低于4mm;液体移行速度应不低于5mm/min。
2.3 阴性符合率应为(-/-)20/20。
2.4 阳性符合率每个过敏原检测项阳性符合率均应为(+/+)5/5。
2.5 最低检测限每个过敏原检测项对应最低检测限质控品L1和L2的检测结果均应为阳性,L3应为阴性。
2.6 精密度每个过敏原检测项10个测试之间反应结果一致,显色度均一。
2.7 稳定性2.7.1热稳定性试验:试剂盒于37±1℃放置6天,检测2.1~2.6各项,结果应符合2.1~2.6各项目要求。
2.7.2效期稳定性试验:试剂盒在2℃~30℃保存,取到效期后的试剂盒,检测2.1~2.6各项,结果应符合2.1~2.6各项目要求。
2.8 批间差三批每个过敏原检测项各10个精密度质控品测试之间反应结果应一致,显色度均一。
2.9 特异性测10份特异性质控品血清(S1~S10),其结果为阴性。
过敏原特异性IgE抗体检测试剂技术审查指导原则

附件2过敏原特异性IgE抗体检测试剂技术审查指导原则本指导原则旨在指导注册申请人对过敏原特异性IgE抗体(Allergenspecific IgE)检测试剂注册申报资料得准备及撰写,同时也为技术审评部门审评注册申报资料提供参考。
本指导原则就是对过敏原特异性IgE抗体(Allergenspecific IgE)检测试剂得一般要求,申请人应依据产品得具体特性确定其中内容就是否适用,若不适用,需具体阐述理由及相应得科学依据,并依据产品得具体特性对注册申报资料得内容进行充实与细化。
如申请人认为有必要增加本指导原则不包含得研究内容,可自行补充。
本指导原则就是供申请人与审查人员得指导文件,不涉及注册审批等行政事项,亦不作为法规强制执行,如有能够满足法规要求得其她方法,也可以采用,但应提供详细得研究资料与验证资料。
应在遵循相关法规得前提下使用本指导原则。
本指导原则就是在现行法规、标准体系及当前认知水平下制定得,随着法规、标准得不断完善与科学技术得不断发展,本指导原则相关内容也将适时进行调整。
一、范围I型过敏反应性疾病相当普遍,人群总发病率高达10%~30%,就是当前世界性得重大卫生学问题,被世界卫生组织(WHO)列为二十一世纪重点防治得三大疾病之一。
过敏性疾病就是患者吸入、食入或者注入含有致敏成分得物质(称为过敏原或变应原,Allergen)后触发机体得B细胞产生特异性免疫球蛋白E(Immunoglobulin E, IgE),IgE以其Fc 段与肥大细胞或嗜碱性粒细胞得表面相应得FcεRI结合,使机体处于对该过敏原得致敏状态。
当相同过敏原再次或多次进入致敏机体时,可与肥大细胞或嗜碱性粒细胞表面得IgE发生特异性结合,当过敏原与致敏细胞表面得两个或两个以上相邻得IgE结合时,发生Fc εRI 交联,使肥大细胞与嗜碱性粒细胞活化,导致细胞脱颗粒并释放储存在细胞浆颗粒里得炎性介质——组胺,并通过花生四烯酸途径合成新介质——白三烯、免疫反应性前列腺素与IL4、IL5等细胞因子及趋化因子,从而引发过敏反应(或称变态反应,Allergy)得疾病及相关症状,如过敏性哮喘、枯草热、荨麻疹、过敏性鼻炎、湿疹、结膜炎及胃肠道I型过敏性疾病及严重过敏反应等。
食物特异性抗体IgG检测试剂盒(化学发光免疫分析法)产品技术要求新华联
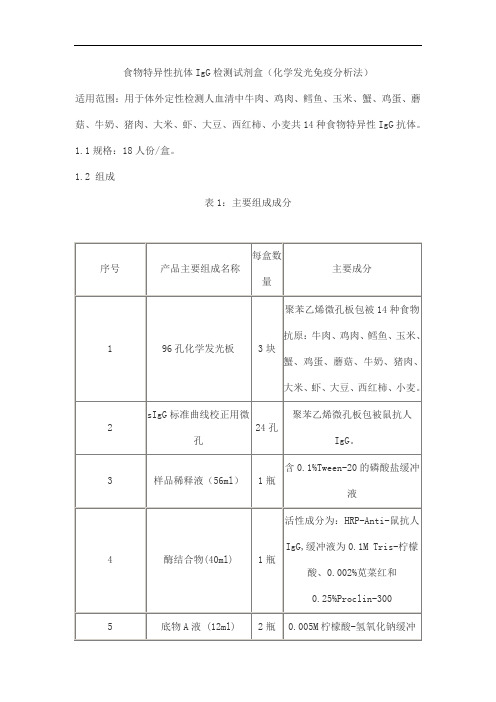
食物特异性抗体IgG检测试剂盒(化学发光免疫分析法)适用范围:用于体外定性检测人血清中牛肉、鸡肉、鳕鱼、玉米、蟹、鸡蛋、蘑菇、牛奶、猪肉、大米、虾、大豆、西红柿、小麦共14种食物特异性IgG抗体。
1.1规格:18人份/盒。
1.2 组成表1:主要组成成分表2:包被微孔布局注:空白对照和阳性对照包被鼠抗人IgG抗体2.1 外观外观应符合如下要求:•试剂盒各组分应齐全、完整,液体无渗漏;•中文包装标签应清晰,无破损。
2.2 溯源性根据GB/T 21415及有关规定提供校准品的来源、赋值过程及测量不确定度等内容,溯源至WHO人血清IgG,IgA, IgM国际标准品(WHO International Standard Immunoglobulins G,A and M,Human serum,100IU/ampoule)。
2.3 准确度2.3.1 相对偏差用WHO人血清IgG,IgA和IgM国际标准品(WHO International Standard Immunoglobulins G,A and M,Human serum.)标定的食物特异性IgG抗体阳性血清作为质控品进行检测,其测量结果的相对偏差应在±25%范围内。
2.3.2符合率a) 阳性符合率每种食物抗原用5份相应食物特异性IgG抗体阳性内部质控品检测,相应检测结果≥50 IU/mL,不得出现阴性。
b) 阴性符合率每种食物抗原用5份相应食物特异性IgG抗体阴性内部质控品检测,相应检测结果<50 IU/mL,不得出现阳性。
2.4最低检测限应不大于5 .0IU/mL。
2.5 线性在5 IU/mL~400 IU/mL线性范围内试剂盒的相关系数r应≥0.95。
2.6 重复性用阴性样本(<50IU/ml)和浓度分别为50 IU/mL±7.5 IU/mL、200IU/mL±30 IU/mL 的样本各重复检测5次,其变异系数(CV)应不大于15%。
一种过敏原特异性IgE抗体免疫分析检测试剂盒及其制备方法[发明专利]
![一种过敏原特异性IgE抗体免疫分析检测试剂盒及其制备方法[发明专利]](https://img.taocdn.com/s3/m/52480f7151e79b8969022623.png)
专利名称:一种过敏原特异性IgE抗体免疫分析检测试剂盒及其制备方法
专利类型:发明专利
发明人:雷均平,黄志坚,邱于斌,何素华,薛晓英,赵振军,和水祥
申请号:CN200910110298.0
申请日:20091030
公开号:CN101696973A
公开日:
20100421
专利内容由知识产权出版社提供
摘要:本发明涉及免疫分析检测试剂盒,提供了一种过敏原特异性IgE抗体免疫分析检测试剂盒及其制备方法。
该检测试剂盒包括:与过敏原蛋白耦联的磁性微珠、与抗人IgE抗体耦联的磁性微珠、人IgE抗体标准品、碱性磷酸酶标记的抗人IgE抗体和碱性磷酸酶化学发光底物AMPPD。
其制备方法包括将过敏原蛋白耦联至磁性微珠上、将抗人IgE抗体耦联至磁性微珠上、制备人IgE抗体标准品、制备碱性磷酸酶标记的抗人IgE抗体、制备碱性磷酸酶化学发光底物AMPPD及组合包装。
本检测试剂盒具有灵敏度高、准确性高且反应快速、使用方便、用量低和成本低的优点,能帮助精确定量测定致敏过敏原,指导临床过敏反应治疗。
申请人:深圳市博卡生物技术有限公司
地址:518000 广东省深圳市宝安区龙华街道油松第十工业区航天科工苑1栋2层南
国籍:CN
代理机构:广州三环专利代理有限公司
更多信息请下载全文后查看。
过敏原特异性抗体IgE免疫印迹法检测试剂盒[实用新型专利]
![过敏原特异性抗体IgE免疫印迹法检测试剂盒[实用新型专利]](https://img.taocdn.com/s3/m/0f6a240986c24028915f804d2b160b4e777f8172.png)
(10)授权公告号 CN 201654038 U (45)授权公告日 2010.11.24C N 201654038 U*CN201654038U*(21)申请号 201020133559.9(22)申请日 2010.03.16G01N 33/53(2006.01)G01N 33/52(2006.01)(73)专利权人湖北楚冠生物药业有限公司地址430070 湖北省武汉市武昌武珞路586号江天大厦18层(72)发明人陈琰 龚镇奎 王帮洲 梅亚红梁智辉 尹玉敏 祝戎飞 陈建军(74)专利代理机构湖北武汉永嘉专利代理有限公司 42102代理人崔友明(54)实用新型名称过敏原特异性抗体IgE 免疫印迹法检测试剂盒(57)摘要本实用新型涉及在一种定性和定量检测人血清或鼻分泌物中过敏原特异性抗体IgE 的免疫印迹检测试剂盒,包括有已包被有吸入性过敏原或食入性过敏原的试纸条、生物素标记的抗人IgE 试剂瓶、亲和素-辣根过氧化物酶试剂瓶和DBA 底物显色液试剂瓶,所述的已包被有吸入性过敏原或食入性过敏原的试纸条包括有试纸条本体和反应槽,试纸条本体位于反应槽的底部。
本实用新型具有如下特点:(1)操作简单、方便;(2)检测成本较低,便于推广和使用。
(51)Int.Cl.(19)中华人民共和国国家知识产权局(12)实用新型专利权利要求书 1 页 说明书 3 页 附图 1 页权 利 要 求 书CN 201654038 U1/1页1.过敏原特异性抗体IgE免疫印迹法检测试剂盒,其特征在于包括有已包被有吸入性过敏原或食入性过敏原的试纸条、生物素标记的抗人IgE试剂瓶(1)、亲和素-辣根过氧化物酶试剂瓶(2)和DBA底物显色液试剂瓶(5),所述的已包被有吸入性过敏原或食入性过敏原的试纸条包括有试纸条本体(4)和反应槽(3),试纸条本体位于反应槽的底部。
过敏原特异性抗体IgE免疫印迹法检测试剂盒技术领域[0001] 本实用新型涉及在一种定性和定量检测人血清或鼻分泌物中过敏原特异性抗体IgE的免疫印迹检测试剂盒。
一种过敏原特异性IgE抗体检测的试剂盒[实用新型专利]
![一种过敏原特异性IgE抗体检测的试剂盒[实用新型专利]](https://img.taocdn.com/s3/m/bea640ba690203d8ce2f0066f5335a8102d26624.png)
(19)中华人民共和国国家知识产权局(12)实用新型专利(10)授权公告号 (45)授权公告日 (21)申请号 201721884731.2(22)申请日 2017.12.28(73)专利权人 深圳市博卡生物技术有限公司地址 518000 广东省深圳市龙华新区龙华街道油松第十工业区航天科工苑1栋2层南端、北端(72)发明人 黄志坚 邓咏海 李昌 钟淑华 曾繁兵 许鑫鑫 雷均平 (74)专利代理机构 广州三环专利商标代理有限公司 44202代理人 郝传鑫 熊永强(51)Int.Cl.G01N 33/68(2006.01)(54)实用新型名称一种过敏原特异性IgE抗体检测的试剂盒(57)摘要本实用新型提供了一种过敏原特异性IgE抗体检测的试剂盒,包括盒体以及盖合所述盒体的盒盖,所述盒体内设有过敏原检测膜条、抗人IgE抗体试剂瓶、链霉亲和素试剂瓶、样本稀释液试剂瓶、显色底物试剂瓶、浓缩洗涤液试剂瓶和反应槽;所述过敏原检测膜条包括混合组过敏原检测膜条、吸入组过敏原检测膜条和食入组过敏原检测膜条中的至少一种。
本实用新型提供的过敏原特异性IgE抗体检测的试剂盒可以根据需要进行选择检测食入类和/或吸入类过敏原,更加方便,具有针对性,检测全面,覆盖范围广。
权利要求书2页 说明书8页 附图1页CN 207611055 U 2018.07.13C N 207611055U1.一种过敏原特异性IgE抗体检测的试剂盒,其特征在于,包括盒体以及盖合所述盒体的盒盖,所述盒体内设有过敏原检测膜条、抗人IgE抗体试剂瓶、链霉亲和素试剂瓶、样本稀释液试剂瓶、显色底物试剂瓶、浓缩洗涤液试剂瓶和反应槽;所述过敏原检测膜条包括混合组过敏原检测膜条、吸入组过敏原检测膜条和食入组过敏原检测膜条中的至少一种。
2.如权利要求1所述的过敏原特异性IgE抗体检测的试剂盒,其特征在于,所述混合组过敏原检测膜条设有第一质控区和第一检测区,所述第一检测区分别设有包被尘螨过敏原的检测线、包被艾蒿过敏原的检测线、包被葎草过敏原的检测线、包被屋尘过敏原的检测线、包被猫毛皮屑过敏原的检测线、包被狗毛皮屑过敏原的检测线、包被矮豚草过敏原的检测线、包被蟑螂过敏原的检测线、包被霉菌过敏原的检测线、包被树木花粉过敏原的检测线、包被贝类过敏原的检测线、包被鸡蛋白过敏原的检测线、包被牛奶过敏原的检测线、包被蟹类过敏原的检测线、包被虾类过敏原的检测线、包被牛肉过敏原的检测线、包被羊肉过敏原的检测线、包被芒果过敏原的检测线、包被花生过敏原的检测线和包被黄豆过敏原的检测线;所述吸入组过敏原检测膜条设有第二质控区和第二检测区,所述第二检测区分别设有包被尘螨过敏原的检测线、包被艾蒿过敏原的检测线、包被葎草过敏原的检测线、包被屋尘过敏原的检测线、包被猫毛皮屑过敏原的检测线、包被狗毛皮屑过敏原的检测线、包被矮豚草过敏原的检测线、包被蟑螂过敏原的检测线、包被霉菌过敏原的检测线和包被树木花粉过敏原的检测线;所述食入组过敏原检测膜条设有第三质控区和第三检测区,所述第三检测区分别设有包被贝类过敏原的检测线、包被鸡蛋白过敏原的检测线、包被牛奶过敏原的检测线、包被蟹类过敏原的检测线、包被虾类过敏原的检测线、包被牛肉过敏原的检测线、包被羊肉过敏原的检测线、包被芒果过敏原的检测线、包被花生过敏原的检测线和包被黄豆过敏原的检测线。
过敏原特异性IgE抗体检测试剂技术审查指导原则

附件2过敏原特异性IgE 抗体检测试剂技术审查指导原则本指导原则旨在指导注册申请人对过敏原特异性IgE 抗体(Allergenspecific IgE) 检测试剂注册申报资料得准备及撰写,同时也为技术审评部门审评注册申报资料提供参考。
本指导原则就是对过敏原特异性IgE 抗体(Allergenspecific IgE) 检测试剂得一般要求,申请人应依据产品得具体特性确定其中内容就是否适用,若不适用,需具体阐述理由及相应得科学依据并依据产品得具体特性对注册申报资料得内容进行充实与细化。
如申请人认为有必要增加本指导原则不包含得研究内容,可自行补充。
本指导原则就是供申请人与审查人员得指导文件,不涉及注册审批等行政事项,亦不作为法规强制执行,如有能够满足法规要求得其她方法,也可以采用,但应提供详细得研究资料与验证资料。
应在遵循相关法规得前提下使用本指导原则。
本指导原则就是在现行法规、标准体系及当前认知水平下制定得,随着法规、标准得不断完善与科学技术得不断发展,本指导原则相关内容也将适时进行调整。
一、范围I型过敏反应性疾病相当普遍,人群总发病率高达10%〜30%, 就是当前世界性得重大卫生学问题,被世界卫生组织(WHO) 列为二十一世纪重点防治得三大疾病之一。
过敏性疾病就是患者吸入、食入或者注入含有致敏成分得物质(称为过敏原或变应原‘Allergen)后触发机体得B细胞产生特异性免疫球蛋白E(Immunoglobulin E, IgE),IgE 以其Fc 段与肥大细胞或嗜碱性粒细胞得表面相应得Fc £ RI结合,使机体处于对该过敏原得致敏状态。
当相同过敏原再次或多次进入致敏机体时,可与肥大细胞或嗜碱性粒细胞表面得IgE 发生特异性结合,当过敏原与致敏细胞表面得两个或两个以上相邻得IgE 结合时,发生Fc £ RI 交联,使肥大细胞与嗜碱性粒细胞活化,导致细胞脱颗粒并释放储存在细胞浆颗粒里得炎性介质——组胺,并通过花生四烯酸途径合成新介质——白三烯、免疫反应性前列腺素与IL4 、IL5等细胞因子及趋化因子,从而引发过敏反应(或称变态反应,Allergy)得疾病及相关症状,如过敏性哮喘、枯草热、荨麻疹、过敏性鼻炎、湿疹、结膜炎及胃肠道I 型过敏性疾病及严重过敏反应等。
抗Jo—1抗体IgG测定试剂盒(化学发光法)产品技术要求参考版

性能指标
2.1外观
试剂盒各组分应齐全、完整,液体无渗漏;
中文包装标签应清晰,无磨损;
磁珠试剂组分为含棕色固体微粒的液体,磁珠无板结,液体无絮状物,无异物;
其他试剂组分应为清澈均匀的液体,无沉淀,无絮状物。
2.2最低检测限
不大于 2.0AU/mL。
2.3准确度
用试剂盒检测浓度为100AU/mL(±20%)的准确度参考品,重复检测3次,其测量结果平均值与标示值的相对偏差应在±10.0%范围内。
2.4重复性
用试剂盒检测浓度分别为10AU/mL(±20%)和100AU/mL(±20%)的重复性参考品,各重复检测10次,其变异系数(CV)应不大于10.0%。
2.5批间差
使用3个批号试剂盒检测浓度为10AU/mL(±20%)和100AU/mL(±20%)的重复性参考品,3个批号试剂之间的批间变异系数(CV)应不大于15.0%。
2.6线性
用线性参考品进行检测,在4AU/mL~190AU/mL范围内,相关系数r≥0.9900。
1。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
过敏原特异性IgE抗体检测试剂盒(化学发光免疫分析法)
适用范围:该产品用于体外半定量检测人血清中蒿属花粉、户尘螨、粉尘螨、猫毛皮屑、狗毛皮屑、蟑螂、豚草花粉、葎草花粉、霉菌混合(点青霉/烟曲霉/交链格孢/枝状枝孢)、树花粉混合(杨树花粉/榆树花粉/柳树花粉)、鸡蛋、牛奶、大豆、花生、海虾、海蟹、海鱼的特异性IgE(specific IgE,简称sIgE)抗体浓度和定量检测人血清中的总IgE(Total IgE,简称TIgE)抗体浓度。
1.1 包装规格
包装规格为36人份/盒
1.2 产品组成
表1. 产品检验项目
表2 产品主要组成表
2.1 外观
外观应符合如下要求:
2.1.1 试剂盒各组分应齐全、完整,液体无渗漏;
2.1.2 中文包装标签应清晰,无破损。
2.2 校准品溯源性
按照GB/T 21415-2008标准,特异性IgE试剂盒校准品溯源到WHO人血清IgE国际标准品(WHO International Standard Immunoglobulin E(IgE),human serum)。
2.3 准确度
2.3.1 特异性IgE
2.3.1.1 偏差
Ⅰ表3中过敏原偏差试验按以下方法操作:
用WHO人血清IgE国际标准品(WHO International Standard Immunoglobulin E(IgE),human serum)标定的过敏原血清作为参考物质进行检测,其测量结果的相对偏差应在±25%范围内;
表3:特异性IgE偏差试验Ⅰ中的过敏原
Ⅱ表4中过敏原偏差试验按以下方法操作:
用Phadia ImmunoCAP试剂标定分级级别的过敏原血清作为参考物质进行检测,其测量结果应该符合对应参考品的分级级别。
表4. 特异性IgE偏差试验Ⅱ中的过敏原
2.3.1.2 符合率
Ⅰ阳性符合率
每种过敏原用5份过敏原阳性内部参考品检测,相应检测结果≥
0.35IU/mL,不得出现阴性。
Ⅱ阴性符合率
每个检测项目用5份相应过敏原阴性内部参考品检测,相应检测结果<0.35IU/mL,不得出现阳性。
2.3.2 总IgE
用WHO人血清IgE国际标准品(WHO International Standard Immunoglobulin E(IgE),human serum)标定的总IgE阳性血清作为血清参考物质进行检测,其测量结果的相对偏差应在±25%范围内;
2.4 最低检测限
2.4.1 特异性IgE
应不大于0.35IU/mL。
2.4.2 总IgE
应不大于5.0IU/mL。
2.5 线性
2.5.1 特异性IgE
在[0.35,100]IU/mL线性范围内试剂盒的相关系数r应≥0.95。
2.5.2 总IgE
在[10,500]IU/mL线性范围内试剂盒的相关系数r应≥0.95。
2.6 重复性
2.6.1 特异性IgE
用阴性样本(<0.35IU/mL)和浓度分别为0.5IU/mL±0.1IU/mL 、
3.5IU/mL±0.5IU/mL和17.5IU/mL±2.5IU/mL 的样本各重复检测5次,其变异系数(CV)应不大于15%。
2.6.2 总IgE
用浓度分别为10IU/mL±1.5IU/mL 、50IU/mL±7.5IU/mL和250IU/mL±35IU/mL 的样本各重复检测5次,其变异系数(CV)应不大于15%。
2.7 批间差
2.7.1 特异性IgE
用3个批号试剂盒检测同一份浓度17.5IU/mL±2.5IU/mL范围内的样本,则3个批号试剂盒之间的批间变异系数(CV)应不大于15.0%。
2.7.2 总IgE
用3个批号试剂盒检测同一份浓度250IU/mL±35IU/mL范围内的样本,则3个批号试剂盒之间的批间变异系数(CV)应不大于15.0%。
2.8 稳定性
2.8.1 特异性IgE
采用以下两种方法进行验证:
2.8.1.1 效期稳定性:2℃~8℃贮存12个月。
取到效期后的样品检测准确度、最低检测限、线性、重复性,应符合2.
3.1~2.6.1的要求;
2.8.1.2 热稳定性试验:取有效期内样品在37℃放置6天。
检测准确度、最低检测限、线性、重复性,应符合2.
3.1~2.6.1的要求。
2.8.2 总IgE
采用以下两种方法进行验证:
2.8.2.1 效期稳定性:2℃~8℃贮存12个月。
取到效期后的样品检测准确度、最低检测限、线性、重复性,应符合2.
3.2~2.6.2的要求;
2.8.2.2 热稳定性试验:取有效期内样品在37℃放置6天。
检测准确度、最低检测限、线性、重复性,应符合2.
3.2~2.6.2的要求。
2.9 分析特异性
2.9.1 特异性IgE
用Phadia 100 鉴定的30份阴性血(所有经Phadia100 鉴定本试剂盒检测项目均为阴性血清样本,其中10份经Phadia100 鉴定除本试剂盒包括的变应原外的其他变应原阳性血清样本进行检测),检测结果应小于0.35IU/mL。
2.9.2 总IgE
用浓度为50IU/mL±7.5IU/mL人 IgG、IgA和IgM 样本进行交叉反应,其检测结果小于5.0IU/mL。
