实验一 绝对乙醇的制备
浙江省富阳中学2024-2025学年高三上学期高考化学模拟试题(含答案)

富阳中学2024-2025学年高三上学期高考化学模拟试题注意事项:1.答题前,考生务必将自己的姓名、班级、学校在答题卡上填写清楚。
2.每小题选出答案后,用2B 铅笔把答题卡上对应的答案标号涂黑,如需改动,用橡皮擦干净后,再选涂其他答案标号。
在试卷上作答无效。
3.考试结束后,请将答题卡、试卷、草稿纸交回。
满分100分,考试用时75分钟。
相对原子质量: H-1 B-11 C-12 N-14 O-16 Mg-24Al-27 S-32 Fe-56 Cu-64 Sn-119 W-184一、单项选择题(共13个小题,每小题3分,共39分,每小题只有一个选项符合题目要求)1.化学与社会、生活密切相关。
对下列现象或事实的描述正确的是A.游泳场馆常用硫酸铜做泳池消毒剂,因为铜盐水解生成的胶状物质可吸附细菌B.在聚氯乙烯高分子链中加入邻苯二甲酸二丁酯是为了起润滑作用,利于高分子链运动C.铜的合金在生活中运用广泛,其中白铜是铜镍合金,黄铜是铜锌合金,紫铜是铜铬合金,青铜是铜锡合金D.“冬日灶中所烧薪柴之灰,令人以灰淋汁,取碱浣衣”中的“薪柴之灰”,与铵态氮肥一同使用效果更佳2.下列说法正确的是A.顺-2-丁烯与反-2-丁烯互为同素异形体B.基态Fe 3+的核外电子有26种不同的运动状态C.O 2、O 3均有非极性共价键D.富勒烯与碳纳米管组成元素相同3.下列化学用语或图示表示正确的是A.氮原子的电子排布图:B.Si O 2的电子式:C.4-甲氧基苯胺:D.中子数为10的氧原子:818O4.下列过程对应的反应方程式正确的是A. 将SnC l 4放入水中:SnC l 4+(x+2)H 2O Sn O 2 · x H 2O ↓+4HClB. 将过量S O 2通入次氯酸钙溶液:Ca 2++SO 2+H 2O +3ClO −CaS O 4↓+Cl −+2HClOC. 乙醚的制备:2C 2H 5OH 140℃(C 2H 5)2O +H 2OD. 制备84消毒液:Cl 2+2NaOH ≜NaCl +NaClO +H 2O5.如右图所示的化合物是制备某些食品添加剂的中间体,其中X 、Y 、Z 、P 、Q 、R 、M 为原子序数依次增大的短周期元素,下列说法正确的是A.简单氢化物的沸点:Z <QB.M 的最高价含氧酸与Y 反应体现氧化性和酸性C.Q的第一电离能是同周期元素中最大的D.P分别与X、Q形成的化合物空间结构一定相同6.处理废弃的锂电池正极材料Li CoO2以回收Li、Co等金属的部分工艺路线如下,已知气体1无毒无害,烧渣中Co仅有一种价态,下列说法错误的是A.500℃焙烧生成的烧渣成分有LiCl、SiO2、CoCl2B.滤饼2转化为Co3O4的反应中氧化剂∶还原剂=1∶6C.若500℃焙烧后直接水浸可能会产生大量烟雾,腐蚀设备D.流程中仅有滤液3和气体1可直接在该工艺路线中再利用7.下列陈述Ⅰ与陈述Ⅱ均正确,且具有因果关系的是选项陈述Ⅰ陈述ⅡA用pH计分别测量等浓度的HCl、HBr、HI溶液,pH值:HCl<HBr<HI非金属性:Cl>Br>IB取F e3O4加稀硫酸至全部溶解,滴加少量KMn O4后紫色褪去F e3O4中含有Fe(Ⅱ)C向熔融氯化钾中加入钠单质,有钾单质蒸汽放出,同时生成氯化钠高温下活泼性Na>KD将打磨后的铝箔直接在酒精灯上加热,铝箔融化滴落熔点:A l2O3<Al8.一种含锡的多元金属硫化物的晶胞结构为四方晶系,已知金属原子均呈四面体配位,晶胞棱边夹角均为90°,其结构可看作是由两个立方体A、B上下堆叠而成。
无水酒精的制备

分子筛吸附具 有低能耗、 易 操作、 易批量 生产等优点,已 经大量应用于 无水酒精的规 模化生产, 其发 展前景主要为 进一步优化工 艺参数和提高 吸附剂性能。
生物质吸附 作为继分子筛吸 附之后的新兴技 术, 尚处于小型 验阶段,因为继承 了分子筛吸附的 优点,并具有绿色 吸附剂的独特优 势, 使其有望成 为分子筛吸附的 保替代工艺。
Thank You!
核心技术就是脱去酒 精与水共沸混合物中 的水含量, 的水含量,使酒精净 含量达到99.5%(质 含量达到 ( 量分数)以上。 量分数)以上。
主要方法
吸水剂脱水法 特殊的精馏方式 膜分离 真空脱水 超临界流体萃取法
吸水剂脱水法
以固体吸水剂(如生石灰、分子筛)或液态吸水剂(如甘油、汽油)脱水。 生物质吸附(如纤维素、玉米粉、 麦秆、 蔗渣、 淀粉、 半纤维素、 木屑、 其他谷物、 农产品残渣等) 现在用的比较多 用离子交换树脂脱水(聚苯乙烯钾型强酸性树脂)
无水酒精的制备方法介绍
无水酒精
酒精学名乙醇,它以玉米、 酒精学名乙醇,它以玉米、小麦、 糖蜜等为原料, 薯类、糖蜜等为原料,经发酵精馏 而制成。 而制成。常压下酒精水溶液质量浓 度为95.57%(质量分数)时, 酒精 度为 (质量分数) 和水形成共沸物。 和水形成共沸物。 无水酒精,又称绝对酒精, 无水酒精,又称绝对酒精,是由 95.57%(质量分数)的酒精经脱水 (质量分数) 精制而成的含水量较少的酒精。 精制而成的含水量较少的酒精。 无水酒精的应用方向主要有两个:一 无水酒精的应用方向主要有两个 一 是研究用纯净的无水酒精,其社会需 是研究用纯净的无水酒精 其社会需 求量少;二是燃料用无水酒精 二是燃料用无水酒精,这方 求量少 二是燃料用无水酒精 这方 面社会需求量巨大,已成为各国能源 面社会需求量巨大 已成为各国能源 的主要补充。 的主要补充。
常用有机溶剂的精制

在有机化学实验中,经常使用各类溶剂作为反应介质或用来分离提纯粗产物。
由于反应的特点和物质的性质不同,对溶剂规格的要求也不相同。
有些反应(如格氏试剂的制备反应)对溶剂的要求较高,即使微量杂质或水分的存在,也会影响实验的正常进行。
这种情况下,就需对溶剂进行纯化处理,以满足实验的正常要求。
这里介绍几种实验室中常用的有机溶剂的纯化方法。
1.无水乙醚市售乙醚中常含有微量水、乙醇和其他杂质,不能满足无水实验的要求。
可用下述方法进行处理,制得无水乙醚。
在250mL干燥的圆底烧瓶中,加入100mL乙醚和几粒沸石,装上回流冷凝管。
将盛有10mL 浓硫酸的滴液漏斗通过带有侧口的橡胶塞安装在冷凝管上端接通冷凝水后,将浓硫酸缓慢滴入乙醚中,由于吸水作用产生热,乙醚会自行沸腾。
当乙醚停止沸腾后,拆除回流冷凝管,补加沸石后,改成蒸馏装置,用干燥的锥形瓶作接收器。
在接液管的支管上安装一支盛有无水氯化钙的干燥管,干燥管的另一端连接橡胶管,将逸出的乙醚蒸气导入水槽中。
用事先准备好的热水浴加热蒸馏,收集34.5℃馏分70~80mL,停止蒸馏。
烧瓶内所剩残液倒入指定的回收瓶中(切不可向残液中加水!)。
向盛有乙醚的锥形瓶中加入1g钠丝,然后用带有氯化钙干燥管的塞子塞上,以防止潮气侵入并可使产生的气体逸出。
放置24h,使乙醚中残存的痕量水和乙醇转化为氢氧化钠和乙醇钠。
如发现金属钠表面已全部发生作用,则需补加少量钠丝,放置至无气泡产生,金属钠表面完好,即可满足使用要求。
2.绝对乙醇市售的无水乙醇一般只能达到99.5%的纯度,而许多反应中需要使用纯度更高的绝对乙醇,可按下法制取。
在250mL干燥的圆底烧瓶中,加入0.6g干燥纯净的镁丝和10mL99.5%的乙醇,安装回流冷凝管,冷凝管上口附加一支无水氯化钙干燥管。
在沸水浴上加热至微沸,移去热源,立刻加入几粒碘(注意此时不要振荡),可见随即在碘粒附近发生反应,若反应较慢,可稍加热,若不见反应发生,可补加几粒碘。
中性乙醇的配制方法

中性乙醇的配制方法中性乙醇是一种常用的溶剂和消毒剂,其配制方法较为简单。
中性乙醇是无色透明液体,具有挥发性和易燃性,因此在配制和使用过程中需要注意安全。
中性乙醇的配制方法一般可以采用乙醇和水的混合物来制备。
以下是中性乙醇的两种常用配制方法:方法一:以无水乙醇为原料1. 准备纯度高的无水乙醇。
在一实验室中,通常使用95%或99%的乙醇作为原料。
确保乙醇的纯度,不含有其他杂质。
2. 在一个干净的容器中取一定量的乙醇。
根据需要制备的中性乙醇的量确定取用的乙醇的量。
一般来说,需要的量越大取用的乙醇的量也就越大。
3. 在乙醇中加入少量的水。
一般情况下,可以按照1:1的比例添加水和乙醇。
慢慢搅拌混合,直至乙醇和水充分混合均匀。
4. 经混合后的液体澄清透明即可。
混合后的液体应该是无色透明的,且没有悬浮物。
配制好的中性乙醇应该能够在常温下稳定存放,且不含有沉淀。
方法二:以绝对乙醇和蒸馏水为原料1. 准备绝对乙醇和蒸馏水。
绝对乙醇的纯度为99.5%以上,蒸馏水应为去离子水或者经过蒸馏的纯净水。
2. 在一个干净的容器中取适量的绝对乙醇,根据需要的中性乙醇的量确定取用的乙醇的量。
3. 在乙醇中加入适量的蒸馏水。
一般情况下,可以按照7:3的比例添加乙醇和蒸馏水。
慢慢搅拌混合,直至乙醇和水充分混合均匀。
4. 经混合后的液体澄清透明即可。
混合后的液体应该是无色透明的,且没有悬浮物。
配制好的中性乙醇应该能够在常温下稳定存放,且不含有沉淀。
无论采用哪种方法配制中性乙醇,都需要严格按照配比比例进行配制。
另外,为了确保配制出的中性乙醇的质量,建议使用灌有刻度的容器或称量器具来准确取用和称量原料。
此外,配制过程中应注意操作人员的安全,避免中性乙醇的挥发和接触皮肤和粘膜。
除此之外,值得一提的是,配制好的中性乙醇应该储存在密封容器中,并放置于阴凉、干燥的地方。
同时,要远离火源和易燃物品。
在使用时,要避免产生火星和高温。
在配制和使用中性乙醇的过程中,要严格遵守相关的安全操作规程和标准。
最新实验-----绝对无水乙醇的制备

实验一、绝对无水乙醇的制备一、实验目的:1 巩固实验室制备绝对无水乙醇的原理2 掌握制备绝对无水乙醇的方法3 熟练掌握蒸馏、回流装置的安装和使用方法二、实验原理:为了制得乙醇含量为99.5%的无水乙醇,实验室中常用最简便的制备方法是生石灰法,即利用生石灰与工业酒精中的水反应生成不挥发、一般加热不分解的熟石灰(Ca(OH)2),以得到无水乙醇。
为了使反应充分进行,除了将反应物混合放置过夜外,还让其加热回流一段时间。
制得的无水乙醇(纯度可达99.5%)用直接蒸馏法收集。
若要制得绝对无水乙醇(纯度>99.95%),则将制得的无水乙醇和金属钠进一步处理,除去残余的微量水分即可。
三、仪器与试剂试剂:95%乙醇生石灰钠邻苯二甲酸二乙脂仪器:回流装置一套四、实验步骤1. 前期准备将100ml 95%乙醇、15g生石灰装入100ml圆底烧瓶,摇匀后用橡皮塞塞紧并放置过夜。
称取12g镁粉,放入稀盐酸中,反应后过滤,放干燥器中干燥。
2. 钠干将过夜处置后的乙醇,加入钠片,继续放置直至没有气泡冒出为止。
3. 回流把处理过的镁粉放入圆底烧瓶中,加入放置过的物料无水乙醇20ml,装上回流装置,加热至微沸,移去热源,加入几粒碘单质引发,引发完毕后,加入沸石、100ml无水乙醇,加热回流2h。
4. 蒸馏回流结束后,待反应体系稍冷,将其改装成蒸馏装置。
用电热套加热蒸馏出绝对无水乙醇。
产品储于带有磨口塞或橡皮塞的容器中。
五、注意事项1. 要过量加入干燥剂,让干燥剂充分吸收多余的水分。
2. 加钠后,不要把瓶塞塞紧,防止产生的氢气压力加大伤到。
3. 加碘单质引发时,要移去热源,防止暴沸;因引发过程中放出大量的热。
4. 蒸馏开始时,应缓慢加热,当温度达到乙醇的沸点时,在收集馏分。
5. 控制好温度,使之不要超过80o C。
6. 所用仪器要干燥或是润洗,防止带入水分。
2013年小车C1考试模拟试题(最新题库)总分100分(90分过关)2013年小车C1考试,考倒一大片。
巴比妥 Barbital 的合成

巴比妥B a r b i t a l的合成Standardization of sany group #QS8QHH-HHGX8Q8-GNHHJ8-HHMHGN#综合化学实验报告院系化学化工学院班级应用化学101班学号姓名董煌杰实验名称巴比妥(Barbital)的合成一、实验目的1.通过巴比妥的合成了解药物合成的基本过程。
2.掌握无水操作技术。
3.复习有机化学的基本操作,回流,蒸馏,减压蒸馏,重结晶。
二、实验原理巴比妥为长时间作用的催眠药。
主要用于神经过度兴奋、狂躁或忧郁引起的失眠。
巴比妥化学名为5,5-二乙基巴比妥酸。
巴比妥为白色结晶或结晶性粉末,无臭,味微苦。
Mp189—192℃。
难溶于水,易溶于沸水及乙醇,溶于乙醚,氯仿及丙酮。
合成路线:三、仪器与试剂仪器:回流装置,蒸馏装置,磁力加热搅拌器,分液漏斗,恒压滴液漏斗,真空泵,抽滤瓶,克式蒸馏头。
试剂:无水乙醇(.),金属钠,邻苯二甲酸二乙酯(.),无水硫酸铜(.),丙二酸二乙酯(.),溴乙烷(.),乙醚(.),无水硫酸钠(.),尿素(.),浓盐酸(.)。
四、主要物料物理常数五、实验步骤(1)绝对乙醇的制备在装有球形冷凝器(顶端附有CaCl2干燥管)的250mL圆底烧瓶中加入无水乙醇180mL,金属钠2g,几粒沸石,加热回流30min,加入邻苯二甲酸二乙酯6mL,再回流10min。
将回流装置改为蒸馏装置,蒸去前馏份。
先接收少量用无水硫酸铜检验是否含水,如不变色,用干燥的圆底烧瓶做接收器,蒸馏至几乎无液滴留出为止,醇密封贮存。
(2)二乙基丙二酸二乙酯的制备在装有搅拌器、滴液漏斗及球形冷凝器(顶端附有CaCl2干燥管)的250mL三颈瓶中,加入制备的绝对乙醇75mL,分次加入剪细的钠丝6g,此处不应过慢,免的纳被氧化二影响下一步的操作。
在应缓慢时,开始搅拌,用油浴加热(油温不超过90℃),金属钠消失后,由滴液漏斗加入丙二酸二乙酯18mL,在10-15min内加完,回流15min,冷却至50℃以下后慢慢滴加溴乙烷20mL,约15min加完,持续回流。
绝对乙醇的制备实验报告

竭诚为您提供优质文档/双击可除绝对乙醇的制备实验报告篇一:无水乙醇的制备实验报告化学工程学院实验专班姓日指导机化学实验报告名称:无水乙醇的制备业:化学工程与工艺级:化工13-6班名:白慧超学号134020XX636期:20XX年10月31日教师:有一、实验目的1.了解氧化钙法制备无水乙醇的原理和方法。
2.熟练掌握回流装置的安装和使用方法。
二、实验原理为了制得乙醇含量为99.5%的无水乙醇,实验室中常用最简便的制备方法是生石灰法,即利用生石灰与工业酒精中的水反应生成不挥发、一般加热不分解的熟石灰(氢氧化钙)cao它在常温、常压下是一种易燃、易挥发的无色透明液体,它的水溶液具有特殊的、令人愉快的香味,并略带刺激性。
四、五、仪器装置(二)实验装置图七、八、实验讨论1.数据分析a无水乙醇产率较高,说明蒸馏过程进行的比较充分bcuso4检验后没有变蓝,说明实验仪器干燥较彻底,实验过程操作较规范2.结果讨论a回流一定要从第一滴液体滴下开始计时,否则时间不够,cao与95%乙醇反应不完全,导致产率偏低b蒸馏开始时,应缓慢加热,使烧瓶内的物料缓慢升温。
当温度计的温度达到乙醇的沸点时(78℃),再收集馏分;控制好温度,使之不超过80℃,否则会使产率偏高c蒸馏过程一定要充分,否则产率会明显偏低d量无水乙醇的量筒要经过润洗,否则会引入水,导致结果有误3.实际操作对实验结果的影响a仪器应事先干燥,否则将带进水,影响实验结果b使用颗粒状的氧化钙,用粉末状的氧化钙将严重暴沸c安装温度计时,使红色水银球紧贴支管口下侧,确保蒸馏时水银球能完全被蒸汽包围,从而获得准确的读书d安装冷凝管时,要使冷凝水从下口进,上口流出,保证“逆流冷却”e必须在烧瓶中加入沸石,以防在回流和蒸馏过程中发生暴沸f蒸馏装置的安装顺序一般由左至右,由下至上,首先从左下侧的热源开始安装g当烧瓶中的物料变成糊状物时,表示蒸馏已接近尾声。
此时,应立即停止加热,利用电炉的余温将剩余的液体蒸出,以避免烧瓶过热破裂4.实验注意事项a仪器应事先干燥。
乙醇的制备pdf
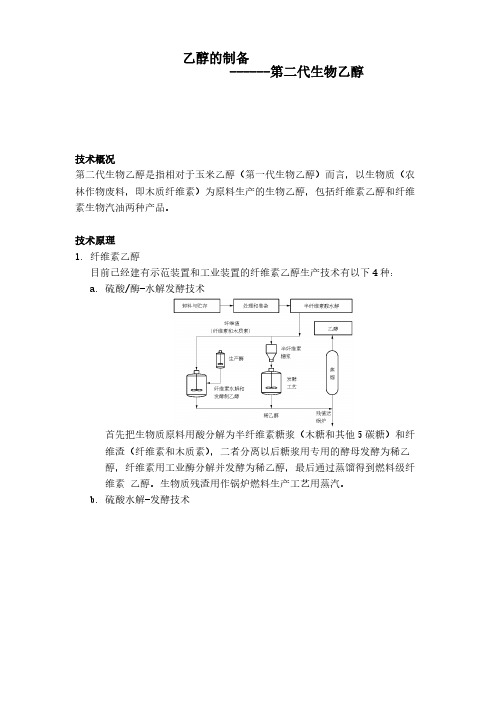
技术概况第二代生物乙醇是指相对于玉米乙醇(第一代生物乙醇)而言,以生物质(农林作物废料,即木质纤维素)为原料生产的生物乙醇,包括纤维素乙醇和纤维乙醇的制备 ------第二代生物乙醇素生物汽油两种产品。
技术原理1. 纤维素乙醇目前已经建有示范装置和工业装置的纤维素乙醇生产技术有以下4种: a. 硫酸/酶-水解发酵技术首先把生物质原料用酸分解为半纤维素糖浆(木糖和其他5碳糖)和纤维渣(纤维素和木质素),二者分离以后糖浆用专用的酵母发酵为稀乙醇,纤维素用工业酶分解并发酵为稀乙醇,最后通过蒸馏得到燃料级纤维素 乙醇。
生物质残渣用作锅炉燃料生产工艺用蒸汽。
b. 硫酸水解-发酵技术用浓硫酸作催化剂,把纤维素和半纤维素原料转化为葡萄糖和木糖,收率是用稀硫酸和酶水解的1.5-3.0倍。
首先把原料干燥到水分少于10%,然后与75%的浓硫酸接触,在85℃左右和常压下蒸煮30min,再把水解得到的6碳糖、5碳糖与酸和木质素及其他固体物分离。
木质素和其他固体物用作锅炉燃料生产工艺用蒸汽和工厂用电。
约98%的酸和100%的糖在模拟移动床色谱分离器中回收。
酸循环使用,糖通过酵母连续发酵转化为乙醇(6碳糖100%转化,5碳糖20%转化)。
该工艺的关键技术一是用浓硫酸进行水解,二是用色谱分离回收酸,而不是中和并处理废料。
c.酸水解-发酵-酯化-加氢技术1—生物质:硬木、软木、柳枝草、玉米秸秆;2—化学分级分离;3—糖液;4—发酵;5—乙酸;6—生产酯;7—乙酸乙酯;8—乙酸乙酯外销;9—加氢;10—乙醇外销;11—氢气;12—气化;13—残渣去气化以废木材等为原料,通过酸水解得到葡萄糖和木糖溶液,然后用乙酸菌发酵把糖转化为乙酸,接着再酯化得到乙酸乙酯,乙酸乙酯(全部或部分)加氢得到乙醇。
氢气由酸水解得到的木质素气化生产。
由于用乙酸菌发酵把所有糖都转化为乙酸,不产生CO和其他副产物,因此碳没有2损失。
常规工艺是通过酵母发酵生产乙醇,每生产1个分子乙醇放出1个分子CO。
2-庚酮的制备

2-庚酮的制备摘要:本实验以正丁基乙酰乙酸乙酯为原料,在弱碱性条件搅拌半小时,温度控制在80℃左右,在搅拌下慢慢加入稀硫酸溶液其间进行多次蒸馏和萃取,最后得出产物为无色液体,称重得1.8克,计算产率为72%关键词:2-庚酮;蒸馏;萃取;回流;绝对乙醇一.前言2-庚酮是一种存在于成年工蜂和小黄蚁体内的昆虫警戒信息素,微量存在丁香油、肉桂油和椰子油中,具有强烈的水果香味,可用作香精的添加剂2-庚酮的制备,合成方法归纳起来主要有天然原料提取法、格氏试剂法、生物发酵法、乙酰乙酸乙酯法、丙二酸二乙酯法、羟醛缩合法、催化加氢法和气相法等,本实验用乙酰乙酸乙酯法,先用乙酰乙酸乙酯和正丁基溴缩合,然后再稀碱中水解,再在稀酸中脱羧生成2-庚酮。
二、实验部分1、实验仪器及药品仪器:回流冷凝管100mL圆底烧瓶、氯化钙干燥管、分液漏斗、锥形瓶、蒸馏头、温度计(200℃)、冷凝管、接收弯头、三口瓶(100mmL 250mL)、滴液漏斗、玻璃棒、试剂:金属钠、99%乙醇、邻苯二甲酸二乙酯、绝对乙醇、碘化钾、乙酰乙酸乙酯、正溴丁烷、盐酸、二氯甲烷、无水硫酸镁、氢氧化钠、正丁基乙酰乙酸乙酯、硫酸、氯化钙溶液可能副反应:4、实验步骤及现象三、实验结果产物为2-庚酮,无色液体,称量后得1.8g,理论产值为2.5g,因此计算产率为1.8g/2.5g*100%=72%。
四、实验结果分析及讨论得出的产品质量为1.8g,产率为72%,与理论产值相差不大,导致产率低的原因有:1、所制备的原料不纯2、仪器不干净,密封不严实3、蒸馏与回流中温度控制的不是很好4、萃取和过滤时有损耗5、转移试剂时也有损耗做实验时应该谨慎小心,称取或量取时要准确,在制备无水乙醇时要特别注意,所用仪器要干燥,之后的馏分收集要用磨口的锥形瓶,防止产品挥发。
参考文献[①]作者:王清廉、李瀛、高坤等;2009年;出版物:《有机化学实验<第三板>》;出版社:高等教育出版社;页码:451、296-297。
实验室合成丙戊酸钠条件的探索

c o , o cH
e CH5 { 2 00
2 乙醇钠 制备
+C 5 a 2, 0 HN …
—— {O — CO Na — l
+C 4。 2O HH 5 ‘
选最 佳 配 比条 件 。实 验 表 明 ,( 1 二丙 基丙 二 酸二 乙 3 . 酯 ) n 氢氧化 钠 ) :( 的最 佳 配 比为 5 1 :。通 过选 择 不 同配 比溶 液 , 每种 配 比下 进行 三 次重现性 试验 , 以每 种 配 比下 酸产 量 的平 均 值为 指标 , 进行 比较 , 结果 表 明 : m( 以 氢氧 化 钠 )V( ) V( 5 乙醇 ): : : : 水 : 9% 3 3 l 0为最佳 , 酸产率 最高 。 4 2 二丙基 丙 二酸 的制 备 .
I l
o
‘
l7 j {c
t7 t C3
Na : Ol tl t { j
\
C3 /
H t / \∞ H }2mn l , j 7 0 s
件渊 : … ∞一 》M t
1 绝对乙醇的制备 在装有 回流冷凝管、 滴液漏斗、 氯化钙干燥管、
收稿 日期 :02—0 — 9 21 1 0
作者 简介 : 曲迪 (9 O ) 山东淄博人 , 19 一 , 本科 , 究方向 : 研 药物合成。
第 3期
曲
迪: 实验室合成丙戊酸钠条件的探索
・3 1・
温 度计 的 50 L四颈 瓶 中 , 加 人 1m 0m 先 0 L普 通无 水 乙醇 , 减重法 称取 40 用 .g金属钠 , 去表 面 的煤 油 , 擦 去 除氧 化层 , 小 刀 切 成 碎 块 , 速 投 入 到 反 应 瓶 用 迅 中 , 后 由滴液 漏斗慢 慢滴 加 普通 无水 乙醇 20 L, 然 9m
无水乙醇理化性质

名称中文名称:无水乙醇中文别名:无水酒精,绝对酒精英文别名:DehydratedAlcohol,Ethanoldenatured,Ethanol,Spiritofwine,Alcoholanhydrous,Ethylalcohol,Grainalcohol,Anhydrousalcohol,Dehydratedalcohol,Ethylhydrate化学式结构简式:C2H5OH分子式:C2H6O相对分子质量46.07性状无色澄清液体。
有愉快的气味和灼烧味。
易流动。
极易从空气中吸收水分,能与水和氯仿、乙醚等多种有机溶剂混溶。
能与水形成共沸混合物(含水4.43%),共沸点78.15℃。
相对密度(d204)0.789。
熔点-114.1℃。
沸点78.5℃。
折光率(n20D)1.361。
闪点(闭杯)13℃。
易燃。
蒸气与空气能形成爆炸性混合物,爆炸极限3.5%~18.0%(体积)储存密封阴凉干燥保存。
用途溶剂。
分析镍、钾、镁及脂肪的酸价。
萃取剂。
脱水剂。
清洗剂。
安全措施贮于低温通风处,远离火种、热源。
与酸类、胺类分储。
误食,饮温水,催吐。
灭火:抗溶性泡沫、二氧化碳、干粉、砂土。
灭火方法燃烧性:易燃闪点(℃):12爆炸下限(%):3.3爆炸上限(%):19.0引燃温度(℃):363最大爆炸压力(MPa):0.735灭火剂:抗溶性泡沫、干粉、二氧化碳、砂土。
灭火注意事项:尽可能将容器从火场移至空旷处。
喷水保持容器冷却,至灭火结束。
紧急处理吸入:迅速脱离现场至新鲜空气处。
就医。
误食:饮足量温水,催吐,就医。
皮肤接触:脱去被污染衣着,用流动清水冲洗。
眼睛接触:提起眼睑,用流动清水或生理盐水冲洗。
就医。
编辑本段理化常数英文名:absolute alcohol;anhydrous ethanolCAS:64-17-5分子式:C2H6O结构简式:CH3CH2OH或C2H5OH官能团:—OH(羟基)主要成分:纯品外观与性能:无色液体,有醇香制取:实验室制备无水酒精时,在95.57%酒精中加入生石灰(CaO)加热回流,使酒精中的水跟氧化钙反应,生成不挥发的氢氧化钙来除去水分,然后再蒸馏,这样可得99.5%的无水酒精。
实验室制取无水乙醇的原理

实验室制取无水乙醇的原理
制取无水乙醇的原理及实验室操作步骤可以概括为:
一、无水乙醇的理论依据
无水乙醇指绝对乙醇,即纯Ethyl alcohol(C2H5OH),不含任何水分。
为无色透明液体,可与水以任意比例混溶。
无水乙醇主要利用分子间的氢键相互作用,可吸收溶解空气中的水分,是强吸湿性物质。
将普通的乙醇脱水,可以得到无水乙醇。
二、无水乙醇的制取方法
1. 物理吸附法:用分子筛、硅胶等物理吸附水分的方法。
操作简单,但筛子易吸湿,效果不稳定。
2. 化学反应法:利用无水氧化钙、氧化铝、硫酸镁等吸湿剂与乙醇反应生成无水产物的方法。
效果好但复杂。
3. 活塞压式水分测定仪法:利用仪器测定乙醇含水量,加入吸湿剂使含水量降到0,效率高。
4. 重馏分离法:利用蒸馏原理馏取不同沸点成分的简易有效方法。
三、实验室制取无水乙醇的操作步骤
1. 配制装置:三颈烧瓶加热电源,连塑料软管至Graham冷凝器,收集瓶接凝液端。
2. 材料配比:95% 乙醇1000毫升,无水硫酸钠粉末20克,搅拌溶解。
3. 装入三颈烧瓶,加热迅速沸腾,收集最初50毫升热馏分防吸湿。
4. 继续收集约60C时馏出的乙醇,用氧化钙槽除去痕量水分。
5. 收集约78C沸点馏出液,即为无水乙醇成分。
6. 留取少量产品,用活塞压式水分仪测试确定含0%水分。
7. 将无水乙醇置于干燥瓶中,密封保存,贴无水标识。
以上是制取无水乙醇的基本方法和步骤。
有些步骤需在通风橱操作,注意防火及避免吸入蒸气。
掌握技巧后可顺利制得纯度高的无水乙醇。
乙醇和水的分离实验报告

蒸馏乙醇溶液可获得95%的酒精,这时是恒沸液,可以加入氧化钙充分混合后蒸馏,可以获得99%的乙醇。
要想获得绝对乙醇,再加镁粉精制。
将你的酒精和水的混合液放入一个容器,比如一个小盆中,然后将盆子放入冰箱的冷冻室,经过12小时以后将盆子拿出来,将盆子内结冰的冰块取出剩余没有结冰的液体就是酒精,因为酒精的冰点是-114度而水是0度,所以原理就是使混合液体降至0度水的冰点以下导致水结冰而酒精还是液态的,从而分离! 这个方法比使用蒸馏的技术较简单轻松的多也不用那么多繁琐的设备!如果要纯度较高的酒精需要反复几次!1蒸馏(包括精馏)、2过滤(用只能透过水而不能透过酒精的膜)、3如果酒精浓度已经较高含水较少而且要求浓度接近100%,可以加入生石灰(或者类似物)充分搅拌,放置一定时间后蒸出。
乙醇比水易气化,乙醇沸点低,水的沸点相对较高。
乙醇的蒸发点比较低,可以用蒸发的方法,让混合液体自然蒸发,用冷却的金属板在杯子上对乙醇蒸汽再次冷却即可。
根据沸点不同用蒸馏的方法进行分离(1)从实验表格的最后一列可以看出,水和酒精刚开始没有凝固,而当体积比达到一定值时,混合液可以凝固,但是并没有将水和酒精分离开,所以用张小同学的方案不能将水和酒精从混合液中分开。
(2)通常情况下水的凝固如果酒精水溶液的浓度小于95%,则酒精水溶液蒸馏的最终产物是水和95%的酒精溶液,因为酒精和水可形成恒沸混合物(恒沸混合物不能利用二者的沸点不同而蒸馏分离),酒精和水的恒沸混合物是浓度95%酒精溶液。
如果要制取无水酒精,需要在95%的酒精中再加入干燥剂(如无水氯化钙),脱水后可制得99%以上的无水酒精。
(1)先加入略过量的碱(如碳酸钠或氢氧化钠),充分反应后蒸馏出乙醇。
再在剩余液体中加硫酸,现蒸馏出乙酸。
(2)将混合液加入饱和碳酸钠溶液中,充分振荡后分液上层是乙酸乙酯,下层液体蒸馏分离乙醇。
乙醇提取工艺和方法

一、生物发酵法酿造酒精1。
1生物发酵法的地位由于化学合成法酒精有含有较多杂质等缺陷,其应用受到限制,因此我国酒精生产以发酵法为主,尤其是随着石油储量的锐减,发酵法酒精工业将日趋重要。
我国酒精年产量为300万吨,仅次于巴西、美国,列为世界第3位.其中发酵法酒精占绝对优势,80%左右的酒精用淀粉质原料生产、约有10%的酒精用废糖蜜生产、以亚硫酸盐纸浆废液等纤维原料生产的酒精约占2%左右,合成酒精占酒精总产量的3.5%左右。
1.2生产原料淀粉质原料是生产酒精的主要原料。
用于发酵法生产酒精的原料主要有:薯类(甘薯、马铃薯、木薯、山药等);粮谷类(高粱、玉米、大米、谷子、大麦、小麦、燕麦、黍等);糖质原料(甘蔗、甜菜、糖蜜等);野生植物(橡子仁,土茯苓、蕨根、石蒜等);农产品加工副产品(米糠饼、麸皮、高粱糠、淀粉渣等);纤维质原料(秸秆、甘蔗渣等);亚硫酸造纸废液等。
我国大多数工厂是采用红薯和玉米为原料生产酒精。
玉米化学成分:红薯化学成分:1。
3辅助物料辅助物料包括:酵母培养和糖化剂制备所需营养盐,调PH所用酸类、洗涤剂、消毒剂、脱水剂等。
酒母,就是将酵母菌扩大培养,获得足够数量酵母菌的酵母培养液,以供酒精发酵之用。
酒精生产用水,按水的用处不同,大体分为以下三种:(1)酿造用水:或称工艺用水,凡制曲时拌料,微生物培养,制曲原料的浸泡、糊化、稀释、设备及工具的清洗等因其与原料、半成品、成品的直接接触,故统称为工艺用水。
通常要求具有弱酸性,PH为4.0-5。
0。
(2)冷却用水:蒸煮醪和糖化醪的冷却,发酵温度的控制,需大量的冷却用水。
因其不与物料直接接触,故只需温度较低;硬度适中。
为节约用水,冷却水应尽可能予以回收利用.(3)锅炉用水:通常要求无固型悬浮物,总硬度和碱度应尽可能低,PH在25°时高于7,含油量及溶解物等越少越好。
1。
4淀粉性质1。
4。
1淀粉颗粒的形状淀粉颗粒呈白色,不溶于冷水和有机溶剂,颗粒内部呈复杂的结晶组织。
质量分数10%无水乙醇

质量分数10%无水乙醇全文共四篇示例,供读者参考第一篇示例:无水乙醇,即绝对乙醇,是一种无水溶剂,分子式为C2H5OH。
质量分数10%无水乙醇指的是在水溶液中,无水乙醇占总质量的百分比为10%。
这种溶液常用于实验室和工业生产中,具有一定的特性和用途。
质量分数10%无水乙醇在实验室中有广泛的应用。
实验室中常常需要使用无水乙醇作为溶剂,用于溶解各种物质。
10%无水乙醇的浓度适中,既能满足溶解物质的需要,又能避免过高浓度对实验结果的影响。
在生物化学实验中,常常需要用10%无水乙醇来固定细胞膜,进行细胞膜蛋白的研究。
在有机化学实验中,10%无水乙醇可用于萃取、结晶和溶解实验物质。
质量分数10%无水乙醇在工业生产中也有一定的用途。
工业生产中常常需要使用溶剂进行反应或分离过程,无水乙醇是一种常用的有机溶剂。
10%无水乙醇的浓度适中,不仅能满足工业生产中的需求,同时也有较低的成本。
某些制药厂家在生产药品时,需要用到10%无水乙醇作为溶剂,用于溶解药物原料或进行结晶纯化。
质量分数10%无水乙醇在化妆品行业也有一定的应用。
无水乙醇具有良好的溶解性和杀菌性,常常被用于化妆品的生产中。
10%无水乙醇同时具有适中的浓度,可以在化妆品中起到保湿、抗菌和稳定化妆品配方的作用。
某些护肤品中添加了10%无水乙醇,可以有效促进皮肤吸收养分、消除皮肤表面细菌,并且具有一定的保湿效果。
质量分数10%无水乙醇在实验室、工业生产和化妆品行业中都有着重要的用途。
它不仅具有良好的溶解性和稳定性,同时还具有一定的抗菌性和分离效果。
人们可以根据需要选用适合的无水乙醇浓度,并在具体的应用领域中发挥其优势,为实验研究和生产制造提供便利。
【文章字数已达要求,可根据需要继续补充】。
第二篇示例:无水乙醇,即无水乙醇,是一种非常常见的有机溶剂,化学式为C2H5OH。
由于它在工业生产与实验室中的广泛应用,因此其质量分数也是非常重要的。
在本文中,我们将重点聚焦于质量分数为10%的无水乙醇,探讨其特性、用途以及注意事项。
常用溶剂的物理性质和纯化

常用溶剂的物理性质和纯化化学合成实验经常会用到溶剂,溶剂不仅作为反应介质,产物的纯化和后处理例如重结晶、萃取、层析等操作也经常用到溶剂。
由于溶剂的用量总是比较大,即使溶剂中微量杂质也会对反应和产物的纯化带来一定的影响。
一些有机反应(如Grignard反应等)对溶剂的要求更高,微量的水和醇都会使反应难以发生。
因此,溶剂在使用前应检验其纯度,需要时将其纯化。
下面介绍常用有机溶剂的物理性质和一般纯化方法。
1.石油醚石油醚为轻质石油产品,是低分子量的烃类(主要是戊烷和己烷)的混合物。
其沸程为30~1500C,收集的温度区间一般为300C,有30~600C、60~900C、90~1200C等沸程规格的石油醚。
石油醚中含有少量不饱和烃,沸点和烷烃相近,用蒸馏法无法分离,必要时可用浓硫酸和高锰酸钾把它除去。
通常将石油醚用其体积十分之一的浓硫酸洗涤两三次,再用10%的硫酸加入高锰酸钾配成的饱和溶液洗涤,直至水层中的紫色不再消失为止,然后再用水洗,经无水氯化钙干燥后蒸馏。
如要绝对干燥的石油醚则再用金属钠进一步干燥(见“无水乙醚”)。
2.苯bp80.10C,mp5.50C,d4200.87865,n D201.5011普通的苯含有少量的水(200C时,苯能溶解0.06%的水),苯和水形成的共沸混合物在69.250C沸腾,含有91.17%的苯。
由煤焦油加工得到的苯还含有少量的噻吩(沸点840C)。
欲除去水和噻吩,可用等体积的15%硫酸洗涤,直至酸层为无色或浅黄色,或检查无噻吩为止(取5滴苯,加入5滴浓硫酸及1~2滴1%α,β-吲哚醌-浓硫酸溶液,振荡,如酸层呈墨绿色或兰色,表示有噻吩存在)。
苯层再依次用水、10%Na2CO3水溶液、水洗涤,无水氯化钙干燥过夜后,蒸馏。
若要高度干燥可加入金属钠进一步除水。
3.甲苯bp110.60C,d4200.8669,n D201.4961甲苯与水形成共沸混合物,在84.10C沸腾,含81.4%的甲苯。
药物化学 实验教学大纲.
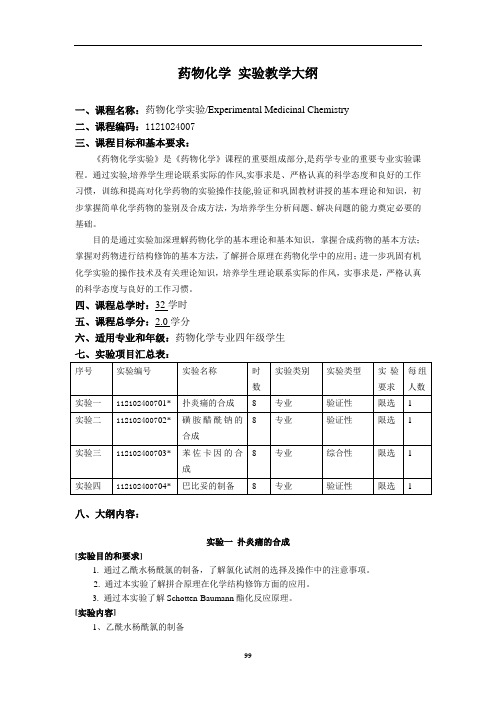
药物化学实验教学大纲一、课程名称:药物化学实验/Experimental Medicinal Chemistry二、课程编码:1121024007三、课程目标和基本要求:《药物化学实验》是《药物化学》课程的重要组成部分,是药学专业的重要专业实验课程。
通过实验,培养学生理论联系实际的作风,实事求是、严格认真的科学态度和良好的工作习惯,训练和提高对化学药物的实验操作技能,验证和巩固教材讲授的基本理论和知识,初步掌握简单化学药物的鉴别及合成方法,为培养学生分析问题、解决问题的能力奠定必要的基础。
目的是通过实验加深理解药物化学的基本理论和基本知识,掌握合成药物的基本方法;掌握对药物进行结构修饰的基本方法,了解拼合原理在药物化学中的应用;进一步巩固有机化学实验的操作技术及有关理论知识,培养学生理论联系实际的作风,实事求是,严格认真的科学态度与良好的工作习惯。
四、课程总学时:32学时五、课程总学分:2.0学分六、适用专业和年级:药物化学专业四年级学生七、实验项目汇总表:八、大纲内容:实验一扑炎痛的合成[实验目的和要求]1. 通过乙酰水杨酰氯的制备,了解氯化试剂的选择及操作中的注意事项。
2. 通过本实验了解拼合原理在化学结构修饰方面的应用。
3. 通过本实验了解Schotten-Baumann酯化反应原理。
[实验内容]1、乙酰水杨酰氯的制备2、扑炎痛的制备3、精制4、结构确证[主要实验仪器与器材]1、主要药品:阿司匹林、氯化亚砜、吡啶、扑热息痛、氢氧化钠等2、主要仪器:三颈烧瓶、温度计、回流冷凝管、磁力搅拌器、圆底烧瓶、球形冷凝管、烧杯、气体回收装置等实验二磺胺醋酰钠的合成[实验目的和要求]1. 学习安息香缩合反应的原理和应用氰化钠及维生素B1为催化剂进行反应的实验方法。
2. 了解剧毒药氰化钠的使用规则。
[实验内容]1、磺胺醋酰的制备2、磺胺醋酰钠的制备3、结构确证[主要实验仪器与器材]1、主要药品:磺胺、氢氧化钠、醋酐、盐酸等2、主要仪器:三颈烧瓶、温度计、回流冷凝管、磁力搅拌器、圆底烧瓶、球形冷凝管、烧杯等实验三苯佐卡因的合成[实验目的和要求]1. 通过苯佐卡因的合成,了解药物合成的基本过程。
无水乙醇的制备流程

无水乙醇的制备流程英文回答:To prepare anhydrous ethanol, also known as absolute ethanol, there are several methods that can be used. One common method involves the use of a drying agent, such as calcium oxide or molecular sieves, to remove the water from ethanol.First, I would start by obtaining a sample of ethanol, which can be purchased commercially or obtained through the fermentation of sugars. It is important to ensure that the ethanol is of high purity, as impurities can affect the effectiveness of the drying process.Next, I would choose a suitable drying agent. Calcium oxide, also known as quicklime, is commonly used for this purpose. It reacts with water to form calcium hydroxide, effectively removing the water from the ethanol. Another option is to use molecular sieves, which are porousmaterials that can selectively adsorb water molecules.If using calcium oxide, I would add a small amount of the drying agent to the ethanol and stir the mixture. The calcium oxide will react with the water present in the ethanol, forming calcium hydroxide. I would then allow the mixture to settle, and decant or filter off the calcium hydroxide.If using molecular sieves, I would place the sieves in a container and add the ethanol. The molecular sieves will adsorb the water molecules, leaving behind anhydrous ethanol. After a sufficient amount of time, I would remove the molecular sieves from the container.In both cases, it is important to handle the drying agents with care, as they can be caustic and may react violently with water. It is also important to ensure that the equipment used is clean and dry, as any residual water can contaminate the anhydrous ethanol.Once the water has been removed, the anhydrous ethanolcan be further purified if desired. This can be done through distillation or other purification techniques.中文回答:制备无水乙醇,也被称为绝对乙醇,有几种方法可以使用。
实验一 绝对乙醇的制备

一、实验目的1、学习隔绝空气中湿气的回流反应装置使用。
2、掌握无水乙醇、绝对乙醇的制备方法。
二、实验原理市售的无水乙醇一般只能达到99.5%的纯度,在许多反应中需用纯度更高的绝对乙醇,经常需自己制备。
通常工业用的95.5%的乙醇不能直接用蒸馏法制取无水乙醇,因95.5%乙醇和4.5%的水形成恒沸点混合物。
要把水除去,第一步是加入氧化钙(生石灰)煮沸回流,使乙醇中的水与生石灰作用生成氢氧化钙,然后再将无水乙醇蒸出。
这样得到无水乙醇,纯度最高约99.5%。
纯度更高的无水乙醇可用金属镁或金属钠进行处理。
三、药品和仪器药品:95%乙醇 生石灰 氯化钙 镁条 金属钠 碘粒 邻苯二甲酸二乙酯仪器: 圆底烧瓶 冷凝管 干燥管 烧杯四、实验步骤1、无水乙醇(含量99.5%)的制备在100 mL 圆底烧瓶[1]中,放置50 mL 95 %乙醇和12 g 生石灰[2],用木塞塞紧瓶口,放置至下次实验[3]。
下次实验时,拔去木塞,装上回流冷凝管,其上端接一氯化钙干燥管,在水浴上回流加热1.5-2 h ,稍冷后取下冷凝管,改成蒸馏装置。
蒸去前馏分后,用干燥的吸滤瓶或蒸馏瓶作接受器,其支管接一氯化钙干燥管,使与大气相通。
用水浴加热,蒸馏至几乎无液滴流出为止。
称量无水乙醇的质量或量其体积,计算回收率。
2、绝对乙醇(含量99.95 %)的制备①用金属镁制取 在250 mL 的圆底烧瓶中,放置0.6 g 干燥纯净的镁条,10 mL 99.5 %乙醇,装上回流冷凝管,并在冷凝管上端附加一只无水氯化钙干燥管。
在沸水浴上或用火直接加热使达微沸,移去热源,立刻加入几粒碘片(此时注意不要振荡),顷刻即在碘粒附近发生作用,最后可以达到相当剧烈的程度。
有时作用太慢则需加热,如果在加碘之后,作用仍不开始,则可再加入数粒碘(一般讲,乙醇与镁的作用是缓慢的,如所用乙醇含水量超过0.5 %则作用尤其困难)。
待全部镁已经作用完毕后,加入100mL 99.5 %乙醇和几粒沸石。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
实验一 绝对乙醇的制备
一、实验目的
1、学习隔绝空气中湿气的回流反应装置使用。
2、掌握无水乙醇、绝对乙醇的制备方法。
二、实验原理
市售的无水乙醇一般只能达到%的纯度,在许多反应中需用纯度更高的绝对乙醇,经常需自己制备。
通常工业用的%的乙醇不能直接用蒸馏法制取无水乙醇,因%乙醇和%的水形成恒沸点混合物。
要把水除去,第一步是加入氧化钙(生石灰)煮沸回流,使乙醇中的水与生石灰作用生成氢氧化钙,然后再将无水乙醇蒸出。
这样得到无水乙醇,纯度最高约%。
纯度更高的无水乙醇可用金属镁或金属钠进行处理。
三、药品和仪器
药品:95%乙醇 生石灰 氯化钙 镁条 金属钠 碘粒 邻苯二甲酸二乙酯
仪器: 圆底烧瓶 冷凝管 干燥管 烧杯
四、实验步骤
1、无水乙醇(含量%)的制备
在100 mL 圆底烧瓶[1]中,放置50 mL 95 %乙醇和12 g 生石灰[2],用木塞塞紧瓶口,放置至下次实验[3]。
下次实验时,拔去木塞,装上回流冷凝管,其上端接一氯化钙干燥管,在水浴上回流加热 h ,稍冷后取下冷凝管,改成蒸馏装置。
蒸去前馏分后,用干燥的吸滤瓶或蒸馏瓶作接受器,其支管接一氯化钙干燥管,使与大气相通。
用水浴加热,蒸馏至几乎无液滴流出为止。
称量无水乙醇的质量或量其体积,计算回收率。
2、绝对乙醇(含量 %)的制备
①用金属镁制取 在250 mL 的圆底烧瓶中,放置 g 干燥纯净的镁条,10 mL %乙醇,装上回流冷凝管,并在冷凝管上端附加一只无水氯化钙干燥管。
在沸水浴上或用火直接加热使达微沸,移去热源,立刻加入几粒碘片(此时注意不要振荡),顷刻即在碘粒附近发生作用,最后可以达到相当剧烈的程度。
有时作用太慢则需加热,如果在加碘之后,作用仍不开始,则可再加入数粒碘(一般讲,乙醇与镁的作用是缓慢的,如所用乙醇含水量超过 %则作用尤其困难)。
待全部镁已经作用完毕后,加入100 mL %乙醇和几粒沸石。
回流1 h ,蒸馏,产物收集于玻璃瓶中,用一橡皮塞或磨口塞塞住。
②用金属钠制取 装置和操作同①,在250 mL 圆底烧瓶中,放置2 g 金属钠[4]
和100 mL 纯度至少为99 %的乙醇,加入几粒沸石。
加热回流30 min 后,加入4 g 邻苯二甲酸二乙酯[5]
,再回流10 min 。
取下冷凝管,改成蒸馏装置,按收集无水乙醇的要求进行蒸馏。
产品储于带有磨口塞或橡皮塞的容器中。
五、注意事项
1、本实验中所用仪器均需彻底干燥。
由于无水乙醇具有很强的吸水性,故操作过程中和存放时必须防止水分侵入。
2、一般用干燥剂干燥有机溶剂时,在蒸馏前应先过滤除去。
但氧化钙与乙醇中的水反应生成的氢氧化钙,因在加热时不分解,故可留在瓶中一起蒸馏。
3、若不放置,可适当延长回流时间。
4、金属钠遇水即燃烧、爆炸,故使用时应严格防止与水接触。
在称量和切片过程中应当迅速,以免空气中水气侵蚀或被氧化。
5、加入邻苯二甲酸二乙酯的目的,是利用它和氢氧化钠进行如下反应: 2C 2H 5OH + Mg (C 2H 5O)2Mg + H
(C 2H 5O)2Mg + 2H 22C 2H 5OH + Mg(OH)2
C 2H 5OH + Na C 2H 5ONa + H 12
C 2H 5ONa + H 2O
C 2H 5OH + NaOH
或COO COO C 2H 5C 2H 5
Na Na +2C 2H 5OH
+
因此消除了乙醇和氢氧化钠生成乙醇钠与水的作用,这样制得的乙醇可达到极高的纯度。
六、乙醇的纯度和密度对照表
七、思考题
为什么工业酒精不能直接用蒸馏法制取无水乙醇?。
