初中化学原子思维导图.
合集下载
初三化学九年级化学思维导图(1-12单元)-(2)

必须将纯物质质量 化学方程式的计算 带入方程式计算
溶质和溶剂的判断 质量关系
均一性 稳定性 混合物
NH4NO3
NaOH、H2SO4等
溶质
溶剂 组成
吸热 放热 溶解 现象
乳化
乳浊液和乳化现象
特征
温度和压强
饱和 溶液 分类 不饱和 溶液
定义
影响 因素 概念
溶液
气体 溶解度
定义、判断方法、 相互转化方法、 溶液的饱和不饱和 与浓稀的关系
净化方法
现状 水资源 爱护水污染 防治水体 污染 水的净化
水的电解 水的组成 氢气 实验结论 用途
自然界的水
物理性质 化学性质
验纯 可燃性
节约用水
还原性
第四单元 自然界的水
化合价
一般规律 应用
常见化合价 表示的意义 根据化学式求化合价 根据化合价写化学式
宏观
表示一种物质
微观
表示物质的一个分子 元素符号或 元素符号加小数字 根据化合价书写 三种以上含原子团
物质构成组成分子原子离子构成构成元素定义性质由分子构成的物质离子符号定义性质结构核外电子排布由原子构成的物质定义分类概念分类分布元素符号元素周期表由离子构成的物质元素符号表示的意义小动有间隔hcl等小动有间隔fecumghene常见离子物质构成的奥秘净化方法氢气水的电解硬水和软水硬水的软化区分方法概念硬水的危害水的组成水的净化水资源消毒蒸馏吸附过滤沉淀节约用水爱护水污染现状化学性质物理性质实验结论气体检验现象还原性可燃性用途加肥皂水煮沸或蒸馏防治水体污染计算相对分子质量化学用语化学式化合价相对分子质量相关计算计算元素质量比应用常见化合价一般规律化合物单质微观宏观写法和读法表示的意义表示一种物质表示物质的一个分子元素符号或元素符号加小数字根据化合价书写三种以上含原子团计算元素的质量分数根据化学式求化合价根据化合价写化学式计算某元素的质量自然界的水化学方程式书写质的方面应用质量守恒定律内容微观解释五个一定不变两个一定改变一个可能改变书写原则第五单元书写步骤配平方法意义定义量的方面粒子方面读法变与不变原子的三不变相关计算常见类型计算步骤理论依据已知反应物求生成物含杂质的计算涉及溶液的有关计算质量守恒定律下列叙述不适合用质量守恒定律解释的是
人教版九年级化学上册 《分子和原子》思维导图课件

思维导图解读——分 子
(4)用分子的观点解释问题 ①用分子观点解释物理变化、化学变化 由分子构成的物质,发生物理变化时分子本身未变,发生化学变化时分子本身 发生了变化,生成了其他物质的分子。例如,水变成水蒸气,水分子本身没有变, 只是分子间的间隔变大,这是物理变化;水通直流电,生成了氢分子和氧分子, 水分子发生了变化,这是化学变化。 ②用分子的观点解释纯净物和混合物 由同种分子构成的物质是纯净物,如水是由水分子构成的,它的组成和性质是 固定的;混合物是由不同种分子构成的,如空气是由氮气分子、氧气分子等构成 的,它的组成不固定,混合物中各物质仍保持各自原来的性质。
或反应中各原子种类和数目未发生改变等)
典例精析
【解析】 从第一个图分析知:每一个碳酸分子是由一个碳原子、两个 氢原子和三个氧原子构成的;对比第一、第二个图可知,在此变化过程中 体现了化学变化的本质,即一个碳酸分子分解成一个碳原子、两个氢原子 和三个氧原子,分子可以再分,而原子在化学变化中不可再分,是化学变 化中的最小粒子;第二、第三个图说明,原子可重新结合成分子,两个氢 原子和一个氧原子结合成一个水分子,两个氧原子和一个碳原子结合成一 个二氧化碳分子。
谢谢观看
思维导图解读——分 子
【注意】①分子只能保持物质的化学性质,但不能保持物理性质;物质 的物理性质(如:颜色、状态等)需要大量的集合体一起来共同体现,单个 分子无法体现物质的物理性质。例如,水和冰都是由水分子构成的,化学 性质相同,但物理性质不同,水是液态,冰是固态。
②分子是保持物质化学性质的“最小粒子”,不是“唯一”粒子,如构 成金刚石的“最小”粒子是碳原子。
典例精析
【例3】氧化汞受热时的变化可用下图表示(图中大圆圈表示汞原子,小圆圈 表示氧原子),下列根据图得出的结论错误的是 ( D )
人教版九年级化学上册 《元素》思维导图课件

思维导图解读——元 素
(6)元素与原子的区别和联系
项目 定义含义Βιβλιοθήκη 区别 适用范围联系
元素
原子
质子数(即核电荷数)相同的一类原子的总称 化学变化中的最小粒子
宏观概念:只表示种类,不表示个数
微观概念:既表示种类又表示个数
表示物质的宏观组成。如:水是由氢元素和 表示物质的微观构成。如:一个水分子是由
氧元素组成的
典例精析
【解析】对元素周期表的发现和完善做出贡献的科学家有门捷列 夫、道尔顿、张青莲等;由元素周期表可查出碳的相对原子质量为 12.01,16号元素是S;由于元素的种类由原子的核电荷数(或质子数)决 定,因此不同种元素最本质的区别是质子数不同;在元素周期表中, 原子序数=核电荷数。
谢谢观看
思维导图解读——元素周期表
(1)定义 根据元素的原子结构和性质,把现在已知的100多种元素科学有序地排列起 来,这样得到的表叫做元素周期表。 (2)编排依据 元素的性质随着原子序数的递增而呈周期性变化。 (3)编排原则 ①把电子层数相同的各种元素,按原子序数递增的顺序从左到右排成一横 行——周期。 ②把不同横行中最外层电子数相同的元素(个别例外),按电子层数递增的顺 序由上而下排成纵行——族。
思维导图解读——元素周期表
(7)元素周期表的简单应用 ①查找元素的相对原子质量、性质(金属元素、非金属元素、稀有气体元 素)。 ②判断元素的活动性。在同一族中越到下面的金属元素金属性越强,在同 一周期中越到左边金属性越强,所以金属活动性K>Na,Na>Mg>Al。 ③判断元素的化合价。元素的最高正价数=族序数;元素的最低负价=最高 正价数-8(稀有气体除外)。例如,镁、钙为+2价,铝为+3价,硫为+6价和-2 价,氯为+7价和-1价。
九年级化学思维导图(1-12单元最新)

催化剂
化合反应
不一定
氧化反应
分解反应
定义 性质
分子 概念 组成
小、动、有间隔
构成
构成 原子
由分子构成 的物质
H2 O2、N2、Cl2 H2O、CO2 、HCl等
分类
定义
性质 小、动、有间隔
核外电子排布
分布
元素
物质
元素符号
元素 周期表
构成
结构
由原子构成 的物质
元素符号 表示的意义
离子
Fe Cu Mg 、 He Ne、 C S P等
玻璃 造 纸 纺织 洗涤剂
俗名 纯碱,苏打 用途
俗名 食盐
用途
调味品,选种, 工业原料,生 理盐水
盐+金属=新盐+新金属 俗名 (盐可溶,前换后) 小苏打 盐的化性 盐+酸=新盐+新酸 常见的盐 有 ↓ ,↑ 或 NaHCO3 盐 + 碱 = 新盐 + 新碱 治疗胃 水生成 反应物 酸过多 用途 盐 可溶 盐1+盐2=盐3+盐4 发酵粉 复分解反应的定义,特 CaCO3 点,发生条件 大理石,石灰 石的主要成分 化肥 看外观 闻 鉴别 加碱,有刺激性气 用途 味气体放出为铵态氮 种类 建筑材料 氮肥 肥(铵盐的通性) 补钙剂 复合肥 茎,叶生长, 注:铵态氮肥不能与 磷肥 叶色浓绿 钾肥 两种或两种 碱性物质混合施用
金属的 存在形式
金银等——单质 大多数——化合物
铁的冶炼
反应原理
设备和产品 高炉——生铁 含杂质物质的
CO还原Fe2O3的 现象及注意事项 酒精灯迟到早退 尾气处理
必须将纯物质质量 化学方程式的计算 带入方程式计算
溶质和溶剂的判断 质量关系
化合反应
不一定
氧化反应
分解反应
定义 性质
分子 概念 组成
小、动、有间隔
构成
构成 原子
由分子构成 的物质
H2 O2、N2、Cl2 H2O、CO2 、HCl等
分类
定义
性质 小、动、有间隔
核外电子排布
分布
元素
物质
元素符号
元素 周期表
构成
结构
由原子构成 的物质
元素符号 表示的意义
离子
Fe Cu Mg 、 He Ne、 C S P等
玻璃 造 纸 纺织 洗涤剂
俗名 纯碱,苏打 用途
俗名 食盐
用途
调味品,选种, 工业原料,生 理盐水
盐+金属=新盐+新金属 俗名 (盐可溶,前换后) 小苏打 盐的化性 盐+酸=新盐+新酸 常见的盐 有 ↓ ,↑ 或 NaHCO3 盐 + 碱 = 新盐 + 新碱 治疗胃 水生成 反应物 酸过多 用途 盐 可溶 盐1+盐2=盐3+盐4 发酵粉 复分解反应的定义,特 CaCO3 点,发生条件 大理石,石灰 石的主要成分 化肥 看外观 闻 鉴别 加碱,有刺激性气 用途 味气体放出为铵态氮 种类 建筑材料 氮肥 肥(铵盐的通性) 补钙剂 复合肥 茎,叶生长, 注:铵态氮肥不能与 磷肥 叶色浓绿 钾肥 两种或两种 碱性物质混合施用
金属的 存在形式
金银等——单质 大多数——化合物
铁的冶炼
反应原理
设备和产品 高炉——生铁 含杂质物质的
CO还原Fe2O3的 现象及注意事项 酒精灯迟到早退 尾气处理
必须将纯物质质量 化学方程式的计算 带入方程式计算
溶质和溶剂的判断 质量关系
初中化学知识思维导图
已知某一反应物计算另一种物质
【分析】图像型计算
【分析】无数据或缺数据型化学方程式计算
质量守恒定律概念 化学方程式的概念及意义
有关化学方程式的计算
考法
质量守恒定律
乳化现象
溶解时的吸热和放热现象 溶解过程中的热量变化
饱和溶液与不饱和溶液概念
溶液概念及组成
溶液及溶解现象
饱和溶液与不饱和溶液转化
固体的溶解度
气体的溶解度
趋势图-平缓和陡升组合
趋势图-陡升和下降组合
趋势图-下降+陡升+平缓组合
趋势图-先升后降 溶解度曲线和溶液综合
溶解度曲线应用
溶解度曲线含义
降温结晶 蒸发结晶
混合物分离方法
溶解度
溶质析出大小比较 状态转换方法选择
动点问题
流程类计算
文字表述型计算
曲线图型计算
实验操作图型计算
溶质质量分数及其计算
酸碱盐间转化关系
pH与溶液酸碱度的关系
溶液酸碱度的表示方法
pH的测定方法
pH曲线
pH曲线变化趋势
根据曲线图判断溶液成分
化学肥料
常用化肥的种类和作用 合理使用化肥和农药
化肥的简易鉴别
考法
微观角度认识化学
质量守恒定律的验证
质量守恒定律的微观解释
质量守恒定律探究实验
解释宏观现象
化学式的推断
元素组成判断
质量守恒定律应用确定反应物或生成物质量
确定物质的相对原子质量
确定化学反应类型
化学方程式配平
化学方程式的书写
根据微观示意图书写方程式
【技巧】含杂质化学方程式的计算
【技巧】差量法计算
【分析】表格型计算
初中化学《原子》单元教学设计以及思维导图

主题单元规划思维导图(说明:将主题单元规划的思维导图导出为 jpeg 文件后,粘贴在这里;如果提交到平台,则需要使用图片导入的功能, 具体操作见《2013 学员教师远程研修手册》。)
主题单元学习目标(说明:依据新课程标准要求描述学生在本主题单 元学习中所要达到的主要目标) 知识与技能: 认识原子的真实存在,了解原子的基本性质,认识原子核的结构, 理 解原子的概念,会用分子、原子的观点来解释物理变化和化学变化; 掌握质量数、质子数、中子数、电子数间的关系。能进行质量数、质 子数、中子数、电子数间的简单计算 掌握原子核外电子的排布规律,理解最外层电子数对原子化学性质的
题设计
2、核外电子的排布有什么规律?
3、如何表示原子的质量?
专题划分
专题一:原子结构
(1 课时)
专题二:核外电子的排布
( 1 课时)
专题三:相对原子质量
( 1课
时)
专题一
原子的结构
所需课时
:课内共用一课时,每周三课时
专题学习目标 (说明:描述学生在本专题学习中所要达到的学习目 标,注意与主题单元的学习目标呼应)
原子
适用年级
九年级
所需时间
课内共用 4 课时,每周 3 课时;课外共用 3 课时
主题单元学习概述(说明:简述主题单元在课程中的地位和作用、单元 的组成情况,单元的学习重点和难点、解释专题的划分和专题之间的 关系,单元的主要学习方式和预期的学习成果,字数 300-500。)
从宏观到微观、从定性到定量,体现了化学学科发展的趋势。对物质 组成的微观研究和定量研究使化学逐步成为能在实验和理论两个方面 都获得迅速发展的一门自然科学。 本 主题旨在帮助学生用微粒的观念去学习化学,通过观察、想象、类 比、模型化的方法使学生初步理解化学现象的本质;从五彩缤纷的宏 观世界步入充满神奇色彩的微 观世界,激发学生学习化学的兴趣;利 用有关探索原子结构的科学史实,使学生了解科学家严谨求实的科学 态度;通过对问题的探究和实践活动,提高学生的想象能 力、创新能 力,帮助学生初步认识辩证唯物主义的一些观点。 本主题的教学应结合学生熟悉的现象和已有的经验,创设生动直观的 情景,从身边的现象和简单的实验入手认识物质的微粒性,理解有关 物质构成的微观概念;引导学生运用物质构成的初步知识解释一些简 单的化学现象。
初三化学九年级化学思维导图(1-12单元) (2)
反应
定义、常见铁合金——生铁和钢 合金与纯金属的性质比较
原料 铁矿炼
金银等——单质
大多数——化合物
含杂质物质的
必须将纯物质质量 带入方程式计算
化学方程式的计算
2021/6/21
高温条件下,利用焦炭反应
反应原理 生成的一氧化碳将铁从铁矿
石中还原出来
设备和产品 高炉——生铁
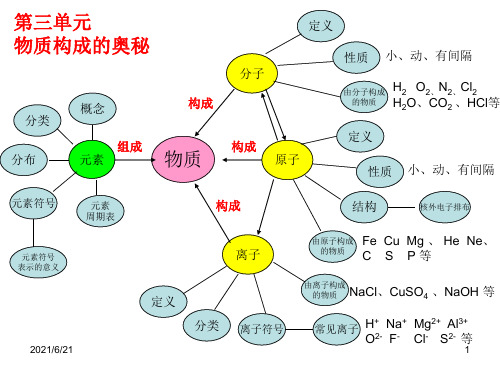
第三单元 物质构成的奥秘
分类 分布
概念
构成
组成
元素
物质
定义
分子
性质 小、动、有间隔 由分子构成 H2 O2、N2、Cl2
的物质 H2O、CO2 、HCl等
构成 原子
定义 性质 小、动、有间隔
元素符号
元素 周期表
元素符号 表示的意义
2021/6/21
构成
结构
核外电子排布
离子
由原子构成 Fe Cu Mg 、 He Ne、 的物质 C S P 等
反应后溶液 质量的计算
概念
溶解度
溶液 的浓度
溶质的 质量分数
相关计算
概念
固体 溶解度
结晶 方法
蒸发结晶
影响
溶解度 降温结晶
因素
内因:
曲线
溶解性
表示的意义:
溶质2和02溶1/6剂/2的1 性质 外因:温度
划分方法
点、交点、线 相关应用:
液体的 体积分数
75%的 酒精溶液
溶液的配制
固体配制
计算 称量 溶解
CO还原Fe2O3的 酒精灯迟到早退 现象及注意事项 尾气处理
10
溶质和溶剂的判断 NH4NO3
质量关系
均一性
溶质 溶剂
