第五届Chemy化学奥林匹克竞赛联赛试题
05高中学生化学竞赛试题及参考答案

浙江省高中学生化学竞赛试题考生须知:1.全卷分为试题卷和答题卷两部分。
试题共有六大题,27小题,满分150分。
考试时间120 分钟。
2.本卷答案必须做在答题卷相应位置上,做在试题卷上无效,考后只交答题卷。
必须在答题卷上写明县(市)、学校、姓名、准考证号,字迹清楚。
相对原子质量:H-1 C-12 N-14 O-16 Na-23 Al-27 Si-28 S-32 K-39 Cl-35.5 Fe-56 Cu-64 Hg-200.6一、选择题(本题包括10小题,每小题4分,共40分,每小题只有一个选项符合题意)1.我国“神舟5号”宇宙飞船的运载火箭的推进剂引燃后发生剧烈反应,产生大量高温气体从火箭尾部喷出。
引燃后的高温气体成分有CO2、H2O、N2、NO等,这些气体均为无色,但在卫星发射现场看到火箭喷射出大量红烟,产生红烟的原因是(A) 高温下N2遇空气生成NO2(B) NO遇空气生成NO2(C) CO2与NO反应生成NO2(D) NO与H2O反应生成NO22.下列物质使用合理的是(A) 在制玻璃的原料中再加入Co2O3制成蓝色玻璃(B)用加酶洗衣粉洗涤毛料服装(C)用甲醛溶液浸泡海产食品(D)用酚醛树脂制作高弹力运动鞋3.对盐类物质可有下列分类:如氯化硝酸钙[Ca(NO3)Cl]是一种混盐,硫酸铝钾KAl(SO4)2是一种复盐,冰晶石(六氟合铝酸钠)Na3AlF6是一种络盐。
对于组成为CaOCl2的盐可归类于(A)混盐(B)复盐(C)络盐(D)无法归属于上述类别4.某同学在做苯酚的性质实验时,将少量溴水滴入苯酚溶液中,结果没有发生沉淀现象,他思考了一下,又继续在反应混合液中滴入足量的氢氧化钠溶液,此时他发现(A) 溶液中仍无沉淀(B) 溶液中产生白色沉淀(C) 先产生沉淀后沉淀溶解(D) 溶液呈橙色5.镓是1871年俄国化学家门捷列夫在编制元素周期表时曾预言的“类铝”元素。
镓的原子序数为31,属ⅢA族。
五大竞赛考试题目及答案

五大竞赛考试题目及答案一、单项选择题(每题2分,共10题)1. 以下哪个选项是计算机科学领域中著名的算法?A. 牛顿法B. 欧几里得算法C. 傅里叶变换D. 麦克斯韦方程组答案:B2. 化学中,哪种元素的原子序数为26?A. 铁B. 铜C. 铁D. 锌答案:B3. 在物理学中,光速在真空中的速度是多少?A. 299,792,458米/秒B. 299,792,458千米/秒C. 299,792,458厘米/秒D. 299,792,458英里/秒答案:A4. 数学中,勾股定理描述的是哪种关系?A. 三角形的面积B. 三角形的周长C. 直角三角形的边长关系D. 三角形的内角和答案:C5. 生物学中,DNA的双螺旋结构是由哪位科学家提出的?A. 达尔文B. 孟德尔C. 沃森和克里克D. 摩尔根答案:C二、多项选择题(每题3分,共5题,每题至少有两个正确答案)1. 以下哪些是编程语言?A. PythonB. JavaC. HTMLD. C++答案:A, B, D2. 以下哪些是有机化学中的官能团?A. 羟基B. 羧基C. 氨基D. 甲烷答案:A, B, C3. 在物理学中,以下哪些是基本力?A. 重力B. 电磁力C. 核力D. 摩擦力答案:A, B, C4. 数学中,以下哪些是几何图形?A. 圆B. 三角形C. 函数D. 矩形答案:A, B, D5. 生物学中,以下哪些是细胞器?A. 线粒体B. 核糖体C. 细胞壁D. 叶绿体答案:A, B, D三、填空题(每题4分,共5题)1. 计算机存储单位中,1TB等于_______GB。
答案:10242. 化学方程式2H2 + O2 → 2H2O中,反应物和生成物的摩尔比是_______。
答案:2:1:23. 物理学中,牛顿第二定律的公式是_______。
答案:F = ma4. 数学中,圆的面积公式是_______。
答案:πr²5. 生物学中,细胞分裂过程中,染色体数量在有丝分裂后期是_______。
Chemy化学竞赛联赛试题集

Chemy化学竞赛联赛试题集1. 题目一题目描述在实验室中进行酸碱中和反应时,为了准确地确定终点,通常会使用酸碱指示剂。
常见的酸碱指示剂有酚酞、溴酚蓝等。
请解释为什么酚酞适用于中和硫酸钡和硫酸钙的反应中,而溴酚蓝适用于中和盐酸和氢氧化钠的反应中。
解答酚酞是一种酸碱指示剂,其分子结构中含有酚酞的酮式、酮酸式和酸式三种共存。
在酸性溶液中,酚酞处于酮酸式,为无色;在碱性溶液中,酚酞处于酸式,呈现亮红色。
硫酸钡和硫酸钙是强酸与弱碱的中和反应,所以在反应过程中,随着酸的逐渐中和,溶液的pH值会逐渐升高,变为碱性。
因此,当反应快接近中和点时,溶液中的酚酞会呈现亮红色,这是因为反应中初始的强酸会先中和完,而剩下的弱碱会使溶液呈碱性。
溴酚蓝也是一种酸碱指示剂,其分子结构呈靛蓝色。
溴酚蓝在酸性溶液中呈黄色,而在碱性溶液中呈蓝色。
盐酸和氢氧化钠的反应是强酸与强碱的中和反应,所以在反应过程中,酸和碱的浓度会逐渐减小,直到完全中和。
当反应接近中和点时,溶液中的酸和碱的浓度相等,此时溶液呈中性。
溴酚蓝在中性溶液中显示出的颜色正好是靛蓝色,因此可以作为该中和反应的指示剂。
总结起来,酚酞适用于中和硫酸钡和硫酸钙反应是因为反应是强酸与弱碱的中和反应,而溴酚蓝适用于中和盐酸和氢氧化钠反应是因为反应是强酸与强碱的中和反应。
在选择适用的酸碱指示剂时,需要考虑到反应中酸碱的强度差异,以及反应接近中和点时溶液的pH值变化情况。
2. 题目二题目描述浑浊的水中常常含有多种悬浮物质,如粉尘、细菌、藻类等。
使用澄清剂可以将这些悬浊物质沉淀下来,从而净化水质。
请简要介绍澄清剂的工作原理,并举例说明一种常见的澄清剂及其应用。
解答澄清剂是一种可以将悬浮物质沉淀下来的化学物质,其工作原理主要包括两个方面:吸附和沉淀。
首先,澄清剂中的吸附剂可以吸附水中的悬浮物质。
吸附剂通常具有较大的比表面积,可以提供更多的接触面积,使得悬浊粒子更容易和吸附剂接触并吸附上去。
第五届Chemy化学奥林匹克竞赛联赛试题答案

第五届Chemy化学奥林匹克竞赛联赛试题答案第五届Chemy化学奥林匹克竞赛联赛试题答案(2021年8月27日 9:00 ~ 12:00)题号满分得分评卷人 1 13 2 11 3 13 4 10 5 11 6 8 7 9 8 14 9 11 总分 100 ・竞赛时间3小时。
迟到超过半小时者不能进考场。
开始考试后1小时内不得离场。
时间到,把试卷(背面朝上)放在桌面上,立即起立撤离考场。
・试卷装订成册,不得拆散。
所有解答必须写在指定的方框内,不得用铅笔填写。
草稿纸在最后一页。
不得持有任何其他纸张。
・姓名、报名号和所属学校必须写在首页左侧指定位置,写在其他地方者按废卷论处。
・允许使用非编程计算器以及直尺等文具。
H He 相对原子质量 1.008 4.003 Li Be B C N O F Ne 6.941 9.012 10.81 12.01 14.01 16.00 19.00 20.18 Na Mg Al Si P S ClAr 22.99 24.31 26.98 28.09 30.97 32.07 35.45 39.95 K Ca Sc Ti V Cr Mn Fe Co Ni Cu Zn Ga Ge As Se Br Kr 39.10 40.08 44.96 47.88 50.94 52.00 54.94 55.85 58.93 58.69 63.55 65.41 69.72 72.61 74.92 78.96 79.90 83.80 Rb Sr Y Zr Nb Mo Tc RuRh Pd Ag Cd In Sn Sb Te I Xe 85.47 87.62 88.91 91.22 92.91 95.94 [98] 101.1 102.9 106.4 107.9 112.4 114.8 118.7 121.8 127.6 126.9 131.3 Cs Ba La-Hf Ta WRe Os Ir Pt Au Hg Tl Pb Bi Po At Rn 132.9 137.3 Lu 178.5 180.9 183.8 186.2190.2 192.2 195.1 197.0 200.6 204.4 207.2 209.0 [210] [210] [222] Fr Ra Ac-Rf Db Sg Bh Hs Mt Ds Rg Cn Uut Uuq Uup Uuh Uus Uuo [223] [226] La LaCe Th Pr Pa Nd U Pm Np Sm Pu Eu Am Gd Cm Tb Bk Dy Cf Ho Es Er Fm Tm Md YbNo Lu Lr Ac第1题(13分)1-1 氢化锂铝是有机反应常用的还原剂,过量的氢化锂铝常使用叔丁醇淬灭,写出淬灭过程的反应方程式。
化学奥林匹克竞赛精选真题

化学奥林匹克竞赛精选真题化学奥林匹克竞赛一直以来都备受关注,它不仅可以培养学生对化学的兴趣和探索精神,还能锻炼他们的思维能力和解决问题的能力。
本文将为大家提供一些化学奥林匹克竞赛的精选真题,希望能够帮助大家更好地理解和应对这些竞赛。
第一题:单质与化合物某化学实验室用硅和氯化铝作为原料合成了硅氯化铝。
已知合成反应的化学方程式为:Si + 3Cl2 → SiCl4(1) 请写出该反应中化学键的断裂和形成;(2) 简要解释该反应中氯元素的化合价变化过程。
解析:首先,化学键的断裂和形成如下所示:Si: [Ne]3s2 3p2 → [Ne]3s2 3p1 (断裂)Cl2: [Ne]3s2 3p6 → ([Ne]3s2 3p6) → [Ne]3s2 3p5 (断裂、形成)SiCl4: ([Ne]3s2 3p2) + 4([Ne]3s2 3p5) → [Cl]3s2 3p6 + [Si]3s2 3p0 (形成)其次,氯元素的化合价变化过程如下所示:Cl2的化合价是0,形成化学键后,每个氯原子失去一个电子,化合价变为-1。
由于氯元素和硅元素原子通过共价键结合,硅元素的化合价为+4。
第二题:溶液滴定某溶液中含有未知浓度的硫酸(H2SO4)。
为了确定其浓度,需要用0.10 mol/L的氢氧化钠(NaOH)溶液进行滴定。
已知反应方程式如下所示:H2SO4 + 2NaOH → Na2SO4 + 2H2O(1) 写出该反应中的物质进量关系;(2) 若滴定过程中,我们向硫酸溶液中加入了酚酞指示剂,请问溶液开始变为粉红色的现象是在何时出现的?解析:首先,该反应中的物质进量关系如下所示:1 mol H2SO4 反应生成 1 mol Na2SO42 mol NaOH 反应生成 1 mol Na2SO4根据化学方程式,可知物质进量的配比关系为H2SO4:NaOH=1:2。
其次,在滴定过程中加入了酚酞指示剂后,硫酸溶液开始变为粉红色的现象是在中和点附近出现的。
1995年(第五届天原杯)初中奥林匹克化学竞赛试题

1995年(第五届天原杯)初中奥林匹克化学竞赛试题
1995年(第五届天原杯)初中奥林匹克化学竞赛试题点击这里下载WORD版内容预览:
原子量:H-1 C-12 N-14 O-16 Na-23
Mg-24 Al-27 S-32 K-39 Ca-40
Fe-56 Cu-64 Zn-65 Ag-108 Ba-137
一、(本题共40分)下列小题分别有1个或2个正确答案,把正确答案的编号填在括号里。
1.天原化工厂是氯碱工业的现代化工厂,原料食盐用水溶解制得饱和食盐水,在电解前要除去杂质(如氯化钙、硫酸钙、氯化镁),通常要加入的试剂是( )
①AgNO3 ②BaCl2 ③NaOH ④Na2CO3
⑤Ca(OH)2
(A) ①②③ (B)②③④ (C)①④⑤
(D)②③⑤
2.下列各组物质中,前者属纯净物,后
者属混合物的是( )
(A)汽油丁烷 (B)钢生铁
(C)水水煤气 (D)乙烯聚氯乙烯
3.下列叙述中正确的是( )
(A)混合物中元素一定呈化合态。
(B)某物质中只含有一种元素,该物质一定是纯净物。
(C)同素异形体之间的转变一定是化学变化。
(D)某纯净物质不是化合物就是单质。
高中化学奥林匹克竞赛(有机化学)高二检测题(附答案)
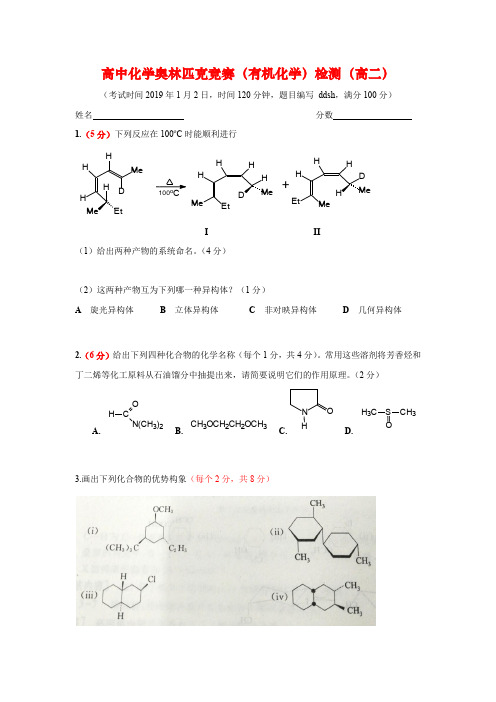
高中化学奥林匹克竞赛(有机化学)检测(高二)(考试时间2019年1月2日,时间120分钟,题目编写 ddsh ,满分100分) 姓名 分数 1.(5分)下列反应在100o C 时能顺利进行I II(1)给出两种产物的系统命名。
(4分)(2)这两种产物互为下列哪一种异构体?(1分)A 旋光异构体B 立体异构体C 非对映异构体D 几何异构体2.(6分)给出下列四种化合物的化学名称(每个1分,共4分)。
常用这些溶剂将芳香烃和丁二烯等化工原料从石油馏分中抽提出来,请简要说明它们的作用原理。
(2分)A. B.C.D.3.画出下列化合物的优势构象(每个2分,共8分)+H CO N(CH 3)2CH 3OCH 2CH 2OCH 3N OHH 3C S OCH 34.判断下列分子是否具有光学活性(共10分)5.下列各组化合物都能够发生分子内的SN2反应。
对各组反应的难易程度进行排序(6分)6.(每式1分,每个命名1分,共9分)2004年是俄国化学家马科尼可夫(V . V . Markovnikov ,1838-1904)逝世100周年。
马科尼可夫因提出C =C 双键的加成规则(Markovnikov Rule )而著称于世。
本题就涉及该规则。
给出下列有机反应序列中的A 、B 、C 、D 、E 、F 和G 的结构式,并给出D 和G 的系统命名。
7.(13分)写出下列反应的每步反应的主产物(A 、B 、C )的结构式;若涉及立体化学,请用Z 、E 、R 、S 等符号具体标明。
(B 是两种几何异构体的混合物)8.(13分)以氯苯为起始原料,用最佳方法合成1-溴-3-氯苯(限用具有高产率的各反应,标明合成的各个步骤)。
CH 2COOH CH 2COOHACH CHO(等摩尔)BHBrC9.(10分)用苯、不超过四个碳的有机化合物和合适的无机试剂为原料合成以下产物:10.(20分)写出下列转化的反应流程高中化学奥林匹克竞赛(有机化学)检测(高二)(答案和评分)(满分100分,时间120分钟)考试时间2019年1月2日 试题编制 dds姓名 分数 1. (5分) 下列反应在100o C 时能顺利进行:I II(1)给出两种产物的系统命名。
化学竞赛决赛试题及答案

化学竞赛决赛试题及答案一、选择题(每题3分,共30分)1. 下列哪种元素的原子序数最小?A. 氢B. 氦C. 锂D. 铍答案:A2. 化学反应中,能量变化通常表现为哪两种形式?A. 光能和热能B. 电能和热能C. 光能和电能D. 机械能和热能答案:A3. 根据元素周期表,下列元素中属于第ⅢA族的是?A. 硼(B)B. 铝(Al)C. 镓(Ga)D. 铟(In)答案:C4. 以下哪个化学式表示的是二氧化硫?A. SO2B. SO3C. SO4D. S2O2答案:A5. 酸碱中和反应的实质是什么?A. 酸碱的离子交换B. 酸碱的电子转移C. 酸碱的质子转移D. 酸碱的分子结合答案:C6. 哪种类型的晶体结构中,原子排列是三维周期性的?A. 非晶态B. 多晶态C. 单晶态D. 混合晶体答案:C7. 根据化学键理论,下列哪种键属于离子键?A. 氢键B. 金属键C. 共价键D. 离子键答案:D8. 以下哪种物质是强酸?A. 醋酸B. 碳酸C. 硫酸D. 氢氧化钠答案:C9. 哪种元素的电子构型是1s²2s²2p⁶3s²3p⁶?A. 氧(O)B. 钠(Na)C. 镁(Mg)D. 硫(S)答案:B10. 以下哪种反应属于氧化还原反应?A. 酸碱中和B. 沉淀形成C. 单质之间的反应D. 同素异形体之间的转化答案:C二、填空题(每题4分,共20分)1. 元素周期表中,第______周期包含的元素种类最多。
答案:六2. 一个水分子(H₂O)中含有______个原子。
答案:33. 化学方程式2H₂ + O₂ → 2H₂O中,反应物和生成物的摩尔比是______。
答案:1:14. 元素周期表中,第ⅤⅡA族元素的原子序数范围是______。
答案:57-715. 摩尔质量的单位是______。
答案:g/mol三、简答题(每题10分,共30分)1. 请简述什么是化学平衡,并举例说明。
答案:化学平衡是指在一个封闭系统中,正向反应和逆向反应的速率相等,反应物和生成物的浓度不再发生变化的状态。
历年化学竞赛试题及答案

历年化学竞赛试题及答案1. 题目:下列物质中,属于纯净物的是:A. 空气B. 蒸馏水C. 盐水D. 石油答案:B2. 题目:在化学反应中,能够作为催化剂的物质是:A. 反应物B. 生成物C. 反应前后质量不变的物质D. 反应前后质量增加的物质答案:C3. 题目:下列关于原子结构的描述中,正确的是:A. 原子核由质子和中子组成B. 电子在原子核内运动C. 原子核内只有质子D. 电子在原子核外运动答案:A4. 题目:下列物质中,属于化合物的是:A. 铁B. 氧气C. 水D. 氢气答案:C5. 题目:在标准状况下,1摩尔任何气体的体积都是:A. 22.4LB. 22.4mLC. 224LD. 2240L答案:A6. 题目:下列元素中,属于碱金属元素的是:A. 钠B. 镁C. 铝D. 钾答案:A7. 题目:下列关于化学键的描述中,正确的是:A. 离子键是由正负离子之间的吸引力形成的B. 共价键是由原子核之间的吸引力形成的C. 金属键是由金属原子之间的排斥力形成的D. 氢键是一种化学键答案:A8. 题目:下列关于溶液的描述中,正确的是:A. 溶液是均一、稳定的混合物B. 溶液中的溶质和溶剂可以是固体C. 溶液中的溶质和溶剂可以是液体D. 溶液中的溶质和溶剂可以是气体答案:A9. 题目:在化学反应中,能够作为还原剂的物质是:A. 氧化剂B. 还原剂C. 催化剂D. 反应物答案:B10. 题目:下列关于酸碱中和反应的描述中,正确的是:A. 酸和碱反应生成盐和水B. 酸和碱反应生成气体和水C. 酸和碱反应生成盐和气体D. 酸和碱反应生成盐和氧化物答案:A。
第二届Chemy化学奥林匹克竞赛联赛试题
(2016 年 9 月 28 日 18:00 ~ 22:00) 题号 1 2 3 4 5 6 7 8 9 总分 满分 10 11 10 12 10 13 8 14 12 100 得分
评卷人
·竞赛时间 4 小时。迟到超过半小时者不能进考场。开始考试后 1 小时内不得离场。时间到, 把试卷(背面朝上)放在桌面上,立即起立撤离考场。 ·试卷装订成册,不得拆散。所有解答必须写在指定的方框内,不得用铅笔填写。草稿纸在 最后一页。不得持有任何其他纸张。 ·姓名、报名号和所属学校必须写在首页左侧指定位置,写在其他地方者按废卷论处。 ·允许使用非编程计算器以及直尺等文具。
Vilsmeier salt 和等当量的碱与邻氨基苯甲酰胺反应合成化合物 A,但是发现 没有 A 生成,却得到了黄色低熔点不易结晶的化合物 B。经过液相质谱仪
碳一化学指以只含一个碳原子的化合物(如 CO、CH4等)为原料来合成一系列化工原料和 燃料的化学。其中甲烷是碳一化学中的重要组成部分,甲醇则作为碳一化学的核心产品。用
甲烷生产甲醇有蒸汽转化、催化部分氧化、非催化部分氧化等方法。其中蒸汽转化法包括以
下四个反应:
已知在 298K 下:
(1) CH4(g) + H2O(g) = CO(g) + 3H2(g) (2) CO(g) + H2O(g) = CO2(g) + H2(g)
3.75
0.42
1.5
1.5
3.95
0.42
1.5
6.75
3.55
0.68
1.5
4.5
3.55
0.61
1.5
5.8
4.15
0.62
Chemy化学竞赛联赛试题集答案

Chemy化学竞赛联赛试题合集第一辑(第一届~第八届)参考答案Chemy化学竞赛团队两周年献礼2018年5月本版试题合集仅用于非商业用途交流使用,婉拒商业机构等盈利组织未经授权的转载行为。
版权归全体试题作者共有,侵权必究。
第一届Chemy化学奥林匹克竞赛联赛答案(2016年7月24日19:00 ~ 21:00)·竞赛时间3小时。
迟到超过半小时者不能进考场。
开始考试后1小时内不得离场。
时间到,把试卷(背面朝上)放在桌面上,立即起立撤离考场。
·试卷装订成册,不得拆散。
所有解答必须写在指定的方框内,不得用铅笔填写。
草稿纸在最后一页。
不得持有任何其他纸张。
·姓名、报名号和所属学校必须写在首页左侧指定位置,写在其他地方者按废卷论处。
·允许使用非编程计算器以及直尺等文具。
第1题(8分)1-1 将明矾置于河水中搅拌,生成载带着悬浮物的氢氧化铝,然后沉降,使水澄清。
但若用蒸馏水代替河水,便不会发生以上现象,请解释该过程的原因,并写出生成氢氧化铝的方程式。
程式。
出化学反应方程式。
第2题(8分)有一个经验规则可以用于估算基元反应的活化能。
①反应中没有键的断裂的反应;②自由基与分子的放热反应;③反应中键不完全断裂(如协同反应)的反应。
④反应中键完全断裂的反应。
遵循上述情况时,分别通过对应下表中计算方法计算活化能:BE是反应中断掉的键的键能之和。
根据上述经验规则及所提供的键能信息,估算氢气与氯气反应中各步基元反应的活化能,并与所给出的实验值比较。
Cl2 = 2Cl·E a1 = 242.8 kJ·mol-1Cl· + H2 = HCl + H·E a2= 25.1 kJ·mol-1H· + Cl2 = HCl + Cl·E a3= 12.6 kJ·mol-1-1-1-1第3题(8分)3-1 Cr2,Mo2与W2分子中存在着六重键,金属的ns轨道与(n-1)d轨道参与成键。
第五届国际生物奥林匹克竞赛模拟试题——其他题型

第五届国际生物奥林匹克竞赛试题其他题型101.下列生物高分子:核酸、蛋白质和多糖可能有以下特点:A 线状,几乎无分枝B 线状或有分枝C 同聚物,由完全相同的单体组成D 杂聚物,由不同的单体组成将正确答案填入下表,用字母代表各种特点。
注意一种高分子可能有几种特点。
生物高分子特点核酸蛋白质多糖102.下面图示表明红色面包霉通常通过一套酶系统由原料合成它自身的氨基酸。
根据字母A~D代表的意思,分别将其与下面的6句话对应起来。
A 根据上图作出的合乎逻辑的假说B 不合逻辑的假说C 与上图无关的假说D 只是重复上图中已有的信息①酶A催化由原料形成鸟氨酸的反应;②若基因B不存在,则鸟氨酸可直接形成精氨酸;③老基因A被破坏,则向培养基中加入鸟氨酸,面包霉仍能存活;④者基因B被破坏,则向培养基中加入酶B,面包霉仍能存活;⑤基因C指导酶C的形成;⑥不同的霉菌对氨基酸的要求不同。
103.T一控制A植物的显性等位基因,表现为高植株。
t一隐性等位基因,表现为矮植株。
R一显性基因,控制茎的绿色。
r一隐性基因,控制茎的紫色。
在随机受粉的A植表现型高植株矮植株绿茎紫茎绿茎紫茎%63 21 12 4回答下列问题:A.基因型为TT的植物的百分比是多少?B.基因型为TTRR的植物百分比是多少?104.根据字母A~E代表的意义,分别将其与给出的演化概念(①一⑤)对应起来。
①基因流动,②有性繁殖的种,③自然选择,④突变后遗传漂变。
A 新的等位基因的唯一来源B 一种群中等位基因相对频率增加或减少的机会C 一个或多个种群中的成员可进行交配并产生有生育能力的后代D 由于迁入或迁出,等位基因在种群中的频率发生变化E 种群中变种成员在生存和繁殖力上的差别105参考答案与解析101.核酸——A,D;蛋白质——A,D;多糖——B,C,D核酸、蛋白质都是没有分枝的线状分子。
核酸由不同的核苷酸组成,蛋白质由不同的氨基酸组成。
多糖类可能是线状(如直链淀粉、纤维素),也可能有分枝(如支链淀粉、糖元),可能由一种单体组成(如淀粉、纤维素均由葡萄糖组成),也可能由两种或两种以上单体组成(如木一葡聚糖由木糖与葡萄糖组成)。
2008年第五届我爱奥赛网高中化学网络联赛试题答案

我爱奥赛网2008年第五届“我爱奥赛杯”高中化学竞赛试题参考答案第1题(6分)1-1、80 (2分)1-2、P , 铼(2分,各1分)1-3、3(NH4)2SO4+ 6 NaBH4 == 2B3N3H6 + 3Na2SO4 + 18 H2B3N3H6 == 3BN + 3H2 (2分,各1分)第2题(10分)2-1、(2)>(3)>(1) (2分)2-2、碱性增加,2NH3NH4+ + NH2—NH3 + N3- = HN2- + NH2-或2NH3 + N3- = 3NH2-(2分)2-3、HS-,H2O2,N2H5+ (全对给2分,其他合理结论也给分)2-4、NH3F的吸电子能力强,使N上电子云密度降低(2分,各1分)2-5、H[SbF5(OSO2F)]+HSO3F =H2SO3F++[SbF5(OSO2F)]-(2分)第3题(8分)3-1、NO2-为角型,(1分)由于只一种N-O键长,应为氮原子配位(1分)3-2、若R中不含N,则氧元素含量为(0.3033/14) x32=0.6933,M,N,O之和将超过1,是不可能的。
所以R必为含氮配体。
设R中含x个N,则有n M : n N = 0.2127/M M : 0.3033/14.01 = 1 :(2x+ 4)M M=19.65(x+2)x=1时,有合理解,M M=58.95 为Co元素,(元素,1分)配离子摩尔质量=277g/mol,扣除掉1个Co,6个N,8个O后还剩下6,应为6个H,故配体R为NH3,配离子化学式为[Co(NH3)2(NO2)4]-,(化学式,2分)名称为四亚硝酸根·二氨合钴(|||)离子(1分)3-3、由于只一种N-O键长,所有氧原子等价,则配离子结构应为:(2分)第4题4-1、X:Ag2S, A:SC(NH2)24Ag + 2H2S + O2 = 2Ag2S + 2H2O. (各1分共3分)4-2、(1)2Al +3Ag2S+6H2O+3 Na2CO3=2Al(OH)3 +6Ag+ 3NaHS +3NaHCO3或负极:Al -3e- = Al3+正极:3Ag2S + 6e-= 6Ag+3S2-(3)Ag 2S + 8SC(NH 2)2 = 2Ag[SC(NH 2)2]4+ + S 2-. (各1分 共3分)4-3、Ag 2S 2Ag + + S 2-,S 2- + H 2O HS - + OH - ,HS - + H 2O H 2S + OH -.C s = [H 2S] + [HS -] + [S 2-], [Ag +] = 2C s ,[S 2-] = α C s , Ag 2S ksp 极小,[H +]可视为10—7mol/L (1分)2122222222K K ][H K ][H 1][S S][H ][S ][HS 1][S S][H ][HS ][S α1++------++=++=++=,104,910109,510109,51010109,5K K ][H K ][H K K α81487814148211221--------++⨯=⨯⨯+⨯⨯+⨯⨯==++=[Ag +] = 2C s ,K Sp (Ag 2S) = [Ag +]2 ⨯ [S 2-] = 4αC S 3,153850106,9104,94106,5S ---⨯=⨯⨯⨯= mol/L 或1.7⨯ 10—12g/L ;1.7⨯ 10—13g/100g 水(2分)4-4. HNO 3中的溶解性更好 (1分)3Ag 2S + 8HNO 3 = 6AgNO 3 + 2NO + 3S + 4H 2O (1分)(生成物写成H 2SO 4也对)第5题(9分)5-1 A :BF 3, B :(CH 3CH 2)2O ·BF 3 (2分 ,各1分)5-2 3H 2SO 4 + 2H 3BO 3 + 3CaF 2 === 2BF 3 + 3CaSO 4 + 6H 2O 2分5-3 2CH 3COOH CH 3COOH 2+ + CH 3COO -,加入(CH 3CH 2)2O ·BF 3后,(CH 3CH 2)2O ·BF 3是强路易斯酸,形成了CH 3COOBF 3-离子,促进了乙酸的自偶电离2CH 3COOH + BF 3 == CH 3COOBF 3- + CH 3COOH 2+ (2分)5-4 乙酸中存在单分子和缔合分子两种状态 (1分)5-5 水溶液中难溶或不溶的物质在非水电解质中可以研究,故扩大了研究的物质范围;在水溶液中,电解电位受到析氢电位和析氧电位的区间限制,而非水电解质中扩大了研究的电位区间限制。
英国化学奥林匹克竞赛UKChO近5年真题汇总

曲网左ψ}≡矣闫刃型璇UKChO⅛N 4>αJ血254ff 3sl 阳 rS a H S i ^≡H I(UKCHO砂邨Mnfl-ZEII le ⅜w]B B 楙E左聊回醐-。
a -R )⅛Im w>回JΣΠH g ≡l 圈#茁昔肆砌召3聲-H IKI 俳4H ⅜≡O 命W >酸嶷曲呻何-»觀迪羽血÷2戏3課叶7髒聖样母7l g >κg l汞糰芽闫器関UKChO≡54ff刘墜□四 那>+剤和就≥4ffs ≡報娜软測閒・血妙岂阳砂滋s ÷完弃—翦淆妙吸—T O CB一2・ThjSquestion ωa b o H detec-≡∙gm o φc u φs ΞSeptember 224∙ the BBC announced 59l r a d k >astronomers had discovered -he ・30ω→ ComP 一exmolecce ∙O da φ≡∙SPaC e ∙FOUnd in .Sagittahus- B2(N)∙—Ihe ωrg e sαstar-forming region 3OUr GalaXy IthiSis -he firsi molecule defected ∖M ≡abranched CarbonChaim The SyStematiC namefor-he molecuφis 2∙me3y1propane Mrile∙ -tWaSfoundiobeA nitrileis ω molecule in WhiChOne Of-heCarbonShas a=iple bond-Onitrogen,(a) (D=)DraW the StrUC c r e and g_ve 5esysαemabcnameOfanothernitrile .SomedcWHh2,me-<PΓOPanenMle .AS=OnomerS are nowIooking for the nextSerieSOfnit2esWith5eformuωCSHD N ・(b)DraWa 一二heISOmehC nitriles Wi 5the formuωCSH ⅛∙ MoSiOfthemo_ecu_es defectedby radk>-as≡τonomers 3∙IeSS ac-iveregions OfSPaCe φn d O have -5'e arstructures Theωrges -So farde-ectedhas ≡eUn-ike-y ∙look5∙gfornluωH p z∙(C)DraW -he S-HJCtUreOf ≡e-inear moφcu φWiih ≡e formula X o --z ∙The Signa-S de-ec-ed 55eradio WaVeregionOf 5e elec-romagneuc SPeCtrUm are due OKansibons between r θa t δ∙n a - energy-e v e ω・each OfWhiCh has ω PartiCU ωr energy, Mo-ecu-es have many roiauona- energy -eve-s avai_ab_e ~0 Ihem ・ each -eve-With a different energy beingSPeCmed by ≡e SO-Ca 一Ied65Γb o n ωquancm number ∙ J. WhiCh ωk e s ≡,一eger <ωE φω fromO UPWards ・Theenergy (3∙jou_es) Of≡e S rog o-na -energy-eveLEyisgivenbythefofmu-ω EJ關h ×BX J(JH)WhereBU ≡erotauonωConStasOf 一he3o-φ0⊂-φ (inHZ)h Mp-anck ∙sCOnSta H M 6.626×12∙Js ・ and一<≡∙3OffreqUenCyf(HZ)hasenergy hM f oou-es) TWO Signa ωhavebeendetected due一oZ o l z - O s e2016年考题2. ThlS question is about the ChOmiStry Of tungstenThe ChemIStry Of the transition metal tungsten has Cenain SimilaritieS to that Of the mai∩∙group element SUlfUr SinCe both atoms have a total Of SiX VaIenCeelectrons. BOth elements reach their maximum ÷6 OXidatiOnStateS when COmblned Wrth electronegative elementsfluorine and OXygeITWhilSt tungsten(VI) fluonde is USed in the Semi∞nductorindustry, the OXide is USed in electrochromic windows.TheSe Change ∞lour When an electrical VOltage is applied,as ShOWn in the airσaft WindOWS On the right.MoSt tungsten OCCUfS naturally in the tungstate anion,WO42", analogous to the sulfate. SO42". A COmmOn tungsten mineral is Scheelite, CaICiUm tungstate, CdWO4.(a)DraW a StrUctUre ShOWing the bonding in the WθΛ ion and give the O-W-O bond angle.Treatment Of SCheellte Wlth aqueous SOdiUm CarbOnate gives a SOlutKXI Of SOdiUm tungstate and a White insoluble salt. AdditiOn Of hydrochloric add to aqueous SOdiUm tungstate PrOdUCeS tungstic acid. WhiCh On heating gives Iungsten(VI) oxide. ThiS may be reduced Wrth hydrogen to give PUre UJngSten metal.(b)(i) GiVe the equation for the reaction between SCheeIite and aqueous SodiUmCart)Onate.(ii) GiVe the equation for the reactiOn Of aqueous SOdiUm tungstate Wrth hydrochloric acid and SUggeSt a StrUctUre for tungstic acid・(Iii) GiVe the equation for the formation Of tungsten(VI) OXKje from tungstic aαd.(iv) GiVe the equation for the (OrmatiOn tungsten metal.In electrochromic Windows. a VOltage is applied between a WanSParent Iayer Of Iungsten(VI) OXkje and a SOUrCe Of ions SUCh as a IrthIUm SaIt・and the following reacbo∩ takes PIaCe during wħich SOme Of the IrthiUm ions are in∞rporated into the StrUCtUre Of the oxide:WO3÷ xU* ÷ Xe- ---------- ► LiXWo3The PrOdUct t Li1WO3. is known as a tungsten bronze, and its ColoUr depends On the ValUe Of x. The VaIUe Of X Can Vary from O to 1: a typical ValUe giving a blue-black COlOUr is When X = 0.3.(C) (i) CaIcUlate the OXidatiOn State Of the tungsten When X= 1 ・(ii) CakXIIate the average OXidatiOn State Of the tungsten When X = 0.3.BOth elemental SUlfUr and tungsten react Wrth fluorir»e gas to form the hexafluorides. SFe and WF6are both gases at r∞m temperature and PreSSUre. Wrth WF6being the most dense gas known Underthese ∞nditio∩s. WF6is extremely toxic due to its rapid reaction With Water to form twoSUbStances. In COntrast, SF6is inert in Water and non-toxic・(d)By assuming air to be made UP Of nItrOgen gas OnM CaICUlate the densities Of SF e and WF6relative to air.(e)CaleUlate the actual density Of WFβ(g) in g cm"3 at 298 K and Standard PreSSUre.(f)SUggeSt an equation for the reaction Of WF e Wfth water.2017年考题ThiS question is about the Green POOl Of RiOWhen the Water in the diving PoOI at the RiO OlymPiC GameS turned green, it WaS SUggeSted that Ihe growth Of algae WaS to blame; this WaS StrOngM COnteSted by the organisers. EVen after Ihe OffiCial report WaS PUbliShed t there is StiIl much SPeCUIation as to theactual reason behind the ∞tour Change-One Of the most COmmOnfy USed ComPOUndS in thechlorination Of SWimming POoIS is SOdiUmhypochlorite・ NaCIO.(a)Determine the OXidatiOn State Of ChiOrine inSOdiUm hypochlorite, NaelO.OnCe dissolved, an equilibrium is established between CIO" and its COnjUgate acid.(b)GrVe an equation for this equilibrium.ThiS equilibrium is highly PH dependent and Un der acidic co nd tons ChIOrine is produced.(C) GiVe an equation for the generation Of cħlorine from hypochlorite and HCLThe Organisers eventually explained the green COlOUr in the POOI as being due to the growth Of algae after the i∩advertent addition Of a Iarge quantity Of hydrogen PerOXide. WhiCh destroyed thehypochk>rrte and formed ChlOride ions.(d)GiVe an equation for the reaction between hydrogen PeroXkJe and hypochlorite.KyPoChlOrrteS also have a tendency to react Wrth ammonia and ammonia-like ComPOUndS to form ∞mpou∩ds COntaining nitrogen and ChlOnne. One SUCh COmPOUnd is nitrogen trichloride. WhiCh Can CaUSe eyeirritation and Ihe distinctive SmeIl Of Swimmlng p∞ls(e)(i) GiVe an equation for the formation Of nitrogen trichloride.(ii) DraW a StrUCtUre for nitrogen trichloride, ShOWing its shape, and State the approximate CkN-Cl bond angle.DePending On reacting ratios, another POSSibIe OUtCOme Of Ihe reaction between ammonia and hypoChlorrte is the formation Of hydrazine. H2N-NH2. and ChlOride ions.(O GrVe an equation for this reaction.COPPer(II) SUtfate is SOmetimeS added to SWimming POOIS and this WaS also suggested as the CaUSe Of the green ∞lour. COPPer(II) ions Wefe also blamed for the green t int given to Ihe bleached hair Of the AmeriCan SWimmer Ryan LoChte・ The COPPer(Il) ions precipitate On the hair due to the high PH OfCertain sħamp∞s・(g)SUggeSt a formula for the blue PreCiPitate On Ryan LOChte,s h.2018年考题4. ThiS question is about COUgh SUPPreSSantSIn SePtember 2017. the UK Prime MiniSter l ThereSa May, had a bad ∞υgh during her SPeeCh at the ConSerVatiVe Party COnferenCe- The COUgh suppressant drugOextromethorphan, WhiCh is PreSent in ∞ugh remedies SUCh as BenyIin®. CoUld have helped her out. ThiS questiOn is about the SyntheSlS Of dextromethorphan. The SyntheSiS involves the formation Of SOme Str(Jng b∞ds and SOme StabIe CarbOCations.DeXtromethorphan is Onen administered as the hydrobromide monohydrate salt.(a) In the anSWer b∞k. Ci rCle the atom in dextromethorphan that is PrOtOnated in the salt. (b) Determine the molecular formula Of dextromethorphan and hence CaIaJlate Ihe molar mass Of thedextromethorphan hydrobromkie monohydrate salt. The SyntheSiS Of dextRxnethorphan takes a number Of StePS. PteaSe note that in the SChemeS describing the Synthesis, by-products Of the reactions are not always shown.The SyntheSiS Of dextromethorphan begins With the SyntheSiS Of COmPoUnd F.1 MgS∞h ICO 2 SOCh ------------------------ COmPOUnd A ■ COmPOUnd B 3 M ZMzOIR 3100 Cm t (v9rybΦM1716 Cm ' (3hΛφ)A COmPOUnd D c ∙ - W 2 HZH 2O♦ CoIOUrIeSS gas X π⅞o∕∙ mass of 44 01 g moi 1COnIPOUnd C♦COmPOUnd ECOmPOUnd FDraW the StUCtUreS Of COmPOUndS A. B. C. D. E and g‘COmPOUnd CCOmPOUnd EO δ2019年考题4・ ThiS question is about CarbOn dioxideThe food and drink industries USe a IOt OfCarbon dioxide DUring SUmmer 2018, a globalShOrtage Ied to SUPermarketS Iimiting frozenfood deliveries and ratbning beer. ThiS isironic COnSidering the do∞mented rise Ofatmospheric CO2 IeVeIs.(a) (i) DraW dot and CrOSS diagrams forCarbon dioxide and CartXXI monoxide.(Ii) CalaJlate the difference in the OXIdatiOn State between the CarbOnS in CarbOn dioxide and in CarbOn monoxide・The EngIiSh ChemiSt WiIliam Henry StUdied the equilibria When a gas dissolves in a IiqUid He PrOPOSed Ihat Ihe ConCentratiOn Of a gas dissolved in a IlqUld IS ProPOrt)Onal to the gas' PartiaI PreSSUre When in the gas phase. The PrOPOrti∞alrty fac tor is CaIIed the Henry l S IaW ∞nstant. The Henry S IaW ConStant for 82 is 3.3 × 1(Γ2 mol dm'3 atm"1.SeaIed COntainerS Of fizzy drinks COntain dissolved CQ. ThiS dissolved CO: is in equilibrium With a SmaIl quantity Of gase∞s CQ at the top Of the COn tain er.(b) (i) The Partial PreSSUre Of CO2gas in a 250 αn3 Can Of fizzy drink is 3.0 atm at25 0C. What is the COnCentratiOn Of CO2 in the fizzy drink?(H) What mass Of CO2 is ClISSOIVed in a 250 cm3 Can Of fizzy drink?(III)If the Can c∞ta∣ned Onty the mass Of C O? CaICUIated in Part (O) as a gas. CaIaJlate the PreSSUre in Ihe Can When it is StOred at 25 °C.(IV)Under What ∞nditio∩s WoUId CO2 gas be most SOlUble jn water?TiCk the COrreet OPtiOn in the anSWer b∞klet:•high PreSSUre and IOW temperature•high PreSSUre and high temperature•IoW PreSSUre and IOW temperature•IOW PreSSUre and high temperature2020年考题2. ThiS question is about hydrogen as a fuelCart)On dioxide emissions from fossil fuelsare a major factor in Climate change.Hydrogen is a Potenual alternative tofossil fuels. PrOViding ,dean energy* WrthOnly Water as a byproduct. The UK govemmentis in vestIgatlng COnVeftIng the naturalgas ghd to Carry hydrogen instead.FOr this question・ assume all PrOCeSSeStake PIaCe at 298 K.EnthaIPy Change Of formation Of CH4(g). ∆∕^f = -74.8 kJ moΓ'EnthaIPy Change Of formation Of CO?(g). Δ∕Λ = -393.5 kJ moΓ1EnthaIPy Change Of (Ofmation Of H2O(∣> ∆∕^f ≡ -285 8 kJ mol*1EntroPy Change Of formation Of H2O(I). ∆^e f = -163.0 J K*1moΓ1One IOW COSt method for PrOdUCing hydrogen is reforming methane. ThoUgh this PrOdUCeS CO2, this Can be easily captured. The reforming ProCeSS Can be represented by the OVeraH reaction:CH4(g) ÷ 2H2O(I) -→ CO2(g) + 4H2(g)(a) CalCUIate the enthalpy Change for this reaction.EleCtr OIySiS Of Water is another method Of producing hydrogen On a Iarge SCaIe .it OJrrently ∞sts more than reforming methane.In POIymer electrolyte membrane electrolysts, PfOlOnS are transferred thr∞gh a membrane between Ihe two electrodes. The two half reactions are:1.2H2O(l) → O2(g) + 4Hφ(aq) + 4eβ2.2H∙(aq) ÷ 2e" → H2(g)WhiCh Of these half reactions OCeUrS at the cathode?。
2024化学奥林匹克竞赛试题

2024 化学奥林匹克竞赛试题一、试题有一化学反应 A + B → C,在一定温度下,当A 的浓度为0.5mol/L,B 的浓度为1mol/L 时,反应速率为0.2mol/(L·s)。
若将 A 的浓度增大到1mol/L,B 的浓度不变,此时反应速率变为多少?解析根据反应速率方程v = k[A]^m[B]^n,设该反应中 A 的反应级数为m,B 的反应级数为n。
1. 首先求反应级数:-当 A 的浓度为0.5mol/L,B 的浓度为1mol/L 时,反应速率v1 = 0.2mol/(L·s),可得方程①:0.2 = k×0.5^m×1^n。
-当A 的浓度增大到1mol/L,B 的浓度不变时,设此时反应速率为v2,可得方程①:v2 = k×1^m×1^n。
-用方程①除以方程①可得:v2/0.2 = (k×1^m×1^n)/(k×0.5^m×1^n),化简得v2/0.2 = 2^m。
-由于只改变了A 的浓度,B 的浓度不变,且反应速率变为原来的倍数只与A 的浓度变化有关,所以可以通过设特殊值来确定m 的值。
-假设m = 1,则v2/0.2 = 2,解得v2 = 0.4mol/(L·s)。
-假设m = 2,则v2/0.2 = 4,解得v2 = 0.8mol/(L·s)。
-假设m = 3,则v2/0.2 = 8,解得v2 = 1.6mol/(L·s)等,依次类推,可通过给出的选项来确定m 的值,进而确定反应速率v2。
二、试题已知在25①时,水的离子积常数Kw = 1×10^(-14)。
在该温度下,某溶液的pH = 3,求该溶液中氢氧根离子的浓度。
解析1. 因为pH = -lg[H①],已知pH = 3,则[H①]=1×10^(-3)mol/L。
2. 又因为在任何水溶液中,Kw = [H①][OH①]。
第四届Chemy化学奥林匹克竞赛联赛试题参考答案

第四届Chemy化学奥林匹克竞赛联赛试题参考答案第四届Chemy化学奥林匹克竞赛联赛试题答案·竞赛时间3小时。
迟到超过半小时者不能进考场。
开始考试后1小时内不得离场。
时间到,把试卷(背面朝上)放在桌面上,立即起立撤离考场。
·试卷装订成册,不得拆散。
所有解答必须写在指定的方框内,不得用铅笔填写。
草稿纸在最后H、3He。
1215β+衰变。
2在反应MnO2+4HCl=MnCl2+Cl2+2H2O中,c(H+)=c(Cl-),气体分压为101325Pa,假定其他离子浓度均为1mol·L-1,实验员欲使反应自发进行,通过理论手段对于该反应能够进行的盐酸最低浓度进行了计算,并记录了如下求盐酸最低浓度的方法:对于该反应而言,能够自发进行,即使得ΔG<0,而ΔG=-RTlnK,即需使K>1反应即可自发进行。
列出平衡常数表达式K,由[H+]=[Cl-],解得[H+]<1mol·L-1,即求得盐酸最高浓度为1mol·L-1,也就是说,如果盐酸浓度高于1mol·L-1,根据实验员的求法,该反应无法自发进行。
3-1根据实验员的求法,我们发现与我们的认知不同。
我们知道,二氧化锰和浓盐酸反应需要在加热条件下进行,用1mol·L-1的盐酸和二氧化锰混合加热反应无法进行。
是我们的认知出现了偏差还摇匀,,生D加热到晶体X只含钠、镁、铅三种元素。
在不同的温度和压力下,晶体X呈现不同的晶相。
α-X是一种六方晶系的晶体,而γ-X是立方晶系的晶体。
在α-X中,镁和铅按1:1的比例形成类似于石墨的层状结构,钠填在层间。
在γ-X中,铅做立方最密堆积,其余两种原子填满所有的四面体空隙和八面体空隙。
6-4-2画出由铅形成的八面体空隙仅被钠占据时,γ-X的立方晶胞。
(每个第7题(11分)近期,研究人员于-30°C令硅?卡宾配合物A与CO2在THF中反应,成功制备了具有“二碳酸硅”结构的D。
化学竞赛试题(含答案)

化学竞赛试题2015.4一、物理化学部分单选题:1. 为测定物质在600~100℃间的高温热容, 首先要精确测量物系的温度。
此时测温元件宜选用:( D ) (2分)(A) 贝克曼温度计(B) 精密水银温度计(C) 铂-铑热电偶(D) 热敏电阻2. 电导率仪在用来测量电导率之前, 必须进行:( D) (2分)(A) 零点校正(B) 满刻度校正(C) 定电导池常数(D) 以上三种都需要3. 实验室常用的气体钢瓶颜色分别是:( B) (2分)(A) N2瓶蓝色, H2瓶黑色, O2瓶绿色(B) N2瓶黑色, H2瓶绿色, O2瓶蓝色(C) N2瓶绿色, H2瓶黑色, O2瓶蓝色(D) N2瓶黑色, H2瓶蓝色, O2瓶绿色4. 用最大气泡压力法测定溶液表面张力的实验中, 对实验实际操作的如下规定中哪一条是不正确的? (D ) (2分)(A) 毛细管壁必须严格清洗保证干净(B) 毛细管口必须平整(C) 毛细管应垂直放置并刚好与液面相切(D) 毛细管垂直插入液体内部, 每次浸入深度尽量保持不变5. 实验室内因用电不符合规定引起导线及电器着火,此时应迅速:(D )(2分)(A) 首先切断电源,并用任意一种灭火器灭火(B) 切断电源后,用泡沫灭火器灭火(C) 切断电源后,用水灭火(D) 切断电源后,用CO2灭火器灭火6. 用热电偶温度计测温时,热电偶的冷端要求放置在:(C )(2分)(A) 0℃(B) 一般室温范围(C) 只要温度恒定的任一方便的温度即可(D) 任意温度都可7. 设大气压力计制造时,在汞柱的上方尚残存少量空气, 则该大气压力计的读数:(B ) (2分)(A) 偏高(B) 偏低(C) 无偏差(D) 晴天偏高,雨天偏低8. 饱和标准电池在20℃时电动势为:( A) (1分)(A) 1.01845 V (B) 1.01800 V(C) 1.01832 V (D) 1.01865 V二、分析化学部分(15分)(一)单项选择(每题1分,共5分)1. 测定FeCl3中Cl 含量时,选用(C )指示剂指示终点。
五大竞赛考试题目及答案

五大竞赛考试题目及答案一、选择题(每题2分,共10分)1. 以下哪项是计算机编程中常用的数据结构?A. 线性表B. 树形结构C. 链式存储D. 所有选项都是答案:D2. 化学中,元素周期表的第118号元素是什么?A. 氧B. 氢C. 氦D. 奥格尼森答案:D3. 在物理学中,光速在真空中的速度是多少?A. 299,792,458米/秒B. 299,792,458千米/秒C. 299,792,458厘米/秒D. 299,792,458光年/秒答案:B4. 数学中,圆的面积公式是什么?A. A = πr²B. A = 2πrC. A = πrD. A = 4πr²答案:A5. 生物学中,DNA的双螺旋结构是由哪位科学家发现的?A. 达尔文B. 孟德尔C. 沃森和克里克D. 爱因斯坦答案:C二、填空题(每题3分,共15分)1. 在计算机科学中,二进制数1011转换为十进制数是______。
答案:112. 化学中,水的化学式是______。
答案:H2O3. 物理学中,牛顿第二定律的公式是______。
答案:F=ma4. 数学中,勾股定理的公式是______。
答案:a² + b² = c²5. 生物学中,细胞的有丝分裂过程中,染色体的数量在后期会______。
答案:加倍三、简答题(每题5分,共20分)1. 请简述计算机操作系统的主要功能。
答案:计算机操作系统的主要功能包括管理计算机硬件资源,提供用户界面,控制程序执行,以及处理数据存储等。
2. 描述化学中的酸碱中和反应。
答案:酸碱中和反应是指酸和碱在一定条件下反应生成盐和水的过程,反应中酸的氢离子和碱的氢氧根离子结合生成水分子。
3. 简述物理学中的相对论。
答案:相对论是爱因斯坦提出的物理理论,包括狭义相对论和广义相对论。
狭义相对论主要描述在没有重力作用下的物体运动规律,广义相对论则描述了在重力作用下的物体运动规律。
全国大学生化学实验竞赛第五届笔试Word版

第五届全国大学生化学实验邀请赛笔试试卷选手编号:总成绩:题型一、选择题二、填空题总分得分评卷人可能用到的原子量数据:元素H C N O Na S Cl Cu Fe Zn 原子量1121416233235.563.55665.4一、选择题(选择题为单项选择,每题1分,共70分),请将答案填入答题卡中1、某同学在玻璃加工实验过程中,不小心被灼热的玻璃棒烫伤,正确的处理方法是()。
A、用大量水冲洗即可B、直接在烫伤处涂上烫伤膏或万花油C、直接在烫伤处涂上碘酒D、先用水冲洗,再在烫伤处涂上烫伤膏或万花油2、实验过程中,不慎有酸液溅入眼内,正确的处理方法是()。
A、用大量水冲洗即可B、直接用3%~5% NaHCO3溶液冲洗C、先用大量水冲洗,再用3%~5% NaHCO3溶液冲洗即可D、先用大量水冲洗,再用3%~5% NaHCO3溶液冲洗,然后立即去医院治疗3、被碱灼伤时的处理方法是 ( )。
A、用大量水冲洗后,用1%硼酸溶液冲洗B、用大量水冲洗后,用酒精擦洗C、用大量水冲洗后,用1%碳酸氢钠溶液冲洗D、涂上红花油,然后擦烫伤膏4、停止减压蒸馏时,正确的操作顺序是 ( )。
A、通大气、关泵后停止加热B、边通大气、边关泵后停止加热C、边通大气、边关泵、边停止加热D、停止加热后再通大气、最后关泵5、在玻璃真空系统中安置稳压瓶的作用是()。
A、加大系统的真空度B、降低系统的真空度C、减小系统真空度的波动范围D、便于实验操作6、实验室内因用电不符合规定引起导线及电器着火,此时应迅速()。
(共12页)1A、首先切断电源,并用任意一种灭火器灭火B、切断电源后,用泡沫灭火器灭火C、切断电源后,用水灭火D、切断电源后,用CO2灭火器灭火7、有关气体钢瓶的正确使用和操作,以下哪种说法不正确?()。
A、不可把气瓶内气体用光,以防重新充气时发生危险B、各种压力表可通用C、可燃性气瓶(如H2、C2H2)应与氧气瓶分开存放D、检查减压阀是否关紧,方法是逆时针旋转调压手柄至螺杆松动为止8、氧化剂要与()之类的化学品分隔开来存放。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第五届Chemy化学奥林匹克竞赛联赛试题
·竞赛时间3小时。
迟到超过半小时者不能进考场。
开始考试后1小时内不得离场。
时间到,把试卷(背面朝上)放在桌面上,立即起立撤离考场。
·试卷装订成册,不得拆散。
所有解答必须写在指定的方框内,不得用铅笔填写。
草稿纸在最后一页。
不得持有任何其他纸张。
·姓名、报名号和所属学校必须写在首页左侧指定位置,写在其他地方者按废卷论处。
第1题(13分)
1-1氢化锂铝是有机反应常用的还原剂,过量的氢化锂铝常使用叔丁醇淬灭,写出淬灭过程的反应方程式。
1-2工业上常以黄铜矿为原料制备胆矾。
方法为将黄铜矿在一定条件下氧化焙烧,后用水浸取即可得到胆矾。
写出该法制备胆矾的反应方程式。
1-3锂金属的液氨溶液与乙炔反应无气体生成,产物均为二元化合物,写出反应的化学方程式。
1-4在农场中,常在潮湿的仓库中放置几片磷化铝片剂用于杀灭害虫。
该过程应用了什么化学原理?试用化学术语表达之。
1-5实验室常用氯酸钾在二氧化锰催化的条件下分解制备少量氧气。
然而在没有催化剂时,氯酸钾加热至熔化也不会放出气体。
试写出没有催化剂的条件下氯酸钾加热分解的化学方程式。
1-6核化学是军工业的重要组成部分。
研究发现锕-227是一种不稳定的同位素,其会自发衰变生成钫-223,写出衰变反应方程式。
第2题(11分)
配合物可看作正负电荷相互作用而形成的一种酸碱加合物。
配合物中的配体按配位原子的个
数可分为单齿配体与多齿配体两类。
2-1试画出下列按端基配位形成配合物的结构:
Fe(SCN)63-Ni(CN)42-Mn2(CO)10
2-2多齿配体有的可以作为螯合配体,有的可作为桥联配体。
试画出下列各化合物的结构:
Al(EDTA)-H3F4-Fe2(CO)9
2-3一些特殊的配体与一些特殊的金属可形成一些超分子化合物。
现有一种由Pt(II)、邻二氮菲以及配体X所组成的超分子化合物,已知该配合物中C与Pt的质量分数分别为49.40%、33.43%,且在该配合物中,所有组成部分均为其常见配位形式。
已知分子中存在S4轴(分子沿轴旋转90°做镜面操作与原分子重合),试画出该超分子化合物的骨架。
第3题(13分)
根据中学所学的知识,铁制品在空气(p(O2) = 20 kPa)中放置得到铁锈,而铁丝在装满氧气(p(O2) = 100 kPa)的广口瓶中燃烧,火星四溅并得到黑色固体。
已知铁、四氧化三铁和三氧化二铁的熔点分别为1538 ℃、1597 ℃和1565 ℃。
假设上述物质的焓和熵不随温度变化,此题仅从热力学角度考虑。
3-1请通过计算确定铁锈的主要成分。
3-2-1铁丝在纯氧中燃烧时的反应温度至少为______℃。
3-2-2在该温度下通过计算确定黑色固体的主要成分。
3-3计算测定三氧化二铁的熔点时需要的氧气分压(kPa)。
有关物质的热力学数据:
第4题(10分)
已知X是一种一元强酸,常温下为无色透明的液体。
工业上可通过如下过程制备X:电解一定浓度的NaClO3溶液,得到一种单质气体和一种盐Y,然后Y经酸化可得X。
实验测定结果表明,X中键角∠O-Cl-O有两种大小,分别为105.8°和112.8°,而X的酸根离子中,键角∠O-Cl-O只有一种。
X与过量P4O10反应,得到两种产物,其中一种含两个六元环。
4-1写出X的化学式。
4-2在X的两种∠O-Cl-O键角中,哪一种键角为112.8°?简述原因。
4-3 分别写出电解NaClO3溶液时,阴阳两极的电极反应方程式。
4-4分别画出两分子X与一分子P4O10反应得到的两种产物的结构。
4-5 硫酸的酸性弱于X,但实验室中仍可采取用X的钾盐与浓硫酸反应的方法制备X,简述原因。
4-6人们已经制得X的水合晶体X·H2O。
按键型分类,X·H2O属于哪种晶体?
第5题(11分)
某化合物X仅含A和B两种元素。
在高压下,X形成了一种原子晶体。
此晶体为正交晶系,其中A均为四配位,B均为二配位,a = 622 pm,b = 435 pm,c = 607 pm,ρ = 3.56 g·cm-3,Z = 8。
5-1 试通过计算确定X的化学式。
5-2 画出X在200 K,500 kPa下形成的晶体的正当晶胞,此时该晶体为立方晶系,Z = 4,只画出A原子即可。
判断该晶体的点阵类型?
5-3 在高压下,X还能形成一种四方晶系的分子晶体,晶胞参数a = 354 pm,c = 413 pm,Z = 2。
在一个正当晶胞中,若以A原子为顶点,则两个B的坐标分别为(0.266,0.266,0)和(0.766,0.234,0.5)。
5-3-1 画出一个正当晶胞沿c方向的投影图,用黑球表示A原子,白球表示B原子,用短线表示键联关系。
5-3-2判断以下说法的正误:
(1)此晶体中有对称中心。
(2)此晶体中有不通过任何原子的镜面。
(3)此晶体中有穿过B原子的二重旋转轴。
(4)此晶体中没有不穿过A原子的二重旋转轴。
第6题(8分)
实验室用酸碱滴定法测定酯化反应的平衡常数:
(1)准确量取0.200 mol的乙醇和0.200 mol乙酸混合,用移液枪加入200 μL浓硫酸,将混合液在电加热磁力搅拌器上加热搅拌回流1.5小时。
(2)量取0.200 mol乙酸溶于与乙醇等体积的水中,从中取出1.00 mL,加水稀释至20 mL。
以酚酞为指示剂,用浓度为c (mol·L-1)的NaOH标准溶液滴定,消耗NaOH标准溶液的体积为V1 (mL)。
(3)量取与乙酸和乙醇等体积的水,向其中用移液枪加入200 μL浓硫酸,从中取出1.00 mL,加水稀释至20 mL。
以酚酞为指示剂,用相同浓度的NaOH标准溶液滴定,消耗NaOH标准溶液的体积为V0 (mL)。
(4)回流1.5小时结束后,将反应液充分冷却至室温,从中取出1.00 mL反应液,加水稀释至20 mL后以酚酞为指示剂,用相同浓度的NaOH标准溶液滴定,消耗NaOH标准溶液的体积为V2 (mL)。
(5)将剩余的反应液继续回流半小时后,充分冷却至室温,从中再取出1.00 mL反应液,加水稀释至20 mL后以酚酞为指示剂,用相同浓度的NaOH标准溶液滴定,记录滴定体积。
6-1写出乙醇和乙酸发生酯化反应得到乙酸乙酯的平衡常数K的表达式。
6-2用题中所给字母表达平衡常数K。
6-3(5)的目的是什么?
第7题(9分)
7-1画出上述反应A和B的结构简式,注意立体化学并标出B中手性碳的构型。
7-2试画出上述反应C和D的结构简式,注意立体化学并标出D中环上手性碳的构型。
7-3实验发现,在一特殊的溶剂中,可分离得到化合物甲基乙基氨基锂的两种异构体。
其中锂离子为三配位,试画出在此种溶剂中两种异构体的结构简式,溶剂分子以S表示。
第8题(14分)
二甲基亚砜(DMSO)是实验室常用的反应溶剂和反应试剂。
二甲亚砜的性质与其分子结构密切相关。
8-1 画出二甲亚砜的共振结构式。
8-2-1 二甲亚砜属于()。
①质子溶剂②偶极溶剂③极性溶剂④非极性溶剂
8-2-2在二甲亚砜中,_____(选填“正”、“负”)离子更容易被溶剂化。
8-3 二甲亚砜在有机合成中常作为氧化剂使用,例如著名的Swern氧化反应:
实验时首先将二甲亚砜和草酰氯加入底物醇中,低温下发生反应,生成大量气体,得到中间体A。
然后再加入三乙胺,经中间体B后得到产物醛。
8-3-1试画出中间体A和B的结构,并指出中间体B属于哪一类有机化合物?
8-3-2写出Swern氧化反应配平的化学方程式。
8-4 人们发现,二甲亚砜除能够氧化醇生成醛酮外,还可以氧化苯胺等含有富电子苯环的化合物。
如下图所示氧化反应,二甲亚砜氧化苯胺生成单一产物X:
8-4-1 写出产物X的结构简式。
8-4-2 画出生成X的反应机理。
并指出在该反应中,哪种元素被氧化?
第9题(11分)
在一个相互联系的系统中,一个很小的初始能量就可能产生一系列的连锁反应,人们把这种现象称为“多米诺骨牌效应”或“多米诺效应”。
在有机合成中,随着人们对反应效率和原子利用率的注重以及科学家们更希望合成复杂天然产物的愿望,这就要求用最简便的步骤实现最大的复杂性。
一种有效提高合成效率的方式是将多个反应条件相似的反应结合起来一次性完成,将上一个反应得到的官能团用于下一个反应,从而简化反应步骤,有机化学上将这类反应称之为“多米诺反应”。
以下三个反应都可看作“多米诺反应”:
9-1 画出以上反应的产物X、Y和Z的结构简式,已知Z的结构中存在金刚烷骨架(不要求立体化学)。
9-2人们欲通过下列反应制备吡啶衍生物A,然而却得到了4H-吡喃衍生物B(C18H18O2N2)。
B在PhNCO和碘单质的作用下成功转化为A。
反应步骤如下图所示:
9-2-1给出B的结构简式。
9-2-2指出B转化为A的过程中,碘单质的作用。
