无菌检查记录表
无菌检查记录

无菌检查记录一、任务背景无菌检查是医疗领域中非常重要的环节,用于确保手术和医疗器械操作的无菌状态。
本文将详细介绍无菌检查的记录要求和标准格式。
二、记录要求1. 检查时间:记录无菌检查的具体日期和时间。
2. 检查人员:记录进行无菌检查的人员姓名或者工号。
3. 检查位置:记录无菌检查的具体位置,如手术室、器械准备室等。
4. 检查项目:记录进行无菌检查的具体项目,如手术器械、手术台面、手术包装等。
5. 检查结果:记录无菌检查的结果,包括合格或者不合格。
6. 异常情况:如果检查结果为不合格,需要详细描述异常情况,如污染、破损等。
7. 处理措施:针对不合格的情况,记录采取的处理措施,如更换器械、重新清洁等。
8. 备注:可根据需要记录其他相关信息。
三、标准格式无菌检查记录日期:20XX年XX月XX日时间:XX:XX检查人员:XXX(工号:XXX)检查位置:XXX检查项目:1. 手术器械:- 序号器械名称结果- 1 手术刀合格- 2 针线盒合格- 3 钳子合格- ...2. 手术台面:- 序号区域名称结果- 1 左侧合格- 2 右侧合格- 3 中央合格- ...3. 手术包装:- 序号包装名称结果- 1 包装A 合格- 2 包装B 不合格(污染) - 3 包装C 合格- ...检查结果:合格异常情况:无处理措施:无备注:无四、示例无菌检查记录日期:2022年05月10日时间:10:30检查人员:张三(工号:12345)检查位置:手术室检查项目:1. 手术器械:- 序号器械名称结果- 1 手术刀合格- 2 针线盒合格- 3 钳子合格2. 手术台面:- 序号区域名称结果- 1 左侧合格- 2 右侧合格- 3 中央合格3. 手术包装:- 序号包装名称结果- 1 包装A 合格- 2 包装B 不合格(污染)- 3 包装C 合格检查结果:不合格异常情况:手术包装B存在明显污染。
处理措施:即将更换手术包装B,并进行重新清洁消毒。
无菌技术操作检查记录表

1项不符扣1分
打开无菌包,手不触内面;取用物品未完,立即按原折痕包好无菌包,并注明开包日期、时间并签名,24h内有效
7
1项不符扣1分
铺无菌盘方法正确,注明铺盘日期、时间,4h内有效
5
1项不符扣1分
戴无菌手套
剪短指甲,洗手,核对手套号码、有效期
5
1项不符扣1分Biblioteka 戴无菌手套方法正确,符合无菌技术原则
5
1项不符扣1分
打开无菌包、取持物钳(镊)及容器方法正确,持物钳(镊)与容器配套
5
1项不符扣1分
干燥保存使用,记录打开时间,4小时内有效;每个容器放一把持物钳(镊)
5
1项不符扣1分
取放、使用持物钳(镊)方法正确,疑污染重新更换
5
1项不符扣1分
取用无菌溶液
按需准备无菌溶液,瓶身清洁无积灰。核对品名、有效期,检查瓶盖、瓶体、溶液,有无异常
无菌技术操作检查记录表
市县(市、区)(填写机构名称)
项 目
操 作 要 求
分值
扣分标准
扣分及
理 由
用物
准备齐全、放置合理
5
1项不符扣0.5分
操作步骤
操作前准备
自身准备、环境准备符合规范
5
1项不符扣1分
无菌持物钳
(镊)使用
检查无菌持物钳(镊)包:品名、有效期,有无破损、潮湿、消毒指示带是否变色
5
1项不符扣1分
5
1项不符扣1分
开启瓶盖,消毒无菌溶液瓶口,打开瓶塞,瓶塞内面不污染
5
1项不符扣1分
倒无菌溶液方法正确,如溶液需再用,塞好瓶塞、用碘伏消毒后盖好,注明开瓶日期、时间并签名,24h内有效
无菌检查记录

无菌检查记录引言概述:无菌检查是医疗领域中非常重要的一项工作,它用于确保手术器械和医疗设备的无菌状态,以防止感染的发生。
本文将介绍无菌检查记录的重要性以及其内容和格式。
正文将分为五个部分,分别是检查记录的目的、记录的内容、记录的格式、记录的示例以及记录的保存和归档。
一、检查记录的目的:1.1 确保无菌状态: 无菌检查记录的主要目的是确保手术器械和医疗设备的无菌状态。
通过检查记录,可以追踪每个器械和设备的无菌处理过程,以确保它们在使用前是无菌的。
1.2 防止感染传播: 无菌检查记录的另一个目的是防止感染的传播。
如果手术器械或设备未经过正确的无菌处理,可能会引发感染,并且可能对患者的健康造成严重威胁。
通过记录无菌检查结果,可以及时发现问题并采取措施,以防止感染的发生。
1.3 提供质量控制依据: 无菌检查记录还提供了质量控制的依据。
通过分析记录,可以评估无菌处理过程的有效性,及时发现并纠正潜在的问题,从而提高无菌处理的质量。
二、记录的内容:2.1 检查日期和时间: 无菌检查记录应包括检查的日期和时间。
这些信息对于追溯和跟踪无菌处理过程非常重要。
2.2 检查人员信息: 记录中应包括进行无菌检查的人员的姓名和职务。
这有助于追责和责任分配。
2.3 检查结果: 记录中应详细描述每个手术器械或设备的检查结果。
这包括是否通过无菌检查以及检查结果的详细说明。
三、记录的格式:3.1 表格形式: 无菌检查记录通常以表格形式呈现。
表格应包括检查日期、检查人员、器械或设备名称、检查结果等列,以便清晰地记录和查看。
3.2 规范化的标准: 无菌检查记录应根据相关的规范和标准进行填写。
这有助于确保记录的准确性和一致性。
3.3 详细描述: 记录中应提供详细的描述,包括检查过程中使用的方法和工具,以及检查结果的具体细节。
这有助于其他人员了解检查的过程和结果。
四、记录的示例:4.1 器械无菌检查记录示例:日期: 2022年1月1日检查人员: 张医生器械名称: 手术剪刀检查结果: 通过无菌检查,无菌包装完好,无异常。
无菌检查记录表

无菌检查记录
供试品名称:规格:
批号:送检数量:
检验日期:完成日期:
检验依据:《中国药典》2015版第四部通则1101“无菌检查法”
培养基硫乙醇酸盐流体培养基
胰酪大豆胨液体培养基
配制批号:
配制批号:
稀释液、缓冲液□pH7.0氯化钠-蛋白胨缓冲
液
□0.9%无菌氯化钠溶液
配制批号:
阳性菌
阳性菌液取阳性菌新鲜培养物培养后所得的菌体,用稀释液制成每1ml含菌(或孢子)数小于100cfu的菌悬液作为对照菌液。
第代培养物计数结果:cfu/ml
检查方法□薄膜过滤法□直接接种法
培养结果
培养温度30℃~35℃20℃~25℃
鉴别菌需氧菌、厌氧菌真菌、需氧菌
组别样品阳性阴性暨培养基无菌检查样品样
品
阳性阴性暨培养基无菌检查
编号
培养天数
A1 B1 1 2 3 4 5 A2 A3 B2 6 7 8 9 10 1
2
3
4
5
6
7 8 9
10
11
12
13
14
检查标准供试样品管均澄清,或虽显浑浊但经确认为无菌;阳性管菌液应生长良好;
阴性暨培养基无菌检查管应无菌生长。
检查结论
检验人/日期:复核人/日期:。
商业无菌检验原始记录表2013

外观检查
马口铁容器,无泄漏或锈蚀、压痕、膨胀 马口铁容器,无泄漏或锈蚀、压痕、膨胀
保温前称重(g) 356.3
367.9
保温观察现象 无泄漏或膨胀
无泄漏或膨胀
保温后称重(g) 355.7
365.7
组织 紧密略有弹性,略粘
紧密略有弹性,略粘
形态 方块状
开
罐
色泽 不均匀的粉红色
检 查
气味 芳香,无不良异味
5 个视野
与对照样品相比, 无 明显的微生物增殖现象。数量比: 6 / 6
结封性检查见附页
校核者:
某某检验机构
商业无菌检验原始记录表
(受控文件号)************
样品流转号
食检 14-0374
样品名称
共 页第 页 午餐肉罐头
生产批号 检验地点 检验依据
培养基 检验日期
20131209
洁净实验室 508-2
GB 4789.26-2013 商业无菌检验 结晶紫染色液 20131226 无菌蒸馏水 20140313
14 年 3 月 13 日~ 3 月 23 日
仪器和设备
SC6010 电子天平 恒温培养箱 冰箱 □超净工作台 PHS-3C 酸度计 Olympus 显微镜
编号 W036 编号 W007 编号 W041 编号 W016 编号 W002 编号 W022
检验步骤
保温样品 36℃±1℃,10 d
对照样品 2℃~5℃,10 d
内壁 无锈斑
方块状 不均匀的粉红色 芳香,无不良异味 无锈斑
鉴别
无 腐败变质的迹象
pH 测定两次 等量蒸馏水混匀
7.41 7.43
平均值:7.42
7.45 7.45
无菌检查方法验证
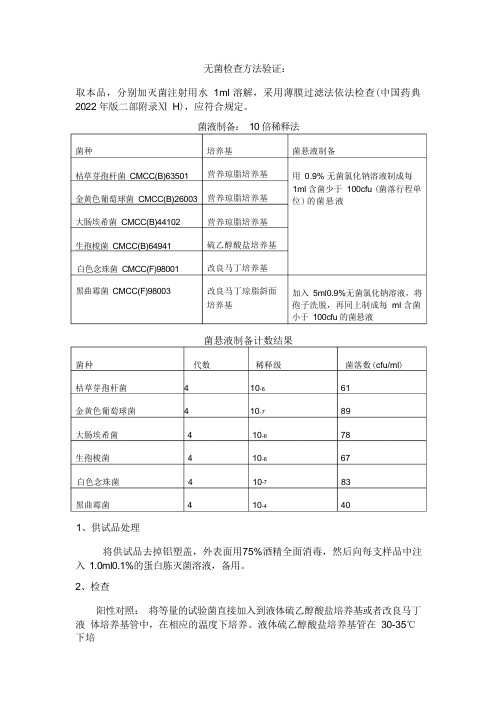
无菌检查方法验证:取本品,分别加灭菌注射用水 1ml 溶解,采用薄膜过滤法依法检查(中国药典 2022 年版二部附录Ⅺ H ),应符合规定。
菌液制备: 10 倍稀释法培养基 营养琼脂培养基营养琼脂培养基营养琼脂培养基硫乙醇酸盐培养基改良马丁培养基改良马丁琼脂斜面 培养基菌悬液制备计数结果菌种 代数 稀释级 菌落数(cfu/ml )枯草芽孢杆菌 4 10-6 61金黄色葡萄球菌 4 10-7 89大肠埃希菌 4 10-6 78生孢梭菌 4 10-6 67白色念珠菌 4 10-7 83黑曲霉菌 4 10-4 401、供试品处理将供试品去掉铝塑盖,外表面用75%酒精全面消毒,然后向每支样品中注 入 1.0ml0.1%的蛋白胨灭菌溶液,备用。
2、检查阳性对照: 将等量的试验菌直接加入到液体硫乙醇酸盐培养基或者改良马丁液 体培养基管中,在相应的温度下培养。
液体硫乙醇酸盐培养基管在 30-35℃下培菌种枯草芽孢杆菌 CMCC(B)63501 金黄色葡萄球菌 CMCC(B)26003 大肠埃希菌 CMCC(B)44102生孢梭菌 CMCC(B)64941白色念珠菌 CMCC(F)98001黑曲霉菌 CMCC(F)98003菌悬液制备用 0.9% 无菌氯化钠溶液制成每 1ml 含菌少于 100cfu (菌落行程单 位)的菌悬液加入 5ml0.9%无菌氯化钠溶液,将 孢子洗脱,再同上制成每 ml 含菌 小于 100cfu 的菌悬液养;改良马丁液体培养基管在23-28℃下培养3-5 天。
观察记录。
阴性对照:将灭菌的液体硫乙醇酸盐培养基或者改良马丁液体培养基管直接放在相应的温度下培养。
液体硫乙醇酸盐培养基管在30-35℃下培养;改良马丁液体培养基管在23-28℃下培养3-5 天。
观察记录。
样品 (薄膜过滤法):每种实验菌取10 支处理好的供试品溶液,将溶液合并后加入制备好的菌悬液1ml,用0.1%的蛋白胨灭菌溶液稀释至100ml,按薄膜过滤法过滤,取出滤膜,将其分为3 等份,分别置于含硫乙醇酸盐流体培养基及改良马丁培养基的容器中,其中一份作为阳性对照用。
微生物检验记录表
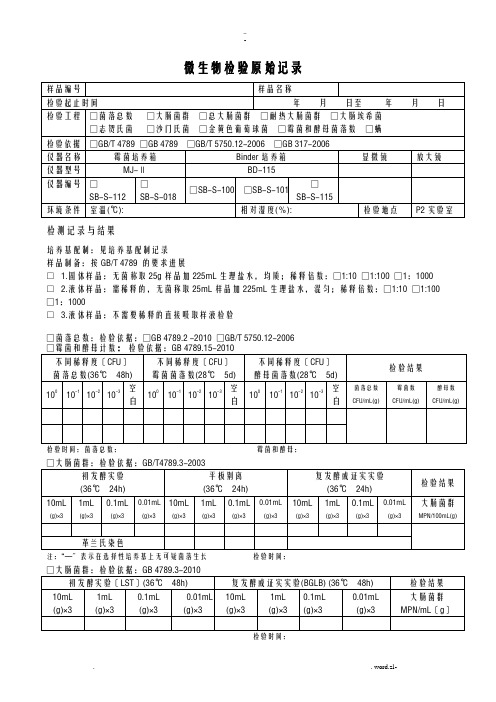
微生物检验原始记录
检测记录与结果
培养基配制:见培养基配制记录
样品制备:按GB/T 4789 的要求进展
□ 1.固体样品:无菌称取25g样品加225mL生理盐水,均质;稀释倍数:□1:10 □1:100 □1:1000 □ 2.液体样品:需稀释的,无菌称取25mL样品加225mL生理盐水,混匀;稀释倍数:□1:10 □1:100 □1:1000
□ 3.液体样品:不需要稀释的直接吸取样液检验
□菌落总数:检验依据:□GB 4789.2 -2010 □GB/T 5750.12-2006
检验时间:菌落总数:霉菌和酵母:
注:“—〞表示在选择性培养基上无可疑菌落生长检验时间:
检验时间:
□总大肠菌群:检验依据:GB/T 5750.12-2006
注:“—〞表示在选择性培养基上无可疑菌落生长检验时间:□耐热大肠菌群:检验依据:GB/T 5750.12-2006
注:“—〞表示在选择性培养基上无可疑菌落生长检验时间:□大肠埃希氏菌:检验依据:GB/T 5750.12-2006
□致病菌□沙门氏菌□志贺氏菌□金黄色葡萄球菌
检验依据GB 317.4-.10-2006
检测人:复核人:微生物限度检验记录〔复合膜〕
检验人:复核人:微生物限度检验记录〔辅料〕
检验人:复核人:
微生物限度检验记录〔铝箔、PVC硬片〕
微生物限度检验记录〔半成品、成品〕
微生物限度检验记录〔辅料〕。
无菌检查方法验证表和检查记录表

无菌方法验证品名:规格:批号:检查时间:1.培养基:硫乙醇酸盐流体培养基,批号:由:提供;营养肉汤,批号:由:提供;改良马丁培养基批号:由:提供。
2.验证试验用菌种:(1) 金黄色葡萄球菌(Staphylococcus aureus)[CMCC(B) 26003];(2) 枯草芽孢杆菌(Bacillus subtilis)[CMCC(B) 63501];(3) 大肠埃希菌(Escherichia coli)[CMCC(B) 44102];(4) 铜绿假单胞菌(Pseudomonas aeruginosa) [CMCC(B) 10104](5) 生孢梭菌(Clostridium sporogenes)[CMCC(B) 64941];(6) 白色念珠菌(Candida albicans)[CMCC(F) 98001];(7) 黑曲霉菌(Aspergillus niger) [CMCC(F)98003]。
3. 仪器和滤器:HTY-2000A集菌仪,STV3封闭式/开放式无菌检查薄膜过滤器,浙江宁海白石药检仪器厂。
4.方法:中国药典2005版二部附录。
5.操作方法:5.1 菌液制备:取金黄色葡萄球菌、枯草芽孢杆菌、大肠埃希菌、铜绿假单胞菌的新鲜培养物少许接种至营养肉汤培养基中, 生孢梭菌的新鲜培养物少许接种至硫乙醇酸盐流体培养基中, ℃培养小时。
取大肠埃希菌、金黄色葡萄球菌、枯草芽孢杆菌、铜绿假单孢菌、生孢梭菌肉汤培养物,加生理盐水,10倍递增稀释至约10-5~10-8之间,其中金黄色葡萄球菌取稀释级,铜绿假单孢菌取稀释级,大肠埃希菌取稀释级,枯草芽孢杆菌取稀释级,生孢梭菌取稀释级。
白色念珠菌的新鲜培养物接种至改良马丁培养基中, ℃培养小时。
再取白色念珠菌真菌斜面培养物,加入生理盐水洗下孢子,吸出转移至空试管作为原液,取加生理盐水,10倍递增稀释至,取加生理盐水,混匀备用。
将黑曲霉菌斜面的新鲜培养物接种至改良马丁培养基上,℃培养,使大量的孢子成熟。
无菌检查记录(薄膜过滤法)

品名:生产单位:批号:亚批号:规格:剂型:1.检验依据:《中华人民共和国药典》2015年版三部□本企业注册标准□其它:□2.检验方法:薄膜过滤法3.操作规程:SOP-04-13-4501《无菌检查SOP》4.判定标准:4.1 试验成立条件:阳性对照应生长良好,阴性对照不得有菌生长。
否则,试验无效。
4.2 供试品应澄清,或虽显浑浊但经确证无菌生长,判供试品符合规定;若供试品中任何一管显浑浊并确证有菌生长,判供试品不符合规定。
5.检验操作5.1供试品无菌检查5.1.1 材料及设施仪器5.1.1.1培养基及稀释液5.1.1.2设施品名:批号:5.1.1.3仪器5.1.1.4耗材5.1.2实验步骤5.1.2.1试验前环境检查5.1.2.1.1洁净室试验条件:温度18℃~26℃,湿度45%~65%,压差≥10Pa 是□否□5.1.2.1.2操作间工作台面是否有与本次操作无关的物品是□否□确认人:确认日期:5.1.2.2操作步骤品名:批号:5.1.2.3试验后清场5.1.2.4环境监测结果5.1.2.5 培养及观察:“-”表示无菌生长,“+”表示有菌生长无菌检查记录(薄膜过滤法)品名:批号:5.1.2.6结果:品名:批号:5.2阳性菌试验5.2.1 材料及设施仪器5.2.1.1 菌株5.2.1.2设施5.2.1.3 仪器5.2.2实验步骤5.2.2.1试验前环境检查5.2.2.1.1洁净室试验条件:温度18℃~26℃,湿度45%~65%,压差≥10Pa是□否□5.2.2.1.2 操作间内工作台面是否清除与本次操作无关的物品是□否□确认人:确认日期:品名:批号:5.2.2.2 操作步骤操作间:微生物限度区阳性菌室操作间编号:27145.2.2.3试验后清场品名:批号:5.2.2.4培养及观察:“-”表示无菌生长,“+”表示阳性菌生长。
5.2.2.5 结果:6.结论:结果符合规定□结果不符合规定□检验人:检验日期:复核人:复核日期:。
微生物检验记录簿表格
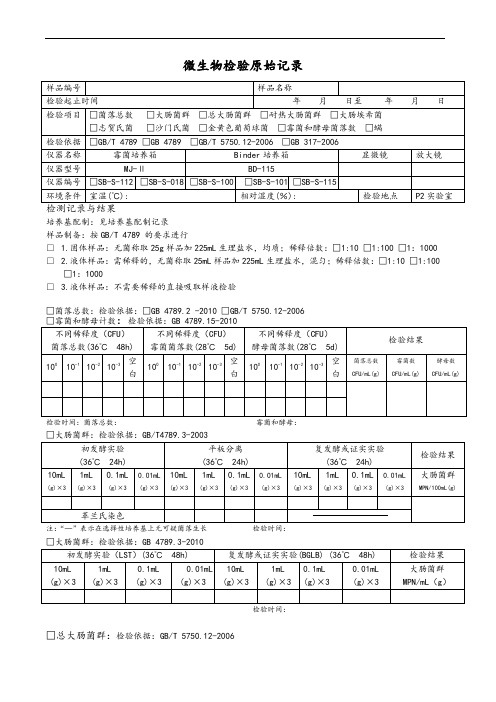
微生物检验原始记录
培养基配制:见培养基配制记录
样品制备:按GB/T 4789 的要求进行
□ 1.固体样品:无菌称取25g样品加225mL生理盐水,均质;稀释倍数:□1:10 □1:100 □1:1000 □ 2.液体样品:需稀释的,无菌称取25mL样品加225mL生理盐水,混匀;稀释倍数:□1:10 □1:100 □1:1000
□ 3.液体样品:不需要稀释的直接吸取样液检验
□菌落总数:检验依据:□GB 4789.2 -2010 □GB/T 5750.12-2006
检验时间:菌落总数:霉菌和酵母:
□大肠菌群:检验依据:GB/T4789.3-2003
注:“—”表示在选择性培养基上无可疑菌落生长检验时间:
检验时间:
□总大肠菌群:检验依据:GB/T 5750.12-2006
注:“—”表示在选择性培养基上无可疑菌落生长检验时间:
注:“—”表示在选择性培养基上无可疑菌落生长检验时间:
检验时间
□致病菌□沙门氏菌□志贺氏菌□金黄色葡萄球菌
□螨:检验依据 GB 317.4-.10-2006
检测人:复核人:
微生物限度检验记录(复合膜)
检验人:复核人:
微生物限度检验记录(辅料)
检验人:复核人:
微生物限度检验记录(铝箔、PVC硬片)
检验人:复核人:
微生物限度检验记录(半成品、成品)
检验人:复核人:
微生物限度检验记录(辅料)
检验人:复核人:。
无菌室的无菌程度检查方法及登记
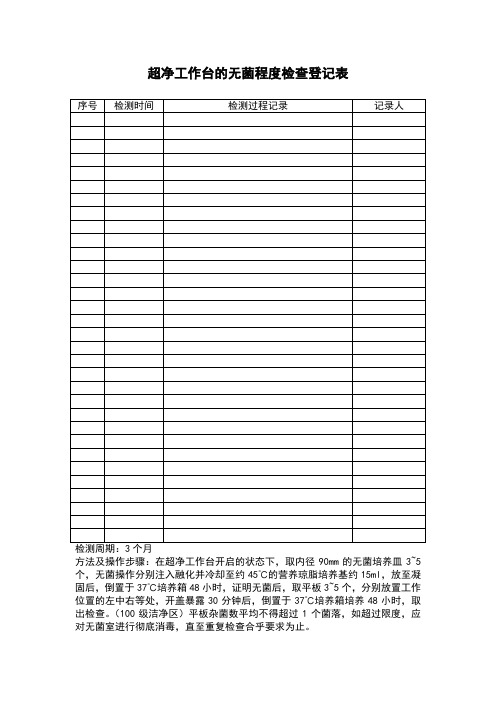
Байду номын сангаас序号
检测时间
检测过程记录
记录人
检测周期:3个月
方法及操作步骤:在超净工作台开启的状态下,取内径90mm的无菌培养皿3~5个,无菌操作分别注入融化并冷却至约45℃的营养琼脂培养基约15ml,放至凝固后,倒置于37℃培养箱48小时,证明无菌后,取平板3~5个,分别放置工作位置的左中右等处,开盖暴露30分钟后,倒置于37℃培养箱培养48小时,取出检查。(100级洁净区)平板杂菌数平均不得超过1个菌落,如超过限度,应对无菌室进行彻底消毒,直至重复检查合乎要求为止。
无菌检查记录

无菌检查记录
标题:无菌检查记录
引言概述:
无菌检查记录是医疗机构中非常重要的一项工作,它是确保手术室、医疗器械、药品等都符合无菌要求的重要手段。
无菌检查记录可以匡助医疗机构及时发现问题,保障患者手术安全,提高医疗质量。
一、手术室无菌检查记录的重要性
1.1 确保手术室环境无菌
1.2 预防手术感染
1.3 保障患者手术安全
二、医疗器械无菌检查记录的作用
2.1 确保医疗器械无菌
2.2 预防交叉感染
2.3 提高医疗质量
三、药品无菌检查记录的必要性
3.1 防止药品污染
3.2 保障用药安全
3.3 提高治疗效果
四、无菌检查记录的内容和方式
4.1 记录无菌检查的时间、地点、人员等信息
4.2 记录无菌检查的结果和结论
4.3 建立完善的无菌检查记录档案
五、如何做好无菌检查记录工作
5.1 建立规范的无菌检查流程
5.2 培训医护人员无菌检查知识和技能
5.3 定期检查和评估无菌检查记录的质量
结语:
无菌检查记录是医疗机构保障医疗质量、提高患者安全的重要手段,惟独做好无菌检查记录工作,才干确保医疗过程中的无菌要求得到有效执行,降低医疗事故的发生率,提升医疗服务水平。
无菌检查记录

无菌检查记录标题:无菌检查记录引言概述:无菌检查记录是医疗机构和实验室中非常重要的一项工作,通过记录无菌检查结果,可以确保医疗器械和实验室设备的无菌状态,保障患者和实验人员的安全。
本文将详细介绍无菌检查记录的重要性以及记录的内容和格式。
一、无菌检查记录的重要性1.1 确保患者和实验人员的安全:无菌检查记录可以及时发现医疗器械和实验室设备的无菌状态,避免无菌状态不达标而导致交叉感染的风险。
1.2 提高医疗质量:无菌检查记录可以监控医疗机构和实验室设备的无菌状态,及时发现问题并进行处理,提高医疗质量和安全水平。
1.3 合规管理:无菌检查记录是医疗机构和实验室的管理要求之一,记录无菌检查结果可以保证医疗机构和实验室的合规管理。
二、无菌检查记录的内容2.1 检查日期和时间:记录无菌检查的具体日期和时间,确保检查结果的准确性和时效性。
2.2 检查项目:详细记录检查的医疗器械或实验室设备的名称和编号,确保每个项目都有相应的检查记录。
2.3 检查结果:准确记录每个项目的检查结果,包括是否符合无菌标准以及存在的问题和处理情况。
三、无菌检查记录的格式3.1 表格记录:通常使用表格形式记录无菌检查结果,包括检查日期、时间、项目、结果等信息,便于查阅和整理。
3.2 电子记录:现代医疗机构和实验室多采用电子记录方式,可以方便快捷地记录和查询无菌检查结果。
3.3 签名确认:每份无菌检查记录都需要相关人员的签名确认,确保记录的真实性和可靠性。
四、无菌检查记录的保存和归档4.1 保存期限:无菌检查记录需要保存一定的时间,以备日后查阅和复核。
4.2 归档管理:无菌检查记录需要按照规定的管理要求进行归档,确保记录的完整性和安全性。
4.3 定期清理:定期清理无用的无菌检查记录,避免占用过多的存储空间和资源。
五、无菌检查记录的审查和改进5.1 定期审查:医疗机构和实验室需要定期审查无菌检查记录,发现存在的问题并进行改进。
5.2 持续改进:不断完善和改进无菌检查记录的内容和格式,提高记录的准确性和实用性。
无菌检查记录

无菌检查记录一、任务背景无菌检查是医疗机构中非常重要的一项工作,用于确保手术器械和手术环境的无菌状态,以减少手术感染的风险。
本文旨在记录无菌检查的过程和结果,并提供相应的标准格式。
二、无菌检查记录格式无菌检查记录应包含以下内容:1. 日期和时间:记录无菌检查的具体日期和时间,以便追溯和核对。
2. 检查人员:记录进行无菌检查的人员姓名或工号,以确保责任明确。
3. 检查项目:列出需要进行无菌检查的项目,如手术器械、手术室环境等。
4. 检查方法:描述无菌检查所采用的方法和步骤,确保检查的准确性和一致性。
5. 检查结果:记录每个项目的检查结果,包括合格或不合格。
对于不合格的项目,应记录具体的问题描述。
6. 处理措施:对于不合格的项目,记录相应的处理措施,如重新清洗、更换器械等。
7. 处理结果:记录处理后的结果,包括重新检查的结果和最终是否合格。
8. 备注:可在此处记录其他相关信息,如异常情况、特殊处理等。
三、示例日期和时间:2022年1月10日 09:30-10:00检查人员:李医生检查项目:1. 手术器械:手术刀、镊子、钳子、针线等2. 手术室环境:手术台、墙壁、地面、空气质量等检查方法:1. 手术器械:使用目视检查和放大镜检查手术器械表面是否有污物、破损或锈蚀等问题。
2. 手术室环境:使用洁净度检测仪器测量手术室空气中的微生物数量,并使用洁净度指标评估手术室环境的无菌程度。
检查结果:1. 手术器械:- 手术刀:合格- 镊子:合格- 钳子:不合格,表面有少量污物,需重新清洗- 针线:合格2. 手术室环境:- 手术台:合格- 墙壁:合格- 地面:合格- 空气质量:不合格,微生物数量超标,需进行空气净化处理处理措施:1. 钳子:将不合格的钳子送至器械科进行重新清洗和消毒。
2. 空气质量:立即启动空气净化设备,对手术室进行空气净化处理。
处理结果:1. 钳子:经过重新清洗和消毒后,再次进行无菌检查,结果合格。
无菌检查记录

无菌检查记录一、任务描述根据要求,编写一份无菌检查记录的标准格式文本。
二、无菌检查记录表日期:2022年10月15日检查人员:张三检查地点:XX医院手术室序号项目名称结果备注1 消毒操作合格无异常2 空气质量合格 PM2.5浓度符合标准3 器械包装合格无破损、湿润等异常4 器械包装合格无破损、湿润等异常5 操作人员合格穿戴无菌手套和口罩6 操作环境合格温度、湿度符合要求7 操作时间合格手术开始前完成无菌检查8 检查结果合格无菌指标符合要求备注:本次无菌检查记录表共检查8项,检查结果全部合格。
三、解析和说明1. 消毒操作:检查消毒操作是否符合要求,包括消毒剂的使用方法、浓度和时间等。
2. 空气质量:检查手术室空气中PM2.5浓度是否符合标准,确保手术环境无污染。
3. 器械包装:检查手术器械包装是否完好无损,无湿润、破损等异常情况。
4. 操作人员:检查手术人员是否穿戴无菌手套和口罩,确保操作人员不会引入细菌。
5. 操作环境:检查手术室的温度和湿度是否符合要求,保证手术环境适宜。
6. 操作时间:检查无菌检查是否在手术开始前完成,确保手术过程中的无菌状态。
7. 检查结果:综合以上各项检查结果,判断整体的无菌指标是否符合要求。
四、参考数据1. 消毒操作:消毒剂浓度为1:100,消毒时间为30分钟。
2. 空气质量:PM2.5浓度应低于35μg/m³。
3. 器械包装:器械包装应完好无损,无湿润、破损等异常情况。
4. 操作人员:手术人员应穿戴无菌手套和口罩。
5. 操作环境:手术室温度应控制在20-25摄氏度,湿度应控制在40%-60%。
六、总结本次无菌检查记录表详细记录了无菌检查的各项指标,包括消毒操作、空气质量、器械包装、操作人员、操作环境、操作时间等。
通过对以上指标的检查,确认手术室的无菌状态符合要求。
无菌检查记录的编写和记录对于手术室的无菌操作和术后感染的预防具有重要意义,保证了手术的安全性和患者的健康。
无菌检查记录

无菌检查记录一、任务背景无菌检查是医疗机构中非常重要的环节之一,用于确保手术室、实验室和其他无菌操作区域的无菌状态。
本文将详细介绍无菌检查记录的标准格式。
二、无菌检查记录标准格式无菌检查记录应包括以下几个部分:1. 日期和时间:记录无菌检查的具体日期和时间,以确保检查的准确性和时效性。
2. 检查人员信息:记录进行无菌检查的人员姓名、职称和执业证书号码等信息,以便追溯和确认检查人员的身份和资质。
3. 检查区域信息:记录无菌检查的具体区域,如手术室、实验室或其他无菌操作区域的名称和编号。
4. 检查项目:列出无菌检查的具体项目,如无菌器械、手术台面、工作台面、无菌包装材料等。
5. 检查结果:对每个检查项目进行记录,包括检查结果和评价。
检查结果可以分为合格和不合格两种情况,评价可以根据具体情况选择适当的描述词语,如“良好”、“一般”、“不合格”等。
6. 备注:在需要补充说明或解释的情况下,可以在备注栏中填写相关信息,如具体的不合格原因、处理措施等。
7. 签字:无菌检查记录应由检查人员本人签字确认,并可以附上其他相关人员的签字,如监督人员或负责人的签字。
三、示例日期和时间:2022年1月1日 08:00-09:00检查人员信息:检查人员姓名:张三职称:无菌检查员执业证书号码:XXXXXX检查区域信息:区域名称:手术室A区域编号:A001检查项目:1. 无菌器械2. 手术台面3. 工作台面4. 无菌包装材料检查结果:1. 无菌器械:合格2. 手术台面:良好3. 工作台面:一般4. 无菌包装材料:不合格备注:无菌包装材料未正确密封,需要更换。
签字:检查人员:张三监督人员:李四四、总结无菌检查记录是医疗机构中确保无菌操作区域无菌状态的重要手段。
标准格式的无菌检查记录应包括日期和时间、检查人员信息、检查区域信息、检查项目、检查结果、备注和签字等内容。
通过详细记录无菌检查的过程和结果,可以确保无菌操作的质量和安全性,为医疗工作提供可靠的保障。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
德信诚培训网
更多免费资料下载请进:
好好学习社区
无菌检查记录
供试品名称: 规 格: 批 号: 送检数量: 检验日期:
完成日期:
检验依据: 《中国药典》2015版第四部通则1101“无菌检查法”
培养基
硫乙醇酸盐流体培养基 胰酪大豆胨液体培养基 配制批号: 配制批号:
稀释液、缓冲液 □pH7.0氯化钠-蛋白胨缓冲
液
□0.9%无菌氯化钠溶液
配制批号:
阳性菌
阳性菌液 取阳性菌新鲜培养物培养后所得的菌体,用稀释液制成每1ml 含菌(或
孢子)数小于100cfu 的菌悬液作为对照菌液。
第 代培养物
计数结果: cfu/ml 检查方法 □ 薄膜过滤法
□ 直接接种法
培养结果
培养温度 30℃~35℃ 20℃~25℃ 鉴别菌 需氧菌、厌氧菌
真菌、需氧菌 组别 样品
阳性 阴性暨培养基无菌检查 样品
样品
阳性 阴性暨培养基无菌检查
编号 培养天数
A1 B1 1 2 3 4 5 A2 A3 B2 6 7 8 9 10 1 2 3 4 5 6。
