2021药品不良反应报告年度总结
2021年药品不良反应总结分析反馈
2021年药品不良反应总结分析反馈2021年全院药品不良反应上报情况
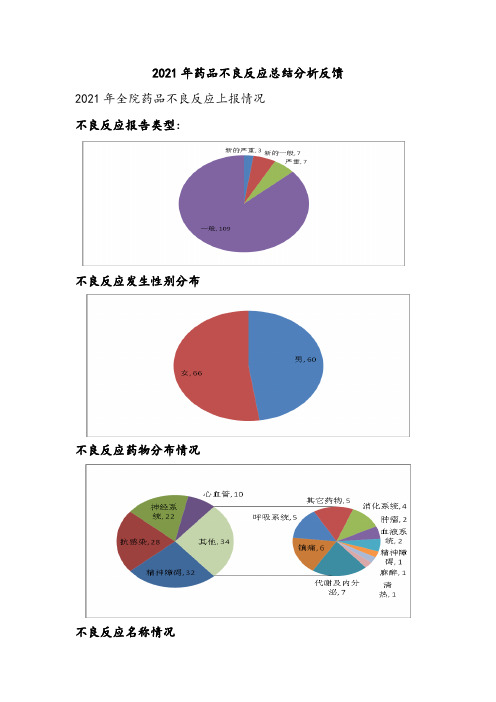
不良反应报告类型:
不良反应发生性别分布
不良反应药物分布情况
不良反应名称情况
总体情况
全年共上报126例,包括新的严重3例,严重7例,新的一般7例,一般109例。
不良反应发生性别分布:男性60例,女性66例。
药物分布情况:精神障碍33例,抗感染28例,神经系统22例,心血管10例,代谢及内分泌7例,镇痛6例,呼吸系统5例,其它药物5例,消化系统4例,肿瘤2例,血液系统2例,麻醉药1例,中成药清热剂1例。
严重和新的分布情况
新的严重的3例:碘海醇注射液引起的药物过敏;注射用奥美拉唑钠吡拉西坦注射液引起的输液反应(寒战、气紧、胸闷、皮肤紫绀);盐酸利多卡因注射液引起的头昏、乏力、心悸。
严重的7例:注射用头孢噻肟钠引起的药物热;注射用胞磷胆碱钠引起的胸闷、呼吸困难;唑来膦酸注射液引起的发热;注射用头孢噻肟钠引起的迟发性过敏;丙戊酸钠缓释片引起的嗜睡状,呼之不应,全身无力,伴局部震颤;注射液头孢哌酮钠舒巴坦钠引起的发热;盐酸曲唑酮片引起的低血压。
新的一般的7例:注射用哌拉西林钠舒巴坦钠引起的白细胞减少,血小板减少;注射用盐酸川芎嗪引起的头痛;利培酮胶囊引起的白细胞减少;注射用七叶皂苷钠引起的输液侧手臂肿胀;奥氮平片引起的尿酸升高;连花清瘟颗粒引起的胃肠道不适;氯氮
平片引起的尿酸升高。
临床药师将年度药品不良反应情况通报给各临床科室,要求各科室引起重视,尽量避免出现严重不良反应,临床药师将在随后工作中进行跟踪。
药学部
2022年1月。
药品不良反应个人年终总结

药品不良反应个人年终总结各位领导、同事们:在即将迎来新年之际,我谨向各位汇报本年度的工作情况和业绩。
本年度,我在药品不良反应的监测和分析工作中承担了重要的责任,同时也面临了一些挑战。
在此,我将总结过去一年的工作,并对未来的工作提出一些建议和展望。
一、工作回顾本年度,我全力致力于药品不良反应的监测和分析工作。
我按照规定的流程,准确记录和上报了不良反应的相关信息,并且及时进行了分析和总结。
通过与各个部门的紧密合作,我成功提高了信息的收集效率和准确性。
在工作中,我积极探索新的监测方法和技术工具,以提高药品不良反应监测的效率和准确性。
通过引入自动化系统和大数据分析工具,我成功提高了信息的处理速度和准确性,并且有效地减少了人为错误的发生。
二、工作亮点本年度,我在药品不良反应的监测和分析工作中取得了一些亮点和成绩,并为公司的发展做出了积极贡献。
首先,我建立了一个完善的药品不良反应数据库,并对其中的数据进行了深入的分析。
通过对数据的挖掘和对比,发现了一些药品的潜在安全隐患,并及时向公司管理层提出了风险警示。
其次,我积极参与了公司内部和外部举办的培训和学术交流活动。
通过与同行的交流和学习,我不断提升了自己的业务水平和专业知识,并将所学的新技术和方法应用到实际工作中,取得了显著的效果。
三、问题和挑战在药品不良反应的监测和分析工作中,我也面临了一些问题和挑战,这些问题需要得到合理的解决和改进。
首先,由于药品不良反应的信息较为敏感,存在一定的保密性要求,因此我需要更加严格地管理和保护相关数据,以防止信息泄露和滥用的风险。
其次,目前药品不良反应的监测和分析仍然依赖于人工的判断和处理,存在着一定的主观性和局限性。
因此,我需要不断提高自己的专业水平和分析能力,使得信息的处理更加客观和准确。
四、未来展望针对问题和挑战,我提出了以下几点建议和展望,以便更好地推进药品不良反应的监测和分析工作。
首先,加强与不同部门的合作,推动信息的共享和汇总。
国家药品不良反应监测年度报告-注射剂不良反应监测情况
国家药品不良反应监测年度报告(2021年)4.4 注射剂不良反应监测情况2021年注射剂(不含疫苗)不良反应/事件总体报告数量与2020年同期相比增长14.7%,在药品总体报告中占比与近年来总体情况基本一致。
按照剂型统计,2021年药品总体不良反应/事件报告中注射剂(不含疫苗)占55.5%,严重报告中注射剂(不含疫苗)占70.9%。
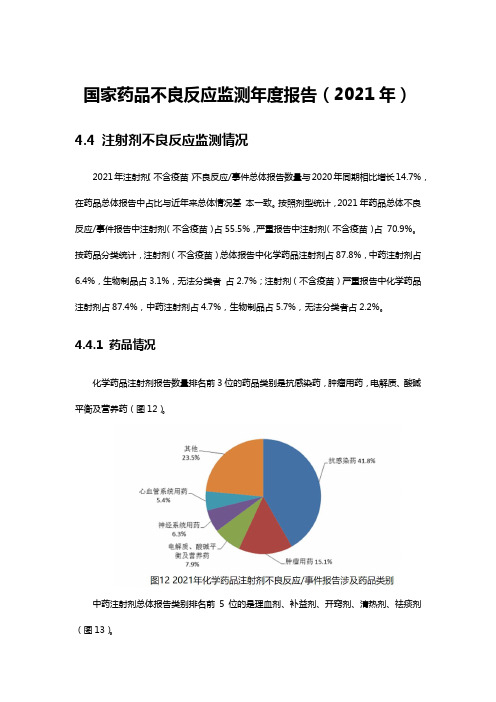
按药品分类统计,注射剂(不含疫苗)总体报告中化学药品注射剂占87.8%,中药注射剂占6.4%,生物制品占3.1%,无法分类者占2.7%;注射剂(不含疫苗)严重报告中化学药品注射剂占87.4%,中药注射剂占4.7%,生物制品占5.7%,无法分类者占2.2%。
4.4.1 药品情况化学药品注射剂报告数量排名前3位的药品类别是抗感染药,肿瘤用药,电解质、酸碱平衡及营养药(图12)。
中药注射剂总体报告类别排名前5位的是理血剂、补益剂、开窍剂、清热剂、祛痰剂(图13)。
4.4.2 累及器官系统情况2021年注射剂总体不良反应/事件报告中,累及器官系统排名前5位的是皮肤及皮下组织类疾病、胃肠系统疾病、全身性疾病及给药部位各种反应、各类神经系统疾病和各类检查。
注射剂严重不良反应/事件中,累及器官系统排名前5位的是血液及淋巴系统疾病、各类检查、皮肤及皮下组织类疾病、全身性疾病及给药部位各种反应和胃肠系统疾病(图14)。
4.4.3 监测情况分析及安全风险提示从剂型统计情况看,2021年注射剂(不含疫苗)不良反应/事件总体报告数量与2020年同期相比增长14.7%,在药品总体报告中占比与近年来总体情况基本一致。
从用药人群统计情况看,儿童的注射剂(不含疫苗)不良反应/事件报告数量与2020年同期相比增长19.7%,总体占比与近年来总体情况基本一致。
根据注射剂监测情况,建议临床医生用药前仔细阅读产品说明书,重点关注相关安全性内容,处方前进行充分的获益与风险分析,始终遵照“能吃药不打针,能打针不输液”的用药原则合理选择用药。
药物不良反应监测与报告工作总结

药物不良反应监测与报告工作总结《篇一》在过去的一年里,我从事药物不良反应监测与报告工作,这是一个极具挑战性,同时也充满成就感的工作。
通过这项工作,我更深入地理解了药物的不良反应对患者的影响,以及如何有效地管理和报告这些不良反应,保障患者的安全。
一、基本情况我主要的工作职责是监测药物不良反应,及时向相关部门报告,并跟踪处理情况。
在这个过程中,我需要与医生、护士、药剂师等不同职能的同事进行沟通和合作,以确保药物不良反应能得到及时有效的处理。
二、工作重点我的工作重点是及时发现和报告药物不良反应,以及分析不良反应的原因,提出改进措施。
在这个过程中,我需要对药物的不良反应有一定的了解和认识,同时也要了解医院的工作流程和制度,以便更好地进行监测和报告。
三、取得的成绩和做法在过去的一年里,我成功监测和报告了数十例药物不良反应,有效地保障了患者的安全。
我取得这些成绩的主要做法是,及时与医生、护士、药剂师等同事进行沟通,了解药物的使用情况和不良反应的发生情况,同时也要不断学习和提升自己的专业知识和技能。
四、经验教训和处理办法在工作中,我也遇到了一些困难和挑战。
例如,有时候对于一些不常见的药物不良反应,我可能不够了解,导致无法及时识别和报告。
在面对这些挑战时,我积极地寻求同事的帮助和指导,同时也不断学习和提升自己的专业知识和技能。
五、对今后的打算展望未来,我将继续致力于药物不良反应的监测和报告工作,不断提升自己的专业知识和技能,以更好地服务于患者。
同时,我也希望能与同事一起,共同推动药物不良反应监测和报告工作的发展,为患者的安全保驾护航。
六、回顾工作,总结反思回顾过去的一年,我深感药物不良反应监测和报告工作的重要性和必要性。
这项工作不仅要求我有扎实的专业知识和技能,还需要我有良好的沟通和合作能力。
我相信,通过不断的学习和提升,我能够更好地完成这项工作,为患者的安全贡献自己的力量。
《篇二》从事药物不良反应监测与报告工作以来,我深刻认识到这项工作的重要性和必要性。
药品不良反应监测工作总结_慢病监测工作总结

药品不良反应监测工作总结_慢病监测工作总结在过去的一年里,我负责药品不良反应监测工作,一直以来我都积极履行职责,努力推动工作的顺利进行。
通过对过去一年的工作的总结和反思,我认为有以下几点值得提及:我注重信息收集和分析。
我每天认真浏览相关药品不良反应的报告,并进行分类整理。
对于每个报告,我会仔细阅读,并进行分析研究。
通过这样的工作方式,我能够更好地了解不同药品的不良反应情况,并加深对不良反应的认识。
我积极与相关部门进行合作和沟通。
药品不良反应监测工作需要与医院、药店等各个环节进行有效沟通。
在过去的一年里,我经常与相关部门进行交流,分享药品不良反应的信息,并与他们一起制定相应的应对策略。
这种合作和沟通能够不断提高我们的工作效率,并更好地服务于患者。
我还积极参加相关培训和学习,以提高自己的专业素养和技能。
我参加了多个药品不良反应监测方面的培训和学习活动,并认真学习相关的专业知识。
通过这样的学习,我能够更好地理解药品不良反应的监测和防范工作,并能够更好地应对不同的挑战。
我还注重及时报告和交流工作的成果。
在工作的过程中,我时刻保持与上级的沟通,并及时向上级领导汇报工作进展和问题。
我也与同事们进行交流和讨论,分享我们的工作心得和经验。
这种及时的报告和交流,能够更好地推动整个工作的进展。
过去一年里,我在药品不良反应监测工作中发挥了积极的作用,努力推动工作的进展。
通过信息收集和分析、与相关部门的合作和沟通、参加培训和学习以及及时报告和交流等工作方式,我能够更好地了解药品不良反应情况,并采取相应的措施进行防范和处理。
在未来的工作中,我将继续努力,不断提高自己的专业素养和技能,为药品不良反应监测工作的顺利进行做出更大的贡献。
慢病监测工作总结在信息收集和分析方面,我注重了解慢病的相关数据和研究。
我每天浏览和分析慢病相关的文献和报告,了解慢病的发病率、流行趋势以及治疗方法等方面的信息。
通过这样的工作方式,我能够更好地了解慢病的特点和趋势,并为制定相应的防控措施提供科学依据。
药品不良反应工作总结范文

药品不良反应工作总结范文英文回答:Adverse drug reactions (ADRs) are an important aspectof pharmacovigilance and play a crucial role in ensuringthe safety and efficacy of medications. As a pharmacovigilance officer, I have been responsible for monitoring and reporting ADRs, as well as implementing measures to minimize their occurrence. In this work summary, I will discuss the challenges faced, strategies employed, and outcomes achieved in relation to ADR reporting and management.One of the main challenges in ADR reporting is the underreporting of ADRs by healthcare professionals. Thiscan be attributed to various factors, such as lack of awareness, time constraints, and fear of legal consequences. To address this issue, I have conducted educationalsessions and workshops for healthcare professionals, highlighting the importance of ADR reporting and theprocedures involved. Additionally, I have implemented auser-friendly online reporting system, making it easier for healthcare professionals to report ADRs. These efforts have resulted in an increase in ADR reporting rates, leading toa better understanding of the safety profiles of medications.Another challenge in ADR management is theidentification and causality assessment of ADRs. Sometimes, it can be difficult to determine whether an observedadverse event is truly caused by a medication or is coincidental. To overcome this challenge, I have utilized various tools and resources, such as the Naranjo algorithm and the World Health Organization (WHO) causality assessment criteria. These tools help in systematically evaluating the likelihood of a medication causing anadverse event. By employing these tools, I have been ableto accurately identify and assess ADRs, enablingappropriate actions to be taken to ensure patient safety.In addition to reporting and management, proactive measures to minimize ADRs have also been a focus of my work.This includes conducting regular medication safety audits, reviewing prescribing patterns, and implementing risk minimization strategies. For example, if a particular medication is found to have a high incidence of ADRs, I collaborate with healthcare professionals to develop strategies to minimize the risks associated with its use. This may involve updating prescribing guidelines, providing additional training to healthcare professionals, or implementing stricter monitoring protocols. By taking these proactive measures, I have successfully reduced the occurrence of ADRs and improved patient outcomes.Overall, my work in ADR reporting and management has been instrumental in ensuring the safety and efficacy of medications. Through educational initiatives, improved reporting systems, and proactive risk minimization strategies, I have been able to overcome challenges, accurately identify and assess ADRs, and take appropriate actions to mitigate their occurrence. By continuously monitoring and addressing ADRs, we can contribute to the overall improvement of patient care and medication safety.中文回答:药品不良反应(ADR)是药物监测的重要方面,对于确保药物的安全性和疗效起着至关重要的作用。
医院药品不良反应监测与上报工作年度总结

类型和特点
过敏反应:常见于皮肤、呼吸道、消化 道等部位,表现为红肿、瘙痒、呼吸困 难等
毒性反应:长期使用可能导致肝肾功能 损害、神经系统损伤等
药物相互作用:不同药物之间可能产生 相互作用,影响药效或增加不良反应风 险
剂量依赖性反应:药物剂量过大可能导 致不良反应发生率增加
遗传因素:某些药物的不良反应可能与 遗传因素有关,如某些药物对特定人群 的毒性较大
对提升医疗机构服务水平的贡献
提高医疗服务质量:及时发现并处理药品不良反应,保障患者安全
提升患者构管理:通过监测与上报工作,加强医疗机构的药品管理,提高管理水平
促进医疗行业健康发展:通过监测与上报工作,促进医疗行业对药品不良反应的关注和研究, 推动医疗行业的健康发展
不良反应报告的撰写和上报
报告内容:包括药品名称、不良反应类型、患者信息等 报告格式:按照规定的格式进行撰写,确保信息完整、准确 报告提交:通过医院内部系统或国家药品不良反应监测中心进行上报 报告处理:对上报的不良反应报告进行审核、分析,及时采取措施,保障患者安全
监测与上报工作的成效和亮点
监测覆盖率提高:覆盖更多药品和患者群体 报告质量提升:报告内容更全面、准确,便于分析 及时上报率提高:及时发现并上报不良反应,提高处理效率 培训效果显著:提高医护人员对药品不良反应的认识和上报意识
《药品不 良反应监 测与上报 工作指南》
《药品不 良反应监 测与上报 工作流程》
《药品不 良反应监 测与上报 工作考核 标准》
《药品不 良反应监 测与上报 工作奖惩 制度》
工作目标与任务
确保药品安全,保障患者健康 及时发现药品不良反应,及时采取措施 提高药品质量,促进药品研发 加强药品监管,维护市场秩序
2021年全年药品不良反应总结

2021年药品不良反应工作总结2021年1--11月全院各临床科室上报药品不良反应共计121例,上报10例严重药品不良反应,上报1例新的严重药品不良反应,上报34例新的药品不良反应,上报76例一般的药品不良反应,新的严重药品不良反应占报告总数的0.83%,严重药品不良反应占报告总数的8.26%。
所报药品不良反应中,其中男性61例,女性59例,不良反应人群中最大年龄93岁,最小年龄4岁。
精神科上报34例,老年科上报35例,综合科上报51例。
出现药品不良反应的药物有心血管类药物、抗精神类药物、抗菌类药物、止血类药物、免疫增强剂类药物、治疗结核类药物、激素类药物等,涉及72个不同品种。
我院为做好药品不良反应监测工作作出了积极努力,现总结如下:(一)高度重视、制度完备为更好推进药物不良反应监测工作的开展,医院成立“药物不良反应监测领导小组”,分管药学副院长任组长,“小组”办公室设在临床药事科,办公室主任由临床药事科科长兼任。
设药物不良反应专职人员医务科、药学部各1名,建立、完善了药物不良反应监测工作制度、职责、报告工作机制及报告奖励办法等,药品从采购到使用制度齐全,能达到全程追踪管理。
(二)人员储备、技术支撑药学部共有40余人,其中研究生2名,配有专职临床药师10人,兼职负责全院药品规范使用、药物不良反应跟踪、监测和上报工作。
(四)重点监测、取得实效1、全院使用药品科室均纳入监控范围,重点监控精神科、老年科、神经内科、心理科、肿瘤科、呼吸科、心内科等科室。
2、每月重点跟踪不良反应患者用药及疗效,发现问题及时反馈干预,协助临床医师制定治疗方案。
3、每年开展精麻药品、药物不良反应、药物滥用宣传及培训至少各1次。
以上是我院在药品不良反应监测工作中所采取的几点做法,虽然取得了一定成绩,但还存在一定的问题,在2022年,我们要进一步完善措施,狠抓落实,努力提高全院药品不良反应监测水平,为保障广大人民群众身体健康做出我们积极的贡献。
药物不良反应报告年度总结

药物不良反应报告年度总结引言药物是医学领域中重要的治疗手段之一,通过合理使用可以有效缓解症状、治愈疾病。
然而,药物并非是完全安全的,有时会导致不良反应。
为了保障患者的用药安全,药物不良反应报告系统得以建立。
本文将对过去一年的药物不良反应进行总结分析,以期提高医药领域的安全性和质量。
数据统计与分析报告数量根据统计数据显示,过去一年药物不良反应报告总量为XXX例,较上一年度同比增长X%。
这表明患者对于药物不良反应的报告意识有所提高,也反映了医生和药师对于药物安全的重视程度。
不良反应类型药物的不良反应可以分为多种类型,包括但不限于过敏反应、药物相互作用、器官功能损害等。
据统计结果显示,本年度不良反应类型中,过敏反应占比最高,达到XX%;其次是药物相互作用,占比为XX%;器官功能损害类不良反应占比为XX%。
此数据显示过敏反应和药物相互作用是目前需要重点关注的问题。
药物类型不同种类的药物对于不良反应的发生有着不同的贡献度。
根据报告统计,本年度发生不良反应最多的药物类型为抗生素,占比XX%;其次是非甾体抗炎药,占比为XX%;其他药物(如抗癌药物、心血管药物等)的不良反应占比为XX%。
这一数据可以为临床医生在用药决策时提供参考。
不良反应原因分析药物特性药物不良反应的发生与药物本身的特性密切相关。
其中,药物特异性反应是最常见的原因之一。
比如一些药物可能在少数特定人群中发生过敏反应,而在大多数人中则没有产生不良反应。
另外,部分药物的代谢途径与患者的个体差异也会导致不同程度的不良反应。
因此,在用药前应对患者进行充分的评估和指导,以降低不良反应的风险。
用药过程中的问题不良反应还可能与用药过程中的问题有关。
例如,患者因为个人原因未按照医嘱正确使用药物,导致不良反应的发生。
另外,医生在开药时可能出现用药剂量或使用时间错误的情况,也可能增加了患者出现不良反应的可能性。
因此,加强患者药物使用教育,提高医生的用药技能和知识水平,是减少不良反应发生的重要措施。
《2021年度药品不良反应报告分析》

《202x年度药品不良反应报告分析》目的:药品不良反应(adr)是合格药品在正常用法用量下出现的与用药目的无关或意外的有害反应。
adr监测是提高临床用药质量,确保用药安全的重要举措,分析药品不良反应的特点和规律,促进临床合理用药。
方法:为了解我院adr发生的特点及引发的相关因素,按照患者年龄、药品类型、不良反应涉及系统、给药途径等进行分析,对*例药品不良反应报表进行分析。
结果:涉及不良反应药品*种。
抗感染药物*例居首位;静脉给药引发的药品不良反应*例(*%);药品不良反应的临床表现以皮疹、瘙痒等皮肤损害为主,其次是消化系统损害。
结论:对我院202x年度上报的*例adr报告进行分类统计、分析,为临床合理用药及药物安全性评价提供依据。
应注意合理用药,以避免和减少药品不良反应发生。
关键词:药品不良反应;统计;分析;合理用药一、资料与方法1.资料来源。
医院各科室上报。
2.方法。
采用回顾性研究方法,分别对*例药品不良反应患者的年龄、性别、给药途径、临床表现、涉及药品种类以及新的、严重的不良反应发生情况等进行调查,并对上述结果进行分类统计、分析和评价。
二、结果1.性别与年龄分布*例药品不良反应报告中男性患者*例(*%),女性患者*例(*%),患者年龄最小的*岁,最大的*岁,年龄以*岁者居多,年龄分布情况见表1。
表1发生adr患者的年龄分布例数构成比(%)年龄(岁)≤1920-2930-3940-4950-59≥60合计27.593.453.4517.2413.7934.481002.既往过敏史既往有明确adr史者*例,占*%。
3.用药基本情况引发adr的可疑药品中,西药*例,占*%;中药*例,占*%。
*例药品不良反应报告中,静脉给药引发不良反应的发生率*例占*%;口服给药**例占**%。
静脉给药导致药药品不良反应远高于口服给药的不良反应,注射药物直接进入体内,无肝脏首过效应,药物作用较口服给药迅速强烈,容易发生不良反应。
2021年药品不良反应调查分析整改报告

2021年药品不良反应调查分析整改报告药品不良反应(ADR)监测是合理用药的重要依据,是关系到广大患者用药安全,减少医患纠纷的一项重要工作。
我院2021年共收集上报14例ADR,现就2021年的ADR报告进行统计、分析,了解,为临床合理用药提供依据。
报告人职业和科室分布报告人医生上报14份,ADR报告来自门诊和住院患者,9例住院患者,5例门诊患者。
发生ADR的患者性别及年龄分布情况在报告的14例ADR中,男4例,女10例,年龄分布区间为7-83岁。
用药情况分析用药途径包括静脉给药及口服。
最常见仍为静脉滴注,占引起ADR的可疑药物共包含12个品种,引起ADR例数最多的为抗感染药物。
药物不良反应事件的严重程度及转归 14例都为一般等级统计ADR报表中发现的问题上报数量不足:我院每年住院病人一千多人,门诊诊疗近4万人次,但本年度上报的药品不良反应/事件报告涉及的患者仅14人次,报告率较低。
在临床工作中,护理人员与患者直接接触时间最多,对患者的反应警觉性高,发现ADR概率应较高,护士在ADR中的优势未能充分发挥。
上报药品不良反应类型单一:我院上报的药品不良反应多局限为各种药物致皮疹,且均为轻微皮疹,停药后多自行消散,所涉及药物无上市5年内的新药,亦无目前卫生部正在进行上市后再评价的药物,此类不良反应上报通常被上级药品不良反应监测中心判断为价值不大的报告。
医务人员应对不良反应类别的定义严格掌握,临床应鼓励医务人员积极发现新的、严重的不良反应,对于造成器官损害、致残、致畸、致死、导致住院治疗甚至延长住院时间的药物不良反应,要在规定时限内准确上报。
药物不良反应报表书写不规范:本次回顾分析发现,本院ADR报表书写虽比去年有很大提高,但仍存在部分不规范的情况,如填写漏项、不良反应发生经过描述不详、阐述内容无逻辑关系等,导致这一现象的主要原因是上报人对于表格各项目的要求理解不到位。
对此,临床药学室在2021年度对本院各科室的医护人员进行ADR报表规范化填写的培训,力求使我院上报的ADR报表达到省不良反应检测中心的要求。
2021年药品不良反应监测工作小结

201*年药品不良反应监测工作小结201*年药品不良反应监测工作小结自201*年连云分局开展药械不良反应/事件监测工作以来,分局一直高度重视药品安全工作,把保障人民群众用药安全作为一切工作的出发点。
在上级的正确领导和帮助支持下,通过加强ADR知识的宣传和培训,开通基层医疗机构呈报点等多项切实有效的措施,为做好药械不良反应/事件监测工作,做出了积极努力。
现将我区上半年药品不良反应监测工作情况小结如下基本情况全区已注册开通全国药械不良反应/事件监测网络呈报点139家,201*年全年共上报药品不良反应/事件监测报告300多例,其中新的、严重的15例,药械不良反应/事件监测报告网络直接呈报数量与呈报质量较去年上半年相比得到明显提升。
一是抓组织建设。
从开始推进开通药械不良反应/事件监测报告基层呈报点,在全区乡镇以上医疗机构、药品批发企业、药品零售企业设立不良反应监测呈报点,每个呈报点均明确专人负责呈报,并明确工作要求、职责,积极鼓励基层涉药单位开通药品不良反应基层呈报点,形成有效覆盖全区的不良反应监测网络体系。
截止201*年底已注册全国药械不良反应/事件监测网络呈报点139家,其中201*年新注册开通50多家。
目前我区已开通呈报点中二级以上医疗机构2家、社区卫生服务中心及乡镇卫生院22家,社区卫生服务站及村卫生室34家。
二是抓责任落实。
将全年监测报告任务进行细化,层层分解落实到各监测呈报点,并明确报告责任和完成时限,有效地强化监测呈报点和监测呈报员的责任意识和时效意识,鼓励基层呈报点由过去的书面报告变成自主网络呈报。
对于部分未配备电脑的村卫生室,通过与村卫生室所在街道(乡镇)的社区卫生服务中心协调,要求无法开展网上直接上报的村卫生室将将纸质不良反应报告表统一交至社区卫生服务中心的呈报人员,集中上报,确保按时按质按量完成监测报告任务。
三是抓学习培训。
积极推进基层村卫生室开通药品不良反应监测呈报点,召开药品不良反应监测培训会议,发放“药品不良反应报告表规范填写手册”,现场详细介绍了药品不良反应的基本知识、相关法律法规和药品不良反应上报的相关知识,并结合“药品不良反应监测系统”讲解药品不良反应监测报表的填报方法、上报要求及注意事项等内容。
药品不良反应报告总结

药品不良反应报告总结药品不良反应是指在使用药物过程中出现的与药物有关的不良反应、副作用和禁忌症等。
药品不良反应报告的目的是通过收集和分析不良反应数据,及时发现和评估新的或罕见的药品不良反应,为药物的安全使用提供参考依据。
在不良反应报告中,一般包括不良反应的主要信息,包括不良反应的性质、严重程度、时机和发生率等。
药品不良反应报告是世界各国药品监管机构的重要工作之一,也是保障公众用药安全的重要手段之一。
通过对药品不良反应的收集和报告,可以及时发现和评估药品的不良反应情况,帮助药品监管机构监测药品的安全性,及时采取措施保护用药者的权益。
药品不良反应报告的内容主要包括以下几个方面:1. 不良反应的性质:包括药物的不良反应类型,例如过敏反应、药物中毒、副作用等。
了解不良反应的性质可以帮助评估药物的安全性和适用性。
2. 不良反应的严重程度:不良反应的严重程度分为轻、中、重三个级别。
轻度的不良反应一般不会对患者的健康产生严重威胁,中度的不良反应可能会导致一定的健康问题,重度的不良反应则可能对患者的生命安全造成严重威胁。
3. 不良反应的发生率:不良反应的发生率是指在使用某种药物时出现不良反应的患者比例,通常以千分比或百分比表示。
发生率的高低可以反映药物的安全性和耐受性。
4. 不良反应的时机:不良反应发生的时机可以帮助判断和评估药物的不良反应原因。
有时不良反应可能是由于药物的剂量过大或用药时间过长导致的,也有可能是与患者个体差异有关。
5. 不良反应的处理和预防措施:对于常见的药物不良反应,药品监管机构通常会给出相应的处理和预防措施,以提醒医生和患者在使用药物时要注意的事项。
药品不良反应报告的收集通常依赖于医生、药师和患者的主动上报,也可以通过药品监管机构主动监测和调查,或者通过药物临床试验过程中的不良反应监测。
为了提高药物不良反应报告的准确性和及时性,药品监管机构通常会制定相应的政策和标准,鼓励和规范医生和患者的不良反应上报行为。
2021年药械化不良反应监测工作总结

2021年药械化不良反应监测工作总结
2021年药械化不良反应监测工作总结
2021年以来,我市药械化不良反应监测工作主要取得以下成绩:一是加快监测网络建设,确保各级重视,层层有人抓。
我们建立了由市局不良反应科牵头,各级医疗机构(二级医院、民营医院、乡镇卫生院)、医药生产经营企业、医疗器械生产企业组成的各级监测点,市、乡、村三级监测网络初步形成,并不断得到完善。
二是加强教育培训,确保不良反应监测工作大力开展。
我们采取组织召开会议、专家授课、实地走访监测点等形式,加强对各个监测点的教育培训。
三是2021年至今,药械化不良反应监测科共上报药品不良反应监测报告1364例,严重报告数63例,医疗器械不良反应监测报告375例,化妆品不良反应监测报告170例,已超额完成省局年初制定的工作任务。
对各个监测点报来的报告,未发生一起漏报、瞒报、迟报现象,上报率达100%。
存在问题:一是严重报告数较少,有的单位把发生药品不良反应现象与使用假劣药品混为一谈,怕影响本单位声誉,造成瞒报现象时有发生。
二是部分监测点上报的监测报告水平不高,填写报告欠规范,专业素质亟待提高。
2021年12月24日。
某院2021年度抗菌药物药品不良反应报告分析

某院2021年度抗菌药物药品不良反应报告分析某院2021年度抗菌药物药品不良反应报告分析近年来,随着细菌耐药性不断增强,抗菌药物的使用已成为医疗领域的重要课题。
然而,抗菌药物的不良反应也引起了人们的关注。
为了及时发现和解决药品不良反应问题,某医院每年都对抗菌药物使用过程中的不良反应进行监测和分析。
本文将针对某医院2021年度的抗菌药物药品不良反应报告进行分析,以期为临床合理使用抗菌药物提供参考。
2021年度,某医院收到了共计391份抗菌药物药品不良反应报告,其中男性占40%,女性占60%。
各个年龄段的患者中,以65岁以上的老年人为主,占报告总数的55%;15岁以下的儿童占17%;16至40岁的青年人占23%;41至64岁的中年人占5%。
这其中的不良反应主要包括药物过敏反应、肝损伤、肾损伤、胃肠道反应和神经系统反应等。
药物过敏反应是最常见的不良反应,占报告总数的40%。
其中以荨麻疹和药疹最为常见。
男性在荨麻疹发生率上略高于女性,但在药疹方面两者相差不大。
老年人中荨麻疹发生率最高,而儿童中以药疹发生率居首。
荨麻疹和药疹的发生率与抗菌药物种类关联性不大,而是与个体的过敏史有关。
肝损伤是第二常见的不良反应,占报告总数的25%。
男性中肝损伤发生率略高于女性。
老年人中肝损伤发生率相对较高,可能与老年人的肝功能下降和多重药物治疗有关。
其中,头孢菌素类药物和青霉素类药物是肝损伤的主要原因。
肾损伤占报告总数的15%,男性中肾损伤发生率高于女性。
中年人中肾损伤的发生率相对较高,可能与中年人的肾功能逐渐减弱有关。
青霉素类药物和氨基糖苷类药物是肾损伤的主要原因。
胃肠道反应占报告总数的10%,女性中胃肠道反应发生率高于男性。
儿童中胃肠道反应的发生率相对较高,可能与儿童的消化系统功能尚未完全成熟有关。
头孢菌素类药物和氨基糖苷类药物是胃肠道反应的主要原因。
神经系统反应占报告总数的5%,男性中神经系统反应发生率略高于女性。
老年人中神经系统反应发生率相对较高,可能与老年人的神经系统功能下降有关。
药品不良反应个人工作总结

药品不良反应个人工作总结篇一:药品不良反应监测工作总结与计划药械不良反应监测工作总结与计划20XX年度即将结束,今年我院药械不良反应监测工作,在市食品药品监督管理局、市卫生局的正确领导和帮助下,药械不良反应监测工作顺利开展,取得了一定成绩。
全年上报药品不良反应20例,器械不良事件7例。
首先,通过教育培训,向广大医务人员宣传及时上报药械不良反应的重要性和必要性。
使他们对药械不良反应工作有一个正确的认识,有的医务人员在上报药械不良反应时思想上有顾虑,担心因上报不良反应而受到处罚。
通过宣传,医务人员放下了思想包袱,增加了上报的积极性。
其次,要把药械不良反应上报工作制度化,将药械不良反应监测工作纳入了年终工作目标考核,对于药械不良反应监测工作做得好的科室和各人给与一定的奖励;相反,对于刻意瞒报、漏报的科室或各人给予严厉的处罚。
三是简化流程,临床上只要出现药械不良反应,只要打电话到药剂科,药剂科就会派专人到科室去调查核实,使上报工作变得简单易行。
以上是我们在药品器械不良反应监测工作中所采取的几点做法,虽然取得了一定成绩,但存在的问题还十分突出。
少数科室和个人对开展药品不良反应监测工作的目的意义重视程度不够,主动性、积极性不高,造成漏报、迟报现象时有发生。
因此我们一定要加强宣传,开展多种形式的教育培训活动。
充分利用有关会议、进行宣传,不断提高他们对做好药品器械不良反应监测工作重要意义的认识。
同时,聘请专家就有关方面知识进行培训,努力提高药品器械不良反应的发现率和上报率,杜绝漏报和瞒报现象,努力提高全院药品不良反应监测水平,为保障患者用药安全做出我们积极的贡献。
乌苏市人民医院20XX-12-24篇二:医院药品不良反应监测工作总结药品不良反应监测工作总结今年以来,我县药品不良反应监测工作,在市食品药品监管局、市卫生局的正确领导和帮助下,不断加大措施、健全组织、完善制度、强化督导,促进了监测工作的顺利开展,取得了一定成绩,为做好药品不良反应监测工作,做出了积极努力。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
全文共计1447字
药品不良反应报告年度总结
根据国家《药品不良反应和监测管理办法》和区卫计委要求:20xx 年本中心的药品不良反应工作开展的非常顺利,真正能落到实处。
20xx年通过本中心药品不良反应小组成员的努力和各科室的配合,药品不良反应上报数量52例,和去年同期相比上升2例,现将本年度药品不良反应工作总结如下:
1、本中心上报的不良反应汇总:52例
2、药品不良反应情况介绍:抗菌药物注射剂喹诺酮类(左氧氟沙星注射液)2例,主要不良反应为静脉炎,具体表现为使用后补液处出现发痒、红等症状。
口服制剂49例,主要不良反应为胃肠道不适、头晕、皮疹、乏力、肌肉痛、脚踝肿、面色潮红、肝功能异常等症状。
外用药1例:主要不良反应为感觉异常,表现为刺痛、灼烧感,无发热。
停药后症状消失、好转,均为一般不良反应。
3、不良反应处置及结果分析
处置情况
例数
备注
停药及对症用药
1。
