高中化学 硬水和软水区别方法
什么水可以用来区分软水和硬水

什么水可以用来区分软水和硬水
肥皂水可以区分硬水和软水。
题目:
区分硬水和软水可用.
化学初中
【考点】硬水与软水.
【专题】化学物质的分类思想;空气与水.
【分析】硬水是指含钙镁化合物较多的水,软水含钙镁化合物较少,肥皂水可以区分硬水和软水.
【解答】解:软硬水的区分可用肥皂水,硬水遇到肥皂水易起浮渣,软水遇到肥皂水产生很多泡沫;
故答案为:肥皂水.
【点评】本题属于基础题,也很简单,结合生活常识识记即可.
拓展知识:
软水是指不含或含较少可溶性钙、镁化合物的水;
硬水是指含有较多可溶性钙、镁化合物的水。
通常,自然界中的雨水、雪水属软水;山泉水﹑溪水﹑江河水、部分井水、部分地下水属硬水。
化学硬水与软水知识点

化学硬水与软水知识点做好试验是学好化学的根底.不仅课堂做,课后还要多做,可以用vcm 仿真试验,一种特地做试验的软件.每次试验牢记试验装置的要点,根据操作步骤,细致仔细地操作.其次要学会观看试验。
下面是整理的化学硬水与软水学问点,仅供参考盼望能够帮忙到大家。
化学硬水与软水学问点1、定义硬水是含有较多可溶性钙、镁化合物的水;例:井水软水是不含或含较少可溶性钙、镁化合物的水。
例:开水2.鉴别方法:用肥皂水,有浮渣产生或泡沫较少的是硬水,泡沫较多的是软水3.硬水软化的方法:蒸馏、煮沸4.长期使用硬水的害处:铺张肥皂,洗不洁净衣服;锅炉简单结成水垢,不仅铺张燃料,还易使管道变形甚至引起锅炉爆炸。
水的净化效果由低到高的是沉淀、过滤、吸附、蒸馏(均为物理方法),其中净化效果最好的操作是蒸馏;既有过滤作用又有吸附作用的净水剂是活性炭。
化学的学习方法及技巧是什么勤于预习、擅长听课做笔记。
要想学好化学,必需先了解这门课程。
课前肯定要预习,在预习时,除了要把新课内容认真读一遍外,还应在不懂处作上记号,并试着做一做课本上的练习。
这样带着疑问、难点,听课的效率就会大大地提高。
初中化学内容比拟多,学问比拟零散,教师在讲课时,着重围绕重点内容进展讲授。
因此大家要认真听课仔细做笔记,这不仅有利于进展课后复习,把握重点,而且还可以有效地预防上课时“走神”。
不过在记笔记时,要在听清晰教师所讲内容的根底上,记重点、难点、疑点和课本上没有的内容。
渐渐的培育对化学的兴趣学习任何一门学科,兴趣都是必不行少的。
所以,为了高效地学习化学,学生要努力培育对化学的“好感”。
首先,对化学课堂中的试验课,肯定要仔细看、仔细学习,课下勤于思索,可以自己动手做一些家庭小试验,还可以主动搜集一些与课本相关的化学小故事,通过这些方式渐渐建立起对化学的兴趣。
例如,在学习人教版九年级上册化学第四单元《水的净化》这局部内容时,课本中涉及了一个自制简易净水器的小试验,学生完全可以在家制作这个小装置:找一个空饮料瓶,瓶口用一个单孔胶塞塞住,然后将瓶子倒立过来,瓶子里放一些纱布、活性炭等,制作好后测试它的净化效果。
软水与硬水计算方法

软水与硬水计算方法
软水和硬水是指水中溶解的钙离子和镁离子的含量不同。
软水中这些离子的含量较低,而硬水中含量较高。
下面我将从不同角度来解释软水和硬水的计算方法。
1. 钙和镁离子浓度计算,软水和硬水的区别在于其中钙离子和镁离子的含量。
可以通过化学分析方法来测定水样中钙和镁离子的浓度,常用的方法包括EDTA滴定法和原子吸收光谱法。
这些方法可以精确地测定水样中钙和镁离子的含量,从而区分软水和硬水。
2. 碳酸盐硬度计算,硬水中的主要成分是碳酸钙和碳酸镁。
可以通过滴定法来测定水样中的碳酸盐硬度,常用的指标是以CaCO3的形式表示的硬度值。
软水中的碳酸盐硬度较低,而硬水中的碳酸盐硬度较高。
3. 钠离子浓度计算,软水中的钠离子含量相对较高,可以通过离子色谱法或火焰原子吸收光谱法来测定水样中的钠离子含量,从而判断水样的软硬程度。
4. 皂化值计算,软水和硬水对于洗涤剂的影响不同,可以通过
测定水样的皂化值来判断水样的软硬程度。
皂化值是指一定量水样中所需的洗涤剂用量,软水中的皂化值较低,而硬水中的皂化值较高。
综上所述,软水和硬水的计算方法主要包括测定钙和镁离子浓度、碳酸盐硬度、钠离子浓度和皂化值等指标。
通过这些指标的测定,可以准确地判断水样的软硬程度。
软水和硬水的检验方法

软水和硬水的检验方法
凡是含有较多可溶性钙、镁化合物的叫做硬水。
不含或含较少可溶性钙、镁化合物的叫软水。
检验方法:
1.分别用两只烧杯取等量水样。
向两只烧杯中分别滴加等量肥皂水。
泡沫多、浮渣少的为软水。
反之,泡沫少、浮渣多的为硬水。
2.还可以用烧杯加热,在杯壁留下较多水垢的是硬水。
因为硬水是
含有较多的可溶性钙,镁物质的水,加热后,这些可溶性的钙镁物质转化成不可溶性的物质,沉淀杂质多的是硬水,杂质越多,水的硬度越大。
3.取一干净、干燥的玻璃片。
分别在不同的位置滴等量水样。
待其
完全蒸发后,白色残留物多的为硬水,反之为软水。
拓展资料:
硬水里所含的可溶性钙、镁化合物,如果是酸性碳酸盐,如酸性碳酸钙、酸性碳酸镁等,就叫做暂时硬水。
因为酸性碳酸钙和酸性碳酸镁受热后,就变成碳酸钙和碳酸镁沉淀下来,经过过滤后,就成软水了。
硬水里所含的钙、镁等盐类,如果是硫酸盐,如硫酸钙、硫酸镁等,就叫做永久硬水。
因为硫酸镁是可以溶解于水的,即使煮沸后也
不能把他们全部去掉。
使用硬水会给生产和生活带来许多麻烦,如用硬水洗涤衣物,既浪费肥皂也洗不净衣物,时间长了还会使衣物变硬,锅炉用水硬度高了十分危险,因为锅炉内结垢后不仅浪费燃料,而且会使锅炉内管道局部过热,引起管道变形或损坏,严重时还可能引起爆炸。
常识积累:什么是软水和硬水

什么是软水和硬水软水是指不含或含较少可溶性钙、镁化合物的水。
软水不易与肥皂产生皂垢,而硬水相反。
硬水是指含有较多、可溶性、钙镁化合物的水。
硬水又分为暂时硬水和永久硬水。
暂时硬水的硬度是由碳酸氢钙与碳酸氢镁引起的,经煮沸后可被去掉,这种硬度又叫碳酸盐硬度。
永久硬水的硬度是由硫酸钙和硫酸镁等盐类物质引起的,经煮沸后不能去除。
我们通常把水中钙、镁离子的含量用“硬度”这个指标来表示。
硬度1度相当于每升水中含有10毫克氧化钙。
低于8度的水称为软水,高于17度的称为硬水,介于8~17度之间的称为中度硬水。
天然软水一般指江水、河水、湖(淡水湖)水,自然水中,雨水和雪水属软水,常见的有蒸馏水。
泉水、深井水、海水、江、河、湖水都是硬水。
软水和硬水的鉴别方法1:取一杯热水,倒入肥皂水,轻轻搅拌。
水面上出现泡沫的为软水,水面上出现浮渣的为硬水,浮渣越多,水的硬度越大。
方法2:用烧杯加热,在杯壁留下较多水垢的是硬水。
因为硬水是含有较多的可溶性钙,镁物质的水,加热后,这些可溶性的钙镁物质转化成不可溶性的物质,沉淀杂质多的是硬水,杂质越多,水的硬度越大。
方法3:取一干净、干燥的玻璃片。
分别在不同的位置滴等量水样。
待其完全蒸发后,白色残留物多的为硬水,反之为软水。
软水和硬水的利弊1、软水的利弊软水的优点:(1)软水沏茶,具有泉水的口感,较之自来水感觉更佳更好;(2)软水沐浴、梳洗使头发光滑,皮肤细腻;(3)软水洗衣,节省各种洗涤剂50%~80%;(4)软水降低衣物的磨损,使衣物洗后松软,色泽保持更长久;(5)软水减少热水器维修维护;(6)软水降低管道的维修维护;(7)软水减少洁具污垢的产生。
软水的危害:传统上人们认为软水具有一定好处,而饮用软水则能预防结石病发率,维护健康。
但是,通过最新医学研究表明,软水地区的心脏病死亡率高于硬水地区,主要原因与这些地区水中的镁离子含量太少有关,大约只有硬水的1/4。
2、硬水的利弊硬水的缺点:(1)和肥皂反应时产生不溶性的沉淀,降低洗涤效果。
化学硬水与软水知识点

化学硬水与软水知识点
化学硬水和软水是指水中溶解的矿物质含量不同的两种类型。
1. 硬水:
- 含有较高浓度的溶解性钙离子(Ca2+)和镁离子(Mg2+)。
- 硬水形成的原因是地下水与岩石中的石灰石(CaCO3)或镁矿物接触,溶解出这些离子。
- 硬水对洗涤剂的效果影响较大,因为钙和镁离子与洗涤剂中的表面活性剂发生反应,生成难溶性的肥皂垢。
- 硬水还会导致水垢在热水器、水龙头和水管内积聚,影响热能转移、阻塞水管和减少设备寿命。
2. 软水:
- 含有较低浓度的溶解性钙离子和镁离子。
- 软水可以通过水处理技术获得,例如离子交换、反渗透或蒸馏。
- 软水对洗涤剂的效果更好,因为水中钙离子和镁离子的浓度较低,不会与洗涤剂产生反应,形成肥皂垢。
- 软水也不容易产生水垢,因此设备的维护成本更低。
除了洗涤剂的影响外,硬水和软水还会对其他领域产生一些不同的影响:
- 饮用水:硬水在饮用时不会对健康产生直接影响,但高钙和镁含量可以给水增添一种微妙的味道。
软水则不会有这种味道。
- 煮水:硬水在煮水过程中会形成水垢,使锅具和水壶容易积聚水垢;而软水则不会产生这个问题。
- 植物浇灌:硬水中的钙和镁可以对植物生长产生负面影响,因为它们可以降低土壤的pH值;而软水则不会产生这种影响。
水的硬度可以通过测定水中钙和镁离子的浓度来确定。
常用的度量单位是“硬度度(dH)”或“毫克/升(mg/L)”。
通常,硬度小于4 dH或70 mg/L的水被认为是软水,大于12 dH或200 mg/L的水被认为是硬水。
软水和硬水的区分方法
硬水制成的冰块颜色混浊,有异味;软水制成的冰块晶莹剔透,手感软滑。
水质硬度试纸测试
1. 使用水质硬度试纸分别测试软水和硬水。
试纸上的化学物质会与水中的钙、镁离子发生反应,产生颜色变化。
通过色卡对比知道水的硬度大小。
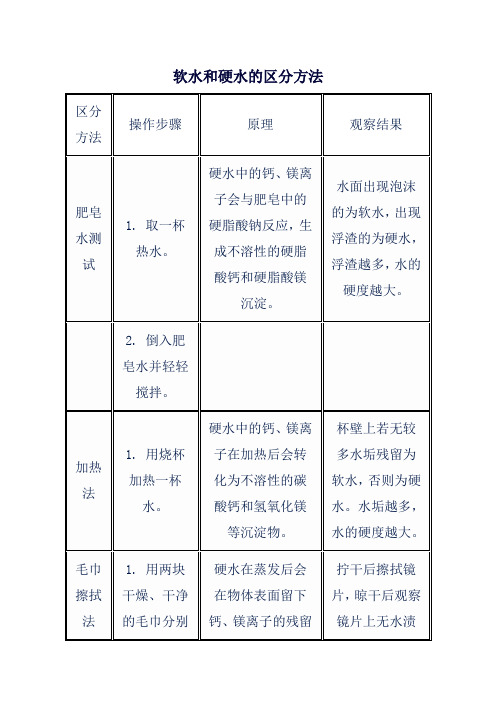
杯壁上若无较多水垢残留为软水,否则为硬水。水垢越多,水的硬度越大。
毛巾擦拭法
1. 用两块干燥、干净的毛巾分别沾上硬水和软水。
硬水在蒸发后会在物体表面留下钙、镁离子的残留物。
拧干后擦拭镜片,晾干后观察镜片上无水渍的为软水,有水渍的为
1. 分别用软水和硬水制成冰块。
软水和硬水的区分方法
区分方法
操作步骤
原理
观察结果
肥皂水测试
1. 取一杯热水。
硬水中的钙、镁离子会与肥皂中的硬脂酸钠反应,生成不溶性的硬脂酸钙和硬脂酸镁沉淀。
水面出现泡沫的为软水,出现浮渣的为硬水,浮渣越多,水的硬度越大。
2. 倒入肥皂水并轻轻搅拌。
加热法
1. 用烧杯加热一杯水。
硬水中的钙、镁离子在加热后会转化为不溶性的碳酸钙和氢氧化镁等沉淀物。
软水和硬水区别

硬水和軟水硬水和軟水概念圖含Ca2+、Mg2+有=> 硬水HCO3–↗暫時硬水=>加熱可使之變成軟水SO4–,Cl–↘永久硬水=>加熱也不能變軟水否=> 軟水註:1. 水是良好的溶劑,會溶解許多金屬離子及非金屬離子。
2. 可利用肥皂來檢驗硬水或軟水。
若是硬水,則無永久泡沫;若是軟水,則產生永久泡沫。
硬水的缺點:1. 和肥皂反應,產生不溶性的沈澱(減低洗滌效果)Ca2+、Mg2++C17H35COO–→鈣皂、鎂皂(硬脂酸根)2. 工業上,鈣鹽鎂鹽的沈澱造成鍋垢(CaSO4) ,妨礙熱傳導,嚴重時導致鍋爐爆炸。
硬水軟化法定義:去除水中Ca2+、Mg2+離子的方法。
1.煮沸法Ca2+(aq)+HCO3–(aq) --﹝加熱﹞->CaCO3(s)+H2O +CO22.石灰-蘇打法(Ca(OH)2-Na2CO3)(工業用)Ca2+(aq) --石灰-蘇打法-->CaCO3(s)Mg2+(aq)--石灰-蘇打法-->Mg(OH)2(s)3.蒸餾法(不是硬水軟化的主要方法)水-﹝加熱﹞->-﹝沸騰﹞->(蒸發成氣態) >﹝冷凝﹞->蒸餾水(CO2會回溶)4. 陽離子交換法原理:硬水通過泡沸石的管柱,Ca2+、Mg2+會被交換。
天然泡沸石(NaAlSiO4,簡式:NaZ,Z-表巨大泡沸石陰離子)NaZ(s) +Ca2+→CaZ2 +2Na+人工合成之陽離子交換樹脂(R-:磺酸化聚苯乙烯陰離子)NaZ(s) +Ca2+→CaR2 +2Na+陽離子樹脂的再生(加入濃食鹽水)CaZ2(s) +2Na+→NaZ(s)+Ca2+水的淨化與消毒1.沉澱法使顆粒大的泥沙或是懸浮物質靜置沉澱。
2.凝聚法加入凝聚劑,在水中產生膠質沉澱物,常用的凝聚劑是鋁鹽(Kal(SO4)2˙H2O),產生的膠狀沉澱物是Al(OH)3。
3.過濾法利用過濾槽過濾消毒和去臭常用的消毒劑:1. Cl2 : 抑制細菌代謝所需的酵素活性,以殺死細菌。
硬水和软水的区别方法

硬水和软水的区别方法硬水和软水是两种不同类型的水,其区别在于其化学成分中主要的离子含量以及水的溶解能力。
下面将详细讨论硬水和软水的区别,并解释这两种水对家庭和工业使用的影响。
1. 离子含量和水质硬度:硬水是指含有大量钙离子(Ca2+)和镁离子(Mg2+)的水。
这些离子是由矿物质和岩石中的钙和镁溶解而来。
硬水的主要特征是其高含钙和镁离子的浓度,通常以质量浓度(如ppm或mg/L)来衡量水的硬度。
硬水对人体没有直接的健康危害,但长期消耗硬水可能会加重尿结石形成的风险。
软水是指钙和镁离子含量较低的水。
软水通常是通过去除或减少硬水中的钙和镁离子实现的。
这可以通过不同的方法,如水软化设备(软水器)、反渗透等。
软水有助于减少钙和镁对管道、家电设备和衣物等表面的沉淀和水垢形成。
2. 形成的原因和净化方法:硬水是由钙和镁离子溶解在水中形成的。
当水通过地下岩层或矿物质时,会溶解其中的矿物质并带走相应的离子。
硬度可以通过工业处理过程中的离子交换或添加特定化学物质的方法来减少。
软水的形成主要通过去除或减少硬水中的钙和镁离子。
这可以通过不同的方法实现,如离子交换、反渗透、蒸馏和水过滤等。
3. 对家庭使用的影响:硬水的使用可能会导致一系列问题和不便。
首先,硬水含有大量的钙和镁离子,会导致水垢和沉淀在管道、水龙头、淋浴头等设备上。
这会限制水流并减少设备的寿命。
其次,硬水会影响洗衣机、洗碗机等家用电器的性能,增加维修和更换部件的成本。
另外,硬水还会降低洗涤剂和肥皂的效果,需要更多的清洁剂才能达到预期的清洁效果。
相比之下,软水对家庭使用更友好。
软水不会导致水垢积聚,因此不会对管道和设备造成损坏。
同时,由于软水改善了肥皂和洗涤剂的效果,家庭使用清洁品的量可以减少,这有助于节省开支。
4. 对工业使用的影响:硬水对工业使用也有一系列的负面影响。
首先,硬水中的水垢和沉淀会堵塞管道、冷却塔和锅炉等设备,并降低热传递效率。
其次,硬水会对工业设备和机械产生腐蚀。
软水与硬水的区分

轧三友发烧结厂题目:软水与硬水我们把水中含有的钙镁离子总浓度用“硬度”这个指标来衡量。
每升水中含有相当于10毫克的氧化钙为1度,硬度低于8度为软水,高于8度为硬水。
1.硬水含有钙盐和镁盐的天然水。
在硬水中,钙、镁可以以碳酸盐、碳酸氢盐、硫酸盐、氯化物和硝酸盐等形式存在。
当硬水中钙和镁主要以碳酸氢盐,如Ca(HCO3)2、Mg(HCO3)2形式存在时,称为暂时硬水,当这种硬水加热煮沸时,碳酸氢盐会分解成碳酸盐而沉淀除去如果硬水中钙和镁主要以硫酸盐、硝酸盐和氯化物等形式存在,则称为永久硬水,它们不能用煮沸的方法除去。
硬水中的钙盐和镁盐能与肥皂(硬脂酸钠)作用,生成不溶性的硬脂酸盐锅炉内使用硬水,当加热时钙盐和镁盐会在锅炉内壁上结成水垢。
降低锅炉的热导率,增加能耗,甚至缩短锅炉的使用寿命,有时还会堵塞管道。
因此,锅炉用水必须经过软化处理(见)。
2.软水只含少量可溶性钙盐和镁盐的天然水,或是经过软化处理的硬水经软化处理的硬水指钙盐和镁盐含量降为 1.0~50 毫克/升后得到的软化水。
虽然煮沸就可以将暂时硬水变为软水,但在工业上若采用此法来处理大量用水,则是极不经济的。
软化水的方法有:①石灰-苏打法。
先测定水的硬度,然后加入定量的氢氧化钙和碳酸钠,硬水中的钙、镁离子便沉淀析出:Ca(HCO3)2+Ca(OH)22CaCO3↓+2H2OMg(HCO3)2+2Ca(OH)2 Mg(OH)2↓+2CaCO3↓+2H2OCaSO4+Na2CO3CaCO3↓+Na2SO4 ②磷酸盐软水法。
对于锅炉用水,可以加入亚磷酸钠(NaPO3)作为软水剂,它与钙、镁离子形成络合物,在水煮沸时钙、镁不会以沉淀形式析出,从而不会形成水垢。
此法不适合于饮用水的软化,可用于工业。
③离子交换法。
沸石和离子交换剂虽然都不溶于水,但其中的钠离子和氢离子可与硬水中的钙、镁离子发生交换反应,使钙、镁离子被沸石、人造沸石、离子交换剂吸附而被除去。
检验硬水和软水的方法

检验硬水和软水的方法
有几种方法可以检验硬水和软水:
1. 肉眼观察法:将硬水和软水都倒入透明的玻璃杯中,用眼睛观察,若硬水中有悬浮物或水质较浑浊,而软水则清澈透明,这样便可通过肉眼观察来区分两者。
2. 沉淀法:将硬水和软水都加入氧化钠(NaOH)溶液中,搅拌并等待静置,若生成白色沉淀则为硬水,若无白色沉淀则为软水。
3. 石皮试纸法:将石皮试纸放入水中,硬水使得试纸颜色变为红色,而软水则不会引起颜色的变化。
4. 肥皂泡法:用同等量的硬水和软水来制造泡沫,硬水泡沫不如软水稳定和丰富,因为硬水中有更多的离子化物,它们会干扰肥皂沐浴露的表面张力而影响泡沫的质量。
以上几种方法中,沉淀法和石皮试纸法是比较常用的方法。
硬水和软水的区别及处理方法

硬水和软水的区别及处理方法水是人类生活中必不可少的元素,而水的硬度则是指水中溶解的钙、镁等金属离子的含量多少。
根据水中金属离子的含量不同,可以将水分为硬水和软水。
本文将从硬水和软水的定义、区别以及处理方法三个方面进行探讨。
一、硬水和软水的定义1. 硬水硬水是指含有较高钙、镁离子的水质。
通常,水中的钙、镁离子来自于岩石和土壤等地下水源。
硬水对于人体并无直接危害,但对生活和工业有一定的影响。
硬水含有的钙、镁离子容易在水壶、水管、洗衣机等使用热水的设备内部产生水垢,降低了设备的使用寿命。
此外,硬水降低了洗衣、洗碗等清洁效果,使得清洁剂的使用量增加。
2. 软水软水是指相对较低含有钙、镁离子的水质。
软水通常来自于经过特殊处理的水源,如软化水设备。
相比硬水,软水更适合用于生活和工业用途。
软水对于清洁效果更好,也能保护设备,延长使用寿命。
二、硬水和软水的区别硬水和软水在硬度、成分和对设备、洗涤效果的影响等方面有一定差异。
1. 硬度硬水的硬度较高,主要表现为水中的钙、镁离子含量较多。
根据国际通用的度量单位,硬水的硬度可以用毫摩尔/升(mmol/L)或者英国硬度单位(dH)来表示。
一般来说,硬度超过17.1mmol/L(或1dH)的水被认为是硬水,而低于该数值的水被认为是软水。
2. 成分硬水主要由钙、镁离子组成,而软水则含有较低的钙、镁离子含量。
除了钙、镁离子之外,软水的含有其它盐类离子,如钠离子。
3. 对设备的影响硬水中的钙、镁离子容易在设备内部产生水垢,降低设备的使用寿命。
硬水使用一段时间后,水壶、洗衣机、热水器等设备的内部会有水垢结构形成,需要定期进行清洗和维护。
而软水相对不会因水垢问题对设备造成损害。
4. 洗涤效果硬水的洗涤效果较差,需要增加清洁剂的使用量。
硬水中的钙、镁离子与清洁剂中的表面活性剂发生反应,产生沉淀物,降低了清洁剂的效果。
相比之下,软水能够更好地溶解清洁剂,提高洗涤效果。
三、硬水和软水的处理方法由于硬水的一些不利特性,许多家庭和工业需要处理硬水,将其转化为软水。
硬水与软水概括及区别

硬水与软水【摘要】水分为软水、硬水,凡不含或含有少量钙、镁离子的水称为软水,反之称为硬水。
【关键词】软水、硬水1. 硬水定义:含有较多可溶性钙镁物质的水是硬水。
所谓"硬水"是指水中所溶的矿物质成分多,尤其是钙和镁。
硬水并不对健康造成直接危害,但是会给生活带来很多麻烦,比如用水器具上结水垢、肥皂和清洁剂的洗涤效率减低等。
水是一种很好的溶剂,能有效去除污物杂质。
纯水--无色、无味、无臭,被称作是"通用溶剂"。
当水和二氧化碳结合生成微量的碳酸时,水的溶解效果更好。
当水流过土地和岩石时,它会溶解少量的矿物质成分,钙和镁就是其中最常见的两种成分,也就是它们使水质变硬。
水中含钙、镁等矿物质成分越多,水的硬度越大。
在英国一般用以下指数表示水硬度:硬度范围软轻硬度中硬度高硬度超强硬度所溶矿物质(毫克/升水)0 - 17.1 17.1 - 60 60 - 120 120 –180 180 & 以上所谓硬水,就是含有大量钙盐和镁盐离子的水。
这种水在家庭使用时,不能使肥皂产生泡沫,还会在所洗涤的衣物上沉淀一层水垢;在烧开水时会在壶底和热水瓶底部渐渐地结上一层坚硬的白色水垢。
如果这种硬水使用在锅炉或蒸汽机车上,会在锅炉底部和管道壁上形成一层硫酸钙或二氧化硅的“硬垢”,或一层碳酸钙的软垢,因而使管壁过热变形,导致锅炉和管道发生爆炸的危险。
这是很令人讨厌和十分可怕的。
当然,水中的铁盐和锰盐离子也是使水变硬的原因之一。
含有此离子的水会把肥皂沉淀出来的水垢在织物上产生锈斑,若再漂白却使污斑变得更糟。
这种水用来泡茶时,茶水面上会显出一层“水皮”,且茶的清香味儿也不翼而飞。
水中的镁的硬度会使水带有腐蚀性和明显的酸性,还会有一种会刺激眼睛的金属味。
镁盐是一种轻泻剂。
但是镁离子仅仅使人讨厌,而不会威胁人的健康。
尽管一定硬度的水,能降低金属的毒性及心血管病的发生率,但是,居民饮用的水还需进行软化处理,以免让硬水带来不良后果。
硬水和软水

水的硬度水的硬度:水中离子沉淀肥皂的能力,一般指水中Ca2+、Mg2+盐类的含量。
单位mmol/L或mg/L包括:总硬度碳酸盐硬度非碳酸盐硬度碳酸盐硬度(暂时硬度): 主要成分是钙、镁的酸式碳酸盐,其次是钙、镁的碳酸盐,由于这些盐类一经加热煮沸就会分解成为溶解度很小的碳酸盐,硬度大部分可以除去。
非碳酸盐硬度(永久硬度):表示水中的钙、镁的氯化物、硫酸盐、硝酸盐等盐类的含量,这些盐类经加热煮沸不会产生沉淀,使硬度不变化。
什么是软水不含或含较少可溶性钙、镁化合物的水叫做软水(soft water)。
软水不易与肥皂产生浮渣,而硬水相反。
天然软水一般指江水、河水、湖(淡水湖)水。
经软化处理的硬水指钙盐和镁盐含量降为 1. 0~50 毫克/升后得到的软化水。
虽然煮沸就可以将暂时硬水变为软水,但在工业上若采用此法来处理大量用水,则是极不经济的。
在日常生活中,我们经常见到水壶用久后内壁会有水垢生成,这是因为在我们取用的水中含有不少无机盐类物质,如钙、镁盐等。
这些盐在常温下的水中肉眼无法发现,一旦它们加温煮沸,便有不少钙、镁盐以碳酸盐形式沉淀出来,它们紧贴壶壁就形成水垢。
我们通常把水中钙、镁离子的含量用“硬度”这个指标来表示。
硬度1度相当于每升水中含有10毫克氧化钙。
低于8度的水称为软水,高于17度的称为硬水,介于8~17度之间的称为中度硬水。
雨、雪水、江、河、湖水都是软水,泉水、深井水、海水都是硬水。
有些钙、镁离子含量很高的水却不见有水垢生成,这是因为这些钙、镁离子以氯化盐形式存在,它们是可溶的,所以在加热时并不能沉淀出来。
水的硬度对日常生活影响是很大的。
如水的硬度大时洗衣服不起泡;旅居异地因饮水的硬度不适应可出现水土不服的症状;壶内结水垢会使壶的导热性下降;工业锅炉的水垢可引起爆炸事故。
所以,生活和工业用水均应适当控制水的硬度。
一般来说,软水多用于生活中,洗澡、洗衣服等。
不用于饮用,所含矿物质过少。
作用软水可将肌肤细胞内的污物彻底清除,延缓皮肤衰老,使清洗后的皮肤无紧绷感,光泽细腻。
化学软水硬水知识点总结

化学软水硬水知识点总结软水和硬水的性质、特点和区别:软水:软水中的钙离子和镁离子含量较低,一般指的是不含或含量很少的含钙离子和镁离子的水。
软水具有以下特点:1. 易起泡:由于软水中没有大量的钙离子和镁离子,所以在使用肥皂时,会很容易起泡。
2. 洗涤效果好:软水能够更好地溶解洗涤剂,因此在使用洗涤剂清洗衣物、餐具时,能起到更好的清洗效果。
3. 不会产生水垢:软水中的碳酸钙和碳酸镁含量较低,不会在管道、热水器等设备上产生水垢。
硬水:硬水中的钙离子和镁离子含量较高,会导致水垢的产生。
硬水具有以下特点:1. 难起泡:在硬水中使用肥皂时,会很难起泡,因为肥皂会与水中的钙离子和镁离子产生化学反应,生成不溶于水的物质,从而影响起泡效果。
2. 洗涤效果差:硬水中的钙离子和镁离子会与洗涤剂结合,形成不溶于水的沉淀,从而影响洗涤效果。
3. 容易产生水垢:硬水中的碳酸钙和碳酸镁含量较高,会在管道、热水器等设备上产生水垢,影响设备的使用寿命。
软水和硬水的分布:软水和硬水的分布与地质构造、地下水渗漏和地表水的特点有关。
一般来说,火山岩、花岗岩等酸性岩石所形成的地区,地下水和地表水中的钙、镁含量较低,属于软水地区;而石灰岩、石膏、盐类矿物所形成的地区,地下水和地表水中的钙、镁含量较高,属于硬水地区。
软水和硬水的影响:软水和硬水对人体健康和日常生活都有一定的影响。
硬水中的钙离子和镁离子对人体有益,但过多摄入会造成结石等问题;而软水中的铅离子和镉离子等重金属对人体则造成不良影响。
另外,硬水在日常生活中会影响洗涤效果,导致水垢的产生,影响热水器、洗衣机等设备的寿命。
因此,在实际应用中,需要根据水质情况进行相应处理,保证水质的安全和适用性。
软水和硬水的检测与处理:为了及时了解水质情况,可以采用试纸、化学分析法、离子交换法等方法检测水中的钙、镁含量。
在实际应用中,可以采用软化处理、过滤处理等方法对水质进行处理,以达到适用的要求。
软化处理:软化处理是指将硬水中的钙离子和镁离子通过化学反应转化为不溶于水的物质,将软水与硬水相对应。
【高中化学】软水和硬水

【高中化学】软水和硬水看见这个题目,觉得奇怪吗?水是流体,又何有软硬之分呢?其实这里所指的软和硬,是就溶于水中钙离子和镁离子的含量而定。
硬水有多于百万分之二百五十的钙离子和镁离子,而软水则含少于百万分之一百。
硬水的形成是由于雨水溶入了石中所含的钙和镁的化合物:caco3+co2+h2o->ca2++2hco3-mgco3.caco3+2co2+2h2o->ca2++mg2++4hco3-此外,硬水可以分成暂时硬水及永久硬水,暂时硬水在煮熟后可以变为软水:2hco3-->co2+co32-+h2oco32-+ca2+->caco3(s)co32-+mg2+->mgco3(s)碳酸钙和碳酸镁就是不容被水所熔化的,茶壶里的茶垢亦就是由此而来,故极难冲洗。
香港所供应的食水已就是软水,故我们不必采用色谱法器(ionexchangers)回去处置洁净或冷却用水中的铁、钙及镁质。
硬水与浮渣(scum)同学看到硬水这个词定必想要浮渣,这个在洗洁剂一课中学至的生字。
难道水中的矿物真的如此一事无成?其实它们对我们身体健康存有一定程度的影响,一份美国的医学杂志(journaloftheamericanmedicalsociety)就曾经报导过亨利史路特博士(drhenryschroeder)的辨认出---存有硬水供应的地区比没硬水供应的地区的死亡率高。
无论如何,我们亦不该服食过量,以免重蹈以往服食过量维生素a及c的覆辙。
矿泉水这种饮料就是一样矿物含量特高的硬水(多于百万分之五百),顾名思义,是从矿泉而来的水---雨水流进石层,溶入各种的矿物,再积蓄而成。
而碳化的矿泉水都从自然而生的,含碳酸盐的石头如石灰石)溶于水中并释放出二氧化碳气体。
在制作的过程中,这些气体会被收集,然后在将水装入瓶中时才加入被收集了的气体以确保瓶子中有一定的气压。
酿酒时,水中含有的矿物亦可以影响酒的质素。
硬水因含矿物以提供更多酵母菌养分,故以硬水科火筒而变成的酒酒质可以比较不好。
烧开的水属于软水吗

烧开的⽔属于软⽔吗
不⼀定,软硬⽔以含有矿物质的多少来区分的,主要指钙离⼦,镁离⼦.软⽔是指矿物质17.1毫克/升⽔以内。
烧开的⽔不能确定是软⽔还是硬⽔,但是其中钙离⼦部分会结为⽔垢,所以其硬度会降低.如果镁离⼦较多烧开是没办法降低硬度的。
软硬⽔的区分⽅法
1、EDTA滴定法。
亦称“⼄⼆胺四⼄酸滴定法”。
它是国际标准的⽔质硬度分析,⼀种络合滴定法。
EDTA(即⼄⼆胺四⼄酸)是⼀种很强的络合剂,能和许多⾦属离⼦形成稳定的络合物。
利⽤它和⾦属离⼦的络合反应为基础,采⽤⾦属指⽰剂的变⾊或电学、光学⽅法确定滴定终点,根据标准溶液的⽤量计算被测物质的含量。
2、利⽤软⽔硬度测试盒直接测定。
软⽔硬度测试盒主要是将标准⽅法中复杂的EDTA滴定过程和使⽤的试剂整合成试剂盒形式,⽅便⾮专业⽤户与现场⽤户快速检测经软化处理后的⽔⽔质硬度,使⽤⽅法极为简单,不需要专业技术⼈员,其检测精度视不同的产品可以达到1PPM或更⾼。
什么是蒸馏⽔
蒸馏⽔是⼀种纯净很⾼的⽔。
它是通过蒸发并冷凝⽔中低沸点的物质⼿段,达到分离出更纯净的⽔的⽬的,同时蒸馏⽔可分为⼀次蒸馏⽔和多次蒸馏⽔,他经常⽤于化学实验和医疗⼿术,除此之外在与机器、电器相关的⼯作中也会使⽤到蒸馏⽔。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
硬水和软水
•定义:
硬水是含有较多可溶性钙、镁化合物的水。
软水是不含或含较少可溶性钙、镁化合物的水。
水的硬度:
水的硬度常用一种规定的标准来衡量,这个标准是:把1L水里含10mgCaO(或相当于10mgCaO)称为1度。
•硬水和软水的检验:
(1)用肥皂水来检验硬水和软水,把肥皂水滴在水里搅拌,产生泡沫多的是软水,产生泡沫少或不产生泡沫的是硬水
(2)用加热煮沸的方法检验硬水和软水。
水加热煮沸时,有较多沉淀的是硬水,不产生沉淀或者产生沉淀较少的是软水。
硬水的软化:
就是设法除去硬水中的钙、镁化合物。
硬水软化的方法:生活中常用煮沸法,工业上常用离子交换法和药剂软化法,实验室常用蒸馏法,蒸馏法是净化程度较高的水,蒸馏时应注意以下几点:
①蒸馏瓶中的液体不能超过其容积的2/3.
②加热时,应在烧瓶中放几粒沸石(或碎瓷片)。
③装置气密性良好
④水银温度计的水银球应放在蒸馏烧瓶的支管口附近。
•使用硬水造成的危害:
饮用水中含有微量的钙、镁成分,对人体健康是有益的。
但是,水中含太多的钙、镁成分,对生活和生产都有危害。
①用硬水洗涤,不仅浪费肥皂,而且会在织物上积有肥皂跟钙、镁反应后生成的沉
淀,不容易洗干净,还会使纤维变脆、易断。
②硬水有苦涩味,长期饮用硬水会使人的胃肠功能紊乱,出现不同程度的腹胀、腹
泻和腹痛。
③锅炉用水硬度太大,会产生水垢,这会大大降低锅炉的导热能力,造成燃料的浪
费。
另外,当水垢爆裂脱落时,会造成炉壁局部受热不均,易引起锅炉爆炸。
离子交换法:
离子交换法是工业生产软化水的重要方法之一。
离子交换法的原理:离子交换树脂是一种聚合物,带有相应的功能基团(一般情况下,常规的钠离子交换树脂带有大量的钠离子),当含钙、镁离子较高的硬水经过离子交换树脂时,离子交换树脂即可以释放出钠离子,其功能基团与钙、镁离子结合。
这样水中的钙、镁离子含量下降,水的硬度降低,硬水即可被软化为软水。
离子交换法的流程为:工作(即交换)、反洗、再生、清洗四个过程。
