【精选】最新高一化学方程式汇总
高中化学必修一二化学方程式汇总

高中化学必修一二化学方程式汇总一、必修一化学方程式1. 钠及其化合物- 钠与氧气常温反应:4Na + O_{2}=2Na_{2}O- 钠在氧气中燃烧:2Na + O_{2}{点燃}{=!=!=}Na_{2}O_{2}- 钠与水反应:2Na + 2H_{2}O = 2NaOH+ H_{2}↑- 过氧化钠与水反应:2Na_{2}O_{2}+2H_{2}O = 4NaOH + O_{2}↑- 过氧化钠与二氧化碳反应:2Na_{2}O_{2}+2CO_{2}=2Na_{2}CO_{3}+O_{2} - 向碳酸钠溶液中滴加少量盐酸:Na_{2}CO_{3}+HCl = NaHCO_{3}+NaCl - 向碳酸钠溶液中滴加过量盐酸:Na_{2}CO_{3}+2HCl = 2NaCl +H_{2}O+CO_{2}↑- 碳酸氢钠受热分解:2NaHCO_{3}{}{=!=!=}Na_{2}CO_{3}+H_{2}O + CO_{2}↑- 碳酸氢钠与氢氧化钠反应:NaHCO_{3}+NaOH = Na_{2}CO_{3}+H_{2}O2. 铝及其化合物- 铝与氧气反应:4Al + 3O_{2}=2Al_{2}O_{3}- 铝与盐酸反应:2Al+6HCl = 2AlCl_{3}+3H_{2}↑- 铝与氢氧化钠溶液反应:2Al + 2NaOH+2H_{2}O = 2NaAlO_{2}+3H_{2}↑ - 氧化铝与盐酸反应:Al_{2}O_{3}+6HCl = 2AlCl_{3}+3H_{2}O- 氧化铝与氢氧化钠溶液反应:Al_{2}O_{3}+2NaOH = 2NaAlO_{2}+H_{2}O - 氢氧化铝的制备(向氯化铝溶液中滴加氨水):AlCl_{3}+3NH_{3}· H_{2}O = Al(OH)_{3}↓+3NH_{4}Cl- 氢氧化铝与盐酸反应:Al(OH)_{3}+3HCl = AlCl_{3}+3H_{2}O- 氢氧化铝与氢氧化钠溶液反应:Al(OH)_{3}+NaOH = NaAlO_{2}+2H_{2}O3. 铁及其化合物- 铁与氧气反应:3Fe + 2O_{2}{点燃}{=!=!=}Fe_{3}O_{4}- 铁与氯气反应:2Fe+3Cl_{2}{点燃}{=!=!=}2FeCl_{3}- 铁与盐酸反应:Fe + 2HCl = FeCl_{2}+H_{2}↑- 铁与硫酸铜溶液反应:Fe + CuSO_{4}=FeSO_{4}+Cu- 氯化亚铁与氯气反应:2FeCl_{2}+Cl_{2}=2FeCl_{3}- 氯化铁与铁反应:2FeCl_{3}+Fe = 3FeCl_{2}- 氯化铁与铜反应:2FeCl_{3}+Cu = 2FeCl_{2}+CuCl_{2}4. 硅及其化合物- 硅与氧气反应:Si + O_{2}{}{=!=!=}SiO_{2}- 硅与氢氧化钠溶液反应:Si + 2NaOH + H_{2}O=Na_{2}SiO_{3}+2H_{2}↑ - 二氧化硅与氢氧化钠溶液反应:SiO_{2}+2NaOH = Na_{2}SiO_{3}+H_{2}O - 二氧化硅与氢氟酸反应:SiO_{2}+4HF = SiF_{4}↑+2H_{2}O- 硅酸的制备(硅酸钠溶液与盐酸反应):Na_{2}SiO_{3}+2HCl =H_{2}SiO_{3}↓+2NaCl5. 氯及其化合物- 氯气与金属铁反应:2Fe + 3Cl_{2}{点燃}{=!=!=}2FeCl_{3}- 氯气与金属铜反应:Cu+Cl_{2}{点燃}{=!=!=}CuCl_{2}- 氯气与氢气反应:H_{2}+Cl_{2}{点燃}{=!=!=}2HCl- 氯气与水反应:Cl_{2}+H_{2}O = HCl + HClO- 次氯酸光照分解:2HClO{光照}{=!=!=}2HCl+O_{2}↑- 氯气与氢氧化钠溶液反应:Cl_{2}+2NaOH = NaCl + NaClO + H_{2}O- 氯气与氢氧化钙反应制漂白粉:2Cl_{2}+2Ca(OH)_{2}=CaCl_{2}+Ca(ClO)_{2}+2H_{2}O6. 硫及其化合物- 硫与氧气反应:S+O_{2}{点燃}{=!=!=}SO_{2}- 二氧化硫与水反应:SO_{2}+H_{2}O = H_{2}SO_{3}- 二氧化硫与氧气反应:2SO_{2}+O_{2}{催化剂}{underset{}{⇌}}2SO_{3} - 三氧化硫与水反应:SO_{3}+H_{2}O = H_{2}SO_{4}- 铜与浓硫酸反应:Cu + 2H_{2}SO_{4}(浓){}{=!=!=}CuSO_{4}+SO_{2}↑+2H_{2}O- 碳与浓硫酸反应:C + 2H_{2}SO_{4}(浓){}{=!=!=}CO_{2}↑+2SO_{2}↑+2H_{2}O7. 氮及其化合物- 氮气与氧气反应:N_{2}+O_{2}{放电或高温}{=!=!=}2NO- 一氧化氮与氧气反应:2NO+O_{2}=2NO_{2}- 二氧化氮与水反应:3NO_{2}+H_{2}O = 2HNO_{3}+NO- 工业合成氨:N_{2}+3H_{2}{催化剂}{underset{高温高压}{⇌}}2NH_{3}- 氨气与水反应:NH_{3}+H_{2}O = NH_{3}· H_{2}O- 氨气与氯化氢反应:NH_{3}+HCl = NH_{4}Cl- 氯化铵受热分解:NH_{4}Cl{}{=!=!=}NH_{3}↑+HCl↑- 碳酸氢铵受热分解:NH_{4}HCO_{3}{}{=!=!=}NH_{3}↑+H_{2}O↑+CO_{2}↑- 硝酸铵与氢氧化钠反应:NH_{4}NO_{3}+NaOH{}{=!=!=}NH_{3}↑+NaNO_{3}+H_{2}O- 铜与稀硝酸反应:3Cu + 8HNO_{3}(稀)=3Cu(NO_{3})_{2}+2NO↑+4H_{2}O- 铜与浓硝酸反应:Cu + 4HNO_{3}(浓)=Cu(NO_{3})_{2}+2NO_{2}↑+2H_{2}O二、必修二化学方程式1. 元素周期律相关反应(以碱金属和卤素为例)- 锂与氧气反应:4Li + O_{2}=2Li_{2}O- 钾与水反应:2K+2H_{2}O = 2KOH + H_{2}↑- 氯气与溴化钠溶液反应:Cl_{2}+2NaBr = 2NaCl+Br_{2}- 溴与碘化钾溶液反应:Br_{2}+2KI = 2KBr+I_{2}2. 化学反应与能量- 氢气燃烧:2H_{2}+O_{2}{点燃}{=!=!=}2H_{2}O(放热反应)- 碳酸钙受热分解:CaCO_{3}{}{=!=!=}CaO + CO_{2}↑(吸热反应)3. 有机化学基础(必修部分)- 甲烷燃烧:CH_{4}+2O_{2}{点燃}{=!=!=}CO_{2}+2H_{2}O- 甲烷与氯气发生取代反应(以一氯取代为例):CH_{4}+Cl_{2}{光照}{=!=!=}CH_{3}Cl+HCl- 乙烯燃烧:C_{2}H_{4}+3O_{2}{点燃}{=!=!=}2CO_{2}+2H_{2}O- 乙烯与溴水反应:C_{2}H_{4}+Br_{2}to C_{2}H_{4}Br_{2}- 乙烯与水加成反应:C_{2}H_{4}+H_{2}O{催化剂}{to}C_{2}H_{5}OH- 苯燃烧:2C_{6}H_{6}+15O_{2}{点燃}{=!=!=}12CO_{2}+6H_{2}O- 苯与液溴反应:C_{6}H_{6}+Br_{2}{FeBr_{3}}{=!=!=}C_{6}H_{5}Br+HBr - 乙醇燃烧:C_{2}H_{5}OH + 3O_{2}{点燃}{=!=!=}2CO_{2}+3H_{2}O - 乙醇与钠反应:2C_{2}H_{5}OH + 2Nato 2C_{2}H_{5}ONa+H_{2}↑- 乙醇的催化氧化:2C_{2}H_{5}OH + O_{2}{Cu或Ag}{underset{}{to}}2CH_{3}CHO + 2H_{2}O- 乙酸与乙醇的酯化反应:CH_{3}COOH+C_{2}H_{5}OH{浓硫酸}{underset{}{⇌}}CH_{3}COOC_{2}H_{5}+H_{2}O。
高一必修1化学方程式总结(汇编3篇)

高一必修1化学方程式总结(汇编3篇)1.高一必修1化学方程式总结第1篇二氧化硅和硅酸必记方程式一二氧化硅二氧化碳的性质(1)与H2O反应 CO2+H2OH2CO3(2)与碱液反应CO2少量: CO2+2NaOH===Na2CO3+H2OCO2足量: CO2+NaOH===NaHCO3(3)与碱性氧化物反应CO2+Na2O=== Na2CO3CaO+CO2===CaCO3(4)与盐反应CO2+Na2CO3+H2O =2NaHCO3二氧化硅的性质(1)与碱液反应 SiO2+2NaOH===Na2SiO3+H2O(2)与碱性氧化物反应 CaO+SiO2高温=====CaSiO3(4)与酸反应只与氢氟酸反应:SiO2+4HF===SiF4↑+2H2O(5)与盐反应SiO2+Na2CO3高温Na2SiO3+CO2↑SiO2+CaCO3高温CaSiO3+CO2↑(6) 2C+SiO2高温=====Si+2CO↑二硅酸硅酸的制备:(1)Na2SiO3溶液与盐酸反应:Na2SiO3+2HCl===H2SiO3↓+2NaCl。
(2)将CO2通入Na2SiO3溶液中:Na2SiO3+CO2+H2O===H2SiO3↓+Na2CO3。
硅酸加热分解H2SiO3△=====SiO2+H2O2.高一必修1化学方程式总结第2篇第四章第四节硫酸和硝酸的氧化性一浓硫酸的特性【课堂导学1】一、浓硫酸的特性将一瓶浓硫酸敞口放置在空气中,其质量的变化是增大,变化的原因是浓硫酸能吸收空气中的水蒸气。
若将一瓶浓盐酸(或浓硝酸)敞口放置在空气中,其质量的变化是减小,原因是浓盐酸(或浓硝酸)易挥发,溶质减少。
将一定量的蔗糖放入小烧杯中,加入浓硫酸,观察到的现象是白色蔗糖变黑、体积膨胀,变成疏松多孔的海绵状的炭,并放出有刺激性气味的气体,发生反应的化学方程式是C12H22O11浓硫酸――→12C+11H2O。
【归纳总结1】浓硫酸的特性(1)吸水性:浓硫酸可以吸收空气或其他气体中的水蒸气、混在固体中的湿存水、结晶水合物中的结晶水。
(完整版)高一所有化学方程式

(完整版)高一所有化学方程式
1. 水的电解:2H2O → 2H2 + O2
这个方程式表示水在电解过程中分解成氢气和氧气。
2. 酸碱中和反应:HCl + NaOH → NaCl + H2O
这个方程式表示盐酸和氢氧化钠反应氯化钠和水。
3. 铁的氧化:4Fe + 3O2 → 2Fe2O3
这个方程式表示铁在氧气中燃烧氧化铁。
4. 铝与盐酸反应:2Al + 6HCl → 2AlCl3 + 3H2
这个方程式表示铝与盐酸反应氯化铝和氢气。
5. 硫酸铜与氢氧化钠反应:CuSO4 + 2NaOH → Cu(OH)2 + Na2SO4
这个方程式表示硫酸铜与氢氧化钠反应氢氧化铜和硫酸钠。
6. 氢气与氧气反应:2H2 + O2 → 2H2O
这个方程式表示氢气与氧气反应水。
7. 碳酸钙与盐酸反应:CaCO3 + 2HCl → CaCl2 + CO2 + H2O
这个方程式表示碳酸钙与盐酸反应氯化钙、二氧化碳和水。
8. 硫酸铜与铁反应:CuSO4 + Fe → FeSO4 + Cu
这个方程式表示硫酸铜与铁反应硫酸亚铁和铜。
9. 氢氧化钠与硫酸反应:2NaO H + H2SO4 → Na2SO4 + 2H2O
这个方程式表示氢氧化钠与硫酸反应硫酸钠和水。
10. 氯化钠与硝酸银反应:NaCl + AgNO3 → AgCl + NaNO3
这个方程式表示氯化钠与硝酸银反应氯化银和硝酸钠。
化学高一方程式整理
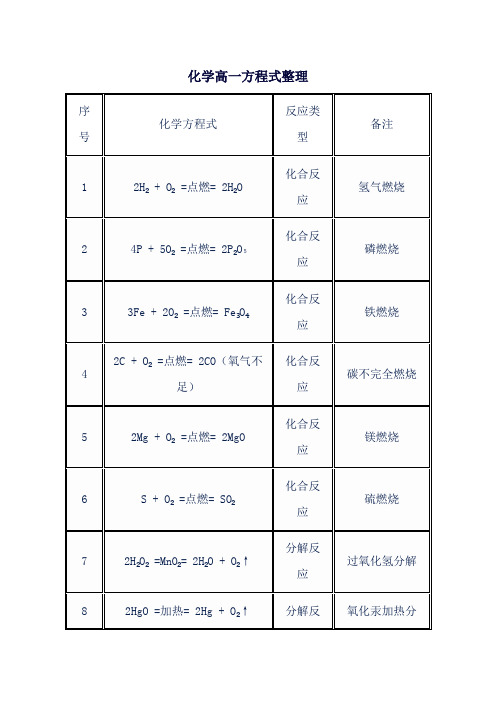
序号
化学方程式
反应类型
备注
1
2H₂ + O₂ =点燃= 2H₂O
化合反应
氢气燃烧
2
4P + 5O₂ =点燃= 2P₂O₅
化合反应
磷燃烧
3
3Fe + 2O₂ =点燃= Fe₃O₄
化合反应
铁燃烧
4
2C + O₂ =点燃= 2CO(氧气不足)
化合反应
碳不完全燃烧
5
2Mg + O₂ =点燃= 2MgO
复分解反应
碳酸钠与稀盐酸反应
23
BaCl₂ + Na₂SO₄ = BaSO₄↓ + 2NaCl
复分解反应
氯化钡与硫酸钠反应
24
AgNO₃ + HCl = AgCl↓ + HNO₃
复分解反应
硝酸银与盐酸反应
25
Ca(OH)₂ + Na₂CO₃ = CaCO₃↓ + 2NaOH
复分解反应
氢氧化钙与碳酸钠反应
19
Zn + H₂SO₄ = ZnSO₄ + H₂↑
置换反应
锌与稀硫酸反应
20
Fe + H₂SO₄ = FeSO₄ + H₂↑
置换反应
铁与稀硫酸反应
21
2NaOH + CuSO₄ = Cu(OH)₂↓ + Na₂SO₄
复分解反应
氢氧化钠与硫酸铜反应
22
Na₂CO₃ + 2HCl = 2NaCl + H₂O + CO₂↑
置换反应
一氧化碳还原氧化铁
15
H₂ + CuO =加热= Cu + H₂O
高中化学方程式总结精选全文完整版

可编辑修改精选全文完整版高中化学方程式总结高中化学方程式总结归纳不要把化学想得太难,化学题看起来很复杂,但是经过推敲之后,只要学生们正确的理解了题目要考察什么内容,寻找到正确的解题方法,就能做出化学题。
下面是小编为大家整理的高中化学方程式总结,希望对您有所帮助!高中化学方程式大全1.碳与氧气(不足)的反应 2C+O2==== 2CO碳与氧气(充足)的反应 C+O2==== CO22.一氧化碳与氧气的反应 2CO+O2==== 2CO23.二氧化碳与碳的反应 CO2+C==== 2CO4.碳酸氢钠与盐酸的反应NaHCO3+HCl==== NaCl+H2O+CO2↑5.碳酸钠与盐酸的反应Na2CO3+ 2HCl==== 2NaCl+ H2O+ CO2↑6.碳酸钙与盐酸的反应CaCO3+2HCl==== CaCl2+ H2O+ CO2↑7.碳酸氢钠与氢氧化钠的反应 NaHCO3+NaOH==== Na2CO3 +H2O8.碳酸钠与氢氧化钙的反应Na2CO3+Ca(OH)2==== CaCO3↓+ 2N aOH9.碳酸氢钠(少量)与氢氧化钙的反应NaHCO3+ Ca(OH)2==== CaCO3↓+NaOH+ H2O 碳酸氢钠(过量)与氢氧化钙的反应 2NaHCO3+ Ca(OH)2==== CaCO3+Na2CO3+2H2O10.碳酸氢钠加热的反应2NaHCO3==== Na2CO3+ H2O+CO2↑11.碳酸氢钙加热的反应Ca(HCO3)2==== CaCO3↓+H2O+CO2↑12.碳酸钙加热的反应CaCO3==== CaO+CO2↑13.二氧化碳(过量)通入氢氧化钙溶液中的反应 Ca(OH)2+2CO2==== Ca(HCO3)2 二氧化碳(少量)通入氢氧化钙溶液中的反应Ca(OH)2+CO2==== CaCO3↓+H2O14.氮气与氧气的反应 N2+O2==== 2NO15.一氧化氮与氧气的反应 2NO+O2==== 2NO216.二氧化氮与水的反应 3NO2+ H2O==== 2HNO3+ NO17.氮气与氢气的反应 N2+3H2========= 2NH318.氨气与水的反应 NH3+H2O==== NH3?H2O19.氨气与盐酸的反应 NH3+HCl==== NH4Cl20.氨气与硫酸的反应 2NH3+H2SO4==== (NH4)2SO421.氨气与强酸的离子的反应 NH3+H+==== NH4+22.氨的催化氧化的反应 4NH3+5O2====== 4NO+6H2O23.碳酸氢铵加热的反应NH4HCO3==== NH3↑+CO2↑+H2O24.氯化铵加热的反应NH4Cl==== NH3↑+HCl↑25.碳酸铵加热的反应(NH4)2CO3==== 2NH3↑+CO2↑+H2O26.氯化铵与氢氧化钙的反应2NH4Cl+ Ca(OH)2==== CaCl2+2NH3↑+2H2O27.氯化铵与氢氧化钠的反应NH4Cl+ NaOH==== NaCl+NH3↑+H2O28.碳酸氢铵与氢氧化钠的反应NH4HCO3+2NaOH==== Na2CO3+NH3↑+2H2O29.碳酸氢铵与氢氧化钙的反应NH4HCO3+Ca(OH)2==== CaCO3↓+NH3↑+2H2O30.硝酸的分解的反应4HNO3========= 4NO2↑+O2↑+2H2O高中化学方程式总结1.铜与浓硝酸的反应 Cu+4HNO3(浓)==== Cu(NO3)2+2NO2↑+2H2O2.铜与稀硝酸的反应 3Cu+8HNO3(稀)==== 3Cu(NO3)2+2NO↑+4H2O3.铁与浓硝酸的反应 Fe+6HNO3(浓)==== Fe(NO3)3+3NO2↑+3H2O4.铁与稀硝酸的反应 Fe+4HNO3(稀)==== Fe(NO3)3+NO↑+2H2O5.碳与浓硝酸的反应 C+4HNO3(浓)==== CO2↑+4NO2↑+2H2O6.一氧化氮与一氧化碳的反应 2NO+2CO====== N2+2CO27.一氧化氮与氧气和水的反应 4NO+3O2+2H2O==== 4HNO38.二氧化氮与氧气和水的反应 4NO2+O2+2H2O==== 4HNO39.氢氧化钠吸收二氧化氮和一氧化氮的反应 2NaOH+NO2+NO==== 2NaNO2+ H2O10.氨气(过量)与氯气的反应 8NH3+3Cl2==== 6NH4Cl+N2氨气(少量)与氯气的反应 2NH3+3Cl2==== 6HCl+N2化学考前学习方法对化学概念重新认识,深刻理解其内涵与外延,区分容易混淆的概念。
高一化学必修一化学方程式大全

高一化学必修一化学方程式大全1、钠在空气中燃烧(黄色的火焰)2Na +O2==【点燃】Na2O2钠块在空气中变暗4Na+O2=2Na2ONa2O在空气中加热(变黄)2Na2O+O2=2Na2O22、钠与水反应(浮、熔、游、响、红)2Na +2H2O =2H2O +H2 ↑2Na +2H2O =2Na+ +2OH- +H2↑3、过氧化钠与水的反应(放热反应、Na2O2是强氧化剂,用于漂白)2Na2O2 +2H2O =4NaOH +O2 ↑2Na2O2 +2H2O =4Na+ +4OH -+O2↑碱性氧化物Na2O与水的反应Na2O+H2O=2NaOH4、过氧化钠可用在呼吸面具和潜水艇中作为氧气来源,原因是:2Na2O2 +2CO2 =2Na2CO3 +O25、苏打(纯碱)与盐酸反应①盐酸中滴加纯碱溶液Na2CO3 +2HCl =2NaCl +H2O+CO2↑CO32- +2H+=H2O +CO2↑②纯碱溶液中滴加盐酸,至过量Na2CO3 +HCl =NaHCO3 +NaClCO32- +H+ =HCO3-NaHCO3+HCl=NaCl+H2O+CO2↑HCO3-+H+ =H2O +CO2↑6、小苏打受热分解2NaHCO3==【加热】Na2CO3 +H2O +CO2 ↑7、固体氢氧化钠和碳酸氢钠混合物在密闭容器中加热NaHCO3 +NaOH==【加热】Na2CO3 +H2OHCO3-+OH - =H2O +CO32-(若是溶液中反应有离子方程式)8、金属锂在空气中燃烧4Li +O2==【加热】2Li2O9、氯气的性质铜丝在氯气中剧烈燃烧(棕色烟)Cu +Cl2==【点燃】CuCl2之后加水,可由绿色溶液(浓)得到蓝色溶液(稀)Cl2 +2FeCl2 =2FeCl32Cl2+2NaBr=2NaCl+Br2Cl2 +2NaI =2NaCl+I2Cl2+SO2 +2H2O=H2SO4 +2HCl2Na +Cl2 ==【点燃】2NaCl10、铁在氯气中剧烈燃烧2Fe +3Cl2==【点燃】3FeCl311、氢气在氯气中燃烧(苍白色火焰)H2 +Cl2==【点燃】2HCl氟气与氢气反应(黑暗处即可爆炸)H2+F2=2HF12、氯气溶于水(新制氯水中含H+、Cl-、ClO-、OH-、Cl2、HClO、H2O)Cl2 +H2O =HCl +HClOCl2 +H2O =H++Cl- +HClO13、次氯酸见光分解(强氧化剂、杀菌消毒,漂白剂)2HClO==【光照】2HCl +O2↑14、工业制漂白粉的原理及漂白粉的失效2Ca(OH)2 +2Cl2 =Ca(ClO)2 +CaCl2 +2H2O2Ca(OH)2 +2Cl2 =2Ca2++2ClO-+2Cl-+2H2OCa(ClO)2+CO2+H2O=CaCO3↓+2HClO2HClO==【光照】2HCl +O2↑Ca2-+2ClO-+CO2 +H2O =CaCO3↓+2HClO15、氯气的实验室制法:(仪器:分液漏斗,圆底烧瓶)MnO2 +4HCl(浓)==【加热】MnCl2+Cl2↑+2H2OMnO2 +4H++2Cl-==【加热】Mn2++Cl2↑+2H2O16、新制氯水注入盛溴化钠溶液的试管中Cl2 +2NaBr =Br2 +2NaClCl2 +2Br- =Br2 +2Cl-17、铁与硫加热反应Fe +S==【加热】FeS铁与氧气加热反应3Fe+2O2==【加热】Fe3O4铁在氯气中加热反应2Fe+3Cl2==【加热】2FeCl318、铜与浓硫酸反应:Cu+2H2SO4 (浓) ==【加热】CuSO4 +2H2O+SO2 ↑19、碳与浓硫酸反应:C+2H2SO4(浓)==【加热】2H2O+CO2↑+2SO2↑20、工业制单质硅(碳在高温下还原二氧化硅)SiO2 +2C=(高温)Si +2CO↑21、二氧化硅与氢氧化钠反应SiO2 +2NaOH =Na2SiO3 +H2OSiO2 +2OH+ =SiO32- +H2O22、氮气和氢气反应(工业合成氨)N2 +3H2→【催化剂】2NH32NH3→【高温高压】N2 +3H223、氮气和氧气放电下反应(雷雨发庄稼)N2 +O2=(放电)2NO2NO +O2=2NO2二氧化氮溶于水3NO2 +H2O =2HNO3 +NO3NO2 +H2O =2H++2NO3-+NO24、HNO3与Fe的反应Al、Fe遇浓HNO3、浓硫酸钝化(常温)Fe与浓HNO3加热Fe+6HNO3==【加热】Fe(NO3)3+3NO2↑+3H2OFe与稀HNO3反应Fe+4HNO3=Fe(NO3)3+NO↑+2H2O3Fe+8HNO3=3Fe(NO3)2+2NO↑+4H2O25、NO2 、O2 的混合气通入水中无剩余气体4NO2 +O2 +2H2O =4 HNO326、NO 、O2 的混合气通入水中无剩余气体4NO +3O2 +2H2O =4 HNO327. 氨的催化氧化4NH3 +5O2 ==【催化剂、加热】4NO +6H2O28. 碳酸氢铵受热分解NH4HCO3==【加热】NH3 ↑+H2O↑+CO2↑29. 用浓盐酸检验氨气(白烟生成)HCl +NH3 =NH4Cl30. 硫酸铵溶液与氢氧化钠溶液混合加(NH4)2SO4 +2NaOH==【加热】2NH3↑+Na2SO2 +2H2O NH4++OH-==【加热】NH3 ↑+H2O31. 硝酸铵溶液与氢氧化钠溶液混合(不加热)NH4NO3 +NaOH =NH3·H2O +NaNO3NH4++OH-=NH3·H2O32. 铝箔在氧气中剧烈燃烧4Al +3O2 ==2Al2O333. 铝片与稀盐酸反应2Al +6HCl =2AlCl3 +3H2↑2Al +6H+=2Al3++3H2↑34. 铝与氢氧化钠溶液反应2Al+2NaOH +2H2O =2NaAlO2 +3H2↑2Al +2OH-+2H2O =2AlO2-+3H2↑35. 铝与三氧化二铁高温下反应(铝热反应)2Al +Fe2O3==【高温】2Fe +Al2O336. 镁在二氧化碳中燃烧2Mg +CO2 ==【点燃】2MgO +C37. 氧化铝溶于氢氧化钠溶液Al2O3 +2NaOH = 2NaAlO2 +H2OAl2O3 +2OH-=2AlO2-+H2O38. 硫酸铝溶液中滴过量氨水Al2(SO4)3 +6NH3·H2O=2Al(OH)3↓+(NH4)2SO4Al3++3 NH3·H2O =Al(OH)3↓+3NH4+39. ①氢氧化铝溶液中加盐酸Al(OH)3 +3HCl =AlCl3 +3H2OAl(OH)3 +3H+=Al3++3H2O②Al(OH)3与NaOH溶液反应Al(OH)3 +NaOH =NaAlO2 +2 H2OAl(OH)3 +OH-=AlO2-+2 H2O40. 高温下铁与水反应3Fe +4H2O(g)==【高温】Fe3O4 +4H241. 铁与盐酸反应Fe +2HCl =FeCl2 +H2↑Fe +2H+=Fe2++H2↑42. 氧化铁溶于盐酸中Fe2O3 +6HCl =2FeCl3 +3H2OFe2O3 +6H+=2Fe3++3H2O43. 氯化铁中滴入氢氧化钠溶液(红褐色沉淀)FeCl3 +3NaOH =Fe(OH)3 ↓+3NaClFe3++3OH-=Fe(OH)3 ↓44. 氢氧化亚铁在空气中被氧化(白色沉淀变为红褐色沉淀)4Fe (OH)2 +O2 +2H2O =4Fe (OH)345. 氯化亚铁溶液中通入氯气2FeCl2 +Cl2 =2FeCl32 Fe2++Cl2 =2 Fe3++2Cl-46. 氯化铁溶液中加入铁粉2FeCl3 +Fe =3FeCl22Fe3++Fe =3Fe2+47. 用KSCN检验的存在离子方程式Fe3++3SCN-= Fe(SCN)3一.物质与氧气的反应:(1)单质与氧气的反应:1. 镁在空气中燃烧:2Mg + O2 点燃2MgO2. 铁在氧气中燃烧:3Fe + 2O2 点燃Fe3O43. 铜在空气中受热:2Cu + O2 加热2CuO4. 铝在空气中燃烧:4Al + 3O2 点燃2Al2O35. 氢气中空气中燃烧:2H2 + O2 点燃2H2O6. 红磷在空气中燃烧:4P + 5O2 点燃2P2O57. 硫粉在空气中燃烧:S + O2 点燃SO28. 碳在氧气中充分燃烧:C + O2 点燃CO29. 碳在氧气中不充分燃烧:2C + O2 点燃2CO(2)化合物与氧气的反应:10. 一氧化碳在氧气中燃烧:2CO + O2 点燃2CO211. 甲烷在空气中燃烧:CH4 + 2O2 点燃CO2 + 2H2O12. 酒精在空气中燃烧:C2H5OH + 3O2 点燃2CO2 + 3H2O二.几个分解反应:13. 水在直流电的作用下分解:2H2O 通电2H2↑+ O2 ↑14. 加热碱式碳酸铜:Cu2(OH)2CO3 加热2CuO + H2O + CO2↑15. 加热氯酸钾(有少量的二氧化锰):2KClO3 ==== 2KCl + 3O2 ↑16. 加热高锰酸钾:2KMnO4 加热K2MnO4 + MnO2 + O2↑17. 碳酸不稳定而分解:H2CO3 === H2O + CO2↑18. 高温煅烧石灰石:CaCO3 高温CaO + CO2↑三.几个氧化还原反应:19. 氢气还原氧化铜:H2 + CuO 加热Cu + H2O20. 木炭还原氧化铜:C+ 2CuO 高温2Cu + CO2↑21. 焦炭还原氧化铁:3C+ 2Fe2O3 高温4Fe + 3CO2↑22. 焦炭还原四氧化三铁:2C+ Fe3O4 高温3Fe + 2CO2↑23. 一氧化碳还原氧化铜:CO+ CuO 加热Cu + CO224. 一氧化碳还原氧化铁:3CO+ Fe2O3 高温2Fe + 3CO225. 一氧化碳还原四氧化三铁:4CO+ Fe3O4 高温3Fe + 4CO2 四.单质、氧化物、酸、碱、盐的相互关系(1)金属单质+ 酸-------- 盐+ 氢气(置换反应)26. 锌和稀硫酸Zn + H2SO4 = ZnSO4 + H2↑27. 铁和稀硫酸Fe + H2SO4 = FeSO4 + H2↑28. 镁和稀硫酸Mg + H2SO4 = MgSO4 + H2↑29. 铝和稀硫酸2Al +3H2SO4 = Al2(SO4)3 +3H2↑30. 锌和稀盐酸Zn + 2HCl === ZnCl2 + H2↑31. 铁和稀盐酸Fe + 2HCl === FeCl2 + H2↑32. 镁和稀盐酸Mg+ 2HCl === MgCl2 + H2↑33. 铝和稀盐酸2Al + 6HCl == 2AlCl3 + 3H2↑(2)金属单质+ 盐(溶液)------- 另一种金属+ 另一种盐34. 铁和硫酸铜溶液反应:Fe + CuSO4 === FeSO4 + Cu35. 锌和硫酸铜溶液反应:Zn + CuSO4 === ZnSO4 + Cu36. 铜和硝酸汞溶液反应:Cu + Hg(NO3)2 === Cu(NO3)2 + Hg(3)碱性氧化物+酸-------- 盐+ 水37. 氧化铁和稀盐酸反应:Fe2O3 + 6HCl === 2FeCl3 + 3H2O38. 氧化铁和稀硫酸反应:Fe2O3 + 3H2SO4 === Fe2(SO4)3 + 3H2O39. 氧化铜和稀盐酸反应:CuO + 2HCl ==== CuCl2 + H2O40. 氧化铜和稀硫酸反应:CuO + H2SO4 ==== CuSO4 + H2O41. 氧化镁和稀硫酸反应:MgO + H2SO4 ==== MgSO4 + H2O42. 氧化钙和稀盐酸反应:CaO + 2HCl ==== CaCl2 + H2O(4)酸性氧化物+碱-------- 盐+ 水43.苛性钠暴露在空气中变质:2NaOH + CO2 ==== Na2CO3 + H2O 44.苛性钠吸收二氧化硫气体:2NaOH + SO2 ==== Na2SO3 + H2O 45.苛性钠吸收三氧化硫气体:2NaOH + SO3 ==== Na2SO4 + H2O 46.消石灰放在空气中变质:Ca(OH)2 + CO2 ==== CaCO3 ↓+ H2O 47. 消石灰吸收二氧化硫:Ca(OH)2 + SO2 ==== CaSO3 ↓+ H2O (5)酸+ 碱-------- 盐+ 水48.盐酸和烧碱起反应:HCl + NaOH ==== NaCl +H2O49. 盐酸和氢氧化钾反应:HCl + KOH ==== KCl +H2O50.盐酸和氢氧化铜反应:2HCl + Cu(OH)2 ==== CuCl2 + 2H2O51. 盐酸和氢氧化钙反应:2HCl + Ca(OH)2 ==== CaCl2 + 2H2O52. 盐酸和氢氧化铁反应:3HCl + Fe(OH)3 ==== FeCl3 + 3H2O53.氢氧化铝药物治疗胃酸过多:3HCl + Al(OH)3 ==== AlCl3 + 3H2O54.硫酸和烧碱反应:H2SO4 + 2NaOH ==== Na2SO4 + 2H2O55.硫酸和氢氧化钾反应:H2SO4 + 2KOH ==== K2SO4 + 2H2O56.硫酸和氢氧化铜反应:H2SO4 + Cu(OH)2 ==== CuSO4 + 2H2O57. 硫酸和氢氧化铁反应:3H2SO4 + 2Fe(OH)3==== Fe2(SO4)3 + 6H2O58. 硝酸和烧碱反应:HNO3+ NaOH ==== NaNO3 +H2O(6)酸+ 盐-------- 另一种酸+ 另一种盐59.大理石与稀盐酸反应:CaCO3 + 2HCl === CaCl2 + H2O + CO2↑60.碳酸钠与稀盐酸反应: Na2CO3 + 2HCl === 2NaCl + H2O + CO2↑61.碳酸镁与稀盐酸反应: MgCO3 + 2HCl === MgCl2 + H2O + CO2↑62.盐酸和硝酸银溶液反应:HCl + AgNO3 === AgCl↓ + HNO363.硫酸和碳酸钠反应:Na2CO3 + H2SO4 === Na2SO4 + H2O + CO2↑64.硫酸和氯化钡溶液反应:H2SO4 + BaCl2 ==== BaSO4 ↓+ 2HCl(7)碱+ 盐-------- 另一种碱+ 另一种盐65.氢氧化钠与硫酸铜:2NaOH + CuSO4 ==== Cu(OH)2↓ + Na2SO466.氢氧化钠与氯化铁:3NaOH + FeCl3 ==== Fe(OH)3↓ + 3NaCl67.氢氧化钠与氯化镁:2NaOH + MgCl2 ==== Mg(OH)2↓ + 2N aCl68. 氢氧化钠与氯化铜:2NaOH + CuCl2 ==== Cu(OH)2↓ + 2NaCl69. 氢氧化钙与碳酸钠:Ca(OH)2 + Na2CO3 === CaCO3↓+ 2NaOH(8)盐+ 盐----- 两种新盐70.氯化钠溶液和硝酸银溶液:NaCl + AgNO3 ==== AgCl↓ + NaNO371.硫酸钠和氯化钡:Na2SO4 + BaCl2 ==== BaSO4↓ + 2NaCl五.其它反应:72.二氧化碳溶解于水:CO2 + H2O === H2CO373.生石灰溶于水:CaO + H2O === Ca(OH)274.氧化钠溶于水:Na2O + H2O ==== 2NaOH75.三氧化硫溶于水:SO3 + H2O ==== H2SO476.硫酸铜晶体受热分解:CuSO4·5H2O 加热CuSO4 + 5H2O77.无水硫酸铜作干燥剂:CuSO4 + 5H2O ==== CuSO4·5H2O化学方程式反应现象应用2Mg+O2点燃或Δ2MgO 剧烈燃烧.耀眼白光.生成白色固体.放热.产生大量白烟白色信号弹2Hg+O2点燃或Δ2HgO 银白液体、生成红色固体拉瓦锡实验2Cu+O2点燃或Δ2CuO 红色金属变为黑色固体4Al+3O2点燃或Δ2Al2O3 银白金属变为白色固体3Fe+2O2点燃Fe3O4 剧烈燃烧、火星四射、生成黑色固体、放热4Fe + 3O2高温2Fe2O3C+O2 点燃CO2 剧烈燃烧、白光、放热、使石灰水变浑浊S+O2 点燃SO2 剧烈燃烧、放热、刺激味气体、空气中淡蓝色火焰.氧气中蓝紫色火焰2H2+O2 点燃2H2O 淡蓝火焰、放热、生成使无水CuSO4变蓝的液体(水)高能燃料4P+5O2 点燃2P2O5 剧烈燃烧、大量白烟、放热、生成白色固体证明空气中氧气含量CH4+2O2点燃2H2O+CO2 蓝色火焰、放热、生成使石灰水变浑浊气体和使无水CuSO4变蓝的液体(水)甲烷和天然气的燃烧2C2H2+5O2点燃2H2O+4CO2 蓝色火焰、放热、黑烟、生成使石灰水变浑浊气体和使无水CuSO4变蓝的液体(水)氧炔焰、焊接切割金属2KClO3MnO2 Δ2KCl +3O2↑ 生成使带火星的木条复燃的气体实验室制备氧气2KMnO4Δ K2MnO4+MnO2+O2↑ 紫色变为黑色、生成使带火星木条复燃的气体实验室制备氧气2HgOΔ2Hg+O2↑ 红色变为银白、生成使带火星木条复燃的气体拉瓦锡实验2H2O通电2H2↑+O2↑ 水通电分解为氢气和氧气电解水Cu2(OH)2CO3Δ2CuO+H2O+CO2↑ 绿色变黑色、试管壁有液体、使石灰水变浑浊气体铜绿加热NH4HCO3ΔNH3↑+ H2O +CO2↑ 白色固体消失、管壁有液体、使石灰水变浑浊气体碳酸氢铵长期暴露空气中会消失Zn+H2SO4=ZnSO4+H2↑ 有大量气泡产生、锌粒逐渐溶解实验室制备氢气Fe+H2SO4=FeSO4+H2↑ 有大量气泡产生、金属颗粒逐渐溶解Mg+H2SO4 =MgSO4+H2↑ 有大量气泡产生、金属颗粒逐渐溶解2Al+3H2SO4=Al2(SO4)3+3H2↑ 有大量气泡产生、金属颗粒逐渐溶解Fe2O3+3H2 Δ 2Fe+3H2O 红色逐渐变为银白色、试管壁有液体冶炼金属、利用氢气的还原性Fe3O4+4H2 Δ3Fe+4H2O 黑色逐渐变为银白色、试管壁有液体冶炼金属、利用氢气的还原性WO3+3H2Δ W +3H2O 冶炼金属钨、利用氢气的还原性MoO3+3H2 ΔMo +3H2O 冶炼金属钼、利用氢气的还原性2Na+Cl2Δ或点燃2NaCl 剧烈燃烧、黄色火焰离子化合物的形成、H2+Cl2 点燃或光照2HCl 点燃苍白色火焰、瓶口白雾共价化合物的形成、制备盐酸CuSO4+2NaOH=Cu(OH)2↓+Na2SO4 蓝色沉淀生成、上部为澄清溶液质量守恒定律实验2C +O2点燃2CO 煤炉中常见反应、空气污染物之一、煤气中毒原因2C O+O2点燃2CO2 蓝色火焰煤气燃烧C + CuO 高温2Cu+ CO2↑ 黑色逐渐变为红色、产生使澄清石灰水变浑浊的气体冶炼金属2Fe2O3+3C 高温4Fe+ 3CO2↑ 冶炼金属Fe3O4+2C高温3Fe + 2CO2↑ 冶炼金属C + CO2 高温2COCO2 + H2O = H2CO3 碳酸使石蕊变红证明碳酸的酸性H2CO3 ΔCO2↑+ H2O 石蕊红色褪去Ca(OH)2+CO2= CaCO3↓+ H2O 澄清石灰水变浑浊应用CO2检验和石灰浆粉刷墙壁CaCO3+H2O+CO2 = Ca(HCO3)2 白色沉淀逐渐溶解溶洞的形成,石头的风化Ca(HCO3)2Δ CaCO3↓+H2O+CO2↑ 白色沉淀、产生使澄清石灰水变浑浊的气体水垢形成.钟乳石的形成2NaHCO3ΔNa2CO3+H2O+CO2↑ 产生使澄清石灰水变浑浊的气体小苏打蒸馒头CaCO3 高温CaO+ CO2↑ 工业制备二氧化碳和生石灰CaCO3+2HCl=CaCl2+ H2O+CO2↑ 固体逐渐溶解、有使澄清石灰水变浑浊的气体实验室制备二氧化碳、除水垢Na2CO3+H2SO4=Na2SO4+H2O+CO2↑ 固体逐渐溶解、有使澄清石灰水变浑浊的气体泡沫灭火器原理Na2CO3+2HCl=2NaCl+ H2O+CO2↑ 固体逐渐溶解、有使澄清石灰水变浑浊的气体泡沫灭火器原理MgCO3+2HCl=MgCl2+H2O+CO2↑ 固体逐渐溶解、有使澄清石灰水变浑浊的气体CuO +COΔ Cu + CO2 黑色逐渐变红色,产生使澄清石灰水变浑浊的气体冶炼金属Fe2O3+3CO高温2Fe+3CO2 冶炼金属原理Fe3O4+4CO高温3Fe+4CO2 冶炼金属原理WO3+3CO高温W+3CO2 冶炼金属原理CH3COOH+NaOH=CH3COONa+H2O2CH3OH+3O2点燃2CO2+4H2OC2H5OH+3O2点燃2CO2+3H2O 蓝色火焰、产生使石灰水变浑浊的气体、放热酒精的燃烧Fe+CuSO4=Cu+FeSO4 银白色金属表面覆盖一层红色物质湿法炼铜、镀铜Mg+FeSO4= Fe+ MgSO4 溶液由浅绿色变为无色Cu+Hg(NO3)2=Hg+ Cu (NO3)2Cu+2AgNO3=2Ag+ Cu(NO3)2 红色金属表面覆盖一层银白色物质镀银Zn+CuSO4= Cu+ZnSO4 青白色金属表面覆盖一层红色物质镀铜Fe2O3+6HCl=2FeCl3+3H2O 铁锈溶解、溶液呈黄色铁器除锈Al2O3+6HCl=2AlCl3+3H2O 白色固体溶解Na2O+2HCl=2NaCl+H2O 白色固体溶解CuO+2HCl=CuCl2+H2O 黑色固体溶解、溶液呈蓝色ZnO+2HCl=ZnCl2+ H2O 白色固体溶解MgO+2HCl=MgCl2+ H2O 白色固体溶解CaO+2HCl=CaCl2+ H2O 白色固体溶解NaOH+HCl=NaCl+ H2O 白色固体溶解Cu(OH)2+2HCl=CuCl2+2H2O 蓝色固体溶解Mg(OH)2+2HCl=MgCl2+2H2O 白色固体溶解Al(OH)3+3HCl=AlCl3+3H2O 白色固体溶解胃舒平治疗胃酸过多Fe(OH)3+3HCl=FeCl3+3H2O 红褐色沉淀溶解、溶液呈黄色Ca(OH)2+2HCl=CaCl2+2H2OHCl+AgNO3= AgCl↓+HNO3 生成白色沉淀、不溶解于稀硝酸检验Cl—的原理Fe2O3+3H2SO4= Fe2(SO4)3+3H2O 铁锈溶解、溶液呈黄色铁器除锈Al2O3+3H2SO4= Al2(SO4)3+3H2O 白色固体溶解CuO+H2SO4=CuSO4+H2O 黑色固体溶解、溶液呈蓝色ZnO+H2SO4=ZnSO4+H2O 白色固体溶解MgO+H2SO4=MgSO4+H2O 白色固体溶解2NaOH+H2SO4=Na2SO4+2H2OCu(OH)2+H2SO4=CuSO4+2H2O 蓝色固体溶解Ca(OH)2+H2SO4=CaSO4+2H2OMg(OH)2+H2SO4=MgSO4+2H2O 白色固体溶解2Al(OH)3+3H2SO4=Al2(SO4)3+3H2O 白色固体溶解2Fe(OH)3+3H2SO4=Fe2(SO4)3+3H2O 红褐色沉淀溶解、溶液呈黄色Ba(OH)2+ H2SO4=BaSO4↓+2H2O 生成白色沉淀、不溶解于稀硝酸检验SO42—的原理BaCl2+ H2SO4=BaSO4↓+2HCl 生成白色沉淀、不溶解于稀硝酸检验SO42—的原理Ba(NO3)2+H2SO4=BaSO4↓+2HNO3 生成白色沉淀、不溶解于稀硝酸检验SO42—的原理Na2O+2HNO3=2NaNO3+H2O 白色固体溶解CuO+2HNO3=Cu(NO3)2+H2O 黑色固体溶解、溶液呈蓝色ZnO+2HNO3=Zn(NO3)2+ H2O 白色固体溶解MgO+2HNO3=Mg(NO3)2+ H2O 白色固体溶解CaO+2HNO3=Ca(NO3)2+ H2O 白色固体溶解NaOH+HNO3=NaNO3+ H2OCu(OH)2+2HNO3=Cu(NO3)2+2H2O 蓝色固体溶解Mg(OH)2+2HNO3=Mg(NO3)2+2H2O 白色固体溶解Al(OH)3+3HNO3=Al(NO3)3+3H2O 白色固体溶解Ca(OH)2+2HNO3=Ca(NO3)2+2H2OFe(OH)3+3HNO3=Fe(NO3)3+3H2O 红褐色沉淀溶解、溶液呈黄色3NaOH + H3PO4=3H2O + Na3PO43NH3+H3PO4=(NH4)3PO42NaOH+CO2=Na2CO3+ H2O 吸收CO、O2、H2中的CO2、2NaOH+SO2=Na2SO3+ H2O 2NaOH+SO3=Na2SO4+ H2O 处理硫酸工厂的尾气(SO2)FeCl3+3NaOH=Fe(OH)3↓+3NaCl 溶液黄色褪去、有红褐色沉淀生成AlCl3+3NaOH=Al(OH)3↓+3NaCl 有白色沉淀生成MgCl2+2NaOH = Mg(OH)2↓+2NaClCuCl2+2NaOH = Cu(OH)2↓+2NaCl 溶液蓝色褪去、有蓝色沉淀生成CaO+ H2O = Ca(OH)2 白色块状固体变为粉末、生石灰制备石灰浆Ca(OH)2+SO2=CaSO3↓+ H2O 有白色沉淀生成初中一般不用Ca(OH)2+Na2CO3=CaCO3↓+2NaOH 有白色沉淀生成工业制烧碱、实验室制少量烧碱Ba(OH)2+Na2CO3=BaCO3↓+2NaOH 有白色沉淀生成Ca(OH)2+K2CO3=CaCO3↓ +2KOH 有白色沉淀生成CuSO4+5H2O= CuSO4·H2O 蓝色晶体变为白色粉末CuSO4·H2OΔ CuSO4+5H2O 白色粉末变为蓝色检验物质中是否含有水AgNO3+NaCl = AgCl↓+Na NO3 白色不溶解于稀硝酸的沉淀(其他氯化物类似反应)应用于检验溶液中的氯离子BaCl2 + Na2SO4 = BaSO4↓+2NaCl 白色不溶解于稀硝酸的沉淀(其他硫酸盐类似反应)应用于检验硫酸根离子CaCl2+Na2CO3= CaCO3↓+2NaCl 有白色沉淀生成MgCl2+Ba(OH)2=BaCl2+Mg(OH)2↓ 有白色沉淀生成CaCO3+2HCl=CaCl2+H2O+CO2 ↑MgCO3+2HCl= MgCl2+H2O+ CO2 ↑NH4NO3+NaOH=NaNO3+NH3↑+H2O 生成使湿润石蕊试纸变蓝色的气体,应用于检验溶液中的铵根离子NH4Cl+ KOH= KCl+NH3↑+H2O 生成使湿润石蕊试纸变蓝色的气体氨:NH3胺:氨分子中的氢被烃基取代而生成的化合物。
高中高一化学方程式大全

高中高一化学方程式大全高中高一化学方程式大全:1、钠与氧气:常温:4na+o2=2na2o点燃:2na+o2=(△)na2o22、钠与水反应:2na+2h2o=2naoh+h2↑离子方程式:2na+2h2o=2na ++2oh-+h2↑3、钠与硫酸反应:2na+h2so4=na2so4+h2↑4、氧化钠与水反应:na2o+h2o=2naoh5、过氧化钠与二氧化碳反应:2na2o2+2co2=2na2co3+o2↑6、过氧化钠与水反应:2na2o2+2h2o=4naoh+o2↑离子方程式:2na2o2+2h2o=4na++4oh-+o2↑7、naoh溶液中通入少量co2:2naoh+co2=na2co3+h2o离子方程式:2oh-+co2=co32-+h2onaoh溶液中通入过量co2:naoh+co2=nahco3离子方程式:oh-+co2=hco3-8、①向碳酸钠溶液滴入少量稀盐酸:na2co3+hcl=nahco3+nacl向稀盐酸滴入少量碳酸钠溶液:na2co3+2hcl=2nacl+h2o+co2↑②除去碳酸氢钠溶液中混有的碳酸钠:na2co3+h2o+co2=2nahco3③碳酸钠与氢氧化钙:na2co3+ca(oh)2=caco3↓+2naoh④碳酸氢钠与盐酸:nahco3+hcl=nacl+h2o+co2↑⑤少量碳酸氢钠溶液滴入氢氧化钙溶液中:nahco3+ca(oh)2=caco3↓+naoh+h2o少量氢氧化钙溶液滴入碳酸氢钠溶液中:2nahco3+ca(oh)2=caco3↓+na2co3+2h2o⑥除去碳酸钠溶液中的碳酸氢钠:nahco3+naoh=(△)na2co3+h2o⑦除去碳酸钠固体中的碳酸氢钠:2nahco3=(△)na2co3+h2o+co2↑⑧鉴别碳酸钠和碳酸氢钠溶液:na2co3+cacl2=caco3↓+2nacl。
高中化学方程式大全高一

高中化学方程式大全高一
以下是部分高一化学方程式:
1. 金属钠与盐酸的化学方程式:2Na+2HCl=2NaCl+H2↑
2. 氢氧化钠方在空气中变质的化学方程式:
3. 金属钠放在空气的氧化:4Na+O2=2Na2O (银白色变暗)
4. 金属钠在空气燃烧:2Na+O2=Na2O2Δ (生成淡黄色粉末)
5. 过氧化钠在空气中变质:
6. 过氧化钠与酸反应:2Na2O2+4HCl=4NaCl+2H2O+O2↑
7. 氧化钠在空气中变质:
8. 氧化钠与酸反应:Na2O+2HCl=2NaCl+H2O
9. 氧化钠在空气中燃烧:2Na2O+O2=2Na2O2Δ
10. 氯气与铜的反应方程式:Cu+Cl2=CuCl2点燃(棕黄色的烟)
11. 氯气与氢气的反应方程式:Cl2+H2=2HCl 点燃(苍白色火焰,生成白雾)
12. 氯气与钠单质的反应方程式:2Na+Cl2=2NaCl 点燃(淡黄色的烟)
13. 氯气与水的方程式:Cl2+H2O=HCl+HClO
以上化学方程式仅供参考,可以查询化学教辅书获取更多相关内容。
高一化学方程式总结(精选17篇)

高一化学方程式总结(精选17篇)(经典版)编制人:__________________审核人:__________________审批人:__________________编制单位:__________________编制时间:____年____月____日序言下载提示:该文档是本店铺精心编制而成的,希望大家下载后,能够帮助大家解决实际问题。
文档下载后可定制修改,请根据实际需要进行调整和使用,谢谢!并且,本店铺为大家提供各种类型的经典范文,如工作报告、合同协议、心得体会、条据书信、规章制度、礼仪常识、自我介绍、教学资料、作文大全、其他范文等等,想了解不同范文格式和写法,敬请关注!Download tips: This document is carefully compiled by this editor. I hope that after you download it, it can help you solve practical problems. The document can be customized and modified after downloading, please adjust and use it according to actual needs, thank you!Moreover, our store provides various types of classic sample essays, such as work reports, contract agreements, personal experiences, normative letters, rules and regulations, etiquette knowledge, self introduction, teaching materials, complete essays, and other sample essays. If you want to learn about different sample formats and writing methods, please pay attention!高一化学方程式总结(精选17篇)高一化学方程式总结(精选17篇)高一化学方程式总结篇1二氧化碳溶解于水:CO2+H2O===H2CO3生石灰溶于水:CaO+H2O===Ca(OH)2氧化钠溶于水:Na2O+H2O====2NaOH三氧化硫溶于水:SO3+H2O====H2SO4硫酸铜晶体受热分解:CuSO4·5H2O加热CuSO4+5H2O 无水硫酸铜作干燥剂:CuSO4+5H2O====CuSO4·5H2O 高一化学方程式总结篇2钠及其化合物的性质1.钠在空气中缓慢氧化:4Na+O2==2Na2O2.钠在空气中燃烧:2Na+O2点燃====Na2O23.钠与水反应:2Na+2H2O=2NaOH+H2↑现象:①钠浮在水面上;②熔化为银白色小球;③在水面上四处游动;④伴有嗞嗞响声;⑤滴有酚酞的水变红色。
化学方程式大全

高中化学(必修一)化学方程式大全一、卤族元素Cl2+Cu Cu Cl23Cl2+2Fe2FeCl3Cl2+2 Na 2Na Cl Cl2 + H22HClCl2+H2O HCl+HClO Cl2+H2O H++Cl-+HClOCl2+2NaOH=NaCl+NaClO+H2O Cl2+2OH—=Cl—+ClO—+H2O2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O Cl2+2OH—=Cl-+ClO-+H2OCl2+2FeCl2=2FeCl3Cl2+2Fe2+=2Fe3++2Cl—Ca(ClO)2+H2O+ CO2=Ca CO3↓+2 HClOCa(ClO)2+2 HCl =CaCl2+2 HClO(强酸制弱酸)ClO—+2 H+=HClO2HClO2HCl+O2↑Cl2+2NaBr=2NaCl+Br2Cl2+2Br-=2Cl-+Br2Cl2 +2 K I =2 KCl+I2 Cl2 +2 I-=2 Cl-+I2Br2 +2 K I =2 K Br+I2 Br2 +2 I-=2 Br-+I24HCl(浓)+MnO2MnCl2+Cl2↑+2H2O 4H++2Cl-+MnO2Mn2++Cl2↑+2H2O HCl + AgNO3=AgCl↓(白色)+HNO3 Cl- + Ag+=AgCl↓(白色)NaBr+AgNO3=AgBr↓(浅黄色)+NaNO3 Br-+Ag+=AgBr↓(浅黄色)NaI + AgNO3=AgI↓(黄色)+ Na NO3 I- + Ag+=AgI↓(黄色)二、碱金属元素4Na+O2=2Na2O 2Na2O+ O22Na2O24Na+2O22Na2O22Na+S=Na2S(爆炸)2Na+2H2O=2NaOH+H2↑2Na+2H2O=2Na++2OH—+H2↑Na2O+H2O=2NaOH Na2O+H2O=2Na++2OH—2Na2O2+2H2O=4NaOH+O2↑2Na2O2+2H2O=4Na++4OH—+O2↑Na2O+CO2=Na2CO32Na2O2+2CO2=2Na2CO3+O2Na2CO3+2HCl=2NaCl+ H2O+ CO2↑ CO32-+2H+=H2O+ CO2↑NaHCO3+HCl=NaCl+H2O+CO2↑HCO3-+H+=H2O+CO2↑2NaHCO3Na2CO3+ H2O+ CO2↑ 2K+2H2O=2KOH+H2↑NaHCO3 + NaOH=Na2CO3 + H2O HCO3—+ OH—=CO32—+ H2ONa2CO3+ H2O+ CO2=2NaHCO3 CO32—+ H2O+ CO2 =2HCO3—2NaOH+ CO2 (少量)=Na2CO3 + H2O 2OH—+ CO2 (少量)=CO32—+ H2O NaOH+ CO2(多量)=NaHCO3OH—+ CO2(多量)=HCO3-Na2CO3+ Ca(OH)2=Ca CO3↓+2 NaOH CO32—+ Ca2+=Ca CO3↓NaOH+HCl=NaCl+H2O OH—+H+=H2OCO2+Ca(OH)2(过量)=CaCO3↓+H2O CO2+Ca2++2OH—(过量)=CaCO3↓+H2O 2CO2(过量)+Ca(OH)2===Ca(HCO3)2 OH—+ CO2(多量) =HCO3—Na2O+2HCl=2NaCl+H2O Na2O+2H+=2Na++H2O2NaCl+2H2O H2↑+Cl2↑+2NaOH2Cl—+2H2O H2↑+Cl2↑+2OH—2NaCl2Na+Cl2↑三、镁2Mg+ O22MgO Mg+Cl2 MgCl23Mg+N2Mg3N22Mg+CO22MgO+CMg+2H2O M g(O H)2+H2↑Mg+2HCl=MgCl2+H2↑Mg+2H+=Mg2++H2↑MgCl2+2NaOH=M g(O H)2↓+2NaCl Mg2++2OH—=M g(O H)2↓四、铝4Al + 3O22Al2O32Al+6HCl=2AlCl3+3H2↑2Al+6H+=2Al3++3H2↑2Al+3H2SO4=Al2(SO4)3+3H2↑ 2Al+6H+=2Al3++3H2↑2Al + 2NaOH +2H2O=2NaAlO2 + 3H2↑2Al + 2OH- +2H2O=2AlO2—+ 3H2↑Al2O3 + 6HCl=2AlCl3+ 3H2O Al2O3 + 6H+=2Al3++ 3H2OAl2O3 + 2NaOH=2NaAlO2 + H2O Al2O3 + 2OH—=2AlO2—+ H2OAl(OH)3 + 3HCl=AlCl3 + 3H2O Al(OH)3 + 3H+=Al3++ 3H2OAl(OH)3 + NaOH=NaAlO2 + 2H2O Al(OH)3 + OH—=AlO2—+ 2H2O2Al(OH)3Al2O3 + 3H2O (Fe(OH)3、Cu(OH)2类似)AlCl3 + 3NH3·H2O=Al(OH)3↓+3NH4Cl Al3++ 3NH3·H2O=Al(OH)3↓+3NH4+ NaAlO2+HCl+H2O=NaCl+Al(OH)3↓AlO2-+H++H2O=Al(OH)3↓CO2+NaAlO2+2H2O=Al(OH)3↓+Na HCO3 CO2+AlO2—+2H2O=Al(OH)3↓+HCO3—3NaAlO2+AlCl3+6H2O=4Al(OH)3↓+ 3 NaCl3AlO2—+Al3++6H2O=4Al(OH)3↓2Al +Cr2O3Al2O3+2Cr 2Al + Fe 2O3Al2O3+2 Fe4Al +3MnO22Al2O3+3Mn 2Al2O34Al+ 3O2↑五、铁Fe + S FeS 3Fe + 2O2Fe3O43Fe + 4H2O Fe3O4 + 4H2↑Fe+2HCl=FeCl2+H2↑ Fe+2H+=Fe2-+H2↑Fe+CuCl2=FeCl2+Cu Fe+Cu2+=Fe2++Cu2FeCl3+Fe=3FeCl22Fe3++Fe=3Fe2+2FeCl3+Cu=2FeCl2+CuCl2 (用于雕刻铜线路版) 2Fe3++Cu=2Fe2++Cu2+2Fe(OH)3Fe 2O3 + 3H2O2FeCl2+Cl2=2FeCl3 2Fe2++Cl2=2Fe3++2Cl—4Fe(OH)2+ 2H2O+ O2=4Fe(OH)3Fe2O3 + 6HCl =2FeCl3 + 3H2O Fe2O3 + 6H+ =2Fe3+ + 3H2OFe2O3 + 3H2SO4 =Fe2(SO4)3 + 3H2O Fe2O3 + 6H+ =2Fe3+ + 3H2O3NaOH + FeCl3 ==Fe(OH)3↓ + 3NaCl3OH—+ Fe3+=Fe(OH)3↓FeCl3+3H2O Fe(OH)3+3HCl Fe3++3H2O Fe(OH)3+3H+FeCl3+3KSCN=Fe(SCN)3+3KCl Fe3++3SCN-=Fe(SCN)3六、氧族元素H2 + S H2S 2Na + S Na2SFe + S FeS S + O2SO23O22O32H2O2 2H2O+ O2↑SO2 + H2O H2SO3SO2 + 2NaOH=Na2SO3 + H2O SO2 + 2OH—=SO32—+ H2OSO2 + Ca(OH)2=CaSO3↓+ H2O 2SO2 + O2 2 SO3Cl2 + SO2 + 2H2O=H2SO4+2HCl (Br2、I2 类似) Cl2 +SO2 +2H2O=4H++SO42-+2Cl—SO3 + H2O=H2SO4 2H2SO4(浓)+Cu CuSO4+2H2O +SO2↑2H2SO4(浓) + C CO2↑+ 2H2O + 2SO2↑2Na2SO3 + O2=2Na2SO44FeS2 + 11O22Fe2O3 + 8SO2Na2SO3+H2SO4=Na2SO4+SO2↑+H2O SO32—+2H+=SO2↑+H2ONa2SO3+ H2O +Cl2=Na2SO4 +2HCl SO32—+ H2O +Cl2=SO42- +2H++2Cl—七、碳族元素C + O2点燃CO22C + O2点燃2CO2CO + O2点燃2CO2CO+ CuO 加热Cu + CO23CO+ Fe2O3高温2Fe + 3CO22NaOH + CO2=Na2CO3 + H2O2NaOH + SO2=Na2SO3 + H2O 2NaOH + SO3=Na2SO4 + H2OCa(OH)2 + CO2=CaCO3↓+ H2O Ca(OH)2 + SO2=CaSO3↓+ H2OCO2 + H2O =H2CO3C+ H2O CO + H2 (生成水煤气) C+CO2加热2CO2C+ SiO22CO↑ + Si Si +O2SiO22F2+ Si=SiF4 Si + 4HF=SiF4↑+2H2↑Si+2NaOH+ H2O=Na2SiO3+2H2↑SiO2+2NaOH =Na2SiO3+H2OSiO2+ 4HF=SiF4+2H2O CaO+ SiO2CaSiO3SiO2 + Na2CO3Na2SiO3+ CO2SiO2 + CaCO3CaSiO3+ CO2↑八、氮族元素NH3 + H2O NH3·H2O NH4++OH-4NH3 + 5O24NO + 6H2ON2 +3Mg Mg3N2N2 + O22NO2NO + O2=2NO23NO2 + H2O =2HNO3 + NO4NO + 3O2 + 2H2O==4HNO34NO2 + O2 + 2H2O=4HNO34HNO34NO2↑+ O2↑+ 2H2O Cu+4HNO3(浓)=Cu(NO3)2 +2NO2↑+2H2O 3Cu+8HNO3(稀)=3Cu(NO3)2 +2NO↑+4H2O C+4HNO3(浓) =CO2↑+4NO2↑+2H2ONH3 + HCl=NH4Cl (白烟)。
高中化学方程式大全

高中化学方程式大全一、氧化还原反应方程式1.金属与非金属的氧化反应例如:2Na+Cl₂→2NaCl2Mg+O₂→2MgO2.金属与酸的反应例如:Zn+2HCl→ZnCl₂+H₂3.金属与水的反应例如:2Na+2H₂O→2NaOH+H₂4.非金属与氧气的反应例如:C+O₂→CO₂5.过氧化氢分解例如:2H₂O₂→2H₂O+O₂6.还原剂与氧化剂的反应例如:Cl₂+2KBr→2KCl+Br₂二、酸碱中和反应方程式1.强酸与强碱的中和反应例如:HCl+NaOH→NaCl+H₂O2.强酸与弱碱的中和反应例如:HCl+NH₄OH→NH₄Cl+H₂O3.弱酸与弱碱的中和反应例如:CH₃COOH+NH₄OH→CH₃COONH₄+H₂O三、水解反应方程式1.盐的水解例如:NaCl+H₂O→NaOH+HCl2.酸酐的水解例如:(CH₃CO)₂O+H₂O→2CH₃COOH3.酯的水解例如:CH₃COOCH₃+H₂O→CH₃COOH+CH₃OH四、氧气化反应方程式1.元素与氧气的直接反应例如:S+O₂→SO₂C+O₂→CO₂2.含氢的有机物燃烧反应例如:CH₄+2O₂→CO₂+2H₂O五、重组反应方程式1.单质重组反应例如:2Na+Cl₂→2NaClN₂+3H₂→2NH₃2.高低价金属的重组反应例如:Cu+2AgNO₃→Cu(NO₃)₂+2Ag3.过氧化物分解例如:2H₂O₂→2H₂O+O₂六、酸反应方程式1.均一催化酸解例如:2H₂O₂→2H₂O+O₂2.酸与金属氧化物反应例如:2HCl+Mg(OH)₂→MgCl₂+2H₂O七、氧化反应方程式1.金属与氧反应生成金属氧化物例如:2Na+O₂→2Na₂O2.非金属与氧反应生成非金属氧化物例如:C+O₂→CO₂八、盐酸与金属氧化物反应方程式例如:2HCl+CuO→CuCl₂+H₂O九、铜与含氧化剂的反应方程式例如:2Cu+O₂→2CuO。
高一化学必修一化学方程式大全(精选96例)

高一化学必修一化学方程式大全高一化学必修一化学方程式大全化学方程式,也称为化学反应方程式,是用化学式表示化学反应的式子。
化学方程式反映的是客观事实。
用化学式(有机化学中有机物一般用结构简式)来表示物质化学反应的式子,叫做化学方程式。
以下是小编为大家整理的高一化学必修一化学方程式大全(精选96例)相关内容,仅供参考,希望能够帮助大家!高一化学必修一化学方程式大全(精选96例)1、金属钠投到硫酸铜溶液中的化学方程式:2Na+2H2O=2NaOH+H2↑CuSO4+2NaOH=Cu(OH) 2↓+ Na2SO4 (先冒气泡再蓝色沉淀)2、金属钠与盐酸的化学方程式:2Na+2HCl=2NaCl+H2↑3、氢氧化钠方在空气中变质的化学方程式:2NaOH+CO2=Na2CO3+H2ONa2CO3+10H2O=Na2CO3·10H2O4、金属钠放在空气的氧化:4Na+O2=2Na2O (银白色变暗)5、金属钠在空气燃烧:2Na+O2=Na2O2 Δ (生成淡黄色粉末)6、过氧化钠在空气中变质:2Na2O2+2H2O=4NaOH+O2↑2Na2O2+2CO2=2Na2CO3+O27、过氧化钠与酸反应:2Na2O2+4HCl=4NaCl+2H2O+O2↑8、氧化钠在空气中变质:Na2O+H2O=2NaOHNa2O+CO2=Na2CO39、氧化钠与酸反应:Na2O+2HCl=2NaCl+H2O10、氧化钠在空气中燃烧:2Na2O+O2=2Na2O211、氯气与铁的反应方程式:2Fe+3Cl2=2FeCl3 点燃(红棕色的烟)12、氯气与铜的反应方程式:Cu+Cl2=CuCl2 点燃(棕黄色的烟)13、氯气与氢气的反应方程式:Cl2+H2=2HCl 点燃(苍白色火焰,生成白雾)14、氯气与钠单质的反应方程式:2Na+Cl2=2NaCl 点燃(淡黄色的烟)15、工业制漂白:2Cl2+2Ca(OH) 2=CaCl2+Ca(ClO) 2+2H2O (为Ca(OH) 2石灰乳)16、氯气与水的方程式:Cl2+H2O=HCl+HClO17、消毒、处理多余的氯气、制84消毒液:Cl2+2NaOH=NaClO+NaCl+H2O18、次氯酸钠在空气中变质:2NaClO+CO2+H2O=2HClO+Na2CO3NaClO+CO2+H2O=HClO+NaHCO319、漂白在空气中变质:Ca(ClO) 2+CO2+H2O=CaCO3↓+2HClO20、次氯酸见光分解:2HClO=2HCl+O2↑ 光照21、氯化铁通入沸水中制氢氧化铁胶体:FeCl3+3H2O=Fe(OH) 3 (胶体)+3HCl Δ22、碳酸钠与盐酸的反应方程式:Na2CO3+2HCl(过)=2NaCl+CO2↑+H2ONa2CO3+HCl(少)=NaHCO3+NaCl23、碳酸氢钠与盐酸的反应方程式:NaHCO3+HCl=NaCl+H2O+CO2↑24、碳酸氢钠与碱反应方程式:NaHCO3+NaOH=Na2CO3+H2ONaHCO3+Ca(OH) 2=2H2O+Na2CO3+CaCO3↓25、碳酸氢钠受热易分解:2NaHCO3=Na2CO3+CO2↑+H2O Δ26、二氧化碳通入碳酸钠溶液中:Na2CO3+CO2+H2O=2NaHCO327、浑浊石灰水变澄清:CO2+CaCO3+H2O=Ca(HCO3) 228、碳酸氢钙受热分解:Ca(HCO3) 2= CO2↑+CaCO3+H2O Δ29、氢氧化亚铁在空气中变质:4Fe(OH) 2+O2+2H2O=4Fe(OH) 3(由白色沉淀变成灰绿色再变成红褐色沉淀)30、保存氯化亚铁溶液:2FeCl3+Fe=3FeCl2 2Fe3++Fe=3Fe2+31、制造印刷线路板:2FeCl3+Cu=2FeCl2+CuCl2 2Fe3++Cu=2Fe2++Cu2+32、2FeCl2+Cl2=2FeCl3 2Fe2++Cl2=2Fe3++2Cl-33、Fe2O3+3CO = 2Fe+3CO2 高温34、Ba2++SO42+=BaSO4↓ Ag++Cl-= AgCl↓35、Zn+Cu2+= Zn2++Cu Zn+Fe2+= Zn2++Fe36、溶洞的形成:CO2+CaCO3+H2O=Ca(HCO3)2Ca(HCO3)2=CO2↑+CaCO3+H2O Δ37、NaHCO3+BaCl2 ?不反应(一般情况下,强酸才能制弱酸)38、工业上制取水煤气:C+H2O(g)=CO+H2 高温39、自然界通过放电把氮气转化为一氧化氮:N2+O22NO 放电(NO无色、难溶于水)40、工业上制备氨气:N2+3H22NH3 高温、高压、催化剂41、一氧化氮在常温下被氧化:2NO+O2=2NO2(NO2红棕色、有刺激性气味的有毒气体、易溶于水)42、工业上制取硝酸、二氧化氮溶于水生成硝酸和一氧化氮:3NO2+H2O=2HNO3+NO43、氨溶解于水:NH3+H2ONH3·H2O(一水合氨、弱碱性、能使酚酞溶液变红)44、一水合氨的电离:NH3·H2ONH4++OH-45、氨与盐酸的反应:NH3+HCl=NH4Cl46、工业上制备硝酸需要的一氧化氮的方程式:4NH3+5O2=4NO+6H2O 高温催化剂47、碳酸氢铵受热分解:NH4HCO3=NH3↑+CO2↑+H2O Δ (密封保存在阴凉处、施肥时埋在土下)48、氯化铵受热分解:NH4Cl=NH3↑+HCl↑ Δ49、铵态氮肥不能与碱(如草木灰)混合施用:NH4++OH-=NH3↑+H2O Δ50、实验室制氨气:2NH4Cl+Ca(OH)2=2NH3↑+CaCl2+2H2O Δ(向上排空气法收集、湿润的红色石蕊试纸)51、硝酸受热分解:4HNO3=4NO2↑+O2↑+2H2O 受热或见光(应保存在棕色试剂瓶中、阴凉处)52、铜与硝酸的反应:Cu +4HNO3(浓) =Cu(NO3)2+2NO2↑+2H2O (遇浓硝酸生成二氧化氮)3Cu+8HNO3(稀) =3Cu(NO3)2+2NO↑+4H2O (遇稀硝酸生成一氧化氮)53、浓硝酸与木炭的反应:4HNO3(浓)+C=CO2↑+4NO2↑+2H2O Δ54、硫单质铁的反应:Fe+S=FeS Δ(硫单质的氧化性、S黄色或淡黄色固体,不溶水、微溶酒精、易溶CS2)55、硫单质与氧气的反应:S+O2=SO2 点燃(硫单质的还原性、SO2有刺激性气味的有毒气体、易溶于水)56、硫粉遇碱发生歧化反应:3S+6NaOH=2Na2S+Na2SO3+3H2O Δ57、黑火药爆炸的化学方程式:S+2KNO3+3C=K2S+3CO2↑+N2↑58、二氧化硫被氧气氧化:2SO2+O22SO3 催化剂Δ59、二氧化硫与硫化氢发生归中反应:SO2+2H2S=3S↓+2H2O (H2S臭鸡蛋气味)60、浓硫酸与铜加热发生反应:2H2SO4(浓)+Cu=CuSO4+SO2↑+2H2O Δ61、浓硫酸与木炭加热发生反应:2H2SO4(浓)+C=2SO2↑+CO2↑+2H2O Δ62、二氧化硫能使澄清石灰水变浑浊:SO2+Ca(OH)2=CaSO3↓+H2O63、二氧化硫与氯气发生氧化还原反应:SO2+Cl2+2H2O=H2SO4+2HCl64、酸雨的形成:2SO2+O22SO3 粉尘等催化SO3+H2O=H2SO4SO2+H2OH2SO32H2SO3+O2=2H2SO465、海水提镁第一步:Mg+2H+=Mg2++H2↑ (盐酸、稀硫酸)66、镁与氮气的反应:3Mg+N2=Mg3N2 点燃67、镁与二氧化碳反应:2Mg+CO2=2MgO+C 点燃(镁着火不能用二氧化碳扑灭)68、海水提溴单质:2Br-+Cl2=Br2+2Cl-69、半导体硅与氧气的'反应:Si+O2=SiO2 Δ(自然界没有游离态的硅)70、工业上制粗硅:SiO2+2C=Si+2CO↑ 高温(光导纤维、沙子和石英的主要成分是SiO2)71、硅与氟气的反应:Si+2F2=SiF472、硅与氢氟酸的反应:Si+4HF=SiF4+2H273、制作黏合剂:Si+2NaOH+H2O=Na2SiO3+2H2↑74、玻璃与烧碱反应:SiO2+2NaOH=Na2SiO3+H2O (Na2SiO3的水溶液称为水玻璃)75、二氧化硅与碱性氧化物的反应:SiO2+CaO=CaSiO3 高温76、刻蚀玻璃:SiO2+4HF=SiF4↑+2H2O77、工业制玻璃:CaCO3+SiO2=CaSiO3+CO2↑ 高温Na2CO3+SiO2=Na2SiO3+CO2↑ 高温78、金属铝在氧气中燃烧:4Al+3O2=2Al2O3 点燃79、铝热反应:2Al+Fe2O3=Al2O3+2Fe高温(铝粉与氧化铁粉的混合物称为铝热剂,用于焊接钢轨)80、金属铝与酸的反应:2Al+6HCl=2AlCl3+3H2↑81、金属铝与碱的反应:2Al+2NaOH+6H2O=2Na[Al(OH)4]+3H2↑ (四羟基合铝酸钠)82、实验室制氢氧化铝:AlCl3+3NH3·H2O=Al(OH)3↓+3NH4Cl(白色沉淀)83、氢氧化铝溶于强酸中:Al(OH)3+3H+=Al3++3H2O84、氢氧化铝溶于强碱中:Al(OH)3+OH-=[Al(OH)4]- (四羟基合铝酸根离子)85、氧化铝溶于强酸:Al2O3+6H+=2Al3++3H2O (氧化铝为两性氧化物)86、氧化铝溶于强碱:Al2O3+2OH-+3H2O=2[Al(OH)4]-87、碱式碳酸铜的制取:2Cu+O2+H2O+CO2=Cu2(OH)2CO3 (绿色)88、铜与氧气的反应:Cu+O2=2CuO Δ89、铜与硫粉的反应:2Cu+S=Cu2S Δ90、4CuO=2Cu2O+O2↑ 高温(黑色物质变为红色物质)91、CuSO4·5H2O=CuSO4+5H2O↑ Δ (蓝色晶体变为白色粉末)92、氯化铝与少量的氢氧化钠反应:Al3++3OH-=Al(OH)3↓93、氯化铝与过量的氢氧化钠反应:Al3++4OH-=[Al(OH)4]-94、四羟基合铝酸根离子与酸的反应:[Al(OH)4]-+H+=H2O+Al(OH)3↓95、实验室制取氯气:4HCl(浓)+MnO2 =MnCl2+Cl2↑+2H2O Δ (黄绿色气体、有毒、密度比空气大)96、实验室制取二氧化碳:CaCO3+2HCl=CaCl2+H2O+CO2↑ (无色无味、密度比空气大,溶于水)。
人教版高一化学方程式大全(最新整理)

高一化学方程式总结一、钠及其化合物1、钠与氧气:常温:4Na + O2== 2Na2O 点燃:2Na + O2Na2O22、钠与水反应:2Na + 2H2O == 2NaOH + H2↑离子方程式:2Na + 2H2O == 2Na++ 2OH-+ H2↑3、钠与硫酸反应:2Na + H2SO4== Na2SO4+ H2↑4、氧化钠与水反应:Na2O+H2O == 2NaOH5、过氧化钠与二氧化碳反应:2Na2O2 + 2CO2== 2Na2CO3+ O26、过氧化钠与水反应:2Na2O2 +2H2O == 4NaOH + O2↑离子方程式:2Na2O2 +2H2O == 4Na+ + 4OH-+ O2↑7、NaOH 溶液通入少量CO2:2NaOH +CO2== Na2CO3 +H2O 离子方程式:2OH-+CO2== CO32-+H2ONaOH 溶液通入过量CO2:NaOH +CO2== NaHCO3离子方程式:OH-+CO2== HCO3-8、①向碳酸钠溶液滴入少量稀盐酸:Na2CO3+ HCl == NaHCO3 + NaCl向稀盐酸溶液滴入少量碳酸钠:Na2CO3+ 2HCl == 2NaCl +CO2↑+H2O②除去碳酸氢钠中混有的碳酸钠:Na2CO3 + CO2 + H2O == 2NaHCO3③碳酸钠与氢氧化钙:Na2CO3 +Ca(OH)2== CaCO3↓+2NaOH④碳酸氢钠与盐酸:NaHCO3 + HCl == NaCl +CO2↑+H2O⑤少量碳酸氢钠溶液滴入氢氧化钙溶液中:NaHCO3 +Ca(OH)2==NaOH+CaCO3↓+H2O少量氢氧化钙溶液滴入碳酸氢钠溶液中:2NaHCO3 +Ca(OH)2== Na2CO3 +CaCO3↓+2H2O⑥除去碳酸钠溶液中的碳酸氢钠:NaHCO3 + NaOH == Na2CO3 +H2O⑦除去碳酸钠固体中的碳酸氢钠:2NaHCO3Na2CO3 +CO2↑+H2O⑧鉴别碳酸钠和碳酸氢钠溶液:Na2CO3 +CaCl2== CaCO3↓+2NaCl二、铝及其化合物1、铝与氧气的反应:4Al + 3O22Al2O32、铝与氧化铁反应(铝热反应):2Al + Fe2O32Fe + Al2O33、铝和稀盐酸:2Al +6HCl == 2AlCl3 +3H2↑离子方程式:2Al + 6H+ ==2Al3+ +3H2↑4、铝和NaOH 溶液:2Al +2NaOH +2H2O == 2NaAlO2 +3H2↑离子方程式:2Al +2OH-+2H2O == 2AlO2-+3H2↑5、氧化铝和稀硫酸:Al2O3 +3H2SO4== Al2(SO4)3 +3H2O 离子方程式:Al2O3 + 6H+ == 2Al3+ + 3H2O6、氧化铝和NaOH 溶液:Al2O3 + 2NaOH == 2NaAlO2 +H2O 离子方程式:Al2O3 + 2OH-== 2AlO2-+ H2O7、氢氧化铝和稀盐酸:Al(OH)3 +3HCl == AlCl3 +3H2O 离子方程式:Al(OH)3 +3H+ == Al3+ + 3H2O8、氢氧化铝和NaOH 溶液:Al(OH)3 + NaOH == NaAlO2 +2H2O 离子方程式:Al(OH)3 +OH-==AlO2-+ 2H2O9、氢氧化铝受热分解:2Al(OH)3Al2O3 +3H2O10、硫酸铝与氨水反应:Al2(SO4)3 +6NH3•H2O == 2Al(OH)3↓+ 3(NH4)2SO4离子方程式:Al3+ + 3NH3•H2O == Al(OH)3↓+ 3NH4+11、AlCl3溶液中加入少量NaOH 溶液:AlCl3 + 3NaOH ==Al(OH)3↓+ 3NaClAlCl3溶液中加入过量NaOH 溶液:AlCl3 + 4NaOH == NaAlO2+ 3NaCl+ 2H2O12、往NaAlO2溶液中通入少量CO2:2NaAlO2 +CO2 + 3H2O == 2Al(OH)3↓ + Na2CO3往NaAlO2溶液中通入过量CO2:NaAlO2 +CO2 + 2H2O == Al(OH)3↓+ NaHCO313、电解氧化铝:2Al2O3(熔融)4Al+3O2↑三、铁及其化合物1、铁与氧气反应:3Fe + 2O2Fe3O4铁与硫反应:Fe + S FeS2、铁与盐酸反应:Fe + 2HCl == FeCl2 +H2↑离子方程式:Fe + 2H+ == Fe2+ +H2↑铁与CuSO4溶液:Fe +CuSO4== FeSO4 + Cu 离子方程式:Fe +Cu2+== Fe2+ + Cu3、铁和水蒸气:3Fe +4H2O(g) Fe3O4 + 4H24、氧化亚铁与盐酸反应:FeO + 2HCl == FeCl2 +H2O 离子方程式:FeO + 2H+ == Fe2+ +H2O5、氧化铁与盐酸反应:Fe2O3 + 6HCl == 2FeCl3 +3H2O 离子方程式:Fe2O3 + 6H+ == 2Fe3+ +3H2O6、CO 还原氧化铁:3CO+Fe2O33CO2 + 2Fe7、氯化铁与NaOH 溶液:FeCl3 +3NaOH == Fe(OH)3↓+3NaCl 离子方程式:Fe3+ +3OH-== Fe(OH)3↓8、硫酸亚铁与NaOH 溶液:FeSO4 + 2NaOH == Fe(OH)2↓+ Na2SO4离子方程式:Fe2+ +2OH-== Fe(OH)2↓9、氢氧化铁加热分解:2Fe(OH)3Fe2O3 +3H2O10、氢氧化亚铁被氧化为氢氧化铁:4Fe(OH)2 + O2 + 2H2O == 4Fe(OH)3(白色沉淀迅速变灰绿色,最后变为红褐色)11、除去FeCl2中的FeCl3:Fe +2FeCl3== 3FeCl2离子方程式:Fe +2Fe3+ == 3Fe2+12、FeCl2与Cl2反应:2FeCl2 + Cl2== 2FeCl3离子方程式:2Fe2+ +Cl2== 2Fe3+ +2Cl-13、FeCl3与Cu 反应:Cu +2FeCl3== 2FeCl2 +CuCl2离子方程式:Cu +2Fe3+ == 2Fe2+ +Cu2+14、氯化铁与硫氰化钾反应:FeCl3 + 3KSCN Fe(SCN)3 + 3KCl(溶液变红)四、硅及其化合物1、硅与氧气加热:Si + O2SiO2硅与氟气:Si + 2F2== SiF42、硅单质与氢氟酸:Si + 4HF == SiF4↑+2H2↑3、硅与NaOH 溶液反应:Si + 2NaOH+ H2O == Na2SiO3 + 2H2↑4、二氧化硅与氢氟酸反应:SiO2 + 4HF == SiF4↑+2H2O5、二氧化硅与氧化钙高温反应:SiO2 + CaO CaSiO36、二氧化硅与NaOH 溶液反应:SiO2 + 2NaOH == Na2SiO3 +H2O7、二氧化硅与碳反应:SiO2 + 2C 2CO + Si8、硅酸钠与与盐酸反应:Na2SiO3 + 2HCl == 2NaCl +H2SiO3↓离子方程式:SiO32-+ 2H+ ==H2SiO3↓9、往硅酸钠溶液中通入二氧化碳:Na2SiO3 + CO2 +H2O == Na2CO3 +H2SiO3↓10、二氧化硅与纯碱反应:SiO2 +Na2CO3Na2SiO3 + CO2↑11、二氧化硅与石灰石反应:SiO2 +CaCO3CaSiO3 + CO2↑12、加热硅酸:H2SiO3SiO2 +H2O五、氯及其化合物1、实验室制氯气:MnO2 +4HCl(浓) MnCl2 +Cl2↑+2H2O 离子方程式:MnO2 +4H++2Cl-Mn2+ +Cl2↑+2H2O2、钠在氯气中燃烧:2Na +Cl22NaCl(产生大量白烟)铁在氯气中燃烧:2Fe +3Cl22FeCl3(产生大量棕黄色的烟)铜在氯气中燃烧:Cu +Cl2CuCl2(产生大量棕黄色的烟)氢气在氯气中燃烧:H2 +Cl22HCl(苍白色火焰,瓶口出现白雾)3、氯气和水反应:Cl2 + H2O HCl + HClO 离子方程式:Cl2 + H2O H++Cl-+ HClO4、次氯酸光照分解:2HClO 2HCl+O2↑5、氯水中通入SO2:Cl2 +SO2 +2H2O==2HCl+H2SO4离子方程式:Cl2 +SO2 +2H2O==4H++2Cl-+SO42-6、氯气与NaOH 溶液:Cl2+2NaOH ==NaCl +NaClO +H2O 离子方程式:Cl2+2OH-==Cl-+ClO-+H2O7、工业生产漂白粉:2Cl2+2Ca(OH)2==CaCl2+Ca(ClO)2+2H2O8、漂白粉漂白原理:Ca(ClO)2+CO2+H2O==CaCO3↓+2HClO9、向漂白粉溶液中加入稀盐酸:Ca(ClO)2+2HCl==CaCl2+2HClO10、氯气通入溴化钾溶液:Cl2 + 2KBr ==2KCl +Br2离子方程式:Cl2 + 2Br-==2Cl-+Br2氯气通入碘化钾溶液:Cl2 + 2KI ==2KCl +I2离子方程式:Cl2 + 2I-==2Cl-+I2溴水和碘化钾溶液:Br2 + 2KI ==2KBr +I2离子方程式:Br2 + 2I-==2Br-+I211、氯化钠和硝酸银溶液:NaCl +AgNO3==AgCl ↓+NaNO3离子方程式:Cl-+Ag+==AgCl ↓六、硫及其化合物1、硫在空气中燃烧:S + O2SO2硫与氢气加热:H2 + S H2S2、二氧化硫与水:SO2 + H2O H2SO3二氧化硫与氧化钙:SO2 +CaO ==CaSO3少量SO2与NaOH 溶液:SO2+2NaOH==Na2SO3 +H2O 离子方程式:SO2+2OH-==SO32-+H2O过量SO2与NaOH 溶液:SO2+NaOH==NaHSO3离子方程式:SO2+OH-==HSO3-3、SO2通入过量的澄清石灰水:SO2+Ca(OH)2==CaSO3↓+H2O 离子方程式:SO2+Ca2++2OH-==CaSO3↓+H2O3 4 过量的 SO 2 通入澄清石灰水:2SO 2+Ca(OH)2 ==Ca(HSO 3)2 离子方程式:SO 2+OH -==HSO -4、二氧化硫与硫化氢:SO 2 + 2H 2S == 3S↓+ 2H 2O5、二氧化硫催化氧化:2SO 2+O 22SO 36、亚硫酸钠和硫酸反应:Na 2SO 3 +H 2SO 4 == Na 2SO 4+SO 2↑+H 2O7、Na 2SO 3 与氧气反应: 2Na 2SO 3+O 2==2Na 2SO 48、三氧化硫与水反应:SO 3 + H 2O ==H 2SO 49、三氧化硫与氧化钙:SO 3 +CaO ==CaSO 410、三氧化硫与氢氧化钙:SO 3 +Ca(OH)2==CaSO 4↓+H 2O 11、铜与浓硫酸反应:Cu +2H 2SO 4(浓) CuSO 4+SO 2↑+2H 2O 12、碳与浓硫酸反应:C +2H 2SO 4(浓) CO 2↑+2SO 2↑+2H 2O13、SO 2+H 2O 2=H 2SO 2七、氮及其化合物1、氮气和氧气反应:N 2+O 22NO2、工业合成氨:N 2+3H 22NH 33、一氧化氮与氧气反应:2NO+O 2==2NO 24、NO 2 溶于水:3NO 2+H 2O ==2H NO 3+NO5、氨气溶于水:NH 3+H 2O NH 3•H 2O 氨水显弱碱性(电离方程式):NH 3•H 2O NH ++OH -6、浓氨水受热分解:NH 3•H 2ONH 3↑+H 2O7、氨气和氯化氢:NH 3+HCl ==NH 4Cl (产生白烟)8、氨的催化氧化:4NH 3+5O 2 4NO+6H 2O 9、氯化铵受热分解:NH 4ClNH 3↑+HCl ↑10、碳酸氢铵受热分解:NH 4HCO 3NH 3↑+CO 2↑+H 2O11、硝酸铵和 NaOH :NH 4NO 3+NaOH NaNO 3+NH 3↑+H 2O 离子方程式:NH 4++OH - NH 3↑+H 2O12、实验室制氨气:2NH 4Cl+Ca(OH)2CaCl 2+2NH 3↑+2H 2O13、浓硝酸与铜反应:Cu +4HNO 3==Cu(NO 3)2+2NO 2↑+2H 2O 离子方程式:Cu +4H ++2NO 3-==Cu 2++2NO 2↑+2H 2O 14、稀硝酸与铜反应:3Cu +8HNO 3==3Cu(NO 3)2+2NO ↑+4H 2O离子方程式:3Cu +8H ++2NO 3-==3Cu 2++2NO ↑+4H 2O15、硝酸见光分解:4HNO 34NO 2↑+O 2↑+2H 2O16、NH 4+检验的离子方程式:NH 4++OH -NH 3↑+H 2O17、NO 2、O 2 混合气通入水中无剩余气体:4NO 2+O 2+2H 2O ==4HNO 318、NO、O2混合气通入水中无剩余气体:4NO+3O2+2H2O==4HNO319、少量氨气与氯气2NH3+3Cl2= N2+6HCl20、过量氨气与氯气8NH3+3Cl2= N2+6NH4Cl“”“”At the end, Xiao Bian gives you a passage. Minand once said, "people who learn to learn are very happy people.". In every wonderful life, learning is an eternal theme. As a professional clerical and teaching position, I understand the importance of continuous learning, "life is diligent, nothing can be gained", only continuous learning can achieve better self. Only by constantly learning and mastering the latest relevant knowledge, can employees from all walks of life keep up with the pace of enterprise development and innovate to meet the needs of the market. This document is also edited by my studio professionals, there may be errors in the document, if there are errors, please correct, thank you!。
最新高一化学方程式汇总

高一化学方程式必修一1、硫酸根离子的检验:BaCl 2 + Na z SO ==== BaSOd + 2NaCl2、碳酸根离子的检验:CaCl2 + Na z CO ===== CaCO J + 2NaCl3、碳酸钠与盐酸反应:Na2CO + 2HCl ===== 2NaCl + H 2O + COd△4、木炭还原氧化铜:2CuO + C = 2Cu + CO2 T5、铁片与硫酸铜溶液反应:Fe + CuSO 4 ===== FeSQ + Cu6 、氯化钙与碳酸钠溶液反应:CaCl2 + Na2CO===== CaCO J + 2NaCl.... ..... ._ △ _7、钠在空气中燃烧:2Na + O2 = Na2Q钠与氧气反应:4Na + O2 ==== 2Na2。
8、过氧化钠与水反应:2NaQ + 2H 2O ==== 4NaOH + Of9、过氧化钠与二氧化碳反应:2NaO + 2CO2 ==== 2Na2CO + O210、钠与水反应:2Na + 2H2O ==== 2NaOH +11、铁与水蒸气反应:3Fe + 4H 2O(g) ==== Fe 3Q + 4H 2 T12、铝与氢氧化钠溶液反应:2Al+ 2NaOH + 2H2O == 2NaAlO2 + 3H 2 T13、氧化钙与水反应:CaO + H2O ==== Ca(OH)214、氧化铁与盐酸反应:FeQ + 6HCl ===== 2FeCl 3 + 3H2O15、氧化铝与盐酸反应:Al2Q + 6HCl ===== 2AlCl 3 + 3H2O16、氧化铝与氢氧化钠溶液反应:Al2Q + 2NaOH ===== 2NaAlQ + H 2O17、氯化铁与氢氧化钠溶液反应:FeCl a + 3NaOH ===== Fe(OH)3 J + 3NaCl18、硫酸亚铁与氢氧化钠反应:FeSO + 2NaOH ==== Fe(OH)2 J + Na2SO19、氢氧化亚铁被氧化成氢氧化铁:4Fe(OH)2 + 2H 2O + O2 == 4Fe(OH) 3△20、氢氧化铁加热分解:2Fe(OH>= Fe?。
(完整版)高一化学必背的化学方程式

1、钠在空气中燃烧:2Na + O2 == Na2O22、钠与氧气常温下反应:4Na + O2 == 2Na2O3、钠与水反应:2Na + 2H2O == 2NaOH + H2↑4、铁片与硫酸铜溶液反应: Fe + CuSO4 == FeSO4 + Cu5、铁与水蒸气反应:3Fe + 4H2O(g) == Fe3O4 + 4H2↑6、铝与氢氧化钠溶液反应:2Al + 2NaOH + 2H2O == 2NaAlO2 + 3H2↑7、铝和盐酸溶液:2Al +6HCl==2AlCl3+3H2↑8、过氧化钠与水反应:2Na2O2 + 2H2O == 4NaOH + O2↑9、过氧化钠与二氧化碳反应:2Na2O2 + 2CO2 == 2Na2CO3 + O210、碳酸钠溶液与盐酸第一步:Na2CO3 +HCl(少)= =NaCl +NaHCO3第二步:NaHCO3 +HCl = = NaCl+ H2O+CO2↑11、碳酸氢钠受热分解:2NaHCO3==Na2CO3+ H2O+CO2↑12、氧化铝与盐酸反应:Al2O3 + 6HCl = =2AlCl3 + 3H2O13、氧化铝与氢氧化钠溶液反应:Al2O3 + 2NaOH == 2NaAlO2 + H2O14、实验室制取氢氧化铝:Al2(SO4)3 + 6NH3·H2O == 2Al(OH)3↓ + 3(NH3)2SO415、氢氧化铝与盐酸反应:Al(OH)3 + 3HCl == AlCl3 + 3H2O16、氢氧化铝与氢氧化钠溶液反应:Al(OH)3 + NaOH == NaAlO2 + 2H2O17、氢氧化铝加热分解:2Al(OH)3 == Al2O3 + 3H2O18、氧化铁与盐酸反应:Fe2O3 + 6HCl == 2FeCl3 + 3H2O19、氯化铁与氢氧化钠溶液反应:FeCl3 + 3NaOH == Fe(OH)3↓+ 3NaCl (制备氢氧化铁)20、硫酸亚铁与氢氧化钠溶液反应:FeSO4 + 2NaOH == Fe(OH)2↓+ Na2SO4(制备氢氧化亚铁)21、氢氧化亚铁被氧化成氢氧化铁:4Fe(OH)2 + 2H2O + O2 == 4Fe(OH)3现象:白色沉淀迅速变为灰绿色,最后变为红褐色。
高一化学所有化学方程式

高一化学所有化学方程式一、金属及其化合物1、钠及其化合物钠在空气中燃烧:2Na + O₂= Na₂O₂钠与水反应:2Na + 2H₂O = 2NaOH + H₂↑过氧化钠与水反应:2Na₂O₂+ 2H₂O = 4NaOH + O₂↑过氧化钠与二氧化碳反应:2Na₂O₂+ 2CO₂= 2Na₂CO₃+O₂碳酸钠与盐酸反应:Na₂CO₃+ 2HCl = 2NaCl + H₂O + CO₂↑碳酸氢钠与盐酸反应:NaHCO₃+ HCl = NaCl + H₂O + CO₂↑碳酸氢钠受热分解:2NaHCO₃= Na₂CO₃+ H₂O + CO₂↑2、铝及其化合物铝与氧气反应:4Al + 3O₂= 2Al₂O₃铝与盐酸反应:2Al + 6HCl = 2AlCl₃+ 3H₂↑铝与氢氧化钠溶液反应:2Al + 2NaOH + 2H₂O = 2NaAlO₂+3H₂↑氧化铝与盐酸反应:Al₂O₃+ 6HCl = 2AlCl₃+ 3H₂O氧化铝与氢氧化钠溶液反应:Al₂O₃+ 2NaOH = 2NaAlO₂+H₂O氢氧化铝与盐酸反应:Al(OH)₃+ 3HCl = AlCl₃+ 3H₂O氢氧化铝与氢氧化钠溶液反应:Al(OH)₃+ NaOH = NaAlO₂+2H₂O3、铁及其化合物铁与氧气反应:3Fe + 2O₂= Fe₃O₄铁与盐酸反应:Fe + 2HCl = FeCl₂+ H₂↑铁与硫酸铜溶液反应:Fe + CuSO₄= FeSO₄+ Cu氧化亚铁与盐酸反应:FeO + 2HCl = FeCl₂+ H₂O氧化铁与盐酸反应:Fe₂O₃+ 6HCl = 2FeCl₃+ 3H₂O四氧化三铁与盐酸反应:Fe₃O₄+ 8HCl = FeCl₂+ 2FeCl₃+4H₂O氯化亚铁与氯气反应:2FeCl₂+ Cl₂= 2FeCl₃氯化铁与铁粉反应:2FeCl₃+ Fe = 3FeCl₂二、非金属及其化合物1、硅及其化合物硅与氧气反应:Si + O₂= SiO₂硅与氢氟酸反应:Si + 4HF = SiF₄↑ + 2H₂↑二氧化硅与氢氟酸反应:SiO₂+ 4HF = SiF₄↑ + 2H₂O二氧化硅与氢氧化钠溶液反应:SiO₂+ 2NaOH = Na₂SiO₃+H₂O硅酸钠溶液与盐酸反应:Na₂SiO₃+ 2HCl = 2NaCl + H₂SiO₃↓2、氯及其化合物氯气与金属钠反应:2Na + Cl₂= 2NaCl氯气与金属铁反应:2Fe + 3Cl₂= 2FeCl₃氯气与氢气反应:H₂+ Cl₂= 2HCl氯气与水反应:Cl₂+ H₂O = HCl + HClO次氯酸光照分解:2HClO = 2HCl + O₂↑氯气与氢氧化钠溶液反应:Cl₂+ 2NaOH = NaCl + NaClO +H₂O氯离子的检验:Ag⁺+ Cl⁻=AgCl↓3、硫及其化合物硫在氧气中燃烧:S + O₂= SO₂二氧化硫与水反应:SO₂+ H₂O = H₂SO₃二氧化硫与氧气反应:2SO₂+ O₂= 2SO₃三氧化硫与水反应:SO₃+ H₂O = H₂SO₄铜与浓硫酸反应:Cu + 2H₂SO₄(浓) = CuSO₄+ SO₂↑ +2H₂O碳与浓硫酸反应:C + 2H₂SO₄(浓) = CO₂↑ + 2SO₂↑ + 2H₂O4、氮及其化合物氮气与氧气反应:N₂+ O₂= 2NO一氧化氮与氧气反应:2NO + O₂= 2NO₂二氧化氮与水反应:3NO₂+ H₂O = 2HNO₃+ NO氨气与水反应:NH₃+ H₂O = NH₃·H₂O氨气与盐酸反应:NH₃+ HCl = NH₄Cl氯化铵受热分解:NH₄Cl = NH₃↑ +HCl↑碳酸氢铵受热分解:NH₄HCO₃= NH₃↑ + H₂O↑ + CO₂↑硝酸铵与氢氧化钠反应:NH₄NO₃+ NaOH = NH₃↑ + NaNO₃+ H₂O。
高一化学方程式汇总

高一化学方程式汇总一、 Na 及其化合物㈠Na 单质4Na+O 2===2Na2O(白色)2Na O+ O2Na O (淡黄色)2224Na+2O 22Na2O2(淡黄色)2Na+S===Na 2S(爆炸)2Na+2H 2O===2NaOH+H 2↑㈡氧化物1、 Na2O+H 2O===2NaOH2Na2 O2+2H 2O===4NaOH+O2↑ 2、 Na2O+CO 2===Na 2CO 32Na2O2+2CO 2===2Na 2CO3+O2 3、 Na2O+2HCl===2NaCl2Na2O2+4HCl===4NaCl + O 2↑㈢盐1、 Na2CO 3+2HCl===2NaCl+H 2O+CO 2↑NaHCO 3+HCl===NaCl+H 2O+CO 2↑2、 Na2CO 3+ Ca(OH) 2=Ca CO 3↓+2 NaOHNaHCO 3 + NaOH== Na 2CO 3 + H 2O2NaHCO 3 + Ca(OH) 2(少许) = Ca CO 3↓+2 H2O+ Na2CO 3NaHCO 3 + Ca(OH) 2(多量) = Ca CO3↓+ H 2O+ NaOH互相转变:固体: 2NaHCO 3Na2CO 3+ H 2O+ CO 2↑溶液: NaHCO 3 + NaOH== Na 2CO 3 + H2O Na2CO 3+ H 2O+ CO 2 = 2NaHCO 3㈣碱与酸性氧化物反响1、 2NaOH+ CO 2 (少许 )== Na 2CO 3 +H2O Na2CO 3+ H 2O+ CO 2 = 2NaHCO3 NaOH+ CO 2(多量) == NaHCO 32、2NaOH+SO 2(少许) ===Na2SO3+H 2ONa2 SO3+SO2+H 2O=== 2NaHSO 3NaOH+SO 2(足量) ===NaHSO 33、CO 2+Ca(OH) 2(过度 )===CaCO 3↓+H 2OCaCO 3+ CO2+H 2O===Ca(HCO 3)22CO 2(过度 )+Ca(OH) 2===Ca(HCO 3)24、SO2+Ca(OH) 2(过度 )===CaSO3↓+H 2OCaSO3+ SO2+H 2O===Ca(HSO 3 )22SO2(过度 )+Ca(OH) 2===Ca(HSO 3)2二、镁1、在空气中焚烧2Mg+O 22MgO2Mg+CO 22MgO+C3Mg+N 2Mg 3N22、其余△2Mg(OH) 2+H 2↑Mg +2H O电解Mg + Cl 2↑MgCl 2三、氯气㈠、单质Cl 2+Cu Cu Cl 2(棕色的烟)3Cl 2+2Fe2FeCl 3(棕黄色的烟)Cl 2+2 Na === 2Na Cl (黄色火焰,白色的烟)Cl 2+ H22HCl (苍白色火焰,瓶口有白3Cl2+2P2PCl35Cl 2+2PCl 32PCl 5(现象:白色烟雾, PCl 3为雾, PCl 5为烟)Cl 2+H 2O HCl+HClOCl 2 +2NaOH===NaCl+NaClO+H2O—尾气汲取2Cl 2 +2Ca(OH) 2===CaCl 2 +Ca(ClO) 2+2H 2O——工业制漂白粉Cl 2 +2FeCl2===2FeCl 3㈡、漂白粉的使用Ca(ClO) 2+H 2O+ CO 2(少许)== Ca CO 3↓+2 HClO Ca(ClO) 2+2H 2O+ 2CO 2(多量) == Ca(HCO 3)2+2 HClOCa(ClO) 2+2 HCl == CaCl 2+2HClO (强酸制弱酸)㈢、氯水变质Cl 2 +H 2O HCl+HClO2HClO2HCl+O 2↑㈣、氯气的制法1、实验室制法:4HCl( 浓 )+MnO 2 MnCl 2+Cl 2↑+2H 2O 2、工业制法2NaCl +2H 2O 电解2NaOH + H 2↑+ Cl 2↑㈤、卤素其余性质1、F2+ H2 === 2HFBr 2 + H2 === 2HBr(500 o C)I 2+ H22HI2、 2F2 +2H2O===4HF+O 2Cl2+H O HCl+HClO 2Br 2+H 2O HBr +HBrOI+HO HI +HIO223、互相置换Cl 2+2NaBr===2NaCl+Br 2Cl 2 +2KI ===2KCl+I2Br 2 +2KI ===2KBr+I24、 HCl + AgNO 3 =AgCl ↓(白色) +HNO 3NaBr+AgNO 3 = AgBr ↓(浅黄色) +NaNO3 NaI + AgNO 3 === AgI ↓(黄色 )+ Na NO 32AgBr2Ag+Br 2(AgCl 、AgI 近似 )四、硫及其化合物㈠、S单质H2+S△2Na + S△H 2S Na2SFe + S△2Cu + S△FeS Cu 2SS+O2点燃SO2㈡、 SO21、SO2 + H2O H2SO3SO2 + 2NaOH=Na 2SO3 + H2ONa2SO3 + H2 O+ SO2 =2NaHSO3SO + Ca(OH)2= CaSO ↓+ H O232CaSO3+SO2 +H2O===Ca ( HSO 3)2SO + CaO ===CaSO32SO + Na2O2=== Na S O422SO2(少许 )+2NH 3+H 2O===(NH 4)2SO3SO +(NH4)SO+H O===2NH HSO322324即 : SO2(足量 )+ NH 3·H 2O===NH 4HSO3 2、2SO + O22 SO23SO3+ H2O = H2SO42Na2SO3 + O2 =2Na2SO4Cl2+SO +2H2O=H SO +2HCl (Br2、I2近似 ) 2243、 SO2+2H 2S===3S↓+2H 2O㈢、H2SO41、 2H2SO4(浓 )+Cu CuSO4+2H2O +SO2↑2H2SO(浓)+C CO ↑+2H O+2SO ↑4222 2、 2NaCl+H 2SO4(浓 )Na2SO4+2HClFeS+ H2SO4=H2S↑+FeSO4Na2SO3+H 2SO4=Na2SO4+SO2 +H 2O3、硫酸的工业制法4FeS 2 + 11O 22Fe 2O 3 + 8SO 22SO 2 + O 2 2 SO 3 SO + H O=H SO32 2 4五、碳和硅点燃 CO 21、C + O 2点燃2CO2C+O 2点燃2CO + O 22CO 2加热2COC+CO 2C+ 2CuO高温2Cu + CO 2↑ 3C+ 2Fe O 高温4Fe + 3CO ↑322C+ H 2O(g)CO + H 2 (生成水煤气 ) 2、 CO+ CuO 加热Cu + CO 23CO+ Fe 2O 3 高温2Fe + 3CO 2CO 2 + H 2O H 2CO 33、硅的提炼2C+ SiO 22CO ↑+ Si (粗)Si (粗) + 2Cl 2 SiCl 4SiCl 4 + 2H 2Si (精) + 4HCl4、 Si +O 2 SiO 22F + Si== SiF 42Si + 4HF== SiF 4↑ +2H ↑Si+2NaOH+ H 2O= Na 2SiO 3+2H 2↑ 5、 SiO +2NaOH ===Na SiO +H 2 O223SiO 2+ 4HF ===SiF 4+2H 2 O CaO+ SiO 2CaSiO3SiO 2 + Na 2CO 3 Na 2SiO 3+ CO 2 SiO 2+ CaCO3 CaSiO + CO ↑326、Na 2SiO 3 + 2HCl==2NaCl+ H 2SiO 3↓Na 2SiO 3 +H 2O +CO 2== Na 2CO 3 + H 2 SiO 3↓六、氮及其化合物㈠、 N 2 及氧化物1、N 2 +3H 22NH 3N 2 + 3MgMg 3N 2 N 2 + O 22NO2、2NO + O 2== 2NO 23NO 2+ H O ==2HNO 3+ NO24NO + 3O 2 + 2H 2O==4HNO 34NO 2 + O 2 + 2H 2O ==4HNO 3 2NO 2N 2O 4㈡、氨气与铵盐3 23 · 2+-NH NH ONH 4 +OH+ H OH4NH 3 + 5O 2 4NO + 6H 2O NH Cl NH +HCl43NH HCO3NH ↑+ H O+CO ↑4322NH 3 + HCl==NH 4Cl ( 白烟 ) NaOH+ NH 4Cl NaCl+NH ↑+H2O32NH 4Cl + Ca(OH) 2CaCl 2 + 2NH 3↑+2H 2O——实验室制氨气NH 4++ OH —NH 32↑+H O㈢、硝酸4HNO 34NO 2↑+ O 2↑+ 2H 2OCu+4HNO 3(浓 )== Cu(NO 3)2 +2NO 2↑+2H 2 O 3Cu+8HNO (稀 )===3Cu(NO 3 ) +2NO ↑+4H O3 2 2C+4HNO 3(浓 ) ==CO 2↑+4NO 2↑+2H 2O8HNO 3(稀)+3Fe (过度) ==3Fe(NO 3)2+2NO ↑ +4H 2O4HNO 3(稀)+Fe (不足) ===Fe(NO 3)3+NO ↑ +2H 2O七、几种常有的金属㈠、铝及其化合物 1、单质 4Al + 3O 22Al2O 32Al+6HCl===2AlCl3+3H 2↑2Al+3H 2SO 4===Al 2(SO 4)3+3H 2↑2Al + 2NaOH +2H 2O==2Na[Al(OH) 4 ]+ 3H 2↑铝热反响:2Al +Cr 2O3Al 2 O +2Cr32Al + Fe 2O 3 Al 2O 3+2 Fe 4Al +3MnO22Al 2O +3Mn32、氧化物Al O 3 + 6HCl==2AlCl 3 +3H O22Al 2 O 3 + 2NaOH + 3H 2O==2 Na[Al(OH) 4 ]2Al电解 4Al + 3O 2↑2 O 33、氢氧化铝Al(OH) 3 + 3HCl==AlCl 3 + 3H 2OAl(OH) 3 + NaOH== Na[Al(OH)4 ]2Al(OH) 3Al 2O 3 + 3H 2O ( Fe(OH) 3 、Cu(OH) 2 近似)4、 Al 3+盐AlCl 3 +3 NaOH( 少许 )== Al(OH) 3 ↓+ 3 NaCl AlCl 3+4NaOH( 过度 )==Na[Al(OH) 4 ] +3NaCl AlCl 3 + 3NH 3·H 2O=Al(OH) 3↓+3NH 4Cl5、 [Al(OH) 4 ] -盐Na[Al(OH) 4 ] +HCl =NaCl+Al(OH) 3↓+ H 2ONa[Al(OH) 4 ] +4HCl = AlCl 3 + NaCl + 4H 2O 2Na[Al(OH) ]+CO 2(少) =2Al(OH) ↓+Na CO +4 3 2 3H 2 ONa[Al(OH) 4]+CO 2(多) =Al(OH) 3↓+NaHCO 3㈡、铁及其化合物 1、单质Fe + SFeS3Fe + 2O 2Fe 3O 42Fe +3Cl 2 2FeCl 3 3Fe + 4H O Fe O + 4H 2↑2 3 4Fe+2HCl===FeCl 2+H 2↑Fe+CuCl 2===FeCl2+Cu 2、Fe3+、Fe 2+的查验颜色: Fe 3+——棕黄色 Fe 2+——浅绿色KSCN 法: FeCl 3 +3KSCN=Fe(SCN) 3 + 3KCl血红色NaOH 法:Fe 3++ 3OH —= Fe(OH) 3↓— `红褐色 Fe 2+ + 2OH — = Fe(OH) 2↓快速现象:白色↓灰绿色↓ 红褐色↓4Fe(OH) 2+ 2H 2O+ O 2 ==4Fe(OH)3 3、Fe3+、Fe 2+的转变① Fe 2+Fe 3+4Fe(OH) 2+ 2H 2O+ O 2 ==4Fe(OH)3 2FeCl 2+Cl 2===2FeCl 32Fe 2+ + H 2O 2 + 2H + == 2Fe 3+ + H 2O4Fe 2++ O 2+ 4H +==4Fe 3++ 2H 2O② Fe 3+Fe 2+2FeCl 3+Fe===3FeCl 22FeCl 3+Cu===2FeCl 2+CuCl 2 (用于雕琢铜线路版 )4、其余Fe 2O 3 + 6HCl === 2FeCl 3 + 3H 2OFe 2O 3 + 3H 2SO 4 === Fe 2(SO 4)3 + 3H 2OFeCl +3H 2O Fe(OH) (胶体 ) +3HCl3 3。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
28.四氧化三铁和盐酸的反应 :Fe3O4+8HCl=== FeCl 2+2FeCl3+ 4H2O Fe3O4+8H +=== Fe2++2Fe3++4H 2O
29.二氧化硅与氢氟酸反应 :SiO2 + 4HF === SiF 4↑+ 2H2O(用于玻璃 雕刻 )
30.二氧化硅与氢氧化钠反应 :SiO2 +2NaOH ===Na2SiO3 + H2O
点燃
21. 铁在空气中燃烧: 3Fe+2O2
Fe3O4
22.氢氧化铁胶体的制备:
△
FeCl3+3H2O(沸 )
Fe(OH)3(胶体) +3HCl
Fe3++3H2O(沸 )
△
Fe(OH)3(胶体) +3H+
△
23.氢氧化铁受热分解: 2Fe(OH)3
Fe2O3+3H 2O
24.用氯化铁溶液腐蚀印刷线路板:
江苏省高一化学方程式汇总
1.常温下,钠被空气氧化: 4Na+O2 === 2Na2O
△
2.加热下,钠被空气氧化: 2Na+O2
Na2O2
3.钠 和 水 的 反 应 : 2Na+2H2O === 2NaOH+H2↑
===2Na++2OH -+H 2↑
2Na+2H2O
4.钠 投 入 硫 酸 铜 溶 液 中 : 2Na+2H2O === 2NaOH+H2↑ CuSO4+
12.氧 化 铝 溶 于 氢 氧 化 钠 : Al 2O3+2NaOH === 2NaAlO 2+ H2O
Al 2O3+2OH- === 2AlO 2-+ H2O
13. AlCl 3 溶液中滴入过量的氨水白色沉淀不溶解: 3NH3·H2O+AlCl 3 =Al(OH) 3↓ +3NH4Cl
Al 3++3NH3·H2O ===3NH 4++2Al(OH) 3↓
38.SO2 溶于水: SO2+H2O H2SO3 39.SO2 的尾气吸收: SO2+2NaOH= Na2SO3+H2O
SO2+2OH -= SO32-
+H 2O
40.向氢氧化钠溶液中通过量的二氧化硫: SO2+NaOH=NaHSO3
SO2+OH-= HSO3-
41.SO2 的催化氧化: 2SO2+O2
H2O +2CO2
SO2+2HCO3-=SO32-+ H2O
+2CO2
46.Na2SO3 和 BaCl2 反应: Na2SO3+BaCl2=BaSO3↓ +2NaCl SO32-
+Ba2+=== BaSO3↓ 47.Na2SO3 和 HCl 反应 :Na2SO3+2HCl = 2NaCl+H 2O+SO2↑ SO32+2H+= H2O+SO2↑
SiO2 +2OH- ===SiO32- + H2O
高温
31.二氧化硅和氧化钙的反应: SiO2 +CaO
CaSiO3
32.硅酸钠溶液中通二氧化碳: Na2SiO3 + CO2+H2O===H 2SiO3(胶
体) +Na2CO3
SiO32- + CO2+H2O===H 2SiO3(胶体)
+
CO
23
32.制取漂白粉(氯气通入石灰浆) :2Cl2 + 2Ca(OH) 2 ===CaCl2 #43; 2H 2O ===
4H++SO42-+2Cl-
△
37.实验室制氯气 :MnO2 + 4HCl( 浓)
MnCl 2 + Cl2↑+ 2H2O
MnO2 + 4H++2Cl- △ Mn 2++ Cl2↑+ 2H2O
检验 —— 能使湿润淀粉碘化钾试纸变蓝
除杂质 —— 先通入饱和食盐水 (除 HCl) , 再通入浓 H2SO4(除水蒸气 ) 收集 —— 排饱和食盐水法或向上排气法
Cu
+4H+
+2NO
3
=Cu2+
+2NO
2↑
+2H2O
68. 铜和稀硝酸反应: 3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑ +4H2O 3Cu +8H+ +2NO3-= 3Cu2++2NO↑ +4H2O
69. 非金属单质 C 和浓硝酸反应: C+4HNO3(浓)
4NO2↑ +CO2↑ +2H2O
14. 氢 氧 化 铝 溶 于 盐 酸 : Al(OH) 3+3HCl===AlCl 3+3H2O Al(OH) 3+3H+=== Al 3+ +3H2O
15.氢 氧 化 铝 溶 于 氢 氧 化 钠 : Al(OH) 3+ NaOH=== NaAlO 2+ 2H2O
Al(OH)
3+
OH -
===
AlO
19.硫酸亚铁中滴加氢氧化钠:
FeSO4+2NaOH===Fe(OH) 2+Na2SO4
4Fe(OH)2+O2+2H2O===4Fe(OH)3
Fe2++2OH- === Fe(OH)2↓
现象:产生白色沉淀,迅速变成灰绿色,最终变成红褐色。
高温
20.铁和水蒸气反应: 3Fe+4H2O(g)===Fe3O4+H2
2SO3
42.SO3 溶于水: SO3+H2O= H2SO4
43.亚硫酸变质: 2H2SO3+O2=2H2SO4 44.Na2SO3 溶液变质: 2Na2SO3+O2=2Na2SO4 2SO32-+ O2= 2SO42-
45.除 CO2 中 SO2 用饱和的 NaHCO3 溶液: SO2+2NaHCO3=Na2SO3+
2FeCl3 +Cu===CuCl 2 +2FeCl2
2Fe3++Cu=== 2Fe2++ Cu2+
25.氯化亚铁溶液中滴加新制氯水: 2FeCl2+ Cl 2===2FeCl3 2Fe2++ Cl 2=== 2Fe3++2Cl26.氯化铁溶液中加入过量铁粉: 2FeCl3+Fe===3 FeCl2 2Fe3++ Fe===3Fe2+ 27.氯化铁溶液中滴加硫氰化钾: Fe3++3SCN-=== Fe(SCN)3
2R+2H 2O=2R++2OH-+H 2↑
72.卤素单质间的置换反应:
Cl2+2KI=I 2+2KCl
Cl2+2KBr=Br 2+2KCl
Br 2+2KI=I 2+2KBr
Cl2+2I -=I2+2Cl-
Cl2+2Br-=Br2+2Cl -
Br 2+2I -
=I 2+2Br-
73.4NO+3O2+2H2O=4HNO 3
51. NH3 和 HNO 3 的反应: NH3 + HNO3=NH4NO3
52.S 和 Fe 反应: S+ Fe FeS
53.S 和 Cu 反应: S+ 2Cu Cu2S
54.工业合成氨: N2 + 3 H2
放电 /高温
55.大自然固氮: N2 + O2
催化剂 高温高压
2NH3
2NO
56.NO 易被空气氧化: NO+O2=2NO2 (红棕色气体 )
9. 碳 酸 钠 溶 液 中 通 二 氧 化 碳 : Na2CO3+ H2O+ CO2 ===2NaHCO3
CO32-+
H 2O+
CO2
===2HCO
3
10.碳酸氢钠和氢氧化钠溶液混合 :NaHCO3+ NaOH === Na 2CO3+ H2O HCO 3-+ OH-== CO32-+ H2O 11.氧 化 铝 溶 于 盐 酸 : Al 2O3+6HCl === 2AlCl 3+ 3H2O Al 2O3+6H+ === 2Al 3++ 3H2O
CaCO3↓+ 2HClO
点燃
35.铁和氯气反应: 3Cl2+2Fe
2HClO=== 2HCl + O 2↑
2FeCl3
点燃
Cu+ Cl 2
CuCl 2
氯气与可变价态的金属反应生成高价态的金属氯化物
36.Cl2 与 SO2 等物质的量同时作用物质时 ,不具有漂白性 :
Cl 2 + SO2 + 2H 2O === H 2SO4 + 2HCl
C+4H
++4NO
3
4NO2↑ +CO2↑ +2H2O
70.金属的冶炼: 2HgO 2Hg+O2 2Al 2O3 电解4Al+3O 2
MgCl 2
Mg+ Cl 2
