高中基础有机化学方程式汇总
有机化学方程式(70个)

有机化学基础反应方程式汇总1. 甲烷(烷烃通式:C n H 2n +2)甲烷的制取:CH 3CaO △2CO 3+CH 4↑(1)氧化反应甲烷的燃烧:CH 4+2O 2 点燃CO 2+2H 2O甲烷不可使酸性高锰酸钾溶液及溴水褪色。
(2)取代反应CH 4+Cl 光照3Cl(一氯甲烷)+HClCH 3Cl+Cl 光照2Cl 2(二氯甲烷)+HClCH 2Cl 2+Cl 光照3(三氯甲烷)+HCl (CHCl 3又叫氯仿)CHCl 3+Cl 光照4(四氯化碳)+HCl(3)分解反应甲烷分解:CH 高温22. 乙烯(烯烃通式:C n H 2n )乙烯的制取:CH 3CH 2浓硫酸170℃2=CH 2↑+H 2O(消去反应)(1)氧化反应乙烯的燃烧:CH 2=CH 2+3O 点燃2+2H 2O乙烯可以使酸性高锰酸钾溶液褪色,发生氧化反应。
(2)加成反应与溴水加成:CH 2=CH 2+Br 2Br —CH 2Br与氢气加成:CH 2=CH 2+H 2催化剂CH 3CH 3 与氯化氢加成:CH 2=CH 2+HCl 催化剂CH 3CH 2Cl 与水加成:CH 2=CH 2+H 2O催化剂CH 3CH 2OH(3)聚合反应 乙烯加聚,生成聚乙烯:n CH 2=CH 2催化剂 [CH 2—CH 2 ] n 适当拓展:CH 3CH =CH 2+Cl 3׀ Cl CH -׀ ClCH 2 CH 3CH =CH 2+H 2催化剂CH 3CH 2CH 3 CH 3CH =CH 2+HCl 催化剂CH 3CH 2CH 2Cl 或CH 3׀ ClCHCH 3 CH 3CH =CH 2+H 2O 催化剂CH 3CH 2CH 2OH 或CH 3׀ OHCHCH 3 n CH 2=CH -CH 3催化剂 [CH 2—׀ CH 3CH ] n (聚丙烯) 3. 乙炔(炔烃通式:C n H 2n-2)乙炔的制取:CaC 2+2H 2 CH ↑+Ca(OH)2(1)氧化反应乙炔的燃烧:HC ≡CH+5O 点燃2+2H 2O乙炔可以使酸性高锰酸钾溶液褪色,发生氧化反应。
高考常用有机化学方程式大全

光照 光照 光照 光照 高温 CaO △ 催化剂 加热、加压 催化剂催化剂 △ 催化剂 △ 催化剂 催化剂催化剂催化剂 △ 催化剂催化剂 浓硫酸 △ △高考常用有机化学方程式大全1. CH 4 + Cl 2 CH 3Cl + HCl2. CH 3Cl + Cl 2 CH 2Cl 2 + HCl3. CH 2Cl + Cl 2 CHCl 3 + HCl4. CHCl 3 + Cl 2 CCl 4+ HCl5. CH 4 C +2H 26. C 16H 34 C 8H 18 + C 8H 167. CH 3COONa + NaOH CH 4↑+ Na 2CO 38. CH 2 = CH 2 + Br 2 CH 2Br —CH 2Br9. CH 2 = CH 2 + H 2O CH 3CH 2OH10. CH 2 = CH 2 + HBr CH 3—CH 2Br 11. CH 2 = CH 2 + H 2 CH 3—CH 3 12. nCH 2 = CH 2 [ CH 2—CH 2 ] n13. nCH 2=CH-CH=CH 2 [CH 2-CH=CH-CH 2] n14. 2CH 2 = CH 2 + O 2 2CH 3CHO15. CH ≡CH + Br 2 CHBr = CHBr16. CHBr = CHBr+ Br 2 CHBr 2-CHBr 217. CH ≡CH + HCl H 2C = CHCl18. nCH 2 = CH [ CH 2-CH ] nCl Cl19. CH ≡CH + H 2O CH 3CHO20. CaC 2 + 2H 2O CH ≡CH ↑+ Ca(OH)221. + Br 2 Br + HBr22. + HO -NO 2 NO 2 +H 2O 23. + HO -SO 3H SO 3H+H 2OCH 3 NO 2NO 2 O 2N CH 3催化剂 NaOHH 2O 醇 △ 催化剂 △浓硫酸 170℃浓硫酸 140℃OH Br Br OH 催化剂 △催化剂 △△△ Br 催化剂 △ 24.+ 3H 2 25. +3HO -NO 2 +3H 2O26. 3CH ≡C H → 27. CH 3CH 2Br + H 2O CH 3CH 2OH + HBr28. CH 3CH 2Br + NaOH CH 3CH 2OH + NaBr29. CH 3CH 2Br+ NaOH CH 2 = CH 2 + NaBr +H 2O 30. 2CH 3CH 2OH+2Na 2CH 3CH 2ONa + H 2↑31. 2CH 3CH 2OH+O 2 2CH 3CHO + 2H 2O 32. CH 3CH 2OH CH 2 = CH 2↑+ H 2O 33.C 2H 5OH+C 2H 5OH C 2H 5OC 2H 5+H 2O 34. OH+NaOH ONa+H 2O35. OH+H 2O O -+H 3O +36. ONa+H 2O+CO 2 OH+ NaHCO 337. +3Br 2 ↓+3HBr38. CH 3CHO + H 2 CH 3CH 2OH 39. 2CH 3CHO + O 2 2CH 3COOH 40. CH 3CHO+2Ag(NH 3)2OH CH 3COONH 4+2Ag ↓+3NH 3+H 2O41CH 3CHO+2Cu(OH)2 CH 3COOH+Cu 2O ↓+2H 2O 42. 2CH 3COOH+2Na 2CH 3COONa+H 2↑43.2CH 3COOH+Na 2CO 3 2CH 3COONa+H 2O+CO 2↑44. CH 3COOH+NaHCO 3 CH 3COONa+H 2O+CO 2↑45. CH 3COOH + NaOH CH 3COONa + H 2O浓硫酸△催化剂催化剂催化剂催化剂催化剂△催化剂加热、加压+ 浓硫酸△+ 2H2O O OC —CO OCH2-CH246. 2CH3COOH + Cu(OH)2 (CH3COO)2Cu + 2H2O47.CH3COOH+CH3CH2OH CH3COOCH2CH3 +H2O48. CH3COOCH2CH3+NaOH CH3COONa+CH3CH2OH49. nOHCH2CH2COO H→[ OCH2CH2C ] n +H2O50. C6H12O6 (s) + 6O2 (g)6CO2 (g) + 6H2O (l)51. C6H12O62CH3CH2OH + 2CO252. C12H22O11+H2O C6H12O6+ C6H12O6蔗糖葡萄糖果糖53. C12H22O11 + H2O2C6H12O6麦芽唐葡萄糖54. (C6H10O5)n + nH2O n C6H12O6淀粉葡萄糖55. (C6H10O5)n + nH2O n C6H12O6纤维素葡萄糖56.C17H33COO-CH2C17H35COO-CH2C17H33COO-CH +3H2 C17H35COO-CHC17H33COO-CH2C17H35COO-CH257. C17H35COO-CH2CH2-OHC17H35COO-CH +3NaOH3C17H35COONa+ CH-OHC17H35COO-CH2CH2-OH58. CH2OH COOHCH2OH COOH高中有机化学知识点总结1.需水浴加热的反应有:(1)、银镜反应(2)、乙酸乙酯的水解(3)苯的硝化(4)糖的水解(5)、酚醛树脂的制取(6)固体溶解度的测定凡是在不高于100℃的条件下反应,均可用水浴加热,其优点:温度变化平稳,不会大起大落,有利于反应的进行。
(完美版)高中有机化学方程式总结

高中有机化学方程式总结一、烃 1.甲烷烷烃通式:C n H 2n -2 (1)氧化反应甲烷的燃烧:CH 4+2O 2 CO 2+2H 2O甲烷不可使酸性高锰酸钾溶液及溴水褪色。
(2)取代反应一氯甲烷:CH 4+Cl 2 CH 3Cl+HCl二氯甲烷:CH 3Cl+Cl 2CH 2Cl 2+HCl三氯甲烷:CH 2Cl 2+Cl 2 CHCl 3+HCl (CHCl 3又叫氯仿)四氯化碳:CHCl 3+Cl 2 CCl 4+HCl2.乙烯乙烯的制取:CH 3CH 2OH H 2C=CH 2↑+H 2O 烯烃通式:C n H 2n (1)氧化反应乙烯的燃烧:H 2C=CH 2+3O 2 2CO 2+2H 2O 乙烯可以使酸性高锰酸钾溶液褪色,发生氧化反应。
(2)加成反应与溴水加成:H 2C=CH 2+Br 2 CH 2Br —CH 2Br与氢气加成:H 2C=CH 2+H 2 3CH 3与氯化氢加成: H 2C=CH 2+HCl CH 3CH 2Cl 与水加成:H 2C=CH 2+H 2O CH 3CH 2OH(3)聚合反应乙烯加聚,生成聚乙烯:n H 2C=CH n 3.乙炔乙炔的制取:CaC 2+2H 2O HC ≡CH ↑+Ca(OH)2(1)氧化反应乙炔的燃烧:HC ≡CH+5O 2 4CO 2+2H 2O乙炔可以使酸性高锰酸钾溶液褪色,发生氧化反应。
(2)加成反应与溴水加成:HC ≡CH+Br2 HC=CHBrCHBr=CHBr+Br 2 CHBr 2—CHBr 2与氢气加成:HC ≡CH+H 2 H 2C=CH 2与氯化氢加成:HC ≡CH+HCl CH 2=CHCl(3)聚合反应氯乙烯加聚,得到聚氯乙烯:n CH 2 n乙炔加聚,得到聚乙炔:n HC ≡ n4.苯苯的同系物通式:C n H 2n-6 (1)氧化反应苯的燃烧:2C 6H 6+15O 2 12CO 2+6H 2O 苯不能使溴水和酸性高锰酸钾溶液褪色。
(完美版)高中有机化学方程式总结

高中有机化学方程式总结一、烃 1.甲烷烷烃通式:C n H 2n -2 (1)氧化反应甲烷的燃烧:CH 4+2O 2 CO 2+2H 2O 甲烷不可使酸性高锰酸钾溶液及溴水褪色。
(2)取代反应一氯甲烷:CH 4+Cl 2 CH 3Cl+HCl 二氯甲烷:CH 3Cl+Cl 2 CH 2Cl 2+HCl 三氯甲烷:CH 2Cl 2+Cl 2 CHCl 3+HCl (CHCl 3又叫氯仿) 四氯化碳:CHCl 3+Cl 2 CCl 4+HCl 2.乙烯乙烯的制取:CH 3CH 2OH H 2C=CH 2↑烯烃通式:C n H 2n (1)氧化反应乙烯的燃烧:H 2C=CH 2+3O 2 2CO 2+2H 2(2)加成反应与溴水加成:H 2C=CH 2+Br 2 CH 2Br —CH 2Br 与氢气加成:H 2C=CH 2+H 2 CH 3CH 3 与氯化氢加成: H 2C=CH 2+HCl CH 3CH 2Cl 与水加成:H 2C=CH 2+H 2O CH 3CH 2OH 点燃光光 光光 浓硫酸 170℃ 高温催化剂△图1 乙烯的制取乙烯加聚,生成聚乙烯:n H 2 2 n3.乙炔乙炔的制取:CaC 2+2H 2O HC ≡CH ↑+Ca(OH)2 (1)氧化反应乙炔的燃烧:HC ≡CH+5O 2 4CO 2+2H 2O 乙炔可以使酸性高锰酸钾溶液褪色,发生氧化反应。
(2)加成反应与溴水加成:HC ≡CH+Br 2HC=CH B rCHBr=CHBr+Br 2 CHBr 2—CHBr 2与氢气加成:HC ≡CH+H 2 H 2C=CH 2与氯化氢加成:HC ≡CH+HCl CH 2=CHCl (3)聚合反应氯乙烯加聚,得到聚氯乙烯:n CH 2=CHCl nCHn4.苯苯的同系物通式:C n H 2n-6 (1)氧化反应苯的燃烧:2C 6H 6+15O 2 12CO 2+6H 2O 苯不能使溴水和酸性高锰酸钾溶液褪色。
高中有机化学方程式汇总(全)(已免费)

高中有機化學方程式匯總1. CH4 + Cl 2光照CH3Cl + HCl2. CH3Cl + Cl 2光照CH2Cl2 + HCl3. CH2Cl + Cl 2光照CHCl 3 + HCl4. CHCl 3 + Cl2光照CCl4+ HCl5. CH4高温 C +2H26.C H催化剂 C H+ C H3418161688加热、加压4 ↑+ Na233CaOCH7. CH COONa + NaOH△CO8. CH2 = CH2 + Br2CH2Br—CH2Br9. CH2 = CH2 + H2O 催化剂CH3CH2OH22+ HBr催化剂CH3—CH2Br 10. CH = CH△22+ H2催化剂CH3—CH311. CH = CH△22催化剂[ CH 2—CH2]n12. nCH = CH13. nCH =CH-CH=CH2催化剂[CH -CH=CH-CH ]22 2 n14. 2CH2 = CH2 + O2催化剂2CH3CHO15. CH≡CH + Br 2CHBr = CHBr16. CHBr = CHBr+ Br 2CHBr 2- CHBr 217. CH≡CH + HCl催化剂H 2C = CHCl△18. nCH2 = CH[ CH2-CH ] nCl Cl19.CH≡CH + H 2O 催化剂 CH3CHO20.CaC2 + 2H2OCH ≡CH↑+ Ca(OH)221.催化剂Br + HBr + Br222.+ HO-NO2浓硫酸NO2+H2O△23.+ HO-SO3H △SO3H+H 2O24.+ 3H2催化剂△CH3CH325.+3HO-NO2催化剂O2N NO2+3H O226.→NO3CH≡ CH227. CH3CH 2Br + H2O NaOH CH 3CH2OH + HBr28. CH3CH 2Br + NaOH H 2O CH 3CH2OH + NaBr29. CH3CH 2Br+ NaOH醇CH2 = CH2 + NaBr +H 2O△30.2CH3CH 2OH+2Na2CH3CH2ONa + H2↑31.2CH3CH 2OH+O2催化剂2CH3CHO + 2H2O △32OH浓硫酸CH2= CH2↑+ H2O32. CH CH170℃33.C2H5OH+C2H5OH 浓硫酸C2H5OC2H5+H2O140℃34.OH+NaOH ONa+H2O35.OH+H2O O-+H3O+36.ONa+H2O+CO2OH+ NaHCO3OH OHBr↓Br+3HBr37.+3Br2Br催化剂CH3CH2OH 38. CH3CHO + H 2△催化剂2CH3COOH 39. 2CH3CHO + O2△40. CH3CHO+2Ag(NH 3)2 OH △↓ +3NH3+H2O CH3COONH 4+2Ag41CH3CHO+2Cu(OH)2△CH3COOH+Cu 2O↓ +2H 2O42. 2CH3COOH+2Na2CH 3COONa+H2↑43.2CH3COOH+Na2CO32CH 3COONa+H 2O+CO 2↑44. CH 3COOH+NaHCO 3CH 3COONa+H 2O+CO 2↑45. CH3COOH + NaOH CH3COONa + H2O46. 2CH 3COOH + Cu(OH) 2(CH 3COO) 2Cu + 2H 2O 47.CH 3COOH+CH 3CH 2OH浓硫酸 CH 3COOCH 2CH 3 +H 2O△ 48. CH 3COOCH 2CH 3 +NaOH CH 3COONa+CH 3CH 2OH49. nOHCH 2CH 2COO H →[ OCH 2CH 2C ] n +H 2O 50. C 6 H 12O 6 (s) + 6O 2 (g)6CO 2 (g) + 6H 2O (l) 51. C 6 H 12O 6 催化剂2CH 3CH 2OH + 2CO 252. C 12H 22O 11+H 2O 催化剂 C 6H 12O 6+ C 6H 12O 6蔗糖 葡萄糖 果糖53. C 12H 22O 11 + H 2O 催化剂2C 6H 12O 6麦芽唐 葡萄糖54. (C 6H 10O 5)n + nH 2O催化剂 n C 6H 12O 6 淀粉葡萄糖 6 10 5 ) n 2 O 催化剂 6 12 6 55. (C H O + nH △n C H O 纤维素葡萄糖 56.C 17H 33COO-CH 2催化剂 C 17H 35COO-CH 2C 17H 33COO-CH +3H 2 加热、加压C 17H 35COO-CH C 17H 33COO-CH 2C 17H 35COO-CH 2 57. C 17H 35COO-CH 2CH 2-OH C 17H 35COO-CH +3NaOH3C 17H 35COONa+ CH-OH C 17H 35COO-CH 2O O CH 2-OH 58. CH 2OH COOH+CH 2OH COOHC — C 浓硫酸 O O 2 △光CH 2- CH 2 1.CH 4Cl 2 HCl CH 3 Cl CH 3Cl Cl 2光 HCl CH 2 Cl 2 2.3.4.5.6.7.8.CH 2CH CH CH 2Br29.10.11.12.13.14.15.16.17.HOCH 2 (CHOH ) 4 CHO2Ag (NH 3 ) 2 OH HOCH 2 (CHOH )4 COONH 42Ag3NH 3H 2O18.19.20.21.高中有机化学知识点总结1.需水浴加热的反应有:(1 )、银镜反应( 2)、乙酸乙酯的水解( 3 )苯的硝化( 4)糖的水解(5 )、酚醛树脂的制取( 6)固体溶解度的测定凡是在不高于 100 ℃的条件下反应,均可用水浴加热,其优点:温度变化平稳,不会大起大落,有利于反应的进行。
(完整版)高中有机化学方程式归纳
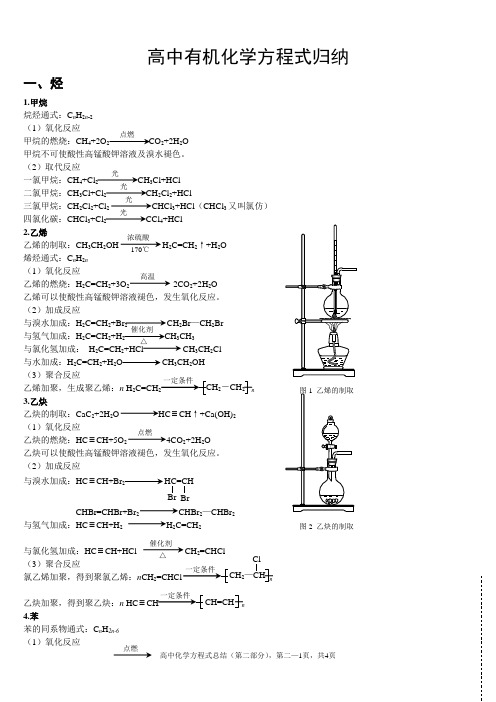
高中有机化学方程式归纳一、烃1.甲烷烷烃通式:C n H 2n -2 (1)氧化反应甲烷的燃烧:CH 4+2O 2 CO 2+2H 2O甲烷不可使酸性高锰酸钾溶液及溴水褪色。
(2)取代反应一氯甲烷:CH 4+Cl 2 CH 3Cl+HCl二氯甲烷:CH 3Cl+Cl 2CH 2Cl 2+HCl三氯甲烷:CH 2Cl 2+Cl 2 CHCl 3+HCl (CHCl 3又叫氯仿)四氯化碳:CHCl 3+Cl 2 CCl 4+HCl2.乙烯乙烯的制取:CH 3CH 2OH H 2C=CH 2↑+H 2O 烯烃通式:C n H 2n (1)氧化反应乙烯的燃烧:H 2C=CH 2+3O 2 2CO 2+2H 2O 乙烯可以使酸性高锰酸钾溶液褪色,发生氧化反应。
(2)加成反应与溴水加成:H 2C=CH 2+Br 2 CH 2Br —CH 2Br与氢气加成:H 2C=CH 2+H 2 CH 3CH 3与氯化氢加成: H 2C=CH 2+HCl CH 3CH 2Cl 与水加成:H 2C=CH 2+H 2O CH 3CH 2OH(3)聚合反应乙烯加聚,生成聚乙烯:n H 2C=CH n 3.乙炔乙炔的制取:CaC 2+2H 2O ≡CH ↑+Ca(OH)2 (1)氧化反应乙炔的燃烧:HC ≡CH+5O 2 4CO 2+2H 2O 乙炔可以使酸性高锰酸钾溶液褪色,发生氧化反应。
(2)加成反应与溴水加成:HC ≡CH+Br2HC=CHCHBr=CHBr+Br 2 CHBr 2—CHBr 2与氢气加成:HC ≡CH+H 2 H 2C=CH 2与氯化氢加成:HC ≡CH+HCl CH 2=CHCl(3)聚合反应氯乙烯加聚,得到聚氯乙烯:n CH 2 n乙炔加聚,得到聚乙炔:n HC ≡ n4.苯苯的同系物通式:C n H 2n-6 (1)氧化反应点燃光光光光浓硫酸170℃ 高温催化剂 △2-CH 2点燃图2 乙炔的制取催化剂△Br 2—CHClCH=CH苯的燃烧:2C 6H 6+15O 2 12CO 2+6H 2O 苯不能使溴水和酸性高锰酸钾溶液褪色。
高中有机化学方程式汇总(大全)

天堂 de 果冻专业贡献高中有机化学方程式汇总1. CH 4 + Cl 2 光照 CH 3Cl + HCl3 2浓硫酸 CH 2= CH 2↑+ H 2170 ℃32. CH CH OHO 2. CH 3Cl + Cl光照CH 2Cl 2 + HCl浓硫酸22 5 2 5OH2 5 2523. CH Cl + Cl光照CHCl + HCl33.C H OH+C H140℃CHOCH+HO23234. OH+NaOHONa+H 2O光照CCl 4+ HCl4. CHCl 3 + Cl 2-+高温35.23C +2H 2OH+H OO+HO5. CH 46. C 16H 34催化剂 C 8H 18 + C 8H 1636. ONa+H 2O+CO 2OH+ NaHCO 3加热、加压7. CH 3COONa + NaOH CaOCH 4 ↑+ Na 2CO 3△8. CH 2 = CH 2 + Br 2CH 2Br —CH 2Br9. CH 2 = CH 2 + H 2O 催化剂 CH 3CH 2OH22+ HBr 催化剂CH 3—CH 2Br10. CH = CH△22+ H 2 催化剂CH 3—CH 311. CH = CH△22 催化剂[ CH 2—CH 2] n12. nCH = CH13. nCH =CH-CH=CH 2 催化剂[CH -CH=CH-CH ]222 n14. 2CH 2 = CH 2 + O 2 催化剂2CH 3CHO15. CH ≡CH + Br 2CHBr = CHBr16. CHBr = CHBr+ Br 2CHBr 2-CHBr 217. CH ≡CH + HCl 催化剂H 2C = CHCl△2[ CH 2-CH ] n18. nCH = CHClCl19. CH ≡CH + H 2O 催化剂 CH 3CHO20. CaC 2 + 2H 2OCH ≡CH ↑+ Ca(OH)2催化剂21.+ Br 2Br + HBr22. + HO -NO 2 浓硫酸NO 2 +H 2O△23. + HO -SO 3H △SO 3H+H 2O24.2 催化剂+ 3H△CH 3CH 325.催化剂 O 2NNO 2+3H 2O+3HO -NO 2NO 226. 3CH ≡CH催化剂27. CH 3CH 2Br + H 2 ONaOHCH 3CH 2OH + HBr28. CH CH Br + NaOH H 2OCH OH + NaBrCH332229. CH CH Br+ NaOH△ CH 2 = CH2+ NaBr +H O32醇 230. 2CH 3CH 2OH+2Na2CH 3CH 2ONa + H 2↑31. 催化剂 2CH 3CHO + 2H 2O2CH 3CH 2OH+O 2△OHOHBrBr↓+3HBr37.+3Br 2Br38. CH 3CHO + H 2 催化剂CH 3CH 2OH△32 催化剂339. 2CH CHO + O△2CH COOH40. CH 3CHO+2Ag(NH 3 )2OH △CH 3COONH 4+2Ag ↓+3NH 3 +H 2O41CH 3CHO+2Cu(OH) 2 △CH 3COOH+Cu 2O ↓+2H 2O42. 2CH 3 COOH+2Na CH 3COONa+H 2↑43.2CH 3COOH+Na 2CO 32CH 3COONa+H 2O+CO 2↑ 44. CH 3COOH+NaHCO 3CH 3 COONa+H 2O+CO 2↑45. CH 3COOH + NaOHCH 3COONa + H 2O46. 2CH 3COOH + Cu(OH) 2(CH 3COO) 2Cu + 2H 2O浓硫酸CH 3COOCH 2CH 347.CH 3COOH+CH 3CH 2OH△+H 2O48. CH 3COOCH 2CH 3+NaOHCH 3 COONa+CH 3 CH 2OH催化剂O49. nOHCH 2CH 2COOH[ OCH 2CH 2C ] n +H 2O50. C 6H 12O 6 (s) + 6O 2 (g)6CO 2 (g) + 6H 2O (l)612 6 催化剂32OH + 2CO 251.CH O2CH CH52. C 12H 22O 11+H 2O 催化剂C 6H 12O 6+ C 6H 12O 6蔗糖葡萄糖果糖53. C 12H 22O 11 + H 2O催化剂2C 6H 12O 6麦芽唐葡萄糖54. (C 6 H 10O 5)n + nH 2O催化剂n C 6H 12O 6淀粉葡萄糖55. (C 6 H 10O 5)n + nH 2O催化剂n C 6H 12O 6纤维素△葡萄糖56.C 17H 33COO-CH 2催化剂C 17H 35COO-CH 2C 17H 33COO-CH +3H 2 加热、加压 C 17H 35COO-CHC 17H 33COO-CH 2 C 17H 35COO-CH 257. C 17H 35COO-CH 2CH 2-OHC 17H 35COO-CH +3NaOHC 17H 35COOH+ CH-OHC 17H 35COO-CH 2 OOCH 2-OH 58. CH 2OH COOH 浓硫酸C — C+OO+H 2O CH 2OH COOH △CH 2-CH2。
高中有机化学方程式大全

光照 光照 光照 光照 高温 CaO △ 催化剂 加热、加压 催化剂催化剂 △ 催化剂 △ 一定 条件 一定 条件 催化剂 催化剂 △ 催化剂催化剂 浓硫酸 △ 高中有机化学方程式1. CH 4 + Cl 2 CH 3Cl + HCl2. CH 3Cl + Cl 2 CH 2Cl 2 + HCl3. CH 2Cl + Cl 2 CHCl 3 + HCl4. CHCl 3 + Cl 2 CCl 4+ HCl5. CH 4 C +2H 26. C 16H 34 C 8H 18 + C 8H 167. CH 3COONa + NaOH CH 4↑+ Na 2CO 38. CH 2 = CH 2 + Br 2 CH 2Br —CH 2Br9. CH 2 = CH 2 + H 2O CH 3CH 2OH10. CH 2 = CH 2 + HBr CH 3—CH 2Br 11. CH 2 = CH 2 + H 2 CH 3—CH 3 12. nCH 2 = CH 2 [ CH 2—CH 2 ] n13. nCH 2=CH-CH=CH 2[CH 2-CH=CH-CH 2] n 14. 2CH 2 = CH 2 + O 2 2CH 3CHO15. CH ≡CH + Br 2 CHBr = CHBr16. CHBr = CHBr+ Br 2 CHBr 2-CHBr 217. CH ≡CH + HCl H 2C = CHCl18. nCH 2 = CH [ CH 2-CH ] n (一定条件)Cl Cl19. CH ≡CH + H 2O CH 3CHO20. CaC 2 + 2H 2O CH ≡CH ↑+ Ca(OH)221. + Br 2 Br + HBr22. + HO -NO 2 NO 2 +H 2OCH 3 NO 2NO 2 O 2N CH 3 催化剂 NaOH△ H 2O △ 醇 △ Cu/Ag △浓硫酸 170℃浓硫酸 140℃OH BrBr OH 催化剂 △催化剂 △△△ Br 催化剂 △ 23. + 3H 224. +3HO -NO 2 +3H 2O25. 3CH ≡C H → 26. CH 3CH 2Br + H 2O CH 3CH 2OH + HBr27. CH 3CH 2Br + NaOH CH 3CH 2OH + NaBr28. CH 3CH 2Br+ NaOH CH 2 = CH 2 + NaBr +H 2O 29. 2CH 3CH 2OH+2Na 2CH 3CH 2ONa + H 2↑30. 2CH 3CH 2OH+O 2 2CH 3CHO + 2H 2O 31. CH 3CH 2OH CH 2 = CH 2↑+ H 2O 32.C 2H 5OH+C 2H 5OH C 2H 5OC 2H 5+H 2O 33. OH+NaOH ONa+H 2O34. OH+H 2O O -+H 3O +35. ONa+H 2O+CO 2 OH+ NaHCO 336. +3Br 2 ↓+3HBr37. CH 3CHO + H 2 CH 3CH 2OH 38. 2CH 3CHO + O 2 2CH 3COOH 39. CH 3CHO+2Ag(NH 3)2OH CH 3COONH 4+2Ag ↓+3NH 3+H 2O40.CH 3CHO+2Cu(OH)2 CH 3COOH+Cu 2O ↓+2H 2O 41. 2CH 3COOH+2Na 2CH 3COONa+H 2↑42.2CH 3COOH+Na 2CO 3 2CH 3COONa+H 2O+CO 2↑43. CH 3COOH+NaHCO 3 CH 3COONa+H 2O+CO 2↑44. CH 3COOH + NaOH CH 3COONa + H 2O45. 2CH 3COOH + Cu(OH)2 (CH 3COO)2Cu + 2H 2O浓硫酸 △催化剂 催化剂 催化剂 催化剂 催化剂 △ 催化剂 加热、加压 + 浓硫酸 △ + 2H 2OO OC — C O O CH 2-CH 2 46.CH 3COOH+CH 3CH 2OH CH 3COOCH 2CH 3 +H 2O47. CH 3COOCH 2CH 3+NaOH CH 3COONa+CH 3CH 2OH48. nOHCH 2CH 2COO H → [ OCH 2CH 2C ] n +H 2O (一定条件)49. C 6H 12O 6 (s) + 6O 2 (g) 6CO 2 (g) + 6H 2O (l)50. C 6H 12O 6 2CH 3CH 2OH + 2CO 251. C 12H 22O 11+H 2O C 6H 12O 6+ C 6H 12O 6蔗糖 葡萄糖 果糖52. C 12H 22O 11 + H 2O 2C 6H 12O 6麦芽唐 葡萄糖53. (C 6H 10O 5)n + nH 2O n C 6H 12O 6淀粉 葡萄糖54. (C 6H 10O 5)n + nH 2O n C 6H 12O 6 纤维素 葡萄糖55.C 17H 33COO-CH 2 C 17H 35COO-CH 2 C 17H 33COO-CH +3H 2 C 17H 35COO-CH C 17H 33COO-CH 2 C 17H 35COO-CH 256. C 17H 35COO-CH 2 CH 2-OHC 17H 35COO-CH +3NaOH 3C 17H 35COONa+ CH-OHC 17H 35COO-CH 2CH2-OH 57. CH 2OH COOH CH 2OH COOH5859.222Br CH CH CH CH +=-=60.61.62.63.64.65.高中有机化学知识点总结1.需水浴加热的反应有:(1)、银镜反应(2)、乙酸乙酯的水解(3)苯的硝化(4)糖的水解(5)、酚醛树脂的制取(6)固体溶解度的测定凡是在不高于100℃的条件下反应,均可用水浴加热,其优点:温度变化平稳,不会大起大落,有利于反应的进行。
高中有机化学方程式汇总

高中有机化学方程式汇总一、取代反应1、CH 4 + Cl 2 HCl + CH 3Cl ( 气态) 一氯甲烷CH 3Cl + Cl 2HCl + CH 2Cl2 ( 液态 ) 二氯甲烷CH 2Cl + Cl 2HCl + CHCl 3 ( 液态 ) 三氯甲烷或氯仿 CHCl 3+ Cl 2HCl +CCl 4 ( 液态 )四氯甲烷或四氯化碳 2、C 2H 6 + Cl 2 HCl + CH 3CH 2Cl3 + Br 2Br + HBr (真正催化剂是FeBr3)3 + Cl 22Cl + HCl3 + 3Cl 2 + 3HCl4 + HONO 2 2 + H 2O+ HOSO 3H 3H + H 2O5 + 3Br 2 + 3HBr+ 3HONO 2 + H 2O6、C 2H 5OH + HBr C 2H 5Br + H 2O C 2H 5Br C 2H 5OH + HBrC 2H 5Br CH 2 CH 2 + HBr7、CH 3COOC 2H 5 + H 2O CH 3COOH + C 2H 5 OH光照光照光照 光照光照Fe 光照无水AlCl 3Cl LNaOHH 2O NaOHC 2H 5OHBr L3H 2SO 4浓50-60℃2NO NO 2 LH 2SO 4浓50-60℃ H 2SO 4浓70-80℃ 无机酸或碱8、 + 3 NaOH + 3C 17H 35 COONa二、加成反应1、CH 2 CH 2 + H 2CH 3 CH 32、CH 2 CH 2 + HCl CH 3 CH 2Cl3、CH 3CH CH 2+ HClCH 3 CHClCH3(马氏加成)CH 3 CHCH 2 + HCl CH 3 CH 2 CH 2Cl (反马氏加成)4、CH CH + H 2 CH 2 CH 2 CH CH + 2 H 2 CH 3 CH 35、CH CH + 2HCl CH 3 CHCl 26、CH 3 CHO + 2 H 2 CH 3 CH 2OH 7+ 3 H 2 + H 2 CH 3 CH 2 CH 3+ H 2 CH 3 CH 2 CH 2 CH 3 ㊣ Pt 比Ni 催化效率高 8+ 3Cl 2 C 6H 6 Cl 69、 CH 2 CH 2 + H 2O CH 3 CH 2OHCH CH + H 2O 2CH 2 CH 2 + O 22 1、CH3 CH 2OH CH 2 2 + H 2O2、2CH 3 CH 2OH+ H 2O (分子间脱水) 3、C 2H 5 Cl CH 2 CH 2 + H ClOOOCH 2 O C C 17H 35 CH O C C 17H 35 CH 2 O C 17H 35CH 2CH OH CH 2 无水AlCl 3/HgCl 2/ZnCl 2150-160℃ 无过氧酸有过氧酸如CH 3COOOH 催化剂加热 HHC CH Cl +--+ H Cl无水AlCl 3 H 2SO 4 或 H 3PO 4 加热 加压HgSO 4(H +)OCH 3 C H高温、高压PdCl 2 或CuCl 2OCH 3 C H三、消去反应H 2SO 4浓170℃ H 2SO 4浓 140℃CH 3 CH 2 O CH 2 CH 3 NaOH C 2H 5OH四、酯化反应 (酯化反应也是取代反应)1、CH 3 COOH + CH 3 CH 2OH CH 3 COOCH 2 CH 3 + H 2O2、 + 3HONO 2+ H 2O3、[C 6H 7 O 2(OH) 3 ]n + 3n HONO 2 [C 6H 7 O 2(NO 2) 3 ]n + 3nH 2O 五、水解反应(卤代烃、酯、油脂的水解见上,也是取代反应)1、CH 3 COONa + H 2O 3 COOH + NaOH2、C 17H 35 COONa + H 2 C 17H 35 COOH + NaOH3、(C 6H 10O 5)n + nH 2O n C 6H 12O 64、C 12H 22O11 + H 2OC 6H 12O 6 + C 6H 12O 6C 12H 22O 11 + H 2O 2C 6H 12O 6麦芽唐 葡萄糖5、CH 3 COOCH 2 CH 3 + H 2O CH 3 COOH + CH 3 CH 2OH六、氧化反应①被强氧化剂氧化 1、2 CH 3 CH 2OH + O 2 2 + H 2O 2、2 + O 2 2 CH 3 COOH 3、2 CH 2 CH 2 + O 2 2 ②被弱氧化剂缓慢氧化1、CH 3 CHO + 2[Ag(NH 3)2] OH CH 3 COOH + 4 NH 3 + 2Ag + H 2O2、CH 3 CHO + 2 Cu(OH)2 CH 3 COOH + 2 Cu 2O + H 2O3、CH 2 OH(CHOH)4 CHO + 2[Ag(NH 3)2] OH CH 2 OH(CHOH)4 COOH + 4 NH 3 + 2Ag + H 2O4、CH 2 OH(CHOH)4 CHO +2 Cu(OH)2 OH(CHOH)4 COOH + 2 Cu 2O + H 2O5、HCOOH + 2[Ag(NH 3)2] OH CO 2 + 4 NH 3 + 2Ag + H 2OH 2SO 4浓 加热CH 2 OH CH OHCH 2 OHCH 2 O NO 2 CH O NO 2 CH 2 O NO 2 H 2SO 4浓 H 2SO 4浓H 2SO 4稀加热淀粉/纤维素 葡萄糖H 2SO 4稀加热蔗糖 葡萄糖 果糖H 2SO 4稀加热无机酸 或碱Cu 或Ag OCH3 C H OCH 3 C H Mn(AC)2 Mn(AC)2 OCH 3 C H 水浴加热 水浴加热 水浴加热6、HCOOH + 2 Cu(OH)2CO 2 + 2 Cu 2O + 2H 2O③有化合机物的燃烧 C x H y + (x+y /4) O 2xCO 2 + y /4 H 2O七、还原反应1、+ H 22、 + H 2 CH 3 CH 2OH3、 八、加聚反应1、n CH 2 CH 22、n CH CH3、 九、缩聚反应1、n+ nH 2O2、+ nH 2O 1、CH 4 C + 2H 2 C 16H 34 C 8H 16 + C 8H 18C 8H 18 C 4H 8 + C 4H 10 C 8H 16 CH 4 + C 7H 12十一、其它有机反应12 + H 2O 3 2、2CH 3 CH 2OH + 2Na 2CH 3 CH 2O Na + H 2 3、OH + 2Na 24、C 12H 22O 11 12C + 11 H 2O C + 2H 2SO 4(浓) CO 2 +2 SO 2 + 2H 2O5、氨基酸的两性点燃 O CH 3 C CH 3 CH 3 C CH 3 OCH 3 C H 2 CH 2 + H 2 2 CH 3nCH 2 CH CH 2 CH 2催化剂[ CH 2 CH CH 2 CH 2]nH N CH 2 C OH H O [N CH 2 C ]n H O催化剂COOH + nHO CH 2 CH 2 OH 催化剂O O CH 2 CH 2 O C C]n [ O 十、裂化反应高温 高温 高温 高温 H 2SO 4浓 + HClCH 2 COOH NH 2 CH 2 COOHNH 3Cl+ NaOHCH 2 COOH NH 2CH 2 COONa + NH 2H 2O。
高中有机方程式大全

nHOOC—
—COOH+ nHOCH2CH2OH
催化剂
HO—[ OC—
—CO OCH2CH2O—]n H +(2n-1)H2O
6、1,6—己二酸与 1,6—己二胺的缩聚: nHOOC(CH2)6COOH+nH2N(CH2)6NH2
催化剂
HO—[ OC(CH2)6CONH(CH2)6NH—]nH+(2n-1)H2O 七、酯类
加热
(三)乙二醛 1、乙二醛与银氨溶液反应:
OHC—CHO+4[Ag(NH3)2]OH 水浴加热 H4NOOC—COONH4+2H2O+4Ag↓+6NH3↑
2、乙二醛与新制的氢氧化铜反应:
加热
OHC—CHO+4Cu(OH)2 +2NaOH
NaOOC—COONa+2Cu2O↓ +6H2O
3、乙二醛的催化氧化:OHC—CHO+O2 催化剂 HOOC—COOH
COOH +2CH3CH2OH
COOH
浓 H2SO4 加热
COOCH2、乙二醇与足量的乙酸和浓硫酸共热:
CH2OH +2CH3COOH
CH2OH
浓 H2SO4 加热
CH2OOCCH3 CH2OOCCH3
+2H2O
二乙酸乙二酯
3、乙二酸与乙二醇和浓硫酸共热:
(一)乙酸乙酯
1、乙酸乙酯的燃烧:CH3COOCH2CH3+5O2 点燃 4CO2+4H2O
2、乙酸乙酯在酸性条件下的水解反应:
CH3COOCH2CH3+H2O 稀硫酸 CH3COOH+CH3CH2OH
加热
3、乙酸乙酯与氢氧化钠溶液共热: CH3COOCH2CH3+NaOH 加热 CH3COONa+CH3CH2OH
加热
12、2—丙醇的催化氧:2(CH3)2CHOH+O2 催化剂 2CH3COCH3+2H2O
完美版)高中有机化学方程式总结

完美版)高中有机化学方程式总结高中有机化学方程式总结一、烃1.甲烷烷烃通式:CnH2n-21)氧化反应甲烷的燃烧:CH4 + 2O2 → CO2 + 2H2O甲烷不能使酸性高锰酸钾溶液及溴水褪色。
2)取代反应一氯甲烷:CH4 + Cl2 光→ CH3Cl + HCl二氯甲烷:CH3Cl + Cl2 光→ CH2Cl2 + HCl三氯甲烷:CH2Cl2 + Cl2 光→ CHCl3 + HCl(CHCl3又叫氯仿)四氯化碳:CHCl3 + Cl2 光→ CCl4 + HCl2.乙烯乙烯的制取:CH3CH2OH + 浓硫酸 170℃ → H2C=CH2 ↑+H2O烯烃通式:XXX1)氧化反应乙烯的燃烧:H2C=CH2 + 3O2 → 2CO2 + 2H2O乙烯可以使酸性高锰酸钾溶液褪色,发生氧化反应。
2)加成反应与溴水加成:H2C=CH2 + Br2 → CH2Br—CH2Br与氢气加成:H2C=CH2 + H2 催化剂→ CH3CH3与氯化氢加成:XXX + HCl △ → CH3CH2Cl与水加成:XXX + H2O → CH3CH2OH3)聚合反应乙烯加聚,生成聚乙烯:nHC=CH2 一定条件→ -(-CH2-CH2-)n-3.乙炔乙炔的制取:CaCO2 + 2H2O → HC CH↑+Ca(OH)21)氧化反应乙炔的燃烧:HC CH + 5O2 点燃→ 4CO2 + 2H2O乙炔可以使酸性高锰酸钾溶液褪色,发生氧化反应。
2)加成反应与溴水加成:HC CH + Br2 → HC=CHBrBr →CHBr=CHBr + Br2与氢气加成:H2C=CH2 + H2 催化剂→ CH3CH3与氯化氢加成:HC CH + HCl 催化剂→ CH2=CHCl3)聚合反应氯乙烯加聚,得到聚氯乙烯:nCH2=CHClCH2—CHn乙炔加聚,得到聚乙炔:nHC CH 一定条件→ -(-C≡C-)n-4.苯苯的同系物通式:CnH2n-61)氧化反应苯的燃烧:2C6H6 + 15O2 点燃→ 12CO2 + 6H2O甲苯不能使溴水褪色,但可以使酸性高锰酸钾溶液褪色。
(完整版)高中有机化学方程式大全.docx

高中有机化学方程式大全1. CH 4 + Cl 2光照CH 3Cl + HCl 2. CH Cl + Cl光照 + HCl2CH Cl2323. CH 2Cl + Cl 2 光照 CHCl 3 + HCl4. CHCl 3 + Cl 2光照CCl 4+ HCl4 高温C +2H 25. CH6. C 16H 34 催化剂C 8H 18 + C 8H 16加热、加压CaO 7. CH 3COONa + NaOHCH 4 ↑+ Na 2CO 3△8. CH = CH 2+ Br2CH 2 Br —CH Br229.CH =CH催化剂CH CH OH2+ H O223210. CH 2 = CH 2 + HBr催化剂CH 3—CH 2Br△催化剂CH 3—CH 311. CH 2 = CH 2 + H 2△22 催化剂 22 ] n12. nCH = CH[ CH —CH催化剂13. nCH 2=CH-CH=CH 2[CH 2-CH=CH-CH 2] n催化剂2CH 3CHO 14. 2CH 2 = CH 2 + O 215. CH ≡CH + Br 2CHBr = CHBr 16. CHBr = CHBr+ Br 2CHBr 2- CHBr 2催化剂17. CH ≡CH + HCl△H 2C = CHCl18. nCH = CH[ CH -CH ] n22Cl Cl19. CH ≡CH + H 2O 催化剂 CH 3CHO20. CaC 2 + 2H 2OCH ≡CH ↑+ Ca(OH)2催化剂21.+ Br 2Br + HBr浓硫酸22.+ HO -NO 2NO 2 +H 2O△23. + HO -SO 3H △SO 3H+H 2O24.+ 3H2催化剂△CH3CH325.+3HO-NO2催化剂O2N NO2+3H O226.3CH≡ CH→NO227. CH3CH 2Br + H2 O NaOH CH 3CH2OH + HBr28. CH CH Br + NaOH H 2O CH3CH OH + NaBr32229. CH3CH 2Br+ NaOH醇CH2 = CH2 + NaBr +H 2O△30.2CH3CH 2OH+2Na2CH3CH2ONa + H2↑31.322催化剂32△32. CH CH OH浓硫酸CH2= CH↑+ H O32170℃2233.C2H5OH+C2H5OH 浓硫酸C2H5OC2H5+H2O 140℃34.OH+NaOH ONa+H O235.OH+H2O-O +H3O+36.ONa+H2O+CO2OH+ NaHCO3OH OHBr Br37.+3Br2↓+3HBrBr38. CH CHO + H催化剂CH OH233239.2CH3CHO + O2催化剂2CH3COOH △40. CH3CHO+2Ag(NH 3)2 OH △CH3COONH 4+2Ag↓ +3NH3+H2O412△CH3COOH+Cu2O↓+2H 2OCH3 CHO+2Cu(OH)42.2CH3COOH+2Na2CH 3COONa+H2↑43.2CH COOH+Na CO32CH COONa+H O+CO ↑3232244. CH 3COOH+NaHCO 3CH 3COONa+H 2O+CO 2↑45. CH3COOH + NaOH CH 3COONa + H2O46. 2CH 3COOH + Cu(OH)2(CH COO) 2Cu + 2H O3247.CH COOH+CH3CH OH 浓硫酸CH COOCH 2CH 3+H O32 3248. CH COOCH CH△CH COONa+CH CH OH+NaOH323 3 3 2 49. nOHCH 2CH 2COO H → [ OCH 2CH 2C ] n +H 2O50. C 6 H 12O 6 (s) + 6O 2 (g)6CO 2 (g) + 6H 2O (l)51. C 6 H 12O 6 催化剂 2CH 3CH 2OH + 2CO 252. C 12H 22O 11+H 2O催化剂C 6H 12O 6+ C 6H 12O 6蔗糖葡萄糖果糖53. C 12H 22O 11 + H 2O催化剂2C 6H 12O 6麦芽唐葡萄糖54. (C 6H 10O 5)n + nH 2 O催化剂n C 6H 12O 6淀粉葡萄糖55. (C 6H 10O 5)n + nH 2 O 催化剂△纤维素56.C 17H 33COO-CH 2 C 17H 33COO-CH +3H C 17H 33COO-CH 257. C 17H 35COO-CH 2C 17H 35COO-CH +3NaOH C 17H 35COO-CH 2 n C 6H 12O 6葡萄糖C 17H 35COO-CH 2C 17H 35COO-CHC 17H 35COO-CH 2CH 2-OH3C 17H 35COONa+ CH-OHOOCH 2-OH58. CH 2OHCOOH+CH 2OH COOHC — C浓硫酸OO2△光CH 2- CH 21.CH 4Cl 2HClCH 3ClCH 3ClCl 2光HClCH 2 Cl 2 2.3.4.催化剂2 加热、加压5.6.7.8.CH 2CH CH CH 2Br29.10.11.12.13.14.15.16.17.HOCH 2 (CHOH ) 4 CHO2Ag (NH 3 ) 2 OHHOCH 2 (CHOH )4 COONH 42Ag3NH 3H 2O18.19.20.21.高中有机化学知识点总结1.需水浴加热的反应有:(1 )、银镜反应( 2)、乙酸乙酯的水解( 3 )苯的硝化( 4)糖的水解(5 )、酚醛树脂的制取( 6)固体溶解度的测定凡是在不高于 100 ℃的条件下反应,均可用水浴加热,其优点:温度变化平稳,不会大起大落,有利于反应的进行。
高中所有有机化学方程式

光照 光照 光照 光照 高温 CaO △ 催化剂 加热、加压催化剂 △ 催化剂高中有机化学方程式汇总1. CH 4 + Cl 2 CH 3Cl + HCl2. CH 3Cl + Cl 2 CH 2Cl 2 + HCl3. CH 2Cl + Cl 2 CHCl 3 + HCl4. CHCl 3 + Cl 2 CCl 4+ HCl5. CH 4 C +2H 26. C 16H 34 C 8H 18 + C 8H 167. CH 3COONa + NaOH CH 4↑+ Na 2CO 38. CH 2 = CH 2 + Br 2 CH 2Br —CH 2Br9. CH 2 = CH 22OH10. CH 2 = CH 23—CH 2Br 11. CH 2 = CH 2CH 3 12. nCH 2 = CH 2 ] n 13. nCH 22-CH=CH-CH 2] n14. 2CH 2 = CH 3CHO15. CH ≡CH + Br 2 CHBr = CHBr16. CHBr = CHBr+ Br 2 CHBr 2-CHBr 217. CH ≡CH + HCl H 2C = CHCl18. nCH 2 = CH [ CH 2-CH ] nCl Cl19. CH ≡CH + H 2O CH 3CHO20. CaC 2 + 2H 2O CH ≡CH ↑+ Ca(OH)2+ Br 2+ HO 2 +H 2O催化剂△浓硫酸170℃浓硫酸140℃催化剂△23. + HO-SO3H 3H+H2O24.+ 3H2-NO22O26. 3CH≡C H27. CH3CH2Br + H228. CH3CH229. CH3CH22O30. 2CH3CH2OH+2Na 2CH3CH2ONa + H2↑31. 2CH3CH2OH+O2 2CH3CHO + 2H2O32. CH3CH2OH CH2 = CH2↑+ H2O+C2H5OH C2H5OC2H5+H2O34. 2O35. 2O -+H3O+233738. CH339. 2CH340. CH34+2Ag↓+3NH3+H2O 41CH3↓+2H2O42. 2CH3COOH+2Na 2CH3COONa+H2↑+Na2CO32CH3COONa+H2O+CO2↑44. CH3COOH+NaHCO3 CH3COONa+H2O+CO2↑45. CH3COOH + NaOH CH3COONa + H2O催化剂 催化剂催化剂 催化剂 催化剂 △ 催化剂 加热、加压 + 46. 2CH 3COOH + Cu(OH)2 (CH 3COO)2Cu + 2H 2O+CH 3CH 2OH CH 2O48. CH 3COOCH 2CH 33COONa+CH 3CH 2OH49. nOHCH 2CH 2COO H → [ OCH 2CH 2C ] n +H 2O50. C 6H 12O 6 (s) + 6O 2 (g) 6CO 2 (g) + 6H 2O (l)51. C 6H 12O 6 2CH 3CH 2OH + 2CO 252. C 12H 22O 11+H 2O C 6H 12O 6+ C 6H 12O 6 蔗糖 葡萄糖 果糖53. C 12H 22O 11 + H 2O 2C 6H 12O 6麦芽唐 葡萄糖 54. (C 6H 10O 5)n + nH 2O n C 6H 12O 6淀粉 葡萄糖55. (C 6H 10O 5)n + nH 2O n C 6H 12O 6 纤维素 葡萄糖C 17H 35COO-CH 2 C 17H 33COO-CH +3H 2 C 17H 35COO-CH C 17H 33COO-CH 2 C 17H 35COO-CH 257. C 17H 35COO-CH 2 CH 2-OHC 17H 35COO-CH +3NaOH COONa+ CH-OHC 17H 35COO-CH 2 58. CH 2OH COOH CH 2OH COOH 1.Cl CH −+24光2.3.4.5.6.7.8.9.10.11.12.13.14.15.16.17.18.19.20.21.高中有机化学知识点总结1.需水浴加热的反应列表有:(1)、银镜反应(2)、乙酸乙酯的水解(3)苯的硝化(4)糖的水解(5)、酚醛树脂的制取(6)固体溶解度的测定凡是在不高于100℃的条件下反应,均可用水浴加热,其优点:温度变化平稳,不会大起大落,有利于反应的进行。
高中有机化学常用反应方程式汇总

光照催化剂催化剂△催化剂△催化剂催化剂催化剂△催化剂浓硫酸△CH3NO2NO2O2NCH3催化剂H2O醇△催化剂△浓硫酸170℃催化剂△高中有机化学方程式1. CH4 + Cl2 CH3Cl + HCl8. CH2 = CH2 + Br2CH2Br—CH2Br9. CH2 = CH2 + H2O CH3CH2OH10. CH2 = CH2 + HBr CH3—CH2Br11. CH2 = CH2 + H2CH3—CH312. nCH2 = CH2[ CH2—CH2 ] n13. nCH2=CH-CH=CH2 [CH2-CH=CH-CH 2] n15. CH≡CH + Br2CHBr = CHBr16. CHBr = CHBr+ Br2 CHBr2-CHBr217. CH≡CH + HCl H2C = CHCl18. nCH2 = CH [ CH2-CH ] nCl Cl20. CaC2 + 2H2O CH≡CH↑+ Ca(OH)221. + Br2Br + HBr22. + HO-NO2NO2 +H2O24.+ 3H225. +3HO-NO2+3H2O28. CH3CH2Br + NaOH CH3CH2OH + NaBr29. CH3CH2Br+ NaOH CH2 = CH2 + NaBr +H2O30. 2CH3CH2OH+2Na 2CH3CH2ONa + H2↑31. 2CH3CH2OH+O2 2CH3CHO + 2H2O32. CH3CH2OH CH2 = CH2↑+ H2O34. OH+NaOH ONa+H2OOH BrBr OH 催化剂 △催化剂 △△△ 浓硫酸 △ Br 稀硫酸 △36. ONa+H 2O+CO 2 OH+ NaHCO 337. +3Br 2 ↓+3HBr38. CH 3CHO + H 2 CH 3CH 2OH 39. 2CH 3CHO + O 2 2CH 3COOH 40. CH 3CHO+2Ag(NH 3)2OH CH 3COONH 4+2Ag ↓+3NH 3+H 2O41.CH 3CHO+2Cu(OH)2+ NaOH CH 3COO Na +Cu 2O ↓+3H 2O42. 2CH 3COOH+2Na 2CH 3COONa+H 2↑43.2CH 3COOH+Na 2CO 3 2CH 3COONa+H 2O+CO 2↑44. CH 3COOH+NaHCO 3 CH 3COONa+H 2O+CO 2↑ 45. CH 3COOH + NaOH CH 3COONa + H 2O46. 2CH 3COOH + Cu(OH)2 (CH 3COO)2Cu + 2H 2O47.CH 3COOH+CH 3CH 2OH CH 3COOCH 2CH 3 +H 2O 48. CH 3COOCH 2CH 3+NaOH CH 3COONa+CH 3CH 2OH48. CH 3COOCH 2CH 3+ H 2O CH 3COOH+CH 3CH 2OH高中有机化学知识点总结1.需用温度计的实验有:(1)、实验室制乙烯(170℃) (2)、蒸馏〔说明〕:(1)凡需要准确控制温度者均需用温度计。
《有机化学基础》必背化学方程式

高中选修有机化学方程式精华版1. CH4+Cl2 CH3Cl + HCl取代反应2. CH2=CH2 + Br2 CH2BrCH2Br加成反应3.nCH2 CH—CH3加聚反应4.CH3CH2OH消去反应(实验室制取乙烯) CaC2+2H2O Ca(OH)2+C2H2↑水解反应(实验室制取乙炔)6.加成反应7.+Br2 CHBr2—CHBr2加成反应8.9.+Br2 +HBr取代反应10.+HO—NO2+H2O 取代反应11.取代反应12. C x H y+(x+y4)O2 xCO2+y2H2O氧化反应13. C2H5—Br+NaOH C2H5—OH+NaBr水解反应(取代反应)14. CH3CH2Br+NaOH CH2 CH2↑+NaBr+H2O消去反应15. 2CH3CH2OH+2Na 2CH3CH2ONa+H2↑置换反应16.CH3CH2OH+HBr CH3CH2Br+H2O取代反应17.2CH3CH2OH+O2 2CH3CHO+2H2O氧化反应18.C6H5ONa+CO2+H2O C6H5OH+NaHCO3复分解反应19.+3Br 2↓+3HBr取代反应20.CH3CHO+2Ag(NH3)2OH CH3COONH4+2Ag↓+3NH3+H2O氧化反应21.CH3CHO+2Cu(OH)2+NaOH CH3COONa+Cu2O↓+3H2O氧化反应22. 2CH3CHO+O2 2CH3COOH氧化反应23.CH3CHO+H2 CH3CH2OH还原反应(加成反应)24. CH3COOH+C2H5OH CH3COOC2H5+H2O 酯化反应(取代反应)25. RCOOR’+H2O RCOOH+R’OH水解反应(取代反应)26. RCOOR’+NaOH RCOONa + R’OH水解反应(取代反应)27. C6H12O6+6O2 6CO2+6H2O氧化反应28. C12H22O11蔗糖+H2O C6H12O6葡萄糖+C6H12O6果糖水解反应30. C12H22O11麦芽糖+H2O2C6H12O6葡萄糖水解反应31. (C6H10O5)n淀粉+nH2O nC6H12O6葡萄糖水解反应32. C6H12O6葡萄糖2C2H5OH+2CO2↑。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
光照 光照 光照 光照 高温 CaO △ 催化剂 加热、加压 催化剂
催化剂 △ 催化剂 △ 催化剂 催化剂
催化剂
催化剂 △ 催化剂
催化剂 浓硫酸 △ △
高中基础有机化学方程式总汇
1. CH 4 + Cl 2 CH 3Cl + HCl
2. CH 3Cl + Cl 2 CH 2Cl 2 + HCl
3. CH 2Cl 2 + Cl 2 CHCl 3 + HCl
4. CHCl 3 + Cl 2 CCl 4+ HCl
5. CH 4 C +2H 2
6. C 16H 34 C 8H 18 + C 8H 16
7. CH 3COONa + NaOH CH 4↑+ Na 2CO 3
8. CH 2 = CH 2 + Br 2 CH 2Br —CH 2Br
9. CH 2 = CH 2 + H 2O CH 3CH 2OH
10. CH 2 = CH 2 + HBr CH 3—CH 2Br 11. CH 2 = CH 2 + H 2 CH 3—CH 3 12. nCH 2 = CH 2 [ CH 2—CH 2 ] n
13. nCH 2=CH-CH=CH 2 [CH 2-CH=CH-CH 2] n
14. 2CH 2 = CH 2 + O 2 2CH 3CHO
15. CH ≡CH + Br 2 CHBr = CHBr
16. CHBr = CHBr+ Br 2 CHBr 2-CHBr 2
17. CH ≡CH + HCl H 2C = CHCl
18. nCH 2 = CH [ CH 2-CH ] n
Cl Cl
19. CH ≡CH + H 2O CH 3CHO
20. CaC 2 + 2H 2O CH ≡CH ↑+ Ca(OH)2
21. + Br 2 Br + HBr
22. + HO -NO 2 NO 2 +H 2O 23. + HO -SO 3H SO 3H+H 2O
CH 3 NO 2
NO 2 O 2N CH 3
催化剂 NaOH
H 2O 醇 △ 催化剂 △
浓硫酸 170℃
浓硫酸 140℃
OH Br Br OH 催化剂 △
催化剂 △
△
△ Br 催化剂 △ 24.
+ 3H 2 25. +3HO -NO 2 +3H 2O
26. 3CH ≡C H → 27. CH 3CH 2Br + H 2O CH 3CH 2OH + HBr
28. CH 3CH 2Br + NaOH CH 3CH 2OH + NaBr
29. CH 3CH 2Br+ NaOH CH 2 = CH 2 + NaBr +H 2O 30. 2CH 3CH 2OH+2Na 2CH 3CH 2ONa + H 2↑
31. 2CH 3CH 2OH+O 2 2CH 3CHO + 2H 2O 32. CH 3CH 2OH CH 2 = CH 2↑+ H 2O 33.C 2H 5OH+C 2H 5OH C 2H 5OC 2H 5+H 2O 34. OH+NaOH ONa+H 2O
35. OH+H 2O O -+H 3O +
36. ONa+H 2O+CO 2 OH+ NaHCO 3
37. +3Br 2 ↓ +3HBr
38. 2CH 3CHO + H 2 2CH 3CH 2OH 39. 2CH 3CHO + O 2 2CH 3COOH 40. CH 3CHO+2Ag(NH 3)2OH CH 3COONH 4+2Ag ↓+3NH 3+H 2O
41CH 3CHO+2Cu(OH)2 CH 3COOH+Cu 2O ↓+2H 2O 42. 2CH 3COOH+2Na 2CH 3COONa+H 2↑
43.2CH 3COOH+Na 2CO 3 2CH 3COONa+H 2O+CO 2↑
44. CH 3COOH+NaHCO 3 CH 3COONa+H 2O+CO 2↑
45. CH 3COOH + NaOH CH 3COONa + H 2O
浓硫酸 △ 催化剂 催化剂 催化剂 催化剂 催化剂 △ 催化剂 加热、加压 + 浓硫酸 △ + 2H 2O
O O
C — C O O CH 2-CH 2
46. 2CH 3COOH + Cu(OH)2 (CH 3COO)2Cu + 2H 2O
47.CH 3COOH+CH 3CH 2OH CH 3COOCH 2CH 3 +H 2O 48. CH 3COOCH 2CH 3+NaOH CH 3COONa+CH 3CH 2OH
49. nOHCH 2CH 2COO H → [ OCH 2CH 2C ] n +H 2O
50. C 6H 12O 6 (s) + 6O 2 (g) 6CO 2 (g) + 6H 2O (l)
51. C 6H 12O 6 2CH 3CH 2OH + 2CO 2
52. C 12H 22O 11+H 2O C 6H 12O 6+ C 6H 12O 6
蔗糖 葡萄糖 果糖
53. C 12H 22O 11 + H 2O 2C 6H 12O 6
麦芽唐 葡萄糖
54. (C 6H 10O 5)n + nH 2O n C 6H 12O 6
淀粉 葡萄糖
55. (C 6H 10O 5)n + nH 2O n C 6H 12O 6 纤维素 葡萄糖
56.C 17H 33COO-CH 2 C 17H 35COO-CH 2 C 17H 33COO-CH +3H 2 C 17H 35COO-CH C 17H 33COO-CH 2 C 17H 35COO-CH 2
57. C 17H 35COO-CH 2 CH 2-OH
C 17H 35COO-CH +3NaOH 3C 17H 35COONa+ CH-OH
C 17H 35COO-CH 2 CH 2-OH 58. CH 2OH COOH CH
2OH
COOH 1.HCl Cl
CH Cl CH +−→−+324光
HCl Cl CH Cl Cl CH +−→−+2223光 2.
3.
4.
5.
6.
7.
8.
222Br CH CH CH CH +=-= 9.
10.
11.
12.
13.
14.
15.
16.
17. OH NH Ag CHO CHOH HOCH 2342)(2)(+
O H NH Ag COONH CHOH HOCH 2344232)(++↓+−→−∆
18.
19.
20.
21.
高中有机化学知识点总结
1.需水浴加热的反应有:
(1)、银镜反应(2)、乙酸乙酯的水解(3)苯的硝化(4)糖的水解
(5)、酚醛树脂的制取(6)固体溶解度的测定
凡是在不高于100℃的条件下反应,均可用水浴加热,其优点:温度变化平稳,不会大起大落,有利于反应的进行。
2.需用温度计的实验有:
(1)、实验室制乙烯(170℃)(2)、蒸馏(3)、固体溶解度的测定
(4)、乙酸乙酯的水解(70-80℃)(5)、中和热的测定
(6)制硝基苯(50-60℃)
〔说明〕:(1)凡需要准确控制温度者均需用温度计。
(2)注意温度计水银球的位置。
3.能与Na反应的有机物有:醇、酚、羧酸等——凡含羟基的化合物。
4.能发生银镜反应的物质有:
醛、甲酸、甲酸盐、甲酸酯、葡萄糖、麦芽糖——凡含醛基的物质。
5.能使高锰酸钾酸性溶液褪色的物质有:
(1)含有碳碳双键、碳碳叁键的烃和烃的衍生物、苯的同系物
(2)含有羟基的化合物如醇和酚类物质
(3)含有醛基的化合物
(4)具有还原性的无机物(如SO2、FeSO4、KI、HCl、H2O2等)
6.能使溴水褪色的物质有:
(1)含有碳碳双键和碳碳叁键的烃和烃的衍生物(加成)
(2)苯酚等酚类物质(取代)
(3)含醛基物质(氧化)
(4)碱性物质(如NaOH、Na2CO3)(氧化还原――歧化反应)
(5)较强的无机还原剂(如SO2、KI、FeSO4等)(氧化)
(6)有机溶剂(如苯和苯的同系物、四氯甲烷、汽油、已烷等,属于萃取,使水层褪色而有机层呈橙红色。
)
7.密度比水大的液体有机物有:溴乙烷、溴苯、硝基苯、四氯化碳等。
8、密度比水小的液体有机物有:烃、大多数酯、一氯烷烃。
9.能发生水解反应的物质有
卤代烃、酯(油脂)、二糖、多糖、蛋白质(肽)、盐。
10.不溶于水的有机物有:
烃、卤代烃、酯、淀粉、纤维素
11.常温下为气体的有机物有:
分子中含有碳原子数小于或等于4的烃(新戊烷例外)、一氯甲烷、甲醛。
12.浓硫酸、加热条件下发生的反应有:
苯及苯的同系物的硝化、磺化、醇的脱水反应、酯化反应、纤维素的水解
13.能被氧化的物质有:
含有碳碳双键或碳碳叁键的不饱和化合物(KMnO4)、苯的同系物、醇、醛、酚。
大多数有机物都可以燃烧,燃烧都是被氧气氧化。
14.显酸性的有机物有:含有酚羟基和羧基的化合物。
15.能使蛋白质变性的物质有:强酸、强碱、重金属盐、甲醛、苯酚、强氧化剂、浓的酒精、双氧水、碘酒、三氯乙酸等。
16.既能与酸又能与碱反应的有机物:具有酸、碱双官能团的有机物(氨基酸、蛋白质等)17.能与NaOH溶液发生反应的有机物:
(1)酚:
(2)羧酸:
(3)卤代烃(水溶液:水解;醇溶液:消去)
(4)酯:(水解,不加热反应慢,加热反应快)
(5)蛋白质(水解)
18、有明显颜色变化的有机反应:
1.苯酚与三氯化铁溶液反应呈紫色;
2.KMnO4酸性溶液的褪色;
3.溴水的褪色;
4.淀粉遇碘单质变蓝色。
5.蛋白质遇浓硝酸呈黄色颜色反应。
