PH值检测数据记录表
水质分析成果台账

水质分析成果台账一、项目描述该项目是对水体的水质状况进行全面分析和评估,以确保水质符合相应的环保要求和安全标准。
本项目主要包括采样、实验室测试、数据分析和结果汇报等环节。
二、采样过程1.采样时间:2024年5月1日至5月5日,每日上午8时至下午5时进行。
2.采样点位:共设立10个采样点,包括山塘、河流、湖泊等不同类型水体。
3.采样工具:采用无菌玻璃瓶作为采样容器,每个采样点位采集2L 水样。
4.采样方法:每个采样点位进行5次独立采样,随机选取5个不同位置,保证样品的代表性。
5.采样记录:每次采样时记录采样点位、采样时间、天气情况、采样深度等信息,并编号标识。
三、实验室测试1.pH值测定:使用PHS-3C电极仪进行检测,采用标准曲线法计算pH 值。
2.溶解氧测定:采用WP6880型溶解氧仪进行检测,测量值以毫克/升为单位。
3. 氨氮测定:使用Nessler法进行测定,结果以毫克/升为单位。
4.总硬度测定:采用EDTA络合滴定法进行测定,结果以毫克/升为单位。
5.总大肠菌群测定:采用多管最概胜法进行测定,结果以最概胜值(MPN)为单位。
6.COD测定:采用高锰酸钾法进行测定,结果以毫克/升为单位。
7.浊度测定:使用NTU浊度计进行测定,结果以浊度单位(NTU)表示。
四、数据分析1.统计分析:对每个指标的测定结果进行统计分析,包括平均值、标准差、最大值和最小值等。
2.对比分析:将测定结果与相关限值进行对比分析,判断是否符合环保要求和安全标准。
3.趋势分析:根据历史数据和测定结果,分析水质状况的变化趋势。
五、结果汇报在本次水质分析中,共采集到50个独立样品,并进行了全面的实验室测试。
下表为各指标的测定结果和分析汇总:采样点位, pH值,溶解氧(mg/L),氨氮(mg/L),总硬度(mg/L),总大肠菌群(MPN), COD(mg/L),浊度(NTU)-,-,-,-,-,-,-,-采样点1,7.2,6.5,0.8,120,300,15,5采样点2,6.8,7.2,1.2,150,500,20,8采样点3,7.5,5.6,0.5,100,200,12,4采样点4,7.0,6.0,1.0,130,400,18,10采样点5,7.4,6.8,0.7,140,250,14,6采样点6,7.1,6.4,0.9,125,350,16,7采样点7,7.3,5.8,0.6,110,150,10,3采样点8,7.6,7.0,1.1,160,450,22,9采样点9,7.0,6.2,0.9,130,400,18,8分析结果显示,各指标测定值均在正常范围内,并且没有超过环保要求和安全标准。
水样采集与pH值测定

通常把粒径在10微米以下的颗粒物称为PM10,又称为 可吸入颗粒物(Inholable Particles,简称IP)。 可吸入颗粒物(PM10)在环境空气中持续的时间很长, 对人体健康和大气能见度影响都很大。
一些颗粒物来自污染源的直接排放,比如烟囱与车辆。
另一些则是由环境空气中硫的氧化物、氮氧化物、挥 发性有机化合物及其它化合物互相作用形成的细小颗 粒物,
总悬浮颗粒物由天然及人为来源产生,包括海洋、泥土、 车辆废气、工业活动、建筑工程以及气相化学反应。
总悬浮颗粒物可分为一次颗粒物和二次颗粒物。
一次颗粒物是由天然污染源和认为污染源释放到大气中 直接造成污染的物质,如:风扬起的灰尘、燃烧和工业 烟尘。
二次颗粒物是通过某些大气化学过程所产生的微粒,如: 二氧化硫转化生成硫酸盐。颗粒物的组成复杂,其中的 粗颗粒主要是由风沙、灰土及机械粉碎的水泥、石灰等 自然因素形成的;细颗粒是人为活动的产物,如燃料未 完全燃烧形成的炭粒、污染物在空气中由于光化学反应 形成的二次污染物气溶胶(如硫酸盐、硝酸盐、铵盐
它们的化学和物理组成依地点、气候、一年中的季节 不同而变化很大。
可吸入颗粒物通常来自在未铺沥青、水泥的路面上行
3. 大气采样器
大气采样器是采集 大气污染物或采集 受污染气体的仪器 或装置。 一般由空气泵、收 集器和流量器三部 分组成。
四、实验步骤
1. 大气滤膜称量; 2. 大气滤膜装载; 3. 参数设定; 4. 仪器启动; 5. 参数读取; 6. 滤膜卸载; 7. 滤膜和样品称重;
空气污染指数对应的空气质量级 别
空气污染指 数(API)
空气质 量级 别
空气质量状 况
对健康的影响
对应空气质量 的适用范围
附录1 推荐的试验检测数据记录文件及报告文唯一性标识编码表汇总

0708
粉煤灰比表面积试验检测记录表(勃氏法)
JJ0708
siO2、Al2O3、Fe2O3含量
0709
SiO2、Al2O3、Fe2O3含量试验检测记录表
JJ0709
8
沥青
密度
0801
沥青密度试验检测记录表
JJ0801
道路石油沥青试验检测报告JB010801
道路用乳化沥青试验检测报告18010802
JJ0218
冲击值
0219
粗集料冲击值试验检测记录表
JJ0219
3
岩石
单轴抗压强度
0301
岩石单轴抗压强度试验检测记录表(立方体)
JJ0301a
岩石试验检测Βιβλιοθήκη 告JB010301岩石单轴抗压强度试验检测记录表(圆柱体)
JJ0301b
抗冻性
0302
岩石抗冻性试验检测记录表
JJ0302
含水率
0303
岩石含水率试验检测记录表
粉煤灰试验检测报告JB010702
无机结合稳定材料击实试验检测报告JB010703
无机结合料无侧限抗压强度试验检测报告JB010704
水泥(石灰)剂量标准曲线试验检测报告JB010705
矿料级配合成试验检测检测报告JB010706
无机结合料配合比设计试验检测报告JB30707
最佳含水量
0702
无侧限抗压强度
附录1推荐的试验检测数据记录文件及报告文唯一性标识编码表
序号
项目
参数
参数号
表格名称
记录表号
报告编号
1
土
颗粒级配
0101
土的颗粒分析试验检测记录表(筛分法)
新方法验证报告(pH 便携式pH计法 《水和废水监测分析方法》)

XXXX有限公司新项目方法验证能力确认报告pH 便携式pH计法《水和废水监测分析方法》(第四版项目名称:增补版)国家环境保护总局(2002年)负责人:审核人:日期:pH 便携式pH计法《水和废水监测分析方法》(第四版增补版)国家环境保护总局(2002年)方法验证能力确认报告1、方法依据及适用范围本方法依据是pH 便携式pH计法《水和废水监测分析方法》(第四版增补版)国家环境保护总局(2002年)本方法能力验证应随标准更新而更新。
本方法还用于水质pH值的测定。
2、方法原理以玻璃电极为指示电极,以Ag/AgCl等为参比电极合在一起组成pH复合电极,利用pH复合电极电动势随似离了活度变化而发生偏移来测定水样的pH值,复合电极pH计均有温度补偿装置,用以校正温度对地极的影响,用于常规水样监测可准确至0.1pH单位。
较精密仪器可准确到0.01pH单位,为了提高测定的准确度,校准仪器时选用的标准缓冲溶液的pH值应与水样的pH值接近。
3、主要仪器、设备及试剂除非另有说明,分析时均使用符合国家标准的分析纯试剂。
3.1试剂和材料3.1.1配制标准溶液所用的蒸馏水应符合下列要求:煮沸并冷却、电导率小于2×10-6S/cm的蒸馏水,其pH 以6.7~7.3之间为宜。
3.1.2测量pH时,按水样呈酸性,中性和碱性三种可能,常配制以下三种标准溶液:1)pH标准溶液(pH4.008 25℃):c(C8H5KO4)=0.05mol/L,标准证书编号:XXXXXXXX,有效期限:XXXX年XX月XX日。
2)pH标准溶液(pH6.865 25℃):c(KH2PO4)=0.025mol/L,标准证书编号:XXXXXXXX,有效期限:XXXX年XX月XX日。
3)pH标准溶液(pH9.180 25℃):c(Na2B4O7)=0.01mol/L,标准证书编号:XXXXXXXX,有效期限:XXXX年XX月XX日。
3.1.3标准溶浓的保存:标准溶液要在聚乙稀瓶中密闭保存,在室温条件下标准溶浓一般以保存1~2个月为宜,当发现有浑浊、发霉或沉淀现象时,不能继续使用。
十标准缓冲液pH值对照参考表
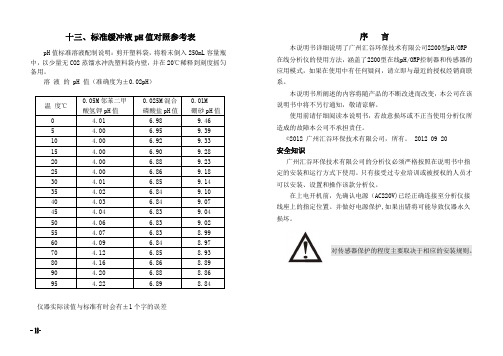
十三、标准缓冲液pH值对照参考表pH值标准溶液配制说明:剪开塑料袋,将粉末倒入250mL容量瓶中,以少量无CO2蒸馏水冲洗塑料袋内壁,并在20℃稀释到刻度摇匀备用。
溶液的 pH 值(准确度为±0.02pH)温度℃0.05M邻苯二甲酸氢钾pH值0.025M混合磷酸盐pH值0.01M硼砂pH值0 4.01 6.98 9.465 4.00 6.95 9.3910 4.00 6.92 9.3315 4.00 6.90 9.2820 4.00 6.88 9.2325 4.00 6.86 9.1830 4.01 6.85 9.1435 4.02 6.84 9.1040 4.03 6.84 9.0745 4.04 6.83 9.0450 4.06 6.83 9.0255 4.07 6.83 8.9960 4.09 6.84 8.9770 4.12 6.85 8.9380 4.16 6.86 8.8990 4.20 6.88 8.8695 4.22 6.89 8.84 仪器实际读值与标准有时会有±1个字的误差序言本说明书详细说明了广州汇谷环保技术有限公司2200型pH/ORP在线分析仪的使用方法,涵盖了2200型在线pH/ORP控制器和传感器的应用模式,如果在使用中有任何疑问,请立即与最近的授权经销商联系。
本说明书所阐述的内容将随产品的不断改进而改变,本公司在该说明书中将不另行通知,敬请谅解。
使用前请仔细阅读本说明书,若故意损坏或不正当使用分析仪所造成的故障本公司不承担责任。
©2012 广州汇谷环保技术有限公司,所有。
2012 09 20安全知识广州汇谷环保技术有限公司的分析仪必须严格按照在说明书中指定的安装和运行方式下使用。
只有接受过专业培训或被授权的人员才可以安装、设置和操作该款分析仪。
在上电开机前,先确认电源(AC220V)已经正确连接至分析仪接线座上的指定位置。
并做好电源保护,如果出错将可能导致仪器永久损坏。
电位法测定水溶液的pH值

实验1 电位法测定水溶液的pH值一、实验目的1.掌握用玻璃电极测量溶液pH值的基本原理和测量技术;2.学会怎样测定玻璃电极的响应斜率,进一步加深对玻璃电极响应特性的了解。
二、方法原理以玻璃电极作指示电极,饱和甘汞电极作参比电极,用电位法测量溶液的pH值,组成测量电池的图解表示式为:电池的电动势等于各相界电位的代数和。
即,其中为试液与饱和氯化钾溶液之间的液接电位E j,于是当测量体系确定后,式中E(电池)、E(Ag,AgCl)及E j均为常数,而合并常数项,电动势可表示为:其中0.059为玻璃电极在25℃的理论响应斜率。
由于玻璃电极常数项,或说电池的“常数”电位值无法准确确定,故实际中测量pH值的方法是采用相对方法。
即选用pH值已经确定的标准缓冲溶液进行比较而得到欲测溶液的pH值。
为此,pH值通常被定义为其溶液所测电动势与标准溶液的电动势差有关的函数,其关系式是: (1)式中pH x和pH s分别为欲测溶液和标准溶液的pH值,E x和E s分别为其相应电动势。
该式常称为pH值的实用定义。
测定pH用的仪器-pH电位计是按上述原理设计制成的。
例如在25℃时,pH计设计为单位pH变化58mV。
若玻璃电极在实际测量中响应斜率不符合58mV的理论值,这时仍用一个标准pH缓冲溶液校准pH计,就会因电极响应斜率与仪器不一致引入测量误差。
为了提高测量的准确度,需用双标准pH缓冲溶液法将pH计的单位pH的电位变化与电极的电位变化校为一致。
当用双标准pH缓冲溶液法时,电位计的单位pH变化率S可校定为: (2)式中pH(s,1)和pH(s,2)分别为标准pH缓冲溶液1和2的pH值,E(s,1)和E(s,2)分别为其电动势。
代入(1)式,得:从而消除了电极响应斜率与仪器原设计值不一致引入的误差。
显然,标准缓冲溶液的pH值是否准确可靠,是准确测量pH值的关键。
目前,我国所建立的pH标准溶液体系有7个缓冲溶液,它们在0~95℃的标准pH值可查阅相关文献。
探究盐溶液的酸碱性试验记录 (2)

02
实验原理
盐的水解原理
盐的水解是指盐溶液中的盐离子 或阴、阳离子与水电离出的氢离 子或氢氧根离子结合,生成弱电
解质的过程。
盐的水解反应通常为可逆反应, 受溶液的酸碱度和温度等因素影
学习使用酸碱指示剂
酸碱指示剂是一种用于指示溶液酸碱性的化学试剂。通过实 验,可以学习如何正确使用酸碱指示剂,了解其在不同酸碱 度下的颜色变化。
在实验过程中,需要注意指示剂的浓度和滴定方法,以确保 实验结果的准确性。
掌握pH值的测定方法
pH值是衡量溶液酸碱性的一个重要指标。通过实验,可以掌握使用pH试纸或pH 计测定溶液pH值的方法。
使用滴管分别取适量的不同种类的盐溶液,滴在pH试纸上 。
观察试纸的颜色变化,与标准比色卡进行对比,记录盐溶 液的pH值。
记录实验数据和现象
记录每种盐溶液的浓度、体积以及测得的pH值。
记录实验过程中观察到的现象,如是否有沉淀生成、颜色变化等。
通过以上实验步骤,我们可以探究不同种类的盐溶液的酸碱性,并记录实验数据和现象。在实验过程中, 需要注意安全事项,如避免试剂接触皮肤和眼睛,以及正确使用实验器材等。
通过实验,我学会了使用酸碱指示剂 和pH试纸测定溶液的酸碱性,以及如 何正确操作滴定管等实验器材。
通过实验观察、记录和分析数据,我 学会了科学探究的方法,提高了分析 和解决问题的能力。
加深对盐类水解的理解
实验让我更加深入地理解了盐类水解 的原理及其在日常生活中的应用,如 食盐、小苏打等。
实验不足与改进建议
04
实验结果与分析
实验数据汇总
污水处理检测记录

污水处理检测记录一、引言污水处理是保护环境和人类健康的重要措施之一。
为了确保污水处理设施的正常运行和效果,进行污水处理检测是必不可少的工作。
本文将详细介绍污水处理检测记录的标准格式。
二、检测记录基本信息1. 检测记录编号:WSD-2022-0012. 检测日期:2022年7月15日3. 检测地点:某市XX污水处理厂4. 检测人员:张工、李工5. 检测设备:pH计、溶解氧仪、浊度计等三、检测项目及结果1. 污水流量检测:- 检测方法:使用流量计测量污水处理厂进水口和出水口的流量- 检测结果:进水口流量为500m³/h,出水口流量为450m³/h2. 污水pH值检测:- 检测方法:使用pH计对进水口和出水口的污水进行检测- 检测结果:进水口pH值为7.2,出水口pH值为7.53. 溶解氧检测:- 检测方法:使用溶解氧仪对进水口和出水口的污水进行检测- 检测结果:进水口溶解氧含量为5.6mg/L,出水口溶解氧含量为6.2mg/L4. 污水浊度检测:- 检测方法:使用浊度计对进水口和出水口的污水进行检测- 检测结果:进水口浊度为50NTU,出水口浊度为10NTU5. 污水COD(化学需氧量)检测:- 检测方法:采用标准化学分析方法对进水口和出水口的污水进行检测- 检测结果:进水口COD浓度为200mg/L,出水口COD浓度为50mg/L6. 污水氨氮检测:- 检测方法:采用标准化学分析方法对进水口和出水口的污水进行检测- 检测结果:进水口氨氮浓度为20mg/L,出水口氨氮浓度为5mg/L四、数据分析与结论根据以上检测结果,可以得出以下结论:1. 污水处理厂的进水口流量为500m³/h,出水口流量为450m³/h,出水口流量略低于进水口流量,可能由于设备运行不稳定导致。
2. 污水处理厂的出水口pH值为7.5,处于中性偏碱性范围,符合环境排放标准。
3. 污水处理厂的出水口溶解氧含量为6.2mg/L,高于进水口溶解氧含量,表明污水处理过程中溶解氧得到一定程度的补充。
土壤学实验报告
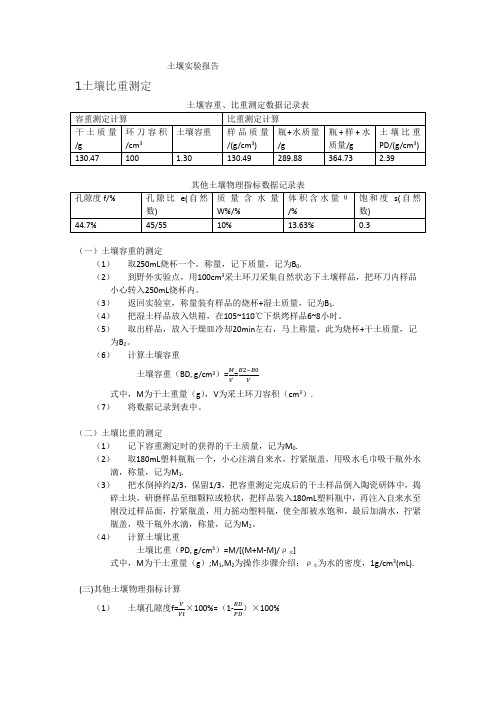
土壤实验报告1土壤比重测定土壤容重、比重测定数据记录表(一)土壤容重的测定(1)取250mL烧杯一个,称量,记下质量,记为B0.(2)到野外实验点,用100cm3采土环刀采集自然状态下土壤样品,把环刀内样品小心转入250mL烧杯内。
(3)返回实验室,称量装有样品的烧杯+湿土质量,记为B1.(4)把湿土样品放入烘箱,在105~110℃下烘烤样品6~8小时。
(5)取出样品,放入干燥皿冷却20min左右,马上称量,此为烧杯+干土质量,记为B2。
(6)计算土壤容重土壤容重(BD, g/cm3)=MV =B2−B0V式中,M为干土重量(g),V为采土环刀容积(cm3).(7)将数据记录到表中。
(二)土壤比重的测定(1)记下容重测定时的获得的干土质量,记为M0.(2)取180mL塑料瓶瓶一个,小心注满自来水,拧紧瓶盖,用吸水毛巾吸干瓶外水滴,称量,记为M1.(3)把水倒掉约2/3,保留1/3,把容重测定完成后的干土样品倒入陶瓷研钵中,捣碎土块,研磨样品至细颗粒或粉状,把样品装入180mL塑料瓶中,再注入自来水至刚没过样品面,拧紧瓶盖,用力摇动塑料瓶,使全部被水饱和,最后加满水,拧紧瓶盖,吸干瓶外水滴,称量,记为M2。
(4)计算土壤比重土壤比重(PD, g/cm3)=M/[(M+M-M)/ρ水]式中,M为干土重量(g);M1,M2为操作步骤介绍;ρ水为水的密度,1g/cm3(mL).(三)其他土壤物理指标计算(1)土壤孔隙度f=VVt ×100%=(1-BDPD)×100%(2)土壤孔隙比e=VfVs =f 1−f(3)质量含水量(即土壤水分含水量)W=MwMs×100(4)容积含水量θ=VwVs=W×BD(%)(5)饱和度s=VwVf =θf2土壤机械组成测定(一)土壤机械组成测定(1)制备悬液柱。
将50g样品全部洗入1000 mL,为土壤悬液柱,用于测定悬液比重。
(2)搅拌样品。
电位法测定水溶液的ph值实验报告

电位法测定水溶液的ph值实验报告下载提示:该文档是本店铺精心编制而成的,希望大家下载后,能够帮助大家解决实际问题。
文档下载后可定制修改,请根据实际需要进行调整和使用,谢谢!本店铺为大家提供各种类型的实用资料,如教育随笔、日记赏析、句子摘抄、古诗大全、经典美文、话题作文、工作总结、词语解析、文案摘录、其他资料等等,想了解不同资料格式和写法,敬请关注!Download tips: This document is carefully compiled by this editor. I hope that after you download it, it can help you solve practical problems. The document can be customized and modified after downloading, please adjust and use it according to actual needs, thank you! In addition, this shop provides you with various types of practical materials, such as educational essays, diary appreciation, sentence excerpts, ancient poems, classic articles, topic composition, work summary, word parsing, copy excerpts, other materials and so on, want to know different data formats and writing methods, please pay attention!电位法测定水溶液的pH值实验报告1. 引言在化学实验中,测定溶液的pH值是一项基础且重要的操作。
水处理实验-混凝

水处理实验设计—污水的混凝处理实验一、实验目的为了深入了解絮凝理论在水处理领域的应用和进一步掌握絮凝剂的特性,针对污染水体进行絮凝沉淀处理实验,观察絮凝沉淀过程并探讨絮凝剂在水处理过程中的最佳添加量。
二、实验要求1、要求认识几种絮凝剂,掌握其配制方法。
2、观察水处理过程中的絮凝现象,从而加深对絮凝理论的理解。
3、认识絮凝理论对污染水处理的重要意义。
三、实验原理所谓絮凝剂或者混凝剂是指:凡是能使水溶液中的溶质、胶体或者悬浮物颗粒产生絮状沉淀的水处理剂。
天然水或工业污水水中除了含有泥砂、颗粒很细的尘土、腐殖质、淀粉、纤维素、细菌、藻类等微生物。
这些杂质与水形成溶胶状态的胶体微粒,由于布朗运动和静电排斥力而呈现沉降稳定性和聚合稳定性,通常不能利用重力自然沉降的方法除去,必须加入絮凝剂以破坏溶胶的稳定性,使细小的胶体微粒凝聚再絮凝成较大的颗粒而沉淀。
絮凝机理一般有三种:(1)电解质对双电层的作用(图1)水中的悬浮物或固体微粒通常呈胶体状态分布,它们具有巨大的比表面,可吸附液体中的正离子或负离子或极性分子,使固液两相界面上的电荷分布不均匀而产生电位差。
加入电解质,使固体颗粒的表面形成的双电层有效厚度减少,使范德华引力占优势而达到彼此吸引,最后达到凝聚。
(2)吸附架桥作用机理(图2)当加入少量高分子电解质时,由于胶粒对高分子物质有强烈的吸附作用,高分子长链一端吸附在一个胶粒表面上,另一端又被其他胶粒吸附,形成一个高分子链状物。
高分子长链像各胶粒间的桥梁,将胶粒联结在一起形成絮凝体,最终沉降。
(3)沉淀物卷扫作用机理(图3)当水中加入较多的铝盐或铁盐等药剂后,在水中形成高聚合度的氢氧化物,可以吸附卷带水中胶粒而沉淀。
图1 固体微粒的双电层结构图2 高分子聚合物的吸附架桥作用图3沉淀物卷扫作用机理本次实验选择铝系絮凝剂(硫酸铝Al2(SO4)3)。
铝离子在水溶液中首先形成水合离子,也可以视为水分子作配位体的络合离子,通过水合离子的酸性离解即水解作用生成氢氧化物或羟基络离子。
环境监测原始数据记录表(参考)

pH、电导率测试原始记录 (3)_____________离子选择电极法分析原始记录 (4)红外(非分散)分光光度法分析原始记录 (5)标准曲线和质控记录 (6)______________分光光度法分析原始记录 (7)容量分析法原始记录(Ⅰ) (8)容量分析法原始记录(Ⅱ) (9)五日生化需氧量分析记录(Ⅰ) (10)五日生化需氧量分析记录(Ⅱ) (11)五日生化需氧量分析记录(Ⅲ) (12)五日生化需氧量分析记录(Ⅳ) (13)重量法分析原始记录 (14)标准溶液配制及标定记录 (15)一般试剂配制记录 (16)分析原始记录 (17)污染源废水采样和交接记录 (18)水生生物采样和交接记录 (20)大气环境采样和交接记录表 (21)大气环境采样和交接记录(24小时) (23)________________噪声监测原始记录 (25)区域环境噪声监测原始记录 (27)工业企业厂界噪声测量记录 (28)铁路边界噪声监测原始记录 (29)交通噪声监测原始记录 (30)样品委托单 (31)监测结果统计表 (32)实验室环境条件记录表 (33)样品保存条件记录表 (34)废(烟)气状态参数现场测试记录(Ⅰ) (35)废(烟)气状态参数现场测试记录(Ⅱ) (36)林格曼黑度原始记录表 (37)生化需氧量原始记录 (38)环境振动测量记录表 (39)pH、电导率测试原始记录项目名称样品性质分析项目分析方法及来源仪器名称及编号电极常数分析日期室温℃标准缓冲液(Ⅰ)理论值标准缓冲液(Ⅱ)理论值标准缓冲液(Ⅲ)理论值样品编号水温(℃)pH 读数值样品PH值电导率kt (μScm-1)25℃电导率kt (μScm-1)计算公式第一次第二次备注分析者___________________________ 校对者____________________ 共__页第__页_____________离子选择电极法分析原始记录项目名称样品性质分析项目分析方法及来源仪器名称及编号分析日期水温℃缓冲液名称及加入量室温______℃分析者___________________________ 校对者____________________ 共__页第__页红外(非分散)分光光度法分析原始记录项目名称分析项目分析方法及来源分析日期仪器名称及编号萃取液名称比色皿mm 参比液室温______℃湿度_______%分析者___________________________ 校对者____________________ 共__页第__页标准曲线和质控记录加标液浓度()响应值A回收率(%)分析者___________________________ 校对者____________________ 共__页第__页______________分光光度法分析原始记录项目名称样品性质分析项目分析日期分析方法及来源仪器名称及编号标准溶液名称显色温度℃显色时间______________显色体积___________参比溶液测定波长nm 比色皿mm室温_____℃湿度____%分析者___________________________ 校对者____________________ 共__页第__页容量分析法原始记录(Ⅰ)项目名称样品性质分析项目分析日期分析方法及来源仪器名称及编号分析者___________________________ 校对者____________________ 共__页第__页容量分析法原始记录(Ⅱ)项目名称样品性质分析项目分析日期分析方法及来源仪器名称及编号分析者___________________________ 校对者____________________ 共__页第__页五日生化需氧量分析记录(Ⅰ)项目名称 样品性质 分析方法及来源 仪器名称及编号培养时间 月 日 时 至 月 日 时 培养箱温度 标准溶液浓度 稀释水制备日期 培养前分析日期 室温 ℃培养后分析日期 室温 ℃分析者___________________________ 校对者_________________________ 共__页 第__页样品编号稀释比f培养瓶号____________________标准溶液消耗量(mL )化学探头测定法溶解氧浓度(mg/L ) 水样BOD 5 浓度(mg/L )培养前培养后 培养前 培养后 终读数始读数用量终读数始读数用量读数Ⅰ读数Ⅱ平均值读数Ⅰ读数Ⅱ平均值培养前培养后五日生化需氧量分析记录(Ⅱ)项目名称样品性质分析方法及来源仪器名称及编号培养时间月日时至月日时培养箱温度标准溶液浓度稀释水制备日期培养前分析日期室温℃培养后分析日期室温℃稀释水____________________标准溶液消耗量(mL)化学探头测定法溶解氧浓度(mg/L)备注培养前培养后培养前培养后终读数始读数用量终读数始读数用量终读数始读数用量终读数始读数用量培养前培养后平行样检平行样编号质控样检定值(mg/L)平均值测的浓度测得值(mg/L)相对偏差(%)相对误差(%)允许相对偏差(%)允许相对偏差(%)结果评判结果评判标定序号0 0 1 2 3 平均值计算公式基准液体积(mL)空白溶液滴定记录(mL)V0V1△VNa2S2O3浓度相对偏差(%)结果评判允许相对偏差(%)分析者___________________________ 校对者_________________________ 共__页第__页五日生化需氧量分析记录(Ⅲ)项目名称样品性质分析方法及来源仪器名称及编号培养时间月日时至月日时培养箱温度稀释水制备日期培养前分析日期室温℃培养后分析日期室温℃分析者___________________________ 校对者_________________________ 共__页第__页五日生化需氧量分析记录(Ⅳ)项目名称样品性质分析方法及来源仪器名称及编号培养时间月日时至月日时培养箱温度计算公式:BOD5(mg/L)=n(C1-C2)-(n-1)(B1-B2)式中n------------稀释倍数C1,C2-----------水样培养五天前后溶解氧值(mg/l)B1,B2-----------稀释水培养五天前后溶解氧值(mg/l)分析者___________________________ 校对者_________________________ 共__页第__页重量法分析原始记录项目名称样品性质分析项目分析日期室温℃湿度% 分析方法及来源仪器名称及编号容器+滤膜+样品分析者___________________________ 校对者_________________________ 共__页第__页标准溶液配制及标定记录分析者___________________________ 校对者_________________________ 共__页第__页一般试剂配制记录配制者____________________________ 校对者__________________ 共__页第__页分析原始记录项目名称样品性质分析项目分析方法及来源仪器名称及编号分析条件_________________________分析日期_______________ 室温_______℃湿度_______%分析者___________________________ 校对者____________________ 共__页第__页污染源废水采样和交接记录项目名称被测单位名称地址邮编电话采样方式混合、连续、间歇、瞬时采样日期天气状况气温℃企业当事人签字样品编号采样点名称采样时间水样外观监测项目排污口规范化情况流速m/s宽度m深度m流量()排放量()采样者________________ PH分析者________________ 送样者_______________ 送样时间_________________ 共____页第_____页接样者________________________________ 接样时间_________________________________水生生物采样和交接记录项目名称水域名称水域功能类别调查船采样工具采样方式采样日期天气气温℃样品现场保存措施:采样者_______________ 采样时间________________ 送样者__________________ 送样时间___________________ 共____页第_____页接样者_______________ 接样时间________________大气环境采样和交接记录表项目名称采样地点测点编号功能区类采样器名称及编号流量校准值校准人校准日期采样者_______________ 采样日期________________ 送样者_______________ 送样时间_______________ 共____页第____页接样者_______________ 接样时间________________大气环境采样和交接记录(24小时)项目名称采样地点测点编号功能区类采样器名称及编号流量校准值校准人校准日期采样者_______________ 送样者_______________ 送样时间_______________ 接样者_______________ 接样时间________________采样者_______________ 送样者_______________ 送样时间_______________ 接样者_______________ 接样时间________________采样者_______________ 送样者_______________ 送样时间_______________ 接样者_______________ 接样时间________________采样者_______________ 送样者_______________ 送样时间_______________ 接样者_______________ 接样时间________________采样者_______________ 送样者_______________ 送样时间_______________ 接样者_______________ 接样时间________________ 共____页第____页________________噪声监测原始记录项目名称被测单位地址邮编联系人电话监测方法及来源测试地点测试仪器及编号测试日期测试者_________________ 校对者__________________ 共_____页第_____页区域环境噪声监测原始记录项目名称监测方法及来源测试地点测量仪器名称及编号天气状况风力测试日期测试者_________________ 校对者__________________ 共_____页第_____页工业企业厂界噪声测量记录项目名称被测单位地址邮编联系人监测方法及来源测试地点电话区域功能类型测试仪器及编号测试日期测试者_________________ 校对者__________________ 共_____页第_____页铁路边界噪声监测原始记录项目名称测试地点区域功能类型天气监测方法及来源测试仪器及编号测试日期背景噪声声级dBA测试者_________________ 校对者__________________ 共_____页第_____页交通噪声监测原始记录项目名称测试地点区域功能类型天气监测方法及来源测试仪器及编号距路肩距离(米)车流量(辆/小时)测试者_________________________ 校对者__________________ 共_____页第_____页样品委托单项目名称委托科室任务来源采样日期委托日期要求完成时间提交结果的方式委托科室室主任送样人接样人受委托科室室主任接样日期监测结果统计表项目名称_________________________ 分析项目__________________________测试日期_______________计算者_________________ 校对者__________________ 共_____页第_____页实验室环境条件记录表科室名称________ 房间号______ 仪器名称________________________样品保存条件记录表科室名称________ 房间号______ 保存的设备名称及编号______________保存类别及温度要求冷藏_______℃冷冻_______ ℃废(烟)气状态参数现场测试记录(Ⅰ)项目名称被测单位电话邮编测试仪器名称编号测试位置管道尺寸工艺设备名称及型号净化器名称及型号排气筒高度m 烟气温度℃干球温度℃湿球温度℃湿球表面压力林格曼黑度废(烟)气静压废(烟)气全压比托管型式及系数测试日期大气压KPa 环境温度℃动压Pa微压计读数测试者_____________________ 校对者_______ 共___页第___页废(烟)气状态参数现场测试记录(Ⅱ)项目名称被测单位电话邮编采样仪器名称编号测氧仪型号及编号烟气测试仪型号和编号测试位置管道尺寸安装孔深度排气筒高度m烟气温度℃工艺设备名称及型号净化器名称及型号测试日期大气压Kpa 环境温度℃测试者_____________________ 校对者____________ 共____页第____页林格曼黑度原始记录表项目名称企业名称测试日期及时间温度℃湿度% 测试仪器名称及编号工艺设备名称烟囱高度m 测试者与排放源的相对位置风向风速天气情况测试者________________ 校对者____________ 共____页第____页生化需氧量原始记录项目名称样品性质仪器名称及编号分析方法及来源室温℃湿度% 分析日期分析者_____________________ 校对者____________ 共____页第____页环境振动测量记录表项目名称企业名称地址邮编联系人电话监测方法及来源测试地点区域功能类型测试仪器及编号测试日期分析者_____________________ 校对者____________ 共____页第____页。
用pH计测定溶液的pH值

用pH计测定溶液的pH值一、实验目的1.熟悉pH构造和测定原理2.掌握用pH计测定溶液pH步骤二、实验原理pH电极的构造:玻璃电极使用前,必须在水溶液中浸泡,使之生成一个三层结构,即中间的干玻璃层和两边的水化硅胶层。
浸泡后的玻璃膜示意图:电池电动势:E电=ESCE - E膜- EAgCl,Ag而其中E膜=E外- E内=k+0.059lgαH所以E电=k′- 0.059lgαH =k′+ 0.059pH水化硅胶层具有界面,构成单独的一相,厚度一般为0.01~10 μm。
在水化层,玻璃上的Na+与H+发生离子交换而产生相界电位,也即道南电位。
水化层表面可视作阳离子交换剂。
溶液中H+经水化层扩散至干玻璃层,干玻璃层的阳离子向外扩散以补偿溶出的离子,离子的相对移动产生扩散电位。
两者之和构成膜电位。
将浸泡后的玻璃电极放入待测溶液,水合硅胶层表面与溶液中的H+活度不同,形成活度差,H+由活度大的一方向活度小的一方迁移,平衡时:H+溶液== H+硅胶E内= k1 + 0.059 lg( a2 / a2’)E外= k2 + 0.059 lg(a1 / a1’)a1 、a2 分别表示外部试液和电极内参比溶液的H+活度;a’1 、a’2 分别表示玻璃膜外、内水合硅胶层表面的H+活度;k1 、k2 则是由玻璃膜外、内表面性质决定的常数。
由于玻璃膜内、外表面的性质基本相同,则k1=k2 ,a’1 = a’2E膜= E外- E内= 0.059 lg( a1 / a2)由于内参比溶液中的H+活度(a2)是固定的,则:E膜= K´+ 0.059 lg a1 = K´- 0.059 pH试液用电位法测定溶液的pH值时,E电池=K+0.059 pH。
由于K是无法测量的,我们可以利用在相同条件下测pH值与之相近的标准缓冲溶液Es=K+0.592 pH,再通过两式来消除K,从而求得pHx= pHs+(Es-Ex)/ 0.0592V三、实验步骤打开电源开关,按“pH/mV”,进入pH测定状态,按“温度”按钮,使显示溶液温度值(25℃),然后按“确认”键,仪器确定溶液温度后回到pH测量状态。
实验报告-pH计测定溶液的pH值及磷酸的电位滴定

药院2017级药学一小班 2018年12月2日用pH计测定溶液的pH值及磷酸的电位滴定一、实验目的1、掌握用pH计测定溶液的pH值的方法及原理。
2、通过实验学会pH计仪器的使用。
3、掌握电位滴定的方法及确定终点的方法。
4、学会用电位滴定法测定弱酸的pKa.二、实验原理1、直接电位法测定溶液的pH,常以pH玻璃电极作为指示电极,饱和甘汞电极作为参比电极,浸入待测液中组成原电池。
(-)Ag|AgCl(s),内充液|玻璃膜|试液|KCl(饱和),HgCl(s)|Hg(+)pHs-25型酸度计使用复合电极,玻璃电极为负极,银-氯化银电极为正极(-)玻璃电极|待测溶液|银-氯化银(+)在实际工作中,采用两次测量法,pHs=pHs+(Ex-Es)/0.059实验操作要求:校准—用一种标准缓冲液按pH计的使用方法校准pH计检验—用校准好了的pH计测量另一种与校准时所用缓冲溶液的pH相差3个单位左右的标准缓冲液,测量值与表中所列值相差不应大于0.1pH单位测定—用校准好了的pH计测定待测溶液的pH2、电位滴定对于容量滴定中的酸碱都能滴定,且对于一些突跃范围小,无合适指示剂,溶液浑浊,有色的酸碱,都能滴定。
此外它还可测弱酸弱碱的解离常数,还可用来寻找合适指示剂或校正指示剂的终点颜色变化。
磷酸为多元酸,其pKa可用电位滴定法测定当磷酸的第一个H+被滴定一半时,此时的pH即为第一步的解离常数。
三、实验步骤(一) 1、用邻苯二甲酸氢钾pH=4.00,测定草酸三氢钾及混合磷酸盐的pH值2、用混合磷酸盐定位pH=6.88,测定硼砂及邻苯二甲酸氢钾的pH值(二)1、实验操作(1)、打开电脑上的软件,用磷酸混合溶液及邻苯二甲酸氢钾标准溶液校准pH计,保存校准数据,接着设置滴定条件,准备滴定。
(2)、用10.0ml移液管吸取磷酸样品溶液10.0ml置于100ml烧杯中,加蒸馏水20ml,放入转子,调节转速,放入复合电极以及氢氧化钠滴液管。
H2S记录表

1、脱硫水温一般在25-30度,在脱硫水箱取样口测量,测量前先放一段时间水在进行万度和PH值测量。
2、换水量、换水周期一般每隔一天更换30公分水。
3、PH值一般在3以下2左右。
4、物料TS根据化验结果记录。
5、加氧量一般在2%,流量不稳定高或低于2%不要调节加氧阀门。
6、加药量根据换水量变化。
7、测脱硫前硫化氢,先打开压力变送器的沼气输送管,放一段时间气后在进行测量。
8、脱硫后硫化氢在引水器上方测量。
9、每天运行人员控制两罐的进料差值,每天不能相差100立方物料。
10、每隔两小时记录一次数据,每两天交一次表。
测试ph值的操作方法

测试ph值的操作方法测试pH 值的操作方法通常包括以下几个步骤:准备样品、取样、调节样品的pH 值、测试pH 值、记录结果和数据分析。
下面我将详细介绍每个步骤。
1. 准备样品:首先,我们需要选择一个含有我们想要测试pH 值的样品。
这个样品可以是液体、固体或气体。
确保选择的样品是纯净的,没有受到任何污染或干扰。
2. 取样:从选定的样品中取一小部分用于测试。
如果是液体样品,使用一个清洁的容器,比如玻璃烧杯,取得适量的样品。
如果是固体样品,可以将其研磨成粉末后取样。
如果是气体样品,可以通过一定的方法将其转化成液体或固体样品,再进行取样。
3. 调节样品的pH 值:在测试之前,有时需要将样品的pH 值调节到一定范围内,以便于测试和分析。
这可以通过添加酸或碱来实现。
如果样品的pH 值过高,可以添加一些酸性物质来降低其pH 值。
如果样品的pH 值过低,可以添加一些碱性物质来提高其pH 值。
在调节之后,需要充分搅拌样品,以确保酸碱物质充分混合。
4. 测试pH 值:现在我们可以使用pH 试纸、pH 仪器或其他pH 检测装置来测量样品的pH 值。
pH 试纸是其中最常用的工具之一。
首先将pH 试纸浸入样品中,并等待一段时间,以使试纸与样品充分接触。
然后将试纸取出,并根据试纸表面的颜色变化与pH 值的颜色比对图进行比对。
通过匹配颜色,就可以得到样品的大致pH 值。
pH 仪器可以提供更精确的pH 值,但通常需要在实验室等专业环境下进行操作。
5. 记录结果:测试完成后,需要准确记录样品的pH 值。
这可以通过将结果写在实验笔记本、记录表格或电脑文档中来实现。
确保记录所有细节、条件和操作步骤,以便于后续的数据分析和比较。
6. 数据分析:最后,可以对测试结果进行数据分析。
将不同样品的pH 值进行比较,找出差异和共同点。
如果有多个样品,可以绘制pH 值的图表或图形来直观地表示不同样品之间的pH 值差异。
通过数据分析,可以得出关于样品的酸碱性质和化学特性的结论。
水处理实验-混凝

水处理实验设计—污水的混凝处理实验一、实验目的为了深入了解絮凝理论在水处理领域的应用和进一步掌握絮凝剂的特性,针对污染水体进行絮凝沉淀处理实验,观察絮凝沉淀过程并探讨絮凝剂在水处理过程中的最佳添加量。
二、实验要求1、要求认识几种絮凝剂,掌握其配制方法。
2、观察水处理过程中的絮凝现象,从而加深对絮凝理论的理解。
3、认识絮凝理论对污染水处理的重要意义。
三、实验原理所谓絮凝剂或者混凝剂是指:凡是能使水溶液中的溶质、胶体或者悬浮物颗粒产生絮状沉淀的水处理剂。
天然水或工业污水水中除了含有泥砂、颗粒很细的尘土、腐殖质、淀粉、纤维素、细菌、藻类等微生物。
这些杂质与水形成溶胶状态的胶体微粒,由于布朗运动和静电排斥力而呈现沉降稳定性和聚合稳定性,通常不能利用重力自然沉降的方法除去,必须加入絮凝剂以破坏溶胶的稳定性,使细小的胶体微粒凝聚再絮凝成较大的颗粒而沉淀。
絮凝机理一般有三种:(1)电解质对双电层的作用(图1)水中的悬浮物或固体微粒通常呈胶体状态分布,它们具有巨大的比表面,可吸附液体中的正离子或负离子或极性分子,使固液两相界面上的电荷分布不均匀而产生电位差。
加入电解质,使固体颗粒的表面形成的双电层有效厚度减少,使范德华引力占优势而达到彼此吸引,最后达到凝聚。
(2)吸附架桥作用机理(图2)当加入少量高分子电解质时,由于胶粒对高分子物质有强烈的吸附作用,高分子长链一端吸附在一个胶粒表面上,另一端又被其他胶粒吸附,形成一个高分子链状物。
高分子长链像各胶粒间的桥梁,将胶粒联结在一起形成絮凝体,最终沉降。
(3)沉淀物卷扫作用机理(图3)当水中加入较多的铝盐或铁盐等药剂后,在水中形成高聚合度的氢氧化物,可以吸附卷带水中胶粒而沉淀。
图1 固体微粒的双电层结构图2 高分子聚合物的吸附架桥作用图3沉淀物卷扫作用机理本次实验选择铝系絮凝剂(硫酸铝Al 2(SO 4)3)。
铝离子在水溶液中首先形成水合离子,也可以视为水分子作配位体的络合离子,通过水合离子的酸性离解即水解作用生成氢氧化物或羟基络离子。
pH计使用和总酸测定评分表--万国福

(4)PH计的使用和总酸度的测定评分表
日期:开始时间:结束时间:
姓名:
2010年江南大学专接本《食品分析实验》考试试题
项目四 PH 计的使用和总酸度的测定
姓名: 日期: 开始时间:
结束时间:
1、测定:吸取10.0mL 食醋样品于100mL 容量瓶中,加水至刻度,混匀。
吸取20.0mL ,置于200mL 烧杯中,加60mL 水,开动磁力搅拌器,用0.05 mol/L NaOH 标准溶液滴定至酸度计指示pH8.2,同时做试剂空白试验。
2、计算 式中:
X 1──试样中总酸的含量(以乙酸计),g/100mL ;
V 1──测定用试样稀释液消耗NaOH 标准液的体积,mL ; V 2──试剂空白消耗NaOH 标准溶液的体积,mL ; C —NaOH 标准溶液的浓度,mol/L ;
0.060—与1.0 mL NaOH 标准溶液[c(NaOH)= 1.000 mol/L]相当乙酸的质
量, g ;
V —试样体积, mL 。
结果的表述:报告算术平均值的三位有效数。
在重复性条件下获得的两次独立测定结果的绝对差值不得超过算术平均值的10%
3、数据记录
100100/20060
.0)(21⨯⨯⨯⨯-=V c V V X。
