传统ES打靶基因敲除敲入小鼠技术
传统ES打靶基因敲除敲入小鼠技能

传统ES打靶基因敲除敲入小鼠技能传统ES 打靶基因敲除/敲入小鼠技术技术原理传统的基因打靶技术制备基因敲除(KO )/敲入(KI )基因打靶技术是建立在DNA同源重组与胚胎干细胞等技术基础上的分子生物学技术。
同源重组是指当外源DNA 片段与宿主基因组片段同源性高时,同源DNA 区部分可与宿主DNA 的相应片段发生交换(即同源重组)。
基因打靶就是通过同源重组技术将外源基因定点整合入靶细胞基因组上某一确定的位点,以达到定点修饰改造染色体上某一基因的目的。
基因打靶技术目前已被广泛认为是一种理想的特定修饰与改造生物体遗传物质的最佳方法。
尤其是条件性和诱导性基因打靶系统的建立,使得对基因在时间和空间上的靶位修饰更加明确、效果更加精确可靠,该技术的发展已经为发育生物学、分子遗传学、免疫学及医学等学科提供了一个全新的、强有力的研究和治疗手段,并已显示出巨大的应用前景及商业价值。
服务流程和周期、管路敷设技术通过管线不仅可以解决吊顶层配置不规范高中资料试卷问题,而且可保障各类管路习题到位。
在管路敷设过程中,要加强看护关于管路高中资料试卷连接管口处理高中资料试卷弯扁度固定盒位置保护层防腐跨接地线弯曲半径标高等,要求技术交底。
管线敷设技术中包含线槽、管架等多项方式,为解决高中语文电气课件中管壁薄、接口不严等问题,合理利用管线敷设技术。
线缆敷设原则:在分线盒处,当不同电压回路交叉时,应采用金属隔板进行隔开处理;同一线槽内,强电回路须同时切断习题电源,线缆敷设完毕,要进行检查和检测处理。
、电气课件中调试对全部高中资料试卷电气设备,在安装过程中以及安装结束后进行高中资料试卷调整试验;通电检查所有设备高中资料试卷相互作用与相互关系,根据生产工艺高中资料试卷要求,对电气设备进行空载与带负荷下高中资料试卷调控试验;对设备进行调整使其在正常工况下与过度工作下都可以正常工作;对于继电保护进行整核对定值,审核与校对图纸,编写复杂设备与装置高中资料试卷调试方案,编写重要设备高中资料试卷试验方案以及系统启动方案;对整套启动过程中高中资料试卷电气设备进行调试工作并且进行过关运行高中资料试卷技术指导。
基因敲除小鼠(Knockoutmice)制备技术方法

基因敲除小鼠(Knockoutmice)制备技术方法基因敲除小鼠,人们使用复杂的方法使小鼠体内的某一个基因不表达,从而使小鼠呈现这个基因缺失的状态,可用于研究这个基因的功能。
但如果某个基因功能特别重要,这个基因缺失可能具有胚胎致死性,那我们就无法得到这种基因敲除的小鼠了,于是人们发明了条件性基因敲除技术。
这一技术可以实现在特定的时间、特定的细胞或组织内使某个基因沉默。
方法是首先在目的基因(就是打算敲除的那个基因)的两侧分别插入一段名为LoxP的DNA序列(LoxP序列是一段34bp的DNA序列,两端的13个碱基为回文序列,中间的8个碱基决定LoxP的方向。
然后我们需要用到一种带有Cre酶的转基因小鼠了。
Cre重组酶于1981年从P1噬菌体中发现,属于λ Int酶超基因家族。
Cre重组酶基因编码区序列全长1029bp(EMBL数据库登录号X03453),编码38kDa蛋白质。
是一种位点特异性重组酶,能介导两个LoxP位点(序列)之间的特异性重组,使LoxP位点间的基因序列被删除或重组。
LoxP(locus of X-over P1)序列来源于P1噬菌体,是有两个13bp反向重复序列和中间间隔的8bp序列共同组成,8bp的间隔序列同时也确定了LoxP的方向。
Cre 在催化DNA链交换过程中与DNA共价结合,13bp的反向重复序列是Cre酶的结合域。
其序列如下:5' - ATAACTTCGTATA - ATGTATGC - TATACGAAGTTAT - 3'3' - TATTGAAGCATAT - TACATACG - ATATGCTTCAATA - 5'Cre-LoxP系统的特性Cre重组酶介导两个LoxP位点间的重组是一个动态、可逆的过程,可以分成三种情况:1、如果两个LoxP位点位于一条DNA链上,且方向相同,Cre重组酶能有效切除两个LoxP位点间的序列;2、如果两个LoxP位点位于一条DNA链上,但方向相反,Cre重组酶能导致两个LoxP位点间的序列倒位;3、如果两个LoxP位点分别位于两条不同的DNA链或染色体上,Cre酶能介导两条DNA链的交换或染色体易位。
小鼠基因敲除的研究进展

第46卷第10期Vol.46No.10山东大学学报(理学版)Journal of Shandong University (Natural Science )2011年10月Oct.2011收稿日期:2011-07-15;网络出版时间:2011-08-1209ʒ42网络出版地址:http ://www .cnki.net /kcms /detail /37.1389.N.20110812.0942.001.html作者简介:张剑(1980-),男,博士,主要研究方向为动物发育与基因工程研究.Email :zhj8226@sdu.edu.cn*通讯作者:高建刚(1963-),男,博士,教授,博士生导师,主要研究方向为干细胞生物学.Email :jggao@sdu.edu.cn杨晓梅(1968-),女,副教授,研究方向为细胞生物学.Email :yxm411@sdu.edu.cn文章编号:1671-9352(2011)10-0183-14小鼠基因敲除的研究进展张剑,杨晓梅*,高建刚*(山东大学生命科学学院,山东济南250100)摘要:随着人类基因组计划(HGP )的顺利完成,后基因时代的生物学研究迫切需要一种有效的基因功能分析方法。
基因敲除小鼠模型的应用,为研究基因的功能和寻找新的治疗人类疾病的干预措施提供了有力支持。
基因打靶和基因捕获是两种不同的通过胚胎干细胞(ES 细胞)制作基因敲除小鼠的技术。
基因捕获具有高通量、随机性、序列标记等特点,而基因打靶则是针对特定基因的敲除。
自基因打靶和基因捕获小鼠首次亮相距今已有近20年的时间。
近年来,针对基因打靶和基因捕获的新工具不断涌现,并且相应的组织也已经成立。
这些组织能够利用这两种方法敲除小鼠基因组中的基因。
国际基因捕获协会(The International Gene Trap Consortium ,IGTC )和基因敲除小鼠计划(The Knockout Mouse Project ,KOMP )已着手创建世界范围内用于科研的便利资源,并且计划敲除所有小鼠的基因。
基因敲除三大技术对比
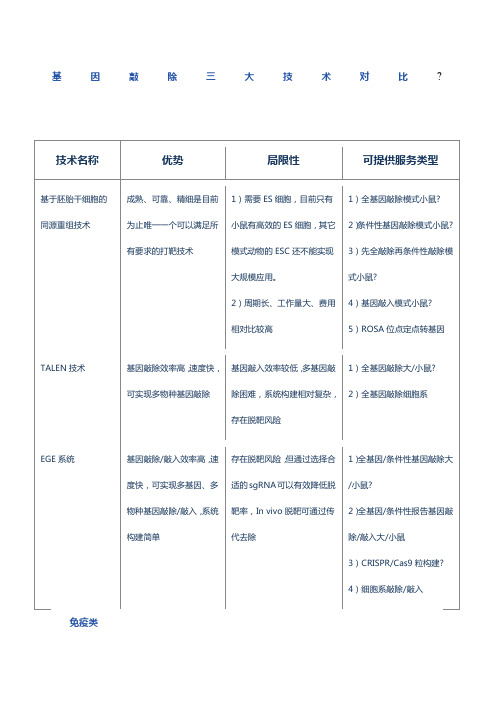
基因敲除三大技术对比? 技术名称优势局限性可提供服务类型基于胚胎干细胞的同源重组技术成熟、可靠、精细是目前为止唯一一个可以满足所有要求的打靶技术1)需要ES细胞,目前只有小鼠有高效的ES细胞,其它模式动物的ESC还不能实现大规模应用。
2)周期长、工作量大、费用相对比较高1)全基因敲除模式小鼠?2)条件性基因敲除模式小鼠?3)先全敲除再条件性敲除模式小鼠?4)基因敲入模式小鼠?5)ROSA位点定点转基因TALEN技术基因敲除效率高,速度快,可实现多物种基因敲除基因敲入效率较低,多基因敲除困难,系统构建相对复杂,存在脱靶风险1)全基因敲除大/小鼠?2)全基因敲除细胞系EGE系统基因敲除/敲入效率高,速度快,可实现多基因、多物种基因敲除/敲入,系统构建简单存在脱靶风险,但通过选择合适的sgRNA可以有效降低脱靶率,In vivo脱靶可通过传代去除1)全基因/条件性基因敲除大/小鼠?2)全基因/条件性报告基因敲除/敲入大/小鼠3)CRISPR/Cas9粒构建?4)细胞系敲除/敲入免疫类B-NSG小鼠:Biocytogen-NOD-SCID-IL2rg?B-NSG小鼠是NOD遗传背景,Prkdc和IL2rg双基因敲除的小鼠,是目前国际公认的免疫缺陷程度最高、最适合人源细胞或组织移植的工具小鼠。
?基本特征??NOD(non-obese diabetes)遗传背景:自发I型糖尿病;其巨噬细胞对人源细胞吞噬作用弱;先天免疫系统,如补体系统和树突状细胞功能降低。
??Prkdcscid :Prkdc(protein kinase DNA-activated catalytic)基因突变,小鼠的功能性T和B细胞缺失,淋巴细胞减少,表现为细胞免疫和体液免疫的重度联合免疫缺陷(severe combined immune deficiency, scid)。
?Il2rgnull:Interleukin-2受体的gamma链(IL-2R γc,又称CD132)位于小鼠X染色体上,是具有重要免疫功能的细胞因子Il2、Il-4、Il-7、Il-9、Il-15和I-21的共同受体亚基,该基因敲除后的小鼠机体免疫功能严重降低,尤其是NK细胞的活性几乎丧失。
转基因小鼠制备方法

转基因小鼠制备方法一、引言转基因小鼠是指通过基因工程技术将外源基因导入小鼠基因组中,使其表达或缺乏特定基因,从而研究基因功能、疾病模型等方面的动物模型。
转基因小鼠制备方法是实现转基因小鼠研究的重要步骤之一,本文将详细介绍转基因小鼠制备的一般步骤和常用技术。
二、转基因小鼠制备的一般步骤1. 选择目标基因和载体转基因小鼠制备的第一步是选择目标基因和适当的载体。
目标基因可以是外源基因、特定基因的突变体或基因敲除。
载体通常是带有选择标记(如抗生素抗性基因)和目标基因的质粒。
2. DNA构建在DNA构建过程中,首先需要将目标基因和选择标记基因插入到载体的适当位点上。
这可以通过限制性内切酶切割和连接、PCR扩增等方法实现。
构建完成后,需要进行酶切鉴定和测序确认。
3. 体外培养胚胎干细胞(ES细胞)转基因小鼠制备中常用的方法是利用ES细胞技术。
首先,从小鼠胚胎中获得内源性干细胞(ES细胞),并进行体外培养。
然后,将构建好的转基因载体导入ES细胞中,通过抗生素筛选获得带有目标基因的转基因ES细胞克隆。
4. 转基因小鼠制备转基因ES细胞的制备完成后,可以进行转基因小鼠的制备。
这一步骤通常有两种方法:内源性重组和外源性重组。
内源性重组是将转基因ES细胞注射到小鼠早期胚胎中,使其整合到小鼠的生殖细胞中,从而获得转基因小鼠。
外源性重组是将转基因ES细胞直接注射到小鼠的细胞团中,形成转基因胚胎,再将转基因胚胎移植到雌性小鼠子宫中,使其发育成为转基因小鼠。
5. 转基因小鼠鉴定转基因小鼠制备完成后,需要对其进行鉴定。
通常采用PCR、Southern blotting、Western blotting等分子生物学方法,检测转基因小鼠是否成功表达目标基因。
三、常用技术1. CRISPR/Cas9技术CRISPR/Cas9是一种新兴的基因编辑技术,可以实现高效、精确地对基因组进行编辑。
通过CRISPR/Cas9技术,可以直接在小鼠胚胎中进行基因编辑,从而制备转基因小鼠。
Knockout(基因敲除) - ES细胞囊胚显微注射

ES细胞囊胚显微注射技术原理囊胚。
将获得的嵌合体小鼠和野生型小鼠交配,以确定嵌合体小鼠的生殖系传递能力,一般情况下,大约有一半左右的嵌合体小鼠具有生殖系传递能力品系选择囊胚品系:C57BL/6×C57BL/6这是目前制备基因敲除鼠最常用品系,也是成功率最高的一敲除鼠需要转换成C57等品系JM8A3(derived from C57BL/6N mice, Coat Color: Agouti囊胚获取2.5 d 培养到3.5 d 囊胚期 3.5 d 囊胚期ES 细胞打靶和筛选1.同源重组臂构建:两侧同源臂之和不小于5 kb, 单侧不最好一长一短是正筛选基因(neo),在长3.保持ES 细胞的分化全能性:1.打靶载体转染ES 细胞:2.电转后的ES 细胞接种到性的细胞克隆3.具有抗性的细胞克隆大多的结果,只有及少部分发服务描述注射ES细胞制备1. 胚胎干细胞在显微注射前必需通过MAP检测,无结果2. 早代数、培养在滋养层上的胚胎干细胞更易于产3.用胰蛋白酶处理胚胎干细胞使细胞呈单细胞状态,ES注射后代小鼠的鉴定传统上最广泛利用的胚胎干细胞系来自129-亚系,具有浅有黑色的毛。
因此,所获得的嵌合体小鼠毛具有黑色和棕由于注射的胚胎干细胞(129)是XY基因型,虽然所获生殖系的传递,这样所获得的嵌合体小鼠将大部分是雄性1.对于首建者小鼠:通常为杂合子,可以通过与野生型小鼠交配,获得纯合转基因小鼠获得该品系的转基因小鼠获取到优良的基因敲除品系。
建系时的鉴定方法除了基表型及经验等方法进行鉴定,如有毛色差异的嵌合体如有生殖系传递的能力;通常情况下,具有低比列的来自ES细胞毛色的嵌合体是不贡献给生殖系的,一般都把它ES注射一些进展The information come from university of california.irvienJM8囊胚注射JM8A3囊胚注射定点原核显微注射谢谢!!!。
基因敲除小鼠的制作方法

一、常规基因敲除鼠( Conventional Knockout )常规基因敲除是通过基因打靶,把需要敲除的基因的几个重要的外显子或者功能区域用 Neo Cassette 替换掉。
这样的小鼠其全身所有的组织和细胞中都不表达该基因产物。
此类基因敲除鼠一般用于研究某个基因在对小鼠全身生理病理的影响,而且这个基因没有胚胎致死性。
二、条件性基因敲除小鼠( Conditional Knockout )条件性基因敲除小鼠是通过基因打靶,把两个 loxP 位点放到目的基因一个或几个重要的外显子的两边。
该小鼠和表达 Cre 酶小鼠杂交之前,其目的基因表达完全正常。
当和组织特异性表达 Cre 酶的小鼠进行杂交后,可以在特定的组织或细胞中敲除该基因,而该基因在其他组织或细胞表达正常。
条件性基因敲除鼠适用范围为:( 1 )该基因有胚胎致死性;( 2 )用于研究该基因在特定的组织或细胞中的生理病理功能。
三、基因敲入小鼠( Knockin )基因敲入小鼠是通过基因打靶,把目的基因序列敲入到小鼠的相应基因位点,使用小鼠的表达调控元件指导目的基因表达。
此类基因敲入鼠一般用于药物的筛选,信号通路的研究等。
一、 ZFN 技术制作基因敲除鼠ZFN 能够识别并结合指定的基因序列位点,并高效精确地切断。
随后细胞利用天然的DNA 修复过程来实现 DNA 的插入、删除和修改,这样研究人员就能够随心所欲地进行基因组编辑。
这在过去是无法想象的,传统的基因敲除技术依赖细胞内自然发生的同源重组,其效率只有百万分之一,而 ZFN 的基因敲除效率能达到 10% 。
利用这些技术进行小鼠基因的定点敲除和敲入,可以把时间从一年缩短到几个月。
这项技术中设计特异性的 ZFN 是最关键的环节,目前研究者采用计算生物学方法设计高特异性的 ZFN,但 ZFN的脱靶( off target ),也就是把不该切的地方切了的问题仍是一个挑战。
也正因为这个原因,利用 ZFN 技术进行小鼠的基因修饰还无法完全取代传统技术。
基因敲除小鼠技术专题

oCassette替换掉。这样的小鼠其全身所有的组 织和细胞中都不表达该基因产物。此类基因敲除 鼠一般用于研究某个基因在对小鼠全身生理病理
的影响,而且这个基因没有胚
胎致死性。 二、条件性基因敲除小鼠(ConditionalKnockout)
条件性基因敲除小鼠是通过基因打靶,把两个 loxP位点放到目的基因一个或几个
DNA分子之间或分子之内的重新组合。在基因敲 除小鼠制作过程中,需要针对目的基因两端特异 性片段设计带有相同片段的重组载体,将重组载
体导入到胚胎干细胞后外源的重组载
体与胚胎干细胞中相同的片段会发生同源重组, 如图1所示:
图2.基因敲除鼠制作过程示意图 1、Knockout载体设计与构建 根据研究项目具体情况和要求
胞注入特定品系小鼠囊胚中,然后将囊胚移植到 假孕的小鼠子宫中。待后代小鼠出生后,通过小 鼠的毛色中来源于ES细胞毛色的比例判断嵌合程
度的高低,以及该小鼠的后代中可能
获得生殖系传递能力。 4、由嵌合体小鼠繁殖出生殖遗传系Knockout小
鼠
将嵌合体小鼠与适当品系的小鼠交配,后代小鼠 出生后,通过PCR方式检测小鼠是否含有
蛋白,从而达到靶向操作内源性
基因的目的,它克服了ZFN方法不能识别任意目 标基因序列,以及识别序列经常受上下游序列影 响等问题,而具有ZFN相等或更好的灵活性,使
基因操作变得更加简单方便。然而
重要的外显子的两边。该小鼠和表达Cre酶小鼠 杂交之前,其目的基因表达完全正常。当和组织 特异性表达Cre酶的小鼠进行杂交后,可以在特
定的组织或细胞中敲除该基因,而
该基因在其他组织或细胞表达正常。 条件性基因敲除鼠适用范围为:(1)该基因有 胚胎致死性;(2)用于研究该基因在特定的组
基因敲除小鼠

基因敲除小鼠摘要基因敲除小鼠是一种常用的实验动物模型,可以帮助科学家研究基因在生物体发育和功能中的作用。
本文将介绍基因敲除小鼠的定义、用途以及常用的敲除方法,帮助读者了解基因敲除小鼠在生物学研究中的重要性和应用。
引言基因敲除小鼠是指通过干扰或删除特定基因,使小鼠体内该基因表达受到抑制或消失的实验模型。
这种模型被广泛应用于基因功能研究、疾病机制研究以及药物开发等领域。
基因敲除方法基因敲除小鼠的制备有多种方法,其中最常用的是胚胎干细胞敲除和CRISPR/Cas9系统。
胚胎干细胞敲除胚胎干细胞敲除是一种传统的基因敲除方法。
首先,从小鼠胚胎中获得胚胎干细胞,然后通过基因转染或基因突变等方式,使目标基因发生敲除突变。
最后,将敲除的胚胎干细胞注入到早期小鼠胚胎中,形成敲除小鼠。
CRISPR/Cas9系统CRISPR/Cas9系统是一种新兴的基因编辑技术,已经在基因敲除小鼠制备中得到广泛应用。
该系统利用Cas9核酸酶和特定的引导RNA来定向切割目标基因的DNA链,从而导致基因发生敲除或突变。
基因敲除小鼠的应用基因敲除小鼠在生物学研究中有着广泛的应用,以下是其中几个重要的应用领域:基因功能研究通过敲除特定基因,科学家可以观察与该基因相关的表型变化,从而揭示该基因在生物体发育和功能中的作用。
这对于揭示基因调控网络、疾病机制的研究具有重要意义。
疾病模型研究基因敲除小鼠常被用来构建各种疾病模型,如癌症、心血管疾病等。
这些模型可以模拟人类疾病的发生和发展过程,为相关疾病的研究提供了有力的工具。
药物开发基因敲除小鼠在药物开发中也起着重要的作用。
通过敲除特定基因可以观察药物对目标基因的影响,从而评估药物的疗效和安全性。
结论基因敲除小鼠是一种重要的实验动物模型,被广泛应用于基因功能研究、疾病模型研究以及药物开发等领域。
不同的敲除方法可根据具体实验需求选择使用。
基因敲除小鼠在解析基因功能、揭示疾病机制和评估药物疗效方面发挥着重要的作用,为生物学研究提供了强大的工具。
基因敲除小鼠制备的流程

基因敲除小鼠的制备流程基因敲除小鼠已经成为现代生命科学基础研究和药物研发领域不可或缺的实验动物模型,在生命科学、人类医药和健康研究领域中发挥着重要的作用。
基于胚胎干细胞的基因打靶技术、EGE技术(基于Crispr cas9技术)是当下比较火热的基因敲除小鼠制备技术。
利用这两种技术制备基因敲除小鼠的流程是什么样的?一、基于胚胎干细胞的基因打靶技术制备基因敲除小鼠的流程:1.课题设计,订购课题BAC菌;2.按照课题设计,完成打靶载体设计和构建;3.将重组载体电转到胚胎干细胞中,用G418筛选转染后的胚胎干细胞,得到阳性克隆;4.进一步通过PCR和southern blot杂交技术(基因敲除小鼠检测金标准)对上一步得到的阳性克隆进行筛选,得到稳定整合外源基因的胚胎干细胞阳性克隆;5.将胚胎干细胞阳性克隆注射到小鼠囊胚中,并植入到假孕小鼠的子宫内;6.得到嵌合鼠,并获得F1阳性杂合子小鼠。
基于胚胎干细胞的基因打靶技术制备基因敲除小鼠是目前为止唯一一个可以满足几乎所有基因组修饰要求的打靶技术,但目前只应用在小鼠的基因敲除上,而且其周期长工作量大。
二、利用EGE技术(基于Crispr cas9技术)制备基因敲除小鼠的流程1.设计构建识别靶序列的sgRNA;2.设计构建致靶基因切割的EGE系统载体质粒;3.利用百奥赛图自主开发的UCA试剂盒对sgRNA/Cas9进行活性检测;4.设计构建打靶载体;5.体外转录sgRNA/Cas9 mRNA;6.小鼠受精卵原核注射sgRNA/Cas9 mRNA和打靶载体;7.获得Fo代小鼠,利用PCR对Fo代小鼠进行基因型鉴定;8.获得F1代小鼠,利用PCR和southern blot杂交技术(基因敲除小鼠检测金标准)对F1代小鼠进行基因型鉴定。
虽然EGE技术(基于Crispr cas9技术)制备基因敲除小鼠看似比基于胚胎干细胞的基因打靶技术制备基因敲除小鼠流程繁琐,其实不然,EGE技术(基于Crispr cas9技术)系统构建简单,基因敲除/敲入效率高,速度快,可实现多基因、多物种基因敲除/敲入,最快2个月即可得到F0代阳性鼠,5个月得到F1F1代杂合子小鼠。
基因敲除小鼠制作的基本流程

基因敲除小鼠制作的基本流程(一)基因打靶载体的构建基因打靶载体的基本结构:中间为正筛选基因和相关序列,左右分别为长短同源臂以及在长同源臂外为负筛选基因。
设计载体时,需要在打靶位点两侧分别设计一段大小为几kb长度的同源臂,用于同源重组。
大家普遍认为同源臂越长,重组效率越高。
不过,也有研究用不到1kb的同源臂完成实验,而同时也有研究证实同源臂长度超过8kb后对于同源重组效率的提高就不再有明显的提高作用。
同源重组效率最主要还是由目标位点和打靶基因周围序列决定的,所以研究者现在普遍采用一长一短的适中长度同源臂设计方式,便于后期用PCR 进行筛选以及最终的DNA印迹(southern blotting)检测确认打靶是否成功。
短同源臂长度为2~3kb,而长同源臂为4~6kb。
(二)ES细胞基因打靶和中靶克隆的筛选目前使用的小鼠ES细胞主要来源于129、 C57BL/6和BALB/c背景的小鼠。
研究者们将同源重组应用到ES细胞中从而获得了定点基因修饰的目的,通过将DNA片段导入细胞中,利用片段上的宿主细胞同源臂进行同源重组,将目的基因置换插入细胞基因组中整合表达。
在ES细胞中进行同源重组需要将打靶载体进行线性化后,通过诸如电转染(electroporation)、核转染等手段导入细胞中,研究已经证明线性化载体更有利于同源重组的发生。
目前,基因打靶事件的确定通常是首先用PCR反应筛选中靶的ES 细胞克隆。
PCR引物的设计原则是一个引物位于同源臂外,另一个引物位于载体内。
用PCR扩增同源臂短臂,成功的基因打靶克隆会有扩增产物出现。
阳性克隆还需要Southem blotting分析进一步验证。
确定正确后,用于下一步的ES细胞显微注射,一体以产生嵌合体小鼠。
(三)ES细胞克隆的胚胎显微注射和胚眙移植筛选得到的中靶细胞通过显微注射的方式注入到囊胚期胚胎的囊胚腔中,然后将囊胚移植到如假孕母鼠体内,从而产生子代嵌合小鼠。
(四)基因敲除小鼠培育嵌合小鼠需与野生型小鼠交配,以实现基因修饰生殖系传递。
基因敲除小鼠饲养繁殖技巧

基因敲除⼩⿏饲养繁殖技巧科研狗但凡要做动物实验的,哪个不需要伺候⼩⿏?每天好吃的好喝地伺候着,定期更换垫料,还要操⼼它们的⼈⽣⼤事,给它分配对象,⽣了娃还要给帮它们做“亲⼦鉴定”,看见⼩⿏脱发了,要想办法,母⿏不⽣了,要想办法。
回头再看看⾃⼰,没头发,还没对象,天天愁⽂章,担⼼毕不了业,全指望⼩⿏们加油,让⾃⼰早⽇出成果,所以可不得好吃好喝的伺候它们嘛!尤其是基因敲除⼩⿏,⾝价昂贵,从接到它的那⼀刻起,整个⼈都⼜兴奋⼜紧张,⽣怕怠慢了这些⼩家伙,那么收到基因敲除⼩⿏后要如何制定计划进⾏扩群繁殖以满⾜实验需要呢?除了了解所选品系的⽣活习性外,我们还要考虑⾃⼰需要的基因编辑⿏可能出现哪些问题,有没有解决或者是改善的⽅法,这些我们可以通过查阅⽂献看有没有关于该基因敲除⼩⿏的相关信息并作出⼀个初步判断。
1.背景品系的特点这个不⽤多说,需要做动物实验的同学,谁还没养过⼏只⼩⿏呀,养之前肯定已经把它的⽣活习性、繁殖特点、饲养要求等了解的很清楚了,举个栗⼦,⽐如说C57BL/6J,该品系的雄⿏好⽃,尤其是刚断奶后不同窝的雄⿏不宜放⼀笼饲养。
2.饲养环境的要求应尽可能地给⼩⿏提供适宜的⽣活环境和营养,这⽅⾯可以参照国家标准来进⾏饲养管理。
⽐如,⼩⿏对于噪⾳、光照⽐较敏感,所以我们应给⼩⿏提供安静的环境,尽量选在⼈员⾛动少的地⽅,也不要频繁查看⼩⿏情况,这样⼩⿏会有压⼒的。
母⿏有筑巢的天性,可以向笼中放柔软的棉垫,⿎励其筑巢,有助于提⾼产量。
3.基因敲除⼩⿏饲养管理应注意哪些问题⼤多数基因敲除⼩⿏相对野⽣型⼩⿏⽽⾔,在某些⽅⾯会存在或⼤或⼩的问题,所以我们需要查阅相关的⽂献,看看有没有该基因敲除⼩⿏的⽂献报道,该基因被修饰后会出现哪些问题?这些问题有没有解决或者是改善的⽅法。
如果是某种基因被修饰后会导致⼩⿏不能合成某种物质,那么可以给⼩⿏额外补充该物质;若是基因敲除⼩⿏的成活率低,问题有可能出现在着床期⾄成年期的任意时间段,通过代乳和改善饲养条件也许能得以解决;如果基因敲除⼩⿏的⽣殖⼒低。
基因编辑小鼠模型构建方法

基因编辑小鼠模型构建方法基因编辑小鼠模型是一种通过基因编辑技术改变小鼠基因组的方法,以研究基因在生物体发育、生理和疾病过程中的功能和机制。
下面是关于基因编辑小鼠模型构建方法的十条详细描述:1. 胚胎干细胞(ES细胞)导入方法:将经过基因编辑的ES细胞注射到小鼠早期胚胎中,使其发育成含有编辑基因的小鼠体。
2. 胚胎干细胞(ES细胞)体外培养方法:将小鼠胚胎中的干细胞分离出来,进行基因编辑后体外培养并转移到小鼠胚胎中,培育出基因编辑小鼠。
3. 基因敲除方法:使用CRISPR/Cas9等基因编辑工具,设计合适的寡核苷酸序列并导入小鼠胚胎,通过切割和删除目标基因,实现基因敲除。
4. 基因突变方法:通过CRISPR/Cas9等基因编辑工具,直接在小鼠基因中引入点突变或插入突变,使其产生突变株。
5. 转基因方法:将外源基因导入小鼠胚胎细胞,并使其嵌入细胞基因组,从而使小鼠表达外源基因。
6. 基因表达调控方法:通过CRISPR/Cas9等基因编辑工具,设计合适的寡核苷酸序列并导入小鼠胚胎细胞,以实现对基因的过表达或下调。
7. 基因标记方法:使用CRISPR/Cas9等基因编辑工具,在小鼠基因中插入标记基因,如荧光蛋白,以便对基因表达进行可视化和追踪。
8. 基因互补方法:通过CRISPR/Cas9等基因编辑工具,将外源基因导入小鼠胚胎细胞,使其与已有基因相互补充或修复,从而恢复基因功能。
9. 基因组工程方法:通过CRISPR/Cas9等基因编辑工具,在小鼠基因组中引入大片段DNA,如全基因组范围的基因敲除、替换或插入。
10. 利用转基因碰撞方法:将两个具有特定基因敲除或表达的小鼠品系交配,使它们的后代同时具有两个基因的敲除或表达,从而模拟一种基因缺失或改变的状态。
这些方法都是对基因编辑小鼠模型构建过程中常用的技术手段,能够有效地改变小鼠基因组,从而研究基因功能和机制。
但是在实际应用过程中需要注意合理选择方法,并根据具体的研究目的进行优化和改进。
基因敲除小鼠的方法

基因敲除小鼠的方法基因敲除小鼠模型是生物医学研究领域中常用的实验动物模型之一。
通过对特定基因进行敲除,科研人员可以研究该基因在生物体内的功能和影响,从而深入了解该基因对生物体的生理和病理过程的调控作用,为人类疾病治疗和药物研发提供重要的实验基础。
下面我们将介绍关于基因敲除小鼠的方法。
一、基因敲除小鼠的原理和意义1.1 基因敲除原理基因敲除是指通过人工手段破坏特定基因的DNA序列,使其失去功能。
在小鼠模型中,通常利用基因敲除技术将目标基因进行突变或删除,从而观察小鼠在不同生理状态下的表型变化,探索目标基因在生物体内的功能和作用机制。
1.2 基因敲除的意义基因敲除小鼠模型可以帮助科研人员研究特定基因的生物学功能,了解其在生物体内的作用机制。
基因敲除小鼠模型也能够为疾病研究和药物开发提供重要的实验依据,有助于发现新的治疗靶点和疾病治疗方法。
二、基因敲除小鼠的制备方法2.1 基因敲除小鼠的选择在进行基因敲除小鼠实验前,首先需要选择合适的小鼠品系和基因靶向。
常用的小鼠品系包括C57BL/6、BALB/c等,而基因敲除的选择通常基于目标基因在疾病或生理过程中的重要性。
2.2 敲除载体的构建和筛选制备基因敲除小鼠需要先构建敲除载体,通常采用基因工程技术将靶向基因进行突变或删除,然后将这些构建好的载体导入至小鼠胚胎干细胞中,进行筛选和培养。
2.3 胚胎干细胞的培养与筛选在培养和筛选过程中,科研人员需要将导入敲除载体的胚胎干细胞引入小鼠胚胎中,然后进行体外培养和筛选,以筛选出正常的敲除基因小鼠。
2.4 敲除小鼠的鉴定和繁殖成功培育出的敲除小鼠需要进行PCR鉴定和繁殖,以得到稳定传代的敲除小鼠品系。
对敲除小鼠进行系统的表型观察和分析,以确定目标基因敲除后的表型变化。
三、基因敲除小鼠的应用和前景3.1 基因敲除小鼠在生物学研究中的应用基因敲除小鼠模型广泛应用于生物学研究领域,包括生理学、免疫学、神经科学、遗传学等各个领域。
敲除小鼠常见问题与回答

敲除小鼠常见问题与回答一、什么是ES细胞显微注射?答:胚胎干细胞显微注射是制作基因敲除小鼠的一个最常用的方法。
主要过程是将携带目的基因的胚胎干细胞注射到小鼠的囊胚腔中获得嵌合体小鼠。
所得嵌合体小鼠的组织,将同时含有来源于囊胚的细胞和胚胎干细胞。
嵌合体小鼠必须和野生型小鼠配种以决定遗传改变的生殖系能否传递,这样可能获得转基因或打靶基因(来源于胚胎干细胞)稳定的生殖系传递的小鼠。
一般情况下,大约能获得50%继承了目的基因的后代。
二、嵌合体遗传学上用以指不同遗传性状嵌合或混杂表现的个体。
免疫学上的涵义则指一个机体身上有两种或两种以上染色体组成不同的细胞系同时存在,彼此能够耐受,不产生排斥反应,相互间处在嵌合状态。
在基因敲除鼠中指通过向囊胚注射被外源基因转化了的胚胎干细胞,使得发育成为的个体中含有不同基因型的细胞,产生的个体也叫嵌合体,即该生物体中嵌合了两种不同遗传结构的细胞(一种是基因型被改变了的细胞,另一种是原来的基因型的细胞)。
三、条件性敲除的原理?答:Cre-LoxP系统是源于P1噬菌体的一个DNA重组体系,由Cre酶和相应的LoxP位点组成,它能导致重组发生在特定的DNA序列处(LoxP位点),该系统可以将外源基因定点整合到染色体上或将特定DNA片段删除。
基于Cre-LoxP的基因打靶要分两步来进行。
首先要在胚胎干细胞的基因组中引入LoxP序列,这一步可以通过打靶载体的设计和对同源重组子的筛选来实现。
下一步通过Cre介导的重组来实现靶基因的遗传修饰或改变。
Cre-LoxP系统既可以在细胞水平上用Cre重组酶表达质粒转染中靶细胞,通过识别LoxP位点将抗性标记基因切除,又可以在个体水平上将重组杂合子小鼠与Cre转基因小鼠杂交,筛选子代小鼠就可得到删除外源标记基因的条件性敲除小鼠。
四、如何鉴定和挑选嵌合体?答:动物只有部分组织细胞整合有外源基因,则称为嵌合体动物。
它的鉴定主要根据毛色去鉴定。
注射的ES和囊胚来源不同的小鼠品系。
基因敲除小鼠概念及原理

基因敲除小鼠概念及原理
基因敲除小鼠是一种通过基因敲除技术创造出来的实验动物模型。
基因敲除技术是一种新的分子生物学技术,建立在基因同源重组技术基础以及胚胎干细胞技术基础上。
基因敲除就是通过同源重组将外源基因定点整合入靶细胞基因组上某一确定的位点,以达到定点修饰改造染色体上某一基因的目的的一种技术。
基因敲除小鼠的原理是利用基因同源重组进行基因敲除。
具体来说,通过同源重组将外源基因定点整合入小鼠的基因组上某一确定的位点,以达到定点修饰改造染色体上某一基因的目的。
这种技术克服了随机整合的盲目性和偶然性,是一种理想的修饰、改造生物遗传物质的方法。
基因敲除小鼠具有广泛的应用前景和商业价值,特别是在发育生物学、分子遗传学、免疫学及医学等学科的研究和治疗中。
这种技术的出现为这些学科提供了一个全新的、强有力的研究、治疗手段,具有重要的意义。
基因敲除技术在小鼠模型制造中的应用

基因敲除技术在小鼠模型制造中的应用在现代医学领域中,基因敲除技术是一种非常重要的技术手段。
它可以在生物体中去除某个特定基因的功能,以研究该基因对该生物体的影响。
这种技术被广泛应用于小鼠模型的制造中,以研究人类疾病,寻找药物,以及了解生物学机制。
本文将重点介绍基因敲除技术在小鼠模型制造中的应用。
一、基因敲除技术的原理基因敲除技术是通过基因重组技术,利用DNA重组酶将需要敲除的基因替代或切除,从而使其不能正确表达,无法正常发挥作用。
这种基因敲除在小鼠中通过转基因技术实现,将目标基因的DNA序列替换为荧光蛋白等DNA序列,用于研究疾病机制和药物筛选。
二、基因敲除技术在小鼠模型制造中的应用基因敲除技术在小鼠模型制造中的应用非常广泛。
由于小鼠与人类的基因组具有很高的相似性,这种技术可以很好地模拟人类疾病的发展过程,为新药发现提供重要的依据。
1. 基因敲除技术在疾病研究中的应用基因敲除技术可以用于研究特定基因在疾病发展中的作用。
例如,最近的一项研究发现,敲除小鼠中的RPAP3基因可以导致血管炎的发生,这为研究人类的自身免疫疾病提供了新的方向。
此外,基因敲除技术还可以用于研究基因调控机制以及新型抗生素药物的开发和筛选。
2. 基因敲除技术在药物研发中的应用基因敲除技术在药物研发中也起到了非常重要的作用。
由于小鼠模型能够较好地模拟人类疾病的特点,因此敲除小鼠中的基因可以用于药物的初步筛选。
例如,现在已经有许多药物被证明可以通过敲除特定基因来预防或治疗人类疾病,比如可以通过敲除PPARG基因来改善非酒精性脂肪性肝病。
3. 基因敲除技术在基因组编辑中的应用基因敲除技术在基因组编辑中也是一个应用非常广泛的技术。
例如,利用基因敲除技术可以制作出缺乏某个基因的小鼠模型,用于研究该基因的生物学特性,从而探究人类基因组结构和功能的各种调控机制。
三、基因敲除技术在小鼠模型制造中的局限性和未来展望在基因敲除技术的应用中,仍然存在一些局限性。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
传统ES打靶基因敲除/敲入小鼠技术
技术原理
传统的基因打靶技术制备基因敲除(KO)/敲入(KI)基因打靶技术是建立在DNA同源重组与胚胎干细胞等技术基础上的分子生物学技术。
同源重组是指当外源DNA片段与宿主基因组片段同源性高时,同源DNA区部分可与宿主DNA的相应片段发生交换(即同源重组)。
基因打靶就是通过同源重组技术将外源基因定点整合入靶细胞基因组上某一确定的位点,以达到定点修饰改造染色体上某一基因的目的。
基因打靶技术目前已被广泛认为是一种理想的特定修饰与改造生物体遗传物质的最佳方法。
尤其是条件性和诱导性基因打靶系统的建立,使得对基因在时间和空间上的靶位修饰更加明确、效果更加精确可靠,该技术的发展已经为发育生物学、分子遗传学、免疫学及医学等学科提供了一个全新的、强有力的研究和治疗手段,并已显示出巨大的应用前景及商业价值。
服务流程和周期
小鼠品系
ES细胞品系:129 (agouti)、C57BL/6N(black)、C57BL/6(agouti)。
基因打靶常用小鼠模型
(1)完全性基因敲除小鼠(Conventional Knockout,KO)
完全性基因敲除是通过基因敲除技术,把需要敲除目的基因的所有外显子或几个重要的外显子或者功能区域敲除掉,获得全身所有的组织和细胞中都不表达该基因的小鼠模型。
应用:用于研究某个基因(要求该基因非胚胎致死性基因)对全身生理病理的功能。
(2)条件性基因敲除小鼠(Conditional Knockout,CKO)
条件性基因敲除是通过基因敲除把两个loxp位点放到目的基因一个或几个重要的外显子的两端制备出floxed小鼠,该floxed小鼠在与表达Cre酶小鼠杂交之前,该目的基因表达完全正常,而当该floxed小鼠与组织特异性表达Cre酶的小鼠进行杂交后,可以在特定的组织或细胞中敲除该基因,而该基因在其它组织或细胞表达正常。
应用:用于具有胚胎致死性目的基因的研究;用于研究基因在特定的组织或细胞中的生理病理功能;与控制Cre或Flp表达的其它诱导系统相结合,还可以对某一基因的表达同时实现在时间和空间两方面的调控。
(3)基因敲入小鼠(Knockin,KI)
基因敲入可以在目的基因位置引进特定的突变或外源基因。
比如在目的基因上引入点突变(模拟人类遗传疾病模型) ;或将报告基因(如EGFP,mRFP,mCherry,mYFP,或LacZ 等)通过同源重组的方式引入目的基因的特定位点,从而可以通过报告基因的表达跟踪目标基因的表达。
通过报告基因的表达可以研究基因的表达谱。
也可以用报告基因取代小鼠本身的基因,使KO/KI同时发生。
应用:用于药物筛选相关研究;用于信号通路的研究;用于示踪的相关研究。
(4)人源化小鼠(Humanized )
人源化小鼠模型是指带有功能性的人类基因、细胞或组织的小鼠模型。
这种模型通常被用于人类疾病体内研究(in vivo study)的活体替代模型。
由于人类生理与动物生理有显著的差别,利用动物模型得到的实验结果有时不能适用到人体上。
比如,有些利用小鼠等动物模型开发的药物在人体上并没有效果。
所以,利用转基因或同源重组的方法,将人类基因“放置”在小鼠模型上所制备的人源化小鼠模型,大大提高了这类小鼠模型作为模拟某些人类疾病的有效性。
应用:在艾滋病、癌症、传染病、人类退化性疾病、血液病研究领域等都有广泛的应用;药物临床前模拟实验。
(5)KO First基因敲除小鼠
KO-First技术是通过在内含子中插入一个两边带有FRT位点的基因破坏盒来达到敲除的目的,这个破坏盒含有Splice acceptor,报告基因和Neo。
除此之外,在目的基因敲除的外显子两侧各插入两个LoxP位点。
因此得到的小鼠是目的基因敲除同时敲入报告基因与抗性基因的小鼠。
通过灵活选择Cre/LoxP重组系统或者Flp/FRT重组系统,可达到同时获得完全性敲除和条件性敲除的实验目的。
即当该小鼠与表达Cre的小鼠交配时,可获得目的基因敲除同时敲进报告基因的小鼠;当该小鼠与Flp小鼠交配时,可还原已敲除基因的表达,获得基因条件性敲除小鼠,在此基础上Cre小鼠交配又可获得目的基因敲除小鼠。
