HPV分子诊断试剂项目调研(201405)
人乳头瘤病毒(HPV)核酸检测及基因分型试剂技术审查指导原则

附件3人乳头瘤病毒(HPV)核酸检测及基因分型、试剂技术审查指导原则本指导原则旨在指导注册申请人对人乳头瘤病毒(HPV)核酸检测及基因分型试剂注册申报资料的准备及撰写,同时也为技术审评部门审评注册申报资料提供参考。
本指导原则是针对人乳头瘤病毒(HPV)核酸检测及基因分型试剂的一般要求,申请人应依据产品的具体特性确定其中内容是否适用,若不适用,需具体阐述理由及相应的科学依据,并依据产品的具体特性对注册申报资料的内容进行充实和细化。
本指导原则是供申请人和审查人员使用的指导性文件,不涉及注册审批等行政事项,亦不作为法规强制执行,如有能够满足法规要求的其他方法,也可以采用,但应提供详细的研究资料和验证资料。
应在遵循相关法规的前提下使用本指导原则。
本指导原则是在现行法规、标准体系及当前认知水平下制定的,随着法规、标准的不断完善和科学技术的不断发展,本指导原则相关内容也将适时进行调整。
一、范围人乳头瘤病毒(Human Papillomavirus, HPV)属于乳头瘤病毒科,是一种小分子的、无被膜包被的1、环状双链DNA病毒,基因组长约8000碱基对(bp),分为3个功能区,即早期转录区(E区)、晚期转录区(L区)和非转录区(长控制区,LCR)。
HPV 通过直接或间接接触污染物品或性传播感染人类。
该病毒不但具有宿主特异性,而且具有组织特异性,只能感染人的皮肤和粘膜上皮细胞,引起人类皮肤的多种乳头状瘤或疣及生殖道上皮增生性损伤。
对于感染生殖道和肛门的HPV,根据各基因型别致病力大小或致癌危险性大小可分为低危型和高危型两大类。
在有性生活史的女性中生殖道HPV感染具有普遍性,据统计70%~80%的女性在其一生中会有至少一次的HPV感染,但大多数感染为自限性,超过90%的感染的女性会出现一种有效的免疫应答,在没有任何长期的健康干预时在6到24个月之间可以清除感染。
而持续性的高危型HPV感染则是导致宫颈上皮内瘤变及宫颈癌的主要原因。
试剂测试项目调研报告模板

试剂测试项目调研报告模板调研报告:一、调研目的本次调研旨在了解当前市场上常见的试剂测试项目情况,为公司进一步的研发和生产提供数据支持。
二、调研方法1. 网上搜索:通过搜索引擎和相关论坛了解市场上常见的试剂测试项目。
2. 电话访谈:与相关公司和实验室进行电话联系,了解其使用的试剂测试项目情况。
三、调研结果1. 市场上常见的试剂测试项目包括:ELISA试剂盒、PCR试剂盒、Western blot试剂盒等。
2. 近年来,基因编辑技术相关的试剂测试项目需求逐渐增加。
3. 一些具有特殊功能的试剂测试项目,如RNA干扰试剂、克隆相关试剂等也受到一定关注。
4. 一些领先企业在试剂测试项目的研发方面具有较为优秀的性能和稳定性,受到了广泛的认可和使用。
四、调研结论根据调研结果,市场上的试剂测试项目品种丰富,需求不断增加,而一些在技术和品质上具有优势的企业在市场上受到了广泛的推崇与使用。
因此,公司可在研发和生产试剂测试项目时,着重提高产品的技术含量和品质稳定性,以更好地满足市场需求。
五、建议针对调研结果,我们建议公司应加大对基因编辑技术相关的试剂测试项目的研发投入,抓住这一市场发展的机遇。
同时,也应关注一些新型的试剂测试项目,如RNA干扰试剂、克隆相关试剂等,这些具有特殊功能的试剂在未来有望成为市场的新增长点。
另外,公司在研发过程中应注重技术创新和质量控制,提高产品的稳定性和可靠性,以提升竞争力。
此外,可以加强与一些领先企业的合作,通过技术引进和技术交流等方式,提高自身的研发实力。
六、展望随着生物技术的不断发展,试剂测试项目市场将面临更多的机遇和挑战。
加大研发力度,提高产品质量和技术含量,与领先企业进行合作,将有助于公司在市场中占据更有利的位置。
七、参考文献1. 张三, 李四. 试剂测试项目市场调研报告[J]. 生物技术,2020(1): 45-56.2. 王五, 赵六. 基因编辑技术相关试剂测试市场前景分析[J]. 生物医药, 2019(3): 78-82.以上为本次试剂测试项目调研报告的全部内容,如有不足之处,敬请指正。
04-HPV 人乳头瘤病毒核酸检测试剂盒-产品介绍13-12-17

14
形态学筛查存在的问题
1、假阴性结果(10-30%)面临医疗纠纷;
2、重复性不好;
3、经验性:需要富有经验的专家; 4、增加筛查成本:复诊率过高; 5、在等待复查中承受焦虑和精神压力;
2014年11月2日星期日
15
宫颈癌临床主要检测方法(二)
HPV DNA分型检测方法
---荧光PCR法(默乐生物) ---杂交信号放大法 (HC2)
1、竞争性内标技术:
监测整个核酸抽提和检测过程是 否有误,有利于消除反应出现的 假阴性,结果更可靠。
2014年11月2日星期日
20
产品特点——独特探针引物设计
高保守
无交叉 阴阳性
无漏检
基于HPV分型原理: 根据HPV L1区基因保守序列设计一系列扩增引物富集24种型别的HPV
PCR产物,再针对不同亚型设计不同探针,进行荧光PCR反应,通过荧光信
2014年11月2日星期日
10
宫颈癌前病变各期及宫颈癌的病理模式图
正常宫颈
轻度不典型增生 中度不典型增生 CIN I CIN II
重度不典型增生 CIN III/CIS
浸润癌 Invasive CA
2014年11月2日星期日
11
宫颈癌筛查方案
• 权威组织一致推荐:采用细胞学检 查和HPV DNA联检进行宫颈癌筛查。
2014年11月2日星期日 31
产品市场容量分析
HPV检测试剂 盒未来的市场 规模达222亿元
我们默乐 HPV产品市 场占有率
?
2014年11月2日星期日 32
2014年11月2日星期日
33
CIN1、CIN2、CIN3:子宫颈上皮内瘤变
ASC-US:意义不明确的非典型鳞状细胞
hpv诊断金标准

hpv诊断金标准
人乳头瘤病毒(HPV)的诊断通常使用多种方法,其中包括病理学、分子生物学和临床表现等。
HPV感染的金标准通常是分子生物学检测,特别是聚合酶链式反应(PCR)检测。
以下是一些用于HPV诊断的常见方法和金标准:
1.PCR检测:PCR是HPV感染的金标准诊断方法。
它可以检测
和鉴定HPV DNA的存在,包括不同型号的HPV。
PCR通常分
为定性PCR(检测HPV是否存在)和定量PCR(测定HPV DNA
的数量)。
PCR方法的高灵敏度和特异性使其成为金标准。
2.病理学检测:组织活检和液体基因检测(如液基细胞学)用于
检测与HPV相关的疾病,如宫颈癌前病变。
这些方法可以通过
检查组织或细胞中的异常细胞来诊断HPV感染。
3.HPV疫苗接种记录:对于预防HPV感染的疫苗接种,可以通
过查看接种记录来确认疫苗接种状态,但这并不直接检测当前
感染的存在。
4.临床表现:临床医生可以通过观察患者的症状和病史来怀疑
HPV感染,但这通常需要进一步的实验室检测以确认。
需要注意的是,不同的HPV型号与不同的疾病有关,有些型号与宫颈癌和其他癌症有关,而其他型号与生殖器疣等非癌症疾病有关。
因此,HPV的诊断方法可以根据具体的病情和病史来选择。
最终,如果存在HPV感染的疑虑,建议咨询医疗专业人员,他们可以根据病情选择适当的诊断方法,以确定感染的类型和严重程度。
早期的诊断和干预对于预防HPV相关的疾病至关重要。
HPV基因分型检测试剂盒常见问题(共54张PPT)

四、IC点弱或者没有,但HPV分型阳性点显色正常
可能原因: ①由于IC和HPV DNA之间存在竞争,高 浓度的HPV DNA可能会对IC点的扩增反 应产生竞争性抑制,此现象出现时如
HPV分型点显色正常,则认为分型结果
正确。
六、Biotin(生物素)点不显色 可能原因:①请确认所使用试剂是否仍在有
试验开展实验室要求
HPV临床样本的采集方法及注意事项 临床试验操作注意事项 临床试验结果分析及常见问题
HPV基因分型检测试验项目
——试验开展实验室要求
临床基因扩增实验室设置的一般原则
各区独立
注意风向
因地制宜
方便工作
“十六字方针”
进入各个工作区必须遵循严格的单 一方向顺序!
PCR后区域
(2) 标本保存不当,可引起PCR失败。 收集的标本乱放(未放冰箱),病原体的破裂, 检测的核酸降解,失去了PCR检测的模板或造成
标本污染。
① 加样器通道易形成气溶胶,造成加样器 通道污染,可通过使用有滤筛的吸头避 免污染
(将模板DNA加入PCR系统时,注 意切勿形成喷雾,后者有可能污染别的 反应,所有并非即用管都应盖严)。
放,飘散在空气中的核酸片段、病原微生物可造成实验室 每个区域必须有其专用的工作服及一次性手套;
常PC见R的后原区域因有正(P以CR下确扩5增点使产:物用分析区移) 液器,移液枪及枪头专用。
PCR操作不当造成污染: 如果这些情况的时候,建议对样本稀释10倍重新PCR,然后杂交, 放,飘散在空气中的核酸片段、病原微生物可造成实验室 样本清楚标记好样本号、与试剂分开贮存,使用过的样本归类放好 可能原因:① 样本中含有抑制PCR反应的物质;
hpv 基因分型检测项目介绍(检验科)

HPV检测在治疗后的随访过程中可提示治疗效果
HPV检测灵敏度明显高于细胞学检查
对经组织学诊断为CIN2 及以上病变检测的灵敏度: 细胞学检查仅为55%, HPV检测的高达96%。
HPV检测——ASCUS的分流处理首选
2006 consensus guidelines for management of women with abnormal cervical cancer screening tests European guidelines for quality assurance in cervical cancer screening: recommendations for clinical management of abnormal cervical cytology, part 1. Cytopathology 2008, 19, 342–354
有效避免假阴性带来的漏检
单次检测标本量可达96份
效率高
所需仪器设备简单、通用性好 技术平台通用
投入低,各级实验室均适宜
该技术平台除了可以开展HPV基因分 型外,还可以开展HBV分型与耐药检 测,结核分枝杆菌耐药检测等分子诊 断项目,提供医院整体诊断水平
业界肯定
No Image
问题?
No Image
HPV 基因分型检测流程
结果判读
单一感染 多重感染 阴性样本
HPV18 HPV35,59,66
No Image
HPV 基因分型检测主要仪器设备
试剂准备区 标本制备区 PCR扩增区
冰箱
冰箱 离心机 微量加样器 生物安全柜 (或超净工作台) 电磁炉(水浴锅 或干式恒温器) 旋涡混合器
PCR仪
宫颈感染人乳头瘤状病毒(HPV)的相关高危因素分析

宫颈感染人乳头瘤状病毒(HPV)的相关高危因素分析目的分析影响人乳头状瘤病毒(HPV)感染宫颈的高危因素。
方法选择2014年1月~12月在我院健康管理中心行人乳头状瘤病毒(HPV)检测及宫颈液基细胞学检查(TCT)的女性体检客户1374人(同意并签署临床研究知情同意书),对其行封闭式不记名问卷调查,通过多因素成组Logistic回归分析宫颈感染HPV的相关高危因素。
结果此次研究检测出HPV阳性305例,HPV总感染率为25.10%,其中单一型感染率为17.86%(217/1215),混合型别感染率为7.24%(88/1215),高危型别感染率为22.06%(268/1215),低危型别感染率2.81%(37/1215)。
通过logistic回归分析,发现宫颈柱状上皮异位,吸烟与HPV感染无关;年龄、性伴侣个数、有无使用避孕套、生殖道炎症与HPV感染有关。
结论本研究发现年龄从20岁起每增加一个等级HPV感染的比数比例为2.52;性伴侣个数每增加一个等级HPV感染的比数比例为4.45;不使用避孕套对使用避孕套的HPV感染的比数比例为22.97;有生殖道炎症对无生殖道炎症的HPV感染的比数比例为7.00。
一般人群需开展性行为的宣教、对重点人群实施定期筛查和密切随访,是降低HPV感染和宫颈癌发病率的重要措施,同时对年龄≥50岁妇女、非避孕套避孕者、性伴侣数目多者、反复发作生殖道炎症的高风险人群,应该严密随访。
标签:HPV感染;相关因素;宫颈宫颈癌是全球范围内威胁女性生殖健康的第二大恶性肿瘤。
近年,宫颈癌发病率有明显上升趋势。
其原因与感染人乳头状瘤病毒(HPV)增加有关,HPV 感染使宫颈癌的相对危险增加250倍,HPV检测是宫颈癌筛查的不可缺少的内容[1]。
1974年,德国病毒学家哈拉尔德·楚尔·豪森(HaraWzurHausen)博士发现了人类乳头瘤病毒(Human papillomavirus,HPV),并首次提出了HPV感染与子宫颈癌存在着密切的关系。
两种分子生物学试剂检测高危型HPV不相符结果的验证分析
9例不相符结果进行验证与 比对。方法
用简并引物 一 巢式 P R检测样本 中是否存在 H V D A; D A测序及 C P N 用 N 通过 引物 M 0 / 1和 G 5 6进行巢式 P R扩增 , Y9I P/ C 9例样本
反 向斑点杂交法对标本 中的 HP V进 行分型。结果
扩增 产物 电泳后均可见清晰单一 的 D A条带 。D A测序证实 , 9例样本 中 H V高危 型 3例 , N N 在 P 低危型 5例 , 另 有1 例测序结果不清晰者经反向斑点杂交法检测 为高危型 H V 9与低危型 HP 4 合感染 。结论 P5 V 0混 备较高 的真阴性率 , 特异性 较好 ; 其 荧光 P R具较 高的真 阳性率 , C 其敏感 性较 高。
龚 文波 , 唐 曙明 , 方红 辉 , 杨 自华 , 何 林
( 深圳 市人 民 医院检验 科 , 广东 深圳 5 2 ) 100 8
摘要 : 目的 对 杂 交 捕 获 2代 试 验 ( e ) 荧 光 聚 合 酶 链 反 应 ( C 检 测 高 危 型 人 乳 头 状 瘤 病 毒 ( P 的 h2 与 P R) H V)
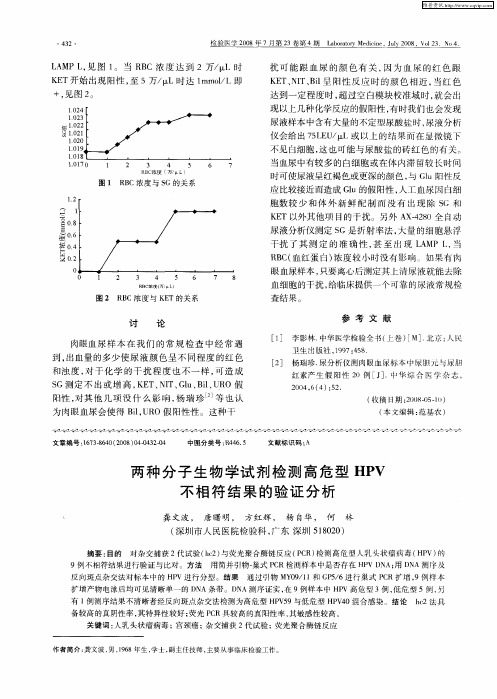
R C 血红蛋 白) 度较 小时 没有影 响 。如 果有 肉 B( 浓
2 3 4 5 6 7 8
眼血尿样本 , 只要离 心后测定其上清 尿液 就能去 除
R BC浓度( 万 L)
血细胞 的干扰 , 给临床提供一 个可靠 的尿 液常规检
杏结果 。
R C浓 度 与 K T的 关 系 B E
维普资讯
验 医学 20 7 08年 月第 2 卷第 4 3 期
Lbro ein, u 08 Vl 3 N ao ty d i Jb20 , o2. o arM c e 4
hpv基因分型检测项目介绍(检验科)

基因分型检测的优缺点
优点
基因分型检测具有高特异性、高灵敏度、可重复性好等优点,能够精确鉴定病 毒的型别和亚型,为临床诊断和治疗提供重要依据。
缺点
基因分型检测成本较高,需要专业的技术人员操作,且对实验条件和设备的要 求较高。此外,由于病毒基因变异和重组的存在,可能导致基因分型检测出现 假阳性或假阴性结果。
个体化治疗
根据检测结果,为患者制 定个体化的治疗方案,提 高治疗效果。
流行病学调查
利用HPV基因分型检测, 开展流行病学调查,了解 病毒的传播方式和流行趋 势。
对社会和个人的影响和意义
提高公共卫生水平
提高个人健康意识
通过HPV基因分型检测,提高宫颈癌 等疾病的预防和治疗水平,降低疾病 的发生率和死亡率。
02
在Hpv基因分型检测中,主要检 测Hpv病毒的基因序列,以确定 病毒的型别和亚型。
基因分型检测的方法和流程
基因分型检测的方法主要包括聚合酶链式反应(PCR)技术、限制性片段长度多态 性分析(RFLP)、单链构象多态性分析(SSCP)和DNA测序等。
基因分型检测的流程通常包括样品采集、DNA提取、PCR扩增、产物电泳和序列 分析等步骤。
治疗方案,提高治疗效果。
流行病学研究
Hpv基因分型检测项目还可以为 流行病学研究提供数据支持,有 助于了解HPV感染的分布和传播 规律,为制定防控策略提供依据。
02
Hpv基因分型检测技术介绍
基因分型检测的基本原理
01
基因分型检测基于DNA的分子生 物学原理,通过检测特定基因的 变异或突变,对生物个体或种群 进行分类和鉴定。
HPV感染不仅与女性宫颈癌的发生有关,也与男性生殖器疣等 生殖系统疾病密切相关。HPV基因分型检测可以帮助男性了解 自身是否感染了HPV,以及感染的具体型别,从而采取相应的 预防和治疗措施。
hpv调研报告

hpv调研报告HPV调研报告引言人乳头瘤病毒(Human Papillomavirus,简称HPV)是一类DNA病毒,可以引起多种不同部位的疾病,包括宫颈癌、外生殖器白斑、生殖器疣等。
近年来,HPV感染患者数量逐年增加,对公共健康和预防控制工作提出了新的挑战。
本调研报告旨在了解HPV的相关知识、流行情况以及预防控制策略,以期提供科学依据。
一、 HPV的基本知识1.1 HPV的分类和特征根据病毒的基因序列差异,人类乳头瘤病毒可分为低危型和高危型。
低危型HPV主要引起外生殖器疣,虽然不会导致癌变,但对患者生活质量产生了一定影响。
高危型HPV是宫颈癌最主要的致病因子,与其他类型的癌症(如肛门癌和口腔癌)也有一定关联。
1.2 HPV的传播途径HPV主要通过性接触传播,尤其是在无保护措施的情况下,如没有使用避孕套等。
此外,HPV还可通过直接接触感染,如母亲感染时会将病毒传给新生儿。
二、 HPV的流行情况2.1 HPV感染率根据调查数据显示,全球范围内HPV感染率较高,其中以发展中国家为主。
HPV感染率在不同地区和人群中存在差异,但总体趋势是逐年上升。
2.2 HPV相关疾病发病率宫颈癌是与HPV感染最为紧密相关的疾病之一,全球每年有超过30万人死于宫颈癌。
除了宫颈癌,HPV还与其他部位的癌症和疾病有关。
三、 HPV的预防和控制策略3.1 HPV疫苗接种HPV疫苗的研发和应用为HPV感染和相关疾病的预防提供了重要手段。
目前,主要有两种可用的HPV疫苗,一种针对高危型HPV,另一种则针对高危型和低危型HPV。
广泛推广HPV疫苗接种可以有效降低HPV感染和相关疾病的发生率。
3.2 宫颈癌筛查宫颈癌筛查是早期发现和治疗宫颈癌的重要手段。
常用的筛查方法包括宫颈薄层细胞学检测(ThinPrep)、宫颈液基细胞学检测(Liquid-based cytology)以及HPV DNA检测等。
3.3 性教育和保护措施加强性教育能提高人们对HPV感染的认知,增强自我保护意识。
HPV-DNA检测(分子生物学实验室建设)等检测

实验室技术层面介绍:
• 按照《医疗机构临床基因扩增检验实验室管理办法》 建设标准化分子生物学实验室
实验室技术层面介绍
• 配备相关检验技术员并按要求取得相关检 验检测资质(上岗证)
实验室技术层面介绍
• 编写了完善的检验管理文件,形成规范的质 量控制管理体系。
临床应用开展情况介绍:
已经开展的临床检测 • 乙型肝炎(HBV)病毒定量检测 • 人乳头瘤病毒(HPV)基因分型 • 结核分支杆菌核酸检测 • B族链球菌核酸检测 2017年计划开展的检测 • 疱疹病毒核酸检测 • 衣原体核酸检测 • 乙型肝炎耐药基因突变 • 丙型肝炎(HCV)RNA定量检测 • 解脲脲原体核酸检测
未来进一步科研应用拓展:
• 利用PCR 技术扩增细菌16SrDNA序列,进行细菌鉴 定及耐药性的相关研究
• 基于PCR技术的肿瘤基因研究
技术难点与创新点:
• 难点:需建立专业的符合标准的分子生物学实验室、 实验人员需经专业委员会培训、考核取得上岗证, 需要有标准化的质控管理文件体系。
• 创新点:分子生物学实验室在安徽省二级医院少有 建立,是医院诊疗相关疾病达到分子学水平的重要 标志,为我院未来生物基因及核酸分子检测的临床 应用和科研打下坚实的基础。
开展初期取得的社会及经济效益
• HPV病毒核酸分型检测(已经完பைடு நூலகம்检测1177例, • 乙型肝炎(HBV)病毒核酸定量检测(已经开展检
测5000例) • 结核分支杆菌核酸检测(已经开展检测1200例) • B族链球菌核酸检测(已经开展检测500例)
已经实现收益70.02元 预计2017年将实现收益超100万元
检验科 三新项目展示
(分子生物实验室建设及相关项目检测)
《人乳头瘤病毒(HPV)核酸检测及基因分型试剂技术审查指导原则》(征求意见稿)精选全文完整版

可编辑修改精选全文完整版人乳头瘤病毒(HPV)核酸检测及基因分型试剂技术审查指导原则(征求意见稿)一、前言本指导原则旨在指导注册申请人对人乳头瘤病毒(HPV)核酸检测及基因分型试剂注册申报资料的准备及撰写,同时也为技术审评部门对注册申报资料的技术审评提供参考。
本指导原则是针对人乳头瘤病毒(HPV)核酸检测及基因分型试剂的一般要求,申请人应依据产品的具体特性确定其中内容是否适用,若不适用,需具体阐述理由及相应的科学依据,并依据产品的具体特性对注册申报资料的内容进行充实和细化。
本指导原则是对申请人和审查人员的指导性文件,不包括注册审批所涉及的行政事项,亦不作为法规强制执行,如果有能够满足相关法规要求的其他方法,也可以采用,但需要详细阐明理由,并对其科学合理性进行验证,提供详细的研究资料和验证资料,相关人员应在遵循相关法规的前提下使用本指导原则。
本指导原则是在现行法规和标准体系以及当前认知水平下制定的,随着法规和标准的不断完善,以及科学技术的不断发展,本指导原则相关内容也将适时进行调整。
二、适用范围人乳头瘤病毒(human papillomavirus, HPV)属于乳多空病毒科的乳头瘤病毒属,是一种小分子的、无被膜包被的、环状双链DNA病毒,基因组长约8000碱基对(bp),分为3个功能区,即早期转录区(E区)、晚期转录区(L区)和非转录区(长控制区,LCR)。
HPV通过直接或间接接触污染物品或性传播感染人类。
该病毒只能感染人的皮肤和粘膜上皮细胞,能引起人类皮肤的多种乳头状瘤或疣及粘膜生殖道上皮增生性损伤。
HPV广泛存在于自然界,据统计70%~80%的女性在其一生中会有至少一次的HPV感染。
但大多数感染为自限性,超过90%的感染的女性会出现一种有效的免疫应答,在没有任何长期的健康干预时在6到24个月之间可以清除感染。
而持续性的高危型HPV感染则是导致宫颈癌及宫颈上皮内瘤变的主要原因。
根据HPV各型别致病力大小或致癌危险性大小不同可将感染生殖道和肛门的HPV分为低危型和高危型两大类。
HPV基因诊断试剂盒

HPV基因分型快速诊断试剂操作流程
采集样本
提取DNA
杂交
显色
PCR扩增
结果判断
检测结果:HPV16、HPV43 检测结果:HPV33、HPV35
HPV检测的临床意义
• (一)宫颈病变的筛查
•1、HPV检测的最大优势之一在于发现高危型HPV阳性而细胞学涂片正 常的妇女,因为这一人群中10%会在四年内发展成CINⅢ。 •2、筛查并浓缩高风险人群,便于进行有效监控,早期发现宫颈癌。 •3、HPV检测的阴性预测值为99%,可将筛查间隔延长至3年一次,大 大地降低了检查成本。
最常见的高危型
53%
HPV16
(HPV16、18、31、
33、45、58 )
宫颈癌患者中高危型HPV感染率(欧州2000年资料)
深 圳 不 同 HPV 亚 型 的 检 出 频 率 统 计 (WHO项目)
注:1.本表统计样本数为1153例,其中阳性样本数为119例; 由于检测样本中存在复合感染,故亚型的检出频率=(该亚型的检出次数 / 所有亚型的检出次数)×100
质的损伤可能已经产生。
病毒学检测:HPV DNA检测(PCR方法),常见方法有:基因芯 片分型检测、HC-2、荧光PCR等
特异性强、灵敏度高,操作简便快捷 (98%)
宫颈分泌物HPV结果
HPV HC2 亚能 凯谱
检测例数 1137 1137 250
阳性例数 159
阳性率(%) 14
111
9.8
98
子宫颈癌的危险因素:
• 行为危险因素:如性生活过早、多个性伴侣、多孕多产、社会经济地位低下、 营养不良及性混乱等; • 生物学因素:如细菌、病毒和衣原体等各种微生物的感染。 • 目前仅有少量研究表明宫颈癌可能存在着家族聚集现象。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
HPV分子诊断试剂 市场/技术/产品/防治2014-04-24 XXXX生物科技有限公司目 录 宫颈癌与HPV HPV检测试剂市场潜力 HPV检测技术 现有HPV分子诊断产品 宫颈癌的防治与筛查宫颈癌 —— 女性第二大癌症这些英年早逝的女艺人,她 这些英年早逝的女艺人 她 们都因罹患宫颈癌而香消玉 殒……z全球每年新增病例56.5 万,新发病例逐年增加, , , 且日渐呈年轻化发展趋 势。
发展中国家宫颈癌发生 率为发达国家6倍,有 50%的病例发生在中国 和印度。
中国每年新增病例 18.15万。
每年有3万多 妇女死于宫颈癌。
妇女死于宫颈癌zz梅艳芳,终年40岁李媛媛,终年41岁宫颈癌生物学病因的研究史宫颈癌与HPV关 系的研究进程1974 1989Zur Hausen提出 HPV与宫颈癌发病可能有 关的假设 国际癌症研究所(IARC)认 为 HPV感染是宫颈癌的主要 病因19951977Keerti Shah证实宫颈癌与 HPV感染有直接关系Laverty在电镜中观察到 宫颈癌活检组织中存在 HPV颗粒 德国科学家豪森(Zur Hausen) 因发现HPV和宫颈癌的关系而获得 2008年诺贝尔生理学或医学奖。
豪森的这一研究成果也使得宫 颈癌成为目前唯一的病因明确的 癌 恶性肿瘤,从而为早期的诊断及 预防提供了理论基础与技术方向。
预防提供了理论基础与技术方向人类乳头瘤病毒 (Human Papillomavirus Papillomavirus, HPV)HPV病毒电镜图种属于乳多空病毒科的乳 一种属于乳多空病毒科的乳 头瘤空泡病毒A属 双链DNA无包膜病毒 环状DNA,约 约8Kb 病毒颗粒直径为50~55 55nm 依靠宿主细胞进行复制、转 录和翻译 宿主和组织特异性HPV病毒结构模式图HPV基因 基因结构及基因分型 结构及基因分型长控制区( LCR) LCRE6早期转录基因区: E6、E7基因 E6、E7蛋白E7L1L1E1 E1以L1、E6和E7基因间的核 苷酸的同源性作为标准,同 源性<90%,属于不同的型 属于不同的型 别。
目前约有170种基因型HPV 被判别出来.晚期转录基因区: 病毒壳粒的蛋白质L2E2 E2 E5 E4HPV基因型分类根据2005年IARC专题讨论会: 9 低危型:6、11、42、43、44、53、81 低危型:6 11 42 43 44 53 81 9 高危型:16、18、26、31、33、35、39、45、 高危型 16 18 26 31 33 35 39 45 51、52、53、56、58、59、66、68、73、82HPV不同亚型感染与许多疾病具有相关性HPV亚型(高危型) 16 18 31、35、45、52、56、58、 66、68 33 39 51、59 HPV亚型(低危型) 6、11 临床病变 肛门生殖器疣、女阴上皮内瘤变、 上皮内瘤变、CIN、宫颈癌 生殖器疣、CIN、宫颈癌 肛门生殖器疣、CIN、宫颈癌 CIN、女阴上皮内瘤变、宫颈癌 肛门生殖器疣、CIN、宫颈癌、 肛门生殖器疣 宫颈癌 鲍 温样丘疹病 肛门生殖器疣 临床病变 尖锐湿疣HPV的致癌机理p53蛋白p53z 细胞中的肿瘤 z HPV表达两 抑制蛋白 种蛋白 — E6 – p53蛋白 — E7 – pRb蛋白E6蛋白抑制p53活性 E7蛋白抑制pRb活性DNA导致两种抑癌蛋白失活,使宫颈细胞 失去抑制癌变的功能 导致细胞恶性 失去抑制癌变的功能,导致细胞恶性 转化,无限增殖,引起宫颈癌 。
HPV致癌机制HPV基因与宿主染色体整合,促进端粒酶活性HPV DNA ,整合通常导致E2 基因中断从而使E6、E7 表达增强。
表达增强 HPV DNA 可能整合在基因不稳定区和转录活跃区,如FRA3B 3p14.2 和 13q14t,而13q14 恰好是pRB 抑癌基因所在位点,整合可使pRB 基因功能失活 而致癌。
而致癌 HPV E2 通过整合到宿主细胞,可调节hTERT 的转录,激活端粒酶。
高危型 高危型HPV的持续感染导致宫颈癌发生 持 导致宫颈癌发 基基 因 检检 测 早早 于 细细 胞 !子宫颈的癌前病变是个相对较长时间的过程,可以进行干预治疗的阶段,是 预防癌的发生、发展和治疗的时期。
因此,宫颈病变的诊治是防癌的重要内容.目 录 宫颈癌与HPV HPV检测试剂市场潜力 HPV检测技术 现有HPV分子诊断产品 宫颈癌的防治与筛查世界范围内HPV 流行状况及基因型分布Lancet Infect Dis. 2007 Jul;7(7):453‐9全球各地宫颈癌发生率分布图z发展中国家的发病率远高于 发达国家。
病例高发区主要集中在非洲、 拉丁美洲及亚洲等地区摘自Human H Papillomavirus P ill i and d Related R l d C Cancers (WHO, 2009)zHPVHPV 感染率 我国各地 感染率中国癌基金会—— 2008年,《中国妇女HPV感染和宫颈癌流行学调查》 ¾中国城市妇女高危型HPV的感染率为15.2% 15 2%,低危型 低危型HPV 感染率为4.4%;农村妇女高危型HPV的感染率为14.6%,低 危型HPV感染率为2.0%; ¾中国妇女HPV感染率的年龄组分布曲线呈现出两个高峰, 分别是20-24 20 24岁和40-44 40 44岁; 岁 ¾我国妇女83%的子宫颈浸润癌由HPV16/18型引起,而84%的 子宫颈鳞癌由HPV16/18型引起。
且未发现子宫颈癌中优势 HPV型别有地区差异。
我国各地宫颈癌发病率 国内宫颈癌高发地区:内蒙 国内宫颈癌高发 内蒙 古、山西、陕西、湖北、湖南、 江西 中国目前每年新发宫颈癌病 例有10万人,占全球病例的1/5。
我国宫颈癌高发区主要集中在 中西部地区,农村略高于城市。
宫颈癌发病高低与生活水平、 卫生和受教育程度相关。
摘自全国肿瘤登记中心 ——《2012中国肿瘤登 记年报》我国各地宫颈癌死亡率我国每年约有 每年 有3万妇女 妇 死于宫颈癌,尤其是 中西部部分地区农村 发病率与死亡率居高 不下,如甘肃武都、 山西阳城等县,宫颈 癌死亡率 36/10万, 万 远高于世界平均水平 (8/10万)。
数据源于中国肿瘤防治数据库HPV筛查的必要性子宫颈癌前病变多无症 状,妇科检查亦难发现。
——有症状的患者80% 以上就诊时已发展为浸润 癌; 从HPV感染到宫颈癌前 颈 病变长达5‐20年 ——此阶段有足够时间 筛查 早期发现 治愈 筛查、早期发现、治愈S hiff Schiffman M C M, Castle l P P. 新英格兰医学杂志 2005; 2005 353:2101 353 2101‐2104诺贝尔奖获得者豪森博 : 诺贝尔奖获得者豪森博士:女性应从30岁起定期检测HPV宫颈癌的发生主要是由于 长期持续的HPV感染而累积 的病变,因此定期检测HPV, 对于开展提前预防与治疗措 施具有重要的意义; 随着宫颈癌的发病率的持 续提高和出现的低龄化现象, 人们对宫颈癌的关注也必将 日益增强,HPV检测将成为 成年女性常规检测项目, HPV诊断试剂产业蕴含着巨 大的市场潜力。
目 录 宫颈癌与HPV HPV检测试剂市场潜力 HPV检测技术 现有HPV分子诊断产品 宫颈癌的防治与筛查现有的代表性HPV分子检测方法 基因芯片法 荧光PCR法 杂交捕获法其中基因芯片法因其具有高通量和分型检测优势而 被广泛使用 与杂交捕获 荧光PCR等不分型方法相 被广泛使用,与杂交捕获、荧光 比更有临床评估意义。
基因芯片法¾设计HPV基因组中的特异性引物 ¾对待测样品中可能存在的HPV基因型进行PCR扩增 ¾扩增产物进行生物素标记 ¾将PCR扩增产物与固定在芯片上的多个亚型HPV特异性探 针进行分子杂交 ¾通过化学显色方式判读结果HPV基因芯片法检测结果判读阴性样本HPV 16 感染HPV 6,52复合感染 PC:positive control,阳性对照荧光PCR法• 荧光PCR法包括:实时荧光定量 法包括 实时荧光定量PCR法和荧 光PCR探针法。
第二代杂交捕获法 (HYBRID CAPTURE 2,HC2)• 利用基因杂交、化学发光、信号放大的原 理,在分子水平同时检测被WHO确认的多 种高危型HPV 病毒DNA。
Qiagen公司产高危 型HPV DNA 检测试 检 试 剂盒(HC2法)杂交捕获法技术流程与原理Step 1:变性 溶解细胞,裂 解和变性核酸, 释放HPV DNA 单链 Step 2:杂交 全长病毒 长病毒RNA探 针与HPV病毒靶 DNA结合,形成 RNA:DNA复合物 Step 3:捕获 RNA:DNA复合物被 包被在微孔板上的 抗体捕获,一抗特 异性结合RNA:DNA 复合物Step 5:产生发光 信号 加入碱性磷酸酶 的底物,产生化 学发光信号 仪 学发光信号,仪 器判读发光信号Step 4:杂交检测 用二抗结合捕获 后的复合物,二 抗偶联有碱性磷 酸酶常用HPV检测方法的比较HPV检测相关专利情况检索关键词:“HPV/包含酶或微生物的测定或检验方法” 检索时间:2014年4月24日 检索专利数据库:国家知识产权局发明专利 检索结果:130项目 录 宫颈癌与HPV HPV检测试剂市场潜力 HPV检测技术 现有HPV分子诊断产品 宫颈癌的防治与筛查国内获批的HPV诊断试剂产品z 目前国内已获得CFDA注册证的国产HPV分子诊断试 剂共计有46项,分属21家公司;进口产品12项,分属5 家公司。
z 生产公司分布:广东(8家)、上海(5家)、北京 (3家)、浙江(1家)、福建(1家)、陕西(1家)、 湖南(1家)、湖北(1家)。
z 获批日期 获批日期:2008-2013年间 年间。
z 涉及的检测方法:PCR荧光法、PCR-荧光探针法、 PCR-反向点杂交法、基因芯片法、PCR PCR PCR-荧光偏振法、 杂交捕获-化学发光法、流式荧光杂交法、表面等离子 谐振法。
