硝酸工业含氮氧化物工艺尾气处理方法
硝酸尾气中氮氧化物净化技术研究

N 超过 允许浓度 的氮氧化物对 人体健 康有极大 的危害 。氮氧化物 尾气处理有 多种方 法 。按 照其 作用 O, 原理不 同有催化还 原法 、 吸收法和 吸附法 三大类 。通过 环境经 济综合 分 析 , 再结 合 具体 情况 选 用液 体 吸 收法 作为硝 酸尾气 的治理方 法。可作 为氮氧化物 吸收剂 的种类很 多 , 如水 吸收 、 硝酸 吸收 、 稀 氨一碱溶 液 吸收 、 亚硫 酸铵 一 亚硫 酸氢铵溶液 吸收 等 , 择尿 素溶 液作为 吸收 剂 。此净 化 过程 是对 氮 氧化 物进 行 还 选
20 1 2年 9月 3
S p.23 e 1 02
文 章 编 号 :0 6—3 9 (0 2 0 0 2 10 2 3 2 o ) 3— 0 7—0 5
硝 酸 尾 气 中 氮 氧 化 物 净 化 技 术 研 究
梁 开 玉 周 应 林 秦 大 超 2 , ,
(. 1 重庆 工商 大 学 化 学 系 , 重庆 4 0 3 ; 重庆 T商 大学 化 学 系 9 00 3 2 7级 学生 , 庆 40 3 ) 重 0 0 3
7. 5
1 6
三级
1 1
2 5
1 0 0 4 硝 酸 , 肥和 火炸 药生 产 氮
氮 氧 化 物 种 类 很 多 , N N 0、 O 、 2 ,N 0 、 s等 , 称 N 造 成 大 气 污 染 的 主 要 是 N 和 有 O、 2 N 2 N 0 、 N O 总 O。 O
摘
要 : 绍 用 酸性 尿 素 溶 液 作 吸 收 剂 , 收 硝 酸尾 气 中 氮 氧 化 物 的 净 化 方 法 。 用 正 交 试 验 介 吸
法 选择 最 佳 工 艺条 件 , 对 其 结 果 进 行 极 差 分 析 和 方 差 分 析 。 该 法 具 有 去 除 率 高、 有 第 二 次 污 并 没
湖南省长沙市长郡中学2022-2023学年高一下学期期末考试化学试题含答案

2022-2023-2长郡集团高一期末考试化学试卷(7月)时量:75分钟满分:100分可能用到的相对原子质量:O ~16Si ~28一、选择题(本题共14小题,每小题3分,共42分。
在每小题给出的四个选项中,只有一项是符合题目要求的)1.打赢蓝天保卫战,提高空气质量。
下列物质不属于空气污染物的是()A.PM 2.5B.O 2C.SO 2D.NO2.下列有关化学用语的表示正确的是()A.甘氨酸的结构简式为B.过氧化氢的电子式:C.空间填充模型可以表示二氧化碳分子,也可以表示水分子D.的名称为2-甲基丙醇3.下列过程中发生的化学反应属于取代反应的是()A.将乙烯通入溴的四氯化碳溶液中B.用光照射甲烷与氯气的混合气体C.在催化剂的条件下,乙烯与氢气反应D.甲烷在空气中不完全燃烧4.下列装置可以用于相应实验的是()A.制备CO 2B.高温熔融烧碱C.验证SO 2酸性D.测量O 2体积5.我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭粉按一定比例混合而成,爆炸时的反应为3222S 2KNO 3C ===K S N 3CO +++↑+↑。
下列说法正确的是()A.该反应氧化产物为CO 2B.该反应的还原剂为SC.C 被氧化,发生还原反应D.KNO 3中的氮元素被氧化6.下列离子方程式书写正确的是()A.氢氧化钡溶液与稀硫酸反应:2244B ==a SO SO =Ba +-+↓B.大理石与醋酸反应:2322CaCO 2H ===Ca H O CO +++++↑C.少量碳酸氢钠溶液与足量石灰水反应:2332HCO OH C ===a CaCO H O -+-++↓+D.将少量CO 2气体通入过量NaOH 溶液中:23===CO OH HCO --+7.下列有关元素单质及其化合物的说法错误的是()A.氨遇到浓盐酸、浓硝酸都会发生反应,产生白烟B.向碳酸氢钠中加入少量水后,碳酸氢钠能溶解,并伴随着吸热现象C.铝制餐具不宜用来蒸煮或长时间存放酸性或碱性食物D.将SO 2气体通入石蕊中,石蕊变红;继续通入SO 2气体,红色褪去8.海水中溴元素以Br -形式存在,工业上用空气吹出法从海水中提取溴的工艺流程如图:下列说法错误的是()A.步骤①、④说明氧化性:Cl 2>Br 2B.步骤②的空气吹出是利用了溴单质易挥发的特点C.步骤③中氧化产物和还原产物的物质的量之比为1:1D.步骤⑤的蒸馏过程中,温度过高可能会降低产品的纯度9.W 、X 、Y 、Z 为原子序数依次增大的短周期主族元素,其中W 元素的最高正化合价与最低负化合价之和为2,Z 的原子序数为X 的两倍,Y 的原子半径在同周期主族元素中最大。
《氨氧化法制硝酸》教案1.docx

《氨氧化法制硝酸》教案•课标要求1.了解我国基本化工的生产资源、基本化工产品的主要种类和发展状况。
2.认识催化剂的研制対促进化学工业发展的重大意义。
•课标解读1.了解氨氧化法制硝酸的工艺流程。
2.明确氨催化氧化制硝酸的原理。
3.掌握在实验室中制备硝酸的方法和操作。
•教学地位硝酸是化工生产屮的重要原料,氨氧化法制硝酸的模拟实验流程及操作方法是高考的高频考点,尤其是氮的循坏对生活、生产的影响为高考的热点。
•新课导入建议1908年,徳国化学家哈伯首先在实验室用氢气和氮气在600 °C. 200个大气压的条件下合成了氨。
后由布什提高了产率,完成了工业化设计,建立了年产1 000吨氨的生产装置,1 000吨氨气利用氨氧化法可生产3 000吨硝酸,利用这些硝酸可制造3 500吨烈性TNT。
这些烈性TNT 支持了德国发动了坚持四个多年头的第一次世界大战。
你知道工业上是如何制备硝酸的吗?•教学流程设计课前预习安排:看教材P:2“,填写[课前自主导学],并完成[思考交流]。
O步骤1:导入新课,本课时教学地位分析。
今步骤2:建议对[思考交流]多提问,反馈学生预习效果。
今步骤3:师生互动完成探究1,可利用[问题导思]作为主线。
步骤7:通过[例2]讲解研析,对“探允2、尾气的净化处理”中注意的问题进行总结。
u步骤6:师生互动完成“探究2”。
u步骤5:指导学生自主完成[变式训练1]和[当堂双基达标]1〜4题。
u步骤4:通过[例1]的讲解研析,对“探究1、硝酸的工业制法”中注意的问题进行总结。
步骤&指导学生自主完成[变式训练2]和[当堂双基达标]中的第5题。
今步骤9:引导学生自主总结木课时知识框架,然后对照[课堂小结]。
安排学生课下完成[课后知能检测]。
1.理解氨氧化法制硝酸的反应原理,并能利用反应原理说明如何制得一氧化氮和选择吸收二氧化氮的条件。
了解氨氧化法制硝酸过程中的尾气对环境的危害及其处理方法,树立环保意识。
硝酸尾气控制与治理进展

硝酸尾气控制与治理进展摘要:本文主要论述了硝酸尾气排放的控制方法和治理方法,综述了近年来一些企业在硝酸尾气治理中的不同方法,达到了节能减排和环境保护的作用。
关键词:硝酸尾气控制治理硝酸尾气治理一直以来是人们关注的焦点问题之一,特别是近几年来对环境污染治理的重视,应该控、治结合,才能达到更好的效果。
1 尾气的工艺控制1.1 优化生产工艺,减少尾气产量1.1.1 优化工艺硝酸生产中,工艺不同,其尾气的产生量也不同,常压法和综合法生产工艺中氮氧化物的含量较高,若未经处理,远达不到国家尾气排放标准,不但对环境造成严重的污染,同时提高了硝酸生产的氨耗,使生产成本增加,而对于较先进的工艺如双加压法,通过严格的控制,即使不进行尾气处理,也可以达标排放,对于新企业,要根据工艺特点,选择合适的尾气处理工艺,及考虑社会效益,同时兼顾经济效益。
1.1.2 优化控制除了工艺对硝酸尾气排放量的影响外,工艺控制对尾气排放量也有一定的影响,合理控制尾气中氧气的含量,可以使NO更好的氧化为NO2,使得吸收率增加,当尾气中O2含量不足时,可以通过补充吸收塔中的二次空气来满足,对于降低尾气中的氮氧化物含量有一定的作用。
2 尾气的治理2.1 吸收法吸收法可以分为化学吸收法和延长吸收法,化学吸收法主要是采用碱性溶液吸收尾气中的一氧化氮和二氧化氮,或者采用具有氧化性的酸性溶液吸收,吸收剂的选择通常以经济、用量小、易再生为前提。
而用碱液吸收处理硝酸尾气的方法使用的更为广泛,优点是处理气量大,不受操作压力的限制,且方法简便,操作稳定。
其缺点是脱除氮氧化物程度不高。
2.1.1 吸收法治理硝酸尾气的机理模型对于吸收法治理硝酸尾气的机理,刘立三[2]在对相关吸收模型研究的基础上,通过平推流和反应动力学两条假设简化了硝酸尾气的碱吸收过程,并在此基础上推导出了吸收速率方程式[3]:-d[NOx]/dt=K1[NOx]2×α×(2-a/α)K1=k1×k3;K1,k3:反应速率常数;α:尾气氧化度;1/a=2-2×K2/K1 这一模型的建立不但使生产厂对生产装置的优化,又方便了设计部门对塔类及其它反应器的设计。
影响氨氧化率的因素

硝酸生产中的氨氧化率及尾气中氮氧化物王靠群硝酸生产过程中,无论是常压法、全高压法、双加压法硝酸装置,液氨在硝酸成本中都占64%~72%左右,以液氨为主要原料的硝酸生产,近来由于液氨价格上涨,生产成本大幅度上升,因此提高液氨的总利用率是降低成本的主要因素之一。
当装置的生产方式确定后,氨氧化率的提高就成了主要因素。
在实际生产中由于氨的氧化率低,造成耗氨高,铂损失大,经济上不合算,铵盐也会增大,因此提高氨的氧化率成为当前硝酸生产中的主要问题。
我国现有大气污染物主要是二氧化硫,其次是氮氧化物。
而今年来氮氧化物的排放量逐渐增多甚至排放总量在以后几年将会超过二氧化硫,成为第一大酸性气体污染排放物。
如今,国家对氮氧化物排放量十分重视,因此硝酸工业生产中的尾气处理十分重要。
硝酸二期生产稀硝酸生产方法采用的是全中压氨氧化法其主要过程为:4NH3+5O2=4NO+6H2O2NO+O2=2NO23NO2+H2O=2HNO3+NO其中氨氧化反应的原理为:将符合工艺要求的氨气和空气,经过严格控制按一定比例混合,自上而下进入氧化炉,在催化剂铂网上. 发生氧化反应,生成一氧化氮,主要反应式:4NH3+5O2=4NO+6H2O+Q另外一小部分生成元素氮损失掉。
反应后的高温氮氧化物气体,经过过热器、废热锅炉等热交换器,温度降到240 摄氏度左右,送入吸收系统。
1.影响氨氧化率的因素:影响因素:(一)铂网暂时性中毒或永久性中毒,由于生产过程中的污染,使铂网活性降低甚至中毒,从而使氨氧化率降低。
铂网中毒的主要原料是气氨、空气中含有油、铁、灰尘等。
铂网破裂脱边,铂网在安装时若安装方式不当,容易一起脱边而造成一部分氨没有反应,而滑过铂网。
(二)氧化炉温度过高或过低,若氧化炉温度过低,触媒尚未活化,氧化率较低。
温度过高,则铂耗高,易出现网前反应,氨氧化率降低。
(三)氧化炉结构形状,设备形状结够要使混合气能在触媒整个截面均匀流过,防止使气体发生涡流或局部浓度过高并防止发生爆炸。
硝酸工艺流程简介
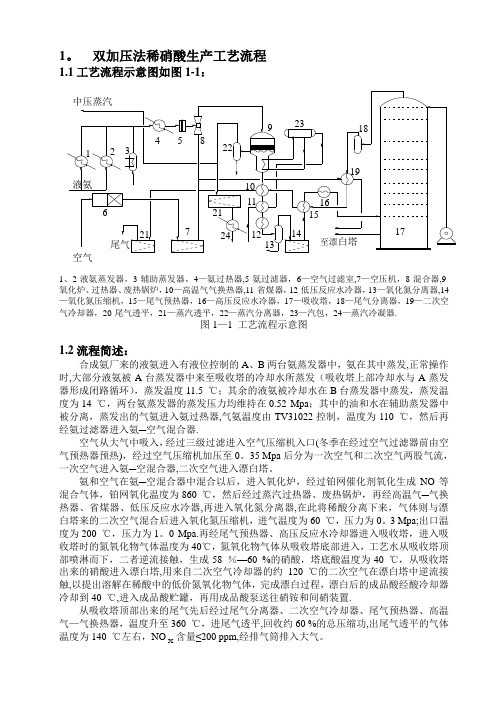
1。
双加压法稀硝酸生产工艺流程1.1工艺流程示意图如图1-1:1、2-液氨蒸发器,3-辅助蒸发器,4—氨过热器,5-氨过滤器,6—空气过滤室,7—空压机,8-混合器,9-氧化炉、过热器、废热锅炉,10—高温气气换热器,11-省煤器,12-低压反应水冷器,13—氧化氮分离器,14—氧化氮压缩机,15—尾气预热器,16—高压反应水冷器,17—吸收塔,18—尾气分离器,19—二次空气冷却器,20-尾气透平,21—蒸汽透平,22—蒸汽分离器,23—汽包,24—蒸汽冷凝器.图1—1 工艺流程示意图1.2流程简述:合成氨厂来的液氨进入有液位控制的A、B两台氨蒸发器中,氨在其中蒸发,正常操作时,大部分液氨被A台蒸发器中来至吸收塔的冷却水所蒸发(吸收塔上部冷却水与A蒸发器形成闭路循环),蒸发温度11.5 ℃;其余的液氨被冷却水在B台蒸发器中蒸发,蒸发温度为14 ℃,两台氨蒸发器的蒸发压力均维持在0.52 Mpa;其中的油和水在辅助蒸发器中被分离,蒸发出的气氨进入氨过热器,气氨温度由TV31022控制,温度为110 ℃,然后再经氨过滤器进入氨─空气混合器.空气从大气中吸入,经过三级过滤进入空气压缩机入口(冬季在经过空气过滤器前由空气预热器预热),经过空气压缩机加压至0。
35 Mpa后分为一次空气和二次空气两股气流,一次空气进入氨─空混合器,二次空气进入漂白塔。
氨和空气在氨─空混合器中混合以后,进入氧化炉,经过铂网催化剂氧化生成NO等混合气体,铂网氧化温度为860 ℃,然后经过蒸汽过热器、废热锅炉,再经高温气─气换热器、省煤器、低压反应水冷器,再进入氧化氮分离器,在此将稀酸分离下来,气体则与漂白塔来的二次空气混合后进入氧化氮压缩机,进气温度为60 ℃,压力为0。
3 Mpa;出口温度为200 ℃,压力为1。
0 Mpa.再经尾气预热器、高压反应水冷却器进入吸收塔,进入吸收塔时的氮氧化物气体温度为40℃,氮氧化物气体从吸收塔底部进入,工艺水从吸收塔顶部喷淋而下,二者逆流接触,生成58 %—60 %的硝酸,塔底酸温度为40 ℃,从吸收塔出来的硝酸进入漂白塔,用来自二次空气冷却器的约120 ℃的二次空气在漂白塔中逆流接触,以提出溶解在稀酸中的低价氮氧化物气体,完成漂白过程,漂白后的成品酸经酸冷却器冷却到40 ℃,进入成品酸贮罐,再用成品酸泵送往硝铵和间硝装置.从吸收塔顶部出来的尾气先后经过尾气分离器、二次空气冷却器、尾气预热器、高温气—气换热器,温度升至360 ℃,进尾气透平,回收约60 %的总压缩功,出尾气透平的气体含量≤200 ppm,经排气筒排入大气。
氮氧化物处理方法

氮氧化物处理方法
氮氧化物的处理主要有以下方法:
1、干法:主要有催化还原法、吸附法等。
催化还原法:适用于治理各种污染源排放出的 NOx。
吸附法:用分子筛等吸附剂,吸附硝酸尾气中的NOx,还可用于其他低浓度NOx 废气的治理。
2、湿法:有直接吸收法、氧化吸收法、氧化还原吸收法、液相吸收还原法和络合吸收法等。
直接吸收法:有水吸收、硝酸吸收、碱性溶液(氢氧化钠、碳酸钠、氨水等碱性液体)吸收,浓硫酸吸收等多种方法,此法可从尾气中回收80~90%的NOx。
氧化吸收法:在氧化剂和催化剂作用下,将NO氧化成溶解度高的NO2和N2O3(三氧化二氮),然后用水或碱液吸收脱氮的方法,在湿法排烟脱氮工艺中应用较多。
氧化还原吸收法:用O3、ClO2等强氧化剂在气相中把NO氧化成易于吸收的NOx 和N2O3,用稀HNO3或硝酸盐溶液吸收后,在液相中用亚硫酸钠(Na2SO3)、硫化钠(Na2S)、硫代硫酸钠(Na2S2O3)和尿素等还原剂将NO2和N2O3还原为N2。
此法已用于加热炉排烟净化。
在同一塔中可同时脱去烟气中SOx和NOx, 脱硫率99%,脱氮率达90%以上。
氮氧化物废气处理方法

氮氧化物废气处理方法氮氧化物废气是工业生产和交通运输中常见的一种废气排放,它对环境和人体健康造成严重危害。
因此,有效处理氮氧化物废气是当前环保工作中的重要任务之一。
本文将介绍几种常见的氮氧化物废气处理方法,希望能为相关行业提供一些参考和帮助。
首先,常见的氮氧化物废气处理方法之一是利用催化剂进行催化还原。
这种方法主要是通过将氮氧化物废气引入催化剂反应器中,在催化剂的作用下,将氮氧化物还原成氮气和水,从而达到净化废气的目的。
这种方法适用于高温下的氮氧化物废气处理,具有处理效率高、操作稳定等优点。
其次,还可以采用吸附剂吸附的方法进行处理。
这种方法通常是将氮氧化物废气通过吸附剂层,利用吸附剂对氮氧化物的吸附作用,将废气中的氮氧化物吸附下来,从而达到净化废气的目的。
这种方法适用于低浓度氮氧化物废气的处理,具有操作简单、成本低等优点。
另外,也可以采用生物法进行处理。
生物法是利用微生物对氮氧化物进行降解,将其转化为无害物质的一种方法。
这种方法适用于低浓度、高湿度的氮氧化物废气处理,具有处理效率高、对环境友好等优点。
除了以上几种方法外,还可以采用化学氧化、等离子体处理等方法进行氮氧化物废气处理。
这些方法各有特点,可以根据具体情况选择合适的处理方法。
总的来说,针对氮氧化物废气的处理方法有多种选择,可以根据废气的特性、处理要求和经济成本等因素进行选择。
希望相关行业能够根据实际情况,选择合适的氮氧化物废气处理方法,从而达到净化废气、保护环境的目的。
同时,也希望相关行业在使用这些方法时,能够严格遵守环保法规,做好废气处理工作,为环境保护贡献自己的力量。
黄烟去除剂-硝酸黄烟(氮氧化物)废气处理最佳选择

黄烟去除剂是针对硝酸黄烟处理的一种专用药剂,是现阶段最经济、最高效去除硝酸黄烟的氮氧化物废气的选择。
黄烟去除剂的研发背景随着国家对酸性废气排放标准的不断提高,硝酸黄烟这一“顽症”,让很多单位尝遍了苦头。
很多企业,尤其是铝氧化、酸洗、光伏能源、电镀、化学抛光等大量使用硝酸的企业,只能是停工停产。
这类对硝酸黄烟(氮氧化物)废气处理需求大企业,普遍出现以下问题:1.硝酸酸雾加再多的碱液还是出现黄色的烟雾,成本也高。
2.硝酸酸雾就算增加多级处理还是不能消除黄色的烟雾,没有有效药剂。
3.硝酸酸雾使用一般的药剂处理出现很大的烟雾,同时臭味特别浓,产生二次污染。
硝酸黄烟出现的本质因素硝酸黄烟是硝酸溶液与金属或其他酸性物质发生化学反应产生的(当金属被氧化成金属离子进入溶液中,硝酸根离子被还原生成NO和NO2气体),其主要组成成分是氮氧化物,包括一氧化氮、二氧化氮、三氧化二氮、四氧化三氮等,其中占比重最大的就是二氧化氮。
针对如何有效去除硝酸黄烟的氮氧化物,北京云程海纳经过清华专家的深入研究实验,最终研发成功了黄烟去除剂-专门处理硝酸黄烟(氮氧化物)废气黄烟去除剂-硝酸黄烟专用药剂黄烟去除剂是北京云程海纳自主研发、生产的一种新型硝酸黄烟废气处理药剂,由无机盐及多种助剂复合而成,呈现黄棕色。
1年升或吨山东25升/桶或1吨/桶云程海纳黄烟去除剂可100%达到国家尾气排放标准要求,使用简单方便,比传统工艺成本降低达50%,是企业去除硝酸黄烟的最佳选择。
深度去除硝酸黄烟和氮氧化物的废气处理,去除率达99%以上!黄烟去除剂反应原理NO2+黄烟去除剂 -> N2 + H2O黄烟去除剂的优势黄烟去除剂如何使用•1、将喷淋净化塔原有废水清空。
•2、计算喷淋净化塔总循环水体积。
•3、加注总体积一半的黄烟去除剂。
•4、同时加入片碱(或液碱)控制PH值在13-14之间,使用过程中当PH值低于10以后加少量碱或黄烟去除剂就可以控制硝酸黄烟。
硝酸尾气处理方法

硝酸尾气处理方法硝酸尾气是指在硝酸生产过程中产生的含有一氧化氮(NO)和二氧化氮(NO2)等氮氧化物的废气。
由于其对环境和人体健康造成的危害,处理硝酸尾气成为了一项重要的任务。
本文将介绍几种常见的硝酸尾气处理方法。
1. 吸收法吸收法是目前最常用的硝酸尾气处理方法之一。
该方法利用吸收剂与硝酸尾气中的氮氧化物发生化学反应,将其转化为无害的化合物。
常用的吸收剂包括碱液和氨水。
碱液可以与一氧化氮反应生成亚硝酸盐,进一步与二氧化氮反应生成硝酸盐,从而实现氮氧化物的吸收和转化。
2. 催化还原法催化还原法是另一种常见的硝酸尾气处理方法。
该方法通过在催化剂的作用下,将硝酸尾气中的氮氧化物还原为氮气和水。
常用的催化剂包括贵金属如铂、钯和铑等。
催化还原法具有高效、节能的优点,但催化剂的选择和使用条件的控制对处理效果至关重要。
3. 吸附法吸附法是利用吸附剂将硝酸尾气中的氮氧化物吸附下来,从而达到净化的目的。
常用的吸附剂包括活性炭和分子筛等。
吸附法具有简单、经济的优点,但吸附剂的选择和再生处理对处理效果和成本起着重要作用。
4. 生物法生物法是一种相对新颖的硝酸尾气处理方法。
该方法利用微生物的生物催化作用,将硝酸尾气中的氮氧化物转化为无害的氮气和水。
常用的微生物包括硝化细菌和反硝化细菌等。
生物法具有无二次污染、低能耗的优点,但对于微生物的培养和环境条件的控制要求较高。
除了上述几种常见的硝酸尾气处理方法,还有一些其他的方法如等离子体法、光催化法等。
这些方法在实际应用中对硝酸尾气的处理效果也得到了验证。
针对硝酸尾气的处理,可以采用吸收法、催化还原法、吸附法、生物法等多种方法。
不同的处理方法有其各自的特点和适用范围,选择合适的处理方法需要综合考虑硝酸尾气的成分、处理效果、成本和环境要求等因素。
通过科学合理的处理方法,可以有效减少硝酸尾气对环境和人体健康的危害,实现清洁生产和可持续发展的目标。
硝酸尾气的处理技术

硝酸尾气的处理技术硝酸尾气的处理国际上对硝酸尾气排放标准日趋严格,一般NOX排放浓度不得大于2×10-4(质量分数),我国规定居住区氮氧化物(换算成NO2)的最高容许浓度为0.15mg/m ,生产车间空气中氮氧化物(换算成NO2)为5mg/m )。
尽管采用加压法产生的尾气中NO 的含量很小,但治理硝酸尾气对环境保护意义重大。
目前,国内外硝酸尾气的处理可归纳为三大类:一是用溶液进行湿法吸收;二是用固体物质进行吸收或吸附;三是用催化剂进行催化转化。
9.1溶液吸收法湿法吸收的优点是处理气量大,不受操作压力限制,且方法简便,操作稳定。
采用常压、低压吸收的硝酸厂用此法处理尾气是比较适合的。
其缺点是处理精度不高,副产物用量不大。
近年来对湿法吸收进行了一些改进,还提出了用新型的活性溶液作吸收剂的方法,如采用酸性尿素溶液或高锰酸钾溶液作吸收剂等。
湿法吸收通用H2SO4、HNO3、NaOH和NaCO3等9.1.1 碱液吸收常用有碱液是NaOH、NaCO3、以及Ca(OH)2、NH4OH和Mg(OH)2等。
用NaOH或NaCO3吸收尾气中氮氧化物的反应如下:2NO2+2NaOH=NaNO2+NaNO3+H2O (1)NO+NO2+2NaOH=2NaNO2+H2O (2)2NO2+Na2CO3=NaNO2+NaNO3+CO2 (3) 由于NaOH价格比较昂贵,而便宜的Ca(OH)2,又因溶解度较小容易堵塞设备,所以目前常用的是NaCO3。
其浓度一般控制在20,30%,浓度过高时速度会稍有下降,且可能会有结晶析出,浓度太低,循环碱液量大,增加设备窖和动力消耗,并蒸浓溶液耗热量多。
碱液吸收中采用Mg(OH)2的悬浮水溶液作吸收剂是较新的方法。
该法的基本原理是:Mg(OH)2水溶液吸收氮氧化物后生成亚硝酸镁悬浮液。
亚硝酸镁加热至140?,便分解为NO和硝酸镁,硝酸镁用氨处理,并以硝酸铵形态回收,所得Mg(OH)2水溶液再用于吸收。
利用SCR脱硝技术处理硝酸排放尾气

利用SCR脱硝技术处理硝酸排放尾气《化工安全与环境》2010年第12期?总第1024期?化工安全与环境?技术专刊利用SCR脱硝技术处理硝酸排放尾气汪家铭(川化集团有限责任公司四川成都610301)摘要:简要介绍了脱硝技术的脱硝原理及工艺流程,对其技术特点进行了分析总结,SCR技术对硝酸生产中排放的尾气进行处理,具有工艺成熟可靠,应用范围广,净化效率高,环保效益好等特点.最后介绍了脱硝技术的应用概况及发展前景,并指出在硝酸生产领域中,SCR技术是一种能够达到严格氮氧化物排放标准的高效可行的实用脱硝技术.关键词:NOx烟气;SCR脱硝;原理;工艺;特点;应用选择性催化还原(SelectiveCatalyticReduction)脱硝技术,简称SCR脱硝技术,是20世纪80年代初开始逐渐应用于工业锅炉和电站锅炉烟气脱硝的工艺,也是目前国际上应用最广,最有成效的烟气脱硝技术之一.在日本,欧洲,美国等国家地区的大多数电厂中基本都应用该技术.SCR技术是在金属催化剂作用下,以氨或尿素作为还原剂,与烟气中的NOx发生还原反应生成无害的氮和水,而不与烟气中的氧气发生反应,达到去除烟气中的NOx的目的,脱硝效率约为80%~90%.与其他脱硝技术相比,具有装置结构简单,脱硝效率高,技术成熟,运行可靠,便于维护等特点,并且没有副产物产生,不形成二次污染.硝酸生产中排放的尾气NOx主要包括NO和NO,是造成大气污染的主要污染源之一,不仅严重污染环境,而且也增加了硝酸生产过程中的氨耗,提高了硝酸生产成本,因此对硝酸尾气进行有效治理并确保达标排放就显得十分重要,对此世界各国都在进行广泛的研究.1脱硝原理SCR脱硝技术的原理是烟气和氨(液氨或氨水)与空气的混合物在经过SCR反应器的蜂窝式或板式催化剂层时,烟气中的NOx和加入SCR反应器中的NH,空气中的0发生选择性催化还原反应,生成无污染的N和水.NOx与NH,的摩尔比为1:1.2,脱除1kgNOx(以NO为例)的氨耗量为0.444kg.其主要反应式如下:4NO+4NH3+02=4N2+6H2O6NO+4NH3:5N2+6H202NO2十4NH3+02=3N2+6H2O6NO2+8NH3:7N2+12H20SCR催化剂一般用使用TiO作为载体的V0,WO及MoO等金属氧化物,其他组成结构的催化剂也已做了大量的实验研究,其催化性能不均.其反应过程为:NO,NH,O从烟气中扩散至催化剂的外表面并进一步向催化剂中的微孔表面扩散,在催化剂的微孔表面上被吸附,随后反应转化成N和H0.N:和H0从催化剂表面上脱附下来,从微孔内向外扩散到催化剂外表面,最后扩散到主流气体中被带走,烟气完成整个脱硝过程.不同催化剂在其不同的活性阶段,最适宜的温度也不同.通常所选催化剂的起燃温度为260~C,最佳的操作温度为26O℃~350~C,该反应为放热反应.由于NOx在烟气中的浓度较低,因此反应引起催化剂温度的升高可以忽略不计.2工艺流程SCR脱硝系统主要由液氨存储与供应,氨/空气喷嘴,SCR控制,SCR反应器,SCR的吹灰和输灰等部分组成.液氨由槽车运送到液氨储罐,以液体形态储存于储罐中,输出的液氨经氨蒸发器后变成气氨,将其送至气氨缓冲槽备用.缓冲槽内的气氨经减压后送人气氨/空气混合器中,与空气预热器出来的热空气混合后,通过喷氨隔栅的喷嘴喷入来自锅炉的烟气中并与之充分混合,继而进入SCR反应器.当烟气流经SCR反应器的催化层时,与雾状氨/空气发生选择性催化还原反应,去除NOx后的烟气经电除尘器进入湿法脱硫系统进一步净化,净化合格后的尾气通过排气筒排放到大气中.整个SCR脱硝系统工艺流程见图1.图1SCR脱硝系统工艺流程图统对于含尘量不同的烟气,SCR反应器分别布置在脱硝流程中的相应位置.高含尘SCR反应器布置在锅炉出口和空气预热器入口之间的烟道上,从锅炉出来的烟气与还原剂氨和空气在烟道中混合后从上部进入SCR反应器,与反应器中的催化剂接触,在活性物质的催化下,烟气中的NOx和还原剂反应生成N,和H,O.高含尘SCR烟气中飞灰含量较高,需要设置蒸气/声波吹灰系统来对催化剂层进行吹扫,以阻止积碳和维持催化剂活性.高含尘SCR反应器布置在高温段,不需要另设加热装置来提升烟气温度即可达到催化剂工作温度. 低含尘SCR反应器布置在除尘器后,从锅炉里出来的烟气经过除尘后,与还原剂氨和空气在烟道中混合,从上部进——cHEM|cALSAFETY&ENVlRONMEN——?13?人SCR反应器,与反应器中的催化剂接触,在活性物质的催化作用下,烟气中的NOx和还原剂反应生成N和H:0.低含尘SCR烟气飞灰含量小,基本不会发生催化剂中毒,失活或堵塞的情况.催化剂使用寿命长,更换费用低.但低含尘SCR烟气经过空气预热器和除尘器后,烟气温度远低于催化剂工作温度,通常需要配置烟气加热装置提高烟温.3技术特点3.1工艺成熟可靠还原剂提供氨水或者液氨两种可选方案,可满足不同需要.催化剂连续使用寿命达到24000h以上,蜂窝状或板式催化剂单元设计,保证最大催化剂表面积.独特的平衡导流板的设计保证脱硝反应器进口烟气和氨均匀分布.氨喷射系统即采用涡流混合方式以保证装置出口氨的低逃逸率.3.2应用范围广适应性强,可用于以烟煤,褐煤,重油,天然气为燃料或焦炉煤气,垃圾焚烧,生物质燃烧的锅炉,窑炉,烧结机,工业炉等不同烟气的脱硝处理.同时具备在高尘,低尘,高温,低温不同工况下烟气脱硝的工艺技术路线.还原剂氨来源容易,质优价廉.3.3净化效率高NOx去除效率达到85%以上,最大脱硝效率超过90%,且排放浓度达到国家有关排放标准.出口氨气排放量<3x 10,SO,/SO转化率不大于1%.具备脱除硝酸尾气,硝酸溶化贵金属尾气等不同浓度NOx烟气脱硝工艺技术,运行可靠,是工程上应用最多的烟气脱硝技术.3.4环保效益好反应器可以布置在省煤器和空预器之间,或脱硫塔之后,反应副产物为N:和H0,无二次污染.具有很好的负荷适应性,在不同负荷下均能保证脱硝率和氨的逃逸率,安全性能好.通过优化设计蜂窝状或板式催化剂单元及其运行方式,能有效抑制SO的产生以降低SCR反应器出口烟气的腐蚀性. 4应用概况硝酸生产废气污染源主要是硝酸排放尾气,稀硝酸储罐放空气,浓硝酸镁尾循环槽和浓硝酸储罐放空气等,其主要污染物为NOx,同时含有少量的硝酸雾,吨硝酸废气排放量为3100~4500m.因生产工艺不同,NOx排放浓度有着明显的差别,必须根据生产工艺采取适当的控制措施.通常,硝酸尾气治理措施是常压法中的低压法采用化学吸收法,中压法采用化学吸收法或SCR法,综合法,高压法和双加压法采用SCR法.SCR法虽然投资较少,但需消耗一定数量的氨,因此相对来说只有在尾气量小,NOx浓度低时才具有一定的优势.硝酸排放尾气处理主要方法的比较见表1.表1硝酸排放尾气处理主要方法比较脱硝方法处理介质操作条件优点缺点催化还原法选择性氨控制氨与尾气中NOx的化学配技术成熟,NOx脱除率高,还原增加硝酸生产过程中的氨耗,运(SCR)比剂消耗少行费用较高催化还原法非选择天然气,石油,控制氨与尾气中NOx的化学配NOx脱除率较高,可回收大量余还原剂消耗量大,NOx不能回收性(NSCR)CO,H2比,不用催化剂热利用物理化学吸附法减湿剂,分子筛水对吸附有影响,分子筛需再生NOx脱除率高,回收NOx返回尾气需经过除湿处理,分子筛再干式吸附系统生频繁物理化学吸附法活性炭,水或硝酸游离氧含量要有一定浓度NOx脱除率较高NOx脱除效率较低,吸收剂用量湿式吸附多,设备庞大增大尾气的氧化空问,延长NO吸收液不需后处理,工艺简单,延伸吸收法水或硝酸老装置改造难度大.投资较多的吸收时间操作稳定碱液,石灰乳,双NO:NO2=1,处理烟气量很小吸收液价廉易得,副产品有利用在尾气中NOx浓度不高时,氧化学吸收法氧水的情况下可使用价值化比较缓慢,影响吸收效果我国现有7O余家硝酸生产企业,这些企业的NOx排放状况相差较大,有的企业生产工艺相对落后,仍然采用常压法,综合法,其NOx排放量较多,甚至有些企业出现超标排放的情况.而有些企业采用先进的清洁生产工艺,并设置了行之有效的尾气处理装置,大大削减了NOx排放量.硝酸尾气治理应该贯彻科学发展观,坚持先抓源头与后治末端相结合的原则,根据所采用的硝酸生产工艺,变末端尾气治理为清洁生产控制,同时采用行之有效的尾气治理方法,使硝酸尾气经治理后能达标排放,实现经济效益,社会效益与环境效益的最佳结合.目前,作为一种颇具潜力的先进实用技术,SCR脱硝技14?术已在欧洲,日本的硝酸企业得到广泛的应用.在我国作为硝酸尾气治理的首选技术,不少国内的硝酸企业也选择了SCR脱硝技术.据统计,我国山西,安徽,四川1,河南,陕西等地6O家主要硝酸生产企业中有18家采用了SCR技术,2 家采用深冷吸收+SCR,这些企业的硝酸生产工艺是常压法,中压法,高压法,综合法和双加压法.不同的硝酸装置,因配置的后加工产品不同,加入硝酸吸收塔的水含酸浓度不同,则SCR技术处理的费用也有所差别,氨耗费用为吨硝酸0.19~15.7元不等.对于不同工艺不同规模的硝酸生产装置,其尾气处理系统的投资各不相同.对中压法硝酸装置,采用SCR技术处理硝酸尾气,年产1万t ——CHEMICALSAFETY&ENVlRONMENT~——硝酸装置需投资l4万元,则年产10万t规模装置建设项目总投资1.5亿元,SCR技术投资需140万元,约占总投资的1%.在采用SCR技术的硝酸尾气处理系统中,如图2所示,SCR装置(图中DeNOx反应器)可以安装在硝酸尾气降压装置的前面(位置一),也可以按照在其后面(图中虚线所示位置二).图2SCR装置在硝酸尾气处理系统中的安装位置5发展前景在众多的脱硝技术中,SCR法是脱硝效率最高,最为成熟的脱硝技术.SCR在全球范围内有数百台的成功应用业绩和十几年的运行经验,日本和德国95%的烟气脱硝装置采用SCR技术,1975年在日本Shimoneski电厂建立了第一个SCR 系统的示范工程,其后SCR技术在日本得到了广泛应用.在欧洲已有12O多台大型装置成功应用的经验,日本大约有170 套装置,接近100GW容量的电厂安装了SCR设备,美国政府也将SCR技术作为主要的电厂控制NOx技术,SCR法已成为目前国内外电厂脱硝比较成熟的主流技术.SCR技术在硝酸生产的应用方面,欧洲硝酸生产中,几乎所有的硝酸企业都采用了SCR脱硝技术,并取得了良好的效果.NOx实际排放浓度基本控制在200~410mg/m范围内, 主要集中在250~350mg/m之间.据统计,在欧洲46个硝酸企业中,NOx排放浓度在200mg/m以下的有11个,占24%. 200~350mg/m的有10个,r与22%.350~410mg/nl的有21 个,占46%.410~1000mg/m的有4个,占8%.美国,日本,欧洲等发达国家和地区现有硝酸企业NOx排放浓度限值在410~1200mg/m之间,新建企业在350~700mg/m之间.有些发达国家硝酸企业已采取了污染防治最佳可行技术BA T 来控制污染物的排放,见表2.工业上生产稀硝酸几乎都是先将氯氧化为NOx混合气,然后用水或低浓度硝酸对混合气进行吸收.由于NOx特殊的化学特性,硝酸吸收塔不能将其完全吸收,总存在一定浓度的NOx随尾气排放.虽然硝酸生产尾气排放量只占工业上向大气排放NOx总量的很小一部分(约为0.2%),但由于其排放相对集中,对当地的环境破坏程度较大,人体健康危害严重.我国硝酸生产企业所排放的尾气中NOx含量很高,有的甚至高达4000mg/m(质量浓度,相当于体积分数约2000×10).由于吸收工艺的不同,硝酸尾气排放中NOx的浓度会有所区别.表2发达国家和地区硝酸企业NOx排放浓度限值mg/in国家与国际组织名称现有企业新建企业执行年份美国一4501975年修订欧盟4503501988年制订日本4lO4l01977年制订德国一4502004年引用英国4503502002年引用意大利5005002000年引用荷兰12004501987年制订新加坡7007002001年修订欧洲化肥工业BA T技术4002002001年制订欧盟硝酸工业BA T技术10~3001O~15O2007年制订英国污染整体控制IPC技术3002001999年制订BAT技术即污染防治最佳可行技术,包括:①优化吸收(高压吸收,延伸吸收,低温吸收或冷冻吸收);②选择性催化还原(SCR) 技术;③非选择性催化还原(NSCR)技术;④HO2化学吸收.目前,我国没有专门的硝酸行\Jl,污染物排放标准,硝酸工业废气排放执行《大气污染物综合排放标准》(GB16297~1996),该标准规定现有硝酸生产装置NOx排放限值为1700mg/m,新建装置NOx排放限值为1400mg/m.据对现有主要硝酸生产企业的调查结果显示,NOx排放浓度为96—3700mg/m,其平均值为862mg/m.虽然平均值没有超过相关标准,但上限值已远远超过标准值.特别是对于常压法,综合法等生产工艺,其硝酸尾气中NOx的质量浓度一般都比较高,与国外的400mg/m的排放标准相比,差距更大.我国目前硝酸工业执行的污染物排放标准较为宽松,远落后于发达国家和地区的控制水平.在当前严峻的环保形势下,现行标准已不能有效控制硝酸企业的污染排放,更不能适应新时期国家环境保护与管理的要求和促进我国硝酸产业结构调整和经济增长的需要.新的国家硝酸工业污染物排放标准的制订势在必行.以后制订的新标准将会与国际接轨,设定更为严格的控制标准,使现有企业和新建企业的NOx排放限值分别为600mg/m和350mg/m,最终使所有硝酸生产企业的NOx排放限值为350mg/m,而达到新的排放标准,要靠硝酸清洁生产工艺和先进的脱硝技术来实现.我国是硝酸生产大国,目前硝酸行业正处于超常高速发展状态.在硝酸生产中,选择尾气处理技术应遵循以下原则: ①NOx的排放浓度和排放量满足有关环保标准;②技术成熟, 运行可靠,有较多业绩,可用率达到90%以上;③尽可能节省建设投资;④布置合理,占地面积较小;⑤吸收剂水和能源消耗少,运行费用低;⑤吸收剂来源可靠,质优价廉;⑥副产物,废水均能得到合理的利用或处置.结合目前国内硝酸生产的发展趋势,国家目趋严格的环保要求,SCR技术的特点并适当兼顾我国现有企业技术水平和实际情况,在硝酸生产领域中,SCR应该是一种具有广阔发展前景的首选脱硝技术,同时也是能够达到严格氮氧化物排放标准的高效可行的实用技术,对我国硝酸工业的技术升级,优化产业结构,有限控制污染物的排放,增强企业的核心竞争力都将会起到积极的促进作用.■参考文献(略)一CHEMICALSAFETY&ENVIRONMEN一?15?。
硝酸生产尾气中NOx和N2O联合脱除技术研究进展

化工进展Chemical Industry and Engineering Progress2023 年第 42 卷第 7 期硝酸生产尾气中NO x 和N 2O 联合脱除技术研究进展李佳,樊星,陈莉,李坚(北京工业大学区域大气复合污染防治北京市重点实验室,北京 100124)摘要:采用氨氧化法生产稀硝酸时会排放NO x (NO 和NO 2)和N 2O 等有害气体,可导致光化学烟雾(NO x )、臭氧层消耗(NO x 和N 2O )、全球变暖(N 2O )等环境问题,减少硝酸生产尾气中NO x 和N 2O 的排放势在必行。
本文在分析硝酸生产过程中NO x 和N 2O 产生途径及减排措施的基础上,根据国内外研发和应用情况总结了联合脱除硝酸生产尾气中NO x 和N 2O 的主要技术路线,包括利用SCR 催化剂同时催化NO x 和N 2O 还原和利用复合式催化剂同时催化NO x 还原和N 2O 分解等一段式工艺以及先催化N 2O 分解后催化NO x 还原、先催化NO x 还原后催化N 2O 还原和先催化NO x 还原后催化N 2O 分解等两段式工艺,分析了不同技术路线的原理、特点及面临的挑战。
文中指出了一段式工艺主要存在N 2O 净化性能有待提升的问题,两段式工艺中先催化NO x 还原后催化N 2O 分解的工艺在减少还原剂消耗量、促进N 2O 去除等方面具有优势,未来需围绕同步降低SCR 脱硝和N 2O 分解所需温度、提高催化剂对共存气体(O 2、H 2O 等)的耐受性等方面开展进一步研究。
关键词:硝酸生产尾气;氮氧化物;温室气体;选择性催化还原;N 2O 分解;催化剂中图分类号:X51 文献标志码:A 文章编号:1000-6613(2023)07-3770-10Research progress of simultaneous removal of NO x and N 2O from the tailgas of nitric acid productionLI Jia ,FAN Xing ,CHEN Li ,LI Jian(Key Laboratory of Beijing on Regional Air Pollution Control, Beijing University of Technology, Beijing 100124, China)Abstract: Harmful gases such as NO x (NO and NO 2) and N 2O are emitted during the production of dilute nitric acid by ammonia oxidation, which can lead to environmental problems such as photochemical smog (NO x ), ozone layer depletion (NO x and N 2O), and global warming (N 2O). It is imperative to remove NO x and N 2O from the tail gas of nitric acid production. After introducing the generation pathways and control measures of NO x and N 2O during nitric acid production, we summarized the main technological routes for simultaneous removal of NO x and N 2O from the tail gas according to the research, development and application situations, including one-stage processes such as simultaneous SCR of NO x and N 2O, SCR of NO x and decomposition of N 2O over a composite catalyst, and two-stage processes such as catalytic N 2O decomposition followed by SCR of NO x , SCR of NO x followed by SCR of N 2O, and SCR of NO x followed by catalytic N 2O decomposition. The principles and characteristics of different technological routes were analyzed. It was pointed out that the one-stage processes face challenges of improving the purification performance toward N 2O. The two-stage process of SCR of NO x followed by catalytic N 2O decomposition, has advantages of low consumption of reducing agent and high purification efficiency of N 2O. Further综述与专论DOI :10.16085/j.issn.1000-6613.2022-1614收稿日期:2022-09-01;修改稿日期:2023-03-03。
考点11氮及其化合物(好题冲关)(原卷版+解析)

考点11 氮及其化合物(好题冲关)【基础过关】1.(2022·重庆市育才中学模拟预测)氯化汞与氨水发生反应2NH3+HgCl2=Hg(NH2)Cl↓+NH4Cl,相关物质的化学用语正确的是( )A.-NH的结构式为Cl的结构示意图为B.+4C.NH3的电子式为D.Hg(NH2)Cl中N的化合价为23.下列制取NH4HCO3的实验原理与装置能达到实验目的的是( )A.用装置甲制取NH3B.用装置乙制取CO2C.用装置丙制取NH4HCO3溶液D.用装置丁获得NH4HCO3固体4.(2023·广东省深圳市高三模拟)含氮化合物的反应具有多样性。
下列有关反应方程式书写不正确...的是C.浓硝酸受热分解:4H++4NO3-4NO2↑+ O2↑+ 2H2O( )A.使用A装置制备NH3时,分液漏斗中应盛放浓氨水,利用了氨水的碱性弱于NaOHB.装置B中盛放湿润蓝色石蕊试纸,打开K2,关闭K1,可证明NH3为碱性气体C.利用C装置模拟候氏制碱法时,可将a和c连接D.将a和d连接验证NH3与Cu2+的配位能力强于H2O6.氨既是一种重要的化工产品,又是一种重要的化工原料。
下图为合成氨以及氨催化制硝酸的流程示意图。
下列说法不正确的是( )A.可以利用NH3易液化的性质分离出NH3B.合成氨以及氨催化制硝酸的流程中氮元素均被氧化C.可以用NH3进行氨氧化物的尾气处理D.吸收塔中通入A是为了提高原料的利用率7.以天然气为原料合成氨是新的生产氮肥的方法,其工艺流程如下。
下列说法正确的是( )A.反应①使用催化剂可提高反应速率和甲烷的平衡转化率B.反应②的原子利用率为100%C.生成1.0 mol NH4NO3至少需要0.75 mol CH4D.反应③理论上当n( NH3):n(O2)= 4:3时,恰好完全反应8.氮及其化合物在生产生活中具有广泛的应用。
氨气可用于生产氮肥和处理NO x 等气体,氨水可用于吸收SO 2,NO x 可用于制取硝酸,硝酸可洗涤试管上的银镜。
工业上生产硝酸的流程

工业上生产硝酸的流程
1.氮气的获取:从空气中直接提取氮气,或者从天然气、工业尾气中提取氮气。
2.氧气的获取:从空气中通过分离技术得到氧气,或者从空气中提取氧气。
3.氮氧混合气的制备:将氮气和氧气按一定比例混合,生成氮氧混合气。
4.氮氧混合气的氧化反应:将氮氧混合气注入反应釜中,控制温度和压力,促进氮氧混合气的氧化反应,生成氮氧化物。
5.氮氧化物的吸收:将氮氧化物通过洗涤设备或吸收塔进行吸收,得到硝酸溶液。
6.硝酸的提纯:通过蒸馏、结晶、吸附等方法将硝酸进行提纯,得到高纯度的硝酸。
7.硝酸的存储:将硝酸储存在专用的储罐中,保持其稳定性和安全性。
8.硝酸的分装:将硝酸按照客户要求进行分装,于是输往各个终端市场。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
精心整理
硝酸工业含氮氧化物工艺尾气处理方案随着二十一世纪的到来,“绿色环保浪潮”已在世界范围掀起,环境保护已成为国际交往与协商的重要议题。
成果内容简介
在各种硝酸工业中会产生大量的含NOX 工艺尾气,NOX 的排空即引起了严重的环境污染又造成了NOX 资源的浪费。
NOX 。
吸收。
从水洗塔出来的尾气依次进入碱吸收塔,此时由于氧化度已经很低,有利于价值较高的亚硝盐生成。
当尾气从系统出来后,已经达到了国家排放标准的净化气体经过引风机排空。
在整个过程中,可以从水洗塔得到稀硝酸,经混入一定比例的浓硝酸后,可返回生产工段继续使用;从碱吸收塔可以得到硝酸盐和亚硝酸盐母液,
去结晶工段经结晶分离最终得到硝酸盐、和亚硝酸盐副产品。
既避免了氮氧化物资源的损失,又减少了氮氧化物对大气的污染。
工业塔的流程简图见图1,填料塔内充高效规整填料,型号为250Y波纹板聚丙烯塑料填料。
由图可知,由草酸反应釜出来的氮氧化物,通入足量空气经缓冲罐后,由防腐风机塔底引入塔内。
塔顶的吸收剂自上而下流动,逐步与气体接触,进行气液反应吸收。
在塔底产生的稀硝酸溶液由硝酸循环泵运送到换热器中进行换热,降温
60米
为
效益突出。
立项情况
化学工业如何实施减少废料、防止污染,向“洁净化工”转化,已成为社会关注的焦点。
在水环境、生态环境遭到人类生产活动严重破坏的同时,大气环境也日趋恶化,历史上世界各地曾多次发生大气污染公害事件,对人类的生存环境构成了极大的威胁。
在各种硝酸工业中会产生大量的含NOX工艺尾气,NOX的排空即引起了严重的环境污染又造成了NOX资源的浪费。
为此,对硝酸工业工艺尾气中的NOX
进行回收利用,既是“洁净化工”生产的要求,又是厂家降低生产成本,提高产品市场竞争力的必然选择。
草酸作为一种基本的化工原料,在国民生产中具有重要的地位。
硝酸氧化法生产草酸是目前最具有市场竞争力,前景最好的一种方法,但该法的生产过程中,会产生大量的含氮氧化物尾气,如不对该部分进行回收利用,在造成环境污染的同时,也大大的提高了草酸生产的成本。
NOX分
降低N
是目前
目前该技术已完成2万吨草酸尾气处理的工业化装置。
本技术共采用七个填料塔完成对该废气的整个处理过程,其中前四塔为水吸收塔,后三塔为碱吸收塔,经过本系统处理的草酸生产过程产生的硝酸尾气,最终氮氧化物排放浓度小于200ppm,根据最新国家标准,60米烟囱的氮氧化物排放浓度为不高于240ppm,因此,所排尾气已完全符合国家标准。
评价情况
1999年6月至1999年10月天津大学,在湖南省株洲选矿药剂厂完成了20000吨/年氧化法草酸NOX回收装置的设计、制造、安装和试车工作,于1999年11月投入运
行,2000年经双方共同测试,结果表明达到合同规定的各项经济技术指标和国家关于氮氧化物的排放标准。
试车成功以来设备运行稳定,氮氧化物各项指标完全达标排放。
和同类技术相比,使用该技术硝酸回收率提高10~15%。
由于常压操作,与同类中高压设备相比每年节能
(1000千瓦/时-39千瓦/时)×7200×0.5元/度=345.96万元
使用该技术每年可以副产硝酸钠1000吨,亚硝酸钠4000吨。
每年为企业新增销售
收入
40000.15万元/)×4000=410
2001年
4.
1998年10至1998年底首先在河北省唐山市石城化工厂3000吨/年氧化法草酸生产装置上实现工业化,运行结果表明达到设计要求和国家关于氮氧化物的排放标准。
1999年6月至1999年10月天津大学与大江研究所合作,在湖南省株洲选矿药剂厂完成了20000吨/年氧化法草酸NOX回收装置的设计、制造、安装和试车工作,于1999年11月投入运行,2000年经双方共同测试,结果表明达到合同规定的各项经济技术指标和国家关于氮氧化物的排放标准。
从工业装置的运行情况来看,本技术同目前同类的其他的技术相比,1、在同等达标的条件下,比中高、压法脱氮操作费用低,以2万吨草酸生产为例,如用高压法,由于系统加压引起动力消耗大约为1000千瓦/小时,而本技术仅用一39千瓦/小时引风机即可;动力消耗每年减少近300万元。
2、与其他低压法脱氮技术相比,本技术易实现达标,而其他技术如喷射吸收等难以有较高的氮氧化物脱除率。
推广的目的和意义
含NOX
功实施具有重要经济及社会效益。
5.推广的主要技术内容
本技术采用天津大学具有新型塔内件的高效规整填料塔技术,大幅度的提高塔的处理能力和吸收效率,降低了设备投资,使吸收过程得以顺利实现;实现了常压下,采用七塔串联处理含氮氧化物硝酸工业工艺尾气,排放达到国标;整个工艺前部分采用水吸收后部分采用碱吸收,水吸收过程生成的稀硝酸会对氮氧化物起到氧化作用,提高氮氧化物的氧化度,使其更加利于吸收。
从碱吸收塔可以得到硝酸盐和亚
硝酸盐母液,去结晶工段经结晶分离最终得到硝酸盐、和亚硝酸盐副产品;该项目实施过程中采用先进的设计理念和计算方法,经实际验证符合实际;所用设备采用槽式液体分布器和双环旋流气体分布装置,同时考虑气体和液体分布,使吸收塔保持大通量和高效率。
运用本技术由酸塔回收所得的硝酸浓度最大可达54.6%,由碱塔所得到的亚硝酸钠与硝酸钠比例可达8:1。
实施该项目的基础条件
该项目属于环境保护领域的高新技术,项目最初应用于处理硝酸氧化法生产草酸过
尾气从系统出来后,已经达到了国家排放标准的净化气体经过引风机排空。
在整个过程中,可以从水洗塔得到稀硝酸,经混入一定比例的浓硝酸后,可返回生产工段继续使用;从碱吸收塔可以得到硝酸盐和亚硝6
盐母液,去结晶工段经结晶分离最终得到硝酸盐、和亚硝酸盐副产品。
既避免了氮氧化物资源的损失,又减少了氮氧化物对大气的污染。
本技术可为20000吨/年氧化法草酸生产厂家每年创利税700多万元,其中由于采用常压操作仅此一项便可为厂家节省耗电340万元;利用本技术碱吸收过程所得的副产品亚硝酸钠与硝酸钠的比
例较高,由于亚硝酸钠价值相对较高。
因此每年可另外为厂家创利税400万元。
本技术经济效益良好。
在环境保护成为人民日益关心的重要议题的前提下,环境保护技术必将会有越来越大的市场,此前,有人估计我国未来10年中环保市场约为5000个亿人民币。
本技术在常压下实现了重要大气污染源氮氧化物的回收利用,同时由于副产品多为价值较高的硝酸盐,使得本技术在本领域具有一定的竞争力,推广前景广阔。
