自动颗粒包装机用户需求书URS
自动装盒机URS

目录目录 (1)背景介绍: (2)范围: (2)依据的法规、标准: (2)内容: (2)1.综述 (2)2.用户需求 (2)3. 术语 (10)4. 附件 (12)分发部门及数量:背景介绍:根据xxx公司固体制剂车间的建设需要,拟采购一台全自动装盒机,该设备的设计制造应满足中国2010版GMP和欧美GMP及相关标准的要求。
目的:本用户需求文件旨在阐述用户对设备的质量要求和用户对该设备工作程序和功能目的要求,主要包括相关法规的符合度和用户的具体需求,是该设备设计和验证的依据,也是设备购置的基础,该设备供应商应在规定的时间内完成并达到本用户需求的设计目标和可接受的质量标准。
范围:本文件的范围涉及到了对此设备的最低要求,供应商应将URS作为详细设计以及报价的基础。
供应商在设计、制造、组装时必须要按照URS来执行。
依据的法规、标准:1. 规范1.1 中国GMP(2010年版)1.2 中国药典(2010年版)1.3 美国GMP1.4欧盟GMP2标准2.1 JB/T20093-2007制药机械行业标准;2.2 TJ36-79工业企业设计卫生标准;2.3 GB-52261-2002 机械安全机械电气设备第一部分:通用技术条件2.5 GB-8196-87 机械设计防护罩安全要求2.6 GB-12265-90 机械防护安全要求2.7 GB 9706.1-1995《医用电气设备第一部分安全通用要求》2.8 GB/T 5226.1-96《机械产品电气安全要求通用要求》2.9 GB/T 19910-93《医用电气设备环境要求及其试验方法》2.10 GAMP5国际制药工程协会生产自动化规范内容:1.综述设备的设计安装及配件均应符合中国2010版GMP、欧盟和美国GMP标准,能够满足车间工艺连续生产,达到生产要求。
2.用户需求2.1 URS01:设备要求2.3 URS03:电气及控制系统要求2.11 URS11:就位吊装、就位、介质连接要求4. 附件4.1 URS确认表(如果符合,请注明是否为标准功能;如果不符合,请详细阐述不符合的部分)4.2 元器件制造商清单。
多列粉末包装机URS(11.05)

多列粉末包装机用户需求说明书1.目的 (2)2.范畴 (2)3.法规和指南规范 (2)4.定义和术语 (2)5.设备介绍 (3)6.用户需求 (3)6.1设备基本参数及工艺需求3 6.2设备需求3 6.3控制标准7 6.4文件系统7 6.5培训7 6.6验收和安装7 6.7售后服务8 6.8响应9 6.9时限9 6.10报价9分发部门:采购部、财务部、质量保证部、设备动力部、工程部、生产部审核:执行日期:1.目的本文件的执行将记录和证明向供应商提出的关于多列粉末包装机的要求的具体内容,供应商应以我公司确认的控制标准为依据进行多列粉末包装机的初步规格选型、功能设计并最终完成详细设计,并经我公司确认后作为将来的设备验证、验收依据。
2.范畴本文件用于确认多列粉末包装机的规格和性能要求。
3.法规和指南规范设备及其所有机械和部件必须符合中国现行制药GMP和安全标准要求。
设备应当符合以下指南/标准:3.1中国药品生产质量管理规范(GMP),2010年版;3.2中华人民共和国药典(2015版);3.3良好自动化生产实践指南,第5版;3.4 GBZ1-2010工业企业设计卫生标准;3.5 GB20021-2004中华人民共和国制药机械行业标准;3.6 GB5226.1-2008机械安全机械电气设备第一部分:通用技术条件;3.7 GB/T8196-2003机械设计防护罩安全要求;3.8 GB28670-2012制药机械实施GMP的通则;3.9国家其它相关行业法律法规。
4.定义和术语4.1与产品接触部件:所有与产品、中间体、内包装材料或原料接触,或与液态物料接触的气体所接触的表面均视为“与产品接触表面”。
4.2 GMP Good Manufacturing Practices 药品生产质量管理规范4.3 PW Purified Water 纯化水4.4 PS Pure Steam 纯蒸汽4.5 CIP Clean-in-Place 在位清洗4.6 SIP Sterilization in Place 在位灭菌4.7 IQ Installation Qualification 安装确认4.8 OQ Operational Qualification 运行确认4.9PQ Performance Qualification 性能确认4.10FAT Factory Acceptance Test 出厂验收测试4.11SAT Site Acceptance Test 现场验收测试4.12SOP Standard Operating Procedure 标准操作规程4.13TOC Total Organic Carbon 总有机碳4.14PCS Process Control System 工艺控制系统4.15URS User Requirement Specification用户需求规范4.16PLC Programmable Logic Controller 可编程逻辑控制器4.17HMI Human Machine Interface 人机界面4.18DQ Design Qualification 设计确认5.设备介绍粉末包装机主要直服饮片粉末的包装。
散剂装盒机URS - 2021
用户需求文件项目名称:生产部手动包装线购买可利美特散剂装盒机目录1.目的.............................................................................................................................2.范围 .............................................................................................................................3.概述背景 ..................................................................................................................... 4内容 .............................................................................................................................4.1 法规与标准……………………………………………………………………….4.2.外观及材质 ..............................................................................................................4.3.功能及能力 ..............................................................................................................4.4安装环境……………………………………………………………………………4.5 EHS要求……………………………………………………………………………4.6 计量…………………………………………………………………………………4.7 培训…………………………………………………………………………………4.8 售后服务与维护………………………………………………………………….4.9 其它………………………………………………………………………………..5.供应商反馈 .................................................................................................................6.变更历史 .....................................................................................................................1.目的为规范用户需求文件(URS)文件编写,并正确指导可利美特散剂自动包装设备的设计选型,同时为验证·合同提供标准,特制定本规程2 范围本文件是可利美特散剂自动装盒机而制订的URS,该自动装盒机用于装盒放置说明书贴标(封盒)。
颗粒分装机URS

颗粒分装机用户需求(URS)设备名称:颗粒分装机××××××制药有限公司2015年3月2日审核批准注:本文件描述为颗粒分装机的工艺技术要求,请文件审核和批准人员仔细阅读每一页后,将意见和建议单独附页在本文件后,在本页签名即代表已审阅并批准本文件的每一页。
目录1、总则1.1 设计依据、制作和验收标准...........................................................错误!未定义书签。
1.2规格参数........................................................................................错误!未定义书签。
1.3名称和体积....................................................................................错误!未定义书签。
1.4其他要求........................................................................................错误!未定义书签。
1.5EHS要求2.服务要求2.1包装运输要求2.2安装3.验证和文件3.1验证错误!未定义书签。
3.2文件资料要求错误!未定义书签。
4.服务和培训 (7)正文1.总则2服务要求3.资料和文件6.有关术语1)GMP:中华人民共和国药品生产质量管理规范2)URS:用户需求标准3)FAT:工厂验收测试4)SAT:现场验收测试5)DQ:设计确认6)IQ:安装确认7)OQ:运行确认8)PQ:性能确认9)FS:功能说明10)DS:设计说明。
自动装盒机的URS

自动装盒机的URS
URS是指用户需求规格(UserRequirementSpecification),是在设备采购过程中的一份文件,详细描述了用户对设备的功能、性能和质量等方面的要求。
对于自动装盒机的URS,以下是一些包含在其中的要求:
1.适用范围:说明自动装盒机的应用领域和产品类型。
2.产能要求:包括最大包装速度、每分钟处理的产品数量等。
3.自动化程度:描述机器的自动化程度,如是否需要自动供料、自动调整等功能。
4.尺寸和重量限制:指定装盒机的最大尺寸和重量限制,以确保设备可以适应工厂的空间和设施。
5.包装规格:描述装盒机可处理的不同包装规格,如盒型、尺寸和重量范围等。
6.稳定性和可靠性:要求装盒机在长时间运行中具有稳定性和可靠性,并能保持一致的包装质量。
7.操作界面和人机交互:说明操作界面的要求,如操作面板、触摸屏等,以及人机交互的需求,如用户友好性、报警系统等。
8.清洁和卫生要求:指定装盒机易于清洁和维护的要求,以确保生产过程的卫生和品质。
9.安全要求:包括装盒机的安全防护措施、急停按钮、安全传感器等。
10.标准和法规要求:根据所在地区的法律法规,列出装盒机需要符合的标准和规定。
实际的自动装盒机的URS会根据具体需求和应用而有所不同。
在制定URS时,最好与装盒机的供应商或制造商进行充分的沟通和讨论,以确保所有要求都得到满足。
400湿法制粒机用户需求URS文件

目录
1背景
2目的
3范围
4法规和标准
5系统要求
5.1设备工艺或技术要求5.2安全要求
5.3安装位置及环境要求5.4设施/公用系统要求5.5外观及材质要求
5.6控制系统要求
5.7清洁要求
5.8润滑剂要求
5.9文件要求
5.10设备运转要求
5.11验证/确认要求
5.12培训要求
5.13质量保证和售后服务6确认
内容
1背景
根据公司异地扩建总体规划及总体设计要求,综合固体制剂车间湿法混合制粒机的需要,需制定新建固体制剂车间所需LHS400湿法混合制粒机URS文件。
2目的
本文件描述了我公司口服固体制剂车间LHS400湿法混合制粒机用户需求的具体内容,供应商应以本文件的要求为依据,进行LHS400湿法混合制粒机的选型、设计和制造,为将来的设备验证提供充分依据。
3范围
适用于新建口服固体制剂车间所需的LHS400湿法混合制粒机。
4法规和标准
药品GMP规范(2010版)
5系统要求
5.7 清洁要求
5.8 润滑剂
6确认
供应商确认签名:日期:客户确认签名:日期:。
15-装盒机URS 符合GMP要求用户需求说明参考模板

装盒机用户需求1、工艺描述装盒机用于片剂或胶囊等的铝塑或铝铝板的装盒。
经过泡罩包装机包装后的铝塑或铝铝板通过输送带输送到装盒机上,按要求进行装盒、装说明书、压印批号,生产日期,有效期,热熔胶封合得到符合要求的小盒,得到的成品通过输送装置进入到称重装置,进行称重检测,不合格品自动剔除。
该系统的配套设备包括模具,洁净压缩空气,说明书折叠装置,批号、有效期、生产日期打印装置,HMI(人机界面)的控制系统。
装盒机的设计和构建要考虑到将来可以轻松实现升级,要求可以通过更换模具的方式进行不同品种的装盒,供应商应建议更换模具的最大和最小规格。
2、要求以下表格详述了特定生产系统的用户需求,其分为以下三类。
每一个用户需求根据表格中的说明加以证实或测试。
所有要求应满足SMART原则(明确性、可衡量性、可达成性、可行性、可追踪性)。
2.1质量性质质量性质(QP)是可衡量的会产生法规或符合性相关影响的性质,可能会是下面的其中一个:2.1.1Critical Aspects 关键部分生产系统的关键部分指生产工艺及系统中的典型职能、特点、能力、性能,以确保生产质量及患者安全。
应基于科学的对产品及工艺的理解进行明确和记录。
系统的每一个关键部分都对关键工艺参数有直接影响或控制,并将形成确认活动的基础。
2.1.2Critical Quality Attributes 关键质量特性关键质量特性是产品的可量性质,被认为与工艺验证并列,对建立预期纯度、效力及安全性产生重要作用。
一个质量特性是法规或合规性相关的性质,其是可被衡量/检测的,且将形成工艺确认检验的基础。
质量关键特性应被定性、证实、记录为所有产品的验证。
2.1.3Critical Process Parameters 关键工艺参数关键工艺参数是工艺变量,应保持在特定范围内,以确保产品在关键质量特性的限度内。
这些参数是法规或合规性相关的性质,其是可被衡量/检测的。
关键工艺参数应被定性、证实、记录为所有产品的验证。
urs内容及怎样写

GHL-250型高速混合制粒机用户需求说明(URS)(编制单位:)(编制时间:)(URS编号:)目录1、综述2、标准及法规3、供货范围4、术语说明5、技术要求5.1生产工艺要求5.2厂房设施及公用系统要求5.3设备主机部分5.4电气控制及安全防爆5.5清洗消毒要求5. 6 EHS要求6、服务要求6.1 FAT要求6.2包装运输要求6.3文件资料要求6.4 备品零件要求6.5安装调试要求6.6 SAT要求6.7培训要求6.8 保修要求6.9 其它要求7、修订历史1、综述目的:提供GHL-250型高速混合制粒机的设计、制造、采购、验收和确认的依据。
范围:本URS适用于GHL-250型高速混合制粒机招标采购和加工制作。
责任:参加投标方即编制方负责编制此URS,招标方对本URS的编制文件审核,确认URS的内容完全满足招标方的需求,作为进行技术及商务招标的依据。
一旦编制方(即供方)中标,必须严格按照本URS所明确的法规标准、技术要求、服务要求,提供相关设备设施和服务,招标方及中标方均有责任对此URS 保密。
工艺描述:物料在添加辅料之后,在设备的容器内,经高速搅拌混合均匀,并在容器内形成一定的高速流动层,切碎刀在此流动层内高速剪切,形成颗粒状,在出料推杆作用下,颗粒被卸出。
整个过程在设备容器内完成,可以有效防止产尘。
密封装置采用净化的气密封。
环境标准:D级净化环境,GMP标准厂房,温度18-26度,湿度45%-65%公用介质情况:压缩空气(气动和净化)、电源、清洁用纯化水2、标准及法规除满足本URS特殊要求外,必须符合中国的相关法规:《药品生产质量管理规范(2010 年修订)》中华人民共和国制药机械行业标准JB20014-20018-2004《中华人民共和国环境保护法》《GB 50231-98 机械设备安装工程施工及验收通用规范》《GB 12348-90工业企业厂界噪声标准》3、供货范围GHL-250型高速混合制粒机1台套(其组成是GHL-250型高速混合制粒机主机,以及随机文件和操作维护工具)4、术语说明词语定义URS User requirement specification 客户需求说明IQ Installation Qualification 安装验证OQ Operational Qualification 操作验证EHS Environment Health Safety 环境健康安全FAT Factory Acceptance Test 工厂接收测试SAT Site Acceptance Test 现场接收测试5、技术要求5.1生产工艺需求编号需求必须/期望URS001 适应制备颗粒,产量:50~100KG/批,用于片剂、胶囊剂的湿混合制粒必须URS002 含量均匀度(标准:RSD%≤2%)必须URS003 筒体容积250L 必须URS004 切割速度双速电机切割功率4.5/5.5KW 必须URS005 混合速度9/11KW 必须5.2 公用系统需求编号需求必须/期望URS006 电源:50HZ-380V 三相五线制,配备功率不大于50KW 必须URS007 设备外形长2050宽1100高1450 必须URS008 设备重量:小于1000KG 必须URS009 压缩空气过滤处理,压力0.7MPA,耗用量1.2M3/H 必须5.3设备主机部分需求编号需求必须/期望URS010 外封板SUS304不锈钢必须URS011 切割刀SUS304不锈钢必须URS012 气缸动作提升容器盖,容器盖有加料口,能有效关闭必须URS013 气缸动作出料必须URS014 搅拌桨SUS304不锈钢必须URS015 旋转部位气密封,可进气或纯化水5.4电气控制需求编号需求必须/期望URS016 5.7英寸触摸屏,PLC流程控制,可控制电机转速、压缩空气、纯化水、出料机构等必须URS017 设备必须有接地装置,接地电阻小于或等于4欧姆必须URS018 电器均为国内知名品牌必须5.5 清洗消毒需求编号需求必须/期望URS019 可自动加纯化水,搅拌清洗,排除清洗水必须URS020 必须方便使用消毒剂擦洗消毒必须5.6 EHS要求:需求编号需求必须/期望URS021 设备绝缘电阻应不小于1MΩ必须URS022 工作噪声:≤70分贝,无异常声响必须URS023 设备边缘应该平整,没有潜在尖角伤及操作员工必须URS024 设备使用、操作和维修等方面的结构设计合理,便于维护操作,设计制造满足相关设备安全设计规范必须URS025 电力故障时设备处于停止状态,电源重新启动必须人工操作后方可启动必须6服务要求6.1 FAT要求需求编号需求必须/期望URS026 设备制做完毕,供方检查测试无问题后将检测结果通知需方必须URS027 在供方现场试机所需模拟物料费用由供方负担必须URS028 现场试机过程中如出现异常,供方应进行原因调查,制定整改方案并对新方案进行风险评估必须URS029 测试时设备应能正常运行,生产能力和粒度符合要求,保证产品质量必须6.2包装运输要求需求编号需求必须/期望URS030 包装满足运输和装卸要求,防潮湿、防磕碰、防振动,由于包装不良而造成的任何锈损,供方承担全部损失和费用必须URS031 运输时间包含在供货周期内,供方负责运输,并承担运输费用必须URS032 机器到货清单必须详列每装箱内容物必须6.3文件资料需求编号需求必须/期望URS033 须提供文件清单,所有文件资料均须提供中文版各一份必须URS034 须提供机器零组件分解组立图及零件编号,名称说明表必须URS035 提供机器操作保养手册或说明书、故障排除说明书、检修规程、润滑图必须URS036 须提供电路控制线路图(电路之配线以符号标明于接在线以便核查) 必须6.4备品零件需求编号需求必须/期望URS037 提供备品配件清单必须URS038 机器试车后于保修期限内其消耗品或电子零件故障需由供应商负责免费供应修缮或更换。
27.颗粒包装全自动装盒机URS

编号:URS-GT-027页码:Page 1 of 15颗粒包装全自动装盒机用户需求标准编号:URS-GT-027页码:Page 2 of 15批准执行签名下面的签名表示对本URS内容已经审核完毕,且表明已经为执行作好了准备。
在批准后,任何针对本文件的内容进行改变或修正的活动,都必须起到完善本URS的作用,所有的改变或修正均应执行变更处理,并经过批准后作为本URS的附件,与本URS一并执行。
设备名称全自动装盒机数量1台审核批准表标准经下列部门审核和批准后生效部门/人员签字日期起草人工程设备部年月日审核人工程设备部部长年月日生产技术部部长年月日质量管理部部长年月日分管副总年月日批准人质量受权人年月日编号:URS-GT-027页码:Page 3 of 15目录1.目的2.范围3.责任4.项目描述5.整体技术要求5.1.技术要求5.2.数据要求5.3.功能要求6.材质与加工要求7.EHS要求8.维护9.仪表10.项目实施用户需求10.1.进度表10.2.法律和法规要求11.供货、服务要求11.1.计划11.2.URS响应和DQ11.3.FAT工厂测试11.4.SAT现场测试11.5.IQ/OQ安装/运行确认12.文件13.交货13.1.货物的运输13.2.安装13.3.培训编号:URS-GT-027页码:Page 4 of 1514.变更管理需求15.变更历史及原因16.附件17.分发部门编号:URS-GT-027页码:Page 5 of 151.目的本URS需求标准旨在从项目和设备的角度阐述用户的需求,包括了用户对该项目的质量要求(符合新版GMP),描述了用户对全自动装盒机的工作过程及功能的期望。
主要包括相关法规符合度和用户的具体需求,这份文件是构建起该项目和设备文件体系的基础,同时也是在全自动装盒机的设计、制造、采购、验收和确认等过程中为用户和设备生产商提供双方可接受的依据标准。
设备生产商应在规定的时间内完成并达到本用户需求的设计目标和可接受的质量标准。
干法造粒机URS

江苏苏中药业集团股份有限公司干法造粒机技术说明(URS文件)干法造粒机用户需求1范围本标准规定了公司购置的干法造粒机应达到的设计、性能、文件等基本要求。
2规范性引用文件下列文件对于本文件的应用时必不可少的。
凡是注日期的引用文件,仅注日期的版本适用于本文件。
凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。
Q/SZ T.00.00.001 标准的结构与编制Q/SZ T.00.00.002 标准的编码规则Q/SZ T.00.00.003 苏中标准体系和苏中标准体系表Q/SZ T.00.00.004 标准汇总表Q/SZ T.07.00.001 设备用户需求编制要求《药品生产质量管理规范》(2010年修订版)《药品生产验证指南》(2003版)现行中国药典GB50093-2002 自动化仪表工程施工及验收规GB 50591-2010 洁净室施工及验收规范GB50257-1996 防爆电气GB 50093-2002 自动化仪表工程施工及验收规范GB5226 -2008 机械电气安全机械电气设备GB 50236-1998 现场设备、工业管道焊接工程施工及验收规范GB/T 13306-2011 标牌GB/T 191-2008 包装储运图示标志3 定义3.1 用户需求user requirement specification (URS):使用方对设备、厂房、硬件设施等提出的自己的期望与使用需求说明的文件。
3.2 工厂验收测试factory acceptance test (FAT)在设备交货前在设备生产厂进行了设备测试,包括指定的系统功能测试、稳定性测试、可用性测试,以确认设备符合设计要求并能正常运行。
3.3 现场验收测试site acceptance test (SAT)在设备运抵现场并安装完成后进行的设备测试,包括指定的系统功能测试、稳定性测试、可用性测试,以确认设备符合设计要求并能正常运行。
(联盛)多列粉末包装机URS

多列粉末包装机用户需求说明书1. 目的 (2)2. 范畴 (3)3. 法规和指南规范 (3)4. 定义和术语 (3)5. 设备介绍 (4)6. 用户需求 (5)6.1 设备基本参数及工艺需求56.2 设备需求56.3 控制标准116.4 文件系统116.5 培训126.6 验收和安装136.7 售后服务156.8 响应156.9 时限16页脚内容16.10 报价 (16)分发部门:采购部、财务部、质量保证部、设备动力部、工程部、生产部审核:执行日期:1.目的本文件的执行将记录和证明向供应商提出的关于多列粉末包装机的要求的具体内容,供应商应以我公司确认的控制标准为依据进行多列粉末包装机的初步规格选型、功能设计并最终完成详细设计,并经我公司确认后作为将来的设备验证、验收依据。
页脚内容22.范畴本文件用于确认多列粉末包装机的规格和性能要求。
3.法规和指南规范设备及其所有机械和部件必须符合中国现行制药GMP和安全标准要求。
设备应当符合以下指南/标准:3.1中国药品生产质量管理规范(GMP),2010年版;3.2中华人民共和国药典(2015版);3.3良好自动化生产实践指南,第5版;3.4GBZ1-2010工业企业设计卫生标准;3.5GB20021-2004中华人民共和国制药机械行业标准;3.6GB5226.1-2008机械安全机械电气设备第一部分:通用技术条件;3.7GB/T8196-2003机械设计防护罩安全要求;3.8GB28670-2012制药机械实施GMP的通则;3.9国家其它相关行业法律法规。
4.定义和术语4.1与产品接触部件:所有与产品、中间体、内包装材料或原料接触,或与液态物料接触的气体所接触的表面均视为“与产品接触表面”。
4.2GMP Good Manufacturing Practices 药品生产质量管理规范页脚内容34.3PW Purified Water 纯化水4.4PS Pure Steam 纯蒸汽4.5CIP Clean-in-Place 在位清洗4.6SIP Sterilization in Place 在位灭菌4.7IQ Installation Qualification 安装确认4.8OQ Operational Qualification 运行确认4.9PQ Performance Qualification 性能确认4.10FAT Factory Acceptance Test 出厂验收测试4.11SAT Site Acceptance Test 现场验收测试4.12SOP Standard Operating Procedure 标准操作规程4.13TOC Total Organic Carbon 总有机碳4.14PCS Process Control System 工艺控制系统4.15URS User Requirement Specification用户需求规范4.16PLC Programmable Logic Controller 可编程逻辑控制器4.17HMI Human Machine Interface 人机界面4.18DQ Design Qualification 设计确认5.设备介绍页脚内容4粉末包装机主要直服饮片粉末的包装。
多列粉末包装机URS

起草人审核人审核人审核人审核人批准人部门多列粉末包装机用户需求说明书1. 目的 .....................................................................................................................................................................2. 2. 畴...........................................................................................................................................................................................2..3. 法规和指南规 ..................................................................................................................................................... 2.4. 定义和术语 ......................................................................................................................................................... 3.5. 设备介绍 .............................................................................................................................................................................4..6.用户需求 .............................................................................................................................................................................4..6.1 设备根本参数及工艺需求 6.2 设备需求 6.3 掌握标准 6.4 文件系统 6.5 培训 6.6 验收和安装 6.7 售11 6.8 响11 4 4 8 8 9 9后服务应6.9 时限116.10报 价11分发部门:选购部、财务部、质量保证部、设备动力部、工程部、生产部审核:姓名签名日期执行日期:1.目的本文件的执行将记录和证明向供给商提出的关于多列粉末包装机的要求的具体容,供给商应以我公司确认的掌握标准为依据进展多列粉末包装机的初步规格选型、功能设计并最终完成具体设计,并经我公司确认后作为将来的设备验证、验收依据。
三维包装机URS-Word-文档

三维包装机URS一、目的:明确设备具体使用需求,提供采购设备的技术依据,以确保设备配置适当、达到GMP 规范和使用要求。
二、需求项目1、名称:三维包装机2、数量及规格:数量1台。
A产品包装规格1×5排列(小盒尺寸71×40.5×40.5mm)B 产品包装规格2×5排列(小盒尺寸52.5×36×36mm)以及正常生产、操作所需的所有辅助设施。
同时应具备不同规格包装盒的拓展要求。
3、环境描述:生产环境为一般区。
4、用途:用于北大医药股份有限公司302车间胶囊包装瓶装联动生产线。
5、设备公用介质需求:提供设备详细参数、详细安装图、各公用介质需求标准、各公用介质与设备连接的具体位置和规格。
三、工艺描述上游装盒设备包装好的纸盒通过输送带出来后进入本次招标采购的三维包装机对连接口包装物品进行自动送料→堆叠→包装→热封→整理→计数。
四、设备符合的技术标准及规范要求三维包装机的设计、材料选择、制造现场、制造工艺、文件记录、检验测试、设备调试、验证应满足以下标准和规范要求:1、本文件所列需求标准;2、2010版GMP规范,设备设计制造应满足2010版GMP规范要求,投标人应承诺供货范围内的设备不得存在导致无法满足最新版本GMP规范要求的瑕疵,即使设备在验收过程中未曾识别出瑕疵,但在之后的使用过程中发现投标人供货范围内的设备存在无法满足最新版本GMP规范要求的瑕疵,并且该瑕疵确属设备本身的问题,投标人也应承诺对供货范围内的设备进行免费整改并使其符合最新版本GMP规范的要求或者退货;3、《工业自动化仪表工程施工及验收规范》;4、自控系统要符合GAMP5要求;5、国家现行机械制造规范及行业标准、安全标准;6、其他与制药设备制造、安装相关法律法规。
五、设备需求1、生产能力要求5、其它六、文件要求供应商应免费提供下列文件,包括纸质版本和电子版本,电子版本是可以更改:七.验收要求八、厂房设施及公用系统要求九、服务要求要求供应商提供以下服务(不仅限于)1、测试及验证服务:3、备品备件要求:4、包装运输要求:5、培训服务:6、售后服务需求。
全自动包装线用户URS需求说明文件

葵花药业集团
(唐山)生物制药有限公司自动装盒机用户
需
求
标
准
二O一三年四月
1、综述
背景:根据公司发展战略要求,在新园区新建年产颗粒剂8.2亿袋、片剂11亿片、胶囊剂8亿粒的口服综合制剂车间,因此,需新购铝塑包装机1台,枕式包装机
2台,全自动装盒机2台(药板型装盒机),电子扫描机2台,激光打码机2台,
印字打包一体机2台。
目的:为用户和供应商提供铝塑包装机,枕式包装机,装盒机,电子扫描机,激光打码机,印字打包一体机的设计、制造、采购、验收和确认依据。
范围:本URS适用于铝塑包装机,枕式包装机,装盒机,包括装盒机。
责任:需方对本URS的编制质量负责。
供方须严格按照本URS所明确的法规标准、技术要求、服务要求,提供相关设备设施和服务,供方须对需方所提供的URS负
保密责任。
工艺描述:药片通过铝塑机进行包装,形成平整的铝塑板,铝塑好的药板经枕式包装后传送带或者手工进入装盒机料仓,通过自动下料装置传送轨道上,纸盒由纸盒贮存仓被吸嘴打开后送到装盒工位,说明书由说明书贮存仓经折叠后送到装盒工位,由推舌将药板及说明书送入张开的纸盒中,再经过折盒封好后,进入装盒机出口传送带,经传送带进入下一工序进行操作。
2、法规标准
法规:
除本URS特殊要求外,须满足中国的2010版《药品生产质量管理规范》法规要求,中国安全环保法规。
标准:
除本URS特殊要求外,须满足ISPE(国际制药工程师协会)所颁布的制药工程设备标准、中国制药装备协会所颁布的制药工程设备标准、ISO14001、OSAHS18001、压力容器和特种设备中国国家制造标准。
3、技术要求
3.1生产工艺要求
3.4RAM要求。
外包装连线用户需求(URS)

全自动包装线用户需求说明XX药业有限公司2018年9月1. 项目介绍 (3)2. 目的 (3)3. 范围 (3)4. 法规、指南和标准 (3)4.1法规 (3)4.2行业标准 (4)4.3国家标准 (4)5. 缩略语 (4)6. 描述 (5)6.1工艺/流程描述 (5)6.2产品介绍 (6)6.3 设备运行环境 (6)7. 用户需求 (6)7.1设备整体要求 (6)7.2铝塑泡罩包装机 (8)7.3自动检片装置 (10)7.4枕式包装机 (12)7.5装盒机 (14)7.6控制系统要求 (15)7.7材质要求 (16)7.8安全及环保要求 (16)8. 服务要求 (17)8.1文件资料要求 (17)8.2服务与维修要求 (19)8.3时间要求 (19)8.4其它要求 (20)1. 项目介绍XX药业有限公司软胶囊剂采用全自动包装线进行包装,包含泡罩机、枕包机和装盒机,货物需求表如下:2. 目的本用户需求文件旨在从项目和系统的角度阐述用户的需求,总括了用户对该项目的质量要求(GMP),描述了用户对该设备的工作过程及功能的期望。
主要包括相关法规符合度和用户的具体需求,这份文件是构建起项目和系统的文件体系的基础,同时也是系统设计和验证的可接受标准的依据。
设备生产商应在规定的时间内完成并达到本用户需求的设计目标和可接受的质量标准。
在本URS中用户仅提出基本的技术要求和设备的基本要求,并未涵盖和限制卖方设备具有更高的设计与制造标准和更加完善的功能、更完善的配置和性能、更优异的部件和更高水平的控制系统。
设备厂方应在满足本URS的前提下提供卖方能够达到的更高标准和功能的高质量设备及其相关服务。
卖方的设备应满足中国有关设计、制造、安全、环保等规程、规范和强制性标准要求。
如遇与卖方所执行的标准发生矛盾时,应按较高标准执行(强制性标准除外)。
3. 范围一、此文件所定义的URS适用于本公司所需的软胶囊剂产品包装生产所需主机及辅机。
600型一步制粒机用户需求(URS)
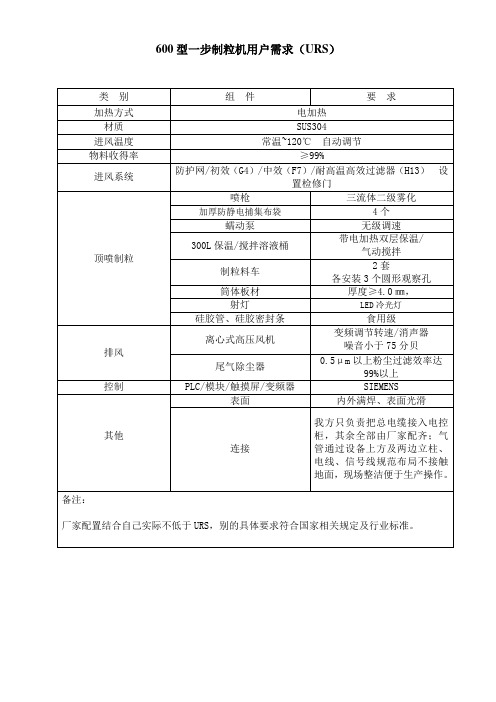
类别
组件
要求
加热方式
电加热
材质
SUS304
进风温度
常温~120℃自动调节
物料收得率
≥99%
进风系统
防护网/初效(G4)/中效(F7)/耐高温高效过滤器(H13)设置检修门
顶喷制粒
喷枪
三流体二级雾化
加厚防静电捕集布袋
4个
蠕动泵
无级调速
300L保温/搅拌溶液桶
带电加热双层保温/
气动搅拌
制粒料车
2套
各安装3个圆形观察孔
筒体板材
厚度≥4.0㎜,
射灯
LED冷光灯
硅胶管、硅胶密封条
食用级
排风
离心式高压风机
变频调节转速/消声器
噪音小于75分贝
尾气除尘器
0.5μm以上粉尘过滤效率达99%以上
控制
PLC/模块/触摸屏/变频器
SIEMENS
其他表面内外满焊、表 Nhomakorabea光滑连接
我方只负责把总电缆接入电控柜,其余全部由厂家配齐;气管通过设备上方及两边立柱、电线、信号线规范布局不接触地面,现场整洁便于生产操作。
备注:
厂家配置结合自己实际不低于URS,别的具体要求符合国家相关规定及行业标准。
摇摆式制粒机URS

URS文件(用户需求)URS编号:URS-XXX-XXXX设备名称:摇摆式颗粒机XXXXXXXXXXXXX生物技术有限公司摇摆式颗粒机用户需求标准URS编号:URS-XXX-XXXX起草人:部门:日期:起草人:部门:日期:审核人:部门:日期:审核人:部门:日期:审核人:部门:日期:批准人:部门:日期:本文件起草后要经过审核人审核,审核人负责文件的审阅,审核人审核文件时应详细阅读文件内容,确认审阅内容的正确性,文件一经签字,审核人即对文件内容负责。
文件经审核人审核签字后,经由批准人签字批准后即可生效。
目录1. 概述: (3)2. 法规标准及指南: (3)3. 采购数量: (3)4. URS需求确认: (4)4.1生产工艺要求 (4)4.2设备要求 (4)4.3厂房设施及公用系统要求 (5)4.4电器自控要求 (5)4.5 QA要求 (5)4.6清洗消毒要求 (5)4.7包装运输要求 (5)4.8文件资料要求 (5)4.9备品零件要求 (6)4.10安装调试要求 (6)4.11现场验收测试要求 (6)4.12培训要求 (7)4.13保修要求 (7)4.14其他要求 (7)5.讨论/审核/评语: (7)6.修订历史: (8)1.概述:1.1背景本设备是为满足本公司内部标准、2010年版GMP、中国国家药品食品监督管理局的要求而进行设计。
主要用于XXXXXXXXXXXXX生物技术有限公司的制粒。
本设备安装于XXXXXXXXXXXXX生物技术有限公司综合制剂车间制粒岗位。
1.2目的本文件目的是用以说明摇摆式颗粒机用户需求,提出重要部件、关键参数和必需的选择,生产供应商应以此为依据进行设备的选型、功能设计并最终完成制造,为设备的验收和验证提供依据。
此文件应作为与选定的设备供应商签订的购买合同的一个主要组成部分。
供应商要遵守该文件里的信息和条件以及购买条款和条件。
1.3范围本URS适用于新购摇摆式颗粒机的规格和性能要求及相关设施、洁净保证系统及控制系统等。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
自动颗粒包装机用户需求书User Requirement Specification
文件变更控制
目录
1、背景介绍
2、目的和范围(URS文件的)
3、法规和国家标准(该设备必须符合的)
3.1、GMP法规
3.2、国家及行业标准
3.3、公司管理要求
4、项目介绍
4.1、项目描述
4.2、工艺/流程描述
4.3、涉及的产品(物料)介绍
5、用户及系统要求
包括:URS01产品特性、URS02设备性能要求、URS03安装要求、URS04公用系统要求、URS05控制系统要求、URS06安全要求、URS07文件要求、URS08服务与维修要求、URS09验证要求
6、附件:URS符合性确认表格
1 背景介绍
我公司计划在2015年进行GMP(2010年修订)认证。
因此,我公司计划购买自动颗粒包装机。
该设备计划于2015年06月完成设备安装调试及相关确认工作后投入使用。
2 目的和范围
本文件为四川ABC制药有限公司新购自动颗粒包装机项目的用户要求文件。
本URS适用于自动颗粒包装机。
需方对本URS的编制质量负责,供方严格按照本URS所明确的法规标准、技术要求、服务要求,提供相关设备设施和服务,供方须对需方所提供的URS 负保密责任。
3 法规和国家标准
该设备用于胶囊充填,必须符合GMP规范、国家及行业标准和本公司管理要求。
3.1 GMP法规
中国《药品生产质量管理规范》(2010年修订)(卫生部令第79号)
3.2 国家及行业标准
国家相关消防安全法律法规要求
3.3 公司管理要求
《设备管理程序》、《质量风险管理程序》
4 项目介绍
4.1 项目描述
依据产品质量管理要求,四川ABC制药有限公司需新购自动颗粒包装机,该设备用于颗粒内包装
4.2 流程/工艺描述
设置好后启动加热,待温度达到设定值时,上好药品包装用复合膜,启动整机开始包装4.3 涉及的产品/物料介绍
新购设备主要用于颗粒内包装。
其产品信息如下:
5、用户及系统要求
URS符合性确认表格
该表格由供应商填写,以确保URS中的各项需求得到供应商的书面回馈。
反馈表应加盖供应商的公章。
