医疗器械不良事件报告记录
医疗器械不良事件报告范例

2、事件发生后未出现上述情况,但根据临床医生的经 验同类事件再次发生时,有可能出现上述情况,例如:患 者使用聚丙烯酰胺水凝胶产品后,因故要求取出注射物而 不能完全取出,尽管没有造成患者伤害,但再次发生同类 事件(如发生感染时)有可能引起患者伤害。 • 3、由于事件涉及器械、使用、个人多个因素,不能排 除与聚丙烯酰胺水凝胶产品有关,例如: • ① 注射后不明原因肩、背等身体部位疼痛; • ② 注射后患者哺乳期出现炎症、感染。 •
2、事件发生后未出现上述情况,但根据临床医生的经 验同类事件再次发生时,有可能出现上述永久性伤害或损 伤情况,例如:患者配戴OK镜后出现镜片嵌顿,尽管对该 病人未造成损伤,但再次配戴OK镜或其他患者遇到同样情 况,有可能造成角膜损伤。 • 3、由于事件涉及器械、使用、个人多个因素,不能排 除与配戴OK镜有关,例如:短期、原因不明的近视加重。 •
1、患者因使用骨科植入物医疗器械导致相关器官功能 或者结构的永久性伤害、损伤,或必须采取医疗措施才能 避免上述永久性伤害或损伤,例如: • ① 颈椎间盘手术中椎间隙放置的Cage移位脱落,压 迫损伤脊髓造成截瘫; • ② 关节产品标签、产品使用说明书中存在错误或缺陷 ,将误导经验不足的临床医生错误使用; • ③一次性包装产品消毒物残留,引起肌体组织损伤。 •
2、事件发生后未出现上述情况,但根据临床医生的经 验同类事件再次发生时,有可能出现上述永久性伤害、损 伤情况,例如:滑动额头钉治疗转子间骨折,因为扩髓器 械标记失效,造成扩髓过深,尽管未对患者造成严重伤害 ,但再次发生时,有可能损伤盆腔脏器。 • 3、由于事件涉及器械、使用、个人多个因素,不能排 除与骨科植入物医疗器械有关,例如: • ① 全髋关节置换术后不明原因脱位、松动; • ② 不明原因钢板、螺钉折断。 • •
医疗机构医疗器械不良事件报告举例

器械开始按钮有时自行停止
自动康复机
脚踏与机器脱离
腿浴治疗器
控制面板失灵、无水干烧漏水、泡浴过程中机器冒火星
智能下肢反馈康复训练系统
屏幕触摸板过于灵敏,操作者对触摸板控制困难,患者等待时间过长
磁疗仪器
脉冲磁场治疗仪
骶部、右上腹烫伤
离子导入治疗仪
未达疗效、电源线插座有打火现象
脑功能治疗仪
机器老化,电路板损坏,工作站故障
不曝光
皮肤划伤
移动式C型X射线机
设备无法透视
X射线手术影像设备
医用X射线摄影装置
c型臂严重故障、无法正常开机、主机接收不到探测器检测信号
X射线计算机断层摄影设备(CT)
C型臂X光机
无法穿透腰椎的显像
X射线血管造影系统
手术过程中X射线不出束、图像数据不能恢复
X射线计算机断层摄影设备
血糖检测值不准、仪器提示操作错误
生化分析系统
全自动生化分析仪
缺油、器械故障,出具检验报告时间延长、漏液、样品进样过程中架子卡住,导致停机
细菌分析系统
哥伦比亚培养基
哥伦比亚培养基溶血
临床医学检验辅助设备
纯水机
零件损坏
其他
一次性营养琼脂培养基
平皿长菌,无法使用
6841医用化验和基础设备器具
医用离心机
医用低速离心机
穴位贴不黏,出现过敏现象
6827中医器械
治疗仪器
电子针疗仪
治疗过程中断电
中医器具
无菌刃刀
刀柄脱离,损伤术者手指
无菌针灸针
针体变弯、生锈、未密封
6828医用磁共振设备
医用磁共振成像设备(MRI)
磁共振成像系统
医疗器械不良事件分析报告范文

医疗器械不良事件分析报告范文一、不良事件概况。
1. 事件描述。
咱就说啊,前几天在使用[医疗器械名称]的时候,出了点岔子。
当时呢,患者正按照正常流程接受治疗或者检查啥的,这器械突然就不正常工作了。
就好比你正开着车,突然车自己乱换挡一样,吓死人了。
具体表现就是[详细描述不良事件的现象,例如器械发出异常声响、显示错误数据、某个部件突然停止工作等]。
2. 涉及器械信息。
这个惹事的器械啊,是[生产厂家名称]生产的,型号是[具体型号],生产日期是[日期]。
它主要是用来[简述器械的功能]的,平时用着也还算顺手,谁知道这次突然就掉链子了呢。
二、不良事件调查。
1. 使用环境调查。
咱先看了看使用环境,发现当时的环境条件好像没有啥特别离谱的地方。
温度、湿度都在正常范围内,也没有啥强烈的电磁干扰之类的。
就好比你在一个普普通通的房间里,既没有火山爆发也没有外星人入侵,那这器械为啥就不正常了呢?这就很让人纳闷了。
2. 使用者操作调查。
接着又调查了一下使用者的操作情况。
操作人员都是经过正规培训的,而且也不是新手,操作流程那是相当熟练的。
就像老司机开车一样,不可能犯低级错误的。
所以呢,从操作这方面来看,也不像是导致不良事件的原因。
3. 器械本身检查。
那没办法,只能把这器械好好检查一下了。
这一检查啊,还真发现了点问题。
原来啊,在器械的[具体部件名称]那里,有一个小零件出现了磨损。
这个小零件就像机器里的一颗小螺丝钉一样,别看它小,作用可大了。
一旦它出问题,就会像多米诺骨牌一样,引发一系列的问题,导致整个器械不正常工作。
三、不良事件原因分析。
1. 根本原因。
经过前面的调查啊,这不良事件的根本原因就是那个小零件的磨损。
那为啥这个小零件会磨损呢?原来啊,这个器械使用的频率比较高,而且在一些操作过程中,这个小零件承受的压力比设计的时候要大一些。
就好比一个人每天都干很多重活,时间长了肯定会累垮的呀。
所以呢,长时间的高频率使用和不合理的压力分布,就导致了这个小零件过早地磨损了。
医疗器械不良事件报告范例

医疗器械不良事件报告范例近年来,随着科技的不断进步和医疗器械的广泛应用,不良事件的发生越来越引起人们的关注。
为了保障患者的权益和医疗安全,各国纷纷建立起医疗器械不良事件报告制度。
本文将通过一个具体的案例来展示医疗器械不良事件报告的范例。
首先,需要明确医疗器械不良事件的定义,它指的是使用过程中产生意外、不良后果或可能对人体造成损害的事件。
在某医院内,使用一台新研发的电子监护仪出现了一起医疗器械不良事件。
下面是报告的过程和范例:1. 事件描述患者小李,在手术后被转入重症监护室进行持续监测。
监护仪是医院最新引进的型号。
在患者连续监测了两天后,突然出现屏幕重叠、数据丢失的现象。
医护人员提醒患者家属,及时更换了另一台监护仪,保证了患者的安全。
2. 风险评估经过医疗团队对该不良事件进行评估,发现该事件可能存在的风险有以下几个方面:(1)患者丢失重要的生命体征数据,医生无法及时有效了解患者的病情;(2)患者的治疗计划可能受到影响,无法进行精准的治疗;(3)设备的可靠性和稳定性有待进一步改进。
3. 不良事件原因分析对于该不良事件的原因,医疗团队进行了详细的分析:(1)监护仪可能存在硬件故障,导致数据传输中断及屏幕显示异常;(2)操作人员可能没有及时发现设备故障,没有采取相应的紧急措施。
4. 管理措施在此事件发生后,医院采取了一系列针对性的管理措施:(1)立即停止使用该型号的电子监护仪,避免类似事件的再次发生;(2)对相关监护仪进行全面检测,找出问题所在;(3)安排专业技术人员进行监护仪的维护和修复;(4)加强对医护人员操作培训,提高其对设备故障的敏感度和应对能力。
5. 不良事件报告和追踪医院制定了全面的不良事件报告和追踪机制,确保每个事件都得到及时记录和处理。
报告包括事件的详细描述、风险评估、原因分析、管理措施等内容。
通过集中汇总和分析,能够及时发现和消除潜在的风险,提高医疗设备的安全性和可靠性。
6. 提高机构和仪器质量管理医院在此次事件的基础上,反思和总结了机构和仪器质量管理的不足之处。
医疗机构医疗器械不良事件报告举例

医疗机构医疗器械不良事件报告举例在医疗机构中,医疗器械不良事件报告具有重要的意义。
不良事件报告旨在监测和管理医疗器械使用中的问题,确保患者的安全和医疗质量的提升。
本文将通过举例的方式,探讨几个医疗器械不良事件的报告案例,以及如何有效应对和解决这些问题。
案例一:手术电刀发生事故引发火灾时间:20XX年5月10日地点:某市某医院手术室事件描述:在一次手术过程中,医生使用手术电刀时,电刀突然发生短路,引发火灾。
患者和医护人员迅速撤离手术室,并及时通知院内消防人员进行灭火。
火势很快得到控制,但手术室内部分设备和物品被烧毁,造成一定财产损失。
报告及处理措施:医院立即启动不良事件报告程序,相关责任人员及时填写不良事件报告表,详细记录了事故发生的过程、损失情况和可能原因。
对于此次事件,医院采取以下措施:1. 暂停使用相关型号的手术电刀,送往生产商进行检测和维修。
2. 成立专门的事故调查组,对此次事件进行调查和分析,找出问题所在。
3. 对相关医护人员进行培训和教育,提高注意手术器械使用安全的意识。
案例二:骨科手术器械断裂引发术中意外时间:20XX年7月5日地点:某市某骨科专科医院手术室事件描述:在一次骨科手术中,使用的骨钉在术中突然发生断裂,导致患者骨骼未能稳定固定,术后出现并发症。
患者经过紧急处理后状况稳定,但术后恢复受到一定影响。
报告及处理措施:医院对这一事件高度重视,立即启动报告程序,全面记录事件的过程和后果,并采取以下应对措施:1. 暂停使用相关型号的骨钉,联系生产商进行调查并更换其他可靠的替代品。
2. 开展术中器械严密检查制度,确保术前术后的所有骨科手术器械可靠和安全。
3. 对术前骨科手术方案进行综合评估,确保手术方案合理,减少患者术中并发症风险。
案例三:输液泵设备故障导致用药错误时间:20XX年9月15日地点:某市某三甲医院病房事件描述:在某病房输液治疗中,输液泵设备故障导致输液速度异常,患者药物过量输注,引发严重不良反应。
医疗器械不良事件分析报告范文

医疗器械不良事件分析报告范文一、事件概述。
咱就说啊,最近发生了这么个事儿。
[具体医疗器械名称]在使用过程中出了些状况,给使用者带来了不好的影响。
这事儿可不能小瞧,就像一颗小石子在平静的湖面上激起了千层浪,让大家都有点慌神儿。
二、不良事件表现。
1. 症状一:奇怪的响声。
这个医疗器械啊,在正常运转的时候,突然就像个小怪兽一样发出“咔咔咔”的怪声。
就好像它在里面开小会,小声嘀咕着什么,可这声音真的很吓人啊,使用者还以为它要爆炸了呢。
这响声是毫无征兆地就冒出来了,就像你正安静地走路,突然脚下的地板开始唱歌一样诡异。
2. 症状二:数据显示异常。
它那个显示屏上的数据啊,就像是喝醉了酒的人写的字,歪歪扭扭,完全不靠谱。
本来应该显示正常的数值,结果一会儿高得离谱,一会儿又低得不像话。
这就好比你看天气预报,一会儿说今天是大晴天,一会儿又说要下冰雹,你说这能让人相信吗?使用者都懵圈了,不知道到底该信哪个数据。
三、调查过程。
1. 硬件检查。
咱就像侦探一样,开始对这个医疗器械进行大检查。
先看看硬件部分,把它拆开来(当然是专业人员操作啦),就像拆一个神秘的礼盒。
结果发现,里面有个小零件有点松动,就像一颗牙齿有点摇晃一样。
这个小零件虽然不起眼,但它松动之后,就可能影响到整个器械的稳定性,说不定那个奇怪的响声就是它在里面晃荡搞出来的。
2. 软件排查。
再看看软件方面,就像是检查一个人的大脑一样。
发现软件里面有个小漏洞,就像是大脑里突然有个小短路。
这个漏洞可能导致数据在传输和处理的时候出岔子,这也就解释了为什么数据显示会像个调皮的孩子一样不听话。
四、原因分析。
1. 设计缺陷。
从调查结果来看,这个医疗器械在设计的时候可能就有点小马虎。
就像盖房子的时候,有些结构设计得不太合理。
比如说,那个容易松动的小零件,它的固定方式可能不够牢固,在长时间使用或者受到一点小震动之后,就开始不安分了。
这就好比你盖房子用的砖头,要是没粘好,稍微有点风吹草动就会松动。
可疑医疗器械不良反应报告表范文

可疑医疗器械不良反应报告表范文英文回答:Adverse Event Reporting Form for Suspected Medical Device Adverse Reactions.Name: [Your Name]Date: [Date]Patient Information:Name: [Patient's Name]Age: [Patient's Age]Sex: [Patient's Gender]Medical History: [Brief summary of patient's medical history]Device Information:Device Name: [Name of the medical device]Manufacturer: [Name of the manufacturer]Model/Serial Number: [Model/Serial Number of the device]Date of Implantation/Use: [Date of deviceimplantation/use]Description of the Adverse Event:Please provide a detailed description of the adverse event experienced by the patient, including any signs or symptoms observed.Example: I recently used a blood pressure monitoring device on a patient. The patient experienced severe painand discomfort during the procedure. The device seemed tobe malfunctioning as it was displaying inconsistentreadings. The patient's blood pressure was also abnormally high, which was concerning.Actions Taken:Please describe any actions taken in response to the adverse event, such as discontinuation of device use, medical intervention, or device replacement.Example: As soon as I noticed the patient's discomfort and the device malfunction, I immediately stopped using the device. I informed the patient about the situation and provided them with alternative methods for monitoring their blood pressure. I also reported the incident to thehospital's medical device department for further investigation.Outcome:Please describe the outcome of the adverse event, including any medical interventions or treatments provided to the patient.Example: After discontinuing the use of the blood pressure monitoring device, the patient's pain and discomfort subsided. The patient was closely monitored for any further complications and was eventually switched to a different device for blood pressure monitoring. No further adverse events were reported.Preventive Measures:Please suggest any preventive measures that can be taken to avoid similar adverse events in the future.Example: To prevent similar adverse events in the future, it is important to conduct regular maintenance and calibration checks on medical devices. Additionally, healthcare professionals should receive proper training on device usage and troubleshooting. It is also crucial to establish a robust reporting system for adverse events to ensure prompt investigation and appropriate action.中文回答:可疑医疗器械不良反应报告表。
医疗器械不良事件报告表案例

医疗器械不良事件报告表案例医疗器械不良事件报告表是用来记录和报告医疗器械不良事件的重要工具。
它是医疗机构和相关部门进行问题溯源和风险评估的重要依据。
下面是一些医疗器械不良事件报告表的案例,以便更好地理解和应用该表格。
1. 报告表的基本信息部分包括医疗机构名称、报告人员信息、报告时间等。
2. 事件描述部分详细描述了医疗器械不良事件的经过。
包括事件发生的时间、地点、涉及的医疗器械型号和批号等。
3. 不良事件的分类部分将事件按照不同的类型进行分类,如设备故障、使用错误、设计缺陷等。
4. 事件的影响部分描述了事件对患者、医疗机构和医疗过程的影响。
例如,患者是否受伤、是否影响正常的医疗流程等。
5. 事件的原因分析部分对不良事件的原因进行分析。
可能的原因包括人为因素、设备质量问题、操作失误等。
6. 对事件的处理和措施部分描述了医疗机构对不良事件的处理措施。
包括停用或更换医疗器械、加强培训和操作指导等。
7. 风险评估部分对事件的风险进行评估,包括患者的风险和医疗机构的风险。
评估结果可能包括患者再次受伤的概率、医疗机构的声誉等。
8. 事件的报告和通知部分描述了医疗机构向相关部门报告和通知的情况。
包括向监管机构报告、向制造商报告等。
9. 预防措施部分提出了医疗机构为避免类似事件再次发生所采取的预防措施。
如加强医疗器械的维护保养、加强人员培训等。
10. 报告的审核和确认部分描述了报告的审核过程和结果。
包括报告的审核人员、审核时间和审核结果等。
医疗器械不良事件报告表是医疗机构和相关部门进行问题溯源和风险评估的重要工具。
通过详细记录和分析不良事件,可以找出问题的根源,采取相应的措施来预防类似事件的再次发生。
同时,报告表也为监管部门提供了及时而准确的信息,帮助他们对医疗器械的安全性和质量进行监督和管理。
医疗器械不良反应报告
医疗机构
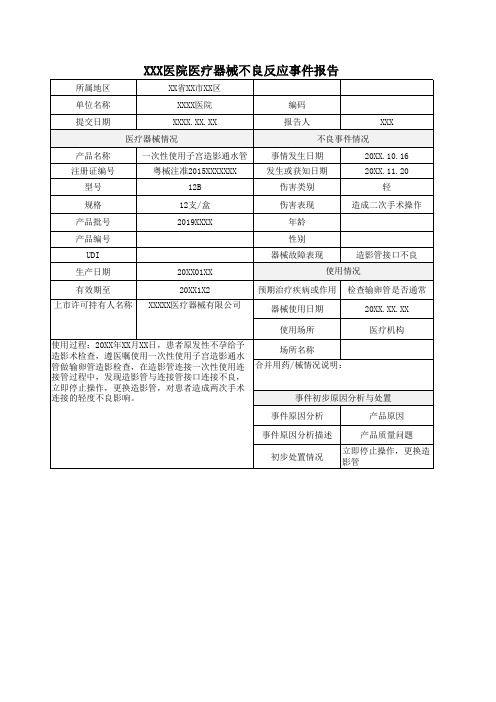
使用过程:20XX年XX月XX日,患者原发性不孕给予 造影术检查,遵医嘱使用一次性使用子宫造影通水 管做输卵管造影检查,在造影管连接一次性使用连 接管过程中,发现造影管与连接管接口连接不良, 立即停止操作,更换造影管,对患者造成两次手术 连接的轻度不良影响。
场所名称 合并用药/械情况说明:
事件初步原因分析与处置
伤害类别
轻
规格
12支/盒
伤害表现
造成二次手术操作
产品批号
2019XXXX
年龄
产品编号
性别
UDI
器械故障表现
造影管接口不良
生产日期
20XX01XX
使用情况
有效期至 上市许可持有人名称
20XX1X2 XXXXX医疗器械有限公司
预期治疗疾病或作用 检查输卵管是否通常
器械使用日期
20XX.XX.XX
使用场所
XXX医院医疗器械不良反应事件报告
所属地区
XX省XX市XX区
单位名称
XXXX医院编码提来自日期XXXX.XX.XX
报告人
XXX
医疗器械情况
不良事件情况
产品名称 注册证编号
一次性使用子宫造影通水管 粤械注准2015XXXXXXX
事情发生日期 发生或获知日期
20XX.10.16 20XX.11.20
型号
12B
事件原因分析
产品原因
事件原因分析描述
产品质量问题
初步处置情况
立即停止操作,更换造 影管
医疗器械不良事件报告记录(表格模板、doc格式)

C.医疗器械情况
12.产品名称:
13.商品名称:
14.生产企业名称:
.生产企业地址:
生产企业联系电话:
15..型号:
规格:
注册证号:
产品编号:
批号:
16.操作人:□专业人员□非专业人员□患者□其它
17.有效期至:年月日
18.停用日期:年月日
19.植入日期(若植入):年月日
20.事件发生原因分析:
21.企业采取补救措施:
省级ADR中心意见陈述:
24.国家ADR 中心意见陈述:
医疗器械不良事件报告表
报告来源:生产企业□经营企业□使用单位□单位名称:
联系地址:联系电话:
报告日期:
A.患者资料
1.患者姓名:
2.年龄:
3.性别:□男□女
4.预期治疗疾病:
5.并发疾病:
6.既往疾病:
B.不良事件情况
7.事件后果
□死亡(时间)□危胁生命
□残疾□出生缺陷□其它
8.事件发生日期:年月日
9.事件报告日期:年月日
10.不良事件的发生地点:□医院□家庭
□门诊诊断□门诊治疗□其它
11.事件的陈述:
医疗机构医疗器械不良事件报告举例

医疗机构医疗器械不良事件报告举例一、报告内容报告人:医院报告时间:YYYY年MM月DD日报告主题:医疗器械不良事件报告二、事件概述医院于YYYY年MM月DD日在使用XX医疗器械过程中发生了不良事件。
该器械为XX型号,用于XX手术。
不良事件发生后,立即采取了紧急处理措施,并将事件报告给相关部门。
本报告将对该事件进行详细描述,并提出预防措施。
三、事件描述1.事件发生时间:YYYY年MM月DD日X时X分。
2.患者信息:患者为XX,性别,年龄XX,病情状况为XX。
3.手术过程:手术开始于XX时XX分,手术医生为XX,护士团队为XX。
手术过程中使用了XX型号的医疗器械。
4.不良事件描述:在手术过程中,XX器械出现XX问题,导致手术进展受阻。
事件发生后,立即停止手术,并采取相应措施处理。
患者的生命体征保持稳定,无进一步不良后果。
四、事件分析1.事件原因分析:经过初步调查和分析,发现该不良事件主要原因为器械XX的设计缺陷,导致在使用过程中出现问题。
2.患者受影响程度分析:虽然手术过程中出现了问题,但患者的生命体征并没有进一步恶化,也未出现其他不良后果。
五、处理措施2.后续处理:会同相关部门对事件进行调查和分析,以确定问题的根源,并采取相应的纠正措施。
3.患者关怀:对患者进行心理疏导和安抚,确保其心理和身体的健康。
六、预防措施1.提高质控意识:加强医院内部的质控培训,提高医护人员对医疗器械不良事件的识别和处理能力。
2.审查医疗器械供应商:对医疗器械供应商进行审查,选择质量可靠、信誉良好的供应商。
3.定期检查和维护:定期对医疗器械进行检查和维护,确保其性能和安全可靠。
七、总结通过对该事件的分析和处理,医院将加强对医疗器械不良事件的预防和处理能力,提高医疗质量和患者安全水平。
同时,也希望相关部门能够加强对医疗器械质量的监管和管理,保障患者的权益和安全。
医疗器械不良事件报告表

医疗器械不良事件报告表疗人员的死亡或严重伤害,应该按可疑医疗器械不良事件报告。
3、主动报告原则:医疗器械生产企业、经营企业、使用单位应该在发现可疑医疗器械不良事件后,主动向药监部门报告。
四、报告流程:1、发现可疑医疗器械不良事件后,立即停止使用该器械,采取必要的救治措施,并将事件报告给医疗器械生产企业、经营企业、使用单位的负责人。
2、医疗器械生产企业、经营企业、使用单位应该及时向药监部门报告可疑医疗器械不良事件,提供详细的事件陈述和医疗器械情况。
3、药监部门收到报告后,将对事件进行调查和分析,评估事件的严重程度,并根据评估结果采取相应的措施,包括通知医疗器械生产企业、经营企业和使用单位,要求其采取必要的措施,防止类似事件再次发生。
五、报告表填写说明:医疗器械不良事件报告表应该详细记录患者资料、医疗器械情况、不良事件情况、事件处理情况等信息,并在事件陈述中尽可能详细地描述事件的经过和影响。
填写报告表时应该注意格式的正确性,删除明显有问题的段落,并尽可能用简明的语言表达。
1、格式错误已经被修正;2、删除明显有问题的段落;3、改写每段话如下:一、报告原则:医疗器械不良事件报告是指在医疗器械使用过程中,发生了与医疗器械有关的意外、事故、质量问题、疾病传播等不良事件,需要向相关部门进行报告。
报告原则包括:必报原则、可疑即报原则和免除报告原则。
二、必报原则:根据《医疗器械不良事件报告管理办法》,以下情况必须报告:1.引起或造成死亡或严重伤害的事件;2.对医疗器械性能的影响性质严重,很可能引起或造成死亡或严重伤害的事件;3.使器械不能发挥其必要的正常作用,并且影响医疗器械的治疗、检查或诊断作用,可能引起或造成死亡或严重伤害的事件;4.医疗器械属于长期植入物或生命支持器械,因此对维持人类生命十分必要的事件;5.医疗器械生产企业需要采取或被要求采取行动来减少产品对公众健康造成损害的风险的事件;6.类似事件在过去实际已经引起或造成死亡或严重伤害的事件。
医疗器械不良事件报告范文

医疗器械不良事件报告范文尊敬的[相关部门/机构]:我得跟您唠唠我遇到的这个医疗器械的事儿,可真是有点让人糟心呢。
我使用的是[医疗器械名称],这东西本来是为了给咱的健康保驾护航的,结果却出了岔子。
一、患者基本信息。
我呢,叫[姓名],性别[性别],今年[X]岁啦。
住在[具体住址],联系电话是[电话号码]。
平常身体虽说不是铁打的,但也没太多大毛病,就一些小问题需要靠这个医疗器械来辅助治疗或者监测啥的。
二、医疗器械信息。
这个[医疗器械名称]是[生产厂家名称]生产的,型号是[具体型号],序列号是[序列号]。
我是在[购买/使用场所(如XX医院、XX医疗器械店)]获得这个器械的,使用这个器械是为了[具体用途,比如测量血压、辅助康复等]。
三、不良事件发生情况。
# (一)事件发生时间。
# (二)事件表现。
这器械突然就像发了疯似的,[具体描述不良事件现象,例如“血糖仪屏幕上的数据乱跳,一会儿显示个超高的数值,一会儿又显示错误代码,根本没法正常测血糖了。
”或者“那个理疗仪在工作的时候突然发出一阵怪声,然后就停止工作了,还冒出一股烧焦的味道,可把我吓了一跳。
”]这可把我给急坏了,本来靠着它来了解自己的身体状况或者进行治疗呢,结果它这样一搞,我都不知道该咋办了。
四、不良事件后果。
# (一)对患者的影响。
这不良事件对我造成的影响可不小呢。
如果是像血糖仪这种测量类的器械出问题,那我就没办法准确知道自己的血糖情况了,可能会影响我对自己饮食和药物使用的判断,这就像在黑暗里走路,没有个指引,心里直发慌。
要是理疗仪之类的治疗器械出问题,那就更糟糕了,本来是为了缓解病痛的,结果不但没治好,还可能因为突然的故障给身体带来一些潜在的风险,比如皮肤烫伤(如果是有发热功能的理疗仪故障的话)或者耽误了病情的治疗,让我多遭了不少罪。
# (二)采取的措施。
当时我第一反应就是赶紧停止使用这个器械。
如果是在医院里发生的,我就马上叫护士或者医生来看是咋回事儿;要是在家呢,我就按照说明书上的一些紧急处理办法试了试,可根本没啥用。
设备科医疗器械不良事件总结报告

设备科医疗器械不良事件总结报告一、背景随着医疗器械在医疗卫生领域的广泛应用,其在临床治疗、诊断等方面的作用日益凸显。
然而,医疗器械不良事件也时常发生,给患者带来了不必要的伤害和风险。
为了加强医疗器械不良事件的监测和管理,提高医疗器械使用安全,我国相关部门制定了一系列政策和规定。
我单位作为医疗机构,积极响应政策,对医疗器械不良事件进行严格监控和管理,以确保患者安全。
二、医疗器械不良事件概述1. 定义:医疗器械不良事件是指在医疗器械使用过程中,由于器械本身、使用方法、维护保养等原因,导致患者受到伤害或者设备功能失效的事件。
2. 分类:根据医疗器械不良事件的严重程度,可以分为严重不良事件和非严重不良事件。
严重不良事件是指可能导致患者死亡、严重伤害、生命危险的医疗器械事件;非严重不良事件是指对患者造成轻微伤害或者不影响医疗器械正常使用的重要事情。
3. 发生原因:医疗器械不良事件的发生原因多样,主要包括:(1) 医疗器械设计不合理:设计缺陷可能导致医疗器械在使用过程中出现功能异常,从而引发不良事件。
(2) 医疗器械质量问题:原材料、生产工艺、组装等环节的质量问题可能导致医疗器械在使用过程中出现故障或者失效。
(3) 医疗器械使用不当:医务人员对医疗器械的使用方法掌握不熟练,或者患者使用不当,可能导致医疗器械不良事件的发生。
(4) 医疗器械维护保养不到位:医疗器械的维护保养是确保其正常运行的重要环节,维护保养不到位可能导致医疗器械不良事件的发生。
三、医疗器械不良事件监测与管理1. 建立不良事件监测制度:成立医疗器械不良事件监测小组,明确职责和任务,建立医疗器械不良事件报告、审核、处置等流程。
2. 加强医疗器械培训:对医务人员进行医疗器械相关知识培训,提高其对医疗器械不良事件的识别、报告和处理能力。
3. 完善医疗器械使用说明:医疗器械使用说明应详细、明了,包含正确的使用方法、注意事项、禁忌症等,以降低不良事件的发生。
医疗器械不良事件过程描述样板

医疗器械不良事件举例(仅供参考,实际上报以临床表现及治疗为准):要求格式:患者何原因在何地使用何种医疗器械,何时出现何不良事件,何时采取何措施,何时终结,何结果。
1.患者于2013年9月2日因皮肤挫裂伤入院治疗,医生在给予清创处理后进行包扎,用胶布固定。
1日后患者感觉胶布黏贴处瘙痒,发现有皮疹,随即用纱布绷带固定,一天后症状减轻。
2.患者因颈椎病于2012年11月23日来院就诊,给予使用颈腰椎牵引器进行牵引,使用前检查无误,在使用12分钟时突然发生漏气,随即停止使用,进行更换新的后,使用正常,未对患者造成影响。
3.2013年09月02日上午9:00左右,护理人员遵医嘱为该患者给予静脉用药时,在患者的静脉输液过程中,护理人员巡视病房时、责任护士发现该患者使用正在输液的输液器莫菲滴管内已无液体,但发现输液药袋中还有余液体约120ml左右,及时发现后立即更换另一输液器进行输液,护理人员并定时、及时巡视病房,观察更换输液器后、输液滴速用药正常。
4.患者因锁骨骨折,于2013年8月5日来我院就诊,行切开复位内固定术,使用电刀切割,使用时发现高频手术设备无输出,减缓手术进程。
经检查,为高频手术电极故障。
遂更换新的高频手术电极,继续手术。
5.患者因“腹股沟部出现可复性肿块1年余,加重1周”于2013年9月7日,遂来我院门诊就治,门诊以“腹股沟斜疝”收入我院给予手术治疗。
在2012年9月10日上午9点给予手术治疗过程中使用该公司高频手术电极(高频手术电刀柄)切割时,使用15mim后出现电刀变钝不快,不利于手术进行,随即更换新的电刀。
6.2014年6月20日患者因足月妊娠前来就诊,入院后行刨宫术使用导尿管导尿2小时候患者自行感觉尿道口周围有瘙痒感检查发现皮疹,立即停止使用并清洗,更换其他批次导尿管,导尿正常,原因分析:导尿管质量不合格,机体对导尿管敏感。
7.患者于2013.10.08因急性尿潴留住院,需行导尿术,在入院后半小时给予用一次性使用无菌导尿管导尿,导尿进行20分钟后发现尿液顺导尿管外壁漏出,立即给予更换导尿管,重新导尿,增加患者病痛。
医疗器械不良事件报告记录

医疗器械不良事件报告记录概述医疗器械的不良事件报告是一项重要的工作,旨在监测和评估医疗器械在使用过程中的安全性和有效性。
本文将介绍医疗器械不良事件报告的步骤和要求,以帮助相关人员正确填写和提交不良事件报告。
步骤1. 识别和收集信息在发生医疗器械不良事件后,第一步是识别和收集相关信息。
这包括:•不良事件的发生时间和地点;•医疗器械的名称、型号和生产商;•不良事件的详细描述;•受影响的患者信息;•医疗人员的联系方式等。
2. 评估事件的严重性根据收集到的信息,对不良事件的严重程度进行评估。
不同的不良事件可能有不同的影响程度,例如对患者的健康造成的影响程度、是否导致死亡等。
3. 填写报告表格根据医疗机构的要求,填写不良事件报告表格。
报告表格通常包括以下内容:•不良事件的描述和分类;•医疗器械的相关信息;•患者和医疗人员的信息;•事件发生的时间和地点;•不良事件的严重程度评估;务必确保填写准确无误的信息,并尽可能提供详细的描述。
4. 提交报告填写完不良事件报告表格后,将报告提交给相关的医疗机构或监管部门。
不同地区和国家可能有不同的提交方式,例如电子提交、邮寄等。
确保按照要求提交报告,并保留好副本作为备份。
5. 跟进和回应医疗机构或监管部门会对收到的不良事件报告进行跟进和回应。
他们可能会要求补充信息或进行进一步的调查。
及时回应并提供所需的信息是至关重要的。
注意事项在填写和提交医疗器械不良事件报告时,还有一些需要注意的事项:1.保护患者隐私:确保不良事件报告中的患者信息不被泄露,遵守相关的隐私保护法规。
2.提供准确的信息:尽量提供准确、详细的信息,包括医疗器械的型号、生产商等,以便于后续的调查和处理。
3.及时提交报告:将不良事件报告及时提交给相关的医疗机构或监管部门,确保他们能够及时采取措施以保障患者的安全。
结论医疗器械不良事件报告是确保医疗器械安全性和有效性的重要环节。
通过正确填写和提交不良事件报告,可以促进医疗机构和监管部门对医疗器械的监测和管理,从而保障患者的健康和安全。
医疗器械不良事件报告表

医疗器械不良事件报告表
医疗器械不良事件报告表是医疗器械监督管理部门规定的一种记录和报告医疗器械不良事件的表格。
医疗器械不良事件是指在医疗器械使用过程中发生的不良事件,包括但不限于器械设计、制造、包装、储运、使用说明、不良反应、事故等各个环节的问题。
医疗器械不良事件报告表的填写是医疗器械生产企业、经营企业和使用单位的一项重要义务,也是保障患者安全的重要措施。
医疗器械不良事件报告表的内容一般包括但不限于以下几个方面,一是事件基本信息,包括事件发生时间、地点、相关人员等;二是器械信息,包括器械名称、型号、规格、生产批号、有效期等;三是事件描述,包括事件经过、可能原因、危害程度等;四是处理措施,包括已采取的应急处理措施、后续处理措施等;五是责任追究,包括相关责任人的处理情况、相关部门的处理意见等。
在填写医疗器械不良事件报告表时,需要尽可能详细地描述事件经过和相关信息,以便医疗器械监督管理部门和相关部门对事件进行调查和处理。
同时,还需要客观、准确地记录事件,避免主观臆断和夸大事实,以免影响事件的处理和后续工作。
医疗器械不良事件报告表的填写需要相关人员严格按照规定进行,不得隐瞒不良事件,不得篡改事件信息,不得迟报不良事件。
医疗器械生产企业、经营企业和使用单位应建立健全不良事件报告制度,加强对相关人员的培训和教育,提高不良事件报告的及时性和准确性。
总之,医疗器械不良事件报告表的填写是保障患者安全的重要环节,是医疗器械监督管理部门和相关部门开展监督检查和风险评估的重要依据。
只有加强对医疗器械不良事件报告表的填写和管理,才能及时发现和处理医疗器械不良事件,最大限度地保障患者的安全和权益。
医疗器械不良事件报告范例

医疗器械不良事件报告范例近年来,随着社会经济的发展和医疗技术的突破,医疗器械在医疗行业中的应用越来越广泛。
然而,与之同时,医疗器械不良事件也时有发生,给人们的生命安全带来了一定的威胁。
为了更好地管理和控制医疗器械不良事件,必须建立一个完善的报告系统。
本文将以一个医疗器械不良事件的报告范例为例,详细介绍该报告的内容和形式。
报告主题:医用电动吸引器失灵一、事件描述根据我院2021年5月1日至5月30日期间发生的医疗器械不良事件报告,报告编号:12345678。
事发时间为2021年5月15日上午10点,患者王某(男,65岁)在我院进行鼻窦炎手术后出现呼吸困难的不良状况。
经过紧急救治,患者目前病情稳定。
二、器械信息患者在手术时使用了我院购买的医用电动吸引器丙型型号(批次号:ABC123456)。
该器械主要用于排除呼吸道分泌物,确保患者的通畅呼吸。
三、失灵情况描述据手术室护士陈某的描述,手术期间,电动吸引器突然停止运转,无法完成抽吸任务。
护士随即通知同事切换到备用吸引器继续手术。
经过后续的检查和调查,确定该电动吸引器发生了严重故障,导致了此次意外。
四、结果由于电动吸引器故障,患者出现呼吸困难。
幸好我们的医护人员反应及时,迅速采取了紧急救治措施,患者目前病情稳定。
五、原因分析根据技术人员的分析,初步判断电动吸引器失灵的原因是设备内部的电线连接问题,导致电路中断,使得设备无法正常运行。
六、整改措施1. 停止使用该型号的电动吸引器,并将其送至供应商修理。
2. 加强器械设备的定期检查和维护,确保设备的正常运行。
3. 设立医疗器械不良事件报告制度,加强对医疗器械的质量监管。
七、教训与总结本次医疗器械不良事件表明,医疗机构在选择和使用医疗器械时必须十分谨慎。
对于设备故障要及时发现和排除,并加强对设备的定期检查和维护。
同时,建立医疗器械不良事件报告制度,及时报告和处理医疗器械不良事件,以提高患者的安全性和医疗服务质量。
医疗器械不良事件报告范例

医疗器械不良事件报告范例哎呀,今天咱们聊聊医疗器械不良事件报告这事儿,听起来有点严肃,但其实也能说得轻松点。
你知道的,医疗器械在医院里可算是个大明星。
没了它们,医生可真是干不了什么活。
可是,这些“大明星”也会掉链子,搞出点小麻烦。
比如,咱们这儿有个小故事,讲的是一个名叫小李的年轻医生。
小李刚刚入职医院,满怀激情,觉得自己是拯救生命的超级英雄。
那天,他正忙着给病人做手术,突然发现那台新来的手术器械没反应。
小李心里一紧,“哎呀,真是倒霉,今天怎么这么多事啊?”他本来以为这只是个小插曲,谁知越看越不对劲。
这台器械像是吃了错药,发出怪声,甚至冒出点烟来。
你说,这也太吓人了吧!小李简直想立刻给这玩意儿打个电话,问问它到底怎么了。
这时候,病人也感觉到了不对劲,瞪大眼睛看着小李,心里肯定在想:“这小医生怎么回事啊?怎么还没动手术?”小李一边安抚病人,一边脑海里飞速转动。
他想,必须得报告这事儿。
可是,报告怎么写呢?他心里想着,“这可真是个考验,别让我把这写得像论文一样复杂。
”于是,他决定用简单易懂的语言,把这事儿给说清楚。
小李一口气把事情的经过写了下来,开头就来个“大家好,我是小李,今天发生了一件有趣又让人紧张的事儿。
”他详细描述了器械的状况,简直像是在讲故事。
什么冒烟啦、发怪声啦,他一一列举,让人听得明明白白。
还不忘加入点幽默,比如“这台机器好像是参加了什么派对,突然兴奋过头了。
”哈哈,谁能想到,写报告也能这么有意思呢。
然后,他把报告发给了医院的质量管理部,心里有点忐忑,毕竟这可不是小事。
等了一会儿,终于收到了回复,质量管理部的工作人员也回复得很快,表示感谢小李的报告,真是让人松了一口气。
他们还表示,这个事件会引起重视,会对这台器械进行彻底的检查,确保不会再出现类似的问题。
小李听了心里乐开了花,原来认真负责也是会有回报的。
接下来的几天,医院的气氛就有点不同了。
大家都知道小李的故事,成了茶余饭后的谈资。
有人甚至打趣说,“小李,这下可真是名声在外了,医疗器械的守护者!”小李虽然不好意思,但心里还是挺得意的。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
21.企业采取补救措施:
22.器械目前状态:
D.不良事件评价
23.省级ADR中心意见陈述:
24.国家ADR中心意见陈述:
医疗器械不良事件报告表
报告来源:生产企业□经营企业□使用单位□单位名称:
联系地址:联系电话:
报告日期:
医疗器械不良事件报告记录
A.患者资料
1.患者姓名:
2.年龄:
3.性别:□男□女
4.预期治疗疾病:
5.并发疾病:
6.既往疾病:
B.不良事件情况
7.事件后果
□死亡(时间)□危胁生命
□残疾□出生缺陷□其它
8.事件发生日期:年月日
9.事件报告日期:年月日
10.不良事件的发生地点:□医院□家庭
□门诊诊断□门诊治疗□其它
11.事件的陈述:
报告人签字:
C.医疗器械情况
12.产品名称:
13.商品名称:
14.生产企业名称:
.生产企业地址:
生产企业联系电话:
15..型号:
规格:
注册证号:
产品编号:
批号:
16.操作人:□专业人员□非专业人员□患者□其它
年月日
19.植入日期(若植入):年月日
