价层电子对互斥理论
价层电子对互斥理论

第7讲价层电子对互斥理论根据预习里已经学习的内容,你发现常见分子或者离子的空间构型可以通过记忆获取。
但是,分子或者微粒的种类数目有许许多多,陌生微粒的空间构型应该如何推断呢?1.价层电子对互斥理论(VSEPR)分子中的价层电子对包括σ键电子对和中心原子上的孤电子对,由于电子对的相互排斥作用,而趋向尽可能彼此远离,分子尽可能采取对称的立体构型,以减小斥力。
2.价层电子对的确定方法(1)a 表示中心原子的价电子数。
对主族元素:a =最外层电子数; 对于阳离子:a =价电子数-离子电荷数; 对于阴离子:a =价电子数+|离子电荷数|。
(2)x 表示与中心原子结合的原子数。
(3)b 表示与中心原子结合的原子最多能接受的电子数,氢为1,其他原子=8-该原子的价电子数。
3.VSEPR 模型预测分子或离子的立体构型 (1)中心原子上的价电子都用于形成共价键的分子讲义一、导入二、知识讲解知识点1 价层电子对互斥理论平面三角形正四面体形(2)中心原子上有孤电子对的分子对于中心原子上有孤电子对(未用于形成共价键的电子对)的分子,中心原子上的孤电子对也要占据中心原子周围的空间,并互相排斥使分子呈现不同的立体构型。
VSEPR模型与分子的立体构型不一定一致,分子的立体构型指的是成键电子对的立体构型,不包括孤电子对(未用于形成共价键的电子对)。
两者是否一致取决于中心原子上有无孤电子对,当中心原子上无孤电子对时,两者的构型一致;当中心原子上有孤电子对时,两者的构型不一致。
三、例题精析【教学建议】此处内容主要用于教师课堂的精讲,每个题目结合试题本身、答案和解析部分,教师有的放矢的进行讲授或与学生互动练习。
例题11.用价层电子对互斥理论判断SO3的分子构型为()A.正四面体形B.V形C.三角锥形D.平面三角形解析:选D SO3中S原子的价层电子对数为3,其全部用于形成共价键,S原子周围有3个氧原子,属于平面三角形。
例题22.连线题。
价层电子对互斥理论

三角 BF3、 SO3 形 SnBr2、 V形 PbCl2
价层 电子 对数 目
价层电 σ 键 孤电 电子对 分子的 子对的 电子 子对 的排列 空间构 实例 空间构 方式 型 对数 数 型
4 4 四面体 形 3 2
0 1 2
四面体 CH4、 CCl4 形
三角锥 NH3、 PCl3 形 V形 H2O
4+2=6 6-1=5
3 3
2 1
1、对阳离子来说,a为中心原子的价电子数减去离子的电荷 数,其它不变。 2、对阴离子来说,a为中心原子的价电子数加上离子的电荷 数,其它不变。
四、分子空间构型的确定
价层电子对有成键电子对和孤电子对之分,在得到价层 电子对数之后可得到VSEPR模型,然后我们略去VSEPR模型 中中心原子上的孤对电子,便可得到分子的立体构型。
NH3
CH4
a
孤对电子对数
x b 中心原子 上的孤电 子对数
分子 中心 或离 原子 子 H2O CO2
O
C N C
6
4 5 4
2
2 3 4
1
2 1 1
2
0 1 0
NH3
CH4
CO32-
H30+ 的孤对电子对数求法?
分子或 中心 离子 原子 CO32H30+ C O
a
x
b
中心原子 上的孤电 子对数 0 1
这样已知价层电子对的数目,就可以确定VSEPR模型。
三、价层电子对的确定方法
注:1、σ键电子对数可由分子式确定,例如:H2O 为2 NH3 为3 2、中心原子的孤对电子 =1/2(a-xb) a为中心原子的价电子数 x为与中心原子结合的原子数 b为与中心原子结合的原子最多能接受的电子数
价层电子对互斥理论使用

价层电子对互斥理论使用价层电子对互斥理论是一种用来解释电子在能级上分布的理论。
该理论认为,在一个多电子系统中,电子倾向于占据不同的能级,这是因为电子之间存在一种互斥作用。
这种互斥作用源于电子之间的库仑排斥和泡利不相容原理。
库仑排斥是指电子之间由于带正电的原子核引力作用而产生的互斥力。
当两个电子靠近时,它们之间产生的排斥力会增加,使得电子倾向于占据不同的能级。
这种互斥作用对电子分布起到了显著的作用。
泡利不相容原理是指每个电子的量子态必须是唯一的。
根据泡利不相容原理,任意两个电子不能具有相同的量子态,即它们的自旋量子数必须不同。
这意味着电子不能全部集中在同一个能级上,而是倾向于分布在不同的能级上,以满足泡利不相容原理。
基于价层电子对互斥理论,可以解释许多电子结构的现象。
首先,可以解释原子的层次结构。
根据互斥理论,电子会填充不同的能级,从低能级开始,一直填充到高能级。
这解释了原子的能级结构和化学性质。
其次,互斥理论还可以解释原子和分子中电子的排布。
在原子中,电子遵循互斥原则,尽量占据不同的价层。
在分子中,电子在不同原子之间的共享和分配也遵循互斥原则。
这解释了化学键的形成和分子的几何结构。
互斥理论还有助于理解电子在固体中的行为。
固体中的电子被束缚在晶体中,组成电子云。
根据互斥理论,这些束缚电子也遵循互斥原则,尽量占据不同的能级。
这解释了导体、绝缘体和半导体的电子行为,以及电子在带隙里的分布。
此外,互斥理论还有助于解释多电子体系的能量分布。
根据互斥原理,电子将占据能量较低的态,使得多电子体系的总能量降低。
这解释了多电子体系的稳定性和能级分布。
总结来说,价层电子对互斥理论是一种解释电子在能级上分布的理论。
这一理论是基于库仑排斥和泡利不相容原理的,可以解释多种电子结构和化学现象。
它为我们理解原子、分子和固体的性质提供了重要的理论依据。
第三章-1节-价层电子对互斥理论PPT课件

对氧 族原 子
作中心体时ne =6 作配体时ne =0
对卤 素原 子
作中心体时ne =7 作配体时ne =1
注意:多重键与单电子作为一对电子处理。
.
4
价层电子对互斥作用的顺序
• 孤电子对-孤电子对 > 孤电子对-成键 电子对> 成键电子对-成键电子对
• 双键、叁键或单个电子均按单键处理, 排斥作用大小:
排除作用更大,因此包含多重键时的键角比只 焓单键的键角大
X2C=O F2CO Cl2CO
∟XCO 126°
124.3 °
X2C=CX2 F2C=CH2 F2C=CFCl
∟XCC 125.3 ° 123 °
.
12
3.对分子键长变化的解释
• 价层电子对之间斥力的差异使键长发生改变, 影响对称性(点群)。 Oh群
.
14
拉长
分子 垂直轴向键长 赤道平面键长
PCl5(气)
210pm
204pm
ClF3
171.6pm
.
162.1pm
13
四.对该理论模型的评述
• 1.能够成功预测主族元素分子的形状,能够解 释键参数的变化规律。
• 2.该模型不需要复杂计算,结果是定性的。
• 3.存在许多例外,对高配位数预测例外更多。
• 5.杂化轨道理论能解释分子的几何构形,但不 能预测,而价层电子对互斥理论能预测分子 的几何构形,但不能解释分子的成键情况, 两者结合,具有一定的互补性,可达到处理 问题简便、迅速、全面的效果。
.
6
第二步:画出价层电对的所以几何构型
• 对于ClF3共有 三种。
第三步:计算各结 构的斥力大小
结果:a < c < b
02考点三价电子对互斥理论杂化轨道理论及应用(教师版)
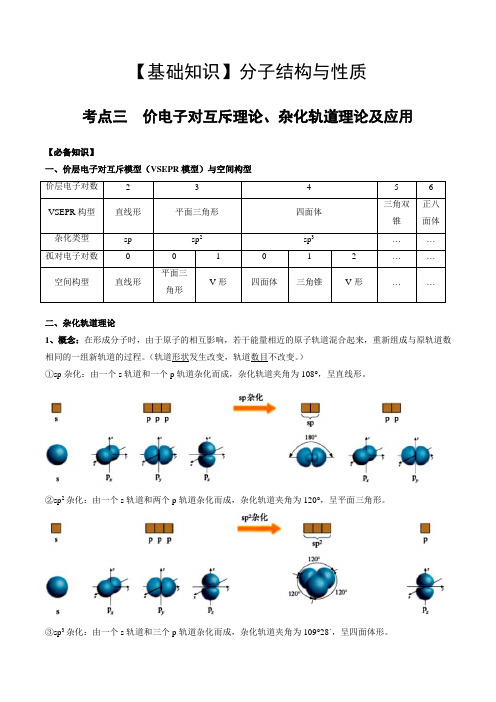
【基础知识】分子结构与性质考点三价电子对互斥理论、杂化轨道理论及应用【必备知识】一、价层电子对互斥模型(VSEPR模型)与空间构型价层电子对数 2 3 4 5 6VSEPR构型直线形平面三角形四面体三角双锥正八面体杂化类型sp sp2sp3……孤对电子对数0 0 1 0 1 2 ……空间构型直线形平面三角形V形四面体三角锥V形……二、杂化轨道理论1、概念:在形成分子时,由于原子的相互影响,若干能量相近的原子轨道混合起来,重新组成与原轨道数相同的一组新轨道的过程。
(轨道形状发生改变,轨道数目不改变。
)①sp杂化:由一个s轨道和一个p轨道杂化而成,杂化轨道夹角为108°,呈直线形。
②sp2杂化:由一个s轨道和两个p轨道杂化而成,杂化轨道夹角为120°,呈平面三角形。
③sp3杂化:由一个s轨道和三个p轨道杂化而成,杂化轨道夹角为109°28´,呈四面体形。
2、价电子对数=σ键电子对数+中心原子的孤电子对数说明:σ键电子对数=中心原子结合的原子数;中心原子的孤电子对数=1/2 (axb ±电荷)①a 表示中心原子的价电子数。
对于主族元素:a=原子的最外层电子数。
②x表示与中心原子结合的原子数。
③b表示与中心原子结合的原子最多能接受的电子数,即化合价绝对值。
例1、完成下列表格AB nб键数孤对电子对数价电子对数中心原子杂空间构型化轨道类型3 14 sp3三角锥形SOCl2中心原子为SNH4+ 4 0 4 sp3四面体SO42 4 0 4 sp3四面体ClO4 4 0 4 sp3四面体NH3 3 1 4 sp3三角锥形H2O 2 2 4 sp3V形SO3 3 0 3 sp2平面三角形BF3 3 0 3 sp2平面三角形SO2 2 1 3 sp2V形NO2 2 1 3 sp2V形CS2 2 0 2 sp 直线形O3 2 1 3 sp2平面三角形例2、判断以下有机物中原子的杂化轨道类型。
价层电子对互斥模型(VSEPR)

02
03
指导新物质合成
基于价层电子对互斥模型,化学家可 以预测新物质的可能几何构型,从而 指导新物质的合成和性质研究。
对其他学科的启示
物理学
价层电子对互斥模型中的电子排斥作用与物理学中的电磁 相互作用有相似之处,为理解电磁现象提供了新的视角。
材料科学
将价层电子对互斥模型应用于材料科学,有助于理解不同材料 的电子结构和性质,为新型材料的研发提供理论支持。
些因素,以更准确地预测分子的空间构型和性质。
04 价层电子对互斥模型的应用
在化学反应中的作用
预测分子间的相互作用
价层电子对互斥模型可以用于预测分子 间的相互作用,如氢键、离子键和共价 键的形成,从而帮助理解化学反应的机 理。
VS
预测反应活性
通过分析分子中的价层电子对分布,可以 预测分子的反应活性,从而预测化学反应 的方向和速率。
概念
该模型认为,在分子中,价层电子对 会尽可能地相互远离,以减少相互排 斥的能量,从而形成稳定的分子构型 。
发展历程与重要性
发展历程
价层电子对互斥模型最初由美国化学 家罗伯特·马利肯和丹麦物理学家哈那 德·詹森在20世纪50年代提出。
重要性
该模型在化学领域中具有重要意义, 因为它提供了一种简便的方法来预测 分子的空间构型,有助于理解分子的 性质和行为。
与价键理论的关系
关系
价层电子对互斥模型和价键理论是相辅相成的理论体 系。
区别
价键理论主要关注电子的成键和反键轨道,而价层电 子对互斥模型则更侧重于预测分子的空间构型。
联系
在价键理论的基础上,价层电子对互斥模型可以进一 步揭示分子构型的奥秘。
价层电子对互斥模型的基本原
价电子互斥理论-PPT

1
价层电子对互斥理论
——一种快速判断分子和 离子构型的方法
2
1、掌握确定分子空间构型的基本方法 2、了解等电子原理及其应用 重点掌握:ABX型分子或离子的空间构型
3
1、内容:
分子中的价电子对(包括成键电子对n,和 孤电子对m)由于相互排斥作用,尽可能 趋向彼此远离以减小斥力。
价电子对数目为2、3、4时,价电子对的几何 分布分别呈直线形、平面三角形、正四面体构型。
15
注意: ①中心原子的价电子数等于中心原 子的最外层电子数。 ②配位原子中卤素原子、氢原子提 供一个价电子,氧原子和硫原子按 不提供价电子计算,但做为中心原 子时提供6个价电子。
③若讨论的是离子,应加上或减去 离子的电荷数。(阳离子应减去电 荷数,阴离子应加上电荷数。)
即:每个碳原子的杂化轨道数=碳原子 所成的σ键数,
21
【规律小结】 判断含碳分子空间构型的步骤: 1. 分析(每个碳原子所成的)____数 2.得出________数 3.确定杂化方式 4.得出杂化轨道空间构型 5.判断分子空间构型
22
三、等电子原理
具有相同价电子数(指全部电子总数或 价电子总数)和相同原子数的分子或离 子具有相同的结构特征。
PF5
CH4 四面体形
BF3 SO3
SF6 正八面体形
8
大家有疑问的,可以询问和交流
可以互相讨论下,但要小声点
9
3、推断分子空间构型的具体步骤:
⑴、先确定中心原子的价层电子对数, 再确定杂化轨道的空间构型
n=2 直线形
n=3 平面三角形
n=4 正四面体
10
⑵、确定中心原子的孤对电子对数, 推断分子的空间构型。
课件13:2.2.1 价层电子对互斥理论

实例解析: H2O中的中心原子为O,O有2个σ键电子对;NH3中的中 心原子为N,有3个σ键电子对。
拓展练习: 指出CO2分子中的中心原子和σ键电子对数: CO2中的中心原子为C,C有2个σ键电子对。
③【理论解析】 中心原子上的孤电子对数 =½(a-xb) a:中心原子的价电子数,(主族元素就是
第1课时 价层电子对互斥理论
【课标要求】 1. 认识共价分子结构的多样性和复杂性。 2. 能根据价层电子对互斥理论判断简单分子或离
子的构型。
一、形形色色的分子 1.三原子分子立体结构
CO2 模型名称:直线形
键 角: 180°
H2O 模型名称: V形
键 角:104.5°
2.四原子分子立体结构
HCHO 模型名称:平面三角形 键 角: 约120°
CH2O
NH3
二、价层电子对互斥理论 1.价层电子对互斥理论 ①【理论内涵】 分子的立体构型是“价层电子对”相互排斥的结果。
分子总是采取电子对相互排斥最小的那种构型,以使彼 此之间远离达到斥力最小,分子体系能量最低,最稳定。
②【概念解析】 分子中的中心原子上的电子对。
价层电子对 包括σ键电子对和中心原子上的孤电子对。
NH3 模型名称:三角锥形 键 角: 107°18′
3.五原子分子立体结构
CH4 模型名称: 正四面体
键 角:109°28′
4.其它
P4 模型名称:正四面体
键 角:60°
C2H2
模型名称:直线形 键 角:180°
思 考1
同为三原子分子,CO2 和 H2O 分 子的空间结构却不同,什么原因?
同为四原子分子,CH2O与 NH3 分 子的的空间结构也不同,什么原因?
价电子对互斥理论

生物化学
03
价电子对互斥理论在生物化学中也有应用,如预测生物大分子
的结构和功能,以及药物与生物大分子的相互作用等。
02 价电子对互斥原理
原子轨道与价电子
原子轨道
描述电子在原子核外运动状态的函数,决定了电子的空间分布和 能量。
价电子
原子参与化学反应的电子,通常位于原子的最外层轨道上。
原子轨道与价电子的关系
当价电子对数目为3时,原子 采用sp2杂化方式,形成平面 三角形分子,如BF3、SO3等 。此外,某些具有孤对电子的 分子也会采用sp2杂化方式, 如H2O、NH3等。
当价电子对数目为4时,原子 采用sp3杂化方式,形成四面 体构型的分子,如CH4、SiH4 等。此外,具有孤对电子的分 子也可能采用sp3杂化方式, 但其几何构型会发生变化,如 NH3为三角锥形,H2O为V形 。
互斥原理与化学键合
互斥原理不仅适用于价电子对之间的排斥,也适用于化学键合过程中 的电子排布和键角预测。
能量最低原则
01
能量最低原则
分子在形成时趋向于达到能量最低的状态,因为这样的状态最稳定。
02
价电子对互斥与能量最低原则的关系
价电子对之间的互斥作用使得分子在形成时趋向于调整几何构型以降低
电子对之间的排斥能,从而达到能量最低的状态。
价电子对数目与键角关系
价电子对数目越多,键角越小。 当价电子对数目相同时,不同杂化类型的分子键角也有所不同。
实例分析
水分子(H2O)
中心原子氧原子有两对价电子对,根据价电子对互斥理论,这两对价电子对应该尽量远离彼此,形成 109.5°的键角。然而,由于氧原子上还有两对孤电子对,这些孤电子对也对键角产生了影响,使得水分子 的键角略小于109.5°,实际测量值为104.5°。
价层电子对互斥理论

价层电子对互斥理论
双价层电子对互斥理论提出了一种新的观点,表明电子是双价的,而不是单价的,即双价层模型是由两个负责一个反应的活性立体复配,整个双价层电子互斥理论给出了一个反应前激子和过渡态之间的立体分子动力学框架,为理解有机分子反应的立体化学提供了基础性的理论支撑。
双价层电子对互斥理论和单价电子理论的核心正在于,电子活性的双价状态是有机反应的一个重要的特征,它们构成“立体复配”,也就是双价层模型,这种差异主要表现在双价层模型的跃迁态过程中的动力学行为上,即每一个轨道状态都只有一个立体结构,而且这两个轨道之间的不对称性也存在。
即使能量有所改变,这种不对称性也不会随之改变。
反应前激子和反应过渡态可以通过这种双轨道立体不对称性来解释,其中重要的是反应中的立体复配。
价层电子对互斥理论使用

价层电子对互斥理论使用价层电子对互斥理论(Valence Shell Electron Pair Repulsion Theory)是一种用于推测分子几何形状的理论。
该理论假设电子对在空间中互相排斥,因此分子的几何构型可以通过电子对的排布来确定。
价层电子对是指与原子之间能够形成共价键或孤对电子的电子对。
理论基础:1.电子对之间的排斥力最小化。
同种电子对之间的排斥力较大,不同种电子对之间的排斥力较小。
2.单独的电子对比成对的电子对更容易被其他电子云所靠近。
3.电子对的排布趋向于最大程度的分离。
根据这些原则,我们可以预测分子的排布形态。
分子的电子对排布方式有多种形态,包括线性、平面三角形、平面四边形、平面五边形、笼形、六边形、八面体等。
以氨分子(NH3)为例,氮原子有5个电子,其中3个与3个氢原子形成共价键,剩下的2个是孤对电子。
根据价层电子对互斥理论,孤对电子会占据较大的空间,使得氨分子呈现出一个三角形构型。
再以甲烷(CH4)为例,碳原子有4个电子,与4个氢原子形成共价键。
根据价层电子对互斥理论,这4个电子对会互相排斥,使得甲烷分子呈现出一个正方形构型。
另外一个例子是水分子(H2O),氧原子有6个电子,与两个氢原子形成共价键,剩下的2个是孤对电子。
根据价层电子对互斥理论,这两个孤对电子会占据较大的空间,使得水分子呈现出一个倾斜的构型。
从上述示例可以看出,通过价层电子对互斥理论,我们可以推测出分子的几何构型,进而推断分子的性质和反应行为。
这为有机化学、无机化学以及生物化学等领域的研究提供了有力的理论基础。
然而,价层电子对互斥理论也有其局限性。
例如在一些分子中,价层电子对排布方式可能不符合预期,这可能是由于额外的电子云效应或分子内相互作用的影响。
此外,该理论只适用于描述小分子的几何构型,对于大分子或者有多个中心原子的分子来说并不适用。
尽管如此,价层电子对互斥理论依然是化学中一项重要的理论工具,为我们理解分子结构和性质提供了实质性的帮助,并促进了分子设计、药物研发以及催化反应等方面的进展。
价层电子对互斥理论

价层电子对互斥理论价层电子对互斥理论(英文:V alence S hell E lectron P air R epulsion (VSEPR)),是一个用来预测单个共价分子形态的化学模型。
理论通过计算中心原子的价层电子数和配位数来预测分子的几何构型,并构建一个合理的路易斯结构式来表示分子中所有键和孤对电子的位置。
[编辑]理论基础价层电子对互斥理论的基础是,分子或离子的几何构型主要决定于与中心原子相关的电子对之间的排斥作用。
该电子对既可以是成键的,也可以是没有成键的(叫做孤对电子)。
只有中心原子的价层电子才能够对分子的形状产生有意义的影响。
分子中电子对间的排斥的三种情况为:孤对电子间的排斥(孤-孤排斥);孤对电子和成键电子对之间的排斥(孤-成排斥);成键电子对之间的排斥(成-成排斥)。
分子会尽力避免这些排斥来保持稳定。
当排斥不能避免时,整个分子倾向于形成排斥最弱的结构(与理想形状有最小差异的方式)。
孤对电子间的排斥被认为大于孤对电子和成键电子对之间的排斥,后者又大于成键电子对之间的排斥。
因此,分子更倾向于最弱的成-成排斥。
配体较多的分子中,电子对间甚至无法保持90°的夹角,因此它们的电子对更倾向于分布在多个平面上。
实际预测下面是价层电子对互斥理论预测的分子形状表。
没有孤电子对电子对数1个孤电子对2个孤电子对3个孤电子对(基本形状)2直线型3平面三角形型角型4四面体型三角锥型角型5三角双锥型变形四面体型T字型直线型6八面体型四角锥型平面四方形型7五角双锥型五角锥型8四方反棱柱型分子类型分子形状中心原子价电子对的排布方式†分子的几何构型‡实例AX1En双原子分子(直线型)HF、O2AX2E直线型BeCl2、HgCl2、CO2AX2E1角型NO2−、SO2、O3AX2E2角型H2O、OF2AX2E3直线型XeF2、I3−AX3E平面三角形型BF3、CO32−、NO3−、SO3AX3E1三角锥型NH3、PCl3AX3E2T字型ClF3、BrF3AX4E四面体型CH4、PO43−、SO42−、ClO4−AX4E1变形四面体型SF4AX4E2平面四方形型XeF4AX5E三角双锥型PCl5AX5E1四角锥型ClF5、BrF5AX6E八面体型SF6AX6E1五角锥型XeOF5−、IOF52−[1]AX7E五角双锥型IF7AX8E四方反棱柱型XeF2−8†孤电子对以淡黄色球体表示。
价层电子对互斥理论

价层电子对互斥理论

109.5°
109.5°
104.5°
107.3°
107.3°
下列分子或离子中,空间构型为V型的是( ) A、CS2 B、H2Se C、HCN D、ICl
B
思考、讨论
思考、讨论
D D
A、NH4+ B、SO2 C、H3O+ D、OF2
3、下列分子和离子中,中心原子的价电子对几何构型为四面体,且分子(离子)空间构型为V形的是( )
杂化类型
sp
sp2
sp3
A的价电子空间构型
直线型
平面三角形
正四面体
对于ABm型分子或离子,其中心原子A的杂化轨道数恰好与A的价电子对数相等。
对于 ABm型分子或离子,其中心原子A的价电子对数可依如下公式算得:
1、推断分子空间构型的具体步骤:
2、ABm型分子的价电子对数n的确定
=
2
中心原子A的价电子数+配位原子B提供的价电子数×m ±离子电荷数
n
n
课堂练习
例3:计算下列分子或离子中的价电子对数,并根据已学填写下表
物质
价电子对数
中心原子杂化轨道类型
杂化轨道/电子对空间构型
轨道夹角
分子空间构型
键角
气态BeCl2
CO2
Hale Waihona Puke BF3CH4NH4+
H2O
NH3
PCl3
2
2
3
4
4
4
4
4
sp
sp
sp2
sp3
直线形
直线形
平面三角形
正四面体
180°
180°
120°
(1)对于主族元素,中心原子价电子数=最外层电子数,配位原子中氢或卤素原子提供价电子数为1;
价层电子对互斥理论

4 正四面体 2
V形
SP3
SO2
3 平面三角形 1
V形
SP2
小结: 价层电子对互斥模型
代表 中心原子 物 结合的原子数
CO2
2
中心原子
无孤对电子 CH2O
3
CH4
4
分子 类型
空间构型
AB2 直线形
AB3 平面三角形
AB4 正四面体Βιβλιοθήκη 中心原子 H2O2
AB2
V形
有孤对电子 NH3
3
AB3 三角锥形
化学式
原则:
±离子电荷数(
负 正
)]
①A的价电子数 =主族序数;
②配体X:H和卤素每个原子各提供一个价 电子,
规定 : 氧与硫不提供价电子;
③正离子应减去电荷数,负离子应加上电荷数。
•2、确定电子对的空间构型: n=2 直线形 n=3 平面三角形 n=4 正四面体 n=5 三角双锥 n=6 正八面体
•3、确定中心原子的孤对电子对数,推断 分子的空间构型。
HCN SO2 NH2- BF3 H3O+ SiCl4 CHCl3 NH4+ SO42-
中心原子 中心原子结 孤对电子数 合的原子数
空间构型
0
2
直线形
1
2
V形
2
2
V型
0
3
平面三角形
1
3
三角锥形
0
4
正四面体
0
4
四面体
0
4
正四面体
0
4
正四面体
基本要点:
•分子或离子的空间构型与中心原子的 价层电子对数目有关。
价层电子对=成键电子对+孤对电子对
【高中化学】高中化学知识点:价层电子对互斥理论

【高中化学】高中化学知识点:价层电子对互斥理论价层电子对互斥理论:1940年,美国sidgwicknv等人相继提出了价壳层电子对排斥理论(简称VSEPR方法),该理论适用于主族元素之间形成的abn类型分子或离子。
该理论认为,在共价分子或离子中,原子B(配位原子)围绕中心原子A的几何构型主要取决于中心原子价电子层中电子对之间的相互排斥。
这些电子对围绕中心原子尽可能远离彼此排列,以最小化彼此之间的排斥能。
所谓价电子对是指形成σ电子对和孤对键。
孤对电子的存在增加了电子对之间的斥力,影响了分子中的键角,并将改变分子构型的基本类型。
根据这一理论,只要已知分子或离子中中心原子上的价电子数,就可以轻松准确地判断ABn共价分子或离子的空间构型。
确定中心原子中价层电子对数:中心原子的价电子数与配体提供的公共电子数之和除以2即为中心原子的价电子对数。
规定:① 作为配体,卤素原子和氢原子提供一个电子,而氧元素的原子不提供电子;②作为中心原子,卤素原子按提供7个电子计算,氧族元素的原子按提供6个电子计算;③ 对于复合离子,在计算价电子的对数时,还应加上负离子的电荷数或减去正离子的电荷数;④计算电子对数时,若剩余1个电子,亦当作1对电子处理。
⑤ 双键、三键和其他多键被视为一对电子判断分子的空间构型:根据中心原子的价电子对数,从表1中找出相应的价电子对构型,然后根据价电子对中孤对电子的数量确定电子对的排列方式和分子的空间构型。
相关高中化学知识点:杂化轨道理论(中心原子杂化方式)混合轨道理论:是鲍林为了解释分子的立体结构提出的。
中心原子杂化轨道、孤电子对数及与之相连的原子数间的关系是:杂化轨道数=孤电子对数+与之相连的原子数。
杂化前后轨道总数比变,杂化轨道用来形成σ键或容纳孤对电子,未杂化的轨道与杂化轨道所在平面垂直,可用来形成π键。
常见的混合方法:(1)sp杂化:直线型如:co二、cs二(2)sp二杂化:平面三角形(等性杂化为平面正三角形)如:bcl三c二h四不等性杂化为v字型如:h二oh二sof二(3)sp三杂化:空间四面体(等性杂化为正四面体)如:ch 四、ccl四不等性杂化为三角锥如:nh三pcl三h三o+sp三d杂化:三角双锥服务提供商3d2混合体:八面体(与正八面体相等的混合体)分子的构型与杂化类型的关系:。
价层电子对互斥理论

目
间构型
对数
孤电子 对数
4
0
4
四面体
3
1
电子对的 排列方式
分子的 空间构型
四面体
三角锥
实例
CH4 CCl4 NH4+ SO42—
NH3 PCl3 SO32- H3O+
2
2
V—型
H2O
6
微粒
结构式
VESPR模型
HCN NH4+ H3O + SO2
HC N
H+ HNH
H
H+
O
H
H
OSO
F
BF3
B
F
F
分子或离子构型
7
化学式
HCN SO2 NH2- BF3 H3O+ SiCl4 CHCl3 NH4+
中心原子 孤对电子数
0 1 2 0
1 0 0 0
电子对数目
空间构型
2
直线形
3 V形
4 3
V形 平面三角形
4
三角锥形
4
正四面体
4
4
四面体
正四面体
8
1、下列物质中分子立体结构与水分子相似的是
A.CO2
B.H2S
B
C.PCl3
D.SiCl4
2、下列分子立体结构其中属于直线型分子的是
A.H2O
B.CO2
BC
C.C2H2
D.P4
3、下列分子立体结构其中属正八面体型分子的
A.H3O + C.PCl5
B.CO32— D.SF6
D
9
价层电子对互斥(VSEPR)理 论
价层电子对互斥(VSEPR)理论 ( Valence Shell Electron Pair Repulsion )
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
价层电子对互斥理论
价层电子对互斥理论(英文:V alence S hell E lectron P air R epulsion (VSEPR)),是一个用来预测单个共价分子形态的化学模型。
理论通过计算中心原子的价层电子数和配位数来预测分子的几何构型,并构建一个合理的路易斯结构式来表示分子中所有键和孤对电子的位置。
[编辑]理论基础
价层电子对互斥理论的基础是,分子或离子的几何构型主要决定于与中心原子相关的电子对之间的排斥作用。
该电子对既可以是成键的,也可以是没有成键的(叫做孤对电子)。
只有中心原子的价层电子才能够对分子的形状产生有意义的影响。
分子中电子对间的排斥的三种情况为:
∙孤对电子间的排斥(孤-孤排斥);
∙孤对电子和成键电子对之间的排斥(孤-成排斥);
∙成键电子对之间的排斥(成-成排斥)。
分子会尽力避免这些排斥来保持稳定。
当排斥不能避免时,整个分子倾向于形成排斥最弱的结构(与理想形状有最小差异的方式)。
孤对电子间的排斥被认为大于孤对电子和成键电子对之间的排斥,后者又大于成键电子对之间的排斥。
因此,分子更倾向于最弱的成-成排斥。
配体较多的分子中,电子对间甚至无法保持90°的夹角,因此它们的电子对更倾向于分布在多个平面上。
实际预测
下面是价层电子对互斥理论预测的分子形状表。
没有孤电子对(基本形状)1个孤电子对 2个孤电子对3个孤电子对
电子对数
2
直线型
3
平面三角形型角型
4
四面体型三角锥型角型
5
三角双锥型变形四面体型T字型直线型
6
八面体型四角锥型平面四方形型
7
五角双锥型五角锥型
8
四方反棱柱型
分子类
型分子形状
中心原子价电子对的排
布方式†
分子的几何
构型‡
实例
AX
1E
n
双原子分子
(直线型)
HF、O
2
AX
2E
直线型BeCl
2
、HgCl
2
、CO
2
AX
2E
1
角型NO
2
−、SO
2
、O
3
AX
2E
2
角型H
2
O、OF
2
AX
2E
3
直线型XeF
2
、I
3
−
AX
3E
平面三角形
型
BF
3
、CO
3
2−、NO
3
−、SO
3
AX
3E
1
三角锥型NH
3
、PCl
3
AX
3E
2
T字型ClF
3
、BrF
3
AX
4E
四面体型CH
4
、PO
4
3−、SO
4
2−、ClO
4
−
AX
4E
1
变形四面体
型
SF
4
AX
4E
2
平面四方形
型
XeF
4
AX
5E
三角双锥型PCl
5
AX
5E
1
四角锥型ClF
5
、BrF
5
AX
6E
八面体型SF
6
AX
6E
1
五角锥型XeOF
5
−、IOF
5
2−[1]
AX
7E
五角双锥型IF
7
AX
8E
四方反棱柱
型
XeF2−8
†孤电子对以淡黄色球体表示。
‡分子的实际几何构型,即不包含孤对电子的构型。
价层电子对互斥理论常用AXE方法计算分子构型。
这种方法也叫ABE,其中A代表中心原子,X或B代表配位原子,E代表孤电子对。
范例
甲烷分子(CH4)是四面体结构,是一个典型的AX4型分子。
中心碳原子周围有四个电子对,四个氢原子位于四面体的顶点,键角(H-C-H)为109°28'。
一个分子的形状不但受配位原子影响,也受孤对电子影响。
氨分子(NH3)中心原子杂化类型与甲烷相同(sp3),分子中有四个电子云密集区,电子云分布依然呈四面体。
其中三个是成键电子对,另外一个是孤对电子。
虽然它没有成键,但是它的排斥力影响着整个分子的形状。
因此,这是一个AX3E型分子,整个分子的形状是三角锥形,因为孤对电子是不可“见”的。
事实上,电子对数为七是有可能的,轨道形状是五角双锥。
但是它们仅存在于不常见的化合物之中,比如在六氟化氙中,有一对孤电子,它的构型趋向于八面体结构,因为孤对电子倾向于位于五角形的平面上。
另一个例子为七氟化碘,碘没有孤电子,七个氟原子呈五角双锥状排列。
电子对数为八也是有可能的,这些化合物一般为四方反棱柱体结构,[2]例子有八氟合氙酸亚硝酰中的 [XeF8]2−离子[3][4]以及八氰合钼(Ⅳ)阴离子 [Mo(CN)8]4−和八氟合锆(Ⅳ)阴离子 [ZrF8]4−。
例外
在一些化合物中VSEPR理论不能正确的预测分子空间构型。
过渡金属化合物
许多过渡金属化合物的几何构型不能用VSEPR理论解释,可以归结于价层电子中没有孤对电子以及核心的d电子与配体的相互作用。
[5]这些化合物的结构可以用VALBOND理论预测,包括金属氢化物和烷基配合物(例如六甲基钨),这个理论的基础是sd杂化轨道和三中心四电子键模型。
[6][7]晶体场理论是另一个经常可以解释配合物几何构型的理论。
IIA族卤化物
较重碱土金属的三原子卤化物的气相结构(例如:钙、锶、钡的卤化物,MX2)并不像预测的那样为直线型,而是V形。
(X-M-X的大致键角: CaF2,145°;SrF2,120°;BaF2,108°;SrCl2,130°;BaCl2,115°;BaBr2,115°;BaI2,105°).[8]格莱斯皮(Ronald Gillespie)提出这是因为配体与金属原子的内层电子发生相互作用,极化使得内层电子云不是完全球面对称,因此导致了分子构型的变化。
[5][9]
]一些AX2E2型分子
一个例子是氧化锂分子,即Li2O,它的中间构型是直线型而不是弯曲的,这一点可以归结于如果构型是弯曲的,锂原子之间将产生强烈的排斥作用。
[10]
另一个例子是O(SiH3)2(二甲硅醚)的Si-O-Si键的键角为144.1°,与其他分子中的键角相比差别较大,比如Cl2O (110.9°)、(CH3)2O (111.7°)以及N(CH3)3 (110.9°)。
格莱斯皮的合理解释是孤对电子的位置不同。
当配体的电负性与中心原子类似或更大时,孤对电子有能力排斥其他电子对,导致键角较小。
[5]当中心原子电负性较大时,就像O(SiH3)2中,孤对电子的定域不明显,排斥作用较弱,这种结合导致了强配体之间的排斥(-SiH3与上面的例子相比是一个比较大的配体)使得Si-O-Si键的键角比预想的要大。
[5]
一些形如AX6E1的分子
一些AX6E1型分子,例如含有Te(IV)或Bi(III)离子的化合物如TeCl62−、TeBr62−、BiCl63−、BiBr63−和BiI63−是正八面体结构;其孤对电子并不影响其构型[11]。
一种合理化解释是因为配体原子排列的拥挤没有给孤对电子留下空间[5];另一种合理化解释是惰性电子对效应。
[12]
与其他相关理论的对比
价层电子对互斥理论、价键理论和分子轨道理论都是关于分子如何构成的理论。
价键理论主要关注于σ键和π键的形成,通过研究受成键情况影响的轨道形状描述分子的形状。
价键理论也会借助VSEPR。
分子轨道理论则是关于原子和电子是如何组成分子或多原子离子的一个更精密的理论。
