附录1常用网络资源【高中化学】
高中化学教材目录--苏教版

高中【1】化学--苏教版目录·必修1 专题一化学家眼中的物质世界第一单元丰富多彩的化学物质第二单元研究物质的实验方法第三单元人类对原子结构的认识专题二从海水中获得的化学物质第一单元氯、溴、碘及其化合物第二单元钠、镁及其化合物专题三从矿物到基础材料第一单元从铝土矿到铝合金第二单元铁、铜的获取及应用第三单元含硅矿物与信息材料专题四硫、氮和可持续发展第一单元含硫化合物的性质和应用第二单元生产生活中的含氮化合物附录一相对原子质量表附录二常见酸、碱和盐的溶解性表(20℃)附录三中英文名词对照表元素周期表高中化学--苏教版目录·必修2专题一微观结构与物质多样性第一单元原子核外电子排布与元素周期律第二单元微粒之间的相互作用力第三单元从微观结构看物质多样性专题二化学反应与能量转化第一单元化学反应速率与反应限度第二单元化学反应中的热量第三单元化学能与电能的转化第四单元太阳能、生物质能和氢能的利用专题三有机化合物的获得与应用第一单元化石燃料与有机化合物第二单元食品中的有机化合物第三单元人工合成有机化合物专题四化学科学与人类文明第一单元化学是认识和创造物质的科学第二单元化学是社会可持续发展的基础附录一相对原子质量表附录二中英文名词对照表元素周期表高中化学--苏教版目录·选修1化学与生活专题一洁净安全的生存环境第一单元空气质量的改善第二单元水资源的合理利用第三单元生活垃圾的分类处理第四单元化学品的安全使用专题二营养均衡与人体健康第一单元提取人体必需的化学元素第二单元提供能量与营养的食物第三单元优化食物品质的添加剂第四单元造福人类的化学药物专题三丰富多彩的生活材料第一单元应用广泛的金属材料第二单元功能各异的无机非金属材料第三单元高分子材料和复合材料附录中英文名词对照表附录一相对原子质量表附录二常见酸、碱和盐的溶解性表(20℃)附录三生活饮用水水质标准附录四人体内常量元素和微量元素的含量附录五一些食物中的营养素含量附录六常见的食品添加剂附录七一些合成纤维的组成及特点元素周期表高中化学--苏教版目录·选修2化学与技术专题一多样化的水处理技术第一单元水的净化与污水处理第二单元硬水软化第三单元海水淡化专题二从自然资源到化学品第一单元氨的合成第二单元氯碱生产第三单元硫酸工业第四单元镁和铝的冶炼专题三让有机反应为人类造福第一单元有机药物制备第二单元合成洗涤剂的生产第三单元纤维素的化学加工第四单元有机高分子合成专题四材料加工与性能优化专题五为现代农业技术添翼2022年3月23日;第1页共3页专题六从污染防治到绿色化学附录一中英文名词对照表元素周期表高中化学--苏教版目录·选修3物质结构与性质专题一揭示物质结构的奥秘专题二原子结构与元素的性质第一单元原子核外电子的运动第二单元元素性质的递变规律专题三微粒间作用力与物质性质第一单元金属键金属晶体第二单元离子键离子晶体第三单元共价键原子晶体第四单元分子间作用力分子晶体专题四分子空间结构与物质性质第一单元分子结构与物质的性质第二单元配合物的形成和应用专题五物质结构的探索无止境附录一中英文名词对照表元素周期表高中化学--苏教版目录·选修4化学反应原理专题一化学反应与能量变化第一单元化学反应中的热效应第二单元化学能与电能的转化第三单元金属的腐蚀与防护专题二化学反应速率与化学平衡第一单元化学反应速率第二单元化学反应的方向和限度第三单元化学平衡的移动专题三溶液中的离子反应第一单元弱电解质的电离平衡第二单元溶液的酸碱性第三单元盐类的水解第四单元难溶电解质的沉淀溶解平衡附录一中英文名词对照表附录二常见酸、碱和盐的溶解性表(20℃)附录三难溶电解质的溶度积常数(25℃)附录四弱电解质在水中的电离平衡常数(25℃)元素周期表高中化学--苏教版目录·选修5 有机化学基础专题一认识有机化合物第一单元有机化学的发展与应用第二单元科学家怎样研究有机物专题二有机物的结构与分类第一单元有机化合物的结构第二单元有机化合物的分类与命名专题三常见的烃第一单元脂肪烃第二单元芳香烃专题四烃的衍生物第一单元卤代烃第二单元醇酚第三单元醛羧酸专题五生命活动的物质基础第一单元糖类油脂第二单元氨基酸蛋白质核酸附录一中英文名词对照表元素周期表高中化学--苏教版目录·选修6实验化学专题一物质的分离与提纯课题1 海带中碘元素的分离及检验拓展课题1-1 茶叶中某些元素的鉴定课题2 用纸层析法分离铁离子和铜离子拓展课题1-2 菠菜的叶绿体中色素的提取和分离拓展课题1-3 用粉笔进行层析分离课题3 硝酸钾晶体的制备拓展课题1-4 粗盐的提纯专题二物质性质的研究课题1 铝及其化合物的性质拓展课题2-1 铝热反应课题2 乙醇和苯酚的性质拓展课题2-2 苯酚与甲醛的反应专题三物质的检验与鉴别课题1 牙膏和火柴头中某些成分的检验拓展课题3-1 新装修居室内空气中甲醛浓度的检测拓展课题3-2 汽车尾气成分的检验课题2 亚硝酸钠和食盐的鉴别拓展课题3-3 真假碘盐的鉴别专题四化学反应条件的控制2022年3月23日;第2页共3页课题1 硫代硫酸钠与酸反应速率的影响因素拓展课题4-1 “蓝瓶子”实验课题2 催化剂对过氧化氢分解反应速率的影响拓展课题4-2 过氧化氢酶的催化作用拓展课题4-3 蔗糖的燃烧课题3 反应条件对化学平衡的影响拓展课题4-4 淀粉与碘显色现象的探究拓展课题4-5 压强对化学平衡的影响专题五电化学问题研究课题1 原电池拓展课题5-1 干电池模拟实验课题2 电解与电镀拓展课题5-2 阿佛伽德罗常数的测定拓展课题5-3 用铜电极电解饱和食盐水专题六物质的定量分析课题1 食醋总酸含量的测定拓展课题6-1 配制并标定氢氧化钠溶液课题2 镀锌铁皮镀锌层厚度的测定拓展课题6-2 水果中维生素C含量的测定专题七物质的制备与合成课题1 硫酸亚铁铵的制备拓展课题7-1 用制氢废液制备硫酸锌晶体课题2 阿司匹林的合成拓展课题7-2 对氨基苯磺酸的合成附录一实验规则附录二实验室安全守则附录三实验室事故的处理附录四常见酸、碱和盐的溶解性表(20℃)附录五常见指示剂附录六基本操作和气体发生装置图附录七误差和有效数字运算规则附录八元素的相对原子质量表附录九中英文名词对照表元素周期表2022年3月23日;第3页共3页。
2023-2024学年高中化学人教版(2023)必修第一册1.1.3 物质的转化 作业(解析版)

2023-2024学年高中化学人教版(2023)必修第一册1.1.3 物质的转化作业(解析版)第一章物质及其变化第一节物质的分类及转化课时作业第三课时物质的转化1.甲物质与强碱溶液反应只生成盐和水,甲一定不属于()A.酸B.盐C.金属单质D.氧化物【答案】C【解析】A.可能为酸,如盐酸与强碱反应生成盐和水,故A不选;B.可能为盐,如碳酸氢钠与NaOH反应生成盐和水,故B不选;C.不可能为金属单质,如Al与强碱反应生成盐和氢气,故C选;D.可能为氧化物,如二氧化碳与NaOH反应生成碳酸钠、水,故D不选;故选C。
2.物质之间的相互转化,可以直接实现,也可以间接实现,下列转化可以一步实现的是()A.B.C.D.【答案】C【解析】A.碳在氧气中燃烧生成二氧化碳,二氧化碳通入石灰水中生成碳酸钙,C不能直接反应产生CaCO3,A不符合题意;B.CuO难溶于水,与水也不发生反应,氧化铜不能直接反应产生Cu(OH)2,B不符合题意;C.Fe与CuSO4发生置换反应产生Cu和FeSO4,可以一步实现上述转化,C符合题意;D.CaCO3高温煅烧反应产生CaO 和CO2,二氧化碳与碳高温下反应生成一氧化碳,碳酸钙不能直接反应转化为CO,D不符合题意;故合理选项是C。
3.X、Y、Z、W各代表一种物质,若X+Y=Z+W,则X和Y的反应不可能是( )A.盐和盐的反应B.碱性氧化物和水的反应C.酸与碱的反应D.酸性氧化物和碱的反应【答案】B【解析】A. 盐和盐反应能生成两种新盐,故A正确;B. 碱性氧化物和水的反应生成相应的碱,只生成一种物质,故B错误;C. 酸和碱反应生成盐和水,故C正确;D. 碱和酸性氧化物反应生成盐和水,故D正确;故选B。
4.化学概念有包含、并列、交叉等不同关系,下列选项符合如图所示关系的是()A B C DX 分解反应化合物物理变化化学反应Y 氧化还原反应混合物化学变化置换反应【答案】A【解析】右图所示关系是交叉关系。
高中化学常见物质及应用

高中化学常见物质及应用高中化学常见物质及其应用:一、无机化合物:1. 水(H2O):水是一种无机化合物,常见于生活中。
它有很多应用,包括饮用、煮饭、清洗、浇灌植物等。
此外,水也是化学反应中的重要参与物,许多反应都需要水作为溶剂。
2. 氧气(O2):氧气是一种气体,在空气中占据很大比例。
它可以用于人类呼吸、火的燃烧和细胞呼吸等生物过程中。
此外,氧气还可以用于氧疗、高效燃烧和氧化反应等许多实验和工业应用中。
3. 二氧化碳(CO2):二氧化碳在大气中也很常见,是一种重要的温室气体。
它还可以用于饮料制作中的注气、灭火装置、气泡发生器等应用。
4. 氯化钠(NaCl):氯化钠是食盐的化学名。
它是一种普遍使用的调味品,用于食品的烹饪和保存。
此外,氯化钠还可以用于净水、制氯和防腐剂等。
5. 重要金属:铁、铜、锌等金属常见于生活中,具有广泛的应用。
铁可用于建筑、制造机械和生产钢铁。
铜可用于电气导线、水管和制作乐器等。
锌可用于镀锌、蓄电池和合金制造等。
6. 硫酸(H2SO4):硫酸是一种强酸,广泛用于实验室和工业领域。
它可用于制作化肥、染料、肥皂和清洗剂等。
7. 氨气(NH3):氨气是一种具有刺激性气味的无色气体。
它可用于制作氮肥、清洗剂、合成纤维等。
8. 氧化铜(CuO):氧化铜是一种黑色固体,可用于制作铜盐、颜料、导电材料等。
二、有机化合物:1. 葡萄糖(C6H12O6):葡萄糖是一种常见的单糖,是人类和其他生物的重要能量来源。
它还用于食品加工、饮料制作和制药工业。
2. 乙醇(C2H5OH):乙醇是一种无色液体,广泛应用于食品饮料、消毒剂、溶剂等。
3. 甘油(C3H8O3):甘油是一种可溶于水的有机液体,主要用于制造肥皂和面霜等化妆品。
4. 丙酮(C3H6O):丙酮是一种无色液体,具有良好的溶剂性,可用于涂料、塑料和胶水的制造。
5. 苯(C6H6):苯是一种无色液体,具有特殊的芳香气味。
它是合成塑料、橡胶、染料和药物的重要原料。
化学学科网络资源网址大全

化学学科网络资源网址大全国内站点化学通报/人教社/中学化学/huaxue/index.htm先得化学教学资源网/化学试题集/hxstj/化学领域多来米站/化学工场/清华附中中学生化学学习/chem2/index.htm化学走廊/化学教学资源网/化学加油站(图片库)广州育才中学化学园/中科院计算机化学开放实验室http://202.127.145.116/无机化学网/~jaechu/无机化学专业网/化学天地/~inorg/电气化学科技信息资源(ESTIR)/estir/大方题库/tihai/化学化工天地/化苑在线/化学作用.hk/~chemmag/化学资讯网.tw/台湾理化学园http://163.18.153.5/pcschool/国际化学品安全卡数据库(中文版)/icsc/中国化学化工网/hxjyphp/hxjy.php深圳中学化学之梦/huaxue/中学化学虚拟教研中心电子刊物/dzkw/index.htm高考热讯/化学/xuexiyd/huaxue/huaxue.htm化学岛/化学世界http://202.110.195.89/chemworld/index.asp中国化工网/环境水化学实验室/skleac/教育资讯站化学网t.hk/教育教学论文网/gb/art/ttd/index.asp元素周期表/教师中心论文会萃/teach/teacher/lunwen/中国化学周报(英文版)China Chemical Week /化学信息网(ChIN)/国外站点美国化学会主页/ortal/chemistry英国皇家化学会主页/新加坡迈阿米科学博物馆/美国化学协会/化学教育资源/divisions/artscience/chemistry/books/非金属元素入门/education/ot ... ducation/chemistry/ 高中化学教材/chem TeamIndex.html化学教育家/chedr/华美化学学会/~cacs/化学工程学的历史/history//h_intro.html诺贝尔化学奖(Nobel Prizes in Chemistry)http://userpage.chemie.fu-berlin ... nobel_chemie_e.html国际网上化学学报/化学工程杂志(Chemical Engineering Magazine) /加拿大化学会/化学在线/Nist化学分子资料库/化学与环境研究/c/index.htm化学因特网杂志(Internet Journal of Chemistry) /化学物理学杂志(Journal of Chemical Physics) /jcpo/美国化学制品图.jm:1104/lectures/top50.html 化学虚拟图书馆.chempointers.html工具网站化学之门/CHEW: Chemistry Higher Education Workgroup中国化学软件网/中学化学课件网/index.htm中学化学/jxzyk/html/hxzy.htm重要化学化工资源导航/化学品安全网/化学软件/化学联盟/hxstj/pw/dg/pick/index.asp化学索引http://www.chemie.fu-berlin.de/chemistry/化学药品/生物软件网/个人主页化学园丁园/k12/飞翔化学网/chemfly/化学教师手记/张矫睦主页/mscx/2001jiaomu/index.htm郭峰初中化学教师园地/ed/down.cgi刘彦民的化学园地/于生化学网姚有为中学化学诗歌/长沙市一中林老师的化学园/焦王化学/吴渊源化学资料库.tw/~iywu/小刚化学园地/生命化学与化学/化学猎人/chemhuman/index.htm杨帆教育天地/?sohu=yes闪闪中学化学网/江汉化学之窗/yalyn/index1.html安之家化学教育资源网/anzhihome/斗门中学化学资源网/etsnoopy/chemdz/index.html化学园丁网/绿树学园/main.htm化学俱乐部/万州化学/?sohu=yes化学乐园/hgc79224/e代化学教学资源网/dybdxh/中学化学课堂/wushishu/中学化学教与学/中学应用化学网/grzy/zbg/化学在线/tuotuo/ChemistryOnline/Index.html化学(试题)园地/chemfield/化学的魔法乐园/babystar/论坛K12虚拟社区/化学生物论坛/forums/list.php3?num=33先得虚拟教研中心/雅虎化学俱乐部/chemdoor/gotourl.asp?url=http%3A%2F%2Fdir%2Eclubs%2Eyahoo%2Ecom%2Fscience%2Fchemistry%2F&id=351化学之约/hxzj/bbs/bbs.cgi?id=200105111451化学村/中基网/化学在线/cbebbs/upload/forumdisplay.php?forumid=42化学在线答疑/fcgi-bin/ ... =jiangxl&page=1棠湖中学化学在线答疑/bbs/show.asp?category=huaxue_zjxx。
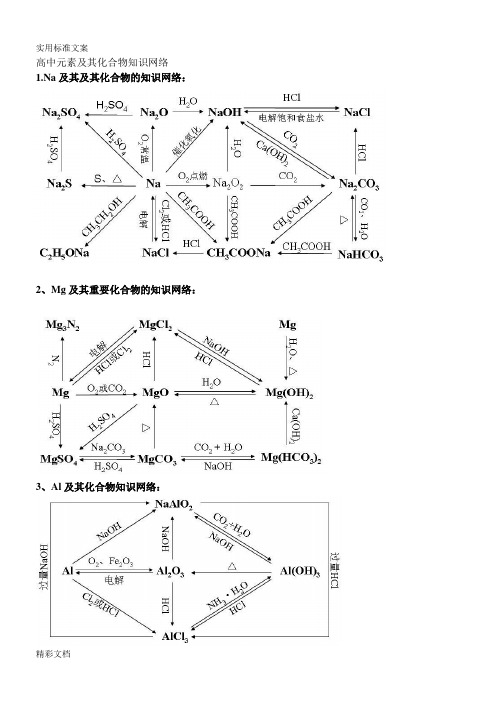
高中化学元素及其化合物知识网络
化学平衡、化学
(平衡标志的判断) 变 条件改变,平衡状态改变
反应速率
影响化学平衡因素
浓度 压强 温度
平衡移动原理 (勒沙特列原理)
精彩文档
实用标准文案
化 合 物
精彩文档
强电解质(完全电离 )AB A-+B-
电
( 弱部
电离平衡 AB
A-+B-
电离度的定义
※表示单质或化合物的化学用语:化学式、结构式、结构简式、电子式等
实用标准文案
色、态、味 溶解度、熔点、沸点 密度、硬度、导电性
导热性、塑性
精彩文档
元素
游离态 单质 化合物
物理性质 宏观
组
金属性、非金属性
氧化性、还原性 酸性、碱性
稳定性、可燃性
化学性质 纯净物
单质 化合物
金属 非金属 稀有气体
分类
实用标准文案 精彩文档
芳香烃(苯和苯的同系物)CnH2n-6(n≥6)
R
卤代烃(官能团:—X):饱和一卤代烃 CnH2n+1X(n≥1)R—X
醇 (官能团:—OH):饱和一元醇 CnH2n+1OH(n≥1)R—OH
实用标准文案 精彩文档
H2O+O2+4e→4OH-(中性、弱酸性 条件下的吸氧腐蚀)
电解池
电能→化学能 (在电流作用下两极分别发生氧化还原反应)
外电路必须有直流电源;两极材料均 能导电即可
阴极——连接电源负极
阳极——连接电源正极
e
e
电源负极→阴极
电源正极→阳极
还原
还原
阴极:2H++2e→H2↑或 M n++ne→M
高中化学主题1空气资源氨的合成课题2氨的工业合成课件鲁科版

合成氨的生产工艺及原料气的制备
【问题导思】
①合成氨生产中需要的原料气是什么? 【提示】 氮气和氢气。 ②如何获得合成氨原料气? 【提示】 获得 N2 的方法:来自空气,分离方法有深冷分离、变压吸附分 离、分离膜分离。获得 H2 的方法:电解水、由煤或焦炭制 H2、由天然气或重油 制 H2。 ③如何能提高合成氨工业中原料气的利用率? 【提示】 使平衡正向移动:加压、不断分离出 NH3、将 N2、H2 循环利用。
1.在合成氨反应 N2+3H2 2NH3 中,在下列情况下,不能使化学反应速
率增大的是( )
A.加入氮气
B.加入合适的催化剂
C.减小压强,扩大容器体积 D.适当升高温度 【解析】 加快反应速率的外界条件有:升高温度、增大压强(有气体参加
的反应)、增大反应物浓度、使用催化剂等。
【答案】 C
2.下列有关合成氨工业的叙述,可用勒·夏特列原理来解释的是 ( ) 【导学号:28920006】
2.评价上述几种制氢方法,你认为哪种方法是最佳选择? 【提示】 电解水制氢气,电能消耗大,成本高;天然气与煤相比较,天
然气输送方便、投资省、能耗低。所以用天然气做合成氨的原料为最佳选择。
怎样利用未转化的氮气和氢气
在实际生产中采用了循环法,先通过冷凝把_氨___从合成塔出来的混合气中 分离出来,余下未反应的__氮__气__和__氢__气__的混合气用循环压缩机重新送入合成 塔进行反应,同时不断地补充新鲜的原料气,这样氨的合成就形成了一个循环 流程,使氮气和氢气得到充分利用。
(2)压强:无论从反应速率还是化学平衡考虑,压强越大越有利于合成氨。 但压强太大,动力消耗大,设备的质量和制造水平要求高,故必须综合考虑。 目前我国合成氨厂一般采用的压强在 20~50 MPa 之间。
必修一化学教辅资料电子版

必修一化学教辅资料电子版# 必修一化学教辅资料## 目录1. 化学基本概念2. 物质的分类3. 化学键与分子结构4. 化学反应的类型5. 化学方程式的书写与平衡6. 化学计量学基础7. 溶液与溶质8. 气体定律9. 化学实验基本操作10. 化学计算例题解析11. 化学知识拓展## 1. 化学基本概念化学是一门研究物质的组成、性质、变化以及伴随这些变化的能量变化的科学。
它涉及到原子、分子、离子等微观粒子,以及它们之间的相互作用。
## 2. 物质的分类物质可以根据其组成和性质被分为混合物和纯净物。
纯净物又可以进一步分为单质和化合物。
单质是由同种元素组成的物质,而化合物是由不同元素以一定比例结合形成的物质。
## 3. 化学键与分子结构化学键是原子之间相互作用的结果,包括离子键、共价键和金属键。
分子结构描述了分子中原子的排列方式和化学键的类型。
## 4. 化学反应的类型化学反应可以根据反应物和生成物的类别进行分类,如合成反应、分解反应、置换反应和复分解反应等。
## 5. 化学方程式的书写与平衡化学方程式是表示化学反应的化学符号表达式。
书写化学方程式时,需要遵循原子守恒原则,并通过平衡系数使反应物和生成物的原子数相等。
## 6. 化学计量学基础化学计量学是研究化学反应中物质量的科学。
它涉及到摩尔的概念、摩尔质量、物质的量浓度等。
## 7. 溶液与溶质溶液是由溶质和溶剂组成的均匀混合物。
溶质可以是固体、液体或气体,而溶剂通常是液体。
## 8. 气体定律气体定律描述了气体体积、压力和温度之间的关系。
包括波义耳定律、查理定律和理想气体定律等。
## 9. 化学实验基本操作化学实验是化学学习的重要组成部分。
基本操作包括实验器材的准备、实验步骤的执行以及实验结果的记录和分析。
## 10. 化学计算例题解析化学计算是理解和应用化学知识的重要手段。
本章节将提供一系列化学计算的例题,包括物质的量计算、浓度计算、化学反应限度的计算等。
普通高中化学课程标准附录

• 6.简单配合物的制备 • 7.乙酸乙酯的制备与性质 • 8.有机化合物中常见官能团的检验 • 9.糖类的性质
感谢聆听观看!
梳理2 小组合作,利用性质图示,梳理从自然 界中的氯到生活中的氯,再到环境中的 氯的转化路径,讨论含氯物质的安全使 用措施。组间汇报交流
发展病诊断学生认识物质转化关系 的水平,结合物质性质,从动态转 化的视角对在真实情景中的元素转 化关系进行整体分析和说明
4.问题解决和展示
【学习任务4】真实问题解决方案的设计和交流,在线展示改进后的方 案并相互评价。
【案例说明】
1.1.线上线下结合,突破学习场域 2.单元整体设计,实现深度学习 3.活动层层递进,发展核心素养 4.思路方法外显,促进自主迁移
附录3
学生必做实验索引
必修课程学生必做实验
1.配制一定物质的量浓度的溶液
6.化学反应速率的影响因素
2.铁及其化合物的性质
7.化学能转化成电能
3.不同价态含硫物质的转化
元素视角:化合价
微粒视角:电子
原因
有化合价变化
有电子转移
代数和为0 表现
代数和为0
3.问题解决 【学习任务4】运用氧化还原反应原理,设计并讨论汽车尾气绿色化处理方案。 【评价任务4】诊断并发展学生对化学价值的认识水平(学科价值视角、社会价值 视角、学科和社会价值视角)。
展示:
汽车尾气污染处理视频
真实情境素材
【学习任务3】讨论、汇报对含氯物质转化关系的梳理情况。
【评价任务3】发展学生认识物质及其转化的思路水平(孤立水平、系统水平)。
学生活动
梳理1 组合实验过程和结论,梳理本节课学习 的氯气和部分含氯物质的性质,小组合 作,用图示梳理结果。组间汇报交流
化学资源

一、网址类,主要包括一些虫友推荐的学化学常用的网址,也包括一些学校的网络课程资源:最全的化学网站厦门大学理科化学系列网络课程建立一个类似hao123的化学网址之家,建设完善中.....分享科研动态与无机化学资源网博士最应该去的10大优秀网站物质性质查询网站汇总图谱数据库一个可以查化学实验常用数据的网站(学化学的错过了可惜)很不错的化学门户网站比较全的化学化工资源北京化工大学物理化学网上精品课推荐可以搜索下载原版外文书的几个网站推荐一个网页:很多期刊的链接一个不错的综述网站二、书刊类,中英文的,包括教材和辅导书,工具书等:1、物理化学:傅献彩《物理化学》(第五版)电子书+课件《物理化学》—傅献彩全上下册《物理化学》天大第二版+第四版分享胡英版《物理化学》《物理化学词典》分享《表面活性剂物理化学》《表面物理化学》W.Adamson和Alice P. Gast合著的中文翻译版《吸附、比表面积与孔隙率》中英文的共同分享《界面及胶体化学》一共六本《表面活性剂作用原理》《计算物理化学》天津大学《物理化学》第四版习题解答【经典物化教材配套解答】《物理化学教学与学习指南》—胡英院士《物理化学》(第四版)配套习题解答《物理化学重点热点导引与解题训练》(傅玉普编写)《物理化学学习指导》沈文霞等编《物理化学解题思路和方法》《物理化学解题指导》—黄绿书《Algebraic Theory of Molecules (Topics in Physical Chemistry Series)》《Instant Notes in Physical Chemistry》《Physical Chemistry-8th By Peter Atkins》djvu格式Springer新书《Physical Chemistry in Depth》《Physicochemical calculations》2、无机化学《21世纪的无机化学》《高等无机化学》《高等无机化学》[美]F.A.科顿著《高等无机化学》中国科学技术大学—郑化桂《高等无机化学》华东理工的《高等无机化学》[英]R.B.赫斯洛普K.琼斯著《无机化学》武汉大学、吉林大学第三版下载经典版本《无机化学》【北师大等校合编第四版】上下册全电子版《无机化学》经典习题答案两套【北师、华师、南师&武大、吉大】《无机化学习题》中科大张祖德【附答案】《无机化学》英文原版书籍免费下载《Advanced Inorganic Chemistry》Third Edition《Advances in Inorganic Chemistry》Volume 61Inorganic Chemistry 1962-2008《Inorganic synthesis》(无机合成经典书籍)《N4-Macrocyclic Metal Complexes》Springer book 《Nomenclature of Inorganic Chemistry: Recommendations》3、手册词典:《常用化学反应速查手册》《化学化工实验师手册》珍藏版下载《兰氏化学手册》(电子版,可检索)《物理化学词典》分享《无机化合物合成手册》全三卷(新增链接)《现代化学试剂手册》全六册《现代化学手册》书籍分享《蓄电池手册》《中国大百科全书-化学》《Encyclopedia of Chemical Physics and Physical Chemistry》pdf 《Handbook of Inorganic Electrochromic Materials》《Handbook of Surface and Colloid Chemistry》3rd EdCRC《Handbook of Chemistry and Physics》89th EditionCRC《Handbook of Chemistry and Physics 》(2007)4、合辑类:史上最全化学类资源和丛书化学资源大放送,如果您认为对你有用,那就给点支持,资源有点长83本经典英文化学书籍免费下载光化学、电致、光致发光书籍及ChemicalReview专刊中英文经典《Advanced Organic Chemistry》书籍大全—8本书籍共享【亲自整理30多本】5、其它中文书籍:《第十三届亚洲化学大会论文摘要集》《最为详尽的实验室无水无氧操作》《现代仪器分析方法》华东理工大学《化学热力学基础》《化学动力学基础》《基础元素化学》PDF下载格林伍德经典《元素化学》,英文版+中文版,识货的进!《量子化学》陈光巨,黄元河主编高清晰版《量子化学》中文译本[美]IRAN.LEVINE《量子化学—基本原理和从头计算法题解》两本电子书共享《普通化学原理(第二版)》《生物化学技术原理及其应用》第三版《海洋涂料与涂装技术》武汉科大《有机化学基础实验》pdf《计算机在化学中的应用》《群论基础及其化学作用》《分子对称性群》《化学哲学》National geographic《爱情是化学作用》(英文版)分享最新一期《科学美国人》好东西不容错过自然-化学(Natural Chemistry)电子杂志(每月更新,配图)6、其它英文书籍:《Adaptronics and Smart Structures》《Adaption of Simulated Annealing to Chemical Optimization Problems》《Advanced Chemistry of Monolayers at Interfaces》Volume 14《Anion Receptor Chemistry》《Bioinorganic Vanadium Chemistry》《Boronic Acids》—Google口碑不错,科研助手:硼酸《Careers in Science and Engineering A Student Planning》做科研不读后悔的书《Characterization and Chemical Modification of the Silica Surface》《Chemically Reacting Flow: Theory and Practice》《Chemistry and Chemical Reactivity》6th Ed《Chemistry of Heterocyclic Compounds》Volumes1-42Chemistry: The Impure Science《Container Molecules (Monographs in Supramolecular Chemistry)》《Controlled Assembly and Modification of Inorganic Systems》吴新涛院士《Cyanide in Water and Soil: Chemistry, Risk, and Management》《Data Analysis for Chemistry》《Electrochemical Sensor Analysi》Volume 49全书下载《Encyclopedia of the Elements》《Formulation Technology: Emulsions, Suspensions, Solid Forms》《Future of Glycerol: New Usages for a Versatile Raw Material》(RSC新书) 《High Pressure Chemistry: Synthetic, Mechanistic, and Supercritical Applications》《High Pressure Effects in Biophysics and Enzymology》《High Pressure Geochemistry & Mineral Physics》Volume 9《Hydrogen Energy: Challenges and Prospects》(RSC Energy Series) 《Inorganic Synthesis》《Nitrides with Nonpolar Surfaces: Growth, Properties, and Devices》《Particles in water: properties and processes》《Polyoxometalate Chemistry: From Topology via Self-Assembly to Applications》《Practical Skills in Chemistry》《Photoacoustic Infrared Spectroscopy》《Reactive Hydrocarbons in the Atmosphere》《The Mathematics of Diffusion》《The Public Image Of Chemistry》《Why Carbon Fuels Will Dominate the 21st Century Energy Economy》《Write Like a Chemist: A Guide and Resource》三、课件类:中科大物理化学课件天津大学物理化学第五版课件PPT物理化学之电解质理论印永嘉第四版的简明物理化学教程PPT物理化学课件PDF版本-华东理工国家精品课程大学物理化学全套课件《表面活性剂应用大全》分享《界面化学课件》北京大学无机化学课件PPT无机合成与制备化学PPT《高等无机化学》吉林大学无机研究生课件朱文祥《配位化学》—2009年春季学期在中科院任教时用的课件《配位化学》课件《配位化学》课件—哈尔滨工程大学《配位化学》讲义—超分子的基础之一南京大学《配位化学》课件有机化合物的命名超级经典课件《表面现象与分散系统》课件结构化学课件五大化学课件(整理版)化学信息学经典课件美国顶级化学家Laisheng Wang 课件四、考试资源类:武汉大学物理化学历年真题(2000-2007)09年中科院物理化学(甲)清晰版中科院2008年物理化学试题(甲)物理化学经典题目物理化学考研课件pdf格式厦门大学2005年物理化学课考研重点笔记扬州大学物理化学考研吉林大学物化习题集物理化学考研复习指南(pdf版)下载物化急感,助你学物化物理化学思考题答案——傅献彩物理化学习题及答案北航物理化学本科生基础考试题南开大学2000年分析化学考研试题综合化学—中山大学2006年硕士研究生入学考试试题1995复旦大学有机试题及答案无机化学精品教案和习题全国第五届化学实验竞赛笔试试题及答案五、视频资源类,包括仪器操作和教学视频等:物理化学实验常用仪器操作教学视频无机几个基本实验视频操作石油大学的物理化学视频教程化学实验基本仪器操作视频清华大学朱文涛教授物理化学视频下载大学化学化工基本实验操作视频指南(非常齐全)麻省理工学院MIT【化学热力学&动力学】全套视频课程迅雷下载六、其它资源,主要是一些包含上面两种以上的资源,致使不好分类的:我的namipan空间有大量珍贵资源,欢迎大家取用科技英语写作(南开大学化学院)最权威的Plackett-Burman实验问答实验室的化学安全与注意事项+实验室常用溶液配制化学实验室仪器操作规程无机化学网上课程收集(几十个学校,课件和视频免费看和下载)中科院的一个FTP电负性元素周期表元素周期表的小软件真空手套箱资料实验室最危险的17种物质实验室安全知识和健康保护实验室安全知识和健康保护课件实验室致癌物质和诱发畸变物质实验安全血的教训四氟乙烯的毒性和致癌性2009化综类中文期刊目录化学词汇中英对照=非常全纯物质化学性质查询软件、粒径分布计算oringin说明书Mestrec4999使用教程湖北大学版化学专业英语命名攻略各种玻璃及常用仪器图(包括一些分子结构图)共379幅(无重复。
【人教版】2019年秋高中化学必修1:全册知识点整理与归纳(完整版)

高一化学必修1知识点综合第|一章从实验学化学一、常见物质的别离、提纯和鉴别1.常用的物理方法- -根据物质的物理性质上差异来别离. 混合物的物理别离方法i、蒸发和结晶蒸发是将溶液浓缩、溶剂气化或溶质以晶体析出的方法.结晶是溶质从溶液中析出晶体的过程,可以用来别离和提纯几种可溶性固体的混合物.结晶的原理是根据混合物中各成分在某种溶剂里的溶解度的不同,通过蒸发减少溶剂或降低温度使溶解度变小,从而使晶体析出.加热蒸发皿使溶液蒸发时、要用玻璃棒不断搅动溶液,防止由于局部温度过高,造成液滴飞溅.当蒸发皿中出现较多的固体时,即停止加热,例如用结晶的方法别离NaCl和KNO3混合物.ii、蒸馏蒸馏是提纯或别离沸点不同的液体混合物的方法.用蒸馏原理进行多种混合液体的别离,叫分馏.操作时要注意:①在蒸馏烧瓶中放少量碎瓷片,防止液体暴沸.②温度计水银球的位置应与支管底口下缘位于同一水平线上.③蒸馏烧瓶中所盛放液体不能超过其容积的2/3 ,也不能少于l/3 .④冷凝管中冷却水从下口进,从上口出.⑤加热温度不能超过混合物中沸点最|高物质的沸点,例如用分馏的方法进行石油的分馏. iii、分液和萃取分液是把两种互不相溶、密度也不相同的液体别离开的方法.萃取是利用溶质在互不相溶的溶剂里的溶解度不同,用一种溶剂把溶质从它与另一种溶剂所组成的溶液中提取出来的方法.选择的萃取剂应符合以下要求:和原溶液中的溶剂互不相溶;对溶质的溶解度要远大于原溶剂,并且溶剂易挥发.在萃取过程中要注意:①将要萃取的溶液和萃取溶剂依次从上口倒入分液漏斗,其量不能超过漏斗容积的2/3 ,塞好塞子进行振荡.②振荡时右手捏住漏斗上口的颈部,并用食指根部压紧塞子,以左手握住旋塞,同时用手指控制活塞,将漏斗倒转过来用力振荡.③然后将分液漏斗静置,待液体分层后进行分液,分液时下层液体从漏斗口放出,上层液体从上口倒出.例如用四氯化碳萃取溴水里的溴.iv、升华升华是指固态物质吸热后不经过液态直接变成气态的过程.利用某些物质具有升华的特性,将这种物质和其它受热不升华的物质别离开来,例如加热使碘升华,来别离I2和SiO2的混合物.2、化学方法别离和提纯物质对物质的别离可一般先用化学方法对物质进行处理,然后再根据混合物的特点用恰当的别离方法(见化学根本操作)进行别离.用化学方法别离和提纯物质时要注意:①最|好不引入新的杂质;②不能损耗或减少被提纯物质的质量③实验操作要简便,不能繁杂.用化学方法除去溶液中的杂质时,要使被别离的物质或离子尽可能除净,需要参加过量的别离试剂,在多步别离过程中,后加的试剂应能够把前面所参加的无关物质或离子除去.对于无机物溶液常用以下方法进行别离和提纯:(1 )生成沉淀法(2 )生成气体法(3 )氧化复原法(4 )正盐和与酸式盐相互转化法(5 )利用物质的两性除去杂质(6 )离子交换法常见物质除杂方法3、物质的鉴别物质的检验通常有鉴定、鉴别和推断三类,它们的共同点是:依据物质的特殊性质和特征反响,选择适当的试剂和方法,准确观察反响中的明显现象,如颜色的变化、沉淀的生成和溶解、气体的产生和气味、火焰的颜色等,进行判断、推理.①常见气体的检验②几种重要阳离子的检验(l )H +能使紫色石蕊试液或橙色的甲基橙试液变为红色.(2 )Na +、K +用焰色反响来检验时,它们的火焰分别呈黄色、浅紫色(通过钴玻片) .(3 )Ba2 +能使稀硫酸或可溶性硫酸盐溶液产生白色BaSO4沉淀,且沉淀不溶于稀硝酸.(4 )Mg2 +能与NaOH溶液反响生成白色Mg(OH)2沉淀,该沉淀能溶于NH4Cl溶液.(5 )Al3 +能与适量的NaOH溶液反响生成白色Al(OH)3絮状沉淀,该沉淀能溶于盐酸或过量的NaOH溶液.(6 )Ag +能与稀盐酸或可溶性盐酸盐反响,生成白色AgCl沉淀,不溶于稀HNO3 ,但溶于氨水,生成[Ag(NH3)2]+ .(7 )NH4 +铵盐(或浓溶液)与NaOH浓溶液反响,并加热,放出使湿润的红色石蓝试纸变蓝的有刺激性气味NH3气体.(8 )Fe2 +能与少量NaOH溶液反响,先生成白色Fe(OH)2沉淀,迅速变成灰绿色,最|后变成红褐色Fe(OH)3沉淀.或向亚铁盐的溶液里参加KSCN溶液,不显红色,参加少量新制的氯水后,立即显红色.2Fe2 + +Cl2=2Fe3 + +2Cl-(9 ) Fe3 +能与KSCN溶液反响,变成血红色Fe(SCN)3溶液,能与NaOH溶液反响,生成红褐色Fe(OH)3沉淀.(10 )Cu2 +蓝色水溶液(浓的CuCl2溶液显绿色) ,能与NaOH溶液反响,生成蓝色的Cu(OH)2沉淀,加热后可转变为黑色的CuO沉淀.含Cu2 +溶液能与Fe、Zn片等反响,在金属片上有红色的铜生成.③几种重要的阴离子的检验(1 )OH-能使无色酚酞、紫色石蕊、橙色的甲基橙等指示剂分别变为红色、蓝色、黄色.(2 )Cl-能与硝酸银反响,生成白色的AgCl沉淀,沉淀不溶于稀硝酸,能溶于氨水,生成[Ag(NH3)2] + .(3 )Br-能与硝酸银反响,生成淡黄色AgBr沉淀,不溶于稀硝酸.(4 )I-能与硝酸银反响,生成黄色AgI沉淀,不溶于稀硝酸;也能与氯水反响,生成I2 ,使淀粉溶液变蓝.(5 )SO42-能与含Ba2 +溶液反响,生成白色BaSO4沉淀,不溶于硝酸.(6 )SO32-浓溶液能与强酸反响,产生无色有刺激性气味的SO2气体,该气体能使品红溶液褪色.能与BaCl2溶液反响,生成白色BaSO3沉淀,该沉淀溶于盐酸,生成无色有刺激性气味的SO2气体.(7 )S2-能与Pb(NO3)2溶液反响,生成黑色的PbS沉淀.(8 )CO32-能与BaCl2溶液反响,生成白色的BaCO3沉淀,该沉淀溶于硝酸(或盐酸) ,生成无色无味、能使澄清石灰水变浑浊的CO2气体.(9 )HCO3-取含HCO3-盐溶液煮沸,放出无色无味CO2气体,气体能使澄清石灰水变浑浊或向HCO3-盐酸溶液里参加稀MgSO4溶液,无现象,加热煮沸,有白色沉淀MgCO3生成,同时放出CO2气体.(10 )PO43-含磷酸根的中性溶液,能与AgNO3反响,生成黄色Ag3PO4沉淀,该沉淀溶于硝酸.(11 )NO3-浓溶液或晶体中参加铜片、浓硫酸加热,放出红棕色气体.二、常见事故的处理汞滴落在桌上或地上应立即撒上硫粉三、化学计量①物质的量定义:表示一定数目微粒的集合体符号n 单位摩尔符号 mol23微粒与物质的量N公式:n =NA②摩尔质量:单位物质的量的物质所具有的质量用M表示单位:g/mol 数值上等于该物质的分子量质量与物质的量m公式:n =M③气体摩尔体积:物质的聚集状态 (1 ) 影响物质体积大小的因素有:①微粒数目;②微粒大小;③微粒之间的距离 . (2 ) 对于固态或液态物质 ,影响其体积的主要因素是微粒的数目和微粒的大小;对于气态物质 ,影响其体积的主要因素是微粒的数目和微粒间距离 . (3 ) 对于一定量的气体 ,影响其体积的因素是温度和压强 . 温度一定 ,压强越大 ,气体体积越小 ,压强越小 ,气体体积越大;压强一定 ,温度越高 ,气体体积越大 ,温度越低 ,气体体积越小 .(1 )气体摩尔体积单位物质的量的气体所占的体积叫做气体摩尔体积 .气体摩尔体积的符号为Vm ,单位为L·mol-1 ,气体摩尔体积的表达V公式:n =Vm在标准状况下 (0℃ ,101kPa ) ,气体摩尔体积Vm≈22.4 L·mol-1也就是说1mol任何气体的体积都约为22.4L .这里的气体可以是单一气体 ,也可以是混合气体 .由此也可以推知在标准状况下气体的密度是用气体的摩尔质量除以Vm ,即由此也可推得:M=ρ·Vm(2)阿伏加德罗定律 1.内容:在同温同压下 ,相同体积的任何气体都含有相同数目的分子 .适用范围:适用于相同条件下任何气体不同表述:①假设T、P、V相同 ,那么N(或n)相同;②假设T、P、n相同 , 那么V相同 .⑤物质的量浓度:单位体积溶液中所含溶质B的物质的量 .符号CB 单位:mol/l公式:C B =n B/V n B =C B×V V =n B/C B溶液稀释规律 C (浓 )×V (浓 ) =C (稀 )×V (稀 )⑥溶液的配置(l )配制溶质质量分数一定的溶液计算:算出所需溶质和水的质量.把水的质量换算成体积.如溶质是液体时,要算出液体的体积.称量:用天平称取固体溶质的质量;用量简量取所需液体、水的体积.溶解:将固体或液体溶质倒入烧杯里,参加所需的水,用玻璃棒搅拌使溶质完全溶解.(2 )配制一定物质的量浓度的溶液 (配制前要检查容量瓶是否漏水 )计算:算出固体溶质的质量或液体溶质的体积.称量:用托盘天平称取固体溶质质量,用量简量取所需液体溶质的体积.溶解:将固体或液体溶质倒入烧杯中,参加适量的蒸馏水(约为所配溶液体积的1/6 ) ,用玻璃棒搅拌使之溶解,冷却到室温后,将溶液引流注入容量瓶里.洗涤(转移):用适量蒸馏水将烧杯及玻璃棒洗涤2-3次,将洗涤液注入容量瓶.振荡,使溶液混合均匀.定容:继续往容量瓶中小心地加水,直到液面接近刻度2-3mm处,改用胶头滴管加水,使溶液凹面恰好与刻度相切.把容量瓶盖紧,再振荡摇匀.补充:1.使用容量瓶的考前须知:a) 按所配溶液的体积选择适宜规格的容量瓶. (50mL、100mL、250mL、500mL ) b) 使用前要检查容量瓶是否漏水. c) 使用前要先用蒸馏水洗涤容量瓶. d) 容量瓶不能将固体或浓溶液直接溶解或稀释,容量瓶不能作反响器,不能长期贮存溶液.5、过滤过滤是除去溶液里混有不溶于溶剂的杂质的方法.过滤时应注意:①一贴:将滤纸折叠好放入漏斗,加少量蒸馏水润湿,使滤纸紧贴漏斗内壁.②二低:滤纸边缘应略低于漏斗边缘,参加漏斗中液体的液面应略低于滤纸的边缘.③三靠:向漏斗中倾倒液体时,烧杯的夹嘴应与玻璃棒接触;玻璃棒的底端应和过滤器有三层滤纸处轻轻接触;漏斗颈的末端应与接受器的内壁相接触,例如用过滤法除去粗食盐中少量的泥沙.补充:一定物质的量浓度溶液配制的误差分析一、误差分析的理论依据根据c B=n B/V可得,一定物质的量浓度溶液配制的误差都是由溶质的物质的量nB和溶液的体积V引起的.误差分析时,关键要看配制过程中引起n和V怎样的变化.在配制一定物质的量浓度溶液时,假设nB比理论值小,或V比理论值大时,都会使所配溶液浓度偏小;假设n B比理论值大,或V比理论值小时,都会使所配溶液浓度偏大.二、误差原因实例归纳为了便于同学们理解,我们对产生误差的原因归纳分析如下:(一)由概念不清引起的误差1.容量瓶的容量与溶液体积不一致.例:用500mL容量瓶配制450mL 0.1 moL/L的氢氧化钠溶液,用托盘天平称取氢氧化钠固体1.8g.分析:偏小.容量瓶只有一个刻度线,且实验室常用容量瓶的规格是固定的(50mL、100mL、250mL、500mL、1000mL ) ,用500mL容量瓶只能配制500mL一定物质的量浓度的溶液.所以所需氢氧化钠固体的质量应以500mL溶液计算,要称取2.0g氢氧化钠固体配制500mL溶液,再取出450mL溶液即可.2.溶液中的溶质与其结晶水合物的不一致.例:配制500mL0.1moL/L的硫酸铜溶液,需称取胆矾8.0g.分析:偏小.胆矾为CuSO4·5H2O ,而硫酸铜溶液的溶质是CuSO4 .配制上述溶液所需硫酸铜晶体的质量应为12.5g ,由于所称量的溶质质量偏小,所以溶液浓度偏小.(二)由试剂纯度引起的误差3.结晶水合物风化或失水.例:用生石膏配制硫酸钙溶液时,所用生石膏已经局部失水.分析:偏大.失水的生石膏中结晶水含量减少,但仍用生石膏的相对分子质量计算,使溶质硫酸钙的质量偏大,导致所配硫酸钙溶液的物质的量浓度偏大.4.溶质中含有其他杂质.例:配制氢氧化钠溶液时,氢氧化钠固体中含有氧化钠杂质.分析:偏大.氧化钠固体在配制过程中遇水转变成氢氧化钠,31.0 g氧化钠可与水反响生成40.0 g氢氧化钠,相当于氢氧化钠的质量偏大,使结果偏大.(三)由称量不正确引起的误差5.称量过程中溶质吸收空气中成分.例:配制氢氧化钠溶液时,氢氧化钠固体放在烧杯中称量时间过长.分析:偏小.氢氧化钠固体具有吸水性,使所称量的溶质氢氧化钠的质量偏小,导致其物质的量浓度偏小.所以称量氢氧化钠固体时速度要快或放在称量瓶中称量最|好.6.称量错误操作.例:配制氢氧化钠溶液时,天平的两个托盘上放两张质量相等的纸片.分析:偏小.在纸片上称量氢氧化钠,吸湿后的氢氧化钠会沾在纸片上,使溶质损失,浓度偏小.7.天平砝码本身不标准.例:天平砝码有锈蚀.分析:偏大.天平砝码锈蚀是因为少量铁被氧化为铁的氧化物,使砝码的质量增大,导致实际所称溶质的质量也随之偏大.假设天平砝码有残缺,那么所称溶质的质量就偏小.8.称量时药品砝码位置互换.例:配制一定物质的量浓度的氢氧化钠溶液,需称量溶质4.4g,称量时天平左盘放砝码,右盘放药品.分析:偏小.溶质的实际质量等于砝码质量4.0g减去游码质量0.4g,为3.6g.即相差两倍游码所示的质量.假设称溶质的质量不需用游码时,物码反放那么不影响称量物质的质量.9.量筒不枯燥.例:配制一定物质的量浓度的硫酸溶液时,用没有枯燥的量筒量取浓硫酸.分析:偏小.相当于稀释了浓硫酸,使所量取的溶质硫酸的物质的量偏小.10. 量筒洗涤.例:用量筒量取浓硫酸倒入小烧杯后,用蒸馏水洗涤量筒并将洗涤液转移至|小烧杯中.分析:偏大.用量筒量取液体药品,量筒不必洗涤,因为量筒中的残留液是量筒的自然残留液,在制造仪器时已经将该局部的体积扣除,假设洗涤并将洗涤液转移到容量瓶中,所配溶液浓度偏高.11.量筒读数错误.用量筒量取浓硫酸时,仰视读数.分析:偏大.读数时,应将量筒放在水平桌面上,使眼睛与量筒中浓硫酸的凹面处相平.仰视读数时,读数偏小,实际体积偏大,所取的硫酸偏多,结果配制的溶液浓度偏大.(四)由溶解转移过程引起的误差12.未冷却溶液直接转移.例:配制氢氧化钠溶液时,将称量好的氢氧化钠固体放入小烧杯中溶解,未冷却立即转移到容量瓶中并定容.分析:偏大.容量瓶上所标示的使用温度一般为室温.绝|大多数物质在溶解或稀释过程中常伴有热效应,使溶液温度升高或降低,从而影响溶液体积的准确度.氢氧化钠固体溶于水放热,定容后冷却至|室温,溶液体积缩小,低于刻度线,浓度偏大.假设是溶解过程中吸热的物质,那么溶液浓度偏小.13.转移溶质有损失.例:转移到容量瓶过程中,有少量的溶液溅出.分析:偏小.在溶解、转移的过程中由于溶液溅出,溶质有损失.使溶液浓度偏小.14.烧杯或玻璃棒未洗涤.例:转移后,未洗涤小烧杯和玻璃棒,或者虽洗涤但未将洗涤液一并转移至|容量瓶中.分析:偏小.溶质有损失.使溶液浓度偏小.(五)由定容过程引起的误差15.定容容积不准确.例:定容时,加水超过刻度线,用胶头滴管吸取多余的液体至|刻度线.分析:偏小.当液面超过刻度线时,溶液浓度已经偏小.遇到这种情况,只有重新配制溶液.16.定容后多加蒸馏水.例:定容摇匀后,发现液面下降,继续加水至|刻度线.分析:偏小.容量瓶摇匀后发现液面下降是因为极少量的溶液润湿磨口或附着在器壁上未流下来,不会引起溶液浓度的改变.此时加水会引起浓度偏小.17.定容时视线不平视.例:定容时仰视.分析:偏低.定容时仰视,容量瓶内液面最|低点高于刻度线,使浓度偏小;反之,俯视时,容量瓶内液面最|低点低于刻度线,使浓度偏大.(六)对实验结果无影响的操作18.称量溶质的小烧杯没有枯燥.分析:无影响.因为所称溶质质量是两次称量数据之差,其溶质的物质的量正确,那么物质的量浓度无影响.19.配制前容量瓶中有水滴.分析:无影响.溶质的质量和溶液的体积都没有变化.20.定容摇匀后少量溶液外流.分析:无影响.定容摇匀后,溶液的配制已经完成.从中任意取出溶液,浓度不会发生改变. 以上分析了配制一定物质的量浓度溶液实验误差的原因及分析方法.从概念不清、药品纯度、称量错误、溶解转移、定容错误五个方面和十七个小点进行了讨论.而有些操作对浓度误差是无影响的,如第六方面也要引起大家的注意.第二章化学物质及其变化一、物质的分类金属:Na、Mg、Al单质非金属:S、O、N酸性氧化物:SO3、SO2、P2O5等氧化物碱性氧化物:Na2O、CaO、Fe2O3氧化物:Al2O3等纯盐氧化物:CO、NO等、H2SO4等净含氧酸:HNO物按酸根分无氧酸:HCl强酸:HNO3、H2SO4、HCl酸按强弱分弱酸:H2CO3、HClO、CH3COOH化一元酸:HCl、HNO3合按电离出的H +数分二元酸:H2SO4、H2SO3物多元酸:H3PO4强碱:NaOH、Ba(OH)2 物按强弱分质弱碱:NH3·H2O、Fe(OH)3碱一元碱:NaOH、按电离出的HO -数分二元碱:Ba(OH)2多元碱:Fe(OH)3CO3正盐:Na盐酸式盐:NaHCO3碱式盐:Cu2(OH)2CO3溶液:NaCl溶液、稀H2SO4等混悬浊液:泥水混合物等乳浊液:油水混合物物胶体:Fe(OH)3胶体、淀粉溶液、烟、雾、有色玻璃等二、分散系相关概念1. 分散系:一种物质(或几种物质)以粒子形式分散到另一种物质里所形成的混合物,统称为分散系.2. 分散质:分散系中分散成粒子的物质.3. 分散剂:分散质分散在其中的物质.4、分散系的分类:当分散剂是水或其他液体时,如果按照分散质粒子的大小来分类,可以把分散系分为:溶液、胶体和浊液.分散质粒子直径小于1nm的分散系叫溶液,在1nm-100nm之间的分散系称为胶体,而分散质粒子直径大于100nm的分散系叫做浊液.下面比拟几种分散系的不同:分散系 溶 液胶 体 浊 液 分散质的直径 <1nm (粒子直径小于10 -9m ) 1nm -100nm (粒子直径在10 -9 ~ 10-7m ) >100nm (粒子直径大于10 -7m )分散质粒子 单个小分子或离子 许多小分子集合体或高分子 巨大数目的分子集合体实例溶液酒精、氯化钠等淀粉胶体、氢氧化铁胶体等 石灰乳、油水等 性质外观均一、透明 均一、透明 不均一、不透明 稳定性 稳定 较稳定 不稳定 能否透过滤纸 能 能 不能 能否透过半透膜能 不能 不能 鉴别 无丁达尔效应 有丁达尔效应 静置分层注意:三种分散系的本质区别:分散质粒子的大小不同 .三、胶体1、胶体的定义:分散质粒子直径大小在10 -9~10 -7m 之间的分散系 .2、胶体的分类:①. 根据分散质微粒组成的状况分类:如:3)(OH Fe 胶体胶粒是由许多3)(OH Fe 等小分子聚集一起形成的微粒 ,其直径在1nm ~100nm 之间 ,这样的胶体叫粒子胶体 . 又如:淀粉属高分子化合物 ,其单个分子的直径在1nm ~100nm 范围之内 ,这样的胶体叫分子胶体 .②. 根据分散剂的状态划分:如:烟、云、雾等的分散剂为气体 ,这样的胶体叫做气溶胶;AgI 溶胶、3)(OH Fe 溶胶、3)(OH Al 溶胶 ,其分散剂为水 ,分散剂为液体的胶体叫做液溶胶;有色玻璃、烟水晶均以固体为分散剂 ,这样的胶体叫做固溶胶 .3、胶体的制备A . 物理方法①机械法:利用机械磨碎法将固体颗粒直接磨成胶粒的大小 ②溶解法:利用高分子化合物分散在适宜的溶剂中形成胶体 ,如蛋白质溶于水 ,淀粉溶于水、聚乙烯熔于某有机溶剂等 .B. 化学方法①水解促进法:FeCl 3 +3H 2O (沸 ) =3)(OH Fe (胶体 ) +3HCl②复分解反响法:KI +AgNO 3 =AgI (胶体 ) +KNO 3 Na 2SiO 3 +2HCl =H 2SiO 3 (胶体 ) +2NaCl思考:假设上述两种反响物的量均为大量 ,那么可观察到什么现象 ?如何表达对应的两个反响方程式 ?提示:KI +AgNO 3 =AgI↓ +KNO 3 (黄色↓ ) Na 2SiO 3 +2HCl =H 2SiO 3↓ +2NaCl (白色↓ )4、胶体的性质:① 丁达尔效应 - -丁达尔效应是粒子对光散射作用的结果 ,是一种物理现象 .丁达尔现象产生的原因 ,是因为胶体微粒直径大小恰当 ,当光照射胶粒上时 ,胶粒将光从各个方面全部反射 ,胶粒即成一小光源 (这一现象叫光的散射 ) ,故可明显地看到由无数小光源形成的光亮 "通路〞 .当光照在比拟大或小的颗粒或微粒上那么无此现象 ,只发生反射或将光全部吸收的现象 ,而以溶液和浊液无丁达尔现象 ,所以丁达尔效应常用于鉴别胶体和其他分散系 . ② 布朗运动 - -在胶体中 ,由于胶粒在各个方向所受的力不能相互平衡而产生的无规那么的运动 ,称为布朗运动 .是胶体稳定的原因之一 .③ 电泳 - -在外加电场的作用下 ,胶体的微粒在分散剂里向阴极 (或阳极 )作定向移动的现象 .胶体具有稳定性的重要原因是同一种胶粒带有同种电荷 ,相互排斥 ,另外 ,胶粒在分散力作用下作不停的无规那么运动 ,使其受重力的影响有较大减弱 ,两者都使其不易聚集 ,从而使胶体较稳定 .说明:A 、电泳现象说明胶粒带电荷 ,但胶体都是电中性的 .胶粒带电的原因:胶体中单个胶粒的体积小 ,因而胶体中胶粒的外表积大 ,因而具备吸附能力 .有的胶体中的胶粒吸附溶液中的阳离子而带正电;有的那么吸附阴离子而带负电胶体的提纯 ,可采用渗析法来提纯胶体 .使分子或离子通过半透膜从胶体里别离出去的操作方法叫渗析法 .其原理是胶体粒子不能透过半透膜 ,而分子和离子可以透过半透膜 .但胶体粒子可以透过滤纸 ,故不能用滤纸提纯胶体 .B 、在此要熟悉常见胶体的胶粒所带电性 ,便于判断和分析一些实际问题 .带正电的胶粒胶体:金属氢氧化物如3)(OH Al 、3)(OH Fe 胶体、金属氧化物 .带负电的胶粒胶体:非金属氧化物、金属硫化物As 2S 3胶体、硅酸胶体、土壤胶体 特殊:AgI 胶粒随着AgNO 3和KI 相对量不同 ,而可带正电或负电 .假设KI 过量 ,那么AgI 胶粒吸附较多I -而带负电;假设AgNO 3过量 ,那么因吸附较多Ag +而带正电 .当然 ,胶体中胶粒带电的电荷种类可能与其他因素有关 .C 、同种胶体的胶粒带相同的电荷 .D 、固溶胶不发生电泳现象 .但凡胶粒带电荷的液溶胶 ,通常都可发生电泳现象 .气溶胶在高压电的条件也能发生电泳现象 .胶体根据分散质微粒组成可分为粒子胶体 (如3)(OH Fe 胶体 ,AgI 胶体等 )和分子胶体[如淀粉溶液 ,蛋白质溶液 (习惯仍称其溶液 ,其实分散质微粒直径已达胶体范围 ) ,只有粒子胶体的胶粒带电荷 ,故可产生电泳现象 .整个胶体仍呈电中性 ,所以在外电场作用下作定向移动的是胶粒而非胶体 .④聚沉 - -胶体分散系中 ,分散系微粒相互聚集而下沉的现象称为胶体的聚沉 .能促使溶胶聚沉的外因有加电解质 (酸、碱及盐 )、加热、溶胶浓度增大、加胶粒带相反电荷的胶体等 .有时胶体在凝聚时 ,会连同分散剂一道凝结成冻状物质 ,这种冻状物质叫凝胶 .胶体稳定存在的原因: (1 )胶粒小 ,可被溶剂分子冲击不停地运动 ,不易下沉或上浮 (2 )胶粒带同性电荷 ,同性排斥 ,不易聚大 ,因而不下沉或上浮胶体凝聚的方法:。
【高中化学电子书】2019版高中化学必修一

【高中化学电子书】2019版高中化学必修一第一章化学基本概念1.1 化学物质的组成化学物质是由原子组成的,原子是化学元素的基本单位。
原子由原子核和核外电子组成。
原子核由质子和中子组成,质子带正电荷,中子不带电荷。
核外电子带负电荷,围绕原子核运动。
1.2 化学物质的分类1.3 化学物质的性质化学物质的性质可以分为物理性质和化学性质。
物理性质是指化学物质在不改变其组成的情况下所表现出来的性质,如颜色、状态、密度、熔点、沸点等。
化学性质是指化学物质在发生化学反应时表现出来的性质,如可燃性、氧化性、还原性等。
1.4 化学反应化学反应是指化学物质在发生化学变化时,原子之间的化学键发生断裂和重新组合的过程。
化学反应可以分为合成反应、分解反应、置换反应和复分解反应。
1.5 化学方程式化学方程式是表示化学反应的符号式,用化学符号和化学式表示反应物和物之间的化学关系。
化学方程式需要遵守质量守恒定律和电荷守恒定律。
1.6 化学计量学化学计量学是研究化学物质之间数量关系的科学。
化学计量学的基本原理是质量守恒定律和摩尔定律。
摩尔定律指出,在相同温度和压力下,相同体积的气体含有相同数量的分子。
1.7 溶液溶液是由溶质和溶剂组成的混合物,其中溶质是被溶解的物质,溶剂是溶解溶质的物质。
溶液可以分为饱和溶液和不饱和溶液,饱和溶液是指在一定温度下,溶液中溶质的质量达到最大值,不再溶解溶质。
不饱和溶液是指在一定温度下,溶液中溶质的质量没有达到最大值,还可以继续溶解溶质。
1.8 氧化还原反应氧化还原反应是指化学反应中,原子或离子的氧化态发生变化的过程。
氧化还原反应可以分为氧化反应和还原反应。
氧化反应是指原子或离子失去电子的过程,还原反应是指原子或离子获得电子的过程。
氧化还原反应的实质是电子的转移。
1.9 化学平衡化学平衡是指化学反应达到动态平衡的状态,反应物和物的浓度不再发生变化。
化学平衡可以分为动态平衡和静态平衡,动态平衡是指反应物和物的浓度保持不变,但反应仍在进行;静态平衡是指反应物和物的浓度保持不变,反应已经停止。
高二化学教学资源推荐优质化学学习网站与应用

高二化学教学资源推荐优质化学学习网站与应用随着信息技术的快速发展,互联网已经成为现代教育不可或缺的一部分。
对于高二学生来说,化学学习网站和应用程序是快速获取知识和提升学习效果的重要工具。
本文将推荐几个优质的化学学习网站和应用,帮助高二学生更好地学习化学知识。
一、优质化学学习网站1. 化学在线学习网站化学在线学习网站是一个全面和易于使用的化学学习资源平台。
它通过提供丰富的教学视频、优质的学习材料和交互式实验模拟等方式,帮助学生理解化学概念和原理。
这个网站还提供在线测验和考试,方便学生自测和评估学习成果。
2. 化学之家化学之家是一个综合性的化学学习网站,提供了大量的化学知识和资源。
学生可以在这个网站上免费获取化学教材、实验指导、习题解析等学习材料。
此外,化学之家还有一个交流社区,学生可以在这里与其他学习化学的同学互动,共同解决问题和分享学习经验。
3. 化学欢乐谷化学欢乐谷是一个让学生在轻松愉快的氛围中学习化学的网站。
它通过生动有趣的动画、游戏和实验模拟,激发学生的学习兴趣。
学生可以在这个网站上参与各种有趣的活动,如化学小测验和实验室模拟,提高化学实践能力和动手操作的能力。
二、优质化学学习应用1. 百词斩百词斩是一款专注于记忆和应用高中化学词汇的学习应用。
它通过智能化的记忆系统和多种学习模式,帮助学生高效地掌握化学词汇并能够熟练应用。
这个应用还提供了在线测验和模拟考试,以帮助学生检验和提高自己的学习成果。
2. 化学实验室化学实验室是一款虚拟实验应用程序,模拟了真实的化学实验。
学生可以在这个应用中进行各种化学实验,如酸碱反应、氧化还原反应等。
通过观察实验过程和结果,学生可以更好地理解化学原理和实验操作。
这个应用还提供了实验记录和报告的功能,方便学生进行实验的记录和整理。
3. 化学计算器化学计算器是一款用于化学计算和问题解答的应用程序。
它提供了各种常用的化学计算工具,如反应平衡计算、物质摩尔质量计算等。
学生可以通过这个应用程序进行各种化学计算,并获得准确的结果。
“互联网+”背景下高中化学课堂教学模式的创新——以“硫酸的工业制法”为例

一、研究背景“互联网+教育”的融合,其关键就是以“育人”为纽带,只有“育人”才能让这个“+”真正有价值、有意义。
本文以“硫酸的工业制法”为例,进行了“互联网+”背景下高中化学课堂教学模式的创新,如此可使学生在收获知识和技能的同时,得到学科素养的提升,并利用大数据时代的特点和优势随时掌握学生的学习情况,由此可更好地实现新课标提倡的“教、学、评”一体化的目标。
二、课堂教学模式的构建Educational Practice and Research———以“硫酸的工业制法”为例孙媛媛,王志庚,冯月新(唐山市第一中学,河北唐山063000)摘要:以“硫酸的工业制法”为例进行教学设计,将互联网与化学教学中的各个环节进行融合,由此可创新化学课堂教学模式。
即在课前预习环节以课题为任务驱动,学生从网络上搜索信息,然后在微信公众号平台学习微课;在课堂教学环节进行小组间交流———既有面对面交流,又可以在班级微信群中交流,扩大了交流范围;在教学评价环节,应用问卷星对学生进行学习评价,如此评价数据更全面快捷,同时又可以应用于线上、线下教学。
关键词:高中化学;硫酸制备;互联网;微信公众号;问卷星中图分类号:G633.8文献标识码:A文章编号:1009-010X (2021)14-0054-04教学环节2课堂交流展示教学环节1利用微课、互联网自主预习教学环节3推进教学重、难点的学习教学环节4利用问卷星进行评价→→→培养表达、交往、合作的能力,获得学习的幸福感。
发展学生的化学学科核心素养。
推进“教、学、评”一体化教学。
培养整合信息、自主学习的能力,激励主动学习。
↓↓↓↓图1互联网+背景下高中化学课堂教学模式本文系河北省教育科学研究“十三五”规划2019年度重点资助课题“互联网+背景下高中化学教学资源开发共享和教学模式的变革研究”(课题编号:1902019)研究成果。
. All Rights Reserved.在此模式下的教学设计,应该考虑到如下两个重要环节:(一)辅助课前教学设计进行课前预习的手段包括阅读课本、观看微课视频、网络搜索等。
2023-2024学年高一上学期化学人教版(2019)必修第一册知识点总结

高一上学期化学必修第一册知识点总结第一章化学物质及其变化一、物质的分类(1)同素异形体;由同一种元素形成几种性质不同的单质Eg:①O2,O3;②金刚石,石墨,C60;③红磷P和白磷P4注意:由同一种元素组成的物质不一定是单质,还可能是几种同素异形体Eg:①O2和O3的混合物(2)分类方法:①树状分类法:按统一标准(采用树状形式)对同类事物进行再分类的方法。
特征:同一层次的物质类别间一般相互独立,没有交叉。
②交叉分类法:根据多种不同分类标准对同一事物进行分类的方法。
特征:物质类别间有交叉的部分。
1、分散系(1)定义:把一种(或多种)物质分散在另一种(或多种)物质中所得到的体系,叫分散系。
被分散的物质称作分散质(可以是气体、液体、固体),容纳分散质作用的物质称作分散剂(可以是气体、液体、固体)。
(2)区别***:分散质粒子的大小是胶体区别于溶液、浊液的本质特征。
(3)溶液、胶体、浊液三种分散系的比较***:分散质粒子大小/nm 外观特征能否通过滤纸能否通过半透膜有否丁达尔效应实例溶液小于1nm均匀、透明、稳定能能没有NaCl 、蔗糖溶液胶体在1—100nm之间均匀、有的透明、较稳定能不能有Fe(OH)3胶体浊液大于100nm 不均匀、不透明、不稳定不能不能没有泥水胶体的性质*****:丁达尔效应*,聚沉*,电泳*,渗析*,介稳性。
丁达尔效应**:可见光通过胶体时,可看到一条“光的通路”,是由于胶体粒子对光的散射形成的。
(鉴别胶体和溶液的物理方法)聚沉的三方法***:加热,加入电解质,加入带相反电荷胶粒的胶体。
注意*:胶体不带电,胶体微粒带电(Fe(OH)3胶体微粒带正电)胶体的分类;根据分散剂的状态胶体根据分散质的构成导师指点:1Fe(OH)3胶体粒子是由许多Fe(OH)3小分子聚集所形成的的微粒,其直径为1~100nm,故称为粒子胶体。
2淀粉属于高分子,其单个分子的直径为1~100nm,故称为分子胶体。
人教版高中化学必修 附录Ⅰ 相对原子质量表 精品

盘锦市第二高级中学高一化学学案(第周)课题:第三章第一节金属的化学性质(第一课时)高一化学组★学习目标1了解金属与非金属的反应,金属钠、铝与氧气的反应,探索金属的性质和金属的原子结构的关系。
2初步学会从实验的角度探索和认识物质的化学性质的本领。
3通过探究实验,学会观察以及从分析现象中得出结论。
★教学重点:金属钠与氧气在不同条件下的反应,铝与氧气的反应。
★教学难点:金属钠与氧气在不同条件下的反应及其产物的分析比较★思考与交流阅读教材g Al的原子结构示意图,分析其结构特点,判断它们与其他物质发生反应时做氧化剂还是还原剂为什么______________________________________________________________________________________________________________________________________________________________________★自主梳理一、金属与非金属的反应(一)金属钠与氧气的反应:【实验3—1】取一小块金属钠,用滤纸吸干表面的煤油后,并在玻璃片上用小刀进行切割,过一段时间再观察其表面的颜色。
【思考一】1记录观察的现象:新切开的钠具有_____色金属光泽,在空气中表面很快变____,生成白色的_____。
2该反应的化学方程式:__________________________用单线桥标出电子转移【实验3—2】把一小块绿豆大小的金属钠放在坩埚里,加热。
3记录观察的现象:加热时能燃烧,产生________火焰,生成_________色的_________。
4简单描述钠的物理性质:______色,有金属光泽的固体,_________ ,熔点_______保存在___________。
5该反应化学方程式:________________________________(用单线桥标出电子转移)(二)铝与氧气的反应:【科学探究】1、用坩埚夹住一小块铝箔(箔厚约),在酒精灯上加热至熔化,轻轻晃动,仔细观察。
新课标人教版高中化学全部教材目录

新课标人教版高中化学全部教材目录必修第一册绪言第一章物质及其变化第一节物质的分类及其转化第二节离子反应第三节氧化还原反应整理与提升第二章海水中的重要元素——钠和氯第一节钠及其化合物第二节氯及其化合物第三节物质的量整理与提升实验活动1 配置一定物质的量浓度的溶液第三章铁金属材料第一节铁及其化合物第二节金属材料整理与提升实验活动2铁及其化合物的性质第四章物质结构元素周期律第一节原子结构与元素周期表第二节元素周期律第三节化学键整理与提升实验活动3同周期、同主族元素性质的递变附录Ⅰ实验室突发事件的应对措施和常见废弃物的处理方法附录Ⅱ一些化学品安全使用标识附录Ⅲ名词索引附录Ⅳ部分酸、碱和盐的溶解性表(室温)附录V一些常见元素中英文名称对照表附录V相对原子质量表必修第二册第五章化工生产中的重要非金属元素第一节硫及其化合物第二节氮及其化合物第三节无机非金属材料整理与提升实验活动4 用化学沉淀法去除粗盐中的杂质离子实验活动5 不同价态含硫物质的转化第六章化学反应与能量第一节化学反应与能量变化第二节化学反应的速率与限度整理与提升实验活动6 化学能转化成电能实验活动7 化学反应速率的影响因素第七章有机化合物第一节认识有机化合物第二节乙烯与有机高分子材料第三节乙醇与乙酸第四节基本营养物质整理与提升实验活动8 搭建球棍模型认识有机化合物分子结构的特点实验活动9 乙醇、乙酸的主要性质第八章化学与可持续发展第一节自然资源的开发利用第二节化学品的合理使用第三节环境保护与绿色化学整理与提升附录Ⅰ名词索引附录Ⅱ部分酸、碱和盐的溶解性表(室温)附录Ⅲ一些常见元素中英文名称对照表附录Ⅳ相对原子质量表元素周期表选择性必修1引言第一章化学反应的热效应第一节反应热第二节反应热的计算整理与提升第二章化学反应速率与化学平衡第一节化学反应速率第二节化学平衡第三节化学反应的方向第四节化学反应的调控整理与提升实验活动1 探究影响化学平衡移动的因素第三章水溶液中的离子反应与平衡第一节电离平衡第二节水的电离和溶液的pH第三节盐类的水解第四节沉淀溶解平衡整理与提升实验活动2 强酸与强碱的中和滴定实验活动3 盐类水解的应用第四章化学反应与电能第一节原电池第二节电解池第三节金属的腐蚀与防护整理与提升实验活动4 简单的电镀实验实验活动5 制作简单的燃料电池附录I 某些物质的燃烧热(25℃,101kPa)附录Ⅱ某些弱电解质的电离常数(25℃)附录Ⅲ常见难溶电解质的溶度积常数(25℃) 附录Ⅳ名词索引元素周期表选择性必修2物质结构与性质第一章原子结构与性质知识点1 能层与能级知识点2 基态与激发态原子光谱知识点3 构造原理与电子排布式知识点4 电子云与原子轨道知识点5 泡利原理、洪特规则、能量最低原理知识点6 原子结构与元素周期表知识点7 原子半径知识点8 电离能知识点9 电负性第二章分子结构与性质知识点1 共价键知识点2 键参数--键能、键长和键角知识点3 分子结构的测定知识点4 多样的分子空间结构知识点5 价层电子对互斥模型知识点6 杂化轨道理论简介知识点7 共价键的极性知识点8 分子间的作用力知识点9 溶解性(相似相溶原理)知识点10 分子的手性第三章晶体结构与性质知识点1 物质的聚集状态知识点2 晶体与非晶体知识点3 晶胞知识点4 晶体结构的测定知识点5 分子晶体知识点6 共价晶体知识点7 金属键与金属晶体知识点8 离子晶体知识点9 过渡晶体与混合型晶体知识点10 配合物与超分子实验探究.【实验3-2】配合物的生成(1)【实验3-3】配合物的生成和析出【实验3-4】配合物的颜色【实验3-5】配合物的生成(2)规律方法方法比较物质熔点、沸点高低的方法选择性必修3 有机化学基础第一章有机化合物的结构特点与研究方法知识点1 有机化合物的分类知识点2 有机化合物中的共价键知识点3 有机化合物的同分异构现象知识点4 有机物的表示方法知识点5 有机化合物的分离、提纯知识点6 确定实验式--元素分析知识点7 确定分子式--质谱法知识点8 确定分子结构--波谱分析规律方法方法1 研究有机化合物的一般方法方法2 同分异构体数目的判断方法方法3 同分异构体书写方法第二章烃知识点1 烷烃的结构和性质知识点2 烷烃的系统命名法知识点3 烯烃知识点4 炔烃知识点5 乙炔的实验室制法知识点6 苯知识点7 苯的同系物知识点8 稠环芳香烃实验探究【实验2-1】苯的分子结构【实验2-2】苯的同系物的性质规律方法方法1 解有机物共线、共面问题的通用模板方法2 烃的比较第三章烃的衍生物知识点1 溴乙烷知识点2 卤代烃知识点3 醇知识点4 酚知识点5 乙醛知识点6 醛类知识点7 酮知识点8 羧酸知识点9 酯知识点10 油脂知识点11 酰胺知识点12 有机合成实验探究【实验3-1】溴乙烷的取代反应【探究】1-溴丁烷的化学性质【实验3-2】乙醇的消去反应【实验3-3】乙醇的氧化反应【实验3-4】苯酚的酸性【实验3-5】苯酚的取代反应【实验3-6】苯酚的显色反应【实验3-7】乙醛的氧化反应(银镜反应)悬浊液的反应【实验3-8】乙醛与新制Cu(OH)2【探究】羧酸的酸性第四章生物大分子知识点1 糖类的组成和分类知识点2 单糖知识点3 二糖知识点4 多糖(淀粉、纤维素)知识点5 氨基酸知识点6 蛋白质知识点7 酶知识点8 核酸实验探究【实验4-1】葡萄糖的性质【实验4-2】纤维素的水解【实验4-3】蛋白质的盐析【实验4-4】蛋白质的变性【实验4-5】蛋白质的显色反应第五章合成高分子基础知识知识点1 加成聚合反应知识点2 缩合聚合反应知识点3 通用高分子材料知识点4 功能高分子材料规律方法方法高聚物单体判断的方法。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
附录:网络教学资源的开发
国际互联网的出现及其迅猛发展,使当今世界跨入了真正的信息时代,它是世界上最大的信息资源库,已经成为人们生活、学习和工作的不可缺少的工具。
在这个信息的海洋中,人们能够以空前速度在网上索取自己需要的信息和知识。
Internet上的化学资源具有分布广泛、数量巨大、互动性强、更新快等特点,已经成为化学教学资源开发的重要领域。
1.互联网上化学教学资源的类别
互联网上的化学教学资源主要表现为以下几种形式:
(1)化学教学参考资料
化学教学参考资料包括化学史、化学与社会、化学与健康、化学与科技、化学与生活、趣味化学、化学游戏、化学谜语、化学练习题、测试题及其参考答案、其他补充资料等。
(2)化学软件、化学教学课件素材
网上有丰富的化学课件和课件素材,其中课件可以直接或者根据需要稍作修改后在课堂上使用;课件素材则需要按照一定的意图设计成课件之后才能用于课堂教学。
此外,网上还可以下载一些化学软件。
(3)化学教研活动信息
这些资源反映开展化学教研活动的情况,提供学习、考察和交流的线索。
(4)化学教学优秀教案
互联网上提供有大量的教案实例,可为教师备课提供参考。
(5)化学教育论坛
登载行内和行外人士的文章或意见,是社会各界(包括教育界)交流化学教育教学观点和思想的场所。
(6)化学图书、杂志、期刊、报纸
互联网上提供了很多有关化学专业的站点,用户可以很方便地访问查阅自己需要的化学资料和文献。
此外,在Internet上出版化学杂志(E-journals and E-publishing)已经成为互联网上化学资源发展的一个重要趋势。
2.化学资源的获取方法
(1)使用通用搜索引擎
搜索引擎是一种搜索工具,它的主要任务是在Internet中主动搜索其他网站的信息并对其自动索引,其索引内容存储在可供查询的大型数据库中。
当用户利用搜索引擎查询信息时,它会提供包含该信息的相关网址及相应的链接。
常用的搜索引擎一般具有分类主题查寻和关键词查寻两种功能。
前者是将搜索引擎收录的网址、文件,依据其内容、动态归档,点击分类名称,查看不同类的网址,也可
以点击各网址上的标题,进入相应的网页去浏览更详细的信息;后者搜寻到的网页不是很多,但通过关键词可以查寻到更多、更准确的信息,可以在输入框里填写关键词,然后提交查寻,这时系统将显示出检索到的与它们相关的网址、主页和简要信息。
常用的英文搜索引擎有:
Yahoo! ()
google ()
Webcrawler ()
常用的中文搜索引擎有:
百度()
搜狐()
新浪()
悠游()
这些通用搜索引擎使用方便、功能强大,但在搜索化学专业信息方面存在搜索结果量过大、信息相关度低、针对性差等缺点。
(2)输入网址直接进入专业网站
化学信息资源是以页面(也称网页或Web页)的形式存诸在服务器中,因此只要知道某化学信息站点的网址,即可在启动Internet Explore后,直接在“地址”栏内输入要访问的Web站点网址进入网站。
如在地址栏输入(中国基础教育网主页),按回车键,则中国基础教育网主页的内容就会显示在浏览器的窗口中。
此外,还可以由某一网页上提供的相关站点链接,进入更多的站点。
(3)化学资源导航系统
Internet化学资源导航系统是(用人工的方法)针对化学领域或与化学有关的某个主题来搜集和组织Internet上的相关资源,并建立基于Web的资源指南系统。
目前Internet化学资源导航系统众多,下面列出了国内外比较重要的化学资源导航系统: 国外重要的化学资源导航系统
① Chemsoc(网址:)
Chemsoc是英国皇家化学会的官方网站,它提供的Web Links是一个较优秀的化学资源导航系统,约有 3 000多个链接。
主要的目录包括:书籍(Books)、环境(Environmental)、数据库(Databases)、期刊(Journals)、职业(Careers)、商业(Business)、软件(Software)、应用化学(Applied Chemistry)、纯粹化学(Pure Chemistry)、生物及医药化学(Biological and Medicinal Chemistry)、协会组织(Societies and Organizations)、研讨会(Conferences & Virtual Meetings)、分析化学(Analytical Chemistry)、在线课程(Online Courses)、教育组织(Educational Institutions)、教育教学资源(Education & Teaching Resources)等。
② Links for Chemist(网址:/Chemistry/Links/links.html)
英国Liverpool大学建立的专为化学家提供资源导航服务的站点,目前已经收录有
8 400余条资源,并同时提供英语、德语和法语三种版本。
③ Chemdex(网址:)
Chemdex是由英国Sheffield大学的Mark Winter建立和维护的资源导航系统,该网站收录了大量的化学资源,至2001年3月份,收录的化学资源已经达到5 806个。
④ Chem Info(网址:/~cheminfo)
Chem Info全称为Chemical Information Sources,是美国印地安纳大学化学信息综合网站,由Gary Wiggins主持。
其中作为资源导航的部分称为SIRCh(Selected Internet Resources for Chemistry),是化学领域最经典和最广为人知的资源导航系统。
Chem Info把传统的主要化学信息源与相关的Internet化学资源有机地组织在一起,为人们获取Internet化学资源提供了较好的背景和内容界面,收录的内容也比较经典和权威,但不足之处是资源的覆盖面相对较窄,容量不是很多,对资源的介绍也比较简单。
⑤ ChemWeb(网址:)
建立于1997年,是目前世界上最具规模的化学虚拟社区。
由著名的科学出版商Elsevier Science拥有。
它可提供数十个数据库的查询、100多种杂志的电子版全文、Internet化学资源导航、自办的快报性网上杂志(Webzine)、会议信息、就业信息、网上购物等。
Chem Web整合了化学研究、化学工业及其相关领域的资源,因此收录的资源更全面,并提供强大的搜索功能。
国内重要的化学资源导航系统
① ChIN(网址:)
ChIN(International Chemical Information Network)是中国科学院化工冶金研究所计算机化学开放实验室建立和维护的Internet重要化学化工资源的导航系统。
② 北京大学化学信息导航(网址:)
由北京大学化学信息中心设计维护,主要内容有北大化学论坛、化学软件、化学信息导航等,并提供国内化学院系、实验室及科研机构的链接,内容丰富。
