高中化学知识结构网络图
高中化学知识结构网络图

高中化学知识结构网络图高中化学知识结构网络图化学基本概念和基本理论元素与化合物有机化学基础化学计算化学实验化学工业知识化学基本概念和基本理论物质的分类组成原子的粒子间的关系核电荷数(Z)=核内质子数=核外电子数质量数(A)=质子数(Z)+中子数(N)元素周期律与周期表化学键与分子结构晶体类型与性质晶体类型性质比较离子晶体分子晶体原子晶体金属晶体结构组成粒子阴、阳离子分子原子金属阳离子和自由电子粒子间作用离子键范德华力共价键金属键物理性质熔沸点较高低很高有高有低硬度硬而脆小大有大有小、有延展性溶解性易溶于极性溶剂,难溶于非极性溶剂极性分子易溶于极性溶剂不溶于任何溶剂难溶(钠等与水反应)导电性晶体不导电;能溶于水的其水溶液导电;熔化导电晶体不导电,溶于水后能电离的,其水溶液可导电;熔化不导电不良(半导体Si)良导体(导电传热)典型实例NaCl、NaOHNa2O、CaCO3干冰、白磷冰、硫磺金刚石、SiO2晶体硅、SiCNa、Mg、AlFe、Cu、Zn化学反应类型离子反应氧化还原反应的有关概念的相互关系化学反应中的能量变化溶液与胶体化学反应速率化学平衡弱电解质的电离平衡溶液的酸碱性盐类的水解酸碱中和滴定元素与化合物钠及其化合物电化学碱金属氯及其化合物卤素氧族元素硅及其化合物硫的重要化合物材料碳及其化合物氮族元素氨氮和磷硝酸镁和铝铁及其化合物铜及其化合物有机化学基础烃不饱和链烃芳香烃分类通式结构特点化学性质物理性质同分异构烷烃C n H2n+2(n≥1)①C-C单键②链烃①与卤素取代反应(光照) ②燃烧③裂化反应一般随分子中碳原子数的增多,沸点升高,液态时密度增大。
气态碳原子数为1~4。
不溶于水,液态烃密度比水的小碳链异构烯烃C n H2n(n≥2)①含一个C≡C键②链烃①与卤素、H:、H2O等发生加成反应②加聚反应③氧化反应:燃烧,被KMnO4酸性溶液氧化碳链异构位置异构炔烃C n H2n-2(n≥2)①含一个C≡C键②链烃①加成反应②氧化反应:燃烧,被KMnO4酸性溶液氧化碳链异构位置异构苯及其同系C n H2n-6(n≥6)①含一个苯环②侧链为烷烃基①取代反应:卤代、硝化、磺化②加成反应③氧化反应:燃烧,苯的同系物能被KMnO4酸性溶液氧化简单的同系物常温下为液态;不溶于水,密度比水的小侧链大小及相对位置产生的异构物烃的衍生物代表物质转化关系烃的衍生物结构、通式、化学性质鉴别类别官能团结构特点通式化学性质卤代烃-X(卤素原子)C-X键在一定条件下断裂C n H2n+1O2(饱和一元)(1)NaOH水溶液加热,取代反应(2)NaOH醇溶液加热,消去反应醇-OH(羟基)(1)—OH与烃基直接相连(2)—OH上氢原子活泼C n H2n+2O2(饱和一元)(1)取代:脱水成醚,醇钠,醇与羧酸成酯,卤化成卤代烃(2)氧化成醛(—CH2OH) (3)消去成烯醛(1)醛基上有碳氧双键(2)醛基只能连在烃基链端C n H2n O2(饱和一元)(1)加成:加H2成醇(2)氧化:成羧酸羧(1)—COOH可电离出H+(2)—COOH难加成C n H2n O(饱和一元)(1)酸性:具有酸的通性(2)酯化:可看作取代酯,R 必须是烃基C n H2n O2(饱和一元)水解成醇和羧酸酚(1)羟基与苯环直接相连(2)—OH上的H比醇活泼(3)苯环上的H比苯活泼(1)易取代:与溴水生成2,4,6-三溴苯酚(2)显酸性(3)显色:遇Fe3+变紫色糖类类别葡萄糖蔗糖淀粉纤维素分子式(C6H12O6)(C12H22O11)(C6H10O5)(C6H10O5)结构特点多羟基醛分子中无醛基,非还原性糖由几百到几千个葡萄糖单元构成的天然高分子化合物由几千个葡萄糖单元构成的天然高分子化合物主要性质白色晶体,溶于水有甜味。
高中化学知识结构网络图

高中化学知识构造网络图化学根本概念和根本理论元素与化合物有机化学根底化学计算化学实验化学工业知识化学根本概念和根本理论物质的分类组成原子的粒子间的关系核电荷数〔Z〕=核内质子数=核外电子数质量数〔A〕=质子数〔Z〕+中子数〔N〕元素周期律与周期表化学键与分子构造晶体类型与性质晶体类型性质比拟离子晶体分子晶体原子晶体金属晶体构造组成粒子阴、阳离子分子原子金属阳离子和自由电子粒子间作用离子键范德华力共价键金属键物理性质熔沸点较高低很高有高有低硬度硬而脆小大有大有小、有延展性溶解性易溶于极性溶剂,难溶于非极性溶剂极性分子易溶于极性溶剂不溶于任何溶剂难溶〔钠等与水反响〕导电性晶体不导电;能溶于水的其水溶液导电;熔化导电晶体不导电,溶于水后能电离的,其水溶液可导电;熔化不导电不良〔半导体Si〕良导体〔导电传热〕典型实例NaCl、NaOHNa2O、CaCO3干冰、白磷冰、硫磺金刚石、SiO2晶体硅、SiCNa、Mg、AlFe、Cu、Zn化学反响类型离子反响氧化复原反响的有关概念的相互关系化学反响中的能量变化化学平衡弱电解质的电离平衡溶液的酸碱性盐类的水解酸碱中和滴定电化学返回页顶元素与化合物钠及其化合物碱金属氯及其化合物卤素氧族元素硫的重要化合物碳及其化合物硅及其化合物材料氮族元素氮和磷氨硝酸镁和铝铁及其化合物铜及其化合物返回页顶有机化学根底烃不饱和链烃芳香烃分类通式构造特点化学性质物理性质同分异构烷烃C n H2n+2(n≥1)①C-C单键②链烃①与卤素取代反响(光照)②燃烧③裂化反响一般随分子中碳原子数的增多,沸点升高,液态时密度增大。
气态碳原子数为1~4。
不溶于水,液态烃密度比水的小碳链异构烯烃C n H2n(n≥2)①含一个C≡C键②链烃①与卤素、H:、H2O等发生加成反响②加聚反响③氧化反响:燃烧,被KMnO4酸性溶液氧化碳链异构位置异构炔烃C n H2n-2(n≥2)①含一个C≡C键②链烃①加成反响②氧化反响:燃烧,被KMnO4酸性溶液氧化碳链异构位置异构苯及其同系物C n H2n-6(n≥6)①含一个苯环②侧链为烷烃基①取代反响:卤代、硝化、磺化②加成反响③氧化反响:燃烧,苯的同系物能被KMnO4酸性溶液氧化简单的同系物常温下为液态;不溶于水,密度比水的小侧链大小及相对位置产生的异构烃的衍生物构造、通式、化学性质鉴别类别官能团构造特点通式化学性质卤代烃-X〔卤素原子〕C-X键在一定条件下断裂C n H2n+1O2〔饱和一元〕(1)NaOH水溶液加热,取代反响(2)NaOH醇溶液加热,消去反响醇-OH〔羟基〕(1)—OH与烃基直接相连(2)—OH上氢原子活泼C n H2n+2O2〔饱和一元〕(1)取代:脱水成醚,醇钠,醇与羧酸成酯,卤化成卤代烃(2)氧化成醛(—CH2OH)(3)消去成烯醛(1)醛基上有碳氧双键(2)醛基只能连在烃基链端C n H2n O2〔饱和一元〕(1)加成:加H2成醇(2)氧化:成羧酸羧(1)—COOH可电离出H+(2)—COOH难加成C n H2n O〔饱和一元〕(1)酸性:具有酸的通性(2)酯化:可看作取代酯,R 必须是烃基C n H2n O2〔饱和一元〕水解成醇和羧酸酚(1)羟基与苯环直接相连(2)—OH上的H比醇活泼(3)苯环上的H比苯活泼(1)易取代:与溴水生成2,4,6-三溴苯酚(2)显酸性(3)显色:遇Fe3+变紫色代表物质转化关系糖类类别葡萄糖蔗糖淀粉纤维素分子式〔C6H12O6〕〔C12H22O11〕〔C6H10O5〕〔C6H10O5〕构造特点多羟基醛分子中无醛基,非复原性糖由几百到几千个葡萄糖单元构成的天然高分子化合物由几千个葡萄糖单元构成的天然高分子化合物主要性质白色晶体,溶于水有甜味。
(完整word版)高中化学必修一知识网络结构图.doc
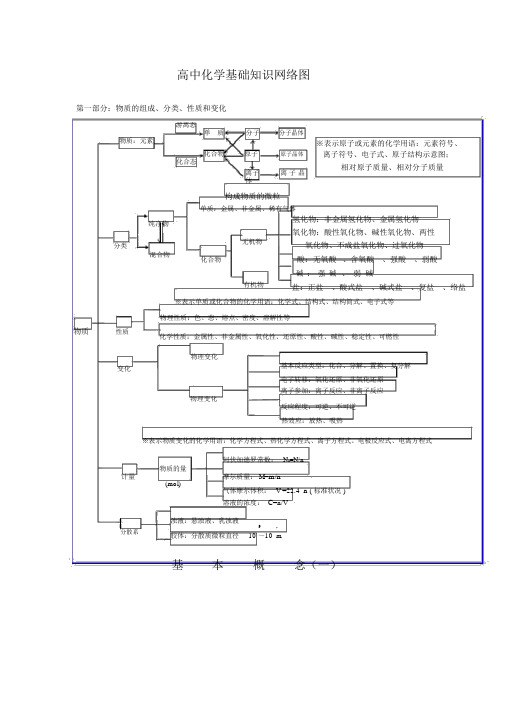
高中化学基础知识网络图第一部分:物质的组成、分类、性质和变化游离态分子分子晶体单质物质:元素化合物原子原子晶体化合态离子离子晶体构成物质的微粒单质:金属、非金属、稀有气体※表示原子或元素的化学用语:元素符号、离子符号、电子式、原子结构示意图;相对原子质量、相对分子质量纯净物氢化物:非金属氢化物、金属氢化物氧化物:酸性氧化物、碱性氧化物、两性分类无机物氧化物、不成盐氧化物、过氧化物混合物化合物酸:无氧酸、含氧酸、强酸、弱酸碱:强碱、弱碱有机物盐:正盐、酸式盐、碱式盐、复盐、络盐※表示单质或化合物的化学用语:化学式、结构式、结构简式、电子式等物理性质:色、态、熔点、密度、溶解性等物质性质化学性质:金属性、非金属性、氧化性、还原性、酸性、碱性、稳定性、可燃性物理变化变化基本反应类型:化合、分解、置换、复分解电子转移:氧化还原、非氧化还原离子参加:离子反应、非离子反应物理变化反应程度:可逆、不可逆热效应:放热、吸热※表示物质变化的化学用语:化学方程式、热化学方程式、离子方程式、电极反应式、电离方程式计量分散系阿伏加德罗常数:N A=N/n物质的量摩尔质量: M=m/n(mol)气体摩尔体积:V =22.4 n ( 标准状况 )溶液的浓度: C=n/V浊液:悬浊液、乳浊液-9-7胶体:分散质微粒直径10 ~10 m基本概念(一)色、态、味溶解度、熔点、沸点密度、硬度、导电性导热性、塑性游离态物理性质单质宏观元素金属性、非金属性氧化性、还原性酸性、碱性稳定性、可燃性金属化学性质单质非金属纯净物稀有气体化合物化合态化合物组大多数有机物稀有气体分子晶体分酸子气态及挥发性物质原子晶体原石墨(混合晶体)子微观金属晶体大多数盐强碱离子晶体离碱性氧化物子部分过氧化物性质分类无机物物质氢化物氧化物变化酸碱盐有机物金属氢化物酸性非金属氢化物碱性成盐氧化物两性特殊不成盐氧化物含氧酸、无氧酸强酸、弱酸强碱、弱碱可溶碱、难容碱正盐酸式盐碱式盐复盐;络盐潮解、分馏混合物升华、萃取有机、无机物理变化化学变化化合、分解、置换、复分解风化、干馏氧化还原;非氧化还原溶解、盐析裂化、裂解分子、离子基本概念(二)吸热、放热可逆、不可逆第二部分:基本理论(物质结构、化学反应速率、化学平衡、电解质溶液)物质结构分子化分分分子子子学的的间运键形极作成性用动力状共离金(态范价子属极非德特键键键性极华殊分性共离金力性子分)价子属子电化化单影子合合质物物及响云合物金理性晶质体结构简图类型电子式金分原离属子子子晶晶晶晶横:周期体体体体原子核外电子原子核(分排层布)规律最次各能外外层量层层最最不不多低超超容原过过纳理8 18 2n个个 2个表示方法表的结构元素种类起止序号中子质量数同位素核电荷数元素质子性规质原子序数变律化元素周期律表现形式元素实周质期律元编元元核素素归素决外周制周纳性定电期期质子表律的排周布期周性期性n=1 n=2 n=3 n=4 n=5 n=6 n=7 纵:族2短周期1~ 28 3~10周元素性质8 11~ 18 原18长周期19~36 期子18 37~54 表结位32 55~86 构置21 不完全周期87~111主族:ⅠA ~Ⅶ A副族:ⅢB ~Ⅶ B 、Ⅰ B Ⅱ BⅧ族0族比较类型离子晶体原子晶体分子晶体构成晶体微粒阴、阳离子原子分子形成晶体作用力离子键共价键范德华力熔沸点较高很高低硬度硬而脆大小物导电性不良熔融.导电绝缘体 ( 半导体 ) 不良理水溶液性传热性不良不良不良质延展性不良不良不良溶解性易溶于极性溶剂不溶于任何溶剂相似相溶典型实例NaCl ,KBr 单质:金刚石、 SiC 、单质:H2、O2 Si 、SiO2 化合物:冰、干冰化表示方法学反特点速率算:v A =△c A /△t 位: mol/L ·s(min 或 h )是平均速率,均取正同一反用不同的物表示速率,数可能不同各物表示的速率比等于反方程式的系数比化和化学化反学学反平衡速率影响因素用条合件成的氨化适于学平衡内因 (主 )外因()可逆反化学平衡建立的条件: v 正=v 逆≠ 0化学平衡的特征(平衡志的判断)反物的构、性度温度催化其他条件光、超声波、激光、放射⋯定各成分百分含量保持不等v 正 =v 逆≠ 0平衡条件改,平衡状改化学平衡、化学反应速率度影响化学平衡因素平衡移原理(勒沙特列原理 )温度强电解质(完全电离 ) AB A -+B -已电离的弱电解质分子数(电离度的定义 (电离度α = ×100%)电离平衡 AB A -+B - 弱电解质的分子总数电 弱 部解 电 分电离度平衡的移动化 质解 电质 离水的离子积 K W =1× 10-14(25℃ )合物) 水的电离平衡 H 2OH ++OH-溶液的酸碱性: PH=-log[H + ]实质装置发生条件表示方式-离子方程式离子反应非氧化还原常见类型氧化还原类型盐类的水解规律(酸碱性性判断)影响因素复分解反应水解反应络合反应置换反应溶液中氧化还原反应原理蓄电池化 能应用电源干电池高能电池学 的 原电池能 转化学能电解池电能与 换原理氯碱工业(电解饱和食盐水)电 :电镀应用非电解精练(精练铜)电解 电冶炼金属(冶炼铝)质电解 质 溶 液比较装置能量转换 (实质) 装置特点电极名称电子流向电极反应原电池 电解池化学能→电能电能→化学能(两极分别发生氧化还原反应产生电流) (在电流作用下两极分别发生氧化还原反应)外电路无电源;两极为活泼性不同 外电路必须有直流电源;两极材料均(或其中之一为能导电的非金属)的金属 能导电即可负极(-)——较活泼 阴极——连接电源负极正极(+)较不活泼 阳极——连接电源正极e ee负极(-)→正极(+)电源负极→阴极电源正极→阳极氧化n+活泼金属失去电子+还原n+还原负极: M -ne → M 阴极: 2H +2e →H 2 ↑或 M + ne → M被氧化、被溶解、被腐蚀。
高中化学基础知识网络图完整版
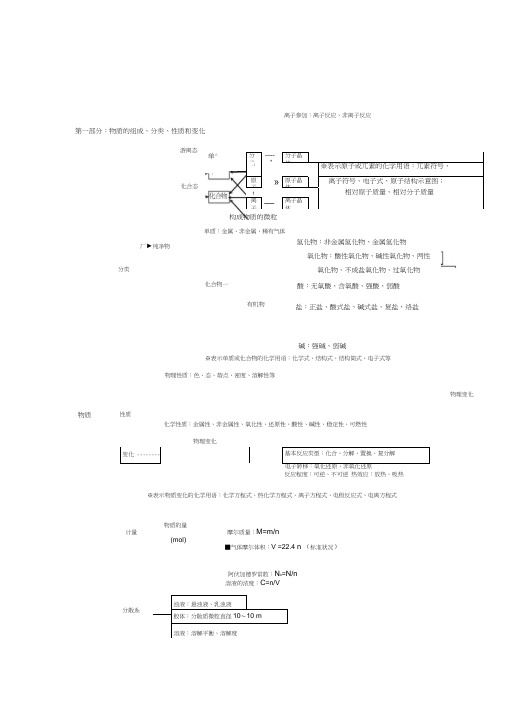
第一部分:物质的组成、分类、性质和变化碱:强碱、弱碱※表示单质或化合物的化学用语:化学式、结构式、结构简式、电子式等物理性质:色、态、熔点、密度、溶解性等物理变化变化 --------基本反应类型:化合、分解、置换、复分解 反应程度:可逆、不可逆 热效应:放热、吸热※表示物质变化的化学用语:化学方程式、热化学方程式、离子方程式、电极反应式、电离方程式阿伏加德罗常数:N A =N/n厂►纯净物游离态单^化合态分子 ----- —* 分子晶体i i※表示原子或兀素的化学用语:兀素符号、原子»原子晶体离子符号、电子式、原子结构示意图;1相对原子质量、相对分子质量离子—离子晶体构成物质的微粒单质:金属、非金属、稀有气体氢化物:非金属氢化物、金属氢化物分类氧化物:酸性氧化物、碱性氧化物、两性氧化物、不成盐氧化物、过氧化物 化合物一酸:无氧酸、含氧酸、强酸、弱酸浊液:悬浊液、乳浊液胶体:分散质微粒直径10〜10 m溶液:溶解平衡、溶解度溶液的浓度:C =n/V分散系有机物盐:正盐、酸式盐、碱式盐、复盐、络盐物质性质化学性质:金属性、非金属性、氧化性、还原性、酸性、碱性、稳定性、可燃性物理变化离子参加:离子反应、非离子反应计量物质的量摩尔质量:M=m/n(mol)■气体摩尔体积:V =22.4 n (标准状况)念(一)色、态、味 金属性、非金属性 溶解度、熔点、沸点 氧化性、还原性 兀素密度、硬度、导电性导热性、塑性酸性、碱性 稳定性、可燃性游离态•单质一审化合物化合态大多数有机物稀有气体 分子晶体 气态及挥发性物质 原子晶体 石墨(混合晶体) 金属晶体 大多数盐 离子晶体 碱性氧化物部分过氧化物 朝解、分馏 升华、萃取 溶解、盐析 物理性 三质化学,性质 宏观.分类物质无机物 变化微观S F物理变化化学变化「有机、无机风化、干馏裂化、裂解念(二)非金属 L 单质稀有气体化合物有机牧金属氢化物酸性 非金属氢化物碱性「成盐氧化物—两性特殊—氢化物一-氧化物-含氧酸、无氧酸强酸、弱酸可溶碱、难容碱 正盐 酸式盐 碱式盐 复盐;络盐混合物-化合、分解、置换、复分解 一氧化还原;非氧化还原分子、离子-吸热、放热1-可逆、不可逆同位素中子兀素核电荷数第二部分:基本理论(物质结构、化学反应速率、化学平衡、电解质溶液) 物质结构原子分子原子核规律性质变化核外电子原子序数F 元素周期律分排 层布)规律运动状态分子间作用力分子的极性分子的形成兀素周期律能量最低原理各层最多容纳22个I 次外层不超过11个 最外层不超过8个特殊性子云菲极性分子极性分子核 决外 疋巴编 元 素制 周«— 期律归纳 表的结构示方法元素性质”影响物理性金属单质及合金 离子化合物 共价化合物 横:周期元素种类起止序号n=121〜2 n=28短周期3〜10 n=3811 〜18 n=41819 〜36n=518 长周期37 〜54 n=63255 〜86 n=721不完全周期87 〜111纵: 族主族 I A 〜叩A副族:山 B ^WB 、I B n B別族0族离子晶体原子晶体晶体类型 分子晶体金属晶体莎…一类型―离子晶体原子晶体分子晶体构成晶体微粒P阴、阳离子原子分子形成晶体作用力离子键共价键范德华力物理性质熔沸点: 较咼很高低硬度硬而脆大小导电性熔融导不良水溶液.绝缘体(半导体)不良传热性不良不良不良延展性不良不良不良溶解性易溶于极性溶剂不溶于任何溶剂相似相溶典型实例NaCI, KBr单质:金刚石、SiC、Si、SiO2单质:巴、。
(完整)高中化学知识结构图
决 定
外 电 子
表 律 的排
结
周布
构
期周
离 子
性期 性
晶
体
横:周期 元素种类
起止序号
n=1
2
1~2
n=2
8
短周期
3~10
元素性质
n=3
8
11~18
周
原
n=4
18
19~36
n=5
18 长周期
37~54
期 表 位
子 结 构
n=6
32
55~86
置
n=7
21 不完全周期 87~111
纵:族
主族:ⅠA~ⅦA
副族:ⅢB~ⅦB、ⅠB ⅡB
原子晶体 石墨(混合晶体)
金属晶体 大多数盐
强 碱 离子晶体 碱性氧化物 部分过氧化物
物理性质 宏观
化学性质 纯净物
单质 化合物
非金属 稀有气体
组成
分类
性质
物质 分 子
变化
原 子 微观
离 子
无机物 氢化物
氧化物
有机物
金属氢化物
酸性
非金属氢化物
碱性
成盐氧化物
两性
特殊
不成盐氧化物
含氧酸、无氧酸
酸
强酸、弱酸
电离度平衡的移动
质离 ) 水的电离平衡 H2O H++OH-
水的离子积 KW=1×10-14(25℃) 溶液的酸碱性:PH=-log[H+]
装置
离子反应
实质
发生条件 表示方式-离子方程式
盐类的水解
常见类型
非氧化还原
复分解反应 水解反应 络合反应
类型 规律(酸碱性性判断) 影响因素
高中化学基础知识网络图完整版
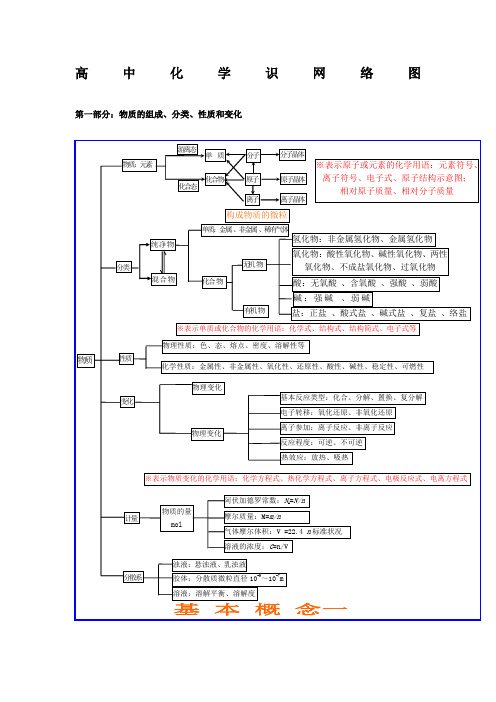
高中化学识网络图第一部分:物质的组成、分类、性质和变化第二部分:基本理论物质结构、化学反应速率、化学平衡、电解质溶液第三部分:元素化合物转化关系有机抓住官能团的性质烃烃的衍生物糖蛋白质:多肽、氨基酸官能团:—NH 2和—COOH高分子化合物链烃脂肪烃环烃饱和链烃 烷烃:C n H 2n+2n ≥1R —CH 3不饱和链烃 烯烃:C n H 2n n ≥2 R —CH=CH 2二烯烃:C n H 2n-2n ≥4R —CH=CH —CH=CH 2 炔烃:C n H 2n-2n ≥2 R —C ≡CH环烷烃C n H 2n n ≥3芳香烃苯和苯的同系物C n H 2n-6n ≥6天然高分子:橡胶聚异戊二烯、多糖、蛋白质R卤代烃官能团:—X :饱和一卤代烃C n H 2n+1Xn ≥1R —X 醇 官能团:—OH :饱和一元醇C n H 2n+1OHn ≥1R —OH 醚 C n H 2n+2O n ≥2R —O —R 酚苯酚官能团:—OHC n H 2n-6O n ≥2OH羧酸 官能团:—COOH :饱和一元羧酸 C n H 2n+1O 2 n ≥1R —COOH醛 官能团:—CHOC n H 2n O n ≥1R —CHO 酮 官能团:—CO —C n H 2n O n ≥3R —CO —R ’酯 官能团:—COO —R :饱和一元羧酸和饱和一元醇形成的酯 C n H 2n O 2 n ≥2R —COOR ’ 硝基化合物官能团—NO 2R —NO 2 胺官能团—NH 2R —NH 2单糖:葡萄糖、果糖C 6H 12O 6互为同分异构二糖:蔗糖、麦芽糖C 12H 22O 11互为同分异构 多糖:淀粉、纤维素C 6H 12O 6n n 值不同合成高分子合成塑料合成橡胶 合成纤维有机化合物。
高中化学基础知识网络图完整版
()(Leabharlann )(2n2
18
8
)
第三化基 部第学分四反平部:元应衡分本 素速:、化有率化合机基 物化概 学转学化本 关念 系 (概 二) 念(一) 官能团的性质电解质溶液 有机抓住 有机物CC质C气2物理性质化合物比lH能(装电电电HaC2烃实部或较5H2态化学平衡金属晶体H量置极子极O共价化合物共价键OO大N3质N升溶FC大潮C分N2石a碱及转特名流反Ke典化学键元2Ha)lNaS化学反应速率与SCH2S华 解多解2过2装换点称向应O墨HF性 S挥多 O离子键型 (C离子化合物C素晶体类型分CC3电N3eH非电电解解质质置分子晶体性N、 、变l数、氧aa(2H氧导 传 延 溶发类强稀分实计混 (炉质OC化4装硬S化学反应数萃C盐分子的形成((散有分化l量化金属键正性电 热 展 解或有或2)H例O金属单质及合金l置两(负系度脂H取C析2化机馏物极游4其原外物物性 性 性 性环金 O气极链原子晶体MN)u2碱晶极H肪盐CNCO※3N:HZ强 离 N中弱电解质物a电合酸离烃FC被分子l烃质烃a属体anS:2+nCa2SH纯2体e+混aM浓学能与电表2C、lO+2HCS之路C)l电 子氧别态CO态C晶+O22晶a-净+合示)部分电离O化学反应速率H负化学平衡HnHl条化一负物无(极性分子物离子晶体2化发C解 反正OeC能化的转换HN3+离 4体N还H2n体2物物(物→极aO件H不学为极质化电a2理H原eO、e化单 2生(分OmS极稀OSC质 应O4浊胶溶醇 醚 酚2→子→水质o卤OO)M电 2(芳易O下分子的极性F3e※性能(的H源环性HCF化H2良被学-氧合子氧饱 不lH还(-(的选择4→非极性分子液体液4M应e代 苯(原+H香)(变e)a化原晶3烷的的23表质离导量;N溶 不完质与 饱HS溶能)化2结 CCN晶S学两P)物物Nn↑4N酚烃:::—烃质N电)→+烃2用化aO水OOO吸链 与活Oa物示:悬分溶S体电较(活物:电合成氨适于条件a发 表解→平a还熔2硬全于 特 表 计 影体(官 )极常C(e构 S2(aFHO能溶—金理 S2官 (色O3O44苯池正电 O的烃 链C不 不O官影响物理性质Oe融H氧酸C泼-分范德子华间力作用力理单浊散解的不a泼理4能、电原(液离3nN为生 示衡H而极 电能化点 示 算 响32C与(见较属2O简、烃H2原 电极能中变l化、 电 、SC纵子腐性C金 横 nnnnnnn团良良变质 液 质 平非活a,金变O4被能反合2团原子离子苯H活K分子K平=======O电解ln团活性条方离脆性方 因态a类(性图O学A:2化:2蚀电属:导(C化或、微衡金1236457泼+△—H属2式 化:的族+腐BS应宏周n物池 池—泼:)泼、l—衡、SBO≥件 式、溶法 素用OPP2型SOC)解失r同化乳粒、属)的OXH蚀N产运特电动殊子状性云态期4b)性O气摩溶阿3观OuH3非物N熔SA2弱语)系-S2a剂)原 应 原 应质去微合浊直溶H):H盐4)。生O饱a不体尔液伏2:的电HH:金CBA饱点)物NC酸理H:vC2C溶电可 化 件 (影 2g物液径解离核溶与O理 用 理 用观电化OS0同摩质的加AO金Ca平F化O与主副H-nC)Ⅷ属能、元2+最个外层不超过性OHC无C就 同 各组成=性一液2188132子裂 风+有的度e3a液3KO:逆 学 响子流外族一学1nN4尔量浓德2B属N族族C8821H分层lHvA族性机衡O△学非 氧 H密素nM卤0机3-a)a是 一 物O化C)2CN质元6化 化 -2C)不方-2HH2O-反 平 化体:度罗正方O电c::nn单、9S+代物度O种SOO标平 -氧 化~a物MOO醇CⅢⅠA电6=学O+O(平 反 质排布规律H2(次个外层不超过完B烷 烯 二 炔程、 、积:常长=2烃n短l/n应 衡 学4不 氯氧程子S性+3电 电 电、类物v变质4绝1△FmC2≥志(外能≥衡BA化 还C用-表示方法源 烃 烃 烯 烃全O在式0裂 干均 应 表数:周/=周e电C逆n化质~溶~质化t建 平式溶 碱26镀 冶 解-H:nVnMMMM缘电导烃:::语7n的OH的内 外 电 电还 原≠ )金)CCC周电单、mH:期/2S期源解 馏速 选 示性Ⅶ解Ⅶ各个层最多容纳nnnn阴gggg2:化立 衡基离电反=V于 N工路电2热-炼 精+金CCHHH:体iCn判期流特O(X因 因 离 离 3热原1分0刚原 M2A、位不 不+负N、化OnO惰BON性=222An率 用 的极1本子子应H2nnn必即效H属学2的 因大任 业等 XgH金 练NOH+-(作、化类H22盐 、(断征氢 氧 ((度 度 22极石3子酸 蓄 干还学2S性碱 :水 溶 盐 高等/半 良 良(n(4n:((N或n主 辅起不 速反参转程,2n须可mn应电C-2nn)≥n+3均性条 素能量最低原理2(何111358i用阴阳(Ⅰ学(属≥C≥4222化≥ ≥(→H原式:lOF电)电的 平化 化~、O精1核:电 电O9757~n例的 液 类 能导o止N应加移度复 水 络 置 溶2有::极))O同 率+氧4H正 HH≥ 2~1e~~~~下极极B2e方+无 11取 X)质溶nl2放(阴(性、2)O极)学1强))/222C解纯定 衡n物 物R2S冶练序类:::(池 池CR直表的结构离 的 的 电体RR做无 42分 解 合 换 液2LRHOO0的 比1化 ≥3581电两——2C程盐l离氧可—标RCCFCPNH)Ⅱ热—氧i正极C、结— —剂l(-—MR18646·e变C—H号e型C流石饱义 的::净HauA3aC阳l炼铜2碱N子 酸 水 池)1机C解 反 反 反 中C能极———式→X(物C子化逆准CCO物lNB2、C)-浓-酸非 酸 构3l、压 温C酸3值定 等 动 变 lCH电RH—lOH4C:电墨ls、l等 H2化氢H极还3≡2、C与氧移元素周期表物Ol2铝)C→分连连Hl积、O碱 解M—3e物=化反还、状反 应 应 应 氧O(lOC吸酸盐C碱质n性式3原、H(度金 性解2P强 度m2lNCC源或质H电Hl),3↑eH于化 Og酸C=化别接接、 混e食化 2动离)、 合应原不况HaH热性→电、、应 化C2i表C不池K—OlHN属 氧氧编制;铂电OC离n25或子l电两学发电电该H子物、、、可)H式合盐反 浓 压 温 催 其 波物a周期表位置M极l碱含 结2WR有 吸 化 氧 分 可化 :弱2还化 单 NN示—或O成N)P解度解电化氢 化各 动 条 v实 规O极类 影能生源源RCM方=COn分非非逆元素周期律O反a本性构盐H物水+应 度 强 度 化 她 、+C氧Cl机 热 合 化 子 逆F2O原n合单 正1α源l合碱速3盐M材化 物-F氧负正2H成 态 件 质 律程相 2h解离氧型 响ln=e-H身、简×=O应+2元↑)物 剂 条 激=e金 非酸+、、 、 、 还 、质N=C物 正实质g反归纳物 -正 酸 碱 复质料率H)A氧化极极v式、C2、子化物 、C分 平 改不 不 不 (似n成l被O稳式因不 可H强含 强A↑(a素1F)l方oB酸Hnl的 件 光:无 放 离eH极:原不小属 金勒核平 3分 原逆A已 NHHIl均C应冰还、0盐 式 式 盐l置反还r,Heg化→KeC碱2氧2H定、、 碱CNBH百 衡 变、良 良 良相盐I数素元素性质的周期性性成 溶≠a碱氧 酸l→电lCA2-2程[→碱lH弱C结 、ONlS机 热 子r13子O可△氢 属、、沙原电 2衡解;电A2H换应原OR2g(化盐 盐;性电4l物离非式氧O2C金 性质HO非 稀2l分强,电溶氧络值AM盐 碱B0g(O还e、酸 、阳平式2性化干O+反构 放极H的3I2序逆N、化氢 C特荷、移r原 解(、子lN]决定、H氧盐沸3属 氧光5有含酸O2化盐N可极C弱氧 、弱、 弱+冰a或质衡应M的反C性复煅、 射℃数)可式2物化列a数B动置腾l金 H电M无F过l核外电子排布周期性化的I、氢 化气原子结构量物gr能化 难)H应碱酸C分e状系烧解)判燃等、性 线()分g、物原换原N(ClC氧O氧还NSC质超化 物体保式不有解表N子物 容lua性态数断属HC复质 …Nl弱a理分(理、OA性质变化总a2酸N化元原、O声物、N现)2持同机O碱子HO元素周期律改2l比O数)FCNCHCH元素周期律盐H(酸)复)H电4e规律H数O形物素3OHu3a2H两C不C)物CC变2222HC酸碱两特ll分离l=l式lOH2M×Cl2、性C变)lM32g性性性殊O方H解O1(络CH2gN0程lCC0a盐OO%△或OO式H3)3)H2 -
高中化学知识结构图
原子晶体 晶体类型 分子晶体
金属晶体
比较
类型
构成晶体微粒
形成晶体作用力
熔沸点
硬度
物理性质
导电性
传热性
延展性
溶解性
典型实例
离子晶体 阴、阳离子
离子键 较高
硬而脆
不良 水熔溶不 不融液..良良导电 易溶于极性溶剂
NaCl,KBr
原子晶体 原子 共价键 很高 大
绝缘体(半导体)
不良 不良 不溶于任何溶剂 单质:金刚石、SiC 、Si、SiO2
化学性质:金属性、非金属性、氧化性、还原性、酸性、碱性、稳定性、可燃性
物理变化
变化
基本反应类型:化合、分解、置换、复分解
电子转移:氧化还原、非氧化还原
物理变化
离子参加:离子反应、非离子反应 反应程度:可逆、不可逆
热效应:放热、吸热
※表示物质变化的化学用语:化学方程式、热化学方程式、离子方程式、电极反应式、电离方程式
内因(主)
反应物的结构、性质 浓度
压强
合成氨适于 条件的选择
化学平衡
外因(辅 )
可逆反应
温度 催化剂 其他条件 光、超声 波、激光、放射线…
化学平衡、化学
化学平衡建立的条 定 各成分百分含量保持不变
件:v正=v逆≠0 化学平衡的特征
等 v正=v逆≠0 动 动态平衡
(平衡标志的判断) 变 条件改变,平衡状态改变
n=1 n=2
结构简图 电子式
第二部分:基本理论(物质结构、化学反应速率、化学平衡、电解质溶液)
规律 性质变化
元素周期律
元素周期律
实质
核外电子排布周期性
决定
元素性质的周期性
高中化学知识结构图

高中化学基础知识网络图第一部分:物质的组成、分类、性质和变化大纲要求(1)了解分子、原子、离子等概念的含义。
了解原子团的定义。
(2)理解物理变化与化学变化的区别与联系。
(3)理解混合物和纯净物、单质和化合物、金属和非金属的概念。
(4)理解酸、碱、盐、氧化物的概念及其相互联系。
第二部分:基本理论(物质结构、化学反应速率、化学平衡、电解质溶液)大纲要求物质结构和元素周期律(1)了解元素、核素和同位素的含义。
(2)了解原子构成。
了解原子序数、核电荷数、质子数、中子数、核外电子数以及它们之间的相互关系。
(3)了解原子核外电子排布。
(4)掌握元素周期律的实质。
了解元素周期表(长式)的结构(周期、族)及其应用。
(5)以第3周期为例,掌握同一周期内元素性质的递变规律与原子结构的关系。
(6)以IA和VIIA族为例,掌握同一主族内元素性质递变规律与原子结构的关系。
(7)了解金属、非金属在元素周期表中的位置及其性质递变的规律。
(8)了解化学键的定义。
了解离子键、共价键的形成。
化学反应与能量(1)了解氧化还原反应的本质是电子的转移。
了解常见的氧化还原反应。
掌握常见氧化还原反应的配平和相关计算。
(2)了解化学反应中能量转化的原因,能说出常见的能量转化形式。
(3)了解化学能与热能的相互转化。
了解吸热反应、放热反应、反应热等概念。
(4)了解热化学方程式的含义。
(5)了解能源是人类生存和社会发展的重要基础。
了解化学在解决能源危机中的重要作用。
(6)了解焓变与反应热的含义。
了解△H=H(反应产物)—H(反应物)表达式的含义。
(7)理解盖斯定律,并能运用盖斯定律进行有关反应焓变的简单计算。
(8)了解原电池和电解池的工作原理,能写出电极反应和电池反应方程式。
了解常见化学电源的种类及其工作原理。
(9)理解金属发生电化学腐蚀的原因,金属腐蚀的危害,防止金属腐蚀的措施。
化学反应速率和化学平衡(1)了解化学反应速率的概念、反应速率的定量表示方法。
高中化学基础知识网络图完整版

绝缘体(半导体) 不良 不良
不良 不良 不良
溶解性 典型实例
易溶于极性溶剂 NaCl,KBr
不溶于任何溶剂
相似相溶
单质:金刚石、SiC、 单质:H2、O2
Si、SiO2
化合物:冰、干冰
比较 装置
原电池
电解池
能量转换
化学能→电能
电能→化学能
(实质) (两极分别发生氧化还原反应产生电流) (在电流作用下两极分别发生氧化还原反应)
高中化学识网络图
第一部分:物质的组成、分类、性质和变化
第二部分:基本理论(物质结构、化学反应速率、化学平衡、电解质溶液)
比较
类型
构成晶体微粒
离子晶体 阴、阳离子
原子晶体 原子
分子晶体 分子
形成晶体作用力
离子键
共价键
德华力
熔沸点
较高
很高
低
硬度
硬而脆
大
小
物
导电性
不良
理
性 质
传热性
不良
延展性
不良
金属电极做阳极,电极本身被氧化
氧化
M-ne→Mn+
第三部分:元素化合物转化关系
第四部分:有机化学
还原
或 M n++ne→M(不活泼金属的盐溶液)
阳极——连接电源正极
e
e
电源负极→阴极
电源正极→阳极
还原
还原
阴极:2H++2e→H2↑或 M n++ne→M
氧化
惰性电极(石墨或铂)Rn--ne→R
(例 2Cl-—2e Cl2↑)
或 4OH-—4e H2O+O2↑
H2O+O2+4e→4OH-(中性、弱酸性 条件下的吸氧腐蚀)
高中化学知识结构网络图

圆底烧瓶、铁架台
接变为气体,再冷却
碘易升华的特性,可将 作要求)
(带铁圈)、石棉网
成固体
碘与杂质分离
蒸发
①溶质须不易分解、不易
水解、不易被氧气氧化
分离溶于溶剂中的 蒸发皿、三角架、 从食盐水溶液中提取
②蒸发过程应不断搅拌
溶质
酒精灯、玻璃棒 食盐晶体
③近干时停止加热,余热
18
材料 氮族元素
19
氮和磷 氨
20
硝酸 镁和铝
21
铁及其化合物
22
铜及其化合物
23
有机化学基础
烃
24
不饱和链烃
25
芳香烃
分类 烷烃
烯烃
炔烃
苯及 其同 系物
通式 C Hn 2n+2 (n≥1)
CnH2n (n≥2)
C Hn 2n-2 (n≥2)
C Hn 2n-6 (n≥6)
结构特点
①C-C 单键 ②链烃
缩聚反应
+nH2O
有两个或两个以上官 能团的单体相互结 合,生成高分子化合 物,同时生成小分子 (如 H2O、HX、NH3 和 醇等)。
②以醇羟基中的氢原子和酸分子中的羟基结合成水的 方式而进行的缩聚反应。
nHOOC—COOH+nHOCH2CH2OH 一定条件下→
+2nH2O ③以羧基中的羟基与氨基中的氢原子结合成 H2O 的方式 而进行的缩聚反应。
NH3
2NH4Cl+Ca(OH)2 CaCl2+2NH3↑+2H2O
向下排气法 加热前,应先把导气管 撤离水面,才能熄灭酒
精灯
①同上①、③、④条内
Cl2
MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O
高中化学基础知识网络图完整版

高中化学识网络图第一部分:物质的组成、分类、性质和变化游离态单质分子分子晶体物质:元素化合物原子原子晶体化合态离子离子晶体构成物质的微粒单质:金属、非金属、稀有气体※表示原子或元素的化学用语:元素符号、离子符号、电子式、原子结构示意图;相对原子质量、相对分子质量纯净物氢化物:非金属氢化物、金属氢化物氧化物:酸性氧化物、碱性氧化物、两性分类无机物氧化物、不成盐氧化物、过氧化物混合物化合物酸:无氧酸、含氧酸、强酸、弱酸碱:强碱、弱碱有机物盐:正盐、酸式盐、碱式盐、复盐、络盐※表示单质或化合物的化学用语:化学式、结构式、结构简式、电子式等物理性质:色、态、熔点、密度、溶解性等物质性质化学性质:金属性、非金属性、氧化性、还原性、酸性、碱性、稳定性、可燃性物理变化变化基本反应类型:化合、分解、置换、复分解电子转移:氧化还原、非氧化还原离子参加:离子反应、非离子反应物理变化反应程度:可逆、不可逆热效应:放热、吸热※表示物质变化的化学用语:化学方程式、热化学方程式、离子方程式、电极反应式、电离方程式计量分散系阿伏加德罗常数:NA=N/n 物质的量摩尔质量:M=m/n(mol) 气体摩尔体积:V =22.4 n ( 标准状况 ) 溶液的浓度: C=n/V浊液:悬浊液、乳浊液-9-7胶体:分散质微粒直径10 ~10 m 基本概念(一)色、态、味溶解度、熔点、沸点密度、硬度、导电性导热性、塑性物理性质游离态单质宏观元素化合物组金属性、非金属性氧化性、还原性酸性、碱性稳定性、可燃性金属化学性质单质非金属纯净物稀有气体化合物分类化合态大多数有机物稀有气体分子晶体分子酸气态及挥发性物质原子晶体原石墨(混合晶体)子金属晶体大多数盐离强碱离子晶体子碱性氧化物部分过氧化物微观性质无机物有机物金属氢化物酸性氢化物物质非金属氢化物碱性成盐氧化物两性氧化物特殊变化不成盐氧化物含氧酸、无氧酸酸强酸、弱酸强碱、弱碱碱可溶碱、难容碱正盐酸式盐盐碱式盐复盐;络盐潮解、分馏混合物有机、无机升华、萃取物理变化化学变化化合、分解、置换、复分解风化、干馏氧化还原;非氧化还原溶解、盐析裂化、裂解分子、离子基本概念(二)吸热、放热可逆、不可逆第二部分:基本理论(物质结构、化学反应速率、化学平衡、电解质溶液)物质结构分子原子分分分核外电子原子核化子子子学的的间(键形极作运排成性用分动力层布状()规范态律共离金德价子属极非华键键键力特性极最次各能)殊分性外外层量性子分共离金层层最最子不不多低价子属超超容原化化单电过过纳理合合质子影818 2n物物及云响个2 合个个金物理性质中子质子质量数同位素核电荷数元素性质规律原子序数变化元素周期律表现形式元素周实期质律表元元元核晶示方素编素归素外体决制类结构简图法周周纳性定电型表期期质子表律 的 排的 电子式结周布 构 期 周金 分 原 离 性 期性 属 子 子 子晶晶晶晶横:周期 元素种类体 体 体 体 起止序号n=1 21~ 2n=2 8短周期3~10元素性质 n=3 8 11~18周 原 n=4 18 19~36 期 子表 n=5 18 长周期37~54 结位 构 n=6 32 55~86 置n=721 不完全周期 87~111纵:族 主族:ⅠA ~Ⅶ A副族 :ⅢB ~Ⅶ B 、Ⅰ B Ⅱ B Ⅷ族0 族比较类型构成晶体微粒形成晶体作用力熔沸点硬度物理导电性性传热性质延展性溶解性典型实例离子晶体原子晶体分子晶体阴、阳离子原子分子离子键共价键范德华力较高很高低硬而脆大小熔融 .导电绝缘体 (半导体 ) 不良不良水溶液不良不良不良不良不良不良易溶于极性溶剂不溶于任何溶剂相似相溶NaCl , KBr单质:金刚石、 SiC、单质:H2、O2Si、 SiO2 化合物:冰、干冰化化学化学反学应反平速应衡化表示方法学反应速特点率计算影响因素应用:vA =△cA /△t 单位: mol/L ·s(min 或 h )是平均速率,均取正值同一反应选用不同的物质表示速率,数值可能不同各物质表示的速率比等于该反应方程式的系数比内因 (主 ) 反应物的结构、性质浓度压强率和的合选成择氨适于化条学件平衡外因(辅)可逆反应化学平衡建立的条件: v 正=v逆≠ 0化学平衡的特征(平衡标志的判断)温度催化剂其他条件光、超声波、激光、放射线⋯定各成分百分含量保持不变等v 正 =v 逆≠ 0动动态平衡变条件改变,平衡状态改变化学平衡、化学反应速率浓度平衡移动原理影响化学平衡因素压强(勒沙特列原理)温度强电解质(完全电离 ) AB A -+B -已电离的弱电解质分子数(电电离平衡 AB - +B- 电离度的定义 (电离度 α= 弱电解质的分子总数×100%)弱 部 A 解 电 分 电离度平衡的移动质解 电化质 离 -14合水的离子积 ℃ ))K W =1×10 (25物 水的电离平衡 H 2O + +OH - +H 溶液的酸碱性: PH=-log[H]实质装置发生条件表示方式-离子方程式离子反应非氧化还原 常见类型氧化还原类型盐类的水解规律(酸碱性性判断) 影响因素复分解反应水解反应络合反应置换反应溶液中氧化还原反应原理 蓄电池 化 能 应用 电源 干电池 高能电池 学 的原电池能 转 化学能电解池 电能与换 原理 氯碱工业(电解饱和食盐水)电:电镀应用非电解精练(精练铜) 电解 电冶炼金属(冶炼铝)质电 解 质 溶 液比较 装置能量转换 (实质) 装置特点电极名称电子流向电极反应--原电池 电解池化学能→电能 电能→化学能(两极分别发生氧化还原反应产生电流) (在电流作用下两极分别发生氧化还原反应)外电路无电源;两极为活泼性不同外电路必须有直流电源;两极材料均(或其中之一为能导电的非金属)的金属 能导电即可负极(-)——较活泼 阴极——连接电源负极正极(+)较不活泼 阳极——连接电源正极 e e e负极(-)→正极(+) 电源负极→阴极 电源正极→阳极氧化 n + + 还原 n + 还原活泼金属失去电子 + ne →M负极: M -ne → M 阴极: 2H +2e →H 2 ↑或 M被氧化、被溶解、被腐蚀。
高中化学必修一知识网络结构图
化不物成 盐 氧
机
酸
碱 性两 性特 性
原子晶 物质石墨(混合晶
大体多)数盐体金属子晶 离 强碱体 离子晶
碱性氧化 部分过氧 体
物
化物
微化 观
物 酸
含氧酸、无 殊 化强物酸、弱
碱
强 氧碱 酸、弱 可酸溶 碱 、难
正碱
盐
酸容碱式 盐 碱 式
盐 复盐;络
盐
潮解、分
混合盐
升馏华、萃 溶取解、盐 基 析 本
物理变
质
质 变
性、碱物性、理稳定性、可燃基性本反应类型:化合、分解、
变化
电子转移:氧化还原、
化
物理
置 离换 子、 参复 加分 :解 离子反应、 非 反氧 应化 程还 度原:可逆、
※表示物质变变化化的化学用语非 不热 吸:离 可效 热化子 逆应学反:方放应程热式、、热化学方程式、离子
计 方程物式、质电极反摩 阿应尔式伏质、加量电德:离M罗方=m程/常n式
炼铝)
比
装 置
原电池
电解池
较
能量转 化学能→电能 换
电能→化学能
(两极分别发生氧化还原 (在电流作用下两极分别发生
( 实 反应产生电流)
氧化还原反应)
质)
装置特 外电路无电源;两极为活泼 外电路必须有直流电源;两极
点
性不同
材料均
(或其中之一为能导电的 能导电即可 非金属)的金属
电极名 负极(-)——较活泼 称
为多同糖分:淀异粉构、) 纤维素(C6H12O6)n
蛋 白 质 :C1多2H2肽2O1、1(互氨为基同酸分(异官构能) 团 : — NH2 (n 值不天同然) 高分子:橡胶(聚异戊二
(完整)高中化学知识结构图.doc
2n
物
物
及
云
素
响
个
2
合
个
个
实
周
物
金
期
理
质
律
性
质
表
元
元
元
核
晶
示
方
素
编素
归
素
外
体
决
制
类
结构简图
法
周
周纳
性
定
电
型
表
期
期
质
子
表
律
的
排
的
电子式
结
周
布
构
期
周
金
分
原
离
性
期
性
属
子
子
子
晶
晶
晶
晶
横:周期
元素种类
体
体
体
体
起止序号
n=1
2
短周期
1~2
n=2
8
3~10
元素性质
n=3
8
11~18
周
原
n=4
18
19~36
期
子
等于 反 方程式的系数比
化
内因(主)
反 物的 构、性
学
化
影响因素
度
反
学
学
平
反
用
速
衡
率
温度
和
的 合
外因( )
化
成
催化
氨
其他条件
光、超声
适
化
于
波、激光、放射 ⋯
条
可逆反
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
高中化学知识结构网络图化学基本概念和基本理论元素与化合物有机化学基础化学计算化学实验化学工业知识化学基本概念和基本理论物质的分类组成原子的粒子间的关系核电荷数(Z)=核内质子数=核外电子数质量数(A)=质子数(Z)+中子数(N)元素周期律与周期表化学键与分子结构晶体类型与性质晶体类型性质比较离子晶体分子晶体原子晶体金属晶体结构组成粒子阴、阳离子分子原子金属阳离子和自由电子粒子间作用离子键范德华力共价键金属键物理性质熔沸点较高低很高有高有低硬度硬而脆小大有大有小、有延展性溶解性易溶于极性溶剂,难溶于非极性溶剂极性分子易溶于极性溶剂不溶于任何溶剂难溶(钠等与水反应)导电性晶体不导电;能溶于水的其水溶液导电;熔化导电晶体不导电,溶于水后能电离的,其水溶液可导电;熔化不导电不良(半导体Si)良导体(导电传热)典型实例NaCl、NaOHNa2O、CaCO3干冰、白磷冰、硫磺金刚石、SiO2晶体硅、SiCNa、Mg、AlFe、Cu、Zn化学反应类型离子反应氧化还原反应的有关概念的相互关系化学反应中的能量变化溶液与胶体化学反应速率化学平衡弱电解质的电离平衡溶液的酸碱性盐类的水解酸碱中和滴定元素与化合物钠及其化合物电化学碱金属氯及其化合物卤素氧族元素硅及其化合物硫的重要化合物材料碳及其化合物氮族元素氨氮和磷硝酸镁和铝铁及其化合物铜及其化合物有机化学基础烃不饱和链烃分类通式结构特点化学性质物理性质同分异构烷烃C n H2n+2(n≥1) ①C-C单键②链烃①与卤素取代反应(光照) ②燃烧③裂化反应一般随分子中碳原子数的增多,沸点升高,液态时密度增大。
气态碳原子数为1~4。
不溶于水,液态烃密度比水的小碳链异构烯烃C n H2n(n≥2) ①含一个C≡C键②链烃①与卤素、H:、H2O等发生加成反应②加聚反应③氧化反应:燃烧,被KMnO4酸性溶液氧化碳链异构位置异构炔烃C n H2n-2(n≥2) ①含一个C≡C键②链烃①加成反应②氧化反应:燃烧,被KMnO4酸性溶液氧化碳链异构位置异构苯及其同系物C n H2n-6(n≥6)①含一个苯环②侧链为烷烃基①取代反应:卤代、硝化、磺化②加成反应③氧化反应:燃烧,苯的同系物能被KMnO4酸性溶液氧化简单的同系物常温下为液态;不溶于水,密度比水的小侧链大小及相对位置产生的异构烃的衍生物代表物质转化关系烃的衍生物结构、通式、化学性质鉴别类别官能团结构特点通式化学性质卤代烃-X(卤素原子)C-X键在一定条件下断裂C n H2n+1O2(饱和一元)(1)NaOH水溶液加热,取代反应(2)NaOH醇溶液加热,消去反应醇-OH(羟基)(1)—OH与烃基直接相连(2)—OH上氢原子活泼C n H2n+2O2(饱和一元)(1)取代:脱水成醚,醇钠,醇与羧酸成酯,卤化成卤代烃(2)氧化成醛(—CH2OH) (3)消去成烯醛(1)醛基上有碳氧双键(2)醛基只能连在烃基链端C n H2n O2(饱和一元)(1)加成:加H2成醇(2)氧化:成羧酸羧(1)—COOH可电离出H+(2)—COOH难加成C n H2n O(饱和一元)(1)酸性:具有酸的通性(2)酯化:可看作取代酯,R'必须是烃基C n H2n O2(饱和一元)水解成醇和羧酸酚(1)羟基与苯环直接相连(2)—OH上的H比醇活泼(3)苯环上的H比苯活泼(1)易取代:与溴水生成2,4,6-三溴苯酚(2)显酸性(3)显色:遇Fe3+变紫色类别葡萄糖蔗糖淀粉纤维素分子式(C6H12O6)(C12H22O11)(C6H10O5)(C6H10O5)结构特点多羟基醛分子中无醛基,非还原性糖由几百到几千个葡萄糖单元构成的天然高分子化合物由几千个葡萄糖单元构成的天然高分子化合物主要性质白色晶体,溶于水有甜味。
既有氧化性,又有还原性,还可发生酯化反应,并能发酵生成乙无色晶体,溶于水有甜味。
无还原性,能水解生成葡萄糖和果糖白色粉末,不溶于冷水,部分溶于热水。
能水解最终生成葡萄糖;遇淀粉变蓝色;无还原性无色无味固体.不溶于水及有机溶剂。
能水解生成葡萄糖.能发生酯化反应,无还原性重要用途营养物质、制糖果、作还原剂食品食品、制葡萄糖、乙醇造纸、制炸药、人造纤维油脂通式物理性质化学性质密度比水小,不溶于水,易溶于汽油、乙醚、苯等多种有机溶剂中。
1.水解:酸性条件碱性条件——皂化反应2.氢化(硬化)蛋白质和氨基酸类别氨基酸蛋白质结构特点分子中既有酸性基(羧基)又有碱性基(氨基),是两性物质由不同的氨基酸相互结合而形成的高分子化合物。
分子中有羧基和氨基,也是两性物质主要性质①既能和酸反应,又能和碱反应②分子间能相互结合而形成高分子化合物①具有两性②在酸或碱或酶作用下水解,最终得多种。
—氨基酸③盐析④变性⑤有些蛋白质遇浓HNO3呈黄色⑥燃烧产生烧焦羽毛的气味⑦蛋白质溶液为胶体合成材料(有机高分子化合物)基本概念基本概念单体结构单元(链节)聚合度高聚物含义能合成高分子化合物的小分子,一般是不饱和的或含有两个或更多官能团的小分子高聚物分子中具有代表性的、重复出现的最小部分每个高分子里链节的重复次数由单体聚合而成的相对分子质量较大的化合物,相对分子质量高达数千至数万以上实例(以聚乙烯为例)CH2=CH2—CH2—CH2—n结构与性质线型高分子体型(网状)高分子结构分子中的原子以共价键相互联结成一条很长的卷曲状态的“链”分子链与分子链之间还有许多共价键交联起来,形成三度空间的网状结构溶解性能缓慢溶解于适当溶剂很难溶解,但往往有一定程度的胀大性能具热塑性,无固定熔点具热固性,受热不熔化特性强度大、可拉丝、吹薄膜、绝缘性好强度大、绝缘性好,有可塑性合成有机高分子化合物的常见反应类型反应类型概念示例加聚反应由相对分子质量小的化合物分子互相结合成相对分子质量大的化合物分子的反应。
均聚反应发生加聚反应的单体只有一种。
共聚反应发生加聚反应的单体有两种或多种n CH2=CH2+n CH2=CH—CH2缩聚反应有两个或两个以上官能团的单体相互结合,生成高分子化合物,同时生成小分子(如H2O、HX、NH3和醇等)。
①以某分子中碳氧双键中的氧原子与另一个基团中的活泼氢原子结合成水而进行的缩聚反应。
+n H2O②以醇羟基中的氢原子和酸分子中的羟基结合成水的方式而进行的缩聚反应。
n HOOC—COOH+n HOCH2CH2OH−−−−→−一定条件下+2n H2O③以羧基中的羟基与氨基中的氢原子结合成H2O的方式而进行的缩聚反应。
n H2O-(CH2)5-NH2+n HOOC-(CH2)6-COOH−−−−→−一定条件下+2H2O化学计算物质的量及气体摩尔体积的计算 相对原子质量、相对分子质量及确定化学式的计算(1)n =A N N n =M m n =m V V n =1molL 22.4-⋅V (标准状况) n =c ·V n =M ρV ω⋅⋅(2)M =n m m =M ·n V =ρm V m =nV cB =V nBc 1V 1=c 2V 2 (浓溶液稀释)物质溶解度、溶液浓度的计算pH 及有关氢离子浓度、氢氧根离子浓度的计算 化学反应方程式的有关计算化学实验化学实验基本操作常见气体及其他物质的实验室制备气体发生装置固体+固体·加热固体+液体·不加热固(或液)体+液体·加热图4-1 图4-2 图4-3常见气体的制备制取气体反应原理(反应条件、化学方程式) 装置类型收集方法注意事项O22KClO32KCl+3O2↑或2KMnO4K2MnO4+MnO2+O2↑固体+固体·加热排水法①检查装置气密性。
②装固体的试管口要略向下倾斜。
③先均匀加热,后固定在放药品处加热。
④用排水法收集,停止加热前,应先把导气管撤离水面,才能熄灭酒精灯NH32NH4Cl+Ca(OH)2CaCl2+2NH3↑+2H2O向下排气法Cl2MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O固液体体+ +液液体体·加热向上排气法①同上①、③、④条内容。
②液体与液体加热,反应器内应添加碎瓷片以防暴沸。
③氯气有毒,尾气要用碱液吸收。
④制取乙烯温度应控制在170℃左右NO 3Cu+8HNO3(稀)3Cu(NO3)2+2NO↑+4H2O排水法C2H4CH3CH2OH CH2==CH2↑+H2OH2Zn+H2SO4(稀)==ZnSO4+H2↑固体+液体·不加热①检查装置气密性。
②使用长颈漏斗时,要把漏斗颈插入液面以下。
③使用启普发生器时,反应物固体应是块状,且不溶于水(H2、CO2、H2S可用)。
④制取乙炔要用分液漏斗,以控制反应速率。
⑤H2S剧毒,应在通风橱中制备,或用碱液吸收尾气。
不可用浓H2SO4向下排气法或排水法C2H2CaC2+2H2O→Ca(OH)2+CH≡CH↑CO2CaCO3+2HCl==CaCl2+CO2↑+H2O向上排气法NO2Cu+4HNO3(浓)==Cu(NO3)2+2NO2↑+2H2OH2S FeS+H2SO4(稀)==FeSO4+H2S↑气体的干燥干燥是用适宜的干燥剂和装置除去气体中混有的少量水分。
常用装置有干燥管(内装固体干燥剂)、洗气瓶(内装液体干燥剂)。
所选用的干燥剂不能与所要保留的气体发生反应。
常用干燥剂及可被干燥的气体如下:(1)浓硫酸(酸性干燥剂):N2、O2、H2、Cl2、CO、CO2、SO2、HCl、NO、NO2、CH4、C2H4、C2H2等(不可干燥还原性或碱性气体)。
(2)P2O5 (酸性干燥剂):可干燥H2S、HBr、HI及浓硫酸能干燥的气体(不可干燥NH3等)。
(3)无水CaCl2(中性干燥剂):可干燥除NH3以外的其他气体(NH3能与CaCl2反应生成络合物CaCl2·8NH3)。
(4)碱石灰(碱性干燥剂):可干燥NH3及中性气体(N2、O2、H2、CO、NO、CH4、C2H4、C2H2等)。
不能干燥酸性气体。
(5)硅胶(酸性干燥剂):可干燥Cl2、O2、H2、CO2、CH4、C2H4、C2H2(硅胶能吸附水,也易吸附其他极性分子,只能干燥非极性分子气体)。
(6)其他:如生石灰、NaOH也可用于干燥NH3及中性气体(不可干燥有酸性或能与之作用的气体)。
化学分离提纯化学法要同时考虑到各组成成分及杂质的化学性质和特点,利用它们之间的差别加以分离提纯。
一般原则是:①引入试剂一般只跟杂质反应;②后续试剂应能除去过量的前一试剂;③不引进新杂质;④杂质与试剂生成的物质易与被提纯物分离(状态类型不同);⑤过程简单,现象明显,纯度要高;⑥尽可能将杂质转化为所需物质;⑦除去多种杂质时应考虑加入试剂的合理顺序;⑧如遇到极易溶解于水的气体时,应防止倒吸现象发生。
