有关镁铝的_图像计算
图像加镁铝计算

图像加镁铝计算1、向AlCl3溶液中逐滴滴入NaOH溶液至过量向NaOH溶液中逐滴滴入AlCl3溶液至过量2、向AlCl3溶液中逐滴滴入氨水至过量3.向AlCl3溶液中逐滴滴入NaAlO2溶液至过量向NaAlO2溶液中逐滴滴入AlCl3溶液至过量4.向NaAlO2溶液中逐滴滴入盐酸至过量向盐酸中逐滴滴入NaAlO2溶液至过量5、向NaAlO2溶液中通入过量的CO29、向MgCl2、AlCl3和盐酸的混合液中滴加NaOH 溶液至过量10、向明矾[KAl(SO4)2·12H2O]溶液中逐滴加入Ba(OH)2溶液至过量。
(1)写出可能发生的有关反应的化学方程式;画出下列图像(2)在下图中,纵坐标表示生成沉淀的物质的量,横坐标表示加入Ba(OH)2溶液的物质的量。
试在下图中画出当溶液中明矾为1 mol 时,生成的每一种沉淀的物质的量随Ba(OH)2物质的量的变化曲线(在曲线上标明沉淀的化学式)。
(3)当向a L M mol / L 的明矾溶液中滴加N mol/L 的Ba(OH)2溶液b L ,用含a 、M 、N 的代数式表示:① 当b 满足________________条件时,沉淀的总的物质的量为最大值;② 当b 满足___________________条件时,沉淀的质量为最大值。
11.向Al 2(SO 4)3和MgSO 4的混合溶液中滴加NaOH 溶液,生成沉淀的量与滴入NaOH 溶液的体积关系如图所示。
则原混合液中Al 2(SO 4)3与MgSO 4的物质的量之比为 ( )A . 6∶1B . 3∶1C .2∶1D .1∶212. 将100mL 1L mol 6.0-⋅氯化铝溶液跟1L mol 4.0-⋅苛性钠溶液混合后,得到3)OH (Al g 9.3沉淀,此时消耗苛性钠溶液的体积是( )A. 250mLB. 375mLC. 475mLD. 500mL13. 将g7.2铝溶解于100mL 1L⋅NaOH溶液中,3-mol然后向所得溶液中加入1400-⋅的盐酸,最后可得沉mL1molL淀多少克?14. 把一小块镁铝合金溶于100mL盐酸中,然后向其中滴入NaOH⋅溶11-Lmol液,生成沉淀的质量和加入NaOH溶液的体积如下图所示。
江苏省徐州市贾汪区建平中学高一化学《镁铝图像计算》教案

备课时间2012 年月日编写人:任响上课时间第周周月日班级8 节次课题镁铝图象计算总课时数第节教学目标1、使学生掌握有关铝的图象知识,巩固对本部分知识的理解和掌握;2、增强学生识别、分析、解决图象题的能力。
教学重难点1、使学生掌握有关铝的图象知识,巩固对本部分知识的理解和掌握。
教学参考书本近几年的高考考题 2012年高考说明授课方法结合练习册总结归纳教学辅助手段多媒体专用教室教室教学教学二次备课1过程设计一、感悟高考:(09上海)镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)关系如右图。
反应中镁和铝的()A.物质的量之比为3:2 B.质量之比为3:2C.摩尔质量之比为2:3 D.反应速率之比为2:3二、教学过程图像计算综合性强,难度大。
解题时,应首先抓住有关化学原理和有关物质的性质以及图像的意义和图像的特点,综合分析、逐步计算。
然后重点抓住图像的“四点”,即①原点(起点)、②交点、③转折点、④终点。
通过对这些点的坐标的分析运算,解出正确答案。
(一)四个基本图象1、向AlCl3溶液中逐滴滴加NaOH溶液直至过量(图中纵轴y表示Al(OH)3沉淀的物质的量,横轴表示加入试剂的物质的量)现象:离子方程式:2、向NaOH溶液中逐滴滴加AlCl3溶液直至过量现象:离子方程式:3、向NaAlO2溶液中逐滴滴加HCl溶液直至过量现象:离子方程式:4、向HCl溶液中逐滴滴加NaAlO2溶液直至过量现象:离子方程式:学生思考左面习题教师解释学生回答学生思考回答教师补充教师指导2教学教学二次备课3过程设计(二)基本图象的拓展1、若AlCl3溶液中混有MgCl2,向此溶液中逐滴滴加NaOH溶液直至过量,发生了什么反应?图象是怎样的?现象:离子方程式:2、若AlCl3溶液中除混有外MgCl2,还混有盐酸,向此溶液中逐滴滴加NaOH溶液直至过量,发生的反应有何不同,图象有什么样的变化?现象:离子方程式:3、若AlCl3溶液中除混有MgCl2和盐酸外,还混有NH4Cl,向此溶液中逐滴滴加NaOH溶液直至过量,发生的反应又有何不同,图象又有什么样的变化?现象:离子方程式:例1向NaOH和NaAlO2的混合液中不断滴加盐酸,下列图象中, 能正确表示上述反应的是(横坐标表示加入HCl溶液的体积, 纵坐标表示反应生成沉淀的质量)()[ 例2]将物质的量相等的硫酸铝和硫酸铵溶水形成V mL混合溶液,向混合溶液中逐滴加入某氢氧化钠的溶液(其物质的量浓度为混合溶液中两溶质的物质的量浓度之和),直至过量。
镁铝图像计算技巧

一、必备知识“铝线法”的基本方法可以由四句话来概括——“相邻粒子不反应,相隔粒子聚中间,隔之越远越易行,所带电荷是关键”1.Al3+―→Al(OH)3(1)可溶性铝盐与少量NaOH溶液反应:Al3++3OH-(少量)===Al(OH)3↓(2)可溶性铝盐与氨水反应:Al3++3NH3·H2O===Al(OH)3↓+3NH4+2.Al(OH)3―→Al3+Al(OH)3溶于强酸溶液:Al(OH)3+3H+===Al3++3H2O3.Al3+―→AlO2-可溶性铝盐与过量的强碱反应:Al3++4OH-(过量)===AlO2-+2H2O4.AlO2-―→Al3+偏铝酸盐溶液与足量的盐酸反应:AlO2-+4H+===Al3++2H2O5.AlO2-―→Al(OH)3 (1)偏铝酸盐溶液中加少量盐酸:AlO2-+H+(少量)+H2O===Al(OH)3↓(2)偏铝酸盐溶液中通入CO2:2AlO2-+CO2(少量)+3H2O==2Al(OH)3↓+CO32-AlO2-+CO2(过量)+2H2O===Al(OH)3↓+HCO3-6.Al(OH)3―→AlO2-Al(OH)3溶于强碱溶液:--二、铝的图像分析1.铝盐溶液和氨水的反应:Al3++3NH3·H2O=Al(OH)3↓+3NH4+ n沉淀n NH33 .H2O2.向AlCl3溶液中滴加NaOH溶液至过量⑴Al3++3OH-=Al(OH)3↓⑵Al(OH)3+OH-=AlO2-+2H2On沉淀VNaOH3.向NaOH溶液中滴加AlCl3溶液至过量⑴Al3++4OH-= AlO2-+2H2O⑵Al3++ 3AlO2-+6H2O =4Al(OH)3↓n沉淀0 1 2 3 4V AlCl3离子方程式:⑴AlO2-+H++H2O =Al(OH)3↓⑵Al(OH)3+3H+=Al3+ +3H2O图像:n沉淀V0 1 2 3 495.向HCl溶液中滴加NaAlO 2溶液至过量图像:n沉淀VNaAlO20 1 2 3 4⑴AlO 2-+4H + =Al 3+ +2H2O ⑵Al 3++3AlO 2-+6H 2O =4Al(OH)3↓离子方程式看面看线看点跟铝有关的图像分析典例分析1.下列曲线图(纵坐标为沉淀的量,横坐标为加入物质的量)与对应的选项相符合的是( )B.向1 L浓度分别为0.1 mol·L-1和0.3mol·L-1的AlCl3、NH4Cl的混合溶液中加入0.1 mol·L-1的稀NaOH溶液D.向AlCl3溶液中滴加过量氨水跟铝有关的图像分析解析 Ba(OH)2和NaAlO2中加入H2SO4,发生的反应依次为,所以加1 L H2SO4时,Ba(OH)2反应完,再加0.5 L H2SO4时,AlO2(-)反应完全,再加1.5 L H2SO4时,Al(OH)3全部溶解,A正确;向1 L浓度分别为0.1 mol·L-1和0.3 mol·L-1的AlCl3、NH4Cl的混合溶液中加入0.1 mol·L-1的NaOH溶液,发生的反应依次是Al3++3OH-===Al(OH)3↓、OH-+NH4+===NH3·H2O、Al(OH)3+OH-===+2H2O,所以沉淀Al3+和溶解Al(OH)3所用NaOH的量之比为3∶1,而图像上看到的是1∶1,B错误;向烧碱溶液中滴加明矾溶液,发生的反应依次是Al3++4OH-==+2H2O、Al3++3+6H2O===4Al(OH)3↓,C错误;AlCl3溶液中滴加过量氨水,沉淀不会溶解,D错误。
有关镁铝的_图像计算

有关镁铝的图像题一、知识梳理Al(OH)3沉淀量的计算讨论:向含有amolAlCl3的溶液中加入含bmolKOH的溶液,求生成沉淀的物质的量分析:n(OH-) :n(Al3+) Al元素的存在形式Al(OH)3沉淀量b:a ______时,Al3++Al(OH)3b:a ______时Al(OH)3____b:a ____时Al(OH)3+[Al(OH)4]-b:a ______时,[Al(OH)4]-例:(1)100 mL 1 mol·L-1的AlCl3溶液与60 mL 6 mol·L-1的KOH溶液混合后,生成沉淀的质量是_______g。
(2)若在200 mL 0.5 mol·L-1的Al2(SO4)3溶液中加入2 mol·L-1的NaOH溶液,可得到7.8 g Al(OH)3沉淀,则NaOH溶液的体积为_________mL。
解:(1)n(Al3+)=0.1 L × 1 mol·L-1=0.1 mol n(OH-)=0.06 L × 6 mol·L-1=0.36 mol Al3+~3OH-~Al(OH)3OH-(剩余)~Al(OH)3~[Al(OH)4]-131 1 1 10.10.30.1 (生成)0.36-0.3 0.06 (继续溶解) 0.06∴n(Al(OH)3)=0.1 mol-0.06 mol=0.04 mol∴mAl(OH)3=78 g/mol × 0.04 mol=3.12g(2)n(Al(OH)3)= =0.1moln(Al3+)=0.2L×0.5mol/L×2=0.2mol画出NaOH溶液滴入Al2(SO4)3溶液中生成沉淀的图像。
∵Al3++3OH-=Al(OH)3↓Al(OH)3+OH-=[Al(OH)4]-+H2O∴当NaOH溶液刚滴入Al2(SO4)3中,立即生成沉淀,n(OH-)=3n(Al3+)=0.6mol时,沉淀量最大,n(Al(OH)3)=0.2mol;随着NaOH溶液继续滴加,溶液中无Al3+,Al(OH)3与过量NaOH生成Na[Al(OH)4]而溶解,当过量n(NaOH)=n(Al3+)时,Al(OH)3完全溶解。
镁铝图像和计算专题

高三专题:有关镁、铝、铁的典型图像、推断、实验题1、在Al2(SO4)3和MgSO4的混合溶液中,滴加NaOH溶液,生成沉淀的量与滴入NaOH溶液的体积关系如下图所示,则原混合液中Al2(SO4)3与MgSO4的物质的量浓度之比为A、6:1B、3:1C、2:1D、1:22、某溶液中可能含有Fe2+、Mg2+、Cu2+、NH4+、Al3+中的一种或几种。
当加入一种淡黄色固体并加热溶液时,有刺激性气体放出和白色沉淀生成,加入淡黄色固体的物质的量(横坐标)与析出沉淀和产生气体的物质的量(纵坐标)的关系,如下图所示。
请填写下列空白:⑴在该溶液中含有的离子是:,它们的物质的量浓度之比为:。
⑵所加的淡黄色固体是(化学式)。
3、将0.1 mol的镁、铝混合物溶于100 mL 2mol/LH2SO 4溶液中,然后再滴加1 mol/L NaOH溶液。
请回答:⑴若在滴加NaOH溶液的过程中,沉淀质量m随加入NaOH溶液的体积V变化如下图所示。
当V1=160mL时,则金属粉末中n(Mg)= mol,V2= mL。
⑵若在滴加NaOH溶液过程中,欲使Mg2+、Al3+刚好沉淀完全,则滴入NaOH溶液的体积V(NaOH) mL。
⑶若混合物仍为0.1 mol,其中Mg粉的物质的量分数为a,用100 mL 2 mol/L的硫酸溶解此混合物后,再加入450 mL 1mol/L的NaOH溶液,所得沉淀中无Al(OH)3。
满足此条件的a的取值范围是:。
4、将一定量混合均匀的铁粉与硫粉在隔绝空气的条件下共热,充分反应后冷却至室温,得到固体A。
将质量为m的固体A加入到300 mL 2 mol/L盐酸中使之完全溶解。
测得室温下加入固体A的质量与收集到气体体积(已换算成标准状况)的关系如右图所示(假设所得氢硫酸溶液饱和前无硫化氢气体逸出)。
已知:①加入固体A的质量m≤3.2 g时,收集到的气体为H2;②当m>3.2 g时,收集到的气体为H2和H2S的混合气体。
镁铝及其化合物知识归纳及巩固之一——镁铝单质

镁铝及其化合物知识归纳之一——镁铝单质一、镁和铝(一)镁和铝的结构:1、原子结构示意图:镁 铝 2、周期表中位置:镁位于第三周期第IIA 族,最外层有2个电子容易失去,显+2价; 铝位于第三周期ⅢA 族,最外层有3个电子,显+3价。
[特别提醒] 镁、铝都是活泼金属,由于它们结构的相似与不同,决定了它们的化学性质有许多共同点和不同点。
共同点:镁、铝都能与氧气及其它许多非金属、酸及其某些氧化物反应,因而镁铝具有较强的还原性。
不同点:由于镁、铝属于同周期元素,镁的核电荷数较少,原子半径比铝大,在化学反应中比铝更易失去价电子,故镁的金属性强于铝。
(二)镁和铝的物理性质:元素名称 元素符号 核电荷数 单质的物理性质颜色和状态 密度/(g ·c m -3)熔点/℃ 沸点/℃ 导电性 传热性延展性镁 Mg 12 银白色固体1.738 645 1090 较好 较好铝 Al 13 银白色固体2.70 660.4 2467 很好 很好[特别提醒] 镁和铝相比较,铝的硬度比镁的稍大,熔点和沸点都是铝比镁的高. (三)镁、铝单质的化学性质1.与非金属反应(1)与O 2反应。
常温下与空气中的O 2反应生成一层致密的氧化物薄膜,所以镁、铝都有抗腐蚀的性能,不需要密封保存。
镁、铝都能在空气中燃烧:2Mg+O 22MgO 4Al+ 3O 22Al 2O 3(2)与卤素单质、硫等反应。
Mg+ Cl 2MgCl 2 2Al+ 3Cl 22AlCl 32Al+ 3S Al 2S 3 (用于工业制备) Mg+ SMgS③集气瓶底部都要放一些细纱,以防止集气瓶炸裂。
[特别提醒] ①镁在空气中用酒精灯火焰点燃即可燃烧,而铝在空气中需要高温点燃才能燃烧。
镁在空气中燃烧时有三个反应发生:2Mg+O 22MgO 3Mg+N 2Mg 3N 2 2Mg+CO 22MgO+C②燃烧时都放出大量的热,发出耀眼的白光。
利用镁的这种性质来制造照明弹。
尖子生培训小专题15 探究镁铝图像问题

尖子生培训小专题15 探究镁铝图像问题氢氧化铝在水溶液中会发生酸式和碱式两种电离,既能与碱反应又能与酸反应生成盐和水。
氢氧化铝和酸、碱反应时,溶液滴加的顺序不同,所加入的量不同,产物也不同;氢氧化镁只溶于酸。
这些性质和量的关系在图像题中有较好的表现,不少同学在解答这一类习题时,往往由于理解分析的不够准确,知识应用不熟练,而出现差错。
本专题探讨如何运用数形相结合的方法,解决此类问题。
◆典型问题1 镁铝基本图像例 1 下列图像中,纵坐标为沉淀量,横坐标为某溶液中加入的反应物的物质的量,选择合适图像对应的字母填空。
(1)AlCl3溶液中加入氨水至过量____________。
(2)AlCl3溶液中加入NaOH溶液至过量___________。
(3)AlCl3、MgCl2混合溶液中加入NaOH溶液至过量_____。
(4)澄清石灰水中通入过量CO2_____________。
(5)含有少量盐酸的AlCl3溶液中加入过量NaOH溶液______。
(6)含有少量HCl的AlCl3溶液中加入过量氨水______。
【思路】解图象试题应注意分析“四点”:“起点”、“折点”、“极点”、“终点”,利用原理引路,图文结合,对号入座。
(2)当Al3+与Mg2+或Cu2+或Fe3+混合在一起,加入过量的NaOH溶液时,生成的沉淀先增大,后减小,但不能减小为0。
【答案】(1)③(2)⑥(3)①(4)②(5)⑤(6)④【解析】(1)AlCl3与NH3·H2O反应生成Al(OH)3沉淀,沉淀不溶于NH3·H2O,故选③。
(2)Al(OH)3溶于强碱NaOH,现象为先生成沉淀后又溶解,且沉淀量最大点左右加入NaOH的物质的量之比为3∶1,故选⑥。
(3)加入NaOH溶液先生成沉淀至最大值,而Al(OH)又溶于NaOH溶液,故选①。
(4)由Ca(OH)2+CO2= CaCO3↓+H2O,CaCO3+CO2+H2O=Ca 3(HCO3)2,知选②。
高一 镁铝图像计算问题

例题评讲:
例1、有MgCl2和Al2(SO4)3的混合溶液,向其 中不断加入NaOH溶液得到沉淀的物质的量与 加入NaOH溶液体积的关系如图所示,则溶液
中Mg2+与Al3+的物质的量浓度之___1_:_O3、Fe2O3、 SiO2)加入100mL硫酸溶液,充分反应后向滤 液中加入10mol/L的NaOH溶液,产生沉淀的 质量与加入NaOH溶液的体积关系如图所示,
入HCl溶液的体积与生成 沉淀的关系如下图所示。
O 10.0
试回答:
B
30.0
C
V(HCl)/ml
(1).混合物中NaOH的物质的量是 0.065 mol,AlCl3的物质 的量是 0.01_mol,MgCl2的物质的量是 0.01 mol。
(2).C点所加的盐酸的体积是 130 ml。
例7、下面有四个实验:
例4、现有AlCl3和MgSO4混合溶液,向其中不 断加入NaOH溶液,得到沉淀的量与加入NaOH 溶液的体积如图所示,原溶液中Cl-与SO42-的
物质的量之比为( C )
沉淀的物质的量
0
A.1 :3
0.4
B.2 :3
0.5
V(NaOH)/L
C.6 :1 D.3 :1
例5、将溶液(或气体)X,逐渐加入(或通 入)到一定量溶液Y中,产生沉淀的量与加入 X的量的关系如下图,符合题意的一组物质是
n[Al(OH)3]
0 1 2 3 4 V(NaAlO2 )
⑥.向NaAlO2溶液中通入CO2至过量 NaAlO2 +CO2 +2H2O ==Al(OH)3 ↓+NaHCO3
n[Al(OH)3]/mol
0
n(CO2)/mol
化学:“镁__铝”图像题解析

“镁 铝”图像题解析学习“镁 铝及化合物”的有关知识时,我们接触到最多的图像题,不少同学在解答这一部分习题,往往由于理解分析的不够准确,知识应用不熟练,而出现差错。
利用图形相结合的方法,可在解决问题时起到事半功倍的效果。
下面举几例进行剖析: 一、向AlCl 3溶液中滴加NaOH 溶液至过量 O ~A 段:()AlOH Al OH 333+-+=↓A ~B 段:()Al OH OH AlO H O 3222+=+--从图1不难看出,向氯化铝溶液中滴加氢氧化钠溶液,若达不到最大沉淀量时,对应的氢氧化钠溶液的体积有两种情况:一是氯化铝过量即加入的氢氧化钠不足;二是加入的氢氧化钠将生成的氢氧化铝溶解了一部分。
图1例1. 向30毫升1 mol/L 的AlCl 3溶液中逐渐加入浓度为4 mol/L 的NaOH 溶液,若产生0.78克白色沉淀,则加入的NaOH 溶液的体积可能为( ) A. 3mL B. 7.5mL C. 15mL D. 27.5mL例2. 向含有a mol AlCl 3的溶液中加入含b mol KOH 的溶液,生成沉淀的物质的量可能是( ) (1)a mol(2)b mol(3)amol 3(4)bmol 3(5)0 mol(6)()4a b mol -A. (1)(2)(4)(5)(6)B. (1)(4)(5)(6)C. (1)(2)(3)(5)(6)D. (1)(3)(5)例3. 等体积的AlCl 3和NaOH 两种溶液混合后,沉淀物中含铝元素的质量与溶液中含铝元素的质量相等,则AlCl 3和NaOH 两种溶液的物质的量浓度之比是( )(1)1:3 (2)2:3 (3)1:4 (4)2:7A. (1)和(2)B. (1)和(3)C. (2)和(4)D. (3)和(4)二、向强碱溶液中滴入铝酸盐溶液,先无沉淀,当Al 3+全部转化为AlO 2-时,再加入铝盐溶液,则偏铝酸盐与铝盐溶液发生了相互促进水解的反应,产物都是()Al OH 3。
教育最新K122019版高考化学总复习 专题 镁铝图像问题导学案

镁铝图像问题考点剖析一、用数形结合思想分析Al(OH)3的图像1.把强碱溶液逐滴加入到铝盐(Al3+)溶液中至过量(1)现象:先有白色沉淀产生,然后沉淀逐渐溶解。
(2)有关反应的离子方程式:A→B:Al3++3OH-===Al(OH)3↓;B→D:Al(OH)3+OH-===AlO-2+2H2O。
2.把铝盐(Al3+)溶液逐滴加入到强碱溶液中至过量(1)现象:先无明显现象,然后逐渐产生大量的白色沉淀。
(2)有关反应的离子方程式:A→B:Al3++4OH-===AlO-2+2H2O;B→C:Al3++3AlO-2+6H2O===4Al(OH)3↓。
3.把强酸溶液逐滴加入到AlO-2溶液中至过量(1)现象:先生成白色沉淀,随后沉淀逐渐溶解。
(2)有关反应的离子方程式:A→B:AlO-2+H++H2O===Al(OH)3↓;B→D:Al(OH)3+3H+===Al3++3H2O。
4.向强酸溶液中逐滴加入AlO-2溶液至过量(1)现象:先无明显现象,反应一段时间后逐渐产生白色沉淀。
(2)有关反应的离子方程式:A→B:4H++AlO-2===Al3++2H2O;B→C:Al3++3AlO-2+6H2O===4Al(OH)3↓。
5.把Ba(OH)2溶液逐滴加入到明矾溶液中至过量O→A反应:2KAl(SO4)2+3Ba(OH)2===2Al(OH)3↓+3BaSO4↓+K2SO4;A→B反应:2Al(OH)3+K2SO4+Ba(OH)2===BaSO4↓+2KAlO2+4H2O。
6.向等物质的量的AlCl3、MgCl2混合溶液中逐滴加入NaOH溶液至过量O→A反应:Al3++3OH-===Al(OH)3↓,Mg2++2OH-===Mg(OH)2↓;A→B反应:Al(OH)3+OH-===AlO-2+2H2O。
[注意]:(1)分析图像时要注意加入酸或碱的强弱。
因为强酸、强碱会使Al(OH)3溶解,而弱酸、弱碱不能使Al(OH)3溶解。
钠镁铝的三类图像题的解题思路和方法

金属钠镁铝的三类图像题的解题思路和方法授课 高一化学组 管细文教学目标:1.通过教学,使学生能够看懂图像的意义,能够分析图像中曲线变化的含义。
2.通过教学,使学生能够掌握解答图像题的基本思路和解题的分析方法。
教学难点:1.学生分析图像的能力的培养。
2.学生解答图像题的分析方法的掌握。
教学内容:与金属钠镁铝和铵根离子有关的三类图像题的解题思路和方法教学过程:一.有关Na2CO3、NaHCO3、NaOH与盐酸反应的图像例1.将0.035mol碳酸钠、碳酸氢钠和氢氧化钠的固体混合物完全溶解于水,制成稀溶液,然后向该溶液中逐滴加入1mol∕L的盐酸,所加入盐酸的体积与产生CO2的体积(标准状况)关系如右图所示:(1)写出固体混合物溶于水时发生的反应离子方程式 。
(2)写出OA段、AB段所发生反应的离子方程式:、。
(3)当加入35mL盐酸时,产生CO2的体积为 mL(标准状况)。
(4)计算原混合物中NaOH的物质的量是 mol。
变式练习1.向200 mL 某物质的量浓度的NaOH溶液中缓慢通入一定量的CO2,充分反应后,得到Na2CO3和NaHCO3的混合溶液。
向上述所得溶液中,逐滴滴加2 mol∕L的盐酸,所得气体的体积与所加盐酸的体积关系如右图所示:(1)OA段、AB段发生反应的离子方程式:、 (2)B点时,反应所得溶液中溶质的物质的量浓度是 。
(3)原NaOH溶液的物质的量浓度是 。
二.有关Al(OH)3沉淀与NaOH反应的图像例2.将镁铝的混合物0.1mol溶于100mL2mol·L-1硫酸溶液中,然后再滴加1mol·L-1氢氧化钠溶液,请回答下列问题:(1)若在滴加NaOH溶液过程中,沉淀质量m随加入氢氧化钠的体积v变化关系如下图:①写出O~V1段反应的离子方程式 。
②在滴加NaOH溶液过程中, 写出与铝有关的反应的离子方程式 、 。
③当V1=160mL时,原镁铝混合物中n(Mg)=mol。
镁铝图象

《镁铝》图象题分类例析镁铝的化合物在溶液中与强碱反应时,一个重要特征是它们相对量不同,沉淀量有所不同,若用文字来表述,沉淀量随强碱量的变化关系则很难表达清楚,但反映它们量的关系图象,不仅有助于理解镁铝化合物与强碱反应的进程,也助于有关计算问题的解决。
一.图象类型图一、往Al3+溶液中逐滴加入强碱溶液oa段是Al(OH)3物质的量逐渐增多,并达到最大值阶段,a点对应的沉淀量最多;ab段是Al(OH)3物质的量逐渐减少阶段,b点对应的沉淀完全溶解。
量的关系:(1)oa段 n[Al(OH)3]=n(OH- )/3;(2)ab段n[Al(OH)3]=4 n(Al3+)- n(OH- )。
图二、往Al3+的酸性溶液中逐滴加入强碱溶液oa段是酸碱中和阶段,ab段是沉淀生成阶段,bc段为沉淀溶解阶段。
图三、往Mg2+与Al3+溶液中逐滴加入强碱溶液oa段是Al(OH)3和Mg(OH)2沉淀生成阶段,其中n1为Al(OH)3和Mg(OH)2物质的量最大值和;ab段是Al(OH)3沉淀溶解阶段,至b点Al(OH)3沉淀完全溶解,其中n2为Mg(OH)2物质的量。
量的关系:(1)n(Al3+)=(b-a)mol(2)n(Mg2+)=(4a-3b)/2 mol图四、往Mg2+与Al3+的酸性溶液中逐滴加入强碱溶液oa段是酸碱中和阶段,ab段是沉淀生成阶段,bc段为沉淀部分溶解阶段。
二.计算例析有关《镁铝》的图象题,常在图象中给出数据,再根据图象中各阶段折线间量的关系,结合有关公式解题。
解题关键是读图、识图。
当然,有时也可以将一些计算题的“数”以“形”的形式反映在图象上,加快解题。
例1.0.1mol/LAl2(SO4)3溶液100mL中,需加入0.5mol/LNaOH 溶液多少毫升才可得沉淀1.17g?解析:此题有关数据可在图五上反映出来。
已知沉淀最大量为0.02mol,现有沉淀0.015mol,根据“形”可知,此题有两个答案:(1)n[Al(OH)3]=n(OH—)/3 ,0015=0.5 V 10-3/3,V=90mL;(2)n[Al(OH)3]=4n(Al3+)- n(OH—),0.015=4 0.02-0.5 V 10-3,V=130mL。
铝的重要图像及有关计算
0
A
B
C
HCl (mol)
铝的化合物有关计算
(1)100mL1mol· L-1的AlCl3溶液与60mL6mol· L1的KOH溶液混合后,生成沉淀的质量是 g。 (2)若在200mL0.5mol· L-1的Al2(SO4)3溶液中 加入2mol· L-1的NaOH溶液,可得到7.8gAl(OH)3 沉淀,则NaOH溶液的体积为 mL。
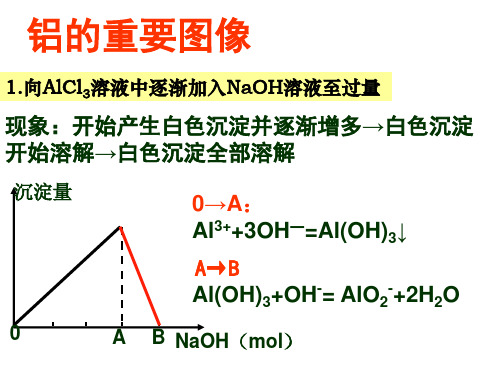
现象:开始产生白色沉淀并逐渐增多→白色沉淀 开始溶解→白色沉淀全部溶解
沉淀量
0→A: AlO2-+H++H2O =Al(OH)3↓ A→ B Al(OH)3+3H+= Al3++3H2O
0
A
B HCl (mol)
铝的重要图像
3.向AlCl3溶液中逐渐加入稀氨水至过量
现象:产生白色沉淀→白色沉淀逐渐增多→ 沉淀量达到最大值不再改变
0 A B
NaAlO2 (mol)
铝的重要图像
7.向含有HCl和AlCl3的溶液中逐渐加入NaOH溶液至过量
现象:开始没有沉淀→产生白色沉淀并逐渐增多 →白色沉淀开始溶解→白色沉淀全部溶解
沉淀量
0→A:H++OH-=H2O A→B: Al3++3OH―=Al(OH)3↓ B→ C: Al(OH)3+OH-=AlO2-+2H2O
沉淀量
0→A: Al3++3NH3· H2O= Al(OH)3↓+3NH4+
0
A
氨水体积
铝的重要图像
4.向NaAlO2溶液中通入CO2至过量 现象:产生白色沉淀→白色沉淀逐渐增多→ 沉淀量达到最大值不再改变
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
有关镁铝的图像题
2012-9-14
(2) ____________________________________________________ 在明矶溶液中加入 NaOH 溶液直至过量 ________________________________________________
(3 )在强碱性溶液中逐滴加入铝盐溶液直至过量 _____________________ (4 )在偏铝酸钠溶液中通入
CO 2直至过量 _____________
(5)在强酸溶液中加入偏铝酸钠溶液直至过量 _____________________
2、0.2moI/L Al 2(SO 4)3溶液100mL ,加入0.4mol/L NaOH 溶液,为得到澄清溶液,最少需 加入NaOH 溶液的体积(mL)为 ( ) A 、200 B 、300 C 、400 D 、700
知识梳理 AI(OH) 3沉淀量的计算 讨论:向含有amolAICI 3的溶液中加入含bmoIKOH 的溶液,求生成沉淀的物质的量 分析: n(OH -) : n(Al 3+) b : a ____ 时, b : a ____ 时 Al 元素的存在形式
Al 3++AI(OH) 3 AI(OH) 3 AI(OH) 3沉淀量
例: ___ b : a __ 时
AI(OH) 3+AIO 2
b : a _______ 时, AIO 2「
(1) 100 mL 1 mol • L -1 的 AICI 3溶液与 60 mL 6 mol
L -1的KOH 溶液混合后,生成 沉淀的质量是 ________ g o (2)若在 200 mL 0.5 mol • L -1 的 AD(SO 4)3溶液中加入 2 mol • L -1 的 NaOH 溶液,可 得到7.8 g AI(OH) 3沉淀,则NaOH 溶液的体积为 ____________ m L o 训练提咼
1.某学生在实验室做了如下 5个实验:根据实验画出下图的 5个图象(纵坐标为沉淀物 质的量,横坐标为溶液中加入物质的物质的量)实验与图象对立关系正确的是:
3、向MgSO4和Al2(SO4)3的混合溶液中,逐滴加入示上述反应的是(横坐标表示加入NaOH
量)( NaOH溶液。
下列图象中,能正确表溶
液的体积,纵坐标表示反应生成沉淀的质
则下列说法不正确的是 (
)
A •镁和铝的总质量为 9g
B .最初20 mLNaOH 溶液用于中和过量的硫酸
C .硫酸的物质的量浓度为
2.5 mol • L 1
D .生成的氢气在标准状况下的体积为
11.2 L
6、某溶液中可能含有 H +、Na +、NH 4+、Mg 2+、 Fe 3+、Al 3+、SO 42「、CO 32「等离子。
当向该溶液中 加入一定物质的量浓度的 NaOH 溶液时,发现生 成沉淀物质的量随 NaOH 溶液的体积变化的图象 如右所示,下列说法正确的是
(
)
A .原溶液中含有的阳离子是 H +、NH 4+、Mg 2+、
B .原溶液中一定含有 SO 42-和Na +
C .原溶液中含有的Fe 3+和Al 3+的物质的量之比为1: 1
D .反应最后形成的溶液中含有的溶质为 Na 2SO 4
7、把由NaOH 、AICI 3、MgCl 2三种固体组成的混合物,溶于足量水中后有
0.58克白色沉
淀,在所得浊液中,逐滴加入 0.5mol/l 的盐酸,加入盐酸的体积与生成沉淀的质量关系如
右图所示:
(a) 混合物中NaOH 的质量为 _________ , (b) 混合物中AlCl 3质量为—
(c) 混合物中 MgCl 2质量为 __________ , (d) P 点表示盐酸的体积是_
4 •将溶液(或气体) X 逐渐加入到(或通入到)一定量的 液中,产生沉淀的量 m 与加入X 物质的量n 的关系如下图, 图中情况的一组物质是
A
B C D X
CO 2
NaOH
NH 3
HCl
Y Ca(OH)2 AlCl 3 MgSO 4 NaAlO 2
200 mL 硫酸中,固体全部溶解后,向所得溶液中加入 n 与加入NaOH 溶液的体积V 的变化如下图所示。
5、将一定质量的镁和铝混合物投入
NaOH 溶液,生成沉淀的物质的量
与Al有关的反应方程式
【目标要求】
1、了解常见金属的活动性顺序。
2、了解铜及其重要化合物的主要性质和应用及合金的概念、重要应用。
一、铜
1、物理性质铜是硬度______ 的____ 色金属,具有良好的_________ 、______ 、________
2、化学性质
(1)铜锈的生成
常温下在干燥的空气中性质稳定,但在潮湿的空气中会被锈蚀,在其表面逐渐形成一层
________________ ,反应的化学方程式为 _______________________________ _ 。
(2)与非金属反应在____ 条件下铜能与许多非金属发生反应,如铜与硫反应
的化学方程式为_________________
(3)与氧化性酸反应例如铜能与 __________ 、 ___________ 、____________ 等酸反应。
(4)与盐溶液反应铜与硝酸银溶液(写离子方程式)______________________________
(5)催化剂_______________________________________________________________ 写出铜在乙醇的氧化过程中的催化原理,用化学方式式表示___________________________________
3、列举铜的应用实例________________________________________________________________
【跟踪练习】
普通铜器时间稍久易出现铜绿,其主要成分为Cu2(OH)3CO3,下列对其原因的分析最可能
的是
A它们的表面都电镀上了一层耐腐蚀的黄金
B环境污染那日趋严重,它们表面的铜绿被酸雨溶解洗去
C铜的金属活动性比氢小,因此不易被氧化
D它们是含一定比例金、银、锡、锌的铜合金
二、铜的化合物
1常见化合物的颜色
CuO ____________ CU2O __________________ 含Cu2+的溶液_____________
Cu(OH)2 ___________ CuSO4 粉末________________ CuSO4.5H2O ________
2、用酒精喷灯加热氧化铜固体现象是_________________________________________________
发生反应的化学方程式是 ______________________________________ 用酒精灯加热硫酸铜晶体现象是 ________________________ 发生反应的化学方程式是_______________________
3、性质应用
(1) CuO可检验___________ 等还原性气体,写出相应方程式________________________ _【跟踪练习】
设计用铜作原料制备硫酸铜晶体的最佳方案,请写出简要的实验步骤和相应的方程式
二、合金
1、合金是指两种或两种以上的金属(或金属跟非金属)熔合而成的具有金属特性的物质。
2、合金的性能一般优于纯金属,如强度________ 。
多数合金的熔点一般比它的各成分金属
的____ 硬度一般比它的各成分金属的 _______ 。
例如:镁合金、铝合金。
【跟踪练习】铝、镁合金因坚硬、轻巧、美观、洁净、易于加工而成为新型建筑装潢材
料,主要用于制作窗框、卷帘门、防护栏等。
下列与这些用途无关的性质是()
A .不宜生锈
B .导电性好C.密度小 D .强度高
【巩固提高】
1、某合金(仅含铜、铁)中铜和铁的物质的量之和为ymol,其中Cu的物质的量分数为a, 将其全
部投入50mLbmol/L的硝酸溶液中,加热使其充分反应(假设NO是唯一的还原产物)。
下列说法正确的是()
A .若金属有剩余,在溶液中再滴入硫酸后,金属又开始溶解
B •若金属全部溶解,则溶液中一定含有Fe3+
C.若金属全部溶解,且产生336mL气体(标准状况),则b=0.3
D .当溶液中金属离子只有Fe3+、Cu2+时,贝V a与b的关系为b>80y(1a/3)
2、铜是生命必要元素,也是人类最早使用的金属之一,铜的生产和使用对国计民生各方面产生深远
影响。
在化学反应中,铜元素可表现为0、+1、+2。
(1 )在西汉古籍中曾有记载:曾青得铁则化为铜(即:曾青CuSO跟铁反应生成铜),试写出该反应的离子方程式:________________ 。
(2)尽管铜比铁较为稳定,但铜器表面经常会生成铜锈[即:铜绿,化学式CuaOWCO], 其中生成铜绿的反应物除铜外还有Q、CQ和HO试写出保护铜制品的方
法:___
(3)铜钱在历史上曾经是一种广泛流通的货币。
试从物理性质和化学性质的角度分析为
什么铜常用于制造货币。
铜的熔点是11834C,铁的熔点是1534 8C)___________________。
