年生产20万吨合成氨合成工段工艺设计书
【】毕业论文毕业设计年产20万吨合成氨厂工艺设计

【】毕业论⽂毕业设计年产20万吨合成氨⼚⼯艺设计年产20万吨合成氨⼚⼯艺设计摘要氨的⼯业⽣产主要是利⽤氮⽓和氢⽓通过催化剂的催化⽽得到。
本设计是年产20万吨合成氨⼚的⼯艺设计,但由于合成氨的整个⽣产⼯艺较长,细节问题较多,鉴于设计时间的紧迫,本设计主要对合成氨的主要⼯段——合成⼯段进⾏了⼯艺计算、设备选型,并绘制了全⼚平⾯布置图、合成氨⼯艺流程⽰意图、合成⼯段带控制点⼯艺流程图、合成⼯段物料流程图、合成车间的⽴⾯图和平⾯图。
关键词:氨,催化剂,⼯艺,图Ammonia Plant Process of The Technological Designof 200,000 t Ammonia Per YearABSTRACTThe industrial production of ammonia is used mainly nitrogen and hydrogen through the catalyst to be obtained. The design of the annual output of 200,000 tons of synthetic ammonia plant process design, but because of the ammonia production process is longer, more details, in view of the urgency of the design time. The main design of the main section of ammonia-synthesis section of the technology, equipment selection, and the mapping of the entire plant layout map Ammonia Process Chart, Synthesis Process control point with the process flow chart Synthesis Process flowchart materials, synthetic workshop elevation and floor plans.KEY WORDS:ammonia ,catalyst ,technology ,chart⽬录摘要........................................................................................................................................... I ABSTRACT .............................................................................................................................. II 1 ⼯程设计背景与发展状况. (1)1.1⼯程设计的背景 (1)1.2我国合成氨产业概况 (1)1.3我国合成氨需求现状及设计规模 (1)2 ⼯程设计条件与总平⾯布置 (3)2.1⼯程设计条件 (3)2.1.1 原材料及辅助物料的资源条件 (3)2.1.2 公⽤⼯程概述 (3)2.1.3 劳动⼒资源条件 (3)2.2总平⾯布置 (3)2.2.1 总平⾯布置的基本原则 (3)2.2.2 总平⾯布置概述 (4)3 化⼯⼯艺设计 (7)3.1车间组成概述 (7)3.2车间⽣产综合叙述 (7)3.2.1 合成⼯段的概况及特点 (7)3.2.2 ⼯作制度 (7)3.2.3 产品的主要技术规格及标准 (8)3.2.4 ⼯艺流程叙述 (8)4 合成⼯段的⼯艺计算及设备选型 (10)4.1合成⼯段设计要求 (10)4.2合成⼯段物料衡算图 (10)4.3.1 物料衡算 (11)4.3.2 热量衡算 (24)4.3.3 主要设备的计算 (31)4.3.4 主要设备型号⼀览表 (45)5 安全⽣产及环境保护 (46)5.1环境保护与综合利⽤ (46)5.2劳动安全卫⽣ (46)致谢 (48)参考⽂献 (49)1⼯程设计背景与发展状况1.1 ⼯程设计的背景合成氨是化学⼯业中的⼀种重要的基础原料。
年产19万吨合成氨合成工段初步工艺设计

合成氨是一种广泛应用于农业、化工、医药等领域的重要化工原料。
根据年产19万吨合成氨合成工段初步工艺设计,以下是一份工艺设计报告,为了保护设计者的利益,本文仅提供一部分内容。
一、工艺概述年产19万吨合成氨合成工段通过从天然气中提取氢气并与氮气在催化剂的作用下进行氨合成反应,得到合成氨产品。
该工艺采用了先进的床层式反应器系统,具有高效、稳定和可控性强的优点。
本工艺设计报告将对该工段的主要设备、流程和参数进行介绍和分析。
二、主要设备1.气体处理单元:主要包括气体压缩机、气体净化器和气体储罐等设备,用于对进入工段的天然气和纯净氮气进行预处理和储存。
2.反应器系统:主要包括催化剂床层反应器、冷凝器和分离器等设备,用于催化氢气和氮气反应生成合成氨,并进行产品分离和冷却。
3.工艺氨回收单元:主要包括氨切割器、热氮技术和氨回收器等设备,用于从反应器中回收未反应的氨气,并返回到催化剂床层反应器进行再次利用。
4.废气处理单元:主要包括废气处理装置和废气净化器等设备,用于对排放的废气进行净化处理,减少对环境的影响。
三、工艺流程1.天然气处理:将进入工段的天然气进行压缩处理,去除其中的杂质和硫化物等物质,然后储存在气体储罐中。
2.氮气制备:将氧气和氮气混合,通过特定的膜分离技术获取纯净氮气,用于后续反应过程中的氧气置换和稀释。
3.氢气制备:将从天然气中提取的氢气经过严格的纯化处理,去除其中的杂质和残留的气体,达到合成氨反应所需的纯度和浓度要求。
4.氨合成:在催化剂床层反应器中,将经过预处理的氢气和纯净氮气按一定的比例加入,通过催化剂的作用进行低温高压下的合成氨反应。
5.产品分离:将合成氨通过冷凝器进行冷却,然后进入分离器,从中分离出未反应的氮气和其他杂质,得到纯净的合成氨产品。
6.氨回收:将反应器中未反应的氨气通过氨切割器进行回收,然后经过热氮技术和氨回收器进行进一步处理,以便于再次利用。
7.废气处理:将反应过程中产生的废气经过废气处理装置净化处理,去除其中的有害物质和污染物,使其符合国家的排放标准。
年产20万吨合成氨脱硫工段工艺设计

吉林化工学院课程设计题目年产20万吨合成氨脱硫工段工艺设计教学院化工与材料工程学院专业班级化工0904学生姓名鞠洪清学生学号 09110437指导教师刘艳杰2012年12月27日前言本设计是年产20万吨合成氨脱硫工段的工艺设计。
对合成氨和脱硫工艺的发展概况进行了概述。
着重详细介绍了脱硫工段的工艺流程、工艺条件、生产流程、技术指标等内容。
就脱硫车间的工艺生产流程,各脱硫方法对比, 栲胶脱硫, 三废治理及利用, 反应条件对反应的影响, 物料流程, 影响的因素, 着重介绍化工设计的基本原理、标准、规范、技巧和经验。
设计总的指导思想是, 理论联系实际、简明易懂、经济实用。
目录前言 (1)摘要 (4)1.总论 (5)1.1.1栲胶法脱硫的发展 (6)1.1.2栲胶脱硫剂介绍 (6)1.1.3栲胶脱硫的反应机理 (7)1.1.4栲胶溶液的预处理 (7)1.1.5生产中副产品硫磺的回收工艺 (8)1.1.5.1劳斯法硫磺回收工艺 (8)1.1.5.2劳斯法硫磺回收工艺原理 (9)1.1.6生产中副产品硫磺的应用 (11)1.1.6.1硫磺的基本应用 (11)1.1.6.2硫磺的几种专门应用 (11)1.2文献综述 (14)1.2.1前言 (14)1.2.2脱硫法介绍 (15)2. 流程方案的确定 (16)2.1各脱硫方法对比 (16)2.2栲胶脱硫法的理论依据 (18)2.3工艺流程方框图 (19)3. 生产流程的简述 (20)3.1简述物料流程 (20)3.1.1气体流程 (20)3.1.2溶液流程 (20)3.1.3硫磺回收流程 (20)3.2工艺的化学过程 (22)3.3反应条件对反应的影响 (23)3.3.1影响栲胶溶液吸收的因素 (23)3.3.2影响溶液再生的因素 (25)3.4工艺条件的确定 (26)3.4.1溶液的组成 (26)3.4.2喷淋密度和液气比的控制 (26)3.4.3温度 (27)3.4.4再生空气量 (27)4. 物料衡算和热量衡算 (27)4.1物料衡算 (27)4.2热量衡算 (30)5. 车间布置说明 (34)6. 三废治理 (35)6.1废水的处理............................................................................. 错误!未定义书签。
【最新版】年产20万吨合成氨合成工艺设计毕业设计

年产20万吨合成氨合成工艺设计The Process Design of 200kta of Synthetic AmmoniaSynthesis目录摘要 (I)Abstract (I)引言 (1)第一章综述 (2)1.1 氨的研究背景 (2)1.2 氨的用途 (2)1.3 氨的生产方法的选择 (3)第二章氨合成过程的步骤及工艺流程 (5)2.1 氨合成的步骤 (5)2.2 氨合成工艺流程简述 (6)第三章工艺计算 (9)3.1 原始条件 (9)3.2 物料衡算 (9)3.2.1 合成塔物料衡算 (9)3.2.2 氨分离器气液平衡计算....................... 错误!未定义书签。
3.2.3 冷凝塔气液平衡计算......................... 错误!未定义书签。
3.2.4 液氨贮槽气液平衡计算....................... 错误!未定义书签。
3.2.5 液氨贮槽物料计算 (14)3.2.6 合成系统物料计算........................... 错误!未定义书签。
3.2.7 合成塔物料计算............................. 错误!未定义书签。
3.2.8 水冷器物料计算 (17)3.2.9 氨分离器物料计算 (18)3.2.10 冷凝塔物料计算 (19)3.2.11 氨冷器物料计算............................ 错误!未定义书签。
3.2.12 冷凝塔物料计算............................ 错误!未定义书签。
3.2.13 液氨贮槽物料计算.......................... 错误!未定义书签。
3.3 热量衡算 (26)3.3.1合成塔热量计算 (26)3.3.2 废热锅炉热量计算 (28)3.3.3 热交换器热量计算 (29)第四章设备的计算与选型..................... 错误!未定义书签。
年产二十万吨合成氨变换工段工艺设计

合成氨变换工段是合成氨生产过程中的关键工艺环节之一,它将合成气中的氮气和氢气在催化剂的作用下,通过催化反应转化为合成氨。
本文将围绕年产二十万吨合成氨的变换工段工艺设计进行详细阐述,旨在提供一个完整的工艺设计方案。
首先,变换工段的催化剂选择非常重要。
对于年产二十万吨合成氨的工艺,常用的催化剂有铁素体、铁铬铝混合催化剂等。
这些催化剂在一定的操作条件下,能够实现高效的合成氨转化率和选择性。
在实际应用中,应根据具体工艺要求和经济效益进行选择。
其次,合成气的净化和预热是变换工段的重要准备工作。
合成气中常含有一定的杂质,如氧、水蒸气、二氧化碳等,这些杂质会影响催化剂的活性和寿命。
因此,合成气需要通过一系列净化设备,如除氧、除硫、除水等步骤,将其净化为适合变换反应的合成气。
同时,为了提高反应的热效应,还需要对合成气进行预热,一般可以采用换热器进行热量回收。
接下来是变换反应的具体设计。
变换反应是一个平衡反应,根据Le Chatelier原理,可以通过提高反应温度、降低反应压力、增加氢气过量等方式推动平衡向产氨方向偏移。
在实际设计中,应在考虑较高转化率的前提下,平衡反应速率和催化剂活性与寿命的关系,做出合理的选择。
另外,变换反应需要保持一定的循环气速和循环气气体组成。
循环气速过高会造成能耗增加,循环气速过低则会影响气体传质效果。
循环气气体组成应符合催化剂的操作条件,一般应保持一定的氢气过量,同时控制氮气和氢气的比例。
最后是变换工段的控制策略。
合成氨变换工段是一个高温高压的工艺过程,对于安全和稳定运行,需要建立完善的自动化控制系统。
控制策略应包括反应温度和压力的控制、循环气速和气体组成的控制、催化剂的修复和更换等。
在实际设计中,应结合具体的工艺要求和设备性能,进行综合技术经济分析,选取最佳的工艺参数和操作条件。
同时,在设计过程中还应考虑到工艺的可持续性和环境保护要求,合理利用资源,减少废物排放,实现工艺的可持续发展。
年产二十万吨合成氨变换工段工艺设计

4、二氧化碳
CO2为变换反应的产物,除去CO2有利于反应平衡向生成H2
的方向移动,从而提高CO的变换率,降低变换气中CO含量。
生产中,若选用中变串低变工艺,可在两个变换炉之间串 入脱碳装置,最终CO含量可降低到0.1%。
CO变换工艺流程
CO水蒸气变换反应,简称CO变换反应:
CO+H2O
H2+CO2
转 化 气
CO 13-15%, 800℃, 3.04MPa
甲烷 化预 热器
饱和器
贫液再沸器
变换气
中串低流程特点
主要工艺参数:中变部分的进口温度~ 3000C、 出口温度~ 450℃,低变部分的进口温度~ 1800C、出口温度~ 2300C,反应汽气比~ 0.5,吨氨蒸汽消耗450Kg,中变催化剂空速 ~ 700 h-1,低变催化剂空速~ 1 800 h-1, 出口CO含量~ 1.5%。 与中变流程相比,中串低工艺蒸汽消耗下降, 饱和塔负荷减轻。
蒸汽转化法 制气
煤连续加压 气化法制气
自给
重油部分氧 化水冷激除 碳黑法制气
提供蒸汽 的方式
外供
煤间歇常压 气化法制气
一、大型氨厂一氧化碳中变串低变流程
370℃,
220℃,
CO 3-4%
废 热 锅 炉
中 变 炉
440℃,
低 变 炉
废 热 锅 炉
235℃,
CO 0. 3-0.5%
CO 3-4%
软水
474017.95
85021.13
15330.33
4737.91
中变炉 二段
89759.04
变换工段存在的意义
合成氨的生产主要分为原料气的制取和 原料气的净化与合成。粗原料气中常含有 大量的C0,由于CO是合成氨催化剂的毒物, 所以必须进行净化处理,通常,先经过CO 变换反应,使其转化为易于清除的CO2和氨 合成所需要的H2。因此,CO变换既是原料气 的净化过程,又是原料气造气的继续。最 后,少量的CO用液氨洗涤法,或是低温变 换串联甲烷化法加以脱除。
年产万吨合成氨变换工段工艺设计终稿

Abstract:This design was mainly for the synthetic ammonia plant shift conversion section.The technological process used the middle temperature changefirst ,and then used the low temperature change .Process calculation mainly included material balance, energy balance and equipmentselection.
变换过程需在高温高压使用催化剂条件下进行,因此变换工序是合成氨生产的高成本工序,其成本降低对合成氨成本的降低有重要意义。
1.3
1.
我国的氮肥工业自20世纪50年代以来,不断发展壮大,目前合成氨产量已跃居世界第一位,已掌握了以焦炭、无烟煤、焦炉气、天然气及油田伴生气和液态烃多种原料生产合成氨、尿素的技术,形成了特有的煤、石油、天然气原料并存和大、中、小生产规模并存的生产格局。目前合成氨总生产能力为5000万吨/年左右[3],氮肥工业已基本满足了国内需求,在与国际接轨后,具备与国际合成氨产品竞争的能力,今后发展重点是调整原料和产品结构,进一步改善经济性。
年产万吨合成氨厂合成工段工艺设计工艺流程选择
年产18万吨合成氨厂合成工段工艺设计
工艺步骤选择
原料气为天然气
1、进行原料气预脱硫(钴钼加氢转化)
2、气态烃类蒸汽转化, CH4+H20==CO+3H2
3、一氧化碳变换, 除去CO, 得到制取尿素原料CO2
4、脱除和回收CO2,
5、甲烷化控制CO 和CO2 含量,
6、氨合成
此次设计关键设计氨合成工段
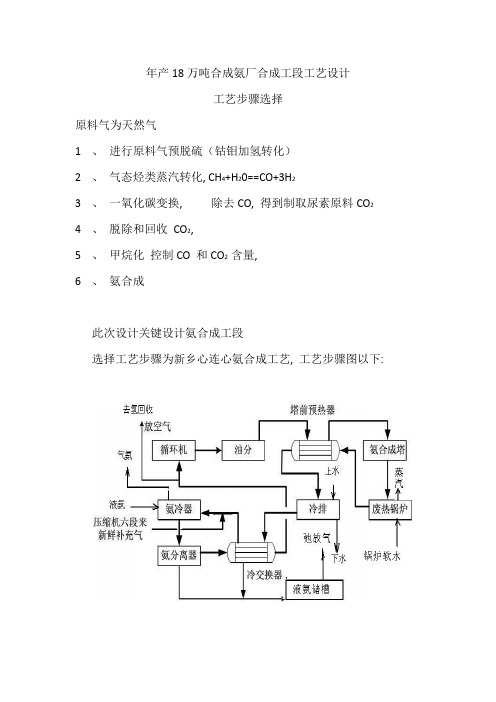
选择工艺步骤为新乡心连心氨合成工艺, 工艺步骤图以下:
具体工艺步骤为:
自烃化工段来原料气和循环机出口循环气精制原料气和循环机出口循环气一起进入油分离器, 分离油污后, 进入塔前预热器, 预热至适宜温度送入氨合成塔, 进行多段合成反应, 反应后热气经合成塔下部换热器冷却进入废热锅炉用锅炉软水回收热量, 以后送入塔前预热器管间冷却, 以后经过冷排器冷却, 温度降至常温进入冷交换管间回收冷量, 下部分离氨后进入卧式氨冷器, 温度降至约10℃左右进氨分离器分离液氨, 气氨回收处理, 液氨经冷交换管内换热升温至25℃进循环机加压与新鲜气混合进氨合成塔进行循环反应, 大部分液氨由氨分离器出口送入液氨储罐。
年产20万吨合成氨合成工艺设计

Harbin Institute of Technology课程设计课程名称:氨合成工段工艺设计设计题目:年产20万吨合成氨合成工段工艺设计院系:化工学院化学工艺系班级:1214221设计者:学号:11214203指导教师:设计时间:2015.6目录课程设计任务书 (1)第一章综述 (2)1.1 氨的研究背景 (2)1.2氨的用途 (2)1.3氨的生产方法的选择 (3)第二章氨合成过程的步骤及工艺流程 (5)2.1氨合成的步骤 (5)2.2氨合成工艺流程简述 (7)第三章工艺计算 (8)3.1 原始条件 (8)3.2 物料衡算 (8)3.2.1 合成塔物料衡算 (8)3.2.2氨分离器气液平衡计算 (9)3.2.3冷凝塔气液平衡计算 (10)3.2.4液氨贮槽气液平衡计算 (11)3.2.5液氨贮槽物料计算 (13)3.2.6合成系统物料计算 (14)3.2.7合成塔物料计算 (15)3.2.8水冷器物料计算 (16)3.2.9氨分离器物料计算 (17)3.2.10冷凝塔物料计算 (18)3.2.11氨冷器物料计算 (20)3.2.12 冷凝塔物料计算 (22)3.2.13液氨贮槽物料计算 (23)3.3 热量衡算 (25)3.3.1合成塔热量计算 (25)3.3.2 废热锅炉热量计算 (27)3.3.3 热交换器热量计算 (28)第四章设备的计算与选型 (30)4.3校核总传热系数K (30)4.3.1 官内给热系数α计算 (30)4.3.2 管外给热系数αo (34)4.3.3 总传热系数K (37)4.4管子拉脱力的计算 (37)4.5 计算是否安装膨胀节 (38)4.6换热器主要结构尺寸和计算结果 (39)结论 (40)参考文献 (41)附录 (42)带控制点的工艺流程图 (42)课程设计任务书课程任务:合成氨合成工段工艺设计设计题目:年产20万吨合成氨合成工段工艺设计设计条件:(1)年产量200kt,年生产时间扣除检修时间后按300天计,则产量为:27.778t/h(2)新鲜补充气组成表3.1新鲜补充气组成(摩尔分数%)组分H2N2CH4Ar 总计含量74.45 24.12 1.10 0.33 100(3)合成塔入口中氨含量:NH3入=2.5%(4)合成塔出口中氨含量:NH3出=16.5%(5)合成塔入口惰性气体含量:CH4 +Ar=15%(6)合成塔操作压力:32Mpa(7)精练气温度:35℃(8)水冷器出口气体温度35℃(9)循环机进出口压差1.47MPa(10)年工作日300 d(11)计算基准生产1t氨第一章综述1.1 氨的研究背景世界合成氨技术的发展经历了传统型蒸汽转化制氨工艺、低能耗制氨工艺、装置单系列产量最大化三个阶段。
合成氨合成工段年产万吨工艺设计毕业设计

合成氨合成工段年产万吨工艺设计毕业设计合成氨是工业生产中的重要化学物品之一,被广泛应用于肥料、塑料、药物等多个领域。
本文将以合成氨合成工段年产万吨工艺设计为主题,为大家介绍合成氨合成过程以及其关键工艺参数的设计要点。
一、合成氨合成过程合成氨的制备主要通过哈伯-卡尔斯过程实现,其反应方程式为:N2 + 3H2 → 2NH3该过程需要高压和高温条件下的催化反应,通常以铁和钼等金属为催化剂。
合成氨合成工段的设计需要精确控制反应条件和原料的配比,以确保高效的氨气生成和产品质量的稳定输出。
二、合成氨合成工段年产万吨工艺设计要点1.反应压力控制反应压力是直接影响哈伯-卡尔斯过程反应速率和氨生成量的重要参数。
在设计合成氨合成工段时,需要通过合理的变量控制方案,确保反应压力的平稳控制。
例如,采用压力传感器和配套控制设备等技术手段,可以根据反应情况及时调整反应压力,以达到最佳工艺效果。
2.反应温度控制反应温度是影响哈伯-卡尔斯过程反应速率和氨生成量的另一个重要参数。
在合成氨合成工段设计中,需要精确控制反应温度,以在确保催化剂稳定性的情况下,使反应率达到最大值。
常见的反应温度控制手段包括热传导油式加热器、蒸汽加热器等。
3.催化剂的选择及生命周期控制在哈伯-卡尔斯过程中,催化剂的选择及其生命周期对合成氨合成工段的效率和质量具有重要影响。
通常采用铁-钼催化剂,具有较高的催化活性和稳定性。
催化剂衰减是一个不可避免的问题,通常采取“烧结-还原”等手段进行再生,以保证催化剂的长期稳定使用。
4.废气净化合成氨合成工段会产生大量的废气,其中含有大量的氮气和氢气等有害气体。
因此,在设计合成氨合成工段时,需要加强废气处理,以防止的环境污染和危害工作人员身体健康。
综上所述,合成氨合成工段的年产万吨工艺设计需要有序、合理地规划反应压力、温度、催化剂及废气净化等关键工艺参数,以确保高效的氨气生成和产品质量的稳定输出。
未来,随着科学技术的不断发展,合成氨合成工段的工艺设计将得到更完善和优化,提高其在工业生产中的重要性和市场竞争力。
化学工程与工艺产万吨合成氨变换工段工艺设计方案[]
![化学工程与工艺产万吨合成氨变换工段工艺设计方案[]](https://img.taocdn.com/s3/m/4cf793226c85ec3a87c2c5f0.png)
第一章物料与热量衡算计算基准:1吨氨计算生产1吨氨需要的变换气量:(1000/17)×22.4/(2×0.2204)=2989.22 M3(标)因为在生产过程中物料可能会有损失,因此变换气量取3000 M3(标)年产10万吨合成氨生产能力(一年连续生产300天):日生产量:100000/300=333.3T/d=13.89T/h要求出低变炉的变换气干组分中CO%不大于0.3%。
假设进中变炉的变换气温度为370℃,取变化气出炉与入炉的温差为20℃,出炉的变换气温度为390℃。
进中变炉干气压力。
P=1.8Mpa.1.水气比的确定:考虑到是天然气蒸汽转化来的原料气,所以取H2O/CO=3.8故V(水)=3.8 Vc=1531.02m3(标) ,n(水)=68.35kmol2.中变炉的计算2.1中变炉CO 的实际变换率的求取假定湿转化气为100mol ,其中CO 湿基含量为8.87%,要求变换气中CO 含量为0.2%,故根据变换反应:CO+H 2O =H 2+CO 2,则CO 的实际变换率公式为:X p %=()a a a a Y Y Y Y '+'-1×100 (2-1)式中a Y 、'a Y 分别为原料及变换气中CO 的摩尔分率(湿基) 所以:X p =()()8.87210010028.87-⨯+⨯ =75.93%则反应掉的CO 的量为:8.87×75.93%=6.73则反应后的各组分的量分别为:H 2O %=33.73%-6.73%=27%CO %=8.87% -6.73%=2.14% H 2% =36.32%+6.73%=43.05% CO 2%=5.99%+6.73%=12.72%中变炉出口的平衡常数:Kp= (H 2%×CO 2%)/(H 2O %×CO %)=9.48 查得Kp=9.48时温度为424℃。
年产18万吨合成氨脱碳工段工艺设计

合成氨脱碳工段是合成氨生产过程中的一个重要环节,主要目的是将合成氨中的CO2去除,以提高合成氨的纯度和质量。
本文将对年产18万吨合成氨脱碳工段的工艺设计进行详细介绍。
1.工艺流程(1)吸收:将合成氨气体通过吸收剂床,与富CO2溶液进行接触,使合成氨中的CO2被吸收到溶液中。
在吸收过程中,需控制吸收剂的流量、压力和温度,以实现高效的CO2吸收。
(2)解吸:将富CO2溶液通过解吸剂床,与低压蒸汽接触,使溶液中的CO2从液体转为气体,同时生成富CO2气体。
解吸过程中需要控制解吸剂的流量、压力和温度,以实现高效的CO2解吸。
(3)净化:将富CO2气体通过一系列的净化装置,如冷凝器、吸附器等,对气体中的杂质进行去除。
净化过程主要包括冷凝、吸附和再生步骤,以确保气体质量的稳定性和CO2的纯度。
(4)再生:将去除杂质后的富CO2溶液进行加热,使其中的CO2从溶液中析出,以得到纯净的CO2、再生过程中需控制溶液的温度和压力,以实现高效的CO2再生。
2.关键技术和设备(1)吸收塔:吸收塔是将合成氨与吸收剂进行接触的装置,主要由塔体和填料组成。
合适的填料能够增加接触面积,提高CO2的吸收效率。
吸收塔还需配置进料系统、排料系统和循环液系统等。
(2)解吸塔:解吸塔是将富CO2溶液与解吸剂进行接触的装置,主要由塔体和填料组成。
解吸塔的设计应考虑接触效果和操作稳定性,以保证CO2的解吸效率和产品质量。
(3)冷凝器:冷凝器主要通过冷却作用,将富CO2气体中的水分和杂质进行去除。
合适的冷凝器设计能够提高气体的净化效果,增加产品的纯度。
(4)吸附器:吸附器主要通过吸附剂对气体中的杂质进行吸附,以净化气体。
合适的吸附剂选择和吸附器设计可以有效去除气体中的杂质,并提高产品的质量。
(5)再生器:再生器主要通过加热作用,将富CO2溶液中的CO2析出,以得到纯净的CO2、再生器的设计应考虑加热方式和操作稳定性,以实现高效的CO2再生。
3.控制策略(1)温度控制:吸收剂和解吸剂的温度是影响CO2吸收和解吸效率的重要因素。
液氨合成工段工艺设计

液氨合成工段工艺设计液氨合成工段工艺设计吉林化工学院化工综合设计2014 届化工原理课程设计设计《年产20万吨天然气合成氨合成段的工艺设计》说明书学生姓名学号所属学院专业班级指导教师二O一二年十二月年产39万吨天然气合成氨合成段的工艺设计任务书一、设计项目:年产20万吨天然气合成氨合成段的工艺设计二、设计规模:20万吨/年,年生产时间:330 三、设计阶段:初步设计四、设计条件与要求1、合成塔进口气体组成(V%)NH3:2.26% H2:58.79% N2:19.55% CH4:17.49% Ar:1.91% 2、合成塔出口气体NH3含量:17.8% 3、水冷器出口温度:35℃4、合成塔操作压力:30.0MPa 五、设计要求和工作量完成设计报告一份六、设计主要内容1、工艺流程设计2、物料衡算3、热量衡算4、主要设备工艺设计与选型化工设计报告(大体章节要求)摘要第一章前言第二章天然气合成氨简介第三章合成氨工艺论证第四章工艺计算4.1物料衡算4.2能量衡算第五章主要设备的工艺计算及选型主要结构参数表第六章设计小结参考文献七、设计主要参考文献《化工原理》;《化工产品手册》;《化工工艺设计手册》;《小氮肥厂工艺设计手册》;《氮肥工艺设计手册》;《小合成氨厂工艺技术与设计手册》;《合成氨》;《无机化工生产技术》等八、设计时间:2012.12.18-2012.12.24 目录设计任务书I 目录II 摘要- 1 - Abstract- 2 - 1 正文- 3 - 1.1 氨的性质、用途及重要性- 3 - 1.1.1 氨的性质- 3 - 1.1.2 氨的用途及在国民生产中的作用- 3 - 1.2 合成氨生产技术的发展- 4 - 1.2.1世界合成氨技术的发展- 4 - 1.2.2中国合成氨工业的发展概况- 6 - 1.3天然气合成氨转变工序的工艺原理- 8 - 1.3.1 天然气合成氨的典型工艺流程介绍- 8 - 1.3.2 天然气合成氨转化工序的工艺原理- 9 - 1.3.3合成氨变换工序的工艺原理- 10 - 1.4 设计方案的确定- 10 - 1.4.1 原料的选择- 10 - 1.4.2 工艺流程的选择- 11 - 1.4.3 工艺参数的确定- 12 - 2 设计工艺计算- 14 - 2.1 转化段物料衡算- 14 - 2.1.1 一段转化炉的物料衡算- 15 - 2.1.2 二段转化炉的物料衡算- 18 - 2.2 转化段热量衡算- 21 - 2.2.1 一段炉辐射段热量衡算- 21 - 2.2.2 二段炉的热量衡算- 28 - 2.3 变换段的衡算- 29 - 2.3.1 高温变换炉的衡算- 29 - 2.3.2 低温变换炉的衡算- 31 - 2.5 设备工艺计算- 34 - 结论- 38 -致谢- 39 - 参考文献- 40 - 主要符合说明- 41 - 附录- 42 - - 43 - 摘要氨是重要的基础化工产品之一,在国民经济中占有重要地位。
化工设计课程设计---合成氨工艺

Keywords: ammonia synthesis section
energy balance accounting
material balance accounting
1.总论..................................................................................................................... 1 1.1 设计任务的依据...................................................................................... 3 1.2 概述.......................................................................................................... 3 1.3 产品方案................................................................................................. 6 1.4 设计产品所需的主要原料规格、来源.................................................. 6 1.5 生产中产生有害物质和处理措施.......................................................... 8 2. 生产流程及生产方法的确定........................................................................... 9 2.1 合成氨生产的特点.................................................................................. 9 2.2 氨合成过程的基本工艺步骤................................................................. 9 2.3 氨合产工艺的选择................................................................................ 12 3. 物料衡算......................................................................................................... 13 3.1 原始条件............................................................................................... 13 3.2 物料衡算............................................................................................... 13 3.2.1 合成塔物料衡算................................................................................ 13 3.2.2 氨分离器气液平衡计算..................................................................... 15 3.2.3 冷交换器气液平衡计算..................................................................... 17 3.2.4 液氨贮槽气液平衡计算..................................................................... 17 3.2.5 液氨贮槽物料计算............................................................................. 20 3.2.6 合成系统物料计算............................................................................. 22 3.2.7 合成塔物料计算................................................................................. 23 3.2.8 水冷器物料计算................................................................................. 24 3.2.9 氨分离器物料计算............................................................................. 25 3.2.10 冷交换器物料计算........................................................................... 25 3.2.11 氨冷器物料计算 ............................................................................... 27 3.2.12 冷交换器物料计算.......................................................................... 29 3.2.13 液氨贮槽物料计算........................................................................... 31 3.2.14 物料衡算结果汇总.......................................................................... 33 4. 热量衡算......................................................................................................... 37 4. 1 冷交换器热量衡算............................................................................... 37
年产20万吨合成氨变换工段工艺设计

年产20万吨合成氨变换⼯段⼯艺设计第1页化⼯设计说明书设计题⽬: 年产20万吨合成氨变换⼯段⼯艺设计系别:化学化⼯学院专业:班级:学⽣:指导⽼师:20年X⽉X⽇本章符号对照表M ——相对分⼦质量,g/mol t/T ——温度,℃ /K Vm ——摩尔体积(0℃,0.1Mpa )22.4/(L/mol) V ——半⽔煤⽓体积,m 3 p co 、p H2O 、p co2 、p H2 ——分别为CO 、H 2 O 、CO 2和H 2各组分的分压H ——标准摩尔焓(kJ /mol )ρ/r ——密度/(kg/ m 3) S ——标准摩尔熵/(J/mol ·k) K p ——平衡常数Kt ——反应速率常数,mol/(MPa0.5·g ·h ) m ——质量,kgy co 、y H2O 、y co2 、y H2 ——分别为CO 、H 2 O 、CO 2和H 2 摩尔分数X ——实际变换率,%y a 、y a ′——分别为原料⽓及变换⽓中⼀氧化碳的摩尔分数Cp ——⽓体的平均⽐热容,kJ/(kmol ·℃)或kJ (kg ·℃)R ——⽓体常数,8.314J/(mol ·K)E ——化学反应活化能,J/molg ——重⼒加速度,m/s2G ——⽓体质量流速,kg/(m2·h) Tm ——最适宜温度,Ki ——⽔蒸⽓在t ℃时的焓,kj/kgΦ——饱和度,% Q ——热量,kJw ——⼲⽓空间速度 m/s u ——催化剂⾃由容积分数 R ——汽/⽓⽐ Di ——塔体内直径,mm d e ——当量直径,m H 塔⾼,mmη——管板填充系数 n ——列管根数 t ——管⼦中⼼距µm ——混合⽓体在温度t 时的黏度,MPa·sµi ——混合⽓体中i 组分在温度t 时的黏度,MPa·sy i ——混合⽓体中i 组分摩尔分数 M i ——混合⽓体中i 组分的分⼦量S a ——⼸形截⾯积,m 2 hˊ——⼸形⾼度,m H ——档板间距,mF ——传热⾯积,m 2 L ——列管长度,m K ——总传热系数,kJ/(m 2 ·h·℃) φ——塔体焊缝隙数 [σ]300 ——筒体材料在设计温度300℃下的许⽤应⼒ C 1 ——钢板厚度负偏差,mm C 2——腐蚀裕量,mm⽬录前⾔ (7)1 绪论 (7)1.1 氨的性质和⽤途 (7)1.2 ⼩型氨⼚的发展 (8)1.3 合成氨⽣产⽅法简介 (8)1.4 ⼀氧化碳变换在合成氨中的意义 (8)2 ⼀氧化碳脱除⽅发和选择 (11)2.1⼀氧化碳的脱除⽅法 (11)2.2⼀氧化碳脱除的⽅案选择 (11)3 ⼀氧化碳变换⽅案 (12)3.1变换原理 (12)3.2变换⽅案的选择 (13)3.3 中变炉的选择 (13)4 变换⼯艺的计算 (15)4.1 中变炉的计算 (15)4.2 饱和热⽔塔出⼝热⽔温度估算 (24) 4.3 饱和热⽔塔物料和热量计算 (24)4.4 换热⽓物料和热量的计算 (28)5 设备的计算 (35)5.1 变换炉的计算 (35)5.2 饱和热⽔塔的计算 (38)5.3主热交换器的计算 (44)5.4 中间换热器的计算 (48)5.5 ⽔加热器的计算 (50)5.6 热⽔循环塔的计算 (53)5.7 变换冷却器的计算 (56)6 变换炉的结构的计算 (60)6.1 变换炉设计条件 (60)6.2变换炉结构计算 (60)7 设备的选型 (66)8 变换反应的⼯艺参数和⼯艺条件 (67) 8.1变换反应的⼯艺参数 (67)8.2 变换过程的⼯艺条件 (67)9 设计结果⼀览表 (70)参考⽂献 (71)致谢 (72)年产20万吨合成氨变换⼯段⼯艺设计指导⽼师:摘要:⽤中温中压三段变换的⽅法,半⽔煤⽓⾸先经过饱和热⽔塔,在饱和热⽔塔内⽓体与塔顶流下的热⽔逆流接触进⾏热量与质量传递,使半⽔煤⽓体温增湿,出塔⽓体进⼊⽓⽔分离器分离夹带的液滴,再进⼊主热换热器、中间换热器和电炉升温,使温度达到320℃左右进⼊变换炉⼀段。
年产20万吨合成氨造气工段工艺设计

摘要本设计是年产能力为20万吨合成氨造气工段(合成氨所需原料气---半水煤气)的初步工艺设计。
本设计采用常压固定床间歇制气法。
根据株化集团合成氨厂现场实习及有关文献资料,完成物料、热量的计算。
此设计配有设计说明书一份,图纸三张。
说明书内容:1.煤造气的发展及发展趋势;2.造气工段的生产原理,流程选择及生产方法的论证与选择;3.物料衡算、热量衡算;4.主要设备的计算及选型;5.安全技术,绿色环保及节能;6.技术经济.三张图纸:1.带控制点的物料流程图;2.设备平面布置图;3.发生炉工艺装配图。
关键词:合成氨;造气;半水煤气;工艺;设计AbstractThis design is a primary design about the synthesis of ammonia 200000T/year techniques accidence contrive. The design owns the process of producing semi-water gas. The design completed the calculation of material and heat quantity according to relevant date. During the design period an instruction and four serials of diagram have been worked out.The instruction includes:1. The development history of producing coal gas and the developing trend.2. The production way of producing semi-water gas、demonstrating and the choosing ,factory chamber plan.3. The calculation of material and the calculation of heat quantity.4. The designing and technological calculation about the main equipment.5. Safety ,Green Initiative and saving energy.6. Economic estimate.Four serious of diagram includes:1. 100000T/Y ammonia process technique flow heat with controlled point.2. The factory chamber plan diagram.3. The factory spare picture.4. The main equipment installing picture.Key words: synthesis ammonia;gas making;semi-water gas;technology design目录第一章前言 (1)第二章合成氨造气概况 (2)2.1 合成气原料的选择 (2)2.2 煤气化发展史 (2)2.3 煤气化技术发展趋势 (2)第三章生产方法的选择及论证 (4)3.1 生产方法的介绍 (4)3.1.1 固定层间歇气化法 (4)3.1.2 固定层连续气化法 (4)3.1.3 沸腾层气化法 (5)3.1.4 水煤浆制气法 (5)3.2 生产方案的选择及论证 (5)第四章常压固定床间歇气化法 (6)4.1 半水煤气定义 (6)4.2 固定床气化法的特点 (6)4.3 生产半水煤气对原料的选择 (6)4.4 半水煤气制气原理 (7)4.5 发生炉内燃料分布情况 (8)4.6 各主要设备的作用 (8)4.6.1 煤气发生炉 (8)4.6.2 燃烧室 (9)4.6.3 废热锅炉 (10)4.6.4 洗气箱 (10)4.6.5 洗涤塔 (11)4.6.6 烟囱 (11)4.6.7 自动机 (11)4.7 间歇式制半水煤气的工艺条件 (11)4.7.1 温度 (11)4.7.2 吹风速度 (11)4.7.3 蒸汽用量 (12)4.7.4 燃料层高度 (12)4.7.5 循环时间 (12)4.7.6 气体成分 (12)4.8 生产流程的选择及论证 (12)4.9 间歇式气化的工作循环 (13)4.10 间歇式制半水煤气工艺流程 (14)第五章工艺计算 (16)5.1 煤气发生炉(含燃烧室)的物料及热量衡算 (16)5.2 物料及热量衡算 (17)5.2.1 物料衡算 (18)5.2.2 热量衡算 (19)5.2.3 吹风效率 (19)5.2.4 热量平衡表 (20)5.3 制气阶段的计算 (20)5.3.1 物料衡算 (20)5.3.2 热量衡算 (22)5.4 总过程计算 (24)5.4.1 燃料使用分配 (24)5.4.2 每100kg燃料的生产指标 (24)5.4.3 物料衡算 (24)5.4.4 热量衡算 (26)5.5 配气计算 (26)5.6 消耗定额 (27)5.7 吹净时间核算 (27)5.8 废热锅炉的热量衡算 (28)5.8.1 设已知条件 (28)5.8.2 热量衡算 (29)5.8.3 热量平衡和总固体平衡 (32)5.9 夹套锅炉的物料及热量衡算 (33)5.9.1 已知条件 (33)5.9.2 产气量及消耗两计算 (33)第六章设备计算.................................................. - 34 -6.1 煤气炉指标计算.............................................. - 34 -6.2 煤气台数的确定.............................................. - 35 -6.3 空气鼓风机的选型及台数确定................................... - 35 -第七章各设备的选型及工艺指标.................................. - 37 -7.1 Φ3米U.G.I型煤气发生炉的工艺指标........................... - 37 -7.2 燃料室的工艺指标............................................ - 37 -7.3 洗气箱工艺指标.............................................. - 38 -7.4 索尔维式废热锅炉工艺指标.................................... - 38 -7.5 填料式洗涤塔工艺指标........................................ - 39 -7.6 煤气发生炉自动加煤机工艺指标................................ - 40 -7.7 10000m3螺旋式气柜的工艺指标................................. - 40 -7.8 集尘器...................................................... - 41 -第八章车间布置简述 ............................................. - 42 -第九章安全技术与节能........................................... - 43 -9.1 安全技术.................................................... - 43 -9.2 绿色环保节能................................................ - 43 -第十章投资和成本估算........................................... - 45 -10.1 人员工资................................................... - 45 -10.1.1 人员编制.............................................. - 45 -10.1.2 一年支付工资及附加费.................................. - 45 -10.2 总投资计算................................................. - 45 -10.2.1 固定资金.............................................. - 45 -10.2.2 建设期贷款利息........................................ - 46 -10.2.3 流动资金.............................................. - 47 -10.3 成本计算................................................... - 47 -第十一章结论 .................................................... - 49 -参考文献........................................................ - 50 -致谢 ........................................................... - 51 -第一章前言本设计为年产20万吨合成氨厂造气工段的初步设计。
年产20万吨合成氨合成工段工艺设计

太原理工大学课程设计题目:年产20万吨合成氨合成工段工艺设计课程设计要求:设计采用中压两级分氨流程,年产20万吨合成氨合成工段的工艺设计。
设计配有设计说明书一份,图纸二张。
说明书内容:原料气来源、流程方案的确定、物料衡算、热量衡算、设备选型及设计计算、车间布置、三废”治理及综合利用。
二张图纸:1.带控制点的合成工段物料流程图; 2.中压合成塔的工艺装配图。
学生应交出的设计文件(纸质及电子版):1.设计说明书(首页附设计任务书)2.工程设计图(CAD版)(1)主要设备图(2)工艺流程图主要参考资料(电子版):一.手册1. 小合成氨厂工艺技术与设计手册(上册),化学工业出版社,1994。
2. 小合成氨厂工艺技术与设计手册(下册) 梅安华主编,化学工业出版社,1994。
3. 氮肥工艺设计手册气体压缩氨合成甲醇合成,化学工业出版社,1989。
4. 氮肥工艺设计手册理化数据分册,石油化学工业出版社,1977。
二.参考文献1中国环球化学工程公司编. 氮肥工艺设计手册[M].19852郝晓刚等编著. 化工原理课程设计. 北京:化学工业出版社,20093陈甘棠主编.化学反应工程[M]. 第三版.北京:化学工业出版社.1990(11)4黄璐. 化工设计. 北京:化学工业出版社,20005陈五平主编.无机化工工艺学.第三版. 北京:化学工业出版社,19856姜胜阶.合成氨工学【J】.石油化学工业出版社,1978(7)7湖北华工设计院.氨合成塔【J】.石油化学工业出版社,1977(12)8化学工业出版社组织编写.中国化工产品大全[M].第二版上卷.9司航主编.化工产品手册[M].第三版.北京:化学工业出版社.10李祥君著.新编精细化工产品手册[M].北京:化学工业出版社.1996.11万家亮曾胜年主编.分析化学[M].第三版. 北京:高等教育出版社.2001(6).12天津化工研究院编.无机与工业手册【M】.北京:化学工业出版,1988(2)13江寿建. 化工厂共用设施设计手册. 北京:化工工业出版社,200014时均等. 化学工程手册. 北京:化学工业出版社,199615赵国方. 化工工艺设计概论. 北京:原子能出版社,199016化工工程师手册编辑委员会. 化学工程师手册. 北京:机械工业出版社,2000 17陈敏恒等. 化工原理,上下册. 北京:化学工业出版社,198518吴志泉等. 化工工艺计算,物料、能量衡算. 上海:华东理工大学出版社,1992 18倪进方. 化工过程设计. 北京:化学工业出版社,1999专业班级化学工程与工艺0802班学生李林豪组别第四组组员李林豪李旭连文豪马楠宋路华要求设计工作起止日期2011.11.21~2011.12.16指导教师签字日期系主任批准签字日期前言《化工设计》课程设计是培养学生化工设计能力的重要教学环节,通过课程设计使我们初步掌握化工设计的基础知识、设计原则及方法;学会各种手册的使用方法及物理性质、化学性质的查找方法和技巧;掌握各种结果的校核,能画出工艺流程、各类塔结构等图形。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
年产20万吨合成氨合成工段工艺设计书1.1 概述氨是一种重要的含氮化合物。
氮是蛋白质质中不可缺少的部分,是人类和一切生物所必须的养料;可以说没有氮,就没有蛋白质,没有蛋白质,就没有生命。
大气中存在有大量的氮,在空气中氨占78%(体积分数)以上,它是以游离状态存在的。
但是,如此丰富的氮,通常状况下不能为生物直接吸收,只有将空气中的游离氮转化为化合物状态,才能被植物吸收,然后再转化成人和动物所需的营养物质。
把大气中的游离氮固定下来并转变为可被植物吸收的化合物的过程,称为固定氮。
目前,固定氮最方便、最普通的方法就是合成氨,也就是直接由氮和氢合成为氨,再进一步制成化学肥料或用于其它工业。
在国民经济中,氨占有重要地位,特别是对农业生产有着重大意义。
氨主要用来制作化肥。
液氨可以直接用作肥料,它的加工产品有尿素、硝酸铵、氯化氨和碳酸氢氨以及磷酸铵、氮磷钾混等。
氨也是非常重要的工业原料,在化学纤维、塑料工业中,则以氨、硝酸和尿素作为氮元素的来源生产己酰胺、尼龙-6、丙烯腈等单体和尿醛树脂等产品。
由氨制成的硝酸,是各种炸药和基本原料,如三硝基申苯,硝化甘油以及其它各种炸药。
硝酸铵既是优良的化肥,又是安全炸药,在矿山开发等基本建设中广泛应用。
氨在其他工业中的应用也非常广泛。
在石油炼制、橡胶工业、冶金工业和机械加工等部门以及轻工、食品、医药工业部门中,氨及其加工产品都是不可缺少的。
例如制冷、空调、食品冷藏系统大多数都是用氨作为制冷剂。
1.2 氨的性质1.2.1 氨的物理性质氨在常温下是无色气体,比空气轻,具有刺激性臭味,能刺激人体感官粘膜空气中,含氨大于0.01%时即会引起人体慢性中毒。
气态氨易溶于水,成为氨水,氨水呈弱碱性。
氨在水中的溶解度随压力增大而降低。
氨水在溶解时放出大量热。
氨水中的氨极易挥发。
常压下气态氨需冷却到-33.35 ℃(沸点)才能液化。
而在常温下需加压到0.87MPa 时才能液化。
液氨为无色液体,气化时吸收大量的热。
1.2.2 氨的化学性质⑴ 氨与氧在催化剂作用下生成氮的氧化物,并能进一步与水作用,制得硝酸: 3224546NH O NO H O +→+⑵ 氨与酸或酐反应生成盐类,是制造氮肥的基本反应:3244242)NH H SO NH SO +=(3343 NH HNO NH NO +=34 NH HCl NH Cl +=334424NH H PO NH H PO +=⑶ 氨与二氧化碳作用生成氨基甲酸铵,进一步脱水成为尿素:32422NH CO NH COONH +=()42222NH COONH CO NH H O =+⑷ 氨与二氧化碳和水作用,生成碳酸氢铵:32243NH CO H O NH HCO ++=(5) 氨可与盐生成各种络合物,如CuCl 2•6NH 3、CuSO 4•4NH 3。
氨与空气(或氧)的混合气,在一定浓度围能发生剧烈的氧化作用而爆炸。
在常温常压下,氨与空气爆炸极限为15%~28%(NH 3)。
100℃,0.1 MPa 下,爆炸极限为14.5%~29.5%(NH3)。
1.3 原料气来源原料气主要有两部分:氮气、氢气。
氮气主要是从空气中提取。
氢气是从半水煤气中提取的,以煤为原料,在一定的高温条件下通入空气、水蒸气或富氧空气-水蒸气混合气,经过一系列反应生成含有一氧化碳、二氧化碳、氢气、氮气、及甲烷等混合气体的过程。
在气化过程中所使用的空气、水蒸气或富氧空气-水蒸气混合气等称为汽化剂。
这种生成的混合气称为煤气。
煤气的成分取决于燃料和汽化剂的种类以及进行汽化的条件。
根据所用汽化剂的不同,工业煤气可分为下列四种:空气煤气:以空气为汽化剂制取的煤气,又称为吹风气。
水煤气:以水蒸气(或水蒸气与氧的混合气)为汽化剂制取的煤气。
混合煤气:以空气和适量的水蒸气为汽化剂制取的煤气,一般作燃料用。
半水煤气:是混合煤气中组成符合(H2+CO)/N2=3.1~3.2的一个特例。
可用蒸气与适量的空气或蒸气与适量的富养空气为汽化剂制得,也可用水煤气与吹风混合配制。
本设计采用半水煤气,半水煤气经过净化后得到纯净的氢气,再配制适量的氮气,成为合成氨的原料气,其中含有氮气、氢气、以及惰性气体甲烷和氩。
1.4 文献综述合成氨工业是氮肥工业的基础,也是一些工业部门的重要原料,它的迅速发展促进了一系列科学技术和化学合成工业的发展,随着科学技术的发展,合成氨工业在国民经济中的作用必将日益显著。
1.4.1 合成氨工业的发展合成氨工业在20世纪初期形成,开始用氨作为火炸药工业的原料,为战争服务;第一次世界大战结束后,转向为农业、工业服务。
随着科学技术的发展,对氨的需要量日益增长,近30年来合成氨工业发展很快。
目前,国合成氨年生产能力30万吨以上的大型企业有26家,合成氨年生产能力10万吨以上的中型企业有100多家,其他还有800多家小氮肥厂也生产约占总量60%的合成氨。
1.4.2 合成氨工业的现状我国合成氨工业存在一些特殊问题,一是氮肥资源紧。
国际上以天然气为原料的氮肥占85%。
而我国氮肥原料以煤为主,天然气仅占20%,我国氮肥行业急需解决采用成熟的粉煤气化技术,以本地粉煤代替无烟块煤。
建议针对不同企业采用不同的技术路线。
技术进行改造。
同时,对于有廉价天然气资源的地区,鼓励采用天然气改造现有装置或建设天然气化肥基地。
二是企业结构不合理,产业集中度低,技术水平不高。
在氮肥行业,要推广新型煤气化技术,包括粉煤气化、水煤浆气化技术等;新型净化技术,如低温变换、低温甲醇洗MDEA等净化技术;新型氨合成塔及大型低压合成的成套技术和装备。
1.4.3 合成氨工业的发展趋势合成氨工业的发展趋势: ①原料路线的变化方向。
煤的储量约为石油、天然气总和的10倍,自从70年代中东石油涨价后,从煤制氨路线重新受到重视,但因以天然气为原料的合成氨装置投资低、能耗低、成本低的缘故,预计到20世纪末,世界大多数合成氨厂仍将以气体燃料为主要原料。
②节能和降耗。
合成氨成本中能源费用占较大比重,合成氨生产的技术改进重点放在采用低能耗工艺、充分回收及合理利用能量上,主要方向是研制性能更好的催化剂、开发新的原料气净化方法、降低燃料消耗、回收和合理利用低位热能等。
③与其他产品联合生产。
合成氨生产中副产大量的二氧化碳,不仅可用于冷冻、饮料、灭火,也是生产尿素、纯碱、碳酸氢铵的原料。
到2010年,力争组建50家大型企业集团,大型氮肥厂合成氨平均规模达40万吨/年以上,中型氮肥厂平均规模达20万吨/年以上。
其产品集中度达到50%,并形成3-5家在国际上有一定影响的大型企业集团。
同时,调整企业结构,减少基础肥料生产厂数量,提高单套装置的规模,使合成氨工业朝现代化又迈进一步。
1.5 设计任务的项目来源本课题是指导老师提高毕业生设计能力而选定的。
希望通过此次课程设计让学生可以较好地把理论学习中的分散知识点和实际生产操作有机结合起来,得到较为合理的设计成果,达到课程设计训练的目的,提高学生分析和解决化工实际问题的能力。
第二章 流程方案的确定2.1 生产原理氨是由气态氮和氢在适宜温度压力,并有触媒的作用下发生反应的,其反应式为: 22331 46.22 22H N NH KJ +→+ 此式为一不可逆,放热,体积缩小的反应,其反应过程为: 223322222N N NH NH NH NH →→→→→(扩散)(吸附)(吸附)(吸附)(附)(扩散到气相)氨合成的反应特点:⑴ 反应过程要在高压下进行,压力越高,越有利于氨的合成。
⑵ 温度低时,反应有利于向氨合成的方向进行,但反应速度较慢,提高温度不利于反应平衡,但可以加快反应速度,在实际操作中,温度的选择取决于触媒的活性。
⑶ 必须借助触媒,以加快反应速度。
⑷ 混合气中氢、氮含量越高越有利于反应,因此,气体中惰性气体含量越少越好。
2.2 各生产方法及特点合成氨的生产主要包括三个步骤 :第一步是造气,即制备含有氢、氮的原料气;第二步是净化,不论选择什么原料,用什么方法造气,都必须对原料气进行净化处理,以除去氢、氮以外的杂质;第三步是压缩和合成,将纯净的氢、氮混合压缩到高压,在铁催化剂与高温条件下合成为氨。
目前氨合成的方法,由于采用的压力、温度和催化剂种类的不同,一般可分为低压法、中压法和高压法三种。
(1) 低压法操作压力低于20 MPa的称低压。
采用活性强的亚铁氰化物作催化剂,但它)要求十分严格。
也可用磁铁矿对毒物很敏感,所以对气体中的杂质(CO、CO2作催化剂,操作温度450~550 ℃。
该法的优点是由于操作压力和温度较低,对设备、管道的材质要求低、生产容易管理,但低压法合成率不高,合成塔出口气体中含氮约8%~10%,所以催化剂的生产能力比较低;同时由于压力低而必须将循环气降至-20℃的低温才能使气体中的氨液化,分离比较完全,所以需要设置庞大的冷冻设备,使得流程复杂,且生产成本较高。
(2) 高压法操作压力为60 MPa 以上的称为高压法,其操作温度大致为550~650 ℃。
高压法的优点是,氨合成的效率高,合成氨出口气体中含氨达25%~30%,催化剂的生产能力较大。
由于压力高,一般用水冷的方法气体中的氨就能得到完全的分离,而不需要氨冷。
从而简化了流程;设备和流程比较低紧凑,设备规格小,投资少,但由于在高压高温下操作,对设备和管道的材质要求比较高。
合成塔需用高镍优质合金钢制造,即使这样,也会产生破裂。
高压法管理比较复杂,特别是由于合成率高,催化剂层的反应热不易排除而使催化剂长期处于高温下操作,容易失去活性。
(3) 中压法操作压力为20~35 MPa的称为中压法,操作温度为450~550 ℃。
中压法的优缺点介于高压法与低压法中间,但从经济效果来看,设备投资费用和生产费用都比较低。
氨合成的上述三种方法,各有优缺点,不能简单的比较其优劣。
世界上合成氨总的发展趋势多采用中压法,其压力围多数为30~35 MPa。
本设计采用中压法,操作压力为32 MPa。
2.3 工艺流程的选择合成氨的生产工艺条件必须满足产量高,消耗低,工艺流程及设备结构简单,操作方便及安全可靠等要求。
决定生产条件最主要的因素有操作压力、反应温度、空间速度和气体组成等。
(1) 最适宜的操作压力氨合成反应是气体体积缩小的反应,提高压力有利于反应平衡向右移动。
压力增加平衡常数增大,因而平衡氨含量也增大。
所以,提高压力对氨合成反应的平衡和反应速度都有利,在一定空速下,合成压力越高,出口氨浓度越高,氨净值越高,合成塔的生产能力也越大。
氨合成压力的高低,是影响氨合成生产中能量消耗的主要因素之一。
主要能量消耗包括原料气压缩功、循环气压缩功和氨分离的冷冻功。
提高操作压力,原料气压缩功增加,合成氨净值增高,单位氨所需要的循环气量减少,因而循环气压缩功减少,同时压力高也有利于氨的分离,在较高气温下,气氨即可冷凝为液氨,冷冻功减少。
