医疗器械库房温湿度记录表
医疗器械库房温湿度记录表

医疗器械库房温湿度记录表
医疗器械库房是医院用于存放各种医疗器械、耗材和药品的场所,对库房内的温度和湿度有非常严格的要求。
因此,需要对库房的温湿度进行记录,以确保医疗器械、耗材和药品的质量和安全。
目的
记录医疗器械库房的温湿度数据,以确保库房温湿度符合要求,并及时发现并解决异常情况,确保库房内的器械、耗材和药品质量和安全。
测量方法
在库房内设置温湿度计,并将数据记录在如下的表格中。
温湿度记录表
库房位置测量时间温度(℃)湿度(%)备注
记录要求
1.库房位置:表示记录温湿度数据的库房位置。
如某某医院一楼康复科
库房、某某中心仪器库房等等。
2.测量时间:表示记录温湿度数据时的时间。
3.温度:表示记录的温度数据,单位为℃(摄氏度)。
4.湿度:表示记录的湿度数据,单位为%(百分比)。
5.备注:表示记录时需要注意的事项,如异常情况的说明等。
数据处理
当记录的温度和/或湿度数据超出规定范围(如温度超过设定的上限,湿度低于设定的下限等)时,需要及时处理。
可以通过调整室内空调、加湿器等设备或者通风换气等方式进行处理。
通过记录医疗器械库房的温湿度数据,并及时处理异常情况,可以保证器械、耗材和药品的质量和安全。
因此,做好记录和处理工作非常重要。
医疗器械GSP文件-库房贮存、养护、出入库管理制度

1.目的为规范公司所有医疗器械产品的贮存、养护、出入库管理,特制订如下制度2.范围:适用于公司的业务部与质量部。
3职责:质量部及业务部执行本制度.4.内容4.1.库房贮存4.1.1应当配备与经营产品相适应的储存条件。
按照医疗器械的贮存要求分库(区)、分类存放,包括待验区、合格品区、不合格品、发货区、退货区等,并有明显区分(如可采用色标管理,设置待验区为黄色、合格品区、发货区为绿色、不合格品区、退货区为红色),退货产品应当单独存放。
4.1.2医疗器械与非医疗器械应该分开存放。
4.1.3库房的条件应当符合以下要求:a)库房内外环境整洁,无污染源;b)库房内墙光洁,地面平整,房屋结构严密;c)有防止室外装卸、搬运、接收、发运等作业受异常天气影响的措施;d)库房有可靠的安全防护措施,能够对无关人员进入实行可控管理。
4.1.4企业应当根据医疗器械的质量特性进行合理贮存,并符合以下要求:a)按说明书或包装标示的贮存要求贮存医疗器械;b)贮存医疗器械应按照要求采取避光、通风、防潮、防虫、防鼠、防火等措施;c)搬运和堆垛医疗器械应按照包装标示要求规范操作,堆垛高度符合包装图示要求,垛与垛之间距离至少相隔30厘米,避免损坏医疗器械包装;d)按照医疗器械的贮存要求分库(区)、分类存放,医疗器械与非医疗器械应分开存放;e)医疗器械应按规格、批号分开存放,医疗器械与库房地面、内墙、顶、灯、温度调控设备及管道等设施间保留有足够空隙,最少相隔10厘米;f)贮存医疗器械的货架、托盘等设施设备应保持清洁,无破损;g)非作业区工作人员未经批准不得进入贮存作业区,贮存作业区内的工作人员不得有影响医疗器械质量的行为;h)医疗器械贮存作业区内不得存放与贮存管理无关的物品。
4.2.库存养护4.2.1仓库保管员要在质量部门的技术指导下,检查并改善贮存条件、防护措施、卫生环境,检查并改善贮存与作业流程,对冷库温度自动报警装置进行检查、保养。
仓库温湿度记录(有数据参考)-
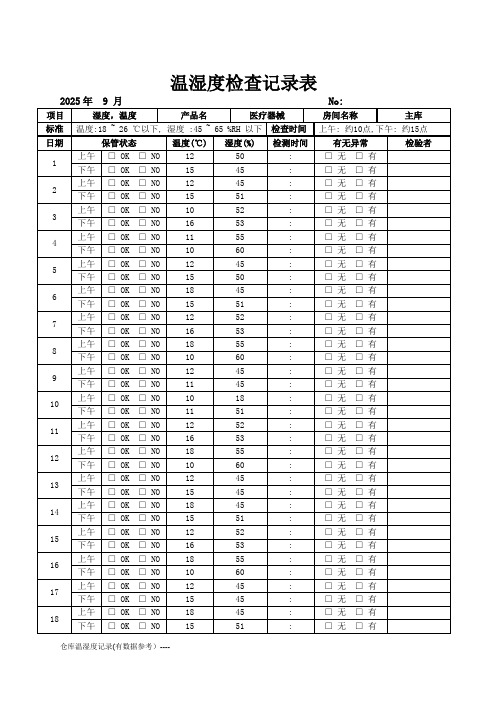
55
:
□ 无 □ 有
下午
□ OK □ NO
10
60
:
□ 无 □ 有
9
上午
□ OK □ NO
12
45
:
□ 无 □ 有
下午
□ OK □ NO
11
45
:
□ 无 □ 有
10
上午
□ OK □ NO
10
18
:
□ 无 □ 有
下午
□ OK □ NO
11
51
:
□ 无 □ 有
11
上午
□ OK □ NO
12
52
:
□ 无 □ 有
12
45
:
□ 无 □ 有
下午
□ OK □ NO
15
45
:
□ 无 □ 有
22
上午
□ OK □ NO
18
45
:
□ 无 □ 有
下午
□ OK □ NO
15
51
:
□ 无 □ 有
23
上午
□ OK □ NO
12
52
:
□ 无 □ 有
下午
□ OK □ NO
16
53
:
□ 无 □ 有
24
上午
□ OK □ NO
18
55
:
□ 无 □ 有
5
上午
□ OK □ NO
12
45
:
□ 无 □ 有
下午
□ OK □ NO
15
50
:
□ 无 □ 有
6
上午
□ OK □ NO
18
医疗器械经营企业质量管理制度及工作程序附属表格(多表格)
产品出库、复核、销售记录
产品购进记录
出库单
入库单
商品投诉、质量查询报告单
医疗器械商品养护记录
医疗器械售后服务反馈登记表
医疗器械效期产品管理记录
用户访问联系记录表
医疗器械商品退货记录
医疗器械安装调试维修记录编号:
可疑医疗器械不良事件报告表国家食品药品监督管理局制
报告来源:生产企业□经营企业□使用单位□单位名称:
联系地址:邮编:联系电话:编码:□□□□□□□□□□□
报告人签名:
医疗器械员工培训档案
库房温湿度记录表年月。
医疗器械库房温湿度记录表

医疗器械库房温湿度记录表医疗器械库房温湿度记录表日期:[日期]库房:[库房名称]记录员:[记录员姓名]温湿度记录时间温度(℃)湿度(%)08:00:00 [温度] [湿度]09:00:00 [温度] [湿度]10:00:00 [温度] [湿度]11:00:00 [温度] [湿度]12:00:00 [温度] [湿度]13:00:00 [温度] [湿度]14:00:00 [温度] [湿度]15:00:00 [温度] [湿度]16:00:00 [温度] [湿度]17:00:00 [温度] [湿度]18:00:00 [温度] [湿度]温湿度说明温度记录范围:15℃ 25℃湿度记录范围:45% 55%温湿度记录应在每小时记录一次数据分析与处理根据以上记录,我们可以对温湿度数据进行分析与处理,确保医疗器械库房的温湿度在合适的范围内。
温度分析根据记录表格中的温度数据,我们可以对温度变化进行分析。
正常情况下,医疗器械库房的温度应保持在15℃ 25℃的范围内。
如果温度超过这个范围,可能会对储存的器械产生不利影响,如过高的温度可能导致器械变质,过低的温度可能对某些器械的性能产生影响。
湿度分析湿度是另一个重要的指标,对器械的贮存也有一定的影响。
根据记录表格中的湿度数据,我们可以对湿度变化进行分析。
一般来说,医疗器械库房的湿度应保持在45% 55%的范围内。
如果湿度过高,可能会导致器械受潮,从而降低器械的性能和质量;如果湿度过低,可能会导致器械干燥,容易损坏。
处理措施根据数据分析的结果,如果温湿度超出正常范围,应立即采取相应的处理措施。
例如,如果温度过高,可以采取降温措施,如增加通风、使用空调等;如果湿度过高,可以采取除湿措施,如加强通风、使用除湿机等;如果温湿度过低,可以采取加温加湿措施,如使用加湿器、加热器等。
结论通过对医疗器械库房的温湿度进行记录、分析和处理,可以确保医疗器械在适宜的环境下贮存,在一定程度上降低器械损坏的风险,提高其使用寿命和质量。
医疗器械仓库温度管理制度

一、目的为确保医疗器械在储存、运输和使用过程中的质量,防止因温度控制不当导致医疗器械变质、损坏,特制定本制度。
二、适用范围本制度适用于公司所有医疗器械产品的储存、运输环节,以及相关设施和设备的温度控制。
三、管理制度1. 温度控制要求(1)医疗器械仓库应保持温度在5-38℃之间,湿度在30-80%之间。
(2)医疗器械储存区、运输工具及运输过程中的温度应按照产品说明书或相关法规要求进行控制。
2. 温湿度监测(1)仓库内应配备温湿度计,用于实时监测库房内的温度和湿度。
(2)温湿度计应悬挂于库房内不易被阳光直射的墙壁上,高度应满足库房管理员平视的要求。
(3)库房管理员应每日上、下午各一次定时填写《温湿度记录表》,记录库房内的温度和湿度。
3. 温湿度异常处理(1)如发现库房内温度、湿度异常,应及时采取以下措施:①关闭门窗,减少外界温度、湿度对库房的影响;②开启空调、除湿设备等设备,调节库房内温度、湿度;③如异常情况无法在短时间内得到控制,应将受影响的产品移至其他库房或临时储存区域;④及时向相关部门报告异常情况,并采取相应措施进行处理。
(2)如异常情况对医疗器械质量造成影响,应立即停止使用该批产品,并向相关部门报告。
4. 设备维护与保养(1)定期对空调、除湿设备等温度控制设备进行维护和保养,确保其正常运行。
(2)定期检查温湿度计的准确性,如有异常,应及时更换。
5. 人员培训与考核(1)对库房管理员进行温度控制方面的培训,使其掌握相关知识和技能。
(2)定期对库房管理员进行考核,确保其能够胜任工作。
四、监督与检查1. 质量管理部门负责对医疗器械仓库温度管理制度执行情况进行监督和检查。
2. 对违反本制度的行为,将根据情节严重程度进行处罚。
五、附则1. 本制度由质量管理部门负责解释。
2. 本制度自发布之日起实施。
2017版医疗器械记录表格

医疗器械质量管理文件记录表格(2017年版)公司名称:XXXX药业有限责任公司修订日期:二〇一七年十月二十日XXXX药业有限责任公司医疗器械记录目录001、XXXX药业有限责任公司采购记录 (3)002、XXXX药业有限责任公司验收记录 (4)003、XXXX药业有限责任公司随货同行单 (5)004、XXXX药业有限责任公司温湿度记录 (7)005、XXXX药业有限责任公司入库记录 (9)006、XXXX药业有限责任公司定期检查记录 (10)007、XXXX药业有限责任公司出库复核记录 (11)008、首营企业审批表 (13)009、客户资质审核表 (14)010、首营品种审批表 (15)011、XXXX药业有限责任公司销售记录 (17)012、XXXX药业有限责任公司不合格品种销毁登记表 (18)013、拼箱单 (19)014、XXXX药业有限责任公司停售通知记录 (21)015、XXXX药业有限责任公司召回记录 (21)016、设施设备检查维护记录 (23)017、XXXX药业有限责任公司设施设备档案 (24)018、仪器、设备使用记录 (25)019、年度企业员工健康检查汇总表 (26)020、员工健康档案 (28)021、年度培训计划 (30)022、培训实施记录表 (31)023、培训签到表 (33)024、员工个人培训教育档案(一) (34)025、医疗器械质量跟踪记录 (35)026、医疗器械用户投诉纪录 (36)027、医疗器械售后服务记录 (38)028、医疗器械运输交接单 (39)001.XXXX药业有限责任公司采购记录XXXX药业有限责任公司采购记录---002.XXXX药业有限责任公司验收记录XXXX药业有限责任公司验收记录---003.XXXX药业有限责任公司随货同行单XXXX药业有限责任公司随货同行单发货日期:单据编号:收货单位名称:收货地址:备注:1.非质量问题概不退货2.特殊储存器械售出后概不退货第1页/共1页------004.XXXX药业有限责任公司温湿度记录XXXX药业有限责任公司温湿度记录.005.XXXX药业有限责任公司入库记录XXXX药业有限责任公司入库记录---006.XXXX药业有限责任公司定期检查记录XXXX药业有限责任公司定期检查记录---XXXX药业有限责任公司出库复核记录发货日期:单据编号:购货单位名称:购货单位地址:008.首营企业审批表首营企业审批表009.客户资质审核表客户资质审核表编号:日期:010.首营品种审批表首营品种审批表编号:日期:011.XXXX药业有限责任公司销售记录XXXX药业有限责任公司销售记录单位名称:单位地址:012.XXXX药业有限责任公司不合格品种销毁登记表XXXX药业有限责任公司不合格品种销毁登记表日期:单据编号:经办人:监督人:013.拼箱单拼箱单拼箱单收货单位:日期:收货单位:复核人:拼箱单收货单位:日期:014.XXXX药业有限责任公司停售通知记录XXXX药业有限责任公司停售通知记录各有关部门:以下医疗器械经检查质量有问题,暂停发货,特此告知。
2024年医疗器械库房贮存、出入库及运输管理制度(三篇)

2024年医疗器械库房贮存、出入库及运输管理制度篇一:医疗器械仓库管理规程仓库管理规程一、目的:为了加强仓库管理工作,防止产品在使用或交付前受到损坏或变质,特制定本规定。
二、适用范围:本制度适用于所有原材料、包装材料及成品的贮存管理。
三、管理制度:1、仓库重地,严禁非仓库工作人员随意出入;有事须进库房时,必须有库房人员陪同。
2、仓库应以“安全、方便、节约”的原则,正确选择仓位,合理使用仓容,堆码合理、整齐,无倒置现象。
物品码放应距墙面20厘米以上,必要时,采取上苫下垫措施。
3、仓库内温度应控制在5-38℃,湿度在____%之间。
做好仓库温湿度管理工作,每日应上、下午各一次定时填写《温湿度记录表》。
温湿度异常应及时向有关部门反馈采取措施。
4、仓库应保持光线充足,保持通风透气,避免阳光直射,不积水,不积尘,不结蜘蛛网,阴雨天气及时关窗。
5、仓库内实行色标管理,合格区为绿色、退货区为黄色、不合格区为红色。
6、仓库内出现产品质量问题,应及时报质管人员确认和处理,将有问题的产品放入不合格区存放,待查明原因后,作退货或销毁处理,处理结果应有记录。
7、仓库应定期进行清洁打扫,保持库房环境清洁,配置消防、安全防鼠、防虫、防尘设施,做好防盗、防火、防潮、防霉、防虫、防鼠、防污染工作。
8、对各类养护仪器及设备设施应定期检查。
9、酒精等化学品必须进行隔离存放,搬运酒精等易燃易爆物品时,严禁烟火,做好防护措施。
9.1化学品管理职责:采购部负责公司化学品采购。
原材料库负责对库存化学品进行管理。
9.2化学品管理规定细则:原材料库对库存化学品进行隔离存放,库区内严禁烟火。
库存化学品台帐,标识卡片等必须标注生产日期,以生产日期为准,按生产日期或保质期出库。
化学品存放地点应避免高温线照射,温度过高应采取通风降温措施。
10、物品入库/出库管理:10.1所有原材料、包装材料及成品必须经检验合格后方可入库,由库管员办理入库手续,填写物料卡片,原材料和配件要填写该批料的生产日期和有效期,填写仓库物料标示卡。
三类医疗器械质量管理记录系列表格

医疗器械质量管理记录1、文件修订申请表 (3)2、文件发放记录表 (4)3、文件回收记录表 (5)4、文件销毁申请表 (6)5、文件销毁记录表 (7)6、质量管理体系问题改进和措施跟踪记录 (8)7、医疗器械群体不良事件基本信息表 (9)8、医疗器械不良反应/事件报告表 (10)9、质量查询、投诉、服务记录 (12)10、质量事故调查、处理表 (13)11、医疗器械质量投诉处理记录 (14)12、质量事故处理跟踪记录 (15)13、员工健康档案表 (17)14、员工健康检查汇总表 (18)15、年度质量培训计划表 (19)16、培训签到表 (20)17、培训实施记录表 (21)18、员工个人培训教育档案 (22)19、设施设备台帐 (23)20、设施设备运行维护使用记录 (24)21、计量器具检定记录 (25)22、医疗器械养护质量情况分析季度报表 (26)23、医疗器械质量信息反馈表 (27)24、医疗器械质量信息传递处理单 (28)25、医疗器械召回记录 (29)26、医疗器械追回记录 (30)27、不合格医疗器械台帐 (32)28、不合格医疗器械报损审批表 (33)29、不合格医疗器械报损销毁审批表 (34)30、质量管理制度执行情况自查及整改记录表 (35)31、质量管理制度执行情况检查和考核记录表 (36)32、医疗器械采购记录 .......................................................................................................................................... .3433、医疗器械收货记录 (35)34、医疗器械验收记录 (36)35、医疗器械出库记录 (37)36、温湿度记录表 (36)37、计算机系统权限授权审批记录表 (36)38、车辆日常保养及卫生检查表 (40)39、月卫生检查记录表 (41)40、设施设备检修维护记录 (42)41、医疗器械质量监控检查记录 (36)42、医疗器械质量复查报告单 (36)43、医疗器械停售通知单 (36)44、医疗器械解除停售通知单 (36)45、医疗器械拒收通知单 (36)46、合格供货方档案表 (36)47、储存作业区来访人员登记表 (36)48、首营企业审批表 (50)49、首营品种审批表 (36)50、全体人员情况表 (36)51、供货企业质量体系评定表 (36)52、质量保证体系调查表 (36)53、医疗器械质量档案表 (36)54、医疗器械质量信息汇总表 (56)1、文件修订申请表编号:JYBN-QXJL-001-012、文件发放记录表编号:JYBN-QXJL-002-013、文件回收记录表编号:JYBN-QXJL-003-014、文件销毁申请表编号:JYBN-QXJL-004-015、文件销毁记录表编号:JYBN-QXJL-005-016、质量管理体系问题改进和措施跟踪记录编号:JYBN-QXJL-006-017、医疗器械群体不良事件基本信息表编号:JYBN-QXJL-007-01报告日期:年月日8、医疗器械不良反应/事件报告表编号:JYBN-QXJL-008-01首次报告□跟踪报告□报告类型:新的□严重□一般□报告单位类别:医疗机构□经营企业□生产企业□个人□其他□9、质量查询、投诉、售后服务记录编号:JYBN-QXJL-009-0110、质量事故调查、处理表11、医疗器械质量投诉处理记录编号:JYBN-QXJL-011-0112、质量事故处理跟踪记录编号:JYBN-QXJL-012-0113、员工健康档案表编号: JYBN-QXJL-013-01注:应将历次体检结果证明文件存入档案14、员工健康检查汇总表编号: JYBN-QXJL-014-01'.年度培训计划表编号:JYBN-QXJL-015-01质管部:行政部:审批人:'...培训签到表编号:JYBN-QXJL-016-0117、培训实施记录表编号:JYBN-QXJL-017-01'.18、员工个人培训教育档案编号:JYBN-QXJL-018-01记录人:'.19、设施设备台帐编号:JYBN-QXJL-019-0120、设施设备运行维护使用记录编号:JYBN-QXJL-020-0121、计量器具检定记录编号:JYBN-QXJL-021-0122、医疗器械养护情况汇总分析季度报表编号:JYBN-QXJL-022-01养护员:汇总日期:年月日23、医疗器械质量信息反馈表编号:JYBN-QXJL-023-0124、医疗器械质量信息传递处理单编号:JYBN-QXJL-024-0125、医疗器械召回记录编号:JYBN-QXJL-025-01'.26、医疗器械追回记录编号:JYBN-QXJL-026-01'.'.27、不合格医疗器械台帐编号:JYBN-QXJL-027-01'.28、不合格医疗器械报损审批表编号:JYBN-QXJL-028-0129、不合格医疗器械报损销毁审批表30、质量管理制度执行情况自查及整改记录表编号:JYBN-QXJL-030-01部门:年月日31、质量管理制度执行情况检查和考核记录表编号:JYBN-QXJL-031-0132、医疗器械采购记录编号:JYBN-QXJL-032-0133、医疗器械收货记录编号:JYBN-QXJL-033-01编号:JYBN-QXJL-034-01..36、温湿度记录表编号:JYBN-QXJL-036-01年月37、计算机系统权限授权审批记录表编号:JYBN-QXJL-037-0138、车辆日常保养及卫生检查表编号: JYBN-QXJL-038-0139、月卫生检查记录表编号:JYBN-QXJL-039-01 检查日期:年月日的符合或不符合的□内打√。
gmp 药品仓库温湿度记录表范文

gmp 药品仓库温湿度记录表范文英文回答:GMP (Good Manufacturing Practice) is a set of guidelines that ensures the quality and safety of pharmaceutical products. As a pharmaceutical company, we have a responsibility to comply with GMP regulations, including the proper storage and monitoring of drugs in our warehouse.One important aspect of GMP compliance is the maintenance of proper temperature and humidity levels in the drug storage area. This is crucial to ensure that the drugs remain stable and effective throughout their shelf life. To monitor and record the temperature and humidity in our warehouse, we use a temperature and humidity recording sheet.The recording sheet contains columns for date, time, temperature, and humidity readings. Every day, ourwarehouse staff takes readings at regular intervals and records them on the sheet. This helps us track any fluctuations in temperature and humidity over time and take corrective actions if necessary.For example, let's say it's a hot summer day and the temperature in the warehouse starts to rise above the recommended range. The recording sheet will show this increase in temperature, and we can take immediate steps to bring it back to the desired level. This may involve adjusting the air conditioning or ventilation systems, or even relocating some of the heat-sensitive drugs to a cooler area of the warehouse.Similarly, if the humidity levels in the warehouse are too high, it can lead to moisture absorption by the drugs, which can affect their stability. By monitoring the humidity readings on the recording sheet, we can identify any deviations from the acceptable range and take appropriate measures to control the humidity levels. This may involve using dehumidifiers or implementing better ventilation systems to maintain optimal conditions for drugstorage.In addition to recording the temperature and humidity, the recording sheet also includes a section for any observations or actions taken. This allows us to document any incidents or issues that may have occurred during the monitoring process. For instance, if there was a power outage that affected the temperature control in the warehouse, we would make a note of it on the recording sheet.By diligently maintaining and reviewing the temperature and humidity recording sheet, we can ensure that our pharmaceutical products are stored under the appropriate conditions as required by GMP regulations. This helps us maintain the quality and efficacy of our drugs, ultimately ensuring the safety and well-being of the patients who rely on them.中文回答:GMP(良好生产规范)是一套确保药品质量和安全的指导方针。
医疗器械仓库温湿度检测和记录规定

存在的问题
部分仓库在温湿度控制方面存在 不足,如设备老化、故障等,导 致温湿度波动较大,对医疗器械
的质量造成潜在威胁。
改进措施
针对存在的问题,相关监管部门 应加强对医疗器械仓库的监督和 检查,督促其及时更换或维修设
备,确保温湿度的稳定控制。
未来发展趋势与展望
智能化发展
随着物联网、大数据等技术的不断发展,未来医疗器械仓 库将实现智能化管理,通过自动化设备对温湿度进行实时 监测和调控,提高管理效率和准确性。
远程监控
借助互联网技术,实现远程监控医疗器械仓库的温湿度状 况,及时发现并解决问题,确保医疗器械的安全和有效性 。
多功能集成
未来医疗器械仓库将不仅具备温湿度检测和记录功能,还 将集成其他功能,如防火、防盗、防潮等,提高仓库的综 合管理水平。
THANK YOU
感谢聆听
特殊器械的温湿度要求
植入类医疗器械
通常要求存放在阴凉库中,温度控制在15-25℃,相 对湿度控制在45%-65%。
体外诊断试剂
一般要求存放在冷藏库中,温度控制在2-8℃,避免 冻结。相对湿度一般控制在30%-70%。
一次性使用无菌医疗器械
一般要求存放在常温库中,温度控制在20-25℃,相 对湿度控制在50%-70%。同时要注意防止阳光直射 和潮湿。
选用专业温湿度控制设备
采用专业的温湿度控制设备,如空调、除湿机、加湿器等,对仓库 的温湿度进行精确控制。
建立温湿度监测系统
安装温湿度监测设备,实时监测仓库内的温湿度变化,并将数据传 输至中央控制系统进行分析和处理。
调节方法与技巧
1 2 3
及时调节仓库门窗
根据室内外温湿度的变化,及时调节仓库门窗的 开关程度,以保持仓库内温湿度的稳定。
医疗器械经营企业质量管理记录

医疗器械经营企业质量管理记录首营企业审批表企业名称:企业地址:社会统一信用代码:许可证号:有效期限:法定代表人:联系人:销售人员:传真:联系身份证号:注册资金:发证日期:经营方式:类别:器械生产企业 / 器械经营企业(生产企业略)经营或生产范围:拟购进品种:采购意见(签字):年月日审核意见:质量负责人(签字):年月日审批意见:法人或企业负责人(签字):年月日审批表应附资料(均应加盖供方原印章):1、医疗器械经营许可证(第二类经营备案凭证)或医疗器械生产许可证(第一类生产备案凭证)复印件;2、营业执照复印件;3、销售人员授权书原件;4、销售人员身份证复印件;5、供货方随货同行单样本。
首营品种审批表产品名称:型号规格:产品性能:结构及组成:产品适用范围:产品禁忌症:生产企业名称:生产地址:供货企业名称:业务联系人:法定代表人:联系法定代表人:联系注册证号(备案凭证号):储运条件:供货企业生产或经营范围:采购意见(签字):年月日审核意见:审批意见:审批表应符资料(均应加盖供货方原印章):1、医疗器械产品注册证(变更文件)或备案凭证;2、产品外包装、标签、说明书;3、样品或宣传彩页;4、采购合同或协议(含质量保证协议);法人或企业负责人(签字):年月日质量负责人(签字):年月日医疗器械采购记录序号购货日期名称规格(型号)产品注册证号或(备案凭证编号)单位数量单价金额供货单位生产厂家备注医疗器械验收记录年度有效期或失效期生产企业供货者到货数量到货日期验收合格数量验收结果验收人员验收日期备注序号名称规格(型号)注册证号或备案凭证号批号或序列号生产日期医疗器械在库养护、检查记录年度检查日期名称规格(型号)注册证号或备案凭证号批号或序列号生产日期有效期或失效期生产企业数量外观是否完好包装有无破损处理结果养护员签字备注医疗器械出库、复核记录年度出库日期购货者名称规格型号注册证号或备案凭证编号批号或序列号生产日期有效期或失效期生产企业数量质量状况复核员备注医疗器械运输记录年度序号送货日期购货者送货地址销售清单(随货同行单)号出发时间送达时间送货车辆接收人送货人备注日期供货者购货者名称号(备案凭证编号)退货原因备注医疗器械销售记录(批发)年度008:本文记录了医疗器械批发销售的详细信息,包括销售日期、名称、规格、型号、注册证号或备案凭证编号、数量、单价、金额、批号或序列号、生产许可证、有效期、生产企业号或备案凭证编号、经营许可证、购货者名称号(备案凭证编号)、经营地址联系方式等。
医疗器械公司医疗器械在库保管、养护制度

医疗器械在库保管、养护制度
一、要根据不同季节、气候变化,做好库房的温湿度管理工作,坚持每日两次(上午9:00-10:00,下午2:00-3:00)按时观察库内温、湿度的变化,认真填写“温湿度记录表”,并根据具体情况和医疗器械的性质及时调节温湿度,保证医疗器械贮存质量。
温度控制:常温库为10—30℃,阴凉库为温度≤20℃;湿度控制在45-75%之间。
二、养护人员应对在库医疗器械每季度至少养护检查一次,可以按照“三三四”循环养护检查,(所谓三三四指一个季度为库存循环的一个周期,第一个月循环库存的30%,第二个月循环库存的30%,第三个月循环库存的40%)并做好养护记录,发现问题,应挂黄牌停止发货并及时填写“质量复检通知单”交质管部门处理。
三、养护员对近效期产品挂牌标示、,对效期在6个月以内的产品应按月填写效期医疗器械催销表。
四、做好货贺的清洁卫生,做好防火、防尘、防潮、防热、防霉、防虫、防鼠、防鸟、防污染等工作。
五、医疗器械实行分类管理:
(一)一次性使用无菌医疗器械单独存放;
(二)三类医疗器械分开存放;
(三)整零分开存放;
(四)有效期器械分开存放;
(五)精密器械分开存放。
(六)在库医疗器械均应实行色标管理。
其统一标准是:待验区、退货区为黄色;合格品区、发货区为绿色;不合格品区为红色。
医用材料类、一次性无菌类和其他有效期要求的产品,应设置效期产品区(蓝色),效期产品应集中存放,并有效期预警机制。
