醇与无机酸
无机酸的酯化反应

无机酸的酯化反应-概述说明以及解释1.引言1.1 概述概述:无机酸酯化反应是一种重要的有机合成方法,通过无机酸与醇发生酯化反应,生成酯化合物。
这种反应在化学工业中具有广泛的应用,可用于制备化学品、药物、香料等化合物。
无机酸酯化反应的原理简单,操作方便,且产率高,因此受到广泛关注。
本文将重点探讨无机酸酯化反应的机理和应用前景。
1.2 文章结构文章结构部分将会对本文的整体框架进行介绍,提供读者对全文内容的整体把握。
首先会简要介绍文章的组织结构,包括引言、正文和结论部分的内容安排。
然后会对每个部分的内容进行概要描述,指导读者了解每个部分所涵盖的主题和重点。
最后,会强调本文将围绕无机酸的酯化反应展开讨论,引导读者在阅读全文时抓住重点,深入理解无机酸酯化反应的原理和机制。
1.3 目的2.正文2.1 无机酸的定义无机酸是指不含碳-碳键的酸,主要由非金属元素或含有氧、硫、氮等元素的有机物组成。
与有机酸不同,无机酸通常具有强酸性和高腐蚀性。
这些无机酸包括硫酸、氯化氢、硝酸等,它们在化学反应中起着重要作用。
无机酸通常是通过离子化反应来释放氢离子,这些氢离子在溶液中可形成酸性溶液。
无机酸的酸性强度取决于其分子结构和溶液中的浓度,一般来说,含有更多氧元素的无机酸具有更强的酸性。
在化学领域,无机酸不仅被用作实验室试剂,还广泛应用于工业生产和其他领域。
无机酸的性质和特点使其在许多化学反应和工艺中扮演重要角色,如催化剂、脱水剂、中和剂等。
总的来说,无机酸的定义是指不含碳-碳键的酸,具有强酸性和高腐蚀性,在化学领域有着广泛的应用和重要性。
在下文中我们将探讨无机酸参与的酯化反应及其机制。
2.2 酯化反应的原理酯化反应是一种重要的有机合成反应,通过酸催化或酶催化,将醇和酸酐或无机酸在合适条件下反应,生成酯和水。
酯化反应的原理是醇与酸酐或无机酸之间发生亲核加成反应,醇中的羟基(-OH)与酸酐或无机酸中的羧基(-COOH)发生酯键形成,同时生成水分子。
有机化学—醇的合成

有机化学——醇的合成前言有机化学主要是介绍化学物质的科学。
目前有机化学物质的分类主要是按照其决定性作用,能代表化学物质的基团也就是官能团的不同来进行分类的。
可分为:烷烃,烯烃,炔烃,芳香烃(以上为烃类);卤代烃,醇,酚,醚,醛,酮,羧酸,羧酸衍生物,胺类,硝基化合物,腈类,含硫有机化合物(如硫醇,硫醚,硫酚,磺酸,砜与亚砜等),含磷有机化合物等元素有机化合物,杂环化合物等。
具体主要是介绍这些化学物质的系统命名,化学反应,反应机理,制备方法。
其中化学反应基本上为基团的取代,能否进行一个反应,取决于热力学和动力学两个方面的因素。
而制备方法主要是通过无机物,石油提取物,以及容易制备或成本低的物质制得难以得到的物质。
反应机理也为基团之间的进攻和离去倾向之间的竞争。
有机合成方面主要研究比较简单的化合物或元素经化学反应合成有机化合物。
19世纪30年代合成了尿素;40年代合成了乙酸。
随后陆续合成了葡萄糖酸、柠檬酸、琥珀酸、苹果酸等一系列有机酸;19世纪后半叶合成了多种染料;20世纪40年代合成了DDT和有机磷杀虫剂、有机硫杀菌剂、除草剂等农药;20世纪初,合成了606药剂,30~40年代,合成了一千多种磺胺类化合物,其中有些可用作药物。
醇醇是脂肪烃分子中的氢原子或芳香烃侧链上的氢原子被羟基所取代后的化合物,羟基(—OH)是醇的官能团。
一、醇的分类、命名和结构(1)醇的分类根据醇分子中所含羟基的数目,可以分为一元醇、二元醇及三元醇等,同时二元醇以上的醇称为多元醇;在一元醇分子中,根据羟基所连接的碳原子的不同级数,可分为一级醇(伯醇)、二级醇(仲醇)和三级醇(叔醇);根据醇分子中烃基的类别,又可分为脂肪醇、脂环醇,或饱和醇、不饱和醇。
伯醇(RCH2OH): CH3CH2OH仲醇(R2CHOH):(CH3)2CHOH叔醇(R3 COH): (CH3)3C-OH注:羟基和碳碳双键直接相连的醇叫烯醇。
在一般情况下,烯醇式互变—烯醇是不稳定,容易互变成为比较稳定的醛或酮。
酯化法

酯化法:是利用酸和醇的酯化反应,向浓度范围在10%到30%之间的醋酸水溶液中加入醇,在无机酸的催化下发生酯化反应。
从而达到生成酯并分离醋酸的目的,酯与水的沸点相差较大,所以可以采用普通精馏方法将生成的酯分离,然后水解可得到醋酸和醇。
案例1:张章福等就利用醋酸和乙醇的酯化反应,以含醋酸的废水生产醋酸乙酯。
开发出了一套新工艺,小试成功后,在椒江市光明化工厂实现了该工艺的工业化。
生产出来的醋酸乙酯达到了工业级的标准,并收到了良好的经济效益。
案例2:辽宁石油化工大学石油化工学院刘春生等采用酯化法,以十二烷基磺酸铁为催化剂使异辛醇与醋酸反应,对质量分数为6%的低含量醋酸水溶液的处理进行了研究。
考察了反应时间、催化剂质量、醇酸摩尔比等因素对醋酸转化率的影响。
结果表明,当质量分数为6%的醋酸溶液为100mL 时,醇酸摩尔比为3∶1,十二烷基磺酸铁质量为0.6g,99℃下反应6h 后醋酸转化率达68.6%。
不仅有效地降低了溶液中的醋酸含量,产物乙酸异辛酯还是重要的化工产品,具有环保和经济双重价值。
此法具有催化剂用量少、不水解、反应条件温和、速度快、转化率高、无污染等优点,操作简单安全,有着良好的实用前景。
络合萃取法:案例:大庆石油化工总厂采用萃取—蒸馏和萃取—反萃取工艺选择了 N235 与磷酸三丁酯混合萃取剂回收大庆石油化工总厂废水中的醋酸,回收率达到 90%以上,并且大大的降低了废水的 COD 。
以叔胺为络合剂的三元混合萃取剂实验了脉冲筛板塔萃取分离醋酸稀溶液过程,并对萃取剂的再生和回收做了详细的研究,结果表明该萃取剂具有良好的稳定性,可以多次循环使用。
合成醋酸盐法合成醋酸盐法是通过对浓醋酸废水或稀醋酸废水经过浓缩后,加入一些化合物,经过反应而生成醋酸盐。
直接用含醋酸质量分数为 30%~40%废醋酸液与质量分数在 98%以上的纯碱为原料合成能广泛运用于化工行业和医药行业中的三水醋酸钠。
该法进行了工业化试验取得了满意效果,得到的醋酸纳产品符合国家标准。
醇化学性质

CH3CH2CHCH3 OH
60%H2SO4 , 95℃
2012-4-25
7
(2)分子间脱水 )
醇与80%浓H2SO4或Al2O3共热,可分子间脱水生成醚
2CH3CH2OH
浓 2SO4 , 140 H ℃ 或 2O3 , 240℃ Al
CH3CH2OCH2CH3 + H 2O
•影响脱水类型的因素
——温度和酸度:较高温度和酸的浓度利于分子内脱水(消除反 应);过量的醇,较低温度利于分子间脱水(亲核取代反应) ——醇本身的结构:仲醇易分子内脱水生成烯烃;叔醇只能得到 烯烃;只有伯醇与路易斯酸共热才能得到醚
2012-4-25
HOCH2CH2O(CH2CH2O)nCH2CH2OH (聚乙二醇)
16
•应用
——高沸点溶剂,防冻剂(含40%(体积)的乙二醇水溶液冰点 为-25℃,60%时,为-49℃ ) ——合成聚酯纤维涤纶、乙二醇硝酸酯炸药的原料 ——聚乙二醇醚类RO-[CH2CH2O-]nH是非离子表面活性剂 ——一缩二乙二醇二丙烯酸酯或三缩三乙二醇二丙烯酸酯是UV固 化的活性稀释单体(但有毒性,现已基本不用) CH2=CH-CO-O-CH2CH2OCH2CH2O-CO-CH=CH2
•说明
醇分子内脱水,主要按E1机理进行,由于碳正离子的生成,易发 2012-4-25 8 生分子重排;用Al2O3脱水,不发生重排
4. 酯的生成
醇与含氧无机酸或有机酸反应,生成酯。
•醇与含氧无机酸(硫酸、硝酸、磷酸)反应生成无机酸酯:
CH3OH + HO SO 2 OH CH3OSO2OH + H OCH CH3OSO2OH + H 2O 硫硫硫硫硫(硫酸硫硫硫硫) CH3OSO2OCH3 硫硫硫硫硫(中酸硫硫硫硫)
有机化学名词解释

有机化学名词解释一、化合物类名无机酸酯:醇与含氧无机酸反应失去一分子水后的生成物称为无机酸酯。
双烯烃:碳碳双键数目最少的多烯烃是二烯烃或称双烯烃。
可分为三类:两个双与同一碳原子结合的二烯烃称为累积二烯烃,其两个双键被两个或多个单键分开的二烯烃称为孤立二烯烃,其两个双键被一个单键分开的二烯烃称为共轭二烯烃。
内酯:分子中羧基和羟基脱水形成的产物称为内酯。
内酰胺:分子内的羧基和胺(氨)基失水的产物称为内酰胺。
季铵盐:季铵盐在强碱(KOH、NaOH)作用下的产物称为季铵盐。
生物碱:从植物体内提取的一类含氮有机化合物,具有强烈的生理作用。
绝大多数游离生物碱为固体,不溶于水,易溶于乙醇等有机溶剂。
大多数天然生物碱是左旋的手性化合物。
半缩醛或半缩酮:醇具有亲核性,在酸性催化剂如对甲苯磺酸、氯化氢的作用下,很容易和醛酮发生亲核加成,一分子醛或酮和一分子醇加成的生成物称为半缩醛或半缩酮。
有机化合物:除一氧化碳、二氧化碳、碳酸盐等少数简单含碳化合物以外的含碳化合物。
多肽:一个氨基酸的羧基与另一分子氨基酸的氨基通过失水反应,形成一个酰氨键,新生成的化合物称为肽,肽分子中的酰氨键叫做肽键。
二分子氨基酸失水形成的肽叫二肽,多个氨基酸失水形成的肽叫多肽。
杂环化合物:在有机化学中,将非碳原子统称为杂原子,最常见的杂原子是氮原子、硫原子和氧原子。
环上含有杂原子的有机物称为杂环化合物。
分为两类,具有脂肪族性质特征的称为脂杂环化合物,具有芳香特性的称为芳杂环化合物。
因为前者常常与脂肪族化合物合在一起学习,所以平时说的杂环化合物实际指的是芳杂环化合物。
杂环化合物是数目最庞大的一类有机物。
多环烷烃:含有两个或多个环的环烷烃称为多环烷烃。
共轭烯烃:单键和双键交替的体系称为共轭体系,含有共轭体系的聚烯烃称为共轭烯烃。
纤维二糖:是由两分子葡萄糖通过1,4两位上的羟基失水而来的,纤维二糖是b-糖苷。
纤维素:由多个纤维二糖聚合而成的大分子。
多稀烃:含有多于一个碳碳双键的烯烃称为多稀烃。
醇的集锦

醇羟基中氢的反应由于醇羟基中的氢具有一定的活性,因此醇可以和金属钠反应,氢氧键断裂,形成醇钠(CH3CH2ONa)和放出氢气。
由于在液相中,水的酸性比醇强,所以醇与金属钠的反应没有水和金属钠的反应强烈。
若将醇钠放入水中,醇钠会全部水解,生成醇和氢氧化钠。
虽然如此,在工业上制甲醇钠或乙醇钠还是用醇与氢氧化钠反应,然后设法把水除去,使平衡有利于醇钠一方。
常用的方法是利用形成共沸混合物将水带走转移平衡。
所沸共合物是指几种沸点不同而又完全互溶的液体混合物,由于分子间的作用力,它们在蒸馏过程中因气相和液相组成相同而不能分开,得到具最低沸点(比所有组分沸点都低)或最高沸点(比所有组分沸点都高)的馏出物。
这些馏出物的组成与溶液的组成相同,直到蒸完沸点一直恒定,如乙醇一苯一水组成三元共沸混合物,其沸点为64.9℃(乙醇18. 5%,苯74%,水7.5%),苯一乙醇组成二元共沸混合物,其沸点为68.3℃(乙醇32.4%,苯67. 6%)。
由于乙醇一水形成共沸混合物,其沸点为78℃(乙醇95. 57%,水4. 43%),所以乙醇中含有少量的水不能通过蒸馏方法除去,可计算加入比形成乙醇苯一水三元共沸混合物稍过量的苯,先将水除去,然后过量苯与乙醇形成二元共沸混合物除去,剩下为无水乙醇。
醇钠的醇溶液,可通过上述去水方法得到。
醇钠及其类似物在有机合成中是一类重要的试剂,并常作为碱使用。
[2]醇与含氧无机酸的反应醇与含氧无机酸反应失去一分子水,生成无机酸酯。
醇与硝酸的反应过程如下:醇分子作为亲核试剂进攻酸或其衍生物的带正电荷部分,氮氧双键打开,而后醇分子的氢氧键断裂,硝酸部分失去一分子水重新形成氮氧双键。
该类反应主要用于无机酸一级醇酯的制备。
无机酸三级醇酯的制备不宜用此法,因为三级醇与无机酸反应时易发生消除反应。
醇与含氧无机酸的酰氯和酸酐反应,也能生成无机酸酯。
含氧无机酸酯有许多用途。
乙二醇二硝酸酯和甘油三硝酸酯(俗称硝化甘油)都是烈性炸药。
醇与无机酸或有机酸的酯化反应原理

醇与无机酸或有机酸的酯化反应原理
[日期:2008-04-03] 来源:桂林中学校园网作者:录入员[字体:大中小] 醇与酸(无机酸或有机酸)作用生成酯和水的反应,称为酯化反应。
酯化和水解是一个可逆平衡:
酯化和水解这两个反应看来很简单,但其反应机理却比较复杂。
在不同的反应物和反应条件下,便可能有不同的反应机理。
这里举例加以说明。
酯化反应为酸性催化反应,酯化速率跟醇和酸的结构类型有关,并与它们的浓度成正比。
酯化反应的化学方程式可表示如下:
醇和无机酸作用时,无机酸分子中的氢原子与醇分子中的羟基生成水并缩合成无机酸酯。
多元酸分子中所有的氢原子都被烃基取代时,则生成中性酯;如果一部分氢原子被取代时则生成酸性酯。
当醇和有机酸作用时,一般地讲,在形成酯的过程中,是羧酸分子中的羟基与醇羟基中的氢原子结合成水;其余的部分缩合成酯。
这里的羧酸是指普通的有机羧酸,而醇为伯醇或仲醇。
因为叔醇很容易在分子内脱水,一般制备第三醇的酯不直接用醇和酸进行酯化,而是用一些其它方法制备的。
酸性催化酯化反应,经反应机理的研究,已知一般是酰-氧键断裂的双分子酯化作用,酸催化的作用首先是使羧基中的羰基上的氧原子接受质子,使羰基碳原子正电荷增加,然后是亲核试剂(如ROH)进攻羰基碳原子形成过渡状态,发生羧酸的酰-氧键断裂而脱去一分子水,最后释放出一个质子而生成酯,它们的反应历程可以表示如下:
醇分子中的氧原子最后保留在酯的分子中。
这样的反应历程,也可根据下列实验进行推断。
用含同位素18O的甲醇和羧酸进行酯化,如按酰-氧键分裂的方式进行,则所得的酯应含有18O,事实上实验证明也是这样:
第 1 页共 1 页。
有机化学—醇的合成

有机化学——醇的合成前言有机化学主要是介绍化学物质的科学。
目前有机化学物质的分类主要是按照其决定性作用,能代表化学物质的基团也就是官能团的不同来进行分类的。
可分为:烷烃,烯烃,炔烃,芳香烃(以上为烃类);卤代烃,醇,酚,醚,醛,酮,羧酸,羧酸衍生物,胺类,硝基化合物,腈类,含硫有机化合物(如硫醇,硫醚,硫酚,磺酸,砜与亚砜等),含磷有机化合物等元素有机化合物,杂环化合物等。
具体主要是介绍这些化学物质的系统命名,化学反应,反应机理,制备方法。
其中化学反应基本上为基团的取代,能否进行一个反应,取决于热力学和动力学两个方面的因素。
而制备方法主要是通过无机物,石油提取物,以及容易制备或成本低的物质制得难以得到的物质。
反应机理也为基团之间的进攻和离去倾向之间的竞争。
有机合成方面主要研究比较简单的化合物或元素经化学反应合成有机化合物。
19世纪30年代合成了尿素;40年代合成了乙酸。
随后陆续合成了葡萄糖酸、柠檬酸、琥珀酸、苹果酸等一系列有机酸;19世纪后半叶合成了多种染料;20世纪40年代合成了DDT和有机磷杀虫剂、有机硫杀菌剂、除草剂等农药;20世纪初,合成了606药剂,30~40年代,合成了一千多种磺胺类化合物,其中有些可用作药物。
醇醇是脂肪烃分子中的氢原子或芳香烃侧链上的氢原子被羟基所取代后的化合物,羟基(—OH)是醇的官能团。
一、醇的分类、命名和结构(1)醇的分类根据醇分子中所含羟基的数目,可以分为一元醇、二元醇及三元醇等,同时二元醇以上的醇称为多元醇;在一元醇分子中,根据羟基所连接的碳原子的不同级数,可分为一级醇(伯醇)、二级醇(仲醇)和三级醇(叔醇);根据醇分子中烃基的类别,又可分为脂肪醇、脂环醇,或饱和醇、不饱和醇。
伯醇(RCH2OH): CH3CH2OH仲醇(R2CHOH):(CH3)2CHOH叔醇(R3 COH): (CH3)3C-OH注:羟基和碳碳双键直接相连的醇叫烯醇。
在一般情况下,烯醇式互变—烯醇是不稳定,容易互变成为比较稳定的醛或酮。
乙醇氧化反应

乙醇氧化反应一、乙醇氧化反应(alcoholic metabolism)Ethanol Oxidation)又称乙醇发酵生成乙醛的反应。
酒精和乙醛都是人体所需的营养物质。
酒精氧化时要消耗葡萄糖,从而产生热量,是酒精发酵成为乙醇的过程,也是葡萄糖被氧化分解成二氧化碳和水的过程。
二、氧化反应中的氧化剂:与乙醇氧化反应的氧化剂有氯酸钾、高锰酸钾、硫酸铜、铁粉、碘、空气等。
其中,以氯酸钾使用最广,操作也较方便,但作为氧化剂存在一些缺点:价格贵;不稳定,见光易分解,对热不稳定,受热易失效;D-在潮湿空气中能被缓慢氧化成为醋酸;C-对水蒸气不太稳定,可被碱类如NaOH除去;C-可被浓硝酸氧化,可被浓盐酸氧化;因此,实际操作中常用KMnO3、 FeCl2、KMnO4、 Na2CO3、 AgCl、 CuCl2、 ZrO2、 Cl2等。
三、乙醇氧化机理: 1。
1。
乙醇氧化过程包括醇羟基的开环和氧化两个步骤。
一般来说,醇羟基比醛羟基容易开环,氧化也相对容易进行。
开环反应主要发生在内酯环上,故内酯是乙醇氧化的主要生成物。
2。
氧化反应是放热反应,并伴随有水生成。
一般来说,在反应开始时,醇羟基容易获得电子,容易开环,因而产物是一元醇。
在氧化剂存在下,醇羟基获得电子的能力大于氧化剂夺去电子的能力,氧化剂的作用大于醇羟基脱氢的作用。
因此,当氧化剂的浓度相同时,乙醇氧化的速率很大程度上取决于氧化剂的浓度。
乙醇氧化后,分子间形成了碳-碳双键,因而使分子的极性增强。
3。
氧化产物中存在着各种醛、酮、酸等有机物。
其中最重要的醛有:乙酸、草酸、蚁酸、醋酸等。
其他主要的醛类有:甲酸、丙酸、丁酸等。
四、影响乙醇氧化的因素: 1。
温度升高,氧化速率加快。
温度升高到一定程度,羟基结构中的氢原子之间的距离逐渐减小,这将会导致分子运动能力减弱,反应速度逐渐降低。
一般情况下,液相中反应速度约为固相的10倍左右。
2。
酸度提高,氧化速率加快。
随着酸度的提高,羧基离解能力加强,氧化速率加快。
酯化反应

酯化反应的原理及其相关实验酯化反应,是一类有机化学反应,是醇跟羧酸或含氧无机酸生成酯和水的反应。
分为羧酸跟醇反应和无机含氧酸跟醇反应何和无机强酸跟醇的反应两类。
羧酸跟醇的酯化反应是可逆的,并且一般反应极缓慢,故常用浓硫酸作催化剂。
多元羧酸跟醇反应,则可生成多种酯。
无机强酸跟醇的反应,其速度一般较快。
典型的酯化反应有乙醇和醋酸的反应,生成具有芳香气味的乙酸乙酯,是制造染料和医药的原料。
酯化反应广泛的应用于有机合成等领域。
一、基本简介醇跟羧酸或含氧无机酸生成酯和水,这种反应叫酯化反应。
分两种情况:羧酸跟醇反应和无机含氧酸跟醇反应。
羧酸跟醇的反应过程一般是:羧酸分子中的羟基与醇分子中羟基的氢原子结合成水,其余部分互相结合成酯。
这是曾用示踪原子证实过的。
口诀:酸去羟基醇去羟基氢(酸脱氢氧醇脱氢)。
酯的读法:R酸R1酯("R"是指R酸中的"R";"R1"是指R1醇中的"R1")羧酸跟醇的酯化反应是可逆的,并且一般反应极缓慢,故常用浓硫酸作催化剂。
多元羧酸跟醇反应,则可生成多种酯。
乙酸和乙醇在浓硫酸加热的条件下反应生成乙酸乙酯和水CH3COOH+C2H5OH---(可逆符号)CH3COOC2H5+H2O乙二酸跟甲醇可生乙二酸氢甲酯或乙二酸二甲酯HOOC—COOH+CH3OH→(可逆符号)HOOC—COOCH3+H2O无机强酸跟醇的反应,其速度一般较快,如浓硫酸跟乙醇在常温下即能反应生成硫酸氢乙酯。
C2H5OH+HOSO2OH→(可逆符号)C2H5OSO2OH+H2O硫酸氢乙酯C2H5OH+C2H5OSO2OH→(可逆符号)(C2H5O)2SO2+H2O硫酸二乙酯多元醇跟无机含氧强酸反应,也生成酯。
一般来说,除了酸和醇直接酯化外能发生酯化反应的物质还有以下三类:酰卤和醇、酚、醇钠发生酯化反应;酸酐和醇、酚、醇钠发生酯化反应;烯酮和醇、酚、醇钠发生酯化反应;酯如果在碱性条件下会水解成相应的醇和有机酸盐。
有机化学 第五版 第十三章答案

第十三章羧酸衍生物1.说明下列名词。
酯、油脂、皂化值、干性油、碘值、非离子型洗涤剂、阴离子型洗涤剂、不对称合成。
1. 解:醇与酸(含无机酸和有机酸)相互作用得到的失水产物叫做酯。
例如,乙醇和乙酸作用失去1分子水的产物是乙酸乙酯;乙醇和浓硫酸作用失去1分子水的产物是硫酸氢乙酯(C2H5OSO2OH)。
油脂是高级脂肪酸的甘油酯。
通常存在于自然界的动植物体内,而且,其中的脂肪酸通常是10个以上双数碳原子的混合酸。
1g 油脂完全皂化所需氢氧化钾的质量(单位mg)称为皂化值。
他是测定油脂中脂肪酸含量的1种参考数据。
具有在空气中很快变成1层干硬而有弹性膜特性的含有共轭双键脂肪酸的油脂称为干性油。
100g 油脂所能吸收碘的质量(单位g)称为碘值,它是决定油脂不饱和程度高低的重要指标。
与肥皂结构和作用相类似,但在水中不解离的1种中性非离子的分子状态或胶束状态的1类合成洗涤剂称为非离子型洗涤剂。
2.试用反应式表示下列化合物的合成路线。
(1)由氯丙烷合成丁酰胺;(2)由丁酰胺合成丙胺;(3)由邻氯苯酚、光气、甲胺合成农药“害扑威”ClOCONHCH3解:(1) CH3CH2CH2Mg/Et2O3CH2CH21) CO22+CH3CH2CH2CO2H1) NH33CH2CH2CONH2(2) CH3CH2CH2CONH NaOH/Br2CH3CH2CH2NH2ClOH +OClClClO C ClCH3NH2ClOCONHCH3(3) 路线1ClOH+O Cl ClCH 3NH ClOCONHCH 3路线2CNH 3C3.用简单的反应来区别下列各组化合物。
(1)CH 3CH(Cl)COOH 和CH 3CH 2COCl(2) 丙酸乙酯和丙酰胺 (3)CH 3COOC 2H 5和CH 3CH 2COCl (4)CH 3COONH 4和CH 3CONH 2 (5) (CH 3CO)2O 和CH 3COOC 2H 5解:CH 3CH 2COClC H 3无白色沉淀(白)(1)CH 3CH 2CONH 2C H 3CH 2COOCH 2CH 2CH无NH 3(2)NH3CH 3CH 2COCl CH 3COOC 2H(3)无白色沉淀(白)CH3COONH 4CH 3CONH2(4)NH 3无NH 3(CH 3CO)2OCH 3COOC 2H5(5)CO 2无CO 24. 由CH 2合成CH 2CN。
醇

(2)分子间脱水生成醚
按照SN2历程进行,与分子内脱水形成竞争。
反应实质:
C-O 键断裂,一分子醇的 –OH 被另一 分子醇的 –OR 所取代(亲核取代)。
1.你知道如何检验酒精中是否含水吗?还有,如何除去酒
精中的水分呢? 分析:无水CuSO4遇水后生成CuSO4· 2O,颜色由白色 5H 变成蓝色,可用于水的检验;由于乙醇和水能形成恒沸
甲醇 乙二醇 丙三醇
多元醇 CH CH CH2 2
OH OH OH
3、按羟基所连碳原子的类型不同分为
一级醇(伯醇)
二级醇(仲醇) 三级醇(叔醇)
R CH2OH
R CH R' OH
R' R C R' ' OH
饱和一元醇的通式为CnH2n+1OH
二、醇的命名 1、习惯命名法 在烃基后面加一“醇”字
CH3 CH3CH2OH CH3CHOH CH3 CH3CCH3 OH
烯丙式醇 > 叔醇 > 仲醇 > 伯醇 > CH3OH
例如,醇与卢卡斯(Lucas)试剂(浓盐酸+无 水氯化锌)的反应:
卢卡斯( Lucas )试剂(无水ZnCl2与浓 HCl配制的溶液)鉴别六个碳以下的 伯、仲、叔醇(烯丙式醇) 现象
R3C-OH
烯丙式醇
R3C-Cl Lucas试剂 R2CHCl
医用酒精的成份主要 是乙醇。日常生活中,常 见一些人用医用酒精来擦 洗伤口,以达到灭菌消毒 的目的。值得注意的是, 在药店买到的酒精有75% 和95%两种浓度,这两种 浓度的酒精用途是不一样 的。
95%的酒精常用于擦拭紫外线灯。这种酒精在医 院常用,而在家庭中则只会将其用于相机镜头的清洁。
醇酚醛酮知识点总结

醇酚醛酮知识点总结一、醇的基本性质醇是一类含有羟基 (-OH) 的有机化合物,它们通常被视为烷烃分子的氢原子部分被羟基取代而形成。
根据羟基数的不同,醇可以分为一元醇、二元醇、三元醇等。
醇的命名按照IUPAC命名法,首先确定主链的碳原子数和官能团的位置,然后在主链名称后加上“-ol”以表示它是一个醇类化合物。
醇具有以下基本性质:1. 醇的饱和脂肪链长度和取代位置对其溶解性有影响,短链醇易溶于水,而长链醇则不溶于水;2. 醇可以和一些无机酸(如HCl、H2SO4)发生酸碱中和反应,生成醇盐;3. 醇在适当条件下可以和醛、酮、酸、卤代烃等发生醚化反应,生成醚类化合物;4. 醇可以和氧化剂反应,发生氧化反应生成醛、酮等化合物。
二、酚的基本性质酚是一类含有苯环结构和羟基 (-OH) 的有机化合物,它们具有独特的芳香性质和化学反应性。
酚的命名通常按照苯环上的取代基和羟基的位置进行命名,并在名字后面加上“phenol”以表示它是一个酚类化合物。
酚具有以下基本性质:1. 酚类化合物通常具有较强的芳香气味,对空气中的氧气具有较强的吸引力;2. 酚具有一定的溶解性,小分子酚可溶于水,大分子酚则不溶于水;3. 酚可以和酸、碱反应,生成酚盐或酚醚;4. 酚在适当条件下可以和羧酸、醛、酮等发生等反应,生成酯类、醚类、醛类和酮类化合物。
三、醛的基本性质醛是一类含有羰基 (-CHO) 的有机化合物,它们是一类重要的有机合成中间体,也是许多生物活性分子的结构基础。
醛的命名按照IUPAC命名法,首先确定主链的碳原子数和官能团的位置,然后在主链名称后加上“-al”或“-aldehyde”以表示它是一个醛类化合物。
醛具有以下基本性质:1. 醛的羰基对亲电试剂具有较强的亲和性,容易发生加成反应;2. 醛可以和亲核试剂发生亲核加成反应,生成醇和酮等化合物;3. 醛可以和酶类催化剂发生还原反应,生成对应的醇;4. 醛可以和醇、酚、胺等发生缩合反应,生成醚类、酚类和胺类化合物。
无机酸催化下的醇类化合物的环化反应机理研究

无机酸催化下的醇类化合物的环化反应机理研究近年来,有机化学领域的研究取得了长足的进步,其中无机酸催化下的醇类化合物的环化反应机理研究备受关注。
醇类化合物的环化反应是一种重要的有机合成方法,能够合成具有特定结构和功能的化合物。
本文将探讨无机酸催化下醇类化合物环化反应的机理,并介绍相关的研究进展。
无机酸催化是一种常用的催化方法,其在醇类化合物环化反应中发挥着重要的作用。
在环化反应中,无机酸能够与醇类化合物中的氧原子发生作用,形成酸-碱对,从而促进反应的进行。
无机酸催化下的醇类环化反应机理主要包括质子转移、亲核攻击和分子内重排等步骤。
在质子转移步骤中,无机酸能够将醇类化合物中的氢原子转移给相邻的氧原子,形成质子化的醇类中间体。
这一步骤是环化反应的关键步骤之一,决定了反应的速率和产物的选择性。
研究表明,不同的无机酸对质子转移步骤的影响是不同的,一些强酸如硫酸和磷酸能够促进质子转移的进行,而一些弱酸如硼酸则会减缓该步骤的进行。
亲核攻击是环化反应中的另一个重要步骤。
在质子转移之后,质子化的醇类中间体会与亲核试剂发生反应,形成新的化学键。
亲核试剂可以是醇类化合物中的氧原子,也可以是其他的亲核基团。
研究发现,无机酸的催化作用可以提高亲核试剂的亲核性,从而促进亲核攻击的进行。
此外,无机酸还可以调节亲核试剂的选择性,使得反应生成特定的产物。
分子内重排是环化反应中的最后一个步骤。
在亲核攻击之后,产生的中间体会发生分子内的重排反应,形成最终的环化产物。
无机酸催化能够加速分子内重排的进行,降低反应的能垒,从而提高反应的速率。
研究发现,无机酸的酸性和催化剂的浓度对分子内重排的影响是显著的,一些强酸和高浓度的催化剂能够加速分子内重排的进行。
总结起来,无机酸催化下的醇类化合物环化反应机理是一个复杂而多样的过程。
质子转移、亲核攻击和分子内重排是环化反应中的关键步骤,无机酸通过调节这些步骤的进行来促进反应的进行。
未来的研究可以进一步探索无机酸催化下醇类化合物环化反应的机理,并寻找更高效、更选择性的催化剂。
大学有机化学------醇酚醚
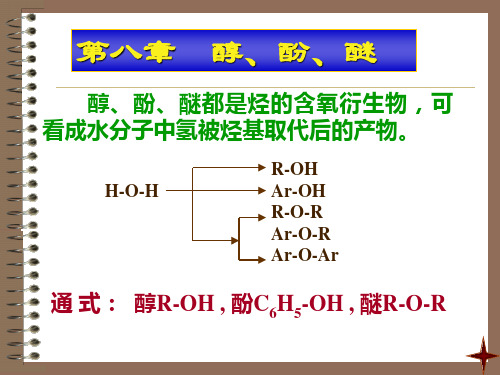
1、酸性
酸性强弱: 羧酸 > H2CO3 > 酚 > H2O > 醇
利用醇、酚与NaOH和NaHCO3反应性的不 同,可鉴别酚,分离和提纯酚。
OH + NaOH
CO2+ H2O
ONa
HCl
OH +
NaHCO3
OH + NaCl
OH + Na2CO3
X
苯环上连有吸电子基( -NO2,-X)使取代酚共 轭碱稳定性增大,酸性增强; 反之,斥电子基 (-R)使酸性减弱。
2、与FeCl3的显色反应
6ArOH + FeCl3
[ Fe(OAr)6 ] 3- + 6H+ + 3Cl -
蓝紫色 棕红色
用于定性分析,鉴别下列基团的存在:
几种常见酚与FeCl3的显色反应的颜色: 苯酚、间苯二酚:蓝紫色;对甲苯酚:蓝色; 邻苯二酚:深绿色;对苯二酚:暗绿色
3、芳环上的亲电取代反应(-OH活化苯环)
低级醇能和一些无机盐(MgCl2、CaCl2、CuSO4等) 作用形成结晶醇,亦称醇化物。
§1.5 化学性质
醇的化学性质主要由羟基官能团所决定,同
时也受到烃基的一定影响,从化学键来看,反
应的部位有 C—OH、O—H、和C—H。
H δδ δ RC O H
H
酸性,生成酯
氧化反应 形成 C ,发生取代及消除反应
CH3OSO2OCH3 CH3CH2OSO2OCH2CH3
有机合成中的烷基化剂,有剧毒
(2) 与有机酸反应
H
R-OH + CH3COOH
CH3COOR + H2O
5.氧化反应
醇

有机化学醇2-82010级化学1班李海波2011-12-01一、醇的分类、结构和物理性质1、醇的分类根据羟基所连接的碳原子的级分类,羟基连在一级碳原子上的醇称为一级醇,也称为伯醇;羟基连在二级碳原子上的醇称为二级醇,也称为仲醇;羟基连在三级碳原子上的醇称为三级醇,也称为叔醇。
羟基与不饱和碳原子相连的醇很不稳定,称为烯醇,它很快会异构化为醛、酮。
2、醇的熔点和沸点低级醇的熔点和沸点比碳原子数相同的碳氢化合物的熔点和沸点高的多,这是因为醇分子间有氢键缔合作用。
醇在固态时,缔合较为牢固,液态时,氢键断开后,还会再形成,但在气相或非极性溶剂的稀溶液中,醇分子彼此相距甚远,各个醇分子可以单独存在。
分子间氢键随着浓度的升高而增加,分子内氢键却不受浓度的影响。
3、醇的结构一般情况下,相邻的两个碳原子上最大的两个基团处于对交叉构象最稳定,是优势构象,担当这两个基团可能以氢键缔合时,由于形成氢键可以增加分子的稳定性。
两个分子处于临交叉构象成为优势构象。
二、醇的酸碱性醇的酸性和碱性与和氧相连的烃基的电子效应相关,烃基的吸电子能力越强,醇的碱性越弱,酸性越强。
相反,烃基的给电子能力越强,醇的碱性越强,酸性越弱。
烃基的空间位阻对醇的酸碱性也有影响,因此分析烃基的电子效应和空间位阻影响是十分重要的。
在气相下研究一系列醇的酸性次序,其排列情况如下:(CH3)3CCH2OH>(CH3)3COH> (CH3)2CHOH>CH3CH2OH>CH3OH>H2O,这说明烷基是吸电子的基团。
醇在气态时,分子处于隔离状态。
因此烷基吸电子反映了分子内在本质。
但是在液相中醇的酸性次序正好相反:CH 2OH>RCH 2OH>R 2CHOH>R 3COH ,只是因为在液相中有溶剂化作用,R 3CO -由于体积大,溶剂化作用小,负电荷不易被分散,稳定性较差,因此R 3COH 中的质子不易解离,酸性小。
无机酸与醇的酯化反应

无机酸与醇的酯化反应
在这个反应中,无机酸中的羧基(-COOH)与醇中的羟基(-OH)发生酯键的形成,生成酯和水。
这个反应通常在酸性条件下进行,
常用的酸催化剂包括硫酸、酚磺酸和氯化亚铁等。
酯化反应在工业上有着广泛的应用,其中最重要的应用之一是
生产酯类化合物。
酯类化合物在化工生产中被广泛应用,用作溶剂、香料、润滑剂等。
此外,酯化反应也在生物化学和医药领域有着重
要的应用,例如合成酯类药物和生物活性分子等。
除了工业应用外,酯化反应也在实验室中被广泛应用。
它常用
于有机合成实验中,用于合成酯类化合物,也是有机化学课程中的
重要实验之一。
总之,无机酸与醇的酯化反应是一种重要的有机化学反应,它
在工业生产和实验室研究中都有着广泛的应用。
通过这种反应,我
们可以合成各种酯类化合物,为化工生产和科学研究提供了重要的
手段和方法。
进行酯缩合反应的条件

进行酯缩合反应的条件
酯化反应的条件:酯化反应,是一类有机化学反应,是醇跟羧酸或含氧无机酸生成酯
和水的反应。
一般都是常温或者加热条件和加入催化剂。
酯化反应,是一类有机化学反应,是醇跟羧酸或含氧无机酸生成酯和水的反应。
分为羧酸跟醇反应和无机含氧酸跟醇反应和
无机强酸跟醇的反应三类。
酯化反应一般是可逆反应。
传统的酯化技术是用酸和醇在酸(常为浓硫酸)催化下加
热回流反应。
这个反应也称作费歇尔酯化反应。
浓硫酸的作用是催化剂和吸水剂,它可以
将羧酸的羰基质子化,增强羰基碳的亲电性,使反应速率加快;也可以除去反应的副产物水,提高酯的产率。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
(二)醇与无机酸的反应
1、与氢卤酸反应(取代反应)
【反应原理】醇与氢卤酸反应,醇中的
C—O键断裂,—OH被卤原子取代生成
卤代烃。
【反应方程式】乙醇和HCl(学生写)
【注意】 ①不同醇与氢卤酸的反应速率快慢 叔醇﹥仲醇﹥伯醇
②卢卡斯试剂:无水氯化锌的浓盐酸溶液
【解释】不同醇与卢卡斯试剂反应出现 浑浊的快慢不同而来区分伯、仲、叔醇。 叔醇立即出现浑浊 仲醇需十几分钟出现浑浊 伯醇需数小时才出现浑浊
心绞痛,但副作用大。
3、三硝酸甘油酯俗称硝酸甘油,能松弛平滑肌,
具有扩张冠状动脉、微血管作用,可用作心脏病的
急救药。
【课堂互动】
1、酯化反应是指(
2、三硝酸甘油酯俗称(
)。
),
能松弛(
(
),具有扩张(
)的作ห้องสมุดไป่ตู้,可用作(
)和
)病
的急救药。
3、完成下列反应
乙醇与盐酸反应 亚硝酸异戊酯的合成 三硝酸甘油酯的合成
【课堂互动】
用化学方法鉴别下列各组物质
正丁醇、仲丁醇和叔丁醇
2、与含氧无机酸的反应(硝酸、亚硝酸、硫酸)
【反应原理】 醇中—OH中的0—H键
断裂,酸提供—OH
【反应式】学生写
异戊醇和亚硝酸的反应 甘油和硝酸的反应
【注意】 1、酯化反应定义:酸与醇脱水生成酯和水的反应。 2、亚硝酸异戊酯作用:用作血管舒张药,可缓解
再 见
