小分子抗肿瘤蛋白激酶抑制剂的研究进展_图文(精)
蛋白酪氨酸激酶小分子抑制剂

状态影响激酶的活性。
蛋白质相互作用
02
与其他蛋白质的相互作用可以调节蛋白酪氨酸激酶的活性,影
响其磷酸化反应。
小分子抑制剂
03
小分子抑制剂是调节蛋白酪氨酸激酶活性的重要手段之一,通
过与激酶结合,抑制其活性。
03
蛋白酪氨酸激酶小分子抑制剂的设计
与发现
小分子抑制剂的设计策略
基于结构的药物设计
利用蛋白质三维结构信息,针对激酶活性位点或调节 位点设计小分子抑制剂。
小分子抑制剂还可以通过影响信号转导通路中其他蛋白质的活性,进一步调节信 号转导通路的输出。
05
蛋白酪氨酸激酶小分子抑制剂的药理
学特性与临床应用
小分子抑制剂的药代动力学特性
01
吸收
小分子抑制剂通常能快速通过胃肠 道吸收,进入血液循环。
代谢
小分子抑制剂在体内经过代谢,产 生药效。
03
02
分布
小分子抑制剂在体内广泛分布,能 快速到达靶组织。
排泄
小分子抑制剂主要通过肾脏排泄, 部分通过胆汁排泄。
04
小分子抑制剂的抗肿瘤活性与作用机制
抑制肿瘤细胞增殖
小分子抑制剂能抑制肿瘤细胞内的蛋白酪氨酸激酶活性,从而阻 止肿瘤细胞增殖。
诱导肿瘤细胞凋亡
小分子抑制剂能诱导肿瘤细胞凋亡,加速肿瘤细胞的死亡。
抑制肿瘤血管生成
小分子抑制剂能抑制肿瘤血管生成,切断肿瘤的营养供给,从而 抑制肿瘤的生长。
蛋白酪氨酸激酶小分子抑 制剂
• 引言 • 蛋白酪氨酸激酶的分类与结构 • 蛋白酪氨酸激酶小分子抑制剂的设计
与发现 • 蛋白酪氨酸激酶小分子抑制剂的作用
机制
• 蛋白酪氨酸激酶小分子抑制剂的药理 学特性与临床应用
小分子蛋白质相互作用抑制剂的设计合成及抗癌研究

小分子蛋白质相互作用抑制剂的设计合成及抗癌研究近年来,小分子蛋白质相互作用抑制剂(SMIs)已成为研究领域的热点。
其作用机制是通过抑制蛋白质与另一种分子的结合,从而达到治疗疾病的目的。
在癌症治疗方面,SMIs已经被广泛应用。
本文将探讨SMIs的设计合成及其在抗癌研究中的应用。
一、SMIs的设计SMIs的设计是一个复杂而有挑战性的过程。
首先,需要确定目标蛋白质的结构和功能。
接着,需要预测与目标蛋白质相互作用的分子。
最后,需要模拟SMIs 与目标蛋白质的相互作用。
一种常见的SMIs设计策略是“生物素类似物系统”,其中SMIs被合成成与生物素类似的分子,以便与目标蛋白质结合。
这种方法的优势在于,生物素与其受体之间的结合方式已经非常清楚,并且可以被用来指导SMIs的设计。
另一种SMIs设计策略是使用“荧光标记法”。
该方法通常用于研究蛋白质与其底物之间的相互作用,通过共价地将SMIs与荧光化合物标记起来,从而实现对SMIs的研究。
二、SMIs的合成经过设计,接下来需要合成SMIs。
SMIs的合成需要考虑物质的理化性质,包括溶解度、热稳定性和化学稳定性等。
同时,还需要在合成中考虑成本和效率等因素。
SMIs的合成通常是基于有机化学反应。
有机化学反应可以通过改变分子中的原子或化学键的结构来产生想要的效果。
因此,有机化学反应可以被应用于SMIs 的合成。
适量的试剂和反应条件是关键因素。
通常使用金属催化剂作为SMIs的合成催化剂,例如钯(Pd)催化的Suzuki偶合反应。
在SMIs的生产过程中,催化剂的选择和使用对于反应物和中间体的组成和构造有很大影响。
三、抗癌研究中的SMIs应用抗癌研究中,SMIs可以被用来阻止肿瘤细胞增殖。
SMIs的作用机制是通过干扰细胞信号传递,从而抑制肿瘤细胞的生长。
SMIs的种类非常多,包括针对蛋白酶、激酶和转录因子等的SMIs。
SMIs的抗肿瘤作用机理是通过特定靶点抑制细胞增殖,从而使得病变细胞难以存活和繁殖。
小分子蛋白酪氨酸激酶抑制剂的研究进展_张磊
制药联合研发的一种口服靶向抗肿瘤药,能抑制 多种受体酪氨酸激酶活性。体外实验表明,索拉 非尼能够抑制 Raf-1、VGFR-2 和 VGFR-3 的活性, IC50 分别为 6、90 和 20 nmol / L。索拉非尼是第一 个对 RAF 激酶和血管内皮生长因子受体( VEGFR) 激酶同时具有抑制作用的靶向抗肿瘤药,既 可通过阻断由 RAF / MEK / ERK 介导的细胞信号 传导通路而直接抑制肿瘤细胞的增殖,还可通过 作用于 VEGFR 达到抑制新生血管的形成和切断 肿瘤细胞的营养供应而达到遏制肿瘤生长的目 的。临床研究表明: 索拉非尼能够显著延长肾癌 等患者无进展生存期,其主要不良反应为恶心、腹 泻、皮疹及高血压等。自 2005 年起,FDA 已批准 索拉非尼用于治疗晚期肾癌、肝癌和甲状腺癌。
适应症 慢性髓性白血病,胃肠道间质肿瘤 非小细胞肺癌 肾细胞癌,肝癌,甲状腺癌 非小细胞性肺癌 胃肠道基质肿瘤,肾细胞癌 慢性粒细胞性白血病,急性髓性白血病 慢性髓性白血病 乳腺癌 晚期肾细胞癌,晚期软组织肉瘤 非小细胞肺癌 甲状腺髓样性髓细胞性白血病 甲状腺髓样癌 慢性粒细胞白血病,急性淋巴细胞白血病 转移性结肠癌 非小细胞肺癌 BRAF 突变的黑色素瘤 BRAF 突变的黑色素瘤 套细胞淋巴瘤,慢性淋巴细胞白血病
瑞戈非尼 ( Regorafenib) [11]是 由 拜 耳 研 发 的 一个口服有效的靶向肿瘤药物,是在索拉非尼结 构基础上改 造 而 来 的,又 被 称 为“多 吉 美 之 子 ”, 其对多种酪氨酸激酶均具有抑制作用( VEGFR1 / 2 /3、PDGFRβ 和 Kit 的 IC50 分别为 13 /4. 2 /46、22 和 7 nmol / L) 。Ⅲ期临床试验中,瑞戈非尼能够 显著改善对伊马替尼和舒尼替尼产生耐药的胃肠 道间质瘤患者的无进展生存期,常见的不良反应
激酶抑制剂在肿瘤治疗中的应用研究

激酶抑制剂在肿瘤治疗中的应用研究随着现代医学技术的不断发展,肿瘤治疗的方法越来越多样化和个性化。
其中,激酶抑制剂技术在肿瘤治疗中的应用引起了广泛关注。
本文将探究激酶抑制剂在肿瘤治疗中的应用研究。
一、激酶抑制剂生物学原理激酶抑制剂是一类能够抑制酶活性的小分子化合物,通过破坏蛋白质酶体系的关键酶活性,从而起到抑制细胞增殖和分裂的作用。
激酶抑制剂被广泛用于治疗很多疾病,特别是肿瘤治疗。
激酶抑制剂更多的是针对特定的激酶,如抑制肝细胞生长因子受体(EGFR)、血小板源性生长因子受体(PDGFR)等,进而阻碍癌细胞的刺激和增殖。
二、激酶抑制剂在肿瘤治疗中的应用(一) EGFR激酶抑制剂人表皮生长因子受体(EGFR)是肿瘤细胞增殖、转移和预后的重要分子靶标。
EGFR激酶抑制剂如培唑帕尼(gefitinib)和厄洛替尼(erlotinib),已被广泛应用于非小细胞肺癌的治疗。
这些药物口服后可抑制EGFR自身酶活性,从而阻止EGFR在癌细胞生长和转移过程中的作用。
因此,EGFR激酶抑制剂已成为一种广泛使用的治疗药物。
(二) PDGFR激酶抑制剂PDGF是一种细胞增殖和迁移的强烈刺激因子,为多种恶性肿瘤的发生和转移贡献了重要因素。
针对PDGFR的激酶抑制剂如伊马替尼(imatinib),已广泛应用于治疗皮肤型软组织肉瘤、胃肠瘤和慢性骨髓性白血病等恶性肿瘤。
(三) mTOR激酶抑制剂哺乳动物雷帕霉素靶蛋白(mTOR)是一种蛋白质激酶,存在于哺乳动物细胞的外涵体中。
mTOR是一种重要的信号转导通路,参与了细胞的增殖、生长和其它许多生命活动。
否定的作用也是负责细胞凋亡的。
目前,mTOR激酶抑制剂如依维莫司(everolimus)已被广泛使用于胰腺神经内分泌瘤、肾脏癌等肿瘤治疗中。
三、激酶抑制剂药物的副作用尽管激酶抑制剂的应用是极其广泛的,但其使用也有其独特的难点。
激酶抑制剂在肿瘤治疗中,药物用量是非常严格的。
如果剂量过大会导致严重的中毒反应,如过度抑制细胞增殖和免疫功能、引起毒性肝损伤等。
小分子EGFR-TKIs在非小细胞肺癌治疗中的研究进展

小分子EGFR-TKIs在非小细胞肺癌治疗中的研究进展
胡亚南
【期刊名称】《药物资讯》
【年(卷),期】2024(13)1
【摘要】小分子表皮生长因子受体酪氨酸激酶抑制剂(epithelial growth factor receptor tyrosine kinase in-hibitor, EGFR-TKI)在治疗伴有EGFR突变的非小细胞肺癌(non-small cell lung cancer, NSCLC)中获得了巨大的临床收益。
但患者经过一段时间EGFR-TKIs治疗,不可避免的出现获得性耐药。
本文主要对小分子EGFR-TKIs在NSCLC治疗中的研究进展及进行综述,为该类药物的临床使用及未来的研究方向提供参考。
【总页数】9页(P1-9)
【作者】胡亚南
【作者单位】南京知和医药科技有限公司南京
【正文语种】中文
【中图分类】R73
【相关文献】
1.小分子化合物(EGFR-TKI)治疗非小细胞肺癌疾病进展后停药与继续原药维持的30例观察
2.非小细胞肺癌小分子化合物(EGFR-TKI)靶向治疗疾病进展后与化疗交替治疗的临床治疗效果分析
3.放疗同步EGFR-TKI治疗与先放疗后EGFR-TKI治疗在EGFR基因突变型非小细胞肺癌脑转移中的应用效果对比
4.EGFR-TKIs与二甲双胍联合治疗在非小细胞肺癌EGFR-TKIs获得性耐药中的研究进展
因版权原因,仅展示原文概要,查看原文内容请购买。
小分子Bcr-Abl激酶抑制剂在Ph +白血病中的研究进展

Zhou Ying—hong,M iao Hong and W ang Xiao—ning (Strategy and planning department,Central Research Institute ofShanghai Pharmaceutical Group Co.Ltd.,Shanghai 201203)
Abstract Bcr-Ablfbreakpoint cluster region—Abelson)is an abnormal fusion protein which is closely related with Ph(Philadelphia chromosome)positive leukemia.As one of the world’s top ten malignant tumors.1eukemia
列 , 白血 病 在 恶 性:肿 瘤 中位 居 第 6位 (男 性 )和 第 8位 基 因 的编 码 产物 为Bcr—Abl融合 蛋 白 。根 据 BCR断裂
(女 性 ),在 儿 童 及 ,;5岁 以下成 人 中则 居 第l位 。CML 位 点 的不 同, BCR.ABL融 合 基 因主 要 有 3种 , 分别
关键 词 : Bcr-Abl;Pl1t白血 病 ;T3151耐 药株 中图分类号:R979.1+4 文献标识码: A
Research progress of sm all m olecular Bcr-Abl inhibitors f0r the treatm ent of Ph leukem ia
收 稿 日期 :2010—06—03 作者简介 :周映 红 ,女 ,生于1982年,研究员 ,主要从事抗肿瘤及糖尿病药物 的研发 。E-mail:zhouyh@pharm.sh. tom .cn
蛋白激酶小分子抑制剂

蛋白激酶主要分为两大类,即丝氨酸/苏氨酸激酶和酪氨酸激酶。蛋白激酶也可以分为7类,即AGC激酶类,包括PKA、PKC和PKG;CAM激酶类包括钙调蛋白酶;CK1类,包括酪蛋白1;CMGC类,包括CDK、MAPK、GSK3和CLK;STE类; TK酪氨酸激酶类;TKL类。
截至2017-12-31,FDA总共批准了38个小分子激酶抑制剂类药物,其中多数为酪氨酸激酶抑制剂,其它属于丝氨酸/苏氨酸激酶抑制剂和少数脂激酶类抑制剂。
2,FDA批准的可逆非受体型酪氨酸小分子激酶抑制剂
注:CMML, chronic myelomonocytic leukemia (慢性粒单核细胞白血病); HES, hypereosinophilic syndrome (高嗜酸性粒细胞综合征); GIST, gastrointestinal stromal tumors (胃肠道间质瘤); PV, Polionyelitis(脊髓灰质炎); RA,rheumatoid arthritis(类风湿性关节炎)。
二、FDA批准的丝氨酸/苏氨酸小分子激酶抑制剂
三、FDA批准的脂激酶小分子抑制剂
注:ALK, anaplasticlymphoma kinase (间变性淋巴瘤激酶)。
FDA批准的可逆受体型酪氨酸小分子激酶抑制剂-其它
注:BC, breast cancer; RCC, renal cell carcinoma (肾细胞癌); MTC, Medullary Thyroid Carcinoma (甲状腺髓样癌);CRC, colorectal cancer(结直肠癌)。
一、FDA批准的酪氨酸小分子激酶抑制剂
1,FDA批准的不可逆小分子激酶抑制剂分子名来自商品名公司主要靶点
小分子抑制剂成为研究的前沿热点

小分子抑制剂成为研究的前沿热点
以蛋白激酶为靶标的分子靶向抗肿瘤药物由于重点针对肿瘤发生发展机制中的关键酶或蛋白,具有选择性好、安全性较高等优点,基于蛋白激酶的分子靶向药物已成为目前抗肿瘤药物研究的前沿领域,至今已有二十余个蛋白激酶小分子抑制剂获批上市。
渐变性淋巴瘤激酶(anaplastic lymphoma kinase,ALK)是蛋白激酶家族重要成员,2007年在非小细胞肺癌中首次发现的ALK融合基因EML4-ALK,引发了靶向ALK 抑制剂的研发热潮。
针对ALK 融合基因的第一代药物—克唑替尼(Crizotinib)已于2011年上市,成为标志性的个性化治疗药物,在ALK阳性患者中获得良好的无进展生存和客观有效率。
不断的反复的实验才能得到需要的结果,陶素生化现可提供诸多不同信号通路的抑制剂、调节剂以及小分子化合物,并附客户评价、产品相关参考文献、技术支持等助力您的实验研究,且保证产品的高纯度和高活性,交货及时并附带完整的谱图信息。
陶素生化能够提供的118种酪氨酸激酶抑制剂的独特集合,可用于高通量筛选和高内涵筛选通过前期临床研究和临床实验,生物活性和安全性得到验证其中一些抑制剂已经得到FDA批准,优点如下:
作用于酪氨酸激酶,如EGFR,VEGFR,SRC,c-Met和JAK
结构多样,药效显著,可渗透细胞
具有充分详细的结构说明,IC50值,及客户反馈资料
NMR和HPLC技术保证产品高纯度。
蛋白酪氨酸激酶小分子抑制剂-PPT课件
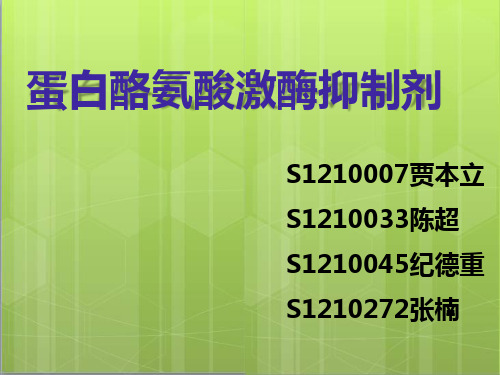
路线三 何茂群,苗得足等在 2019 年报道的专利( CN102584719A) ) 路线二Ⅱ
该路线以3,4-二羟基苯甲醛为原料,经过氰基化,在和氯乙基乙醚反应, 该路线经过氰基化,和氯乙基甲醚反应,再经硝化,还原,然后和DMF硝化,还原,环合,氯代,最后和间氨基苯乙炔反应得到产品。 DMA反应,最后和间氨基苯乙炔反应得到产品。 优点:原料来源简单,合成较方便。 优点:1、避免了在反应中用到国家禁用、对环境污染大、后处理麻烦的 氯化试剂,如草酰氯、五氯化磷、三氯氧磷、氯化亚砜等。 缺点:使用了国家禁止的氯化试剂 2、缩短了合成路线,提高了收率。
基于肿 瘤信号 传导机 制
蛋白酶体抑制剂:硼替佐米
蛋白酪氨酸激酶按其结构可分为受体酪氨酸激酶(RPTK)和非受 体酪氨酸激酶(NRPTK)。许多RPTK都与肿瘤的形成相关,其 原因包括基因突变、染色体易位或简单的激酶过表达。
家族 表皮生长因子受体 受体 EGFR、HER2、HER3和 HER4 表达位置 上皮细胞肿瘤
胰岛素受体 血小板衍化生长因子受体
血管内皮细胞生长因子受体 成纤维细胞生长因子受体 原肌球蛋白受体激酶 肝细胞生长因子受体 红细胞生成素产生肝细胞受体
胰岛素受体等 PDGFR一α 、PDGFR—β
VEGFR一1、VEGFR-2、 VEGFR-3 FGFR-1,FGFR-2,FGFR-3 和FGFR-4。 TRKA、TRKB和TRKC MET、RON
切割方式二(B)
路线四 Jyothi Prasad 等在 2019 年报道的专利( WO201906091 ) 路线五 Jyothi Prasad 等又在 09 年报道的专利( US2009306377A1 )进行工艺改进
该路线以6,7-二甲氧基-3,4-二氢喹唑啉-4-酮(可直接买到)为原料,先 该路线以 6,7-二甲氧基-3,4-二氢喹唑啉-4-酮为原料,经水解,乙酰化保护羟 脱去6,7为上的甲基,保护羟基,氯代,和间氨基苯乙炔反应,然后脱去 基,对甲苯磺酰氯酰化,和间氨基苯乙炔反应,最后脱保护,和卤代乙基乙 保护,最后和卤代乙基甲醚反应得到产品。 醚反应得到产品。 优点:省去了成环一步,避免了前面路线中的硝化反应,降低了成本。 优点:避免使用了国家禁止的氯化试剂,如 SOCl2、(COCl)2等。 缺点:1、该路线先脱甲基再保护,后面还要脱保护,增加了反应的步骤, 缺点:跟上条线一样,经过保护脱保护过程,步骤长。 无形中降低了总产率。 2、氯化试剂依然没有避免。
小分子ERK抑制剂的研究进展_NormalPdf

学报Journal of China Pharmaceutical University2020,51(3):260-269小分子ERK抑制剂的研究进展梁停停1,2,王文杰1,郝思远1,何光超1,2,徐云根1,2*(1中国药科大学药物化学系,南京211198;2江苏省药物分子设计与成药性优化重点实验室,南京211198)摘要细胞外信号调节激酶(ERK)是一种丝/苏氨酸蛋白激酶。
作为RAS-RAF-MEK-ERK信号通路中关键的下游蛋白,其异常活化在肿瘤的发生发展中起着重要作用。
选择性ERK1/2抑制剂能够阻断ERK信号通路,同时克服上游靶点突变而导致的耐药性。
本文概述了MAPK信号通路的组成、ERK的结构与功能以及ERK信号通路在肿瘤发生发展中的作用,并重点介绍一些具有代表性的处于临床和临床前研究阶段的ERK抑制剂。
关键词细胞外信号调节激酶;细胞外信号调节激酶抑制剂;抗肿瘤;耐药性;进展中图分类号R914.5文献标志码A文章编号1000-5048(2020)03-0260-10doi:10.11665/j.issn.1000-5048.20200302引用本文梁停停,王文杰,郝思远,等.小分子ERK抑制剂的研究进展[J].中国药科大学学报,2020,51(3):260–269.Cite this article as:LIANG Tingting,WANG Wenjie,HAO Siyuan,et al.Research progress of ERK small molecule inhibitors[J].J China Pharm Univ,2020,51(3):260–269.Research progress of ERK small molecule inhibitorsLIANG Tingting1,2,WANG Wenjie1,HAO Siyuan1,HE Guangchao1,2,XU Yungen1,2*1Department of Medicinal Chemistry,China Pharmaceutical University,Nanjing211198;2Jiangsu Key Laboratory of Drug Molecular Design and Optimization,Nanjing211198,ChinaAbstract Extracellular signal-regulated kinase(ERK)is a kind of serine/threonine protein kinase.As a key downstream protein in RAS-RAF-MEK-ERK signaling pathway,its abnormal activation plays an important role in the development of tumors.Selective ERK1/2inhibitors can block ERK signaling pathway while overcoming drug resistance caused by upstream target mutation.In this paper,the components of MAPK signaling pathway, the structure and functions of ERK and the role of ERK signaling pathway in tumor development are summarized, and some representative ERK inhibitors in clinical or preclinical studies are emphasized.Key words extracellular signal-regulated kinase(ERK);ERK inhibitors;antitumor;drug resistance;progressThis study was supported by the Undergraduate Innovation and Entrepreneurship Training Program of China Pharmaceutical Univer⁃sity(No.201910316099)RAS-RAF-MEK-ERK信号通路是一条广泛存在于哺乳动物细胞中的信号级联通路,在细胞的分化、存活、衰老和凋亡等细胞活动中发挥着极其重要的作用[1-2]。
小分子药物化学的最新研究进展

小分子药物化学的最新研究进展小分子药物化学是一种通过设计并合成小分子化合物来治疗疾病的学科。
近年来,在药物化学领域的研究中,小分子药物成为研究的热点之一,因为它们具有较低的成本、良好的药代动力学和毒性特性等优点,广泛应用于临床治疗。
目前,小分子药物的研究一直在不断发展,并且取得了一些具有重要意义的成果,下面主要介绍几个最新的研究进展。
一、基于小分子抑制剂的肿瘤治疗肿瘤引起的细胞增殖和凋亡失衡是肿瘤的主要病理生理特征之一,因此,开发具有肿瘤抑制活性的小分子药物是目前肿瘤治疗研究的热点之一。
研究人员通过针对组蛋白去乙酰酶1(HDAC1)的小分子抑制剂的筛选,发现具有良好肿瘤抑制活性的化合物,其作用机制是通过调节细胞周期和蛋白质乙酰化等途径来抑制肿瘤细胞的增殖和生存。
此外,还有一些研究表明,基于蛋白激酶的小分子抑制剂也是治疗肿瘤的有效药物。
例如,Jab1和p53的相互作用可以促进肿瘤细胞的增殖和生存,并且存在在多种肿瘤中,研究人员开发了一种基于Jab1的小分子抑制剂,并通过生物学实验验证了它对肿瘤的有效性,为肿瘤治疗开发提供了新的思路。
二、基于小分子药物的神经系统疾病治疗神经系统疾病是当前临床治疗中的重点之一,众所周知,神经系统疾病大多是由于神经元功能的异常导致的,因此,开发针对神经系统疾病的小分子药物是极其必要的。
研究人员通过对脑缺血模型中神经元的损伤和保护机制的研究,发现β-谷氨酰胺(BAG2)可以防治脑缺血。
BAG2是一种热休克蛋白70(Hsp70)的调节蛋白,控制Hsp70诱导神经元生存和凋亡的平衡。
这些研究揭示了BAG2在神经保护中的潜在作用,可以为神经系统疾病的治疗提供新的靶点。
三、基于小分子药物的免疫调节免疫性疾病是一种病程复杂、病理生理学特异性强、治疗难度较大的疾病。
小分子化合物的免疫调节作用在治疗免疫性疾病中受到了极大的关注。
研究人员利用使用关键小分子拮抗剂来调节细胞因子和受体的活性,能够有效地减轻免疫性疾病的病理反应。
小分子抗肿瘤药物的研究和研发进展

小分子抗肿瘤药物的研究和研发进展随着人类对肿瘤疾病认识的不断深入,小分子抗肿瘤药物研究已成为当前关注的热点和重点。
它们通过特异性地干扰癌细胞内的信号转导、代谢或其它病理生理过程,达到抑制癌细胞生长和扩散的效果。
本文将介绍小分子抗肿瘤药物的研究背景、研发进展及未来发展方向。
1. 研究背景肿瘤疾病一直是人类致死率最高的疾病之一。
传统的肿瘤治疗方式包括手术、放化疗等,但是这些治疗方法存在着一定的局限性。
因此,寻找新的治疗方法是当前的一项重要任务。
小分子抗肿瘤药物的发现为肿瘤治疗提供了一种全新的选择。
小分子药物是指分子量在500道尔顿以下的有机化合物,具有优良的药物代谢和耐受性,容易被肿瘤组织摄取,从而发挥治疗作用。
近年来,小分子药物在肿瘤治疗方面的应用得到不断地拓展,目前已经有多个小分子抗肿瘤药物已经被批准上市,如Gefitinib、Erlotinib等。
2.1 抗癌机理小分子抗肿瘤药物的研究首先需要了解其抗癌机理。
目前,小分子抗肿瘤药物的作用机制主要包括以下几种类型:(1)酪氨酸激酶抑制剂:它们能够选择性地抑制肿瘤细胞内的酪氨酸激酶,从而影响信号传导途径,抑制癌细胞的增殖和生长。
(2)血管生成抑制剂:它们能够抑制肿瘤细胞与周围血管的联系,降低肿瘤细胞生长所需的营养物质和氧气供应。
(3)修饰作用剂:它们通过作用于肿瘤细胞的蛋白,改变蛋白的修饰状态,从而影响肿瘤细胞生长和增殖。
(4)信号途径抑制剂:它们通过干扰肿瘤细胞内信号转导途径,抑制癌细胞增殖和扩散。
在小分子抗肿瘤药物的研发过程中,首先需要寻找合适的靶点,然后设计药物分子。
研究人员需要通过计算机辅助方法、高通量筛选等手段,从大量的小分子化合物中筛选出候选药物。
接下来,需要进行药物合成、药物代谢动力学、毒理学等方面的研究,最终得到具有良好抗癌效果的小分子抗肿瘤药物。
2.3 应用状况目前已经有多个小分子抗肿瘤药物在临床应用中证明其疗效和安全性。
其中最为成功的代表是Gefitinib和Erlotinib等基于酪氨酸激酶抑制剂的药物。
FLT3抑制剂的抗肿瘤研发现状

前言
近年来,蛋白激酶抑制剂一直都是抗肿瘤药物 研发的热点领域,有许多小分子激酶抑制剂如伊马 替尼、索拉非尼和舒尼替尼已经上市,此外还有大 量的小分子激酶抑制剂处于临床研究阶段。FMS 样酪氨酸激酶 3(Fms-like tyrosine kinase,FLT3) 又名胎肝激酶 -2(Fetal Liver Kinase-2,FLK2)和 干细胞激酶 -1(Stem Cell Kinase-1,STK1),是一种 第三类受体酪氨酸激酶[1]。FLT3 在造血作用和 淋巴细胞增殖中发挥关键作用,FLT3 的异常激活 与多种肿瘤特别是急性髓性白血病(Acute Myeloid Leukemia,AML)的发生发展密切相关[2]。FLT3 高
关键词 :FLT3 ;抑制剂 ;肿瘤 中图分类号 :R965.1,R733.3 文献标识码 :A 文章编号 :2095-1264(2015)01-0001-13 doi :10.3969/j.issn.2095-1264.2015.001
Research and Development Status of FLT3 Inhibitors as Antineoplastic Drugs★
★基金项目 :国家自然科学基金项目资助(30873137,30772645,81172927)。 作者简介 :姚磊,男,硕士研究生,研究方向 :小分子抗癌药物的研发,E-mail :yaolei19901014@。 *通讯作者 :余聂芳,男,教授、博士生导师,研究方向 :合理药物设计、抗肿瘤靶向药物筛选与发现、小分子介导的免疫治
癌 ;肾细胞癌 美元(2013年)
2. 舒尼替尼 (SUGEN Inc)
F
小分子抑制剂设计的新策略及研究方法

小分子抑制剂设计的新策略及研究方法小分子抑制剂是一种通过与蛋白质靶点相互作用来调控其活性的化合物。
自20世纪60年代诞生以来,小分子抑制剂已成为药物研究的重要手段,其在治疗癌症、炎症、心血管疾病等方面具有广泛的应用前景。
但是,目前大多数小分子抑制剂的研发仍处于靶点依赖的模式之中,受限于靶点的特异性和亲和力,导致了新药研发的成功率不高。
因此,如何设计出更优异的小分子抑制剂,成为了当前药物研究的重要命题。
一、新策略:靶点无关的小分子抑制剂研究传统的小分子抑制剂设计通常是利用靶点的结构信息来寻找其配体,并通过化学修饰等手段来提高其活性,因此在寻找新的小分子抑制剂时,需要先获得靶点的结构信息。
然而,对于一些难以获得结构信息的靶点,或者靶点结构十分灵活、易变的情况下,这一策略显得不太现实。
在这种情况下,寻找靶点无关的小分子抑制剂成为了一种新的策略。
这种策略的基本思路是,通过高通量筛选等方法,从小分子化合物库中发现与特定细胞或生物过程相关的小分子化合物,并通过验证其抑制作用来确定其活性。
虽然这种策略避免了对靶点结构信息的依赖,但由于小分子化合物的复杂性和多样性,目前仍面临许多的技术挑战。
二、研究方法:计算化学在小分子抑制剂设计中的应用小分子抑制剂的研究方法包括传统的生物实验、靶点结构分析等方法,以及统计学、机器学习等计算方法。
其中,计算化学作为一种有力的工具,可以帮助研究人员在小分子抑制剂研究中更快速、准确地寻找合适的化合物。
基于计算化学的小分子抑制剂设计主要包括以下几个方面:(1)分子对接:将小分子化合物与靶点结合来确定它们的相互作用模式,并评估它们的亲和力。
分子对接可以帮助确定靶点的结构信息,寻找与其结合的小分子化合物,并进行化学修饰优化。
(2)分子动力学模拟:通过模拟蛋白质分子的运动和相互作用过程,分析分子间的相对位置和受力情况,预测其互作模式和稳定性,揭示抑制剂如何影响蛋白质结构和功能,并优化抑制剂的性能。
FDA批准的激酶小分子抑制剂类药物及分类一览

FDA批准的激酶小分子抑制剂类药物及分类一览蛋白激酶蛋白激酶(Kinase)是细胞生命活动重要的信号使者,可催化将ATP末端的γ-磷酸基团转移至底物上,从而将各种信号进行传递(图1)。
蛋白激酶参与了众多的生理过程,包括细胞增殖、存活、凋亡、代谢、转录以及分化等。
药理学及病理学研究表明,对于很多疾病,如肿瘤、炎症性疾病、中枢神经系统疾病、心血管疾病及糖尿病等,蛋白激酶都是一个理想的药物靶点。
图1 Mechanism of protein kinases and related publications对于蛋白激酶的研究始于20世纪50年代,并在90年代随着MAPK/ERK、JAK 及PI3K等信号通路的揭示而达到一个研究热潮。
迄今为止,在人体中发现了518种蛋白激酶,而编码具有激酶活性蛋白的基因则高达900多种。
与之相对应,有关激酶抑制剂的研究也逐步发展,并在激酶作用机制的阐明过程中扮演了重要角色,并成为重要的药物研究热点。
该领域研究的文献数量也是逐年上升,从侧面反映了其在基础研究和药物发现中的重要性。
蛋白激酶抑制剂及其分类过去的15年间,激酶抑制剂作为药物候选的研究取得了长足的进步,不论是基础研究还是在工业界。
在人体现有药物靶点里面,蛋白激酶家族成员占比高达10%(FDA批准药物分子靶点深度解读)。
2001年,第一个激酶抑制剂类药物Imatinib获得FDA批准,成为该领域发展的里程碑,此后十年该类药物以平均每年获批一种的速度稳步发展。
而在2012年1月至2015年2月期间,小分子激酶抑制剂类药物迎来爆发式发展,共有15种新药获得审批。
截至2016年12月底,共有31种小分子激酶抑制剂类药物获得审批,同时还有大量的化合物处于临床或临床前研究中。
除此之外,科研人员还解析了超过5000种的蛋白激酶或蛋白激酶-抑制剂复合体的晶体结构,且超过五分之一的人类蛋白激酶具有明确的小分子抑制剂。
因此,小分子激酶抑制剂已成为药物研发的一个热点领域。
小分子c-Met激酶抑制剂的研究与应用

小分子c-Met激酶抑制剂的研究与应用
赵宝港;齐一琳;王强宇
【期刊名称】《现代医学与健康研究》
【年(卷),期】2018(000)012
【摘要】c-Met是异二聚体受体酪氨酸激酶(RTKs)亚族的原型成员,并且是肝细胞生长因子(HGF)的受体。
HGF与其受体c-Met的结合启动了许多的细胞信号传导,HGF/c-Met信号失调与许多恶性肿瘤的生长有着密切的关系。
因此,cMet激酶已成为癌症药物开发的新希望。
该综述旨在总结近年来小分子c-Met激酶抑制剂药物化学开发的进展,作为潜在的抗癌药物,肯定会有助于未来研究人员在发现小分子c-Met激酶抑制剂方面的发展。
【总页数】2页(P48-48)
【作者】赵宝港;齐一琳;王强宇
【作者单位】河北农业大学理工学院;河北农业大学理工学院;河北农业大学理工学院
【正文语种】中文
【中图分类】R979.1
【相关文献】
1.基于c-Met激酶的小分子抑制剂研究进展 [J], 李丽丽;艾晓杰
2.以c-Met为靶点的小分子酪氨酸激酶抑制剂的研究进展 [J], 赵锐;张喜全;孟庆义
3.针对c-Met激酶的小分子抑制剂研究进展 [J], 陈燕
4.几种小分子c-Met抑制剂类抗肿瘤药物概述 [J], 肖飞;彭红;金鑫;张婷
5.上海药物所靶向c-Met抗肿瘤小分子抑制剂研究取得进展 [J],
因版权原因,仅展示原文概要,查看原文内容请购买。
新型蛋白酪氨酸激酶抑制剂类抗肿瘤药物的研究进展

新型蛋白酪氨酸激酶抑制剂类抗肿瘤药物的研究进展一、概要随着肿瘤发病机制的深入研究和抗肿瘤作用靶点的不断发现,蛋白酪氨酸激酶(PTK)作为信号转导中的关键酶,已经成为抗肿瘤药物研发的重要靶点之一。
PTK在细胞内的信号转导中扮演着至关重要的角色,与肿瘤细胞的生长、增殖、分化和凋亡密切相关。
新型蛋白酪氨酸激酶抑制剂类抗肿瘤药物的研究与开发,对于提高肿瘤治疗效果、改善肿瘤患者生活质量具有重要意义。
本文综述了近年来新型蛋白酪氨酸激酶抑制剂类抗肿瘤药物的研究进展。
我们介绍了PTK的分类及其作用机制,包括受体型和非受体型PTK在细胞信号转导中的作用。
我们详细阐述了PTK抑制剂的设计原理与策略,包括基于结构的小分子抑制剂、抗体药物以及多肽类药物等。
我们还介绍了PTK抑制剂在临床应用中的现状,包括已上市药物的疗效及安全性评价,以及正在研发的药物的临床试验进展。
通过对新型蛋白酪氨酸激酶抑制剂类抗肿瘤药物的深入研究,我们发现这类药物具有显著的抗肿瘤活性,并且在临床上已经取得了一定的疗效。
目前仍存在一些问题,如耐药性、副作用等,需要进一步研究和解决。
未来的研究方向将集中在优化药物结构、提高治疗效果、降低副作用等方面,以期开发出更加安全、有效的蛋白酪氨酸激酶抑制剂类抗肿瘤药物。
新型蛋白酪氨酸激酶抑制剂类抗肿瘤药物的研究进展迅速,为肿瘤治疗提供了新的思路和手段。
随着科学技术的不断进步和临床应用的不断推广,相信这类药物将在未来肿瘤治疗中发挥更加重要的作用。
1. 肿瘤治疗的挑战与现状作为一种复杂的生物学现象,一直是医学界面临的重大挑战。
尽管医学技术和治疗手段不断进步,肿瘤的治疗仍然面临着诸多难题。
肿瘤的异质性使得每一个病例都具有其独特的生物学特征,这为制定统一的治疗方案带来了极大的困难。
肿瘤细胞的快速增殖和侵袭性转移,使得传统的手术、放疗和化疗等手段往往难以彻底清除肿瘤细胞,且在治疗过程中容易产生耐药性。
许多抗肿瘤药物在杀灭肿瘤细胞的也会对正常细胞造成损伤,导致患者的生活质量下降。
小分子药物及其药物靶点的研究进展

小分子药物及其药物靶点的研究进展近年来,小分子药物在医学领域得到广泛应用,成为治疗多种疾病的有效药物。
小分子药物是指分子量较小、分子结构相对简单,具有药理活性的有机化合物。
药物靶点是指药物分子作用的目标分子,是重要的药物研究领域。
本文将综述小分子药物及其药物靶点的研究进展。
一、抗肿瘤药物随着对癌症分子机制的深入研究,抗肿瘤药物的研究也得到了快速发展。
小分子药物以其更高的转化效率、更好的组织分布、更好的穿透能力等特点成为肿瘤治疗的主要选择。
抗肿瘤药物靶点涉及癌细胞自身的多种病理分子,包括细胞周期蛋白激酶、组蛋白去乙酰化酶、PI3K/AKT信号通路等。
二、糖尿病药物糖尿病存在着多种病理机制,小分子药物的研究也涉及到多种药物靶点。
目前,针对糖尿病的小分子药物主要包括胰岛素受体激动剂、GLP-1类似物和DPP-4抑制剂等。
这些药物通过不同机制调节血糖水平,具有较好的治疗效果。
三、神经系统药物神经药物主要用于调节神经系统功能,小分子药物在神经药物领域中发挥着重要的作用。
例如,针对焦虑抑郁症的小分子药物广泛应用于抑制5-HT重摄取并增加NE和DA的释放,从而产生抗抑郁作用。
四、感染病毒药物小分子药物在病毒领域有广泛应用,特别是治疗传染病毒性疾病。
例如,非洲猪瘟毒的小分子药物SR-16234和GFUE-1等治疗尚处于实验室研究阶段,临床应用具有较大的潜力。
五、心血管药物心血管药物主要用于治疗心血管系统疾病。
针对心血管疾病的小分子药物主要包括ACE抑制剂、钙拮抗剂、β受体拮抗剂等,通过调节血压和心率等机制起到治疗作用。
总之,小分子药物及其药物靶点的研究是医药领域的重要研究方向。
通过针对特定疾病分子靶点的开发,可以生产出更加有效、更加安全的药物。
期待未来小分子药物研究能够有新的突破,成为医学领域的热点。
小分子抑制剂的发展和应用

小分子抑制剂的发展和应用小分子抑制剂是一类化学物质,它们可以与蛋白质的活性位点结合,从而抑制蛋白质的功能。
这种药物被广泛应用于治疗癌症、感染和代谢疾病。
随着基因诊断和治疗技术的不断进步,小分子抑制剂的研发和应用也得到了极大的推动。
一、小分子抑制剂的发展小分子抑制剂的研发起源于20世纪上半叶。
当时,研究人员发现一些天然产物拥有非常强的抑制活性,可以用于治疗多种疾病。
然而,这些天然产物的疗效并不稳定,且具有毒性和副作用。
因此,科学家开始尝试合成小分子抑制剂,以替代天然产物。
二、小分子抑制剂的应用1. 抗癌治疗小分子抑制剂在抗癌治疗中具有广泛的应用。
因为癌症是由许多细胞变异和增殖造成的,这些细胞需要一定的蛋白质来支撑它的生长和分裂。
小分子抑制剂可以通过靶向特定的蛋白质,抑制它的功能,从而抑制癌细胞的生长和扩散。
例如,伊马替尼是一种针对骨髓增生性疾病和某些类型的癌症的小分子抑制剂,它可以抑制酪氨酸激酶的活性,阻止癌细胞生长。
另一个例子是厄洛替尼,它是一种针对HER2阳性乳腺癌的小分子抑制剂,可以阻止HER2受体的活性,从而抑制癌细胞生长和扩散。
2. 感染性疾病的治疗小分子抑制剂也可以用于治疗感染性疾病。
例如,奥司他韦和鲍曼氏不动杆菌素是两种广泛用于治疗流感和耐药菌感染的小分子抑制剂。
这些药物可以抑制病毒或细菌的关键酶,从而抑制病原体的生长和扩散。
3. 代谢性疾病的治疗小分子抑制剂还可以用于治疗血管紧张素转换酶抑制剂、利尿剂和胰岛素抵抗等代谢性疾病。
例如,依普利酮是一种常用于治疗高血压和心血管疾病的小分子抑制剂,它可以抑制血管紧张素转换酶的活性,从而降低血压。
另一个例子是哌转唑,它是一种针对胰岛素抵抗的小分子抑制剂,可以通过改善葡萄糖的代谢,降低血糖水平。
三、小分子抑制剂的未来发展随着生物技术和计算机技术的不断发展,小分子抑制剂的研发和应用也会得到极大的推动。
未来研究人员将更加注重小分子抑制剂的设计和合成。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
[8 ] POLVERINO A,COXON A,STARNES C,et al. AMG 706 ,an oral,multikinase inhibitor that selectively targets vascular endothelial growth factor,plateletderived growth factor,and kit receptors,potently inhibits angiogenesis and induces regression in tumor xenografts[J]. Cancer Res, 2006 , 66 ( 17 ):87158721. [9 ] SHANKAR D B,LI J,TAPANG P,et al. ABT869 ,a multitargeted receptor tyrosine kinase inhibitor: inhibition of FLT3 phosphorylation and signaling in acute myeloid leukemia[J] . Blood, 2007 , 109 ( 8 ):34003408. [ 10] SHARMA S, ABHYANKAR V, BURGESS R E, et al. A phase I study of axitinib ( AG013736 ) in combination with bevacizumab plus chemotherapy or chemotherapy alone in patients with metastatic colorectal cancer and other solid tumors[J]. Ann Oncol, 2010 , 21 ( 2 ): 297304. [ 11] SARKER D,MOLIFE R, EVANS T R, et al. A phase I pharmacokinetic and pharmacodynamic study of TKI258 ,an oral,multitargeted receptor tyrosine kinase inhibitor in patients with advanced solid tumors[J]. Clin Cancer Res,2008 , 14 ( 7 ): 20752081. [ 12] SIEMANN D W,BRAZELLE W D,endothelial growth factor receptor2 tyrosine kinase inhibitor cediranib ( Recentin;AZD2171 ) inhibits endothelial cell function and growth of human renal tumor xenografts. [J]. Int J 2009 , 73 ( 3 ): 897903. Radiat Oncol Biol Phys,[ 13] RABBANI S A, VALENTINO M L, ARAKELIAN A, et al. SKI606( Bosutinib ) blocks prostate cancer invasion,growth,and metastasis in vitro and in vivo through regulation of genes involved . Mol Cancer Ther, in cancer growth and skeletal metastasis. [J] 2010 , 9 ( 5 ): 11471157. [ 14 ] DURANTE C,RUSSO D, VERRIENTI A, et al. XL184 ( cabozantinib) for medullary thyroid carcinoma [ J] . Expert Opin Investig Drugs, 2011 , 20 ( 3 ): 407413.[ 15] ESKENS F A,MOM C H,PLANTING A S,et al. A phase I an irreversible dual inhibitor dose escalation study of BIBW 2992 , of epidermal growth factor receptor 1 ( EGFR ) and 2 ( HER2 ) tyrosine kinase in a 2week on,2week off schedule in patients with advanced solid tumours[ J] . Br J Cancer,2008 , 98( 1 ): 8085. [ 16] YANG J L. Nilotibib: A new targeted agent[J]. Oncol Prog(癌 2007 , 5 ( 2 ): 7074. 症进展),[ 17] BOSCHELLI F,ARNDT K,GAMBACORTIPASSERINI C. Bosutinib: a review of preclinical studies in chronic myelogenous leukaemia[J] . Eur J Cancer, 2010 , 46 ( 10 ):17811789. [ 18] KANTARJIAN H,LE COUTRE P,CORTES J,et al. Phase 1 study of INNO406 , a dual Abl / Lyn kinase inhibitor, in Philadelphia chromosomepositive leukemias after imatinib resistance or intolerance[ J] . Cancer,2010 , 116 ( 11 ): 26652672. [ 19] ZHANG J,ADRIáN F J,JAHNKE W,et al. Targeting BcrAbl by combining allosteric with ATPbindingsite inhibitors [J]. Nature, 2010 , 463 ( 7280 ): 501506. [ 20] DONATO N J,FANG D,SUN H,et al. Targets and effectors of the cellular response to aurora kinase inhibitor MK0457 ( VX680 ) in imatinib sensitive and resistant chronic myelogenous leukemia[J] . Biochem Pharmacol, 2010 , 79 ( 5 ): 688697. [ 21]GONTAREWICZ A,BRüMMENDORF T H. Danusertib ( formerly PHA739358 ) a novel combined panAurora kinases and third generation BcrAbl tyrosine kinase inhibitor.Recent Results[J]. Cancer Res, 2010 , 184 : 199214. [ 22] KOSAKA T,YATABE Y,ENDOH H,et al. Analysis of epidermal growth factor receptor gene mutation in patients with onosmall cell lung cancer and acquired resistance to gefitinib [J]. Clin Cancer Res, 2006 , 12 ( 19 ): 57645769. [ 23] JANNE P A,GRAY N,SETTLEMAN J. Factors underlying sensitivity of cancers to smallmolecule kinase inhibitors[J] . Nat Rev 2009 , 8 ( 9 ): 709723. Drug Discov,[ 24]LI D,SHIMAMURA T,JI H,et al. Bronchial andperipheral murine lung carcinomas induced byT790ML858R mutant EGFR re. Cancer spond to HKI272 and rapamycin combination therapy[J] Cell, 2007 , 12 ( 1 ): 8193. [ 25] SEQUIST L V,BESSE B, LYNCH T J, et al. Neratinib, an irreversible panErbB receptor tyrosine kinase inhibitor: results of a phase II trial in patients with advanced nonsmallcell lung cancer [J] . J Clin Oncol, 2010 , 28 ( 18 ): 30763083. [ 26] BURSTEIN J,SUN Y,DIRIX Y,et al. Neratinib,an irreversible ErbB receptor tyrosine kinase inhibitor,in patients with adJ] . J Clin Oncol, 2010 , 28 vanced ErbB2positive breast cancer[( 8 ): 13011307. [ 27] WISSNER A,MANSOUR T S. The development of HKI272 and related compounds for the treatment of cancer[J]. Arch Pharm 2008 , 341 ( 8 ): 465477. [ 28] GENDREAU S B,VENTURA R,KEAST P,et al. Inhibition of the T790M gatekeeper mutant of the epidermal growth factor receptor by EXEL7647[J]. Clin Cancer Res,2007 ,13 ( 12 ): 37133723. [ 29] RIZVI N A,KRIS M G,MILLER V A,et al. Activity of XL647 in clinically selected NSCLC patients ( pts) enriched for the presence of EGFR mutations:Results from Phase 2[J] . J Clin Oncol, 2008 , 26 ( 18 suppl): 437. [ 30]MILLER V A,WAKELEE H A,LARA P N,et al. Activity and tolerance of XL647in NSCLC patients with acquired resistance to EGFRTKIs: Preliminary results of a phase II trial[J]. J Clin Oncol, 2008 , 26 ( 18 suppl): 430. [ 31] LI D,AMBROGIO L,SHIMAMURA T,et al. BIBW2992 ,an irreversible EGFR / HER2 inhibitor highly effective in preclinical lung cancer models[ J] . Oncogene, 2008 ,27 ( 34 ): 47024711. [ 32] YANG C,SHIH J,CHAO T,et al. Use of BIBW2992 ,a novel irreversible EGFR / HER2 TKI,to induce regression in patients with adenocarcinoma of the lung and activating EGFR mutations: Preliminary results of a singlearm phase II clinical trial[J]. J Clin Oncol, 2008 , 26 ( 18 suppl):430.[ 33] JANNE P A, SCHELLENS J H, ENGELMAN J A, et al. Preliminary activity and safety results from a phase I clinical trial of PF00299804 ,an irreversible panHER inhibitor,in patients ( pts ) with NSCLC[J] . J Clin Oncol,2008 , 26 ( 18 suppl): 430 ,[ 34 ] ENGELMAN J A, ZEJNULLAHU K,GALE C M, et al. PF00299804, an irreversible panErbB inhibitor,is effective in lung cancer models with EGFR and ErbB2 mutations that are resistant to gefitinib[ J]. Cancer Res, 2007, 67( 24): 1192411932.[ 35] GONZALES A J,HOOK K E,ALTHAUS I W,et al. Antitumor activity and pharmacokinetic properties of PF00299804 ,a secondgeneration irreversible panErbB receptor tyrosine kinase inhibitor[ J]. Mol Cancer Ther, 2008 , 7 ( 7 ): 18801889.[ 36]HERBST R S, SUN Y, EBERHARDT W E. Vandetanib plus docetaxel versus docetaxel as secondline treatment for patients with advanced nonsmallcell lung cancer ( ZODIAC ): a doubleblind,randomised,phase 3 trial[J]. Lancet Oncol,2010 , 11 ( 7 ): 619626.[ 37] NATALE R B,THONGPRASERT S,GRECO F A,et al. Phase III trial of vandetanib compared with erlotinib in patients with previously treated advanced nonsmallcell Lung cancer[J]. J Clin Oncol,2011 , 29 ( 8 ): 10591066.(收稿日期: 20110531 )中国药学杂志 2011 年12 月第 46 卷第 23 期 Chin Pharm J, 2011 December,Vol. 46 No. 23 · 1789·。
