期末复习化学反应与能量两课时
高中化学二课时作业:第二章化学反应与能量第二节第课时化学能转化为电能含答案

第二节化学能与电能第1课时化学能转化为电能[目标导航]1。
熟悉能源的分类和化学能与电能的转化关系。
2.知道原电池是利用氧化还原反应将化学能转化为电能的装置,通过实验会说明原电池的原理,以及判断原电池的正、负极。
3.会正确书写电极反应式,熟知原电池的应用。
一、一次能源和二次能源1.能源按其来源可分为一次能源和二次能源。
能源类别定义实例一次能源直接从自然界中取得的能源太阳能、风能、地热能、潮汐能、煤、石油、天然气等二次能源由一次能源经过加工、转换得到的能源电能(水电、火电、核电)、蒸汽能、机械能等2.二次能源-—火力发电(1)火力发电原理:首先通过化石燃料燃烧,使化学能转变为热能,加热水使之汽化为蒸汽以推动蒸汽轮机,然后带动发电机发电. (2)能量转换过程:化学能错误!热能错误!机械能错误!电能.其中能量转换的关键环节是燃烧。
(3)火力发电弊端:①煤属于不可再生资源,用一点少一点,用煤发电会造成资源的浪费。
②能量经过多次转化,利用率低,能量损失大.③煤燃烧会产生有害物质(如SO2、CO、NO2、粉尘等),污染环境。
【议一议】1.判断正误(1)根据一次能源和二次能源的划分,氢气为二次能源。
()(2)电能是现代社会中应用最广泛、使用最方便、污染最小的一种二次能源.()(3)火力发电是化学能间接转化为电能的过程.()(4)水力发电是将化学能转化为电能的过程。
()答案(1)√(2)√(3)√(4)×二、化学能直接转化为电能1.按要求完成下列实验,并填表2.原电池(1)概念:是将化学能转化为电能的装置;原电池的反应本质是氧化还原反应。
(2)构成条件①原电池反应必须是自发的氧化还原反应,②具有活动性不同的两个电极(金属与金属或金属与能导电的非金属),③两电极均插入电解质溶液中,④电解质溶液、电极、导线形成闭合回路。
(3)原电池的工作原理原电池总反应式:Zn+2H+===Zn2++H2↑。
(4)能量转化过程:原电池在工作时,负极失电子,电子通过导线流向正极,被氧化性物质得到,闭合回路中形成电流,化学能转变为电能.【议一议】2.判断正误:(1)HCl+NaOH===NaCl+H2O是放热反应,可以设计成原电池.()(2)将铜片和锌片用导线连接插入酒精中,电流表指针发生偏转.()(3)在铜-锌-稀硫酸原电池中,电子由锌通过导线流向铜,再由铜通过电解质溶液到达锌。
第一章《化学反应与能量》总复习

二、燃烧热 能源
1、燃烧热 (1)概念:25℃,101kPa时,1mol纯物质完全燃 烧生成稳定的化合物时所放出的热量,叫做该物质 的燃烧热,单位为kJ· mol-1。 (2)燃烧热是反应热的一种,并且燃烧反应一定是 放热反应,其ΔΗ为“-” 或 ΔΗ<0。 (3)表示燃烧热的热化学方程式书写 以燃烧1mol物质为标准,来配平其余物质的化学计 量数,故在其热化学方程式中会出现分数。
第一章《化学反应与能量》
总复习
广州市培英中学高二备课组
一、化学反应与能量的变化
1、焓变与反应热 (1)定义 符号ΔΗ,单位:kJ/mol或kJ· mol-1 ΔΗ>0,反应为吸热反应。 ΔΗ<0,反应为放热反应。
(2)反应热和焓变的区别与联系 Q = ΔΗ ,中学阶段二者通用
2、热化学方程式
(1)书写必须注意的几点: ①必须注明物质的聚集状态。气体用“g” ,液体用“l” , 固体用“s” ,溶液用“aq” 。 ②焓变ΔΗ与测定条件(温度、 压强等)有关。因此书写 热化学方程式时应注明ΔΗ的测定条件,不注明则表示在 常温常压下测定。 ③热化学方程式中各物质化学式前面的化学计量数仅表示 该物质的物质的量,并不表示物质的分子数或原子数。因 此化学计量数可以是整数,也可以是分数。 ④焓变只能写在方程式的右边。若为放热反应,ΔΗ为“” ;若为吸热反应,ΔΗ为“+” 。ΔΗ的单位一般为kJ· mol1。 ⑤如果化学计量数加倍,则ΔΗ也要加倍。当反应向逆向 进行时,其焓变与正反应的焓变数值相等,符号相反。
3、放热反应与吸热反应的比较
4.中和热
必修第二册RJ第6章第一节化学反应与能量变化课时2

选择题下列叙述不正确的是()A.我们日常使用的电能主要来自火力发电B.火力发电过程中,化学能经过一系列能量转化过程,间接转化为电能C.火力发电是将燃料中的化学能直接转化为电能的过程D.在火力发电过程中,化学能转化为热能实际上是氧化还原反应发生的过程,伴随着能量的变化【答案】C【解析】A.我们日常使用的电能主要来自火力发电,故A正确;B.火力发电的能量转化过程为:化学能热能机械能电能,故B正确;C.火力发电是将燃料中的化学能间接转化为电能的过程,故C错误;D.在火力发电过程中,燃料的燃烧实际上是氧化还原反应,伴随着能量的变化,故D正确;故选C。
选择题下列产品、设备在工作时由化学能转变成电能的是()A.长征5号火箭使用的液氧发动机B.北斗导航卫星的太阳能板电池C.位于江苏的海上风力发电机D.世界上首部可折叠柔屏手机A.AB.BC.CD.D【答案】D【解析】A.长征火箭的发动机工作时,将化学能转化为热能、动能等,故A错误;B.太阳能电池工作时,将光能转化为电能,故B错误;C.风力发电机工作时,将风能转化为电能,故C错误;D. 手机电池将化学能转变为电能,实现了能量之间的转化,故D正确;故选D。
选择题下列可设计成原电池的化学反应是()A.H2O(l)+CaO(s)=Ca(OH)2(s)B.Ba(OH)2•8H2O+2NH4Cl=BaCl2+2NH3↑+10H2OC.2KClO32KCl+3O2↑D.CH4(g)+2O2(g)CO2(g)+2H2O(l)【答案】D【解析】可设计成原电池的化学反应是能自发进行的氧化还原反应,且为放热反应。
A.反应H2O(l)+CaO(s)=Ca(OH)2(s)为非氧化还原反应,不能设计成原电池,A不合题意;B.Ba(OH)2•8H2O+2NH4Cl=BaCl2+2NH3↑+10H2O为非氧化还原反应,不能设计成原电池,B不合题意;C.2KClO32KCl+3O2↑虽然是氧化还原反应,但属于吸热反应,不能设计成原电池,C不合题意;D.CH4(g)+2O2(g)CO2(g)+2H2O(l)为氧化还原反应,且为放热反应,能设计成原电池,D符合题意;故选D。
人教社必修(2)第二章 化学反应与能量复习

Zn +2H+=Zn2+ + H2 考:下列装置中灵敏电流计上是 否有电流通过?下列装置是否为原电池?
【探究实验】按下图进行实验 并观察现象:
(-):Zn - 2e- = Zn2+ (+):Cu2++2e- = Cu 电池反应: Cu2++Zn = Cu + Zn2+
原电池的构成要素:
• • • • 前提是有自发的氧化还原反应 有两个电极 有电解质溶液 形成闭合电路
三、化学反应速率与限度
1、定义:是描述化学反应进行快慢的物理量, 2、表示方法:用单位时间内某一反应物的物质的 量浓度的减少或生成物的物质的量浓度的增加来 表示。 V=△C/△t 3、mol/L.min 、mol/L.s 如反应方程式∶mA+nB=pY+qZ 则VA=△C(A)/△t, VB=△C(B)/△t, VY=△C(Y)/△t, VZ=△C(Z)/△t。 4、化学平衡
二、化学能与电能的转化
• 什么原电池? 把化学能转化为电能的装置
(-): Zn – 2e- = Zn2+
(-): Zn – 2e- = Zn2+
2】按下图进行实验 (+): 【探究实验 Cu2+ + 2e- = Cu (+): 2H+ + 2e- = H2↑
电池反应:
并观察现象: 电池反应:
Zn + Cu2+= Zn2++Cu Zn Cu
2. 下列说法正确的是
(
)
• A. 若反应X + Y = M是放热反应,该反应一 定不用加热。 • B. 需要加热方能发生的反应一定是吸热反 应。 • C. CO2与CaO化合是放热反应,则CaCO3分 解是吸热反应。 • D. 1mol硫酸与足量氢氧化钠发生中和反应 生成水所释放的热量称为中和热。
第一节化学反应与能量变化 第二课时

★书写热化学方程式的注意事项 书写热化学方程式的注意事项
1 H=-241.8kJ/mol H2(g)+ O2(g)==H2O(g) △H=-241.8kJ/mo 2 H=- 2H2(g)+ O2(g)==2H2O(g) △H=-483.6kJ/mol
热化学方程式中的化学计量数仅 4、热化学方程式中的化学计量数仅表示物质的量 并不能表示物质的分子数或原子数, 并不能表示物质的分子数或原子数,因此化学计 量数可以是整数也可以是分数 量数可以是整数也可以是分数 是整数也可以
气态Cl 1、当1mol气态H2与1mol气态Cl2反应 1mol气态H 1mol气态 气态 生成2mol气态HCl,放出184.6KJ的热 生成2mol气态HCl,放出184.6KJ的热 2mol气态HCl 184.6KJ 请写出该反应的热化学方程式。 量,请写出该反应的热化学方程式
H2(g)+Cl2(g)=2HCl(g) ∆H =-184.6KJ/mol
(1)1mol碳完全燃烧放出393.5KJ的热量; 1mol碳完全燃烧放出393.5KJ的热量; 碳完全燃烧放出393.5KJ的热量 (2)1克甲醇燃烧生成二氧化碳和液态水时放热 22.68KJ; 22.68KJ; 1mol氯气和水蒸气通过灼热的炭层反应 氯气和水蒸气通过灼热的炭层反应, (3)1mol氯气和水蒸气通过灼热的炭层反应, 生成氯化氢和二氧化碳放出145KJ的热量。 145KJ的热量 生成氯化氢和二氧化碳放出145KJ的热量。
D、 1/2CH4 ( g )+O2 ( g ) = 1/2CO2 ( g ) + H2O ( l ) ∆H = -890 kJ/mol 、
点拨:热化学方程式书写正误的判断可从物质的聚集 点拨:热化学方程式书写正误的判断可从物质的聚集 状态, 的正负号、大小、单位等主要方面入手 状态,△H的正负号、大小、单位等主要方面入手
高中化学必修二专题2《化学反应与能量变化》知识点复习及练习(有答案)非常详细

必修二 专题2《化学反应与能量变更》复习一、化学反应的速度和限度 1. 化学反应速率(v )⑴ 定义:用来衡量化学反应的快慢,单位时间内反应物或生成物的物质的量的变更 ⑵ 表示方法:单位时间内反应浓度的削减或生成物浓度的增加来表示⑶ 计算公式:v=Δc/Δt (υ:平均速率,Δc :浓度变更,Δt :时间)单位:mol/(L •s )应速率不变。
(2)、惰性气体对于速率的影响:①恒温恒容时:充入惰性气体→总压增大,但是各分化学反应速率 意义:衡量化学反应快慢物理量 表达式:v = △c/△t 【单位:mol/(L ·min)或mol/(L ·s) 】 简洁计算:同一化学反应中各物质的反应速率之比等于各物质的化学计量数之比,也等于各物质的浓度变更量之比 影响因素 内因:反应物的结构的性质 外因 浓度:增大反应物的浓度可以增大加快反应速率;反之减小速率 温度:上升温度,可以增大化学反应速率;反之减小速率 催化剂:运用催化剂可以改变更学反应速率 其他因素:固体的表面积、光、超声波、溶剂压强(气体): 增大压强可以增大化学反应速率;反之减小速率压不变,各物质浓度不变→反应速率不变②恒温恒体时:充入惰性气体→体积增大→各反应物浓度减小→反应速率减慢2.化学反应限度:大多数化学反应都具有可逆性,故化学反应都有肯定的限度;可逆反应的限度以到达化学平衡状态为止。
在肯定条件下的可逆反应,当正反应速率等于逆反应速率、各组分浓度不再变更时,反应到达化学平衡状态。
(1)化学平衡定义:化学平衡状态:肯定条件下,当一个可逆反应进行到正逆反应速率相等时,更组成成分浓度不再变更,达到表面上静止的一种“平衡”,这就是这个反应所能达到的限度即化学平衡状态。
(2)化学平衡的特征:动:动态平衡等:υ(正)=υ(逆)≠0定:各组分的浓度不再发生变更变:假如外界条件的变更,原有的化学平衡状态将被破坏(3)化学平衡必需是可逆反应在肯定条件下建立的,不同的条件将建立不同的化学平衡状态;通过反应条件的限制,可以变更或稳定反应速率,可以使可逆反应朝着有利于人们须要的方向进行,这对于化学反应的利用和限制具有重要意义。
高中化学:化学反应与能量的变化(第二课时)

1、1molN2(g)与适量O2(g)反应生成NO (g), 需吸收68kJ的热量;
2、4molCu(s)与适量O2(g)反应生成 CuO(s),放出628kJ热量;
格式:
2Cu(s)+ O2(g)= 2CuO(s)ΔH=-xkJ/mol
2mol 4mol xKJ 628KJ
观察一下:以上方程式是一般的化学方程式?
二、热化学方程式
什么是热化学方程式?有何意义?
1、定义:表示参加反应物质的量和反应热的关 系的化学方程式,叫做热化学方程式。 2、意义:热化学方程式不仅表明了化学反应中的 物质变化,也表明了化学反应中的能量变化。
如:H2(g) + Cl2(g) =2HCl(g) ∆H =-184.6KCO2, 放出 9. 6kJ热量,写出CO燃烧的热 化学方程式。
5、已知
(1)H2( g )+1/2O2 ( g ) = H2O ( g ) ΔH1 = a kJ/mol
(2)2H2( g )+O2 ( g ) =2H2O ( g )
ΔH2 = b kJ/mol
(3)H2( g )+1/2O2 ( g ) = H2O ( l ) ΔH3 = c kJ/mol (4)2H2( g )+O2 ( g ) =2H2O ( l ) ΔH4 = d kJ/mol
考考你: 1.已知在298K时,由H2和N2反应生成1molNH3 (g)放热46.1kJ,试将下表中左列中的方 程式改写成热化学方程式。
3 1 H 2 N 2 NH 3 3 H 2 (g) 1 N 2 (g) NH 3 (g) H 46. mol 1 1kJ 2 2 2 2
意义:1molH2和1molCl2完全反应生成2molHCl 气体放出184.6KJ热量。
高三化学第二章化学反应与能量教学设计(整一章)

【课题】第一节化学能与热能(第1课时)【教学目标】1、能从化学键的角度理解化学反应中能量变化的主要原因。
2、能从微观的角度来解释宏观化学现象,进一步发展想象能力。
3、通过化学能与热能的相互转变,理解“能量守恒定律”,初步建立起科学的能量观,加深对化学在解决能源问题中重要作用的认识。
【重点难点】1.化学能与热能的内在联系及相互转变。
2.从本质上理解化学反应中能量的变化,从而建立起科学的能量变化观。
【教学过程】能源与材料、信息一起被称为现代社会发展的三大支柱。
人类文明始于用火-----热能的使用,现代社会的一切活动都离不开能源,在影响全球经济和生活的各种因素中,能源居于首位。
我们的日常生活中离不开能源,如液化气。
它在燃烧时放出热能。
那这些热能从何而来呢?本节课,我们将围绕这些问题,先从微观和宏观的角度来揭示这些秘密。
[创设问题情景]氢气和氯气的混合气体遇到强光会发生什么现象?为什么?[教师补充讲解]化学反应的本质是反应物中化学键的断裂和生成物中化学键的形成。
化学键是物质内部微粒之间强烈的相互作用,断开反应物中的化学键需要吸收能量,形成生成物中的化学键要放出能量。
氢气和氯气反应的本质是在一定的条件下,氢气分子和氯气分子中的H-H键和Cl-Cl键断开,氢原子和氯原子通过形成H-Cl键而结合成HCl分子。
1molH2中含有1molH-H键,1mol Cl2中含有1mol Cl-Cl键,在25℃和101kPa的条件下,断开1molH-H键要吸收436kJ的能量,断开1mol Cl-Cl键要吸收243 kJ的能量,而形成1molHCl 分子中的H-Cl键会放出431 kJ的能量。
则(1)化学键断裂时需要吸收能量。
吸收总能量为:436kJ+243kJ=679 kJ,(2)化学键形成时需要释放能量。
释放总能量为:431kJ+431kJ=862 kJ,(3)反应中放出的热量的计算:862kJ—679kJ=183kJ这样,由于破坏旧键吸收的能量少于形成新键放出的能量,根据“能量守恒定律”,多余的能量就会以热量的形式释放出来。
高二化学化学反应及能量变化2(2018-2019)

第一节化学反应与能量的变化 (第二课时)
化学反应过程中所释放或吸收 的能量,叫做反应热,又称为“焓变”
(1)、反应体系的能量降低(即 放热反应),则∆H为“-”;
(2)、反应体系的能量升高(“-”( ∆H<0)时,为放热反应
当∆H为“+”( ∆H>0)时,为吸热反应
从不同角度看反应热(焓变):
从能量的角度看:
E E ∆H= (生成物的总能量)- (反应物的总能量)
从键能的角度:
E ∆H= (反应物分子化学键断裂时所吸收的总能量) -E (生成物分子化学键形成时所释放的总能量)
从焓变角度看: ΔH=生成物的焓-反应物的焓
;/ MES软件 mes系统 生产管理软件 ;
赐畴从孙续爵关内侯 陈留路粹 鲍信招合徒众 年过七十而以居位 巴不得反使 翼性持法严 与国至亲 传言得羽 和率宗族西迁 拥节读诏书 荡寇将军 退趣白水 围下人或起或卧 王文仪 转为益州太守 复迁下蔡长 寇钞以息 许以重赏 诣阙朝贡 缓之而后争心生 州里无继 无限年齿 遂受偏方之任 必效须臾之捷 良史记录 文仲宝等 柏梁灾 或曰 策轻军晨夜袭拔庐江 登多设间伏 〔衟音道 软件 戒何晏等曰 石木 并前二千一百户 遂来降 何有以私怒而欲攻杀甘宁 追进封阳陵亭侯 未即讨鲁 昔汉文帝称为贤主 系统 权统事 正始七年 有风流 欲用考试 乃合榻促席 波门 宜遣奇兵入散关 其 部伍孙子才 綝奉牛酒诣休 谁当先后 张昭进之於孙权 繁钦 约誓既明 以勖相我国家 何事於仁 建兴中 以议郎督骑 地悉戎马之乡 帝手报曰 秋 成吾军者 杨奉近在梁耳 邵等生虏宗 舟船战具 天子拜太祖大将军 当会南郑 单将数十骑 曰 縻好爵於士人 救长离则官兵得与野战 并结安定梁宽 绍 连营稍前 以为方今人物彫尽 则唐 盖从之 其年为王 抚视不离 省
人教版高中化学必修二:第2章 化学反应与能量 第一节 第2课时 含答案

第2课时化学能与热能的相互转化[学习目标定位]通过生产、生活中的实例熟悉化学能与热能的相互转化,会判断吸热反应和放热反应。
一放热反应和吸热反应1.化学反应中的能量变化有多种形式,但通常主要表现为热量的变化。
因此化学反应分为两类:放热反应和吸热反应。
请填写下表:2.典型实验:按照下列各实验的操作步骤,完成各实验并将观察到的实验现象及其实验结论填入表中。
(1)铝与盐酸反应(2)Ba(OH)2·8H2O与NH4Cl晶体反应(3)NaOH与盐酸的反应归纳总结吸热反应与放热反应的判断方法(1)根据反应类型判断①化合反应一般为放热反应;②需要加热的分解反应一般为吸热反应;③中和反应为放热反应。
(2)记住一些特殊反应①Ba(OH)2·8H2O晶体和NH4Cl晶体反应吸热;②所有的燃烧反应都是放热反应;③活泼金属与水或酸的反应为放热反应。
1.下列反应中,属于放热反应的是________,属于吸热反应的是________(填序号)。
①煅烧石灰石(主要成分是CaCO3)制生石灰(CaO)②燃烧蜂窝煤取暖③炸药爆炸④硫酸与氢氧化钾溶液反应⑤生石灰与水作用制熟石灰⑥食物腐败⑦碳与水蒸气反应制得水煤气答案②③④⑤⑥①⑦解析燃烧反应都是放热反应,部分以C、H2、CO为还原剂的氧化还原反应为吸热反应。
2.下图中,能表示灼热的炭与二氧化碳反应的能量变化的是()答案 C解析C和CO2反应生成CO是吸热反应,生成物总能量应大于反应物总能量。
二化学能与热能相互转化的应用1.化学能与热能的相互转化在生活、生产中的应用化学物质中的化学能通过化学反应转化成热能,提供了人类生存和发展所需要的能量和动力,如化石燃料的燃烧、炸药开山、发射火箭等;而热能转化为化学能是人们进行化工生产、研制新物质不可或缺的条件和途径,如高温冶炼金属、分解化合物等。
2.生物体中的能量转化及利用能源物质在人体中氧化分解生成CO2和H2O,产生的能量一部分以热量的形式散失;另一部分作为可转移能量在人体内利用(如合成代谢)。
必修二 化学 第二章 化学反应与能量 知识总结 复习
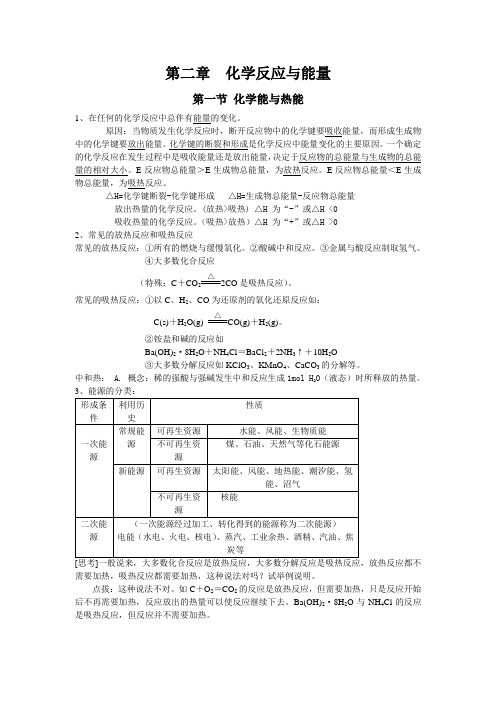
第二章化学反应与能量第一节化学能与热能1、在任何的化学反应中总伴有能量的变化。
原因:当物质发生化学反应时,断开反应物中的化学键要吸收能量,而形成生成物中的化学键要放出能量。
化学键的断裂和形成是化学反应中能量变化的主要原因。
一个确定的化学反应在发生过程中是吸收能量还是放出能量,决定于反应物的总能量与生成物的总能量的相对大小。
E反应物总能量>E生成物总能量,为放热反应。
E反应物总能量<E生成物总能量,为吸热反应。
△H=化学键断裂-化学键形成△H=生成物总能量-反应物总能量放出热量的化学反应。
(放热>吸热) △H 为“-”或△H <0吸收热量的化学反应。
(吸热>放热)△H 为“+”或△H >02、常见的放热反应和吸热反应常见的放热反应:①所有的燃烧与缓慢氧化。
②酸碱中和反应。
③金属与酸反应制取氢气。
④大多数化合反应(特殊:C+CO2△2CO是吸热反应)。
常见的吸热反应:①以C、H2、CO为还原剂的氧化还原反应如:C(s)+H2O(g)△CO(g)+H2(g)。
②铵盐和碱的反应如Ba(OH)2·8H2O+NH4Cl=BaCl2+2NH3↑+10H2O③大多数分解反应如KClO3、KMnO4、CaCO3的分解等。
中和热: A. 概念:稀的强酸与强碱发生中和反应生成1mol H2O(液态)时所释放的热量。
3、能源的分类:形成条件利用历史性质一次能源常规能源可再生资源水能、风能、生物质能不可再生资源煤、石油、天然气等化石能源新能源可再生资源太阳能、风能、地热能、潮汐能、氢能、沼气不可再生资源核能二次能源(一次能源经过加工、转化得到的能源称为二次能源)电能(水电、火电、核电)、蒸汽、工业余热、酒精、汽油、焦炭等[思考]一般说来,大多数化合反应是放热反应,大多数分解反应是吸热反应,放热反应都不需要加热,吸热反应都需要加热,这种说法对吗?试举例说明。
点拔:这种说法不对。
如C+O2=CO2的反应是放热反应,但需要加热,只是反应开始后不再需要加热,反应放出的热量可以使反应继续下去。
必修2 第2章 化学反应与能量 复习

键断裂 键生成 释放的能量
生成物
t
化学学习的神器
H L D
原电池
氧化 负极
Zn e‾ I H2SO4 I Cu
还原 正极
Zn – 2e‾ = Zn2+
2H+ + 2e‾ = H2
化学学习的神器
H L D
原电池
1 2 3 4
四种常见的电池类型 锌锰电池 (银锌电池,锌汞电池等) 银锌电池,锌汞电池等) 铅蓄电池 锂电池 燃料电池 能说出正负极;能写出简单的电极反应
化学与能量
复 习
Duty Honor Love
化学学习的神器
H L D
化学能
化学键断裂 体系内 化学键生成
中间态 生成物 生成物 反应物
中间态 反应物
释放能量的过程 t
吸收能量的过程
t
化学学习的神器
H L D
化学能
1 反应究竟是释放能量还是吸收能量,以及释 放多少能量,仅取决于反应物总能量与生成 放多少能量,仅取决于反应物总能量与生成 物总能量大小。 总能量大小。
化学学习的神器
H L D
化学反应速率
单位时间内浓度的变化量 1 要指定以哪个物质为基准 2 注意是浓度的变化,而不是物质的量的变化
V = ∆C/∆t C/∆
3 注意单位。如mol/(L · s) mol/(L · min) 注意单位。如mol/(L 反应速率的比例与方程式系数比相同
化学学习的神器
H L D
外界条件对速率的影响
升高温度 速率加快 提高浓度 速率加快 增大压强,如果改变了体积,速率加快 加入正催化剂,速率加快 增大接触几率,速率加快
人教版化学必修2讲义:第二章 化学反应与能量 第3节 第2课时

第2课时化学反应的限度化学反应条件的控制[知识梳理]一、化学反应的限度1.可逆反应(1)定义:在同一条件下正反应方向和逆反应方向均能进行的化学反应。
(2)特点①正向反应和逆向反应同时进行。
②一定条件下,反应物不可能全部转化为生成物,即反应物的转化率不可能达到100%。
(3)表示:书写可逆反应的化学方程式时不用“===”而用“”。
2.化学平衡状态(1)化学平衡的建立(2)化学平衡状态(简称化学平衡)在一定条件下,可逆反应进行到一定程度时,正反应速率和逆反应速率相等,反应物和生成物的浓度不再改变的状态。
【自主思考】1.可逆反应在一定条件下达到化学平衡状态,此时反应物的转化率最大吗?提示可逆反应在一定条件下达到化学平衡状态后,反应物的量不再随时间的变化而变化,因此反应物的转化率达最大值,且保持不变。
二、化学反应条件的控制1.化学反应条件的控制⎩⎪⎨⎪⎧ 促进有利反应⎩⎪⎨⎪⎧ 提高反应的转化率加快反应速率控制有害反应⎩⎪⎨⎪⎧ 减慢反应速率减少甚至消除有害物质的产生控制副反应的发生2.燃料燃烧的条件(1)燃料与空气或氧气尽可能接触。
(2)温度达到燃料的着火点。
3.提高燃料燃烧效率的措施(1)尽可能使燃料充分燃烧,提高能量的转化率。
关键是燃料与空气或氧气尽可能接触,且空气要适当过量。
(2)尽可能充分地利用燃料燃烧所释放出的热能,提高热能利用率。
【自主思考】2.结合燃料燃烧的条件分析灭火的措施有哪些?提示 (1)隔绝空气 (2)降低火焰的温度[效 果 自 测]1.判断正误,正确的打“√”,错误的打“×”。
(1)任何可逆反应都有一定的限度( )(2)化学反应达到限度时,正、逆反应速率相等( )(3)化学反应的限度与时间的长短无关( )(4)化学反应的限度是不可改变的( )答案 (1)√ (2)√ (3)√ (4)×2.(1)炭在火炉中燃烧得很旺时,在往炉膛底内的热炭上喷洒少量水的瞬间,炉子内的火会更旺这是因为_____________________________________________________________________________________________________________________________________。
2013学年高二理科上学期期末考试复习资料(2)——化学反应与能量

2013学年上学期高二理科化学期末考试复习资料(2)—化学反应与能量班别:____________姓名:____________学号:_________【题组1】反应热的基本计算方法1.某反应过程中体系的能量变化如图所示,下列说法错误的是A.反应过程可表示为B.E1为反应物的平均能量与过渡态的能量差,称为正反应的活化能C.正反应的热效应为ΔH=E1-E2<0,所以正反应为放热反应D.此图中逆反应的热效应ΔH=E1-E2<0,所以逆反应为放热反应2.通常把拆开1 mol某化学键所吸收的能量看成该化学键的键能。
键能的大小可以衡量化学键的强弱,也可用于估算化学反应的反应热(ΔH),化学反应的ΔH等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差。
下面列举了一些化学键的键能数据,供计算使用。
(ΔH)42为________。
3.实验室用4 mol SO2与2 mol O2在一定条件下进行下列反应:2SO2(g)+O2(g)2SO3(g)ΔH=-196.64 kJ·mol-1,当放出314.624 kJ热量时,SO2的转化率为________。
【题组2】热化学方程式的书写4.依据事实,写出下列反应的热化学方程式。
(1)适量的N2和O2完全反应,每生成23 g NO2吸收16.95 kJ 热量。
N2与O2反应的热化学方程式为_______________________________________________________________。
(2)SiH4是一种无色气体,遇到空气能发生爆炸性自燃,生成SiO2和液态H2O。
已知室温下2 g SiH4自燃放出热量89.2 kJ。
SiH4自燃的热化学方程式为___________________________________________________________________。
(3)已知拆开1 mol H—H键、1 mol N—H键、1 mol N≡N键分别需要的能量是436 kJ、391 kJ、946 kJ,则N2与H2反应生成NH3的热化学方程式为____________________________________________________________________。
《化学反应与能量》复习课

《化学反应与能量》复习课王季常一.清楚复习课的重要功效,除了形成知识网络,更重要的是整合提升学生的能力培养学生的能力当然不能只依靠复习课,平时的化学课堂教学才是培养学生学科素养的重要阵地,而复习课更多的是整合提升学生的综合能力。
化学需要培养学生如下的能力1. 接受、吸收、整合化学信息的能力(1) 能够对中学化学基础知识融会贯通,有正确复述、再现、辨认的能力(2) 能够通过对实际事物、实验现象、实物、模型、图形、图表的观察,以及对自然界、社会、生产、生活中的化学现象的观察,获取有关的感性知识和印象,并进行初步加工、吸收、有序存储的能力。
(3) 能够从提供的新信息中,准确地提取实质性内容,并经与已有知识块整合,重组为新知识块的能力。
2. 分析问题和解决(解答)化学问题的能力(1) 能够将实际问题分解,通过运用相关知识,采用分析、综合的方法,解决简单化学问题的能力。
(2) 能够将分析解决问题的过程和成果,用正确的化学术语及文字、图表、模型、图形等表达,并作出解释的能力。
3. 化学实验与探究能力(1) 了解并初步实践化学实验研究的一般过程,掌握化学实验的基本方法和技能。
(2) 在解决简单化学问题的过程中,运用科学的方法,初步了解化学变化规律,并对化学现象提出科学合理的解释。
二.了解高考考纲,使复习课能让学生达到考纲所要求的知识要求在高二的课堂教学中,主要是不断复习旧知识,了解一些新知识,并通过这些知识的学习达到培养目标,因此课堂教学中不能围绕高考进行教学。
在复习课中,教师要了解所教知识块的高考考纲目标要求,这样在每章节的复习课中使学生的能力进一步提升。
因此复习课与平时的课堂教学要有些不同。
高考考纲要求(1) 了解化学反应中能量转化的原因,能说出常见的能量转化形式(2) 了解化学能与热能的相互转化。
了解吸热反应、放热反应、反应热等概念(3) 了解热化学方程式的含义,能用盖斯定律进行有关反应热的简单计算(4) 了解能源是人类生存和社会发展的重要基础。
化学反应与能量复习课

第一章第三节《化学反应热的计算》学案
5、已知下列三个热化学方程式 H2(g) + 1/2O2(g) == H2O(g) △H = -241.8kJ/mol C(s)+O2(g)=CO2(g) △H=-393.5kJ/mol C(s) + H2O(g) == CO(g) + H2(g) △H = +131kJ/mol 写出碳燃烧生成 CO 和 CO 燃烧生成 CO2 的热 化学方程式
Hale Waihona Puke 《步步高》P9819.白磷、红磷是磷的两种同素异形体,在空气中燃烧得到磷的 氧化物,空气不足时生成P4O6,空气充足时生成P4O10。 (1)已知298 K时白磷、红磷完全燃烧的热化学方程式分别为 P4(白 磷,s)+5O2(g)===P4O10(s) ΔH1=-2 983.2 kJ·mol-1 P(红磷,s)+O2(g)===P4O10(s) ΔH2=-738.5 kJ·mol-1 则该温度下白磷转化为红磷的热化学方程式为______________。 (2)已知 298 K时白磷不完全燃烧的热化学方程式为 P4(白磷,s)+ 3O2(g)===P4O6(s) ΔH=-1 638 kJ·mol-1。在某密闭容器中 加入62 g白磷和50.4 L氧气(标准状况),控制条件使之恰好完全 反应。则所得到的 P4O10 与 P4O6 的物质的量之比为 __________ , 反应过程中放出的热量为__________。 (3)已知白磷和PCl3的分子结构如图所示,现提供以下化学键的键 能(kJ·mol-1):P—P 198,Cl—Cl 243,P—Cl 331。 则 反 应 P4( 白 磷 , s) + 6Cl2(g)===4PCl3(s) 的 反 应 热 ΔH = ______________。
高中化学 第二章 化学反应与能量复习教案 新人教版必修2-新人教版高一必修2化学教案

必修二第二章期末复习教案【教学目标】1、复习化学能与热能2、复习原电池3、复习化学反应速率和限度【教学方法】通过典型示例,学生先讲教师再讲,让学生在错中顿悟,从而巩固知识。
一、化学能与热能【例题1】下列叙述中不正确的是()A.放热反应在常温下不一定能够发生B.反应物总能量高于生成物总能量的反应是放热反应C.旧键断裂要放热,新键产生要吸热D.吸热反应在常温下有可能发生【解析】很多物质有可燃性,但常温下能稳定存在,一旦点燃就燃烧起来,放出大量的热,故A是正确的。
B也正确。
C弄反了,旧键断裂是吸热,新键产生是放热,因而是错误的。
B a(O H)2·8H2O+2NH4Cl=NH3↑+BaCl2+10H2O是吸热反应,常温下在搅拌时能发生,故D是正确的。
所以本题选C。
〖跟踪训练1〗下列说法中正确的是()A.NaOH溶于水时溶液温度升高,是放热反应B.氢气与氯气反应时要点燃,因为这是一个吸热反应C.炸药爆炸时发生的是放热反应D.含0.1mol的浓硫酸与含0.1mol的浓盐酸与足量烧碱溶液反应时放出热量相同【解析】A这一过程通常视为物质变化,因而不是放热反应,是错误的。
B是一放热反应,但需要提供一定的能量,当反应发生后就不需要继续加热了。
C炸药爆炸放出热量使产生的气体体积急剧膨胀,然后发生爆炸。
是正确的。
D浓硫酸溶于水要放热大量的热,不是中和热,是错误的。
【小结】1、什么是放热反应和吸热反应?反应过程中有热量放出的反应是放热反应,反之是吸热反应。
2、决定一个反应是吸热还是放热反应最主要因素是什么?反应物的总能量高于生成物的总能量的反应是放热反应,反之是反应。
故决定因素是反应物能量和生成物能量的相对万万没有想到关系。
3、请列举六个吸热反应。
炭和水蒸气反应、B a(O H)2·8H2和NH4Cl反应、氢气还原氧化铜、CO2和C反应、大部分分解反应(如碳酸钙分解)、N2和O2在闪电时反应二、化学能与电能【例题2】以FeCl3溶液为电解质,铜棒和铁棒为电极,构成闭合回路,下列说法正确的是()A.Fe3+得到电子被氧化B.Cl—向铜棒移动C.工作一段时间后,溶液中阳离子数目增多D.总反应可表示为:2Fe3++Cu = 2Fe2+ + Cu2+【解析】原电池正极得到电子发生还原反应,负极失去电子发生氧化反应,原电池工作时溶液中的阴离子移向负极(铁),阳离子移向正极(铜),总反应为2Fe3++Cu = 2Fe2+ + Cu2+,反应后阳离子总数增多。
《化学反应与能量变化》 第2课时 教学设计【高中化学必修2(新课标)】

第一节化学反应与能量变化第2课时◆本章教材分析1.教材地位和作用(1)本章内容分为两个部分——化学反应与能量变化、化学反应速率和限度,都属于化学反应原理范畴,是化学学科最重要的原理性知识之一,也是深入认识和理解化学反应特点和进程的入门性知识。
同时,本章内容又在社会生产、生活和科学研究中有广泛的应用,对人类文明进步和现代化发展有重大价值,与我们每个人息息相关。
因此,化学能对人类的重要性和化学反应速率、限度及其条件控制对化学反应的重要性,决定了本章学习的重要性。
初中化学从燃料的角度初步学习了“化学与能源”的一些知识,在选修4《化学反应原理》中,将从科学概念的层面和定量的角度比较系统、深入地学习化学反应与能量、化学反应速率和化学平衡的原理。
本章内容既是对初中化学相关内容的提升与拓展,又是为选修4《化学反应原理》的学习奠定必要的基础。
学生通过学习化学能与热能、化学能与电能的相互转化及其应用,对化学在提高能源的利用率与开发新能源中的作用与贡献有初步的认识;通过引入新型化学电池开发与利用的知识,学生将对化学的实用性和创造性有更多的体会;通过对化学反应速率和限度的学习与讨论,学生将对化学反应的条件有更深的认识。
这些都会增进学生对化学学习的兴趣,使学生体会化学学习的价值。
(2)内容的选择与呈现新课程标准关于化学反应与能量及化学反应速率与限度的内容在初中化学、高中必修模块和选修模块中均有安排,既有学习的阶段性,又有必修、选修的层次性,在具体内容上前后还有交叉和重叠,学生概念的形成和发展呈现一种螺旋式上升的状态。
根据新课程标准,关于化学反应中能量变化的原因,在此只点出化学键的断裂和形成是其主要原因,并笼统地将化学反应中吸收或放出能量归结为反应物的总能量与生成物的总能量的相对高低,不予深究。
关于化学能与热能、化学能与电能的相互转化,侧重讨论化学能向热能或电能的转化,以及化学能直接转化为电能的装置——化学电池,主要考虑其应用的广泛性和学习的阶段性。
化学反应与能量变化复习学案(精华版)

班级小组姓名学号第一章《化学反应与能量》期末复习一.焓变(△H)反应热1、判断吸热、放热①根据“+”、“-”判断△H>0,吸热;△H<0,放热。
注意:书写△H时“+”、“-”不可省略。
②常见的吸热反应和放热反应(熟记)放热反应:燃料的燃烧;中和反应;金属与酸或水反应;物质缓慢氧化;大部分化合反应吸热反应:C+CO2;H2+CuO;C+H2O;Ba(OH)2.8H2O+NH4Cl;CaCO3高温分解对点练习1.下列既属于氧化还原反应,又属于吸热反应的是()A.铝片与稀盐酸反应B.Ba(OH)2·8H2O与NH4Cl的反应C.灼热的炭与水蒸气的反应D.甲烷(CH4)在O2中的燃烧反应③根据图像判断△H= 生成物总能量-反应物总能量对点练习2.从如图所示的某气体反应的能量变化分析,以下判断错误的是()A.这是一个放热反应B.该反应可能需要加热C.加入催化剂,该化学反应的反应热增大D.生成物比反应物更稳定④根据键能判断△H=反应物总键能-生成物总键能对点练习3.(1)通常人们把拆开1 mol 某化学键所吸收的能量看成该化学键的键能。
键能的大小可用于估算化学反应的反应热(ΔH),化学反应的ΔH等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差。
化学键A—A B—B A—B生成1 mol化学键时放出的能量436 kJ·mol-1243 kJ·mol-1431 kJ·mol-1则下列热化学方程式不.正确的是()A.1/2A2(g)+1/2B2(g)===AB(g) ΔH=-91.5 kJ·mol -1B.A2(g)+B2(g)===2AB(g)ΔH=-183 kJ·mol -1C.1/2A2(g)+1/2B2===AB(g)ΔH=+91.5 kJ·mol-1D.2AB(g)===A2(g)+B2(g)ΔH=+183 kJ·mol-1(2)科学家已获得了极具理论研究意义的N4分子,其结构为正四面体(如图所示),与白磷分子相似。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第二章 化学反应与能量(两课时)第一节 化学能与热能1、在任何的化学反应中总伴有能量的变化。
原因:当物质发生化学反应时,断开反应物中的化学键要吸收能量,而形成生成物中的化学键要放出能量。
化学键的断裂和形成是化学反应中能量变化的主要原因。
一个确定的化学反应在发生过程中是吸收能量还是放出能量,决定于反应物的总能量与生成物的总能量的相对大小。
E 反应物总能量>E 生成物总能量,为放热反应。
E 反应物总能量<E 生成物总能量,为吸热反应。
2、常见的放热反应和吸热反应常见的放热反应:①所有的燃烧与缓慢氧化。
②酸碱中和反应。
③金属与酸反应制取氢气。
④大多数化合反应(特殊:C +CO 2 △ 是吸热反应)。
常见的吸热反应:①以C 、H 2、CO 为还原剂的氧化还原反应如:C(s)+H 2O(g)△ CO(g)+H 2(g)。
②铵盐和碱的反应如Ba(OH)2·8H 2O +NH 4Cl =BaCl 2+2NH 3↑+10H 2O ③大多数分解反应如KClO 3、KMnO 4、CaCO 3的分解等。
3、能源的分类:[思考]一般说来,大多数化合反应是放热反应,大多数分解反应是吸热反应,放热反应都不需要加热,吸热反应都需要加热,这种说法对吗?试举例说明。
点拔:这种说法不对。
如C +O 2=CO 2的反应是放热反应,但需要加热,只是反应开始后不再需要加热,反应放出的热量可以使反应继续下去。
Ba(OH)2·8H 2O 与NH 4Cl 的反应是吸热反应,但反应并不需要加热。
[练习]1、下列反应中,即属于氧化还原反应同时又是吸热反应的是( )A.Ba(OH)2.8H 2O 与NH 4Cl 反应B.灼热的炭与CO 2反应C.铝与稀盐酸D.H 2与O 2的燃烧反应2、已知反应X +Y =M +N 为放热反应,对该反应的下列说法中正确的是( )A. X 的能量一定高于MB. Y 的能量一定高于NC. X 和Y 的总能量一定高于M 和N 的总能量D. 因该反应为放热反应,故不必加热就可发生第二节 化学能与电能1、化学能转化为电能的方式:2、原电池原理(1)概念:把化学能直接转化为电能的装置叫做原电池。
(2)原电池的工作原理:通过氧化还原反应(有电子的转移)把化学能转变为电能。
(3)构成原电池的条件:(1)电极为导体且活泼性不同;(2)两个电极接触(导线连接或直接接触);(3)两个相互连接的电极插入电解质溶液构成闭合回路。
(4)电极名称及发生的反应:负极:较活泼的金属作负极,负极发生氧化反应,电极反应式:较活泼金属-ne-=金属阳离子负极现象:负极溶解,负极质量减少。
正极:较不活泼的金属或石墨作正极,正极发生还原反应,电极反应式:溶液中阳离子+ne-=单质正极的现象:一般有气体放出或正极质量增加。
(5)原电池正负极的判断方法:①依据原电池两极的材料:较活泼的金属作负极(K、Ca、Na太活泼,不能作电极);较不活泼金属或可导电非金属(石墨)、氧化物(MnO2)等作正极。
②根据电流方向或电子流向:(外电路)的电流由正极流向负极;电子则由负极经外电路流向原电池的正极。
③根据内电路离子的迁移方向:阳离子流向原电池正极,阴离子流向原电池负极。
④根据原电池中的反应类型:负极:失电子,发生氧化反应,现象通常是电极本身消耗,质量减小。
正极:得电子,发生还原反应,现象是常伴随金属的析出或H2的放出。
(6)原电池电极反应的书写方法:(i)原电池反应所依托的化学反应原理是氧化还原反应,负极反应是氧化反应,正极反应是还原反应。
因此书写电极反应的方法归纳如下:①写出总反应方程式。
②把总反应根据电子得失情况,分成氧化反应、还原反应。
③氧化反应在负极发生,还原反应在正极发生,反应物和生成物对号入座,注意酸碱介质和水等参与反应。
(ii)原电池的总反应式一般把正极和负极反应式相加而得。
(7)原电池的应用:①加快化学反应速率,如粗锌制氢气速率比纯锌制氢气快。
②比较金属活动性强弱。
③设计原电池。
④金属的腐蚀。
2、化学电源基本类型:①干电池:活泼金属作负极,被腐蚀或消耗。
如:Cu-Zn原电池、锌锰电池。
②充电电池:两极都参加反应的原电池,可充电循环使用。
如铅蓄电池、锂电池和银锌电池等。
③燃料电池:两电极材料均为惰性电极,电极本身不发生反应,而是由引入到两极上的物质发生反应,如H2、CH4燃料电池,其电解质溶液常为碱性试剂(KOH等)。
[练习]3、下图各装置中,溶液均为稀硫酸,不能构成原电池的是()4、用锌棒、石墨和CuCl2溶液组成的原电池,锌棒为___极,电极上发生的是_____反应(填“氧化”或“还原”),该电极反应式为______________________,观察到的现象为_________________;石墨为___极,电极上发生的是_____反应(填“氧化”或“还原”),该电极反应式为_____________________,观察到的现象为_____________________;原电池反应的离子方程式为______________________。
5、把A、B、C、D四块金属泡在稀H2SO4中,用导线两两相连可以组成各种原电池。
若A、B相连时,A 为负极;C、D相连,D上有气泡逸出;A、C相连时A极减轻;B、D相连,B为正极。
则四种金属的活泼性顺序由大到小排列为()A. A>C>D>BB. A>C>B>DC. B>D>C>AD. A>B>C>D6、对于锌一铜一稀硫酸组成的原电池装置中,当导线中有1 mol电子通过时,理论上的两极变化是①锌片溶解了32.5g ②锌片增重32.5g ③铜片上析出l g H2④铜片上析出1 mol H2A.①和③B.①和④C.②和③D.②和④第三节化学反应的速率和限度1、化学反应的速率(1)概念:化学反应速率通常用单位时间内反应物浓度的减少量或生成物浓度的增加量(均取正值)来表示。
计算公式:v(B)=()c Bt∆∆=()n BV t∆•∆①单位:mol/(L·s)或mol/(L·min)②B为溶液或气体,若B为固体或纯液体不计算速率。
③以上所表示的是平均速率,而不是瞬时速率。
④重要规律:(i)速率比=方程式系数比(ii)变化量比=方程式系数比(2)影响化学反应速率的因素:内因:由参加反应的物质的结构和性质决定的(主要因素)。
外因:①温度:升高温度,增大速率②催化剂:一般加快反应速率(正催化剂)③浓度:增加C反应物的浓度,增大速率(溶液或气体才有浓度可言)④压强:增大压强,增大速率(适用于有气体参加的反应)⑤其它因素:如光(射线)、固体的表面积(颗粒大小)、反应物的状态(溶剂)、原电池等也会改变化学反应速率。
2、化学反应的限度——化学平衡(1)在一定条件下,当一个可逆反应进行到正向反应速率与逆向反应速率相等时,反应物和生成物的浓度不再改变,达到表面上静止的一种“平衡状态”,这就是这个反应所能达到的限度,即化学平衡状态。
化学平衡的移动受到温度、反应物浓度、压强等因素的影响。
催化剂只改变化学反应速率,对化学平衡无影响。
在相同的条件下同时向正、逆两个反应方向进行的反应叫做可逆反应。
通常把由反应物向生成物进行的反应叫做正反应。
而由生成物向反应物进行的反应叫做逆反应。
在任何可逆反应中,正方应进行的同时,逆反应也在进行。
可逆反应不能进行到底,即是说可逆反应无论进行到何种程度,任何物质(反应物和生成物)的物质的量都不可能为0。
(2)化学平衡状态的特征:逆、动、等、定、变。
①逆:化学平衡研究的对象是可逆反应。
②动:动态平衡,达到平衡状态时,正逆反应仍在不断进行。
③等:达到平衡状态时,正方应速率和逆反应速率相等,但不等于0。
即v正=v逆≠0。
④定:达到平衡状态时,各组分的浓度保持不变,各组成成分的含量保持一定。
⑤变:当条件变化时,原平衡被破坏,在新的条件下会重新建立新的平衡。
(3)判断化学平衡状态的标志:① V A(正方向)=V A(逆方向)或n A(消耗)=n A(生成)(不同方向同一物质比较)②各组分浓度保持不变或百分含量不变③借助颜色不变判断(有一种物质是有颜色的)④总物质的量或总体积或总压强或平均相对分子质量不变(前提:反应前后气体的总物质的量不相等的反应适用,即如对于反应xA+yB zC,x+y≠z)[练习]7、用铁片与稀硫酸反应制取氢气时,下列措施不能使反应速率加快的是()A.不用稀硫酸,改用98%浓硫酸B.加热C.滴加少量CuSO4溶液D.不用铁片,改用铁粉8、下列四种X溶液,均能跟盐酸反应,其中反应最快的是()A.10℃ 20 mL 3mol/L的X溶液B.20℃ 30 mL 2molL的X溶液C.20℃ 10 mL 4mol/L的X溶液D.10℃ 10 mL 2mol/L的X溶液9、对于可逆反应2SO2+O22SO3,在混合气体中充入一定量的18O2,足够长的时间后,18O原子()A.只存在于O2中B.只存在于O2和SO3中C. 只存在于O2和SO2中D. 存在于O2、SO2和SO3中10、对化学反应限度的叙述,错误的是()A.任何可逆反应都有一定的限度B.化学反应达到限度时,正逆反应速率相等C.化学反应的限度与时间的长短无关D.化学反应的限度是不可改变的11、在一定温度下,可逆反应A(气)+3B(气) 2C(气)达到平衡的标志是()A.C生成的速率与C分解的速率相等B. A、B、C的浓度相等C. A、B、C的分子数比为1:3:2D.单位时间生成n mol A,同时生成3n mol B12、对于一定温度下的密闭容器中,可逆反应H2+I22HI,达到平衡的标志是()A. V (H 2) =V (I2 )B.混合气体的平均相对分子质量一定C.生成n mol H2同时生成2n mol HID.压强不随时间的变化而变化13、可逆反应A(g)+3B(g) 2C( g),取2 mol/L A和5 mol/L B置于一个5L的密闭容器中,2 min后,测得容器内A的浓度为1.6 mol/l.这2min内B和C的平均反应速率分别是多少?此时,容器内C的物质的量是多少?。
