GB 4789.4-2010食品微生物学检验 沙门氏菌检验
食品中沙门氏菌和副溶血性弧菌污染状况的调查与分析

食品中沙门氏菌和副溶血性弧菌污染状况的调查与分析摘要:考察江苏地区181份高危食品(包括肉制品、熟食制品、水产品、蛋制品)中沙门氏菌和副溶血性弧菌的污染与分布情况。
调查结果显示:181份食品中,肉类食品108份,检出沙门氏菌4株,均在生畜禽肉类中检出。
49份生制水产类食品中检出副溶血性弧菌15份,检出率为30.6%。
针对两菌的污染状况进行分析,为寻找可能引起食源性疾病的重点食品,开展食品安全研究和控制食品市场食源性疾病的发生提供技术依据。
关键词:沙门氏菌副溶血性弧菌污染状况沙门氏菌(salmonella)是一种常见的病原菌,作为温血和冷血动物的肠道菌,分布范围十分广泛,它经污染食品传播,能在人类肠道中迅速繁殖,侵入肠粘膜组织,产生肠毒素,导致发热、腹痛、腹泻等全身症状,严重者出现败血症,由沙门氏菌引起的食物中毒一直占世界食物中毒病例前列。
1998年以来国家食源性疾病监测网的数据显示,副溶血性弧菌(vibrio parahaemolyticus, vp)引起食物中毒的发生规模及人群暴露规模已经超过沙门氏菌,高居微生物性食物中毒首位。
考虑到江苏省某些沿海沿江城市水产品中副溶血性弧菌危害的潜在性,因此同时选择沙门氏菌和副溶血性弧菌作为主要研究对象,考察其在我省地区食品中的污染和分布情况,为了解其在居民主要消费食品污染的本底情况,寻找可能引起食源性疾病的重点食品,为开展食品安全研究和控制食品市场食源性疾病的发生提供技术依据。
1、材料与方法1.1样品来源生肉类、蛋制品类采集自我省大型集贸市场、个体销售点及大型超市;散装熟食制品类采集自个体熟食销售点及大型超市熟食柜台;水产类包括生鲜水产品、冷冻水产品及水产制品类采集自水产品批发市场及大型超市。
1.2材料干燥培养基均使用北京陆桥技术有限公司产品。
沙门氏菌及弧菌显色培养基为郑州博赛生物技术研究所产品。
诊断血清为兰州生物制品研究所产品。
1.3方法1.3.1沙门菌检测参照gb 4789.4—2010《食品安全国家标准食品微生物学检验沙门氏菌检验》。
GB4789.4

表 3 沙门氏菌属生化反应初步鉴别表
硫化氢 反应序号
(H2S)
靛基质
氰化钾 pH7.2尿素 (KCN)
赖氨酸脱羧酶
A1
+
-
-
-
+
A2
+
+
-
-
+
A3
-
-
-
-
+/-
注:+阳性;-阴性;+/-阳性或阴性。
注:+阳性;-阴性;+/-阳性或阴性。 5.4.2.1 反应序号 A1:典型反应判定为沙门氏菌属。如尿素、KCN 和赖氨酸脱羧酶 3 项中 有 1 项异常,按表 4 可判定为沙门氏菌。 如有 2 项异常为非沙门氏菌。 表 4 沙门氏菌属生化反应初步鉴别表
GB 4789.4-2010 食品安全国家标准 食品微生物学检验 沙门氏菌检验
前言 本标准代替 GB/T 4789.4-2008《食品卫生微生物学检验 沙门氏菌检验》。 本标准与 GB/T 4789.4-2008 相比,主要变化如下 ——修改了标准的中英文名称; ——修改了标准的范围; ——修改了培养基和试剂; ——修改了设备和材料; ——修改了附录 A。 本标准的附录 A、附录 B 为规范性附录。 本标准所代替的历次版本发布情况为: ——GB 4789.4-84、GB 4789.4-1994、GB/T 4789.4-2003、GB/T 4789.4-2008。
图 1 沙门氏菌检验程序 5 操作步骤 5.1 前增菌
称取 25 g(mL)样品放入盛有 225 mL BPW 的无菌均质杯中,以 8 000 r/min~10 000 r/min 均质 1 min~2 min,或置于盛有 225 mL BPW 的无菌均质袋中,用拍击式均质器拍打 1 min~2 min。若样 品为液态,不需要均质,振荡混匀。如需测定 pH 值,用 1 mol/mL 无菌 NaOH 或 HCl 调 pH 至 6.8±0.2。 无菌操作将样品转至 500 mL 锥形瓶中,如使用均质袋,可直接进行培养,于 36 ℃±1 ℃培 养 8 h~ 18h。 如为冷冻产品,应在 45 ℃以下不超过 15 min,或 2 ℃~5 ℃不超过 18 h 解冻。 5.2 增菌 轻轻摇动培养过的样品混合物,移取 1 mL,转种于 10 mL TTB 内,于 42 ℃±1 ℃培养 18 h~24 h。同时,另取 1 mL,转种于 10 mL SC 内,于 36 ℃±1 ℃培养 18 h~24 h。 5.3 分离 分别用接种环取增菌液 1 环,划线接种于一个 BS 琼脂平板和一个 XLD 琼脂平板(或 HE 琼脂 平板或沙门氏菌属显色培养基平板)。于 36 ℃±1 ℃分别培养 18 h~24 h (XLD 琼脂 平板、HE 琼脂 平板、沙门氏菌属显色培养基平板) 或 40 h~48 h (BS 琼脂平板),观察 各个平板上生长的菌落, 各个平板上的菌落特征见表 1。 表1 沙门氏菌属在不同选择性琼脂平板上的菌落特征
沙门氏菌检验详细流程图

1 mL+SC10 mL 36 ℃±1 ℃,18 h~24 h
BS
XLD(或HE、科玛嘉显色培养基)
36 ℃±1 ℃,40 h~48 h
36 ℃±1 ℃,18 h~24 h
挑取可疑菌落
TSI,赖氨酸,NA, 靛基质, 尿素 (pH 7.2), KCN
商 品 化 生 化 H2S+靛基质- 尿素- H2S+靛基质+ 尿 H2S-靛基质-尿素 反应结果与左
为了最大可能的检出沙门氏菌,原则上必须使用 两种以上选择性分离培养基。
进口-SS 进口-SS 国产-SS 进口-HE 国产-HE 进口-XLD 国产-XLD 进口-BS 国产-BS CHRO显色 国产-DHL 国产-WS TSA(对照)
65.3 81.0 52.0 83.2 80.0 83.0 86.2 106.6 77.7 68.4 98.4 71.6 100.0
初筛微生 物
沙门氏菌
柠檬酸杆 菌属
变形杆菌
菌落颜色
紫色(直径约 1mm)
蓝色(直径约 1mm)
无色或被抑 制
特异性 灵敏度
89% 100%
---
---
(铜绿假单胞菌也呈紫红色, 可以通过前增菌排除。所以推 荐在检测中的前增菌用TTB。 粉红色、深红色、干燥菌落、 边缘锯齿状等 均非沙门氏菌菌 落。)
被分成2500多个血清型。
Vi抗原 O抗原 H抗原
沙门氏菌命名与书写方式
目前的命名方法规定:
肠道沙门菌肠道亚种(亚种Ⅰ)给予专用名,并采用 标本分离地址的地名。菌名的第一个字母需大写,且 亚种Ⅰ的所用菌名不能用斜体。例如:肠道沙门菌鼠 伤寒血清型应书写为Salmonella enterica subsp.enterica serotype Typhimurium,但在实际工作中,可简写为S. Typhimurium。
中华人民共和国国家标准食品卫生微生物学检验沙门氏菌、志贺氏菌和

中华人民共和国国家标准食品卫生微生物学检验沙门氏菌、志贺氏菌和致泻大肠中华人民共和国国家标准食品卫生微生物学检验沙门氏菌、志贺氏菌和致泻大肠埃希氏菌的肠杆菌科噬菌体检验方法Mic伪biological examination of food hygi叨ewe Examination of Salmonellae , Shigellae , and diarrhoea causative及cherich血coli妙means of thed泣agnostic typing phage set for enterobacteriaceae前言本标准对GB/T4789.31一1994袭食品卫生微生物学检验沙门氏菌、志贺氏菌和致泻大肠埃希氏菌肠杆菌科噬菌体检验方法》进行修订。
本标准与GB/T4789.31一19料相比主要修改如下:―按照GB/T1.1一2000对标准文本的格式和文字进行修改。
―规范原标准中的“设备和材料”。
本标准自实施之日起,GB/T4789.31一19944同时废止。
本标准由中华人民共和国卫生部提出并归口。
本标准起草单位:江西省卫生防疫站、中国疚病预防控制中心营养与食品安全所。
本标准主要起草人:何晓青、付萍、计融。
本标准于1994年首次发布,本次为第一次修订。
范围本标准规定了应用肠杆菌科噬菌体诊断法检验食品中沙门氏菌、志贺氏菌和致泻大肠埃希氏菌的基本要求、操作程序和结果判定本标准适用于各种食品、食物中毒的检验,也适用于食品从业人员的肠道沙门氏菌和志贺氏菌带菌检验.2、规范性引用文件下列文件中的条款通过本标准的引用而成为本标准的条款。
凡是注日期的引用文件,其随后所有的修改单(不包括勘误的内容)或修订版均不适用于本标准,然而,鼓励根据本标准达成协议的各方研究是否可使用这些文件的最新版本。
凡是不注日期的引用文件,其墩新版本适用于本标准。
GB/T4789.4食品卫生微生物学检验沙门氏菌检验GB/T4789.5一2003食品卫生微生物学检验志贺氏菌检验GB/T4780.6食品卫生微生物学检验致泻大肠埃希氏菌检验GB/T4789.28一2003食品卫生微生物学检验染色法、培养基和试剂3、设备和材料3.1恒温培养箱:36℃士1℃。
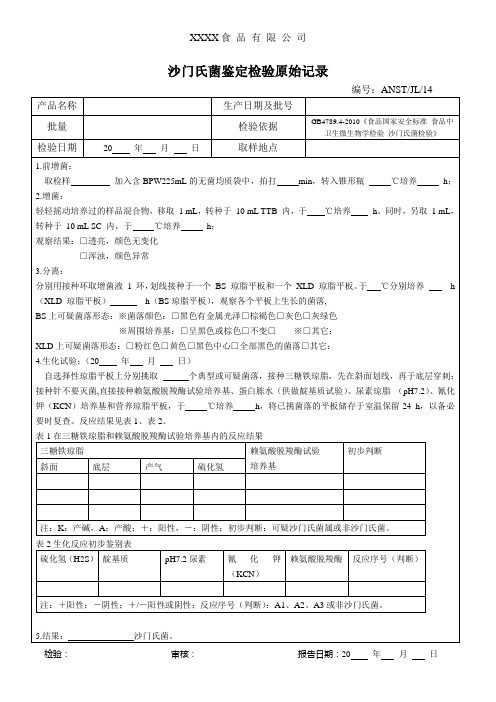
沙门氏菌鉴定检验原始记录
检验:审核:报告日期:20年月日
XXXX食品有限Βιβλιοθήκη 司沙门氏菌鉴定检验原始记录
编号:ANST/JL/14
产品名称
生产日期及批号
批量
检验依据
GB4789.4-2010《食品国家安全标准食品中卫生微生物学检验沙门氏菌检验》
检验日期
20年月日
取样地点
1.前增菌:
取检样加入含BPW225mL的无菌均质袋中,拍打min,转入锥形瓶℃培养h;
2.增菌:
轻轻摇动培养过的样品混合物,移取1 mL,转种于10 mL TTB内,于℃培养h。同时,另取1 mL,转种于10 mL SC内,于℃培养h;
观察结果:□透亮,颜色无变化
□浑浊,颜色异常
3.分离:
分别用接种环取增菌液1环,划线接种于一个BS琼脂平板和一个XLD琼脂平板。于℃分别培养h(XLD琼脂平板)h(BS琼脂平板),观察各个平板上生长的菌落,
表1在三糖铁琼脂和赖氨酸脱羧酶试验培养基内的反应结果
三糖铁琼脂
赖氨酸脱羧酶试验
培养基
初步判断
斜面
底层
产气
硫化氢
注:K:产碱,A:产酸;+:阳性,-:阴性;初步判断:可疑沙门氏菌属或非沙门氏菌。
表2生化反应初步鉴别表
硫化氢(H2S)
靛基质
pH7.2尿素
氰化钾(KCN)
赖氨酸脱羧酶
反应序号(判断)
注:+阳性;-阴性;+/-阳性或阴性;反应序号(判断):A1、A2、A3或非沙门氏菌。
BS上可疑菌落形态:※菌落颜色:□黑色有金属光泽□棕褐色□灰色□灰绿色
※周围培养基:□呈黑色或棕色□不变□※□其它:
XLD上可疑菌落形态:□粉红色□黄色□黑色中心□全部黑色的菌落□其它:
肉鸡中沙门菌污染监测

肉鸡中沙门菌污染监测令狐采学[摘要] 目的对肉鸡养殖和屠宰环节进行沙门菌监测,确定肉鸡在养殖和屠宰环节中沙门菌的污染状况,分析肉鸡中沙门菌的污染来源,为食品安全风险评估提供基础数据,同时也为预防和控制由沙门菌起的食源性疾病提供科学依据。
方法在四川省成都市、遂宁市选取肉鸡养殖场和屠宰场作为监测点。
采集肉鸡活体肛拭、养殖场环境样本,肉鸡胴体,屠宰场环境样本进行沙门菌分离,并对检出菌株运用脉冲场凝胶电泳(PFGE)进行分子分型,用微量肉汤稀释法进行14种抗生素药物敏感实验。
结果共从2个肉鸡屠宰场和1个肉鸡养殖场采集样本417份,检出沙门菌12株,检出率为2.87%。
通过PFGE分型,共得到4个带型。
其中遂宁养殖场的1株环境分离株和遂宁屠宰场的3株肉鸡胴体分离株具有相同PFGE型别,成都屠宰场的2株环境分离株和该屠宰场4株肉鸡胴体分离株具有相似PFGE型别。
遂宁分离的4株沙门菌对14种抗生素100%敏感。
成都分离的8株沙门菌对14抗生素耐药程度各异,其中4株沙门菌能耐受3种以上药物。
结论四川省部分地区肉鸡在养殖和屠宰环节存在沙门菌污染,且有多重耐药菌株出现,应进一步加大监测力度。
沙门菌是引起食源性疾病的常见致病菌之一。
在自然界沙门菌分布广泛, 主要由于食入污染食品,引起感染性腹泻。
在全球范围内沙门菌引起的细菌性食物中毒都位居前列[1,2],并且呈现上升趋势。
在我国导致细菌性食物中毒的致病菌中沙门菌位居首位[3]。
鸡肉作为沙门菌污染的主要食物之一[4],监测肉鸡中沙门菌的来源、污染和耐药状况,对因肉鸡沙门菌污染导致食物中毒的风险评估和预防、控制、治疗沙门菌引起的食物中毒具有非常重要的意义。
近年来养殖中抗生素的过度和不正确使用导致动物中分离到耐药沙门菌的情况越来越普遍,且多重耐药的沙门菌也多有报道[5]。
降低沙门菌对食品的污染是控制沙门菌食源性疾病的总要途径之一。
通过溯源找出并消除污染源是防治沙门菌污染的有效手段。
2010版沙门氏菌检验

返回
表2 沙门氏菌属在不同选择性琼基平板上的菌落特征
三塘铁琼脂
斜面
K K A 初步判断
赖氨酸脱羧酶试验 培养基 硫化氢
+(-) +(-) +(-) + +
底层
A A A
产气
+(-) +(-) +(-)
可疑沙门氏菌 属 可疑沙门氏菌 属 可疑沙门氏菌 属
非沙门氏菌
非沙门氏菌
A
K
A
K
+/+/-
+/+/-
蛋白胨水、靛基质试剂 氰化钾(KCN ) 培养 尿素琼脂 赖氨酸脱羧酶试验培养基 糖发酵管 邻硝基酚 β-D 半乳糖苷 (ONPG)培养基 半固体琼脂 丙二酸钠培养基 沙门氏菌O 和H 诊断血清。 生化鉴定试剂盒
操作步骤
1、前增菌——第一步使食物样品在含有营养的非选择性培养 基中增菌,使受损伤的沙门氏菌细胞恢复到稳定的生理状态。 2、选择性增菌——在含选择性抑制剂的促生长培养基中间, 样品进一步增菌的一个步骤。此培养基允许沙门氏菌持续增 殖,同时阻止大多数其他细菌的增殖。 3、选择性平板分离——这一步采用固体选择性培养基,抑制 非沙门氏菌的生长,提供肉眼可见的疑似沙门氏菌纯菌落的 识别。 4、生物化学筛选——排除大多数非沙门氏菌。也提供了沙门 氏菌培养物菌属的初步鉴定。 5、血清学技术——提供了培养物菌种的鉴定。
返回
表1 沙门氏菌属在不同选择性琼脂平板上的菌落特征
选择性琼 脂平板 BS 琼脂
(36 ℃±1 ℃ 40 h~48 h)
沙门氏菌
菌落为黑色有金属光泽、棕褐色或灰色,菌落周围培养基可 呈黑色或棕色;有些菌株形成灰绿色的菌落,周围培养基不变。
食品微生物检验技术W4304沙门氏菌检验-检验操作程序及要点-传统鉴定-4-微教材

《农产品/食品微生物检验》课程-微教材知识讲解沙门氏菌操作程序及要点——传统鉴定沙门氏菌操作程序及要点分为检验程序和操作步骤一、检验程序根据国标,沙门氏菌的检验程序为: 检样经无菌处理后,称取25 g(mL)样品加入到225 mL BPW中36±1℃培养8~18h;取培养物1mL 接种到10mL的TTB中同时取1mL 接种到10mL 的SC中,分别于42±1℃和36±1℃培养18~24h;取培养后的增菌液分别划线接种于BS琼脂平板和XLD琼脂平板(或HE琼脂平板、显色培养基平板)中,于36±1℃培养18~24h,BS 需延长至40~48h;培养后挑取可疑菌落做生化试验。
挑取2 个以上典型或可疑菌落——接种三糖铁琼脂,赖氨酸脱羧酶试验管和对照管、供做靛基质试验的色氨酸肉汤、尿素(pH7.2),KCN试验管和对照管,同时划线营养琼脂平板——如5项生化都符合——则直接判定为沙门氏菌——如五项中靛基质阳性——则补做甘露醇和山梨醇试验,如果两项均为阳性——为可疑沙门氏菌,但需结合血清学鉴定结果进行判定——如五项中H2S阴性——则需补做ONPG试验,ONPG阴性,同时赖氨酸脱羧酶阳性——为沙门氏菌——也可在三糖铁和赖氨酸脱羧酶试验初步判断结果后,使用商品化的生化鉴定系统进行生化鉴定——判定是否为沙门氏菌——如果5项反应中有2项以上不符合——则沙门氏菌阴性——最后报告结果二、操作步骤主要分为:1、样品处理与前增菌;2、增菌;3、分离;4、传统生化鉴定试验;5、系统生化鉴定试验;6、血清学鉴定。
其中传统生化鉴定试验又分为三糖铁和赖氨酸脱羧酶试验,靛基质、尿素和氰化钾试验、甘露醇、山梨醇以及ONPG试验三个部分。
本片以鸡肉为样品,演示沙门氏菌检验的样品处理和前增菌的操作过程。
1、前增菌:在无菌室内,以75%酒精擦拭样品外包装,尤其是包装的开口处,用无菌剪刀在样品封口处剪开包装袋,换用一个无菌剪刀将鸡肉样品剪碎至无菌罐内,用无菌镊子称取25 g样品至盛有225 mL BPW的样品瓶中,再转入注明样品信息、检测人员以及检测日期的均质袋中,密封,用拍击式均质器拍击2 min。
饼干检测方法清单

饼干检测方法清单
1、GB_T 4789.24-2003 食品卫生微生物学检验糖果、糕点、蜜饯检验
2、GB_T 12456-2008 食品中总酸的测定
3、GB 5009.11-2014 食品中总砷及无机砷的测定
4、GB 5009.12-2010 食品中铅的测定
5、GB_T 5009.37-2003 食用植物油卫生标准的分析方法
6、GB_T 5009.28-2003 食品中糖精钠的测定
7、GB 5009.3-2010食品中水分的测定
8、GBT 5009.56-2003 糕点卫生标准的分析方法
9、食品卫生微生物检测
(1)GB 4789.5-2012 食品微生物学检验志贺氏菌检验
(2)GB 4789.4-2010 食品微生物学检验沙门氏菌检验
(3)GB 4789.15-2010 食品微生物学检验霉菌和酵母计数
(4)GB 4789.10-2010 食品微生物学检验金黄色葡萄球菌检验
(5)GB 4789.2-2010 食品微生物学检验菌落总数测定
(6)GB 4789.3-2010 食品微生物学检验大肠菌群计数
(7)GB 4789.1-2010 食品安全国家标准食品微生物学检验总则(8)
10、GB 1886.37-2015 食品添加剂环己基氨基磺酸钠(又名甜蜜素)
11、GB_T 5538-2005 动植物油脂过氧化值测定。
GB沙门氏菌检验

沙门氏菌(Salmonella)的检验
• 沙门氏菌:革兰氏阴性肠道杆菌 • 导致胃肠炎、伤寒和副伤寒。 • 蛋、家禽和肉类产品是沙门氏菌病的主要传播媒介。
2
《GB 4789.4-2010 食品微生物学检验 沙门氏菌检验》-1
3
《GB/T4789.4-2010 食品微生物学检验 沙门氏菌检验》-2
Nutrient Agar
BactiDrop™ Kovacs Indol RapID™ ONE system
靛基质试剂 Indole reagent
R21522
R8311006
商品化的生化鉴定系统
6
结果观察
BS琼脂
• 产硫化氢菌落为黑色有金属光泽、 棕褐色或灰色,菌落周围培养基可呈 黑色或棕色; • 有些菌株不产生硫化氢,形成灰绿 色的菌落,周围培养基不变。
2 days
18
11
How Inhibigens™ Work
The L-AEP Inhibigen
Inhibigen
Substrate (L-alanine) Inhibitor component L-AEP
Uptake via peptide permease
-
X
Free inhibitor in medium is not actively taken up
该方法通过AFNOR(法国标准化协会)的验 证(UNI 03/06 – 12/07),依照 ISO16140:2003,与ISO 6579:2002的方法 具有等效的结果
17
Precis 沙门氏菌快速培养检测法
增菌 沙门氏菌ONE肉汤
平板分离 Brilliance™ 沙门氏菌显色培养基
沙门氏菌检验详细流程

新的血清型名称的批准必须有巴斯德研究所、德国汉 堡卫生研究所及美国CDC 3个实验室的一致同意。
精品课件
沙门氏菌检验程序
精品课件
前增菌
目的:修复损伤的细菌细胞; 方法:25 g(mL)样品+225 mL BPW的无菌均
57个O抗原 116个H抗原 Vi抗原
被分成2500多个血清型 。
Vi抗原 O抗原 H抗原
精品课件
沙门氏菌命名与书写方式
目前的命名方法规定:
肠道沙门菌肠道亚种(亚种Ⅰ)给予专用名,并采用 标本分离地址的地名。菌名的第一个字母需大写,且 亚种Ⅰ的所用菌名不能用斜体。例如:肠道沙门菌鼠 伤寒血清型应书写为Salmonella enterica subsp.enterica serotype Typhimurium,但在实际工 作中,可简写为S. Typhimurium。
精品课件
血清学鉴定时的注意要点:
做血清凝集时,同时应用生理盐水做对照。 O血清不凝集时,可将菌株转接于琼脂量较高(如
2.5%-3%)的斜面上,再做凝集。 如果由于Vi抗原的存在而阻止了O抗原的凝集反应
时,应挑取菌苔于1mL生理盐水中做成菌悬液。煮 沸后再检查。(常见于伤寒沙门菌)。 有极少数的二相沙门菌会同时出现2相H抗原,也 有一些沙门氏菌在培养过程中H抗原会出现第1项 和第2项之间的转变,所以血清诱导实验要用新鲜 的培养物进行诱导。
GB 4789.4-2010 食品安全国家标准 食品微生物学检验 沙门氏菌检验
精品课件
沙门菌概况
沙门菌是1885年由Salmon氏等在猪霍乱流行 时,分离出的猪霍乱沙门菌,由于Salmon氏 对本属细菌的发现贡献卓越,故定名为沙门 菌属。
沙门氏菌的检验

沙门氏菌的检验食品学院14食品质量与安全1班文敏柳基炜卫杰恒温紫君5 6 1 2摘要:本实验采用GB/T4789.4-2010的检测方法测定鸡场中的沙门氏菌。
通过本实验学习沙门氏菌的检测方法和技术,了解沙门氏菌的一些生化特性;本实验先用显色培养基找出可疑菌落,再做生化试验找出可疑的典型性的沙门氏菌,再通过血清学试验最终确定是否为沙门氏菌属。
关键词:沙门氏菌接种生化试验血清学鉴定前言沙门氏菌病是公共卫生学中具有重要意义的人畜共患病种之一,其病原沙门氏菌属于肠道细菌科。
沙门氏菌是一个统称,泛指 2000 多种有紧密连系的细菌,包括引起食物中毒,导致胃肠炎、伤寒和副伤寒的细菌。
虽然只有少数人因沙门氏菌而患病,但是,在世界围的细菌性食物中毒事件中,由沙门氏菌引起的占大多数。
因此,采用科学、合理的方法检验食品中沙门氏菌,已经成为了人们最关心的问题之一[1]。
国标法(GB4789.4-2010)是目前中国规定的食品中沙门氏菌的标准检测方法,也是基层实验室普遍采用的检测方法,它根据沙门氏菌的生长特点和生化特性,采取前增菌、增菌、分离、生化试验和血清学鉴定5个步骤进行[2]。
1材料与方法1.1实验材料1.1.1仪器设备均质器、三角烧瓶、平皿、玻璃棒、接种棒恒温培养箱:36℃±1℃,42℃±1℃吸管:1 mL(具 0.01 mL刻度)、10mL(具0.1mL刻度或微量移液器及吸头电子天平PL602-S,梅特勒-托利多仪器();手提式不锈钢压力蒸汽灭菌锅SYQ-DSX-280B,申安医疗器械厂1.1.2试剂药品鸡肠、靛基质试剂、沙门氏菌O和H诊断血清、API20E生化试剂盒或VITEKGNI 生化鉴定卡1.1.3培养基蛋白胨水(BPW)、四硫磺酸钠煌绿(TTB)、亚硒酸盐胱氨酸(SC)增菌液、亚硫酸铋(BS)琼脂、HE琼脂、三糖铁琼脂、蛋白胨水、尿素琼脂、氰化钾、氰化钾对照、赖氨酸脱羧酶、赖氨酸脱羧酶对照、甘露醇、山梨醇、β-D半乳糖苷(ONPG)培养基1.2 实验方法1.2.1培养基的制备1.2.1.1培养基的配制步骤蛋白胨水(BPW):称取蛋白胨10g、氯化钠5g、磷酸氢二钠9g、磷酸二氢钠1.5g、蒸馏水1000ml,将各成分加入蒸馏水中,搅混均匀,静置约 10 min,煮沸溶解,调节 pH,高压灭菌 121 ℃,15 min。
微生物学检验标准-4789

食品卫生微生物学检验标准-4789名称∙12/08GB 4789.9-2014 食品安全国家标准食品微生物学检验空肠弯曲菌检验∙12/08GB 4789.11-2014 食品安全国家标准食品微生物学检验β型溶血性链球菌检验∙12/08GB 4789.14-2014 食品安全国家标准食品微生物学检验蜡样芽胞杆菌检验∙12/13GB 4789.7-2013 食品安全国家标准食品微生物学检验副溶血性弧菌检验∙12/13GB 4789.26-2013 食品安全国家标准食品微生物学检验商业无菌检验∙12/13GB 4789.28-2013 食品安全国家标准食品微生物学检验培养基和试剂的质量要求∙12/13GB 4789.31-2013 食品安全国家标准食品微生物学检验沙门氏菌、志贺氏菌和致泻大肠埃希氏菌的肠杆菌科噬菌体诊断检验∙12/13GB 4789.39-2013 食品安全国家标准食品微生物学检验粪大肠菌群计数∙06/12GB 4789.38-2012 食品安全国家标准食品微生物学检验大肠埃希氏菌计数∙06/12GB 4789.34-2012 食品安全国家标准食品微生物学检验双歧杆菌的鉴定∙06/12GB 4789.13-2012 食品安全国家标准食品微生物学检验产气荚膜梭菌检验∙06/12GB 4789.5-2012 食品安全国家标准食品微生物学检验志贺氏菌检验∙06/11现行有效的4789系列食品微生物学检验标准汇编(2012年7月更新)∙04/23食品安全国家标准食品微生物学检验标准汇编 GB4789系列(2010版,已根据卫生部2010年5月26日的勘误公告进行更新)∙04/22GB 4789.40-2010 食品安全国家标准食品微生物学检验阪崎肠杆菌检验∙04/22GB 4789.35-2010 食品安全国家标准食品微生物学检验乳酸菌检验∙04/22GB 4789.30-2010 食品安全国家标准食品微生物学检验单核细胞增生李斯特氏菌检验∙04/22GB 4789.18-2010 食品安全国家标准食品微生物学检验乳与乳制品检验∙04/22GB 4789.15-2010 食品安全国家标准食品微生物学检验霉菌和酵母计数∙04/22GB 4789.10-2010 食品安全国家标准食品微生物学检验金黄色葡萄球菌检验∙04/22GB 4789.4-2010 食品安全国家标准食品微生物学检验沙门氏菌检验∙04/22GB 4789.3-2010 食品安全国家标准食品微生物学检验大肠菌群计数∙04/22GB 4789.2-2010 食品安全国家标准食品微生物学检验菌落总数测定∙04/22GB 4789.1-2010 食品安全国家标准食品微生物学检验总则∙03/19GB/T 4789.39-2008 食品卫生微生物学检验粪大肠菌群计数∙03/19GB/T 4789.38-2008 食品卫生微生物学检验大肠杆菌计数∙03/19GB/T 4789.34-2008 食品卫生微生物学检验双歧杆菌检验∙03/19GB/T 4789.30-2008 食品卫生微生物学检验单核细胞增生李斯特氏菌检验∙03/19GB/T 4789.27-2008 食品卫生微生物学检验鲜乳中抗生素残留检验∙03/19GB/T 4789.10-2008 食品卫生微生物学检验金黄色葡萄球菌检验∙03/19GB/T 4789.9-2008 食品卫生微生物学检验空肠弯曲菌检验∙03/19GB/T 4789.8-2008 食品卫生微生物学检验小肠结肠炎耶尔森氏菌检验∙03/19GB/T 4789.2-2008 食品卫生微生物学检验菌落总数测定∙03/19GB/T 4789.1-2008 食品卫生微生物学检验总则∙09/28GB/T 4789.36-2008 食品卫生微生物学检验大肠埃希氏菌O157:H7/NM检验∙09/28GB/T 4789.4-2008 食品卫生微生物学检验沙门氏菌检验∙09/24GB/T 4789.7-2008 食品卫生微生物学检验副溶血性弧菌检验∙04/11食品卫生微生物学检验标准汇编 GB/T4789系列(2003-2008版)∙04/07GB/T 4789.3-2003 食品卫生微生物学检验大肠菌群测定∙06/21GB/T 4789.32-2002 食品卫生微生物学检验大肠菌群的快速检测∙05/09GB/T 4789.33-2003 食品卫生微生物学检验粮谷、果蔬类食品检验∙05/09GB/T 4789.31-2003 食品卫生微生物学检验沙门氏菌、志贺氏菌和致泻大肠埃希氏菌的肠杆菌科噬体检验方法∙05/09GB/T 4789.30-2003 食品卫生微生物学检验单核细胞增生李斯特氏菌检验∙05/09GB/T 4789.29-2003 食品卫生微生物学检验椰毒假单胞菌酵米面亚种检验∙05/09GB/T 4789.28-2003 食品卫生微生物学检验染色法、培养基和试剂∙05/09GB/T 4789.27-2003 食品卫生微生物学检验鲜乳中抗生素残留量检验∙05/09GB/T 4789.16-2003 食品卫生微生物学检验常见产毒霉菌的鉴定∙05/09GB/T 4789.26-2003 食品卫生微生物学检验罐头食品商业无菌的检验∙05/09GB/T 4789.25-2003 食品卫生微生物学检验酒类检验∙05/09GB/T 4789.24-2003 食品卫生微生物学检验糖果、糕点、蜜饯检验∙05/09GB/T 4789.23-2003 食品卫生微生物学检验冷食菜、豆制品检验∙05/09GB/T 4789.22-2003 食品卫生微生物学检验调味品检验∙05/09GB/T 4789.21-2003 食品卫生微生物学检验冷冻饮品、饮料检验∙05/09GB/T 4789.20-2003 食品卫生微生物学检验水产食品检验∙05/09GB/T 4789.19-2003 食品卫生微生物学检验蛋与蛋制品检验∙05/09GB/T 4789.18-2003 食品卫生微生物学检验乳与乳制品检验∙05/09GB/T 4789.17-2003 食品卫生微生物学检验肉与肉制品检验∙05/09GB/T 4789.15-2003 食品卫生微生物学检验霉菌和酵母计数∙05/09GB/T 4789.14-2003 食品卫生微生物学检验蜡样芽胞杆菌检验∙05/09GB/T 4789.13-2003 食品卫生微生物学检验产气荚膜梭菌检验∙05/09GB/T 4789.12-2003 食品卫生微生物学检验肉毒梭菌及肉毒毒素检验∙05/09GB/T 4789.11-2003 食品卫生微生物学检验溶血性链球菌检验∙05/09GB/T 4789.10-2003 食品卫生微生物学检验金黄色葡萄球菌检验∙05/08GB/T 4789.4-2003 食品卫生微生物学检验沙门氏菌检验∙05/08GB/T 4789.2-2003 食品卫生微生物学检验菌落总数测定∙05/08GB/T 4789.1-2003 食品卫生微生物学检验总则∙05/08GB/T 4789.9-2003 食品卫生微生物学检验空肠弯曲菌检验∙05/08GB/T 4789.7-2003 食品卫生微生物学检验副溶血性弧菌检验∙05/08GB/T 4789.6-2003 食品卫生微生物学检验致泻大肠埃希氏菌检验∙05/08GB/T 4789.5-2003 食品卫生微生物学检验志贺氏菌检验。
沙门氏菌检验PPTGB4789.4-2016 -JW

BS琼脂:某些非典型菌株产生绿色菌落, 其周围培养基稍微或不呈暗色。如果BS平 板培养24±2小时后,没有出现典型菌落, 则不挑取任何菌落,让平板继续培养24±2 小时。如果经48±2小时培养后,仍没有典 型或可疑的菌落出现,则挑取2个或更多个 非典型的菌落。
38
赖氨酸脱羧酶试验
赖氨酸脱羧酶试验培养基:蛋白胨、酵母浸 膏、葡萄糖、溴麝香草酚蓝(紫)。 原理:细菌使氨基酸脱羧,产生胺类,使培 养基变碱,颜色不改变。 沙门菌的反应:阳性。 意义:柠檬酸杆菌、志贺菌 均为阴 性;埃 希氏菌不定。
亚硫酸铋琼脂(BS):含有煌绿、亚硫酸铋能抑制大 肠杆菌、变形杆菌和革兰氏阳性菌的生长,但对伤寒、 副伤寒等沙门菌的生长无影响。伤寒杆菌及其他沙门 菌能利用葡萄糖将亚硫酸铋还原成硫酸铋,形成黑色 菌落周围绕有黑色和棕色的环,对光观察可见有金属 光泽。该培养基制备过程不宜过分加热,以免降低其 选择性,应在临用时配制,超过48h不宜使用。陆桥 的说明书要求提前一天配置?
11
四硫磺酸钠煌绿增菌液(TTB):含有胆盐, 抑制革兰氏阳性球菌和部分大肠埃希氏菌 的生长,而伤寒与副伤寒沙门氏菌仍生长
亚硒酸盐胱氨酸增菌液(SC):可对伤寒 及其他沙门氏菌作选择性增菌,亚硒酸与 蛋白胨中的含硫氨基酸结合,形成亚硒酸 和硫的复合物,影响细菌硫代谢,从而抑 制大肠埃希氏菌、肠球菌和变形杆菌的增 殖。
注:此培养基在制作过程中过分加热可使培养基的选择性降 低,与TTB或SC合用可获得更高的检出率。
35
沙门菌的分离培养基
XLD琼脂:培养基中含有去氧胆酸钠作指示剂, 在该浓度下的去氧胆酸钠也同时作为大肠埃 希氏菌的抑制剂 ,而不影响沙门菌属和志贺 菌属的生长。
XLD培养基分离沙门菌和志贺菌的敏感性超过 了传统的培养基,如:EMB、SS、BS。因这些 培养基尚有抑制志贺菌属生长的潜在因素, 故本培养基是分离鉴定沙门菌及志贺菌属的 可靠培养基。在国外广泛使用。
食品微生物检验标准

(五)即食豆类制品。GB29921中的即食豆类制品包括发酵豆 制品和非发酵豆制品。即食发酵豆制品包括腐乳、豆豉、纳豆和其 他湿法生产的发酵豆制品。即食非发酵豆制品包括豆浆、豆腐、豆 腐干(含豆干再制品)、大豆蛋白类和其他湿法生产的非发酵豆制 品,也包括各种熟制豆制品。
+
(六)巧克力类及可可制品。GB29921中的巧克力类及可可制品包 括巧克力类(包括巧克力及其制品、代可可脂巧克力及其制品、相 应的酱、馅)、可可制品(包括可可液块、可可饼块、可可粉)。 GB29921未对作为原料的各种可可脂进行致病菌限量规定。 (七)即食果蔬制品。GB29921中的即食水果制品指以水果为 原料,按照一定工艺加工制成的即食水果制品,包括冷冻水果、水果 干类、醋/油或盐渍水果、果酱、果泥、蜜饯凉果、水果甜品、发酵 的水果制品及其他加工的即食鲜果制品。即食蔬菜制品指以蔬菜为 原料,按照一定工艺加工制成的即食蔬菜制品,包括冷冻蔬菜、干制 蔬菜、腌渍蔬菜、蔬菜泥/酱(番茄沙司除外)、发酵蔬菜制品及其 他加工的即食新鲜蔬菜制品。 (八)饮料(包装饮用水、碳酸饮料除外)。GB29921中的饮 料包括果蔬汁类、蛋白饮料类、水基调味饮料类、茶、咖啡、植物 饮料类、固体饮料类、其他饮料类等(不包括饮用水和碳酸饮料)。
非预包装食品的生产经营者应当严格生产经营过程卫生管理, 尽可能降低致病菌污染风险。
罐头食品应达到商业无菌要求,不适用于本标准。
+
五、标准适用的主要食品类别 (一)肉制品。GB29921中的肉制品包括熟肉制品和即食生肉制品。 熟肉制品指以猪、牛、羊、鸡、兔、狗等畜、禽肉为主要原料,经酱、卤、 熏、烤、腌、蒸、煮等任何一种或多种加工方法制成的直接可食的肉类加工 制品。即食生肉制品指以畜、禽等肉为主要原料经发酵或特殊工艺加工制成 的直接可食的生肉制品。 (二)水产制品。GB29921中的水产制品包括熟制水产品、即食生制 水产品和即食藻类制品。熟制水产品指以鱼类、甲壳类、贝类、软体类、棘 皮类等动物性水产品为主要原料,经蒸、煮、烘烤、油炸等加热熟制过程制 成的直接食用的水产加工制品。即食生制水产品指食用前经洁净加工而不经 过加热或加热不彻底可直接食用的生制水产品,包括活、鲜、冷冻鱼(鱼片)、 虾、头足类及活蟹、活贝等,也包括以活泥螺、活蟹、活贝、鱼籽等为原料, 采用盐渍或糟、醉加工制成的可直接食用的腌制水产品。即食藻类制品指以 藻类为原料,按照一定工艺加工制成的可直接食用的藻类制品,包括经水煮、 油炸或其他加工藻类。
新实施:GB 4789.4-2024沙门氏菌——的预增菌变化

新实施:GB 4789.4-2024沙门氏菌——的预增菌变化G B4789.420242024年3月,国家卫健委、市场监管总局联合发布了47项食品安全国家标准和6项修改单,其中包含《食品安全国家标准食品微生物学检验沙门氏菌检验》(G B 4789.4-2024)检验方法标准。
这一新标准对实验设备、材料和试剂、检验程序与操作步骤进行了修改,并将于2024年8月8日实施。
本文就该标准主要修订内容、操作注意事项进行解读。
主要变化及原因分析变化1:在“预增菌”步骤中新增了在检验乳粉样品时,须将样品倒入225m L B P W 培养基表面,静置60m i n后再进行预增菌。
乳粉类样品经过高温喷雾干燥,其中的沙门氏菌大多处于受损状态;乳粉相对干燥且水活度低,其中受损的沙门氏菌适应了干燥的环境。
在这种情况下,如果受损的沙门氏菌在B P W中快速混匀水化,受损的沙门氏菌会出现渗透压休克;采用浸泡法在室温条件下静置一段时间后再进行预增菌,可以促进受损沙门氏菌的复苏,提高检出率。
变化2:选择性增菌培养基由氯化镁孔雀绿大豆胨(R V S)增菌液代替亚硒酸盐胱氨酸(S C)增菌液,并且B P W接种量改为0.1m L到10m L R V S中,选择性增菌温度为42℃±1℃。
S C增菌液主要适用于伤寒沙门氏菌的选择性增菌,但通过近几年疾病监测发现,我国伤寒、副伤寒沙门氏菌的发病率从10例/10万下降到0.8例/10万左右,而非伤寒沙门氏菌近年来发病率达到560例/10万,在微生物引发的食源性疾病中排前2位。
从培养基成分上看,R V S中含有孔雀绿,能够抑制非沙门氏菌的生长,大豆蛋白胨有利于沙门氏菌的复苏;S C增菌液配置需要的亚硒酸氢钠具有一定毒性,在健康环保方面也存在安全风险,且原料不稳定,过度加热培养基容易变性导致功能失效。
变化3:T T B四硫磺酸钠煌绿增菌液(T T B)选择性增菌改为:低背景菌培养温度为36℃±1℃,高背景菌培养温度为42℃±1℃。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
食品微生物学检验 沙门氏菌检验GB GB 4789.44789.44789.4-20-20-201010北京陆桥技术有限责任北京陆桥技术有限责任公司公司技术服务电话:010-******** 销售服务电话:010-********技术部邮箱:luqiaotech@www. beijinglandbridge .com北京陆桥技术有限责任公司目 录�沙门氏菌简介�2010版国标主要修订内容�沙门氏菌的检验步骤及注意事项�沙门氏菌检验过程中的常见问题www. beijinglandbridge .com 北京陆桥技术有限责任公司沙门氏菌简介�沙门氏菌属沙门氏菌属:肠杆菌科:肠杆菌科�沙门氏菌能引起胃肠炎、伤寒、败血症等人类疾病,严重时能导致死亡。
�种类繁多,抗原结构复杂,种类繁多,抗原结构复杂,在在《ANTIGENIC FORMULAE OF THE SALMONELLA SEROVARS FORMULAE OF THE SALMONELLA SEROVARS》》(2007 9th edition)(2007 9th edition)中已公布了中已公布了2579个血清型个血清型。
�食物是人类感染沙门氏菌的主要途径。
www. beijinglandbridge .com 北京陆桥技术有限责任公司�形态特征:形态特征:革兰氏阴性革兰氏阴性革兰氏阴性、、两端钝圆短杆菌两端钝圆短杆菌,,无芽孢无芽孢,,一般无荚膜,除鸡沙门氏菌一般无荚膜,除鸡沙门氏菌和和雏沙门氏菌外,都有周身鞭毛,运动力强�培养特性:需氧或兼性厌氧,10℃~42℃都可生长,最适生长温度为37℃,最适pH 为6.8~7.8�革兰氏阴性、需氧或兼性厌氧无芽孢杆菌沙门氏菌简介:生物学特征www. beijinglandbridge .com 北京陆桥技术有限责任公司�修改了标准的中英文名称�修改了标准的范围�修改了培养基和试剂;�修改了设备和材料;�修改了附录修改了附录A A (规范性附录)培养基和试剂2010版国标主要修订内容www. beijinglandbridge .com 北京陆桥技术有限责任公司——关于培养基和试剂的修订说明�修改了修改了HE HE HE琼脂和三糖铁琼脂的配方。
琼脂和三糖铁琼脂的配方。
�删除了删除了080808版国标中一些培养基、试剂盒及设备版国标中一些培养基、试剂盒及设备的商品名,如科玛嘉,的商品名,如科玛嘉,VITEK VITEK VITEK等。
等。
2010版国标主要修订内容我们的产品均按20102010版国标要求的版国标要求的配方生产GB 4789.4-2010检验流程7www. beijinglandbridge .com 北京陆桥技术有限责任公司�称取称取25g 25g 25g((mL mL)样品于盛有)样品于盛有)样品于盛有225mL BPW 225mL BPW 225mL BPW的无菌均质杯中,以的无菌均质杯中,以80008000~~10000r/min 10000r/min均质均质均质1min 1min 1min~~2min 2min,或置于盛有,或置于盛有,或置于盛有225mLBPW 225mLBPW 225mLBPW的的无菌均质袋中,用拍击式均质器拍打无菌均质袋中,用拍击式均质器拍打1min 1min 1min~~2min 2min。
若样品为。
若样品为液态,不需要均质,振荡混匀即可。
�如需测定如需测定pH pH pH值,用值,用值,用1mol/L 1mol/L 1mol/L无菌无菌无菌NaOH NaOH NaOH或或HCl HCl调调pH pH至至6.86.8±±0.20.2。
�无菌操作将样品转至无菌操作将样品转至500mL 500mL 500mL锥形瓶中,如使用均质袋,可直接锥形瓶中,如使用均质袋,可直接培养,培养,363636℃±℃±℃±11℃培养培养8h 8h 8h~~18h 18h。
检验步骤及注意事项:前增菌www. beijinglandbridge .com 北京陆桥技术有限责任公司�任何样品均需进行前增菌。
�缓冲蛋白胨水(缓冲蛋白胨水(BPW BPW BPW):不含任何抑菌成分,有利于受损):不含任何抑菌成分,有利于受损沙门氏菌的复苏,使受损伤细胞恢复到稳定的生理状态。
�冷冻样品解冻:冷冻样品解冻:454545℃℃以下不超过以下不超过15min 15min 15min,或,或,或22℃-5-5℃℃不超过18h 18h。
�建议采用拍击式均质的方式,更为便利,且节省培养空间。
检验步骤及注意事项:前增菌√www. beijinglandbridge .com 北京陆桥技术有限责任公司�轻轻摇动培养过的样品混合物,移取轻轻摇动培养过的样品混合物,移取1mL 1mL 1mL,转种于,转种于,转种于10mL10mL TTB TTB内,于内,于内,于424242℃±℃±℃±11℃培养培养18h 18h 18h~~24h 24h。
同时另取。
同时另取。
同时另取1mL 1mL 1mL转种转种于10mL SC 10mL SC内,于内,于内,于363636℃±℃±℃±11℃培养培养18h 18h 18h~~24h 24h。
�TTBTTB和和SC SC两种选择性增菌肉汤必须同时使用两种选择性增菌肉汤必须同时使用两种选择性增菌肉汤必须同时使用((注意区分增菌培养温度增菌培养温度)。
)。
�SCSC:如果干粉或溶液变红,则不能使用。
:如果干粉或溶液变红,则不能使用。
:如果干粉或溶液变红,则不能使用。
开封后建议用开封后建议用封口膜密封后冷藏保存封口膜密封后冷藏保存,,可延缓变质可延缓变质。
检验步骤及注意事项:选择性增菌www. beijinglandbridge .com 北京陆桥技术有限责任公司�分别用接种环取增菌液分别用接种环取增菌液11环,划线接种于一个环,划线接种于一个BS BS BS琼脂平琼脂平板和一个板和一个XLD XLD XLD琼脂平板(或琼脂平板(或琼脂平板(或HE HE HE琼脂平板或沙门氏菌显色琼脂平板或沙门氏菌显色培养基平板),于培养基平板),于363636℃±℃±℃±11℃分别培养分别培养18h 18h 18h~~24h 24h((XLD XLD、、HE HE、显色培养基)或、显色培养基)或、显色培养基)或40h 40h 40h~~48h 48h((BS BS琼脂平板)琼脂平板)�为了最大可能的检出沙门氏菌,必须使用两种或以上选择性分离培养基检验步骤及注意事项:选择性分离www. beijinglandbridge .com 北京陆桥技术有限责任公司生长抑制粪链球菌棕色至绿色大肠埃希氏菌棕色至绿色弗氏志贺氏菌黑色菌落有金属光泽鼠伤寒沙门氏菌菌落特征菌 名�使用使用注意事项注意事项注意事项::不可过度加热;不可过度加热;使用前一天配制,且在使用前一天配制,且在48h 内使用;内使用;倾注平板前需摇匀;不能反复溶解倾注平板前需摇匀;不能反复溶解倾注平板前需摇匀;不能反复溶解;平板需避;平板需避;平板需避光光保存于室温环境检验步骤及注意事项:选择性分离亚硫酸铋琼脂亚硫酸铋琼脂BSBSwww. beijinglandbridge .com北京陆桥技术有限责任公司�使用注意事项:使用前一天配制,避免过度加热!室温避光储存�该培养基对沙门和志贺氏菌的灵敏度均较高,在国外应用广泛粉红色菌落,有黑心鼠伤寒沙门氏菌生长抑制金黄色葡萄球菌粉红色菌落,无黑心弗氏志贺氏菌黄色菌落,有胆酸盐沉淀大肠埃希氏菌粉红色菌落,无黑心甲型副伤寒沙门氏菌菌落特征菌 名检验步骤及注意事项:选择性分离XLD XLD琼脂琼脂www. beijinglandbridge .com北京陆桥技术有限责任公司�使用注意事项:避免过度加热!黄色菌落,有胆酸盐沉淀大肠埃希氏菌生长抑制金黄色葡萄球菌蓝绿色菌落,无黑心福氏志贺氏菌蓝绿色菌落,有黑心鼠伤寒沙门氏菌菌落特征质控菌株名称检验步骤及注意事项:选择性分离HE HE琼脂琼脂www. beijinglandbridge .com 北京陆桥技术有限责任公司�原理原理::特异性酶与底物特异性酶与底物的的显色反应。
�与传统培养基相比的优势与传统培养基相比的优势::甲型甲型副伤寒副伤寒副伤寒、伤寒、伤寒、伤寒等不产或弱产等不产或弱产等不产或弱产HH 2S 的沙门氏菌在传统培养基上门氏菌在传统培养基上易易漏检;奇异变形杆菌等产漏检;奇异变形杆菌等产HH 2S 的非沙门氏菌在传统培养基上假阳性率很高,会增加后期生化鉴定的工作量。
在传统培养基上假阳性率很高,会增加后期生化鉴定的工作量。
而而使用显色培养基则不存在这些问题使用显色培养基则不存在这些问题。
�沙门氏菌沙门氏菌::紫红色菌落�非沙门氏菌:蓝绿色、无色非沙门氏菌:蓝绿色、无色或抑制或抑制检验步骤及注意事项:选择性分离陆桥陆桥ESM ESM ESM沙门氏菌显色培养基沙门氏菌显色培养基检验步骤及注意事项:选择性分离�沙门氏菌种类复杂,在分离培养基上的菌落形态不唯一�凡是符合表凡是符合表11描述的典型菌落及可疑菌落均需进行后期生化鉴定(科玛嘉、陆桥显色平板上沙门氏菌显现紫红色菌落)www. beijinglandbridge .com北京陆桥技术有限责任公司www. beijinglandbridge .com 北京陆桥技术有限责任公司检验步骤及注意事项:生化鉴定�自分离平板上分别挑取自分离平板上分别挑取22个以上典型或可疑菌落,接种三糖铁琼脂(先在斜面划线,再于底层穿刺)、赖氨酸脱羧酶试验培养基和营养琼脂平板(穿刺脂平板(穿刺TSI TSI TSI后不要烧针,直接接种后两者),于后不要烧针,直接接种后两者),于后不要烧针,直接接种后两者),于3636℃±1℃培养18h 18h~~24h 24h,必要时可延长至,必要时可延长至,必要时可延长至48h 48h 48h。
�结合结合TSI TSI TSI琼脂和赖氨酸脱羧酶试验培养基的结果,可筛掉大部分非沙琼脂和赖氨酸脱羧酶试验培养基的结果,可筛掉大部分非沙门氏菌www. beijinglandbridge .com 北京陆桥技术有限责任公司检验步骤及注意事项:生化鉴定�可以在接种三糖铁琼脂和赖氨酸脱羧酶试验培养基的同时可以在接种三糖铁琼脂和赖氨酸脱羧酶试验培养基的同时,,直接接种蛋白胨水、尿素琼脂、氰化钾(蛋白胨水、尿素琼脂、氰化钾(KCN KCN KCN)培养基;也可在初步判断结果后)培养基;也可在初步判断结果后从营养琼脂平板上挑取可疑菌落再接种这三项。
