第2章 药物合成反应 第三版 课后答案 闻韧
《药物合成反应》闻韧主编第二章烃化反应-知识点总结

#2.10打卡# 李骅轩完成学习目标烃化反应定义:用烃基取代有机分子中的某些功能基上的氢原子得到烃化产物的反应都称为烃化反应。
烃基:饱和、不饱和、脂肪、芳香分类1)按被烃化物不同C-OH(醇或酚羟基)变为-OR醚;C-N(NH3) 变为伯、仲、叔胺;C-C2)按烃化剂的种类分类卤代烷:RX 最常用;硫酸酯、磺酸酯;醇;烯烃;环氧烃:发生羟乙基化;CH2N2:很好的重氮化试剂3)按反应历程分类:SN1 SN2 亲电取代一醇的O-烃化1 卤代烷为烃化剂2 磺酸酯3 环氧乙烷类作烃化剂4 烯烃作为烃化剂5 醇作为烃化剂6 其它烃化剂二酚的O-烃化1 烃化剂2 多元酚的选择性烃化一醇的O-烃化1 卤代烷为烃化剂在碱的条件下与卤代烷生成醚:SN1伯卤代烷RCH2X按SN2历程;随着与X相连的C的取代基数目的增加越趋向SN1。
影响因素 a RX的影响ii)活性:RI>RBr>RCl>RFb 醇的影响苯海拉明合成可采用的两种方法。
可以看到,由于醇羟基氢原子的活性不同,进行烃化反应时所需的条件也不同。
前一反应醇的活性低,要先制成醇钠;而二苯甲醇中,由于苯基的吸电子效应,羟基中氢原子的活性增大,在反应中加入氢氧化钠作除酸剂即可。
显然后一反应优于前一反应,因此苯海拉明的合成采用了后一种方式c催化剂的影响催化剂:醇钠、Na、NaH、NaOH、KOH有机碱:六甲基磷酰胺(HMPA)、N,N-二甲基苯胺(DMA)有些有旋光活性的醇,如果加金属钠制成醇钠,再与卤代烃反应,产物比较复杂,如用氢化钠,则可立体专一性地得到相应的甲醚。
d溶剂影响溶剂: 过量醇(既是反应物又是溶剂)非质子溶剂:苯、甲苯(Tol)、二甲苯(xylene)、DMF、DMSO无水条件下质子性溶剂:有助于R-CH2X 解离,但是与RO-易发生溶剂化,因此通常不用质子性溶剂。
副反应消除反应2 磺酸酯为烃化剂:主要指芳磺酸酯,引入较大的烃基3环氧乙烷类作烃化剂:反应机理:a 酸催化R为供电子基或苯,在a处断裂R'为吸电子基得b处断裂产物b 碱催化SN2 双分子亲核取代,开环单一,立体位阻原因为主,反应发生在取代较少的碳原子上。
药物合成反应习题及答案

药物合成反应习题及答案一、举例解释下列概念:1,官能团保护;为什么保护?当分子中有多个官能团,想在某一官能团进行转换反应,为了不使其他官能团影响反应,需对这些官能团进行衍生化,这就是官能团的保护。
达到反应目的后再还原这些官能团。
理想保护基:试剂易得、无毒,保护基稳定,引入和脱去反应选择性好,收率高。
2,相转移催化剂; 一种与水相中负离子结合的两性物质,可以把亲核试剂转移到有机相进行亲核反应。
相转移催化剂优点:克服溶剂化作用;不需无水操作;可用无机碱代替有机金属碱;降低反应温度。
3,重排反应;重排反应是指在同一分子内,某一原子或基团从一个原子迁移至另一原子而形成新分子的反应。
按反应机理可分为亲电重排、亲核重排、自由基重排和协同重排。
4,合成子;合成子:组成靶分子或中间体骨架的各个单元结构的活性形式.包括:离子合成子、自由基或周环反应所需的中性分子。
离子合成子:包括 d 合成子和a合成子d 合成子: 亲核性的离子合成子d---donor of electrond 合成子等价试剂a合成子:氧化性或亲电性的离子合成子a合成子:等价试剂5,协同反应协同反应:在反应过程中,若有两个或两个以上的化学键破裂和形成时,都必须相互协调地在同一步骤中完成。
6, 非均相催化氢化: 催化剂、反应物、试剂和氢供体在两项或多项中反应,催化剂自成一相,称为非均相催化氢化。
催化剂自成一相称为非均相催化剂如Pd/C为催化剂,氢气为氢供体,在反应液中还原双键的反应。
1) DMAP2) DMF3) DCC4) TBAF1) Aromatic Electrophilic Substitution; 芳香亲电取代2) Phase-transfer catalyst; 相转移催化剂3) Carbocations; 碳负离子4) trifluoroacetic anhydride.三氟乙酸酐Ryoji Noyori was awarded the Nobel Prize in 2001, What did he discover?Ryoji Noyori日本名古屋大学的野伊良治因在手性催化氢化反应方面做出了突出贡献而被授予2001年Nobel化学奖。
(完整word版)药物合成反应(闻韧_第三版)课后翻译(word文档良心出品)

1、About 216–224 g. (1.62–1.68 moles) of powdered anhydrous aluminum chloride is added to a 1Lthree-necked flask.在1L的三口烧瓶中加入大约216-224g(1.62–1.68 moles)的无水三氯化铝。
While the free-flowing catalyst is stirred (Note 3), 81 g. (0.67 mole) of acetophenone is added from the dropping funnel in a slow stream over a period of 20–30 minutes. 自由流动的催化剂边搅拌边用滴液漏斗缓慢滴加81g苯乙酰。
Considerable heat is evolved, and, if the drops of ketone are not dispersed, darkening or charring occurs. 放热反应,假如滴加的酮不能被分散,就会变黑或是碳化。
When about one-third of the acetophenone has been added, the mixture becomes a viscous ball-like mass that is difficult to stir.当三分之一的乙酰苯被滴加,反应混合物变成一个很难搅拌的粘性的球状团块。
Turning of the stirrer by hand or more rapid addition of ketone is necessary at this point. 在这时,改用手动搅拌或快速滴加酮是非常必要的。
The addition of ketone, however, should not be so rapid as to produce a temperature above 180°. 然而,速度不能太快,当反应温度超过180℃时。
闻韧版 药物合成反应 课后翻译

第六章
(1)、二吡啶三氧化铬
在一个干燥的装有密封机械搅拌器,温度计,和干燥管的1L的三颈烧瓶里面装入500毫升无水吡啶,搅拌,用冰浴冷却到大约15°。干燥管是定期拿开,将68克(0.68摩尔)无水三氧化铬在一个30分钟内通过瓶颈分次加入。氧化铬应增加在这样的速度,温度不超过20°,并以这种方式,迅速与吡啶氧化物混合,不粘附瓶内。随着氧化铬的加入,一种深黄色的,絮状沉淀物从吡啶中分离出来,混合物的粘度增加。当添加完后,这混合物
第四章
(1)、 在配有回流冷凝器的3L圆底烧瓶中加入625ml的95%酒精、500ml水、500g(476ml,4,7mol)的苯甲醛和50g 96-98%的氰化钠。混合物加热并保持沸腾1.5小时。在20分钟后晶体开始从热溶液中析出。在最后的30分钟,冷却溶液,抽滤并用少量水洗涤有450-460g白色或亮黄色的干燥的安息香。理论产率90-92%。为了得到纯度高的产品,粗产品要在酒精中重结晶,90g粗品溶解在700ml沸腾的酒精中,冷却, 得到83g熔点为129摄氏度的白色安息香纯品。
合并二氯甲烷溶液_可用稀盐酸,碳酸氢钠溶液和水洗涤,或直接通过助滤剂过滤,或通过色谱柱去除吡啶铬盐_痕迹。去除二氯甲烷获得该产品;少量残余吡啶可通过减少压力下去除。
(3)庚醛
在一个干燥,1L的装有机械搅拌器的三颈烧瓶中加入650ml无水二氯甲烷。开始搅拌,在室温下加入77.5g二吡啶三氧化铬,再一次性加入5.8g 1-庚醇。搅拌20分钟后,倒出上层溶液从这不溶性棕色胶状物中,并用3个100ml乙醚冲洗。乙醚和二氯甲烷的溶液相结合,并先后用300毫升5%氢氧化钠的水,100毫升5%的盐酸(注12),两个100毫升部分饱和碳酸氢钠,并最后用100毫升饱和氯化钠水溶液冲洗。无水硫酸镁干燥有机层,并通过蒸馏去除溶剂。在残余油通过Claisen缩合____减压蒸馏分离4.0-4.8克。 (70-84%)的庚醛,B.P. 80-84°(65毫米),n25D1.4094
药物合成反应(闻韧_第三版)课后翻译

1、216-224g(1.62–1.68 moles)的无水三氯化铝。
While the free-flowing catalyst isfunnel in a slow stream over a period of 20–30 minutes. 自由流动的催化剂边搅拌边用滴液漏斗缓慢滴加81g苯乙酰。
Considerable heat is evolved, and, if the drops of ketone are not dispersed, darkening or charring occurs. 放热反应,假如滴加的酮不能被分散,mixture becomes a viscous ball-like mass that is difficult to stir.当三分之一的乙酰苯被滴加,反应混合物变成一个很难搅拌的粘性的球状团块。
Turning of the stirrer by hand or more rapid addition of ketone is necessary at this point. 在这时,改用手动搅拌或快速滴加酮是非常必要的。
The addition of ketone, however, should not be so rapid as to produce a temperature above 180°. 然而,速度不能太快,当反应温度超过180℃时。
Near the end of the addition, the mass becomes molten and can be stirred easily时,团块开始融化,表明苯乙酰已经和三氯化铝混合完全,颜色也逐渐从黄褐色变为棕色。
Bromine (128 g., 0.80 mole) is added dropwise to the well-stirred mixture over a period of 40 minutes (Note 4). 在40分钟内在搅拌下把溴缓慢滴加到混合物中。
最新《药物合成反应(闻韧主编第三版)》人名反应整理资料

《药物合成反应(闻韧主编第三版)》人名反应整理一、卤化反应1、Hunsdriecke反应(汉斯狄克反应):羧酸银盐和溴或碘反应,脱去二氧化碳,生成比原反应物少一个碳原子的卤代烃。
2、Sandmeyer反应(桑德迈尔反应):用氯化亚铜或溴化亚铜在相应的氢卤酸存在下,将芳香重氮盐转化成卤代芳烃。
3、Gattermann反应(加特曼反应):将Sandmeyer反应条件改为铜粉和氢卤酸。
4、Schiemann反应(席曼反应):将芳香重氮盐转化成不溶性的重氮氟硼酸盐或氟磷酸盐,或将芳胺直接用亚硝酸钠和氟硼酸进行重氮化,此重氦盐再经热分解(有时在氟化钠或铜盐存在下加热),就可以制得较好收率的氟代芳烃。
二、烃化反应5、Willamson合成(威廉姆森合成):醇在碱(钠,氢氧化钠,氢氧化钾等) 存在下与卤代烃反应生成醚的反应。
6、Gabriel合成(盖布瑞尔合成):将氨先制备成邻苯二甲酰亚胺,利用氮上氢的酸性,先与氢氧化钾形成钾盐,然后与卤代烃作用,得N-烃基邻苯二甲酰亚胺,肼解或酸水解即可得纯伯胺。
7、Delepine反应(德勒频反应):用卤代烃与环六亚甲基四胺(乌洛托品Methenamine)反应得季铵盐,然后水解可得伯胺。
8、Leuckart-Wallach反应(鲁卡特-瓦拉赫反应):用甲酸及其铵盐可以对醛酮进行还原烃化,得各类胺。
9、Ullmann反应(沃尔曼反应):卤代芳烃与芳香伯胺在铜或碘化铜及碳酸钾存在并加热的条件下可得二苯胺及其同系物。
三、酰化反应10、Friedel-Crafts反应(傅列德尔-克拉夫茨反应,也称傅-克酰基化反应):羧酸及羧酸衍生物在质子酸或Lewis酸的催化下,对芳烃进行亲电取代生成芳酮的反应。
11、Hoesch反应(赫施):腈类化合物与氯化氢在Lewis 酸催化剂ZnCl2的存在下与烃基或烷氧基取代的芳烃进行反应可生成相应的酮亚胺,再经水解则羟基或烷氧基取代的芳香酮。
12、Gattemann反应(伽特曼反应):将羟基或烷氧基取代的芳烃在AlCl3、ZnCl2催化下与氰化氢及氯化氢反应生成牙胺盐酸盐,再经水解生成相应芳香醛的反应。
《药物合成反应(闻韧主编第三版)》人名反应整理(新)

《药物合成反应(闻韧主编第三版)》人名反应整理一、卤化反应1、Hunsdriecke反应(汉斯狄克反应):羧酸银盐和溴或碘反应,脱去二氧化碳,生成比原反应物少一个碳原子的卤代烃。
☆☆☆☆☆2、Sandmeyer反应(桑德迈尔反应):用氯化亚铜或溴化亚铜在相应的氢卤酸存在下,将芳香重氮盐转化成卤代芳烃。
☆☆3、Gattermann反应(加特曼反应):将Sandmeyer反应条件改为铜粉和氢卤酸。
☆☆4、Schiemann反应(席曼反应):将芳香重氮盐转化成不溶性的重氮氟硼酸盐或氟磷酸盐,或直接将芳胺用亚硝酸钠和氟硼酸进行重氮化,此重氮盐再经热分解(有时在氟化钠或铜盐存在下加热),就可以制得较好收率的氟代芳烃。
☆二、烃化反应5、Willamson合成(威廉姆森合成):醇在碱(钠、氢氧化钠、氢氧化钾等)存在下与卤代烃反应生成醚的反应。
☆☆☆☆6、Gabriel合成(盖布瑞尔合成):将氨先制备成邻苯二甲酰亚胺,利用氮上氢的酸性,先与氢氧化钾形成钾盐,然后与卤代烃作用,得N-烃基邻苯二甲酰亚胺,再经过肼解或酸水解即可得纯伯胺。
☆☆☆☆☆7、Delepine反应(德勒频反应):用卤代烃与环六亚甲基四胺(乌洛托品Methenamine)反应得季铵盐,然后水解即可得伯胺。
8、Leuckart-Wallach反应(鲁卡特-瓦拉赫反应):用甲酸及其铵盐可对醛酮进行还原烃化,得各类胺。
☆9、Ullmann反应(沃尔曼反应):卤代芳烃与芳香伯胺在铜或碘化铜及碳酸钾存在并加热的条件下可得二苯胺及其同系物。
三、酰化反应10、Friedel-Crafts反应(傅列德尔-克拉夫茨反应,也称傅-克酰基化反应):羧酸及羧酸衍生物在质子酸或Lewis酸的催化下,对芳烃进行亲电取代生成芳酮的反应。
☆☆☆☆☆11、Hoesch反应(赫施反应):腈类化合物与氯化氢在Lewis酸催化剂ZnCl2等的存在下与烃基或烷氧基取代的芳烃进行反应可生成相应的酮亚胺,再经水解则得到羟基或烷氧基取代的芳香酮。
药物合成习题答案
C2H5ONa
(COOC2H5)2CH(CH2)6CH(COOC2H5)2 Na, NH3 PhCH3 (CH2)2 HO O O (CH2)2
C2H5OOC(CH2)8COOC2H5
O
O
②试由
O
OCH3 合成
。
OH 0.25 NaBH4 OCH3 H2O H+ OCH3
OH H+ O O
H COOEt CH2CH 2COOH
HO
2.完成下列合成过程 (1)
O CHO CN PCC NaOAc O O O NaOH H3O O O COOH OH
O
(2)
CH3 O CH2OH + CH3 CHO O OC2H5 O O CH3 Claisen
Cope O
CH3 CHO
H2, Pd-C O
CHO CH3
(3)
C2H5 CH3 OCH3 OCH3 C2H5 O CO2CH3 + H3CO2C CH3 CH3 Claisen Rearrangement OH 2,4-O2NC6H5OH Tol C2H5 CH3 CO2CH3 O
药物合成反应习题
参考答案
第一章 卤化反应
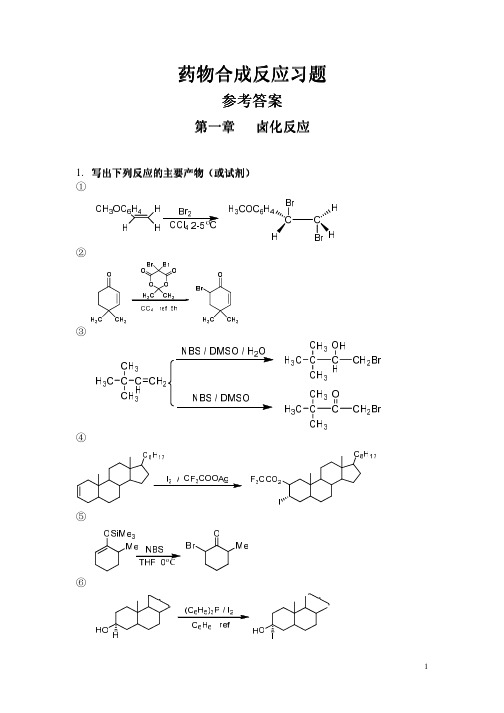
1. 写出下列反应的主要产物( 写出下列反应的主要产物(或试剂) 或试剂) ①
②
③
④
⑤
⑥
1
⑦
⑧
⑨
⑩
2.写出下列反应的可能产物
①
②
2
③
④
3.
①
写出下列反应的主要试剂及条件
②
③ቤተ መጻሕፍቲ ባይዱ
④
第二章 1.
① 完成下列反应
烃化反应
《药物合成反应》 闻韧主编,学习课件(第二章)

消除反应
B-
(H3C)3 CX
(H3C)3 C+
CH3
CH3 C CH2 CH3
C2H5 B B: (CH3)3COH + C2H5X
CH3
欲制备:
H3C C H3C A
O
A:
(CH3)3CX+C2H5OH
欲制备:
Ph Ph
CH
A
O B
CH2CH2N
CH3
A B
Ph Ph Ph Ph
CH-Br + HOCH2CH2 N
第二章 烃化反应
Hydrocarbylation Reaction
Organic Reactions for Drug Synthesis
定义:用烃基取代有机分子中的某些功能基上的氢原子得 到烃化产物的反应都称为烃化反应。 烃基: 饱和 、不饱和 、 脂肪 、芳香
分类 1)按被烃化物不同
被烃化物+烃化剂
Organic Reactions for Drug Synthesis
反应机理:b
碱催化
R'O R-CH-CH2
O O
R-CH-CH
OR'
RCHCH2OR'
O
R'OH RCHCH2OR' +
OH
R'O
SN2 双分子亲核取代,开环单一,立体位阻
原因为主,反应发生在取代较少的碳原子上
Organic Reactions for Drug Synthesis
影响因素 a RX的影响
i) 当R相同C-X极化度
活性
(∵卤素的电负性)
活性:RI>RBr>RCl>RF
药物合成反应(闻韧第三版)课后翻译

1、About 216–224 g. (1.62–1.68 moles) of powdered anhydrous aluminum chloride is added to a 1Lthree-necked flask.在1L的三口烧瓶中加入大约216-224g(1.62–1.68 moles)的无水三氯化铝。
While the free-flowing catalyst is stirred (Note 3), 81 g. (0.67 mole) of acetophenone is added from the dropping funnel in a slow stream over a period of 20–30 minutes. 自由流动的催化剂边搅拌边用滴液漏斗缓慢滴加81g苯乙酰。
Considerable heat is evolved, and, if the drops of ketone are not dispersed, darkening or charring occurs. 放热反应,假如滴加的酮不能被分散,就会变黑或是碳化。
When about one-third of the acetophenone has been added, the mixture becomes a viscous ball-like mass that is difficult to stir.当三分之一的乙酰苯被滴加,反应混合物变成一个很难搅拌的粘性的球状团块。
Turning of the stirrer by hand or more rapid addition of ketone is necessary at this point. 在这时,改用手动搅拌或快速滴加酮是非常必要的。
The addition of ketone, however, should not be so rapid as to produce a temperature above 180°. 然而,速度不能太快,当反应温度超过180℃时。
药物合成反应与设计翻译部分(优.选)

药物合成反应与设计翻译部分(第三版闻韧主编)第一章翻译:About 216–224 g. (1.62–1.68 moles) of powdered anhydrous aluminum chloride is added to a 1Lthree-necked flask.在1L的三口烧瓶中加入大约216-224g(1.62–1.68 moles)的无水三氯化铝。
While the free-flowing catalyst is stirred (Note 3), 81 g. (0.67 mole) of acetophenone is added from the dropping funnel in a slow stream over a period of 20–30 minutes. 自由流动的催化剂边搅拌边用滴液漏斗缓慢滴加81g苯乙酰。
Considerable heat is evolved, and, if the drops of ketone are not dispersed, darkening or charring occurs. 放热反应,假如滴加的酮不能被分散,就会变黑或是碳化。
When about one-third of the acetophenone has been added, the mixture becomes a viscous ball-like mass that is difficult to stir.当三分之一的乙酰苯被滴加,反应混合物变成一个很难搅拌的粘性的球状团块。
Turning of the stirrer by hand or more rapid addition of ketone is necessary at this point. 在这时,改用手动搅拌或快速滴加酮是非常必要的。
The addition of ketone, however, should not be so rapid as to produce a temperature above 180°. 然而,速度不能太快,当反应温度超过180℃时。
最新[工学]《药物合成反应》 学习课件第三章 闻韧主编ppt课件
![最新[工学]《药物合成反应》 学习课件第三章 闻韧主编ppt课件](https://img.taocdn.com/s3/m/dcc07bf2bcd126fff6050b1a.png)
H3C O H2C C C
OC3H+ C4H9OH H2SO4
H3C O H2C C C OC4H9
H2C H2C
O
C + CH3OHCH3ONa
O
O
H2C C OC3H CH2OH
O H3CO C
O
O
CH3ONa
O C CH3 + CH3OH 回流 H3CO C
O
OH+ H3C C OC3H
-酯交换完成某些特殊的合成
C H 2 - C - C H 2 C H 2 O HP h C O O H / T H F C H 3 C H C H 2 C H 2 O C O P h
O H
O H 部 分 选 择 酰 化
Organic Reactions for Drug Synthesis
例:镇痛药盐酸呱替啶的合成
H3CN
O H
△,
H
OH RCOH
H
O O
H
Organic Reactions for Drug Synthesis
(2)Lewis酸催化法: (AlCl3, SnCl4,FeCl3,BF3等)
A lC l3
O
A lC l3
O配 位 键 (增 加 C 的 正 电 性 )
RCO H
RCO H
CH=CH-COOH
(2)催化剂(降低活化能)
Organic Reactions for Drug Synthesis
催化剂
(1)质子酸催化法: 无机酸:浓硫酸,氯化氢气体,
有机酸:苯磺酸,对甲苯磺酸等
简单,但对于位阻大的醇及叔醇容易脱水。
O H+ OH
药物合成反应(第三版_闻韧)第二章课后答案

(7) MeO
N SO2 H
NO2
Ph(CH2)3Br K2CO3, DMF
(8) PhCH2CH2MgBr +
N CHO THF
1
《药物合成反应》(第三版) 闻韧主编
习题及答案
OAC (9) Me
H
Br 1) C5H11O K 2) C5H11OH
O
(10)
+
O SnCl4 0oC
OMe Br
1. 根据以下指定原料、试剂和反应条件,写出其合成反应的主要产物(参考答案)
OCH2Ph NO2
(6) Cl
OTf
Me
+
NH
Ph
Cl
Me N
Ph
习题及答案
(7) O SO2Ph
(8)
OH
N
CHO
O Ph
N CHO
OCH3
O
(9) EtO
(10) MeO
EtO Me
Br
MeO
Me H N Hex
2. 在下列指定原料和产物的反应式中分别填入必需的化学试剂(或反应物)和反应条件。(参考答 案)
To a 1-L solution of aqueous 50% sodium hydroxide (Note 1), mechanically stirred in a 2-L, three-necked flask, was added, at 25°C, 114.0 g (0.5 mol) of triethylbenzylammonium chloride (Note 2). To this vigorously stirred suspension was added a mixture of 80.0 g (0.5 mol) of diethyl malonate and 141.0 g (0.75 mol) of 1,2-dibromoethane all at once. The reaction mixture was vigorously stirred for 2 hr (Note 3). The contents of the flask were transferred to a 4-L Erlenmeyer flask by rinsing the flask with three 75-mL portions of water. The mixture was magnetically stirred and cooled with an ice bath to 15°C, and then carefully acidified by dropwise addition of 1 L of concentrated hydrochloric acid. The temperature of the flask was maintained between 15 and 25°C during acidification. The aqueous layer was poured into a 4-L separatory funnel and extracted three times with 900 mL of ether. The aqueous layer was saturated with sodium chloride and extracted three times with 500 mL of ether. The ether layers were combined, washed with 1 L of brine, dried (MgSO4), and decolorized with activated carbon. Removal of the solvent by rotary evaporation gave 55.2 g of a semisolid residue. The residue was triturated with 100 mL of benzene. Filtration of this mixture gave 43.1–47.9 g (66–73%) of 1 as white crystals, mp 137–140°C.
