2.影响盐类水解平衡的因素
盐类的水解平衡的影响因素及应用

升高 增大 减小
右移右移 右移
外加酸 碱
酸 碱
减小 弱酸根离子的水解程度 增大 ,弱碱阳离子的水解程度____ 增大 弱酸根离子的水解程度 减小 ,弱碱阳离子的水解程度____
3.应用 用离子方程式表示下列应用的反应原理: (1)明矾净水:
Al3++3H2O
Al(OH)3+3H+ 。
(2)制备Fe(OH)3胶体: Fe3++3H2O (3)制泡沫灭火器: 。 Fe(OH)3(胶体)+3H+ 。
二、盐类水解的应用 弱酸强碱盐 ( 或弱碱强酸盐 ) 由于溶于水时发生水解反应,导致溶 液呈碱性(或酸性),其具体应用如下表:
应 用 举 例 Fe(OH)3+3H+
判断溶液的酸碱性
FeCl3显酸性,原因是:Fe3++3H2O
配制或贮存易水解盐 配制CuSO4溶液时,加入少量稀H2SO4,防止Cu2+水解 溶液 判断盐溶液蒸干产物 AlCl3溶液蒸干灼烧时的产物为Al2O3
2.下列过程或现象与盐类水解无关的是( B ) A.纯碱溶液去油污 B.铁在潮湿的环境下生锈 C.加热氯化铁溶液颜色变深 D.浓硫化钠溶液有臭味
D
化肥的使用
典例分析
1.下列有关问题,与盐的水解有关的是( D ) ①NH4Cl与ZnCl2溶液可作焊接金属中的除锈剂 ②用NaHCO3与Al2(SO4)3两种溶液可作泡沫灭火剂 ③草木灰与铵态氮肥不能混合施用 ④实验室盛放碳酸钠溶液的试剂瓶不能用磨口玻璃塞 ⑤加热蒸干AlCl3溶液得到Al(OH)3固体 A.仅①②③ B.仅②③④ C.仅①④⑤ D.①②③④⑤
应
用
举 制取Fe(OH)3胶体的离子反应:
例
胶体的制取 物质的提纯
Fe3++3H2O
影响盐类水解的因素及应用

D.生成了一种强酸弱碱盐
练
习
1.实验室配置AgNO3溶液时,为什 么常加入一些硝酸? 2.含有较多Al3+、Fe3+的土壤, 为什么常显酸性?
3.相同物质的量浓度的NaX、NaY、 NaZ三种盐溶液的pH值分别为7、8、9, 则相同物质的量浓度的HX、HY、HZ的 HX>HY>HZ 酸性强弱顺序为 。 4.将AlCl3溶液蒸干,并灼烧,则最 Al2O3 后所得到的物质是 。
2、为什么生活中常用Na2CO3溶液代 替NaOH溶液去除油污?热溶液去污 力强还是冷溶液去污力强?
三、盐类水解的应用
1.配置FeCl3、AlCl3、SnCl2等溶液时,应滴加少 量相应酸,防止产生浑浊。
2.用热的纯碱去油污效果好。
3.明矾用于净水的原理。 Al3++3H2O 降至水底。 Al(OH)3(胶体)+3H+,胶体具有强 吸附性,可吸附水中悬浮物质而使胶粒变大沉
KW
Ka/Kb
二、影响盐类水解的因素
2、外因
1)温度: 盐的水解反应是吸热反应,升高温度 水解程度增大。 2)浓度: 盐的浓度越小,一般水解程度越大。 加水稀释盐的溶液,可以促进水解 3)外加酸碱: 外加酸碱能促进或抑制盐的水解
讨论题:
1、实验室长时间配制的FeCl3溶液、 CuSO4溶液为什么会出现絮状物? 如何克服?能否通过蒸发FeCl3溶 液制得FeCl3晶体?
选修4Βιβλιοθήκη 第三章 水溶液中的离子平衡3、盐类水解的规律 有弱才水解,无弱不水解;
越弱越水解,都弱双水解; 谁强显谁性,同强显中性。
二、影响盐类水解的因素
水解平衡属于化学平衡(广义)中的一种, 所以,勒夏特列原理同样适用于水解平衡。
高中化学第三章盐类的水解第2课时盐类水解的影响因素及应用学案新人教版
第2课时盐类水解的影响因素及应用[目标导航] 1.掌握影响盐类水解平衡移动的外界因素以及水解程度的变化。
2.了解盐类水解在生产生活中的应用,了解盐类水解在化学实验和科学研究中的应用。
一、影响盐类水解平衡的因素1.内因酸或碱越弱,其对应的弱酸根离子或弱碱阳离子的水解程度越大,溶液的碱性或酸性越强。
2.外因3.以CH3COONa的水解为例(CH3COO-+H2O CH3COOH+OH-)填写下表【合作探究】1.水解平衡右移,盐的离子的水解程度是否一定增大?答案不一定。
加水稀释时,水解平衡右移,水解程度一定增大,但增大水解离子的浓度,平衡也右移,但水解程度减小。
2.稀溶液中,盐的浓度越小,水解程度越大,其溶液酸性(或碱性)也越强吗?答案 盐溶液的浓度越小,水解程度越大,但由于溶液中离子浓度小是主要因素,故溶液酸性(或碱性)越弱。
3.有人认为,向CH 3COONa 溶液中加入少量冰醋酸,会与CH 3COONa 溶液水解产生的 OH -反应,使平衡向水解方向移动,这种说法对吗?为什么?答案 不对,原因是:体系中c (CH 3COOH)增大,抑制了水解,会使平衡CH 3COO -+H 2O CH 3COOH +OH -左移。
4.为使Na 2S 溶液中c (Na +)c (S 2-)的值减小,可以采取什么措施?加入NaOH 、NaHS 是否可以?答案 (1)降温 (2)加入KOH 或KHS 。
加入NaOH 、NaHS 不可以,因为水解平衡虽然左移,c (S 2-)增大,但c (Na +)增大更多,致使c (Na +)c (S 2-)增大。
二、盐类水解的应用 1.作净水剂铝盐、铁盐等部分盐类水解生成胶体,有较强的吸附性,常用作净水剂。
如明矾水解的离子方程式为Al 3++3H 2O Al(OH)3+3H +。
2.热碱水去油污 纯碱水解的离子方程式为 CO 2-3+H 2OHCO -3+OH -。
加热促进CO 2-3的水解,溶液碱性增强,去污能力增强。
2020版化学鲁科版选修4学案:第3章 第2节 第3课时 盐类水解平衡的移动和盐类水解的应用 Word版含解析.docx

第3课时盐类水解平衡的移动和盐类水解的应用[核心素养发展目标] 1.变化观念与平衡思想:了解影响盐类水解平衡的因素,能多角度、动态地分析外界条件对盐类水解平衡的影响。
2.科学探究与创新意识:了解盐类水解在生产生活、化学实验、科学研究中的应用。
能发现和提出有关盐类水解的问题,并设计探究方案,进行实验探究。
一、影响盐类水解的主要因素1.影响盐类水解的主要因素相同条件下,组成盐的酸根离子对应的酸越弱或阳离子对应的碱越弱,水解程度越大。
(1)已知25 ℃时电离常数:K a(HClO)=3.8×10-8 mol·L-1,K a(CH3COOH)=4.6×10-4 mol·L-1。
则25 ℃时溶液pH:0.1 mol·L-1 NaClO溶液>0.1 mol·L-1 CH3COONa溶液。
(2)已知25 ℃时H2CO3的电离常数:K a1=4.2×10-7 mol·L-1,K a2=5.6×10-11 mol·L-1。
则25 ℃时溶液的pH:0.1 mol·L-1 Na2CO3溶液>0.1 mol·L-1NaHCO3溶液。
2.外界因素对盐类水解平衡的影响(1)实验探究外界因素对水解平衡的影响①向盛有0.01 mol·L-1 CH3COONa溶液中滴加一滴酚酞溶液,溶液显浅红色,微热,溶液颜色红色变深,说明升高温度,CH3COO-水解平衡向右移动。
②向试管中加入少量SnCl2·2H2O固体,注入适量蒸馏水,待溶液中产生白色沉淀后,加入一定量的盐酸,振荡试管,观察到的现象是白色沉淀溶解。
说明加入盐酸,水解平衡向左移动。
(2)分析外界因素对CH3COONa溶液水解平衡的影响CH3COO-+H2O CH3COOH+OH-外界因素对水解平衡的影响(1)温度:盐的水解是吸热反应,因此升高温度,水解平衡向水解方向移动,水解程度增大。
《影响盐类水解的主要因素》知识点总结以及例题详解
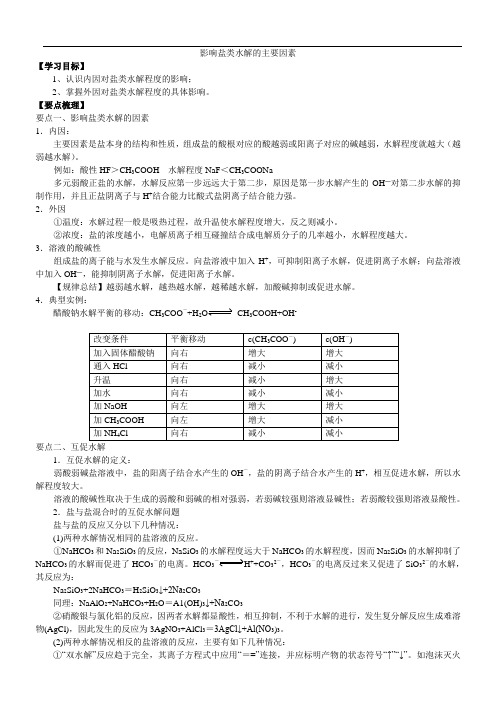
影响盐类水解的主要因素【学习目标】1、认识内因对盐类水解程度的影响;2、掌握外因对盐类水解程度的具体影响。
【要点梳理】要点一、影响盐类水解的因素1.内因:主要因素是盐本身的结构和性质,组成盐的酸根对应的酸越弱或阳离子对应的碱越弱,水解程度就越大(越弱越水解)。
例如:酸性HF>CH3COOH 水解程度NaF<CH3COONa多元弱酸正盐的水解,水解反应第一步远远大于第二步,原因是第一步水解产生的OH―对第二步水解的抑制作用,并且正盐阴离子与H+结合能力比酸式盐阴离子结合能力强。
2.外因①温度:水解过程一般是吸热过程,故升温使水解程度增大,反之则减小。
②浓度:盐的浓度越小,电解质离子相互碰撞结合成电解质分子的几率越小,水解程度越大。
3.溶液的酸碱性组成盐的离子能与水发生水解反应。
向盐溶液中加入H+,可抑制阳离子水解,促进阴离子水解;向盐溶液中加入OH―,能抑制阴离子水解,促进阳离子水解。
【规律总结】越弱越水解,越热越水解,越稀越水解,加酸碱抑制或促进水解。
4.典型实例:醋酸钠水解平衡的移动:CH3COO-+H2O CH3COOH+OH-1.互促水解的定义:弱酸弱碱盐溶液中,盐的阳离子结合水产生的OH-,盐的阴离子结合水产生的H+,相互促进水解,所以水解程度较大。
溶液的酸碱性取决于生成的弱酸和弱碱的相对强弱,若弱碱较强则溶液显碱性;若弱酸较强则溶液显酸性。
2.盐与盐混合时的互促水解问题盐与盐的反应又分以下几种情况:(1)两种水解情况相同的盐溶液的反应。
①NaHCO3和Na2SiO3的反应,NaSiO3的水解程度远大于NaHCO3的水解程度,因而Na2SiO3的水解抑制了NaHCO3的水解而促进了HCO3-的电离。
HCO3-H++CO32-,HCO3-的电离反过来又促进了SiO32-的水解,其反应为:Na2SiO3+2NaHCO3=H2SiO3↓+2Na2CO3同理:NaAlO2+NaHCO3+H2O=A1(OH)3↓+Na2CO3②硝酸银与氯化铝的反应,因两者水解都显酸性,相互抑制,不利于水解的进行,发生复分解反应生成难溶物(AgCl),因此发生的反应为3AgNO3+AlCl3=3AgCl↓+Al(NO3)3。
盐类水解的主要影响因素及应用 高二上学期化学人教版(2019)选择性必修1

A.加水
√B.升温
C.加压
D.加CH3COONa固体
解析:A.醋酸钠溶液显碱性,加水促进CH3COONa水解,但氢氧根离子浓 度减小,pH减小,故A错误; B.水解过程为吸热过程,升温促进CH3COONa水解,碱性增强,pH增大, 故B正确; C.反应没有气体参与,因此加压水解平衡不移动,故C错误; D. 加 CH3COONa 固 体 , 增 大 了 醋 酸 钠 的 浓 度 , 水 解 平 衡 右 移 , 但 CH3COONa水解程度减小,故D错误。
(2)实例:反应条件对FeCl3水解平衡的影响
水解平衡
Fe3++3H2O Fe(OH)3+3H+ ΔH>0
改变 条件
平衡移 动方向
Fe3+ 水解程度
n(H+)
c(H+)
升温 加水 加 FeCl3 加 HCl 加 NaOH
_右__移___ _右__移___ _右__移___ __左__移__ _右__移___
盐溶液水解的特点: 有弱才水解、无弱不水解、越弱越水解、谁强显谁性、同强显中性
【例题】已知酸性:HCO3- <HClO<CH3COOH,相同物质的量Байду номын сангаас度的 下列八种溶液:pH值由大到小的顺序为: ⑤>①>②>③>④>⑥>⑦>⑧
①Na2CO3 ⑤NaOH
②NaClO ⑥(NH4)2SO4
③CH3COONa ⑦NaHSO4
2.外因 (1)反应条件对盐类水解平衡的影响
影响因素
温度
升高
水解 平衡 __右__移____
浓度
增大 减小 (即稀释)
__右__移____ __右__移____
水解 程度 __增__大____
影响盐的水解的因素、盐类水解的应用

5、溶液的蒸干问题:
盐溶液水解生成易挥发性酸,蒸干时得 到氢氧化物,灼烧得氧化物。 盐溶液水解生成难挥发性酸,蒸干时得 到它本身。 加热蒸干AlCl3、MgCl2、FeCl3等溶液时, 得不到AlCl3、MgCl2、FeCl3晶体,必须 在蒸发过程中不断通入HCl气体,以抑制 FeCl3的水解,才能得到其固体。
影响盐类水解的因素
2、外因: (3)溶液的酸、碱性:盐类水解后,溶液会 呈不同的酸、碱性,因此控制溶液的酸、碱 性,可以促进或抑制盐的水解,故在盐溶液 中加入酸或碱都能影响盐的水解。
加酸:抑制强酸弱碱盐水解,促进强碱弱酸盐水解 加碱:抑制强碱弱酸盐水解,促进强酸弱碱盐水解
巩固练习
相同浓度的下列溶液中,[CO32-]的大 小关系依次为( ) ①Na2CO3 ②NaHCO3 ③H2CO3
【思考】 相同条件下测得:①NaHCO3,②
【答案】CH3COONa> NaHCO3
CH3COONa,二种稀溶液的pH值相同,那么,它们 的物质的量浓度由大到小的顺序该怎样?
2.某些盐溶液的配制、保存
(1)在配制FeCl3、Al(NO3)3、CuSO4、SnCl2等易水解 的盐溶液时, 为防止水解,常先将盐溶于少量 相应的酸 中,再加蒸馏水稀释到所需浓度。 (2)Na2SiO3、Na2CO3、NaAlO2等强碱性溶液不能贮 存在 磨口玻璃塞的试剂瓶中. 因Na2SiO3、Na2CO3 、NaAlO2水解呈碱性,产生 较多OH-, OH-能腐蚀玻璃。 【例】为配制CH3COO-与Na+物质的量浓度比尽 可能接近1:1的溶液,可向溶液中加入( CD )
利用水解原理除杂:如Cu2+、Mg2+、Al3+等 中含有Fe3+时,由于Fe3+极易水解,常利用
【高中化学】影响盐类水解的因素

【高中化学】影响盐类水解的因素1.盐类的性质这是影响盐水解的内部因素。
盐的酸碱性越弱,盐的水解程度越大,盐溶液的碱度或酸度也越强。
例如:na2so3与na2s,若温度和物质的量浓度相同时,因na2s对应的弱酸(h2s)较na2so3对应的弱酸(h2so3)弱,所以s2?比so32?易水解,溶液的碱性越强,又如:mgso4和fe2(so4)3对应的弱碱的强弱不同,mg(oh)2的碱性比fe(oh)3强,所以盐mgso4和fe2(so4)3比较,fe2(so4)3溶液酸性较强。
2.盐溶液的浓度:稀释溶液可以促进水解,向右移动,水解的百分率增大;若增大盐的浓度,水解平衡虽然向右移动,但水解百分率反而下降。
例如,在制备FeCl3溶液时,为了防止FeCl3水解,制备的溶液一般为饱和溶液,因此水解程度小,避免浑浊。
注意:饱和fecl3水解程度虽然小,但其溶液呈酸性,而稀释时,其水解程度虽增大,但因本身浓度减小,其酸性反而增大了。
3.温度盐的水解反应是吸热反应,升高温度可促进盐的水解,使水解平衡向右移动,水解百分率增大。
例如,当FeCl 3溶液被加热时,其颜色加深并逐渐变得浑浊,最终沉淀,但由于水解度的增加,其溶液的酸度增强。
[思考]:将fecl3溶液充分加热,最终得到的产物是什么?另一个例子:0.1mol/l Na2CO3溶液,当在室温下添加酚酞时,溶液呈浅红色。
加热时,溶液的红色逐渐加深,盐的水解度增加,溶液的pH值增加。
4.溶液的酸碱性构成盐的离子可以与水一起水解。
在盐溶液中加入H+可以抑制阳离子的水解,促进阴离子的水解。
哦?,它能抑制阴离子水解,促进阳离子水解。
如:配制fecl3溶液时,一般加入少量的hcl,抑制fe3+的水解,因为fe3++3h2o?fe(oh)3+3h+;加入h+时,其浓度增大,平衡向右移动,fe3+水解程度减小了,如果加入oh?,h+与oh?反应,使h+浓度下降,溶液中的平衡向右移动,促进fe3+水解,会出现沉淀。
高二化学寒假作业同步练习题盐类的水解含解析

盐类的水解一、探究盐溶液的酸碱性【结论】盐溶液并不都显中性。
二、盐溶液呈现不同酸碱性的原因1.CH3COONa水溶液呈碱性的原因(1)电离方程式CH3COONa===CH3COO-+Na+、H2O H++OH-.(2)水电离平衡的影响CH3COO-能与H+结合生成弱电解质CH3COOH。
使水的电离平衡向电离的方向移动。
(3)溶液的酸碱性溶液中c(H+)减小,c(OH-)增大,c(H+)〈c(OH-),故CH3COONa溶液呈碱性.(4)水解方程式化学方程式:CH3COONa+H2O CH3COOH+NaOH。
离子方程式:CH3COO-+H2O CH3COOH+OH-。
2.NH4Cl溶液呈酸性的原因(1)电离方程式NH4Cl=NH错误!+Cl-、H2O H++OH-。
(2)水电离平衡的影响NH+4与OH-结合生成弱电解质NH3·H2O,使水的电离平衡向电离的方向移动。
(3)溶液的酸碱性溶液中c(OH-)减小,c(H+)增大,c(H+)〉c(OH-),故NH4Cl 溶液呈酸性。
(4)水解方程式化学方程式:NH4Cl+H2O NH3·H2O+HCl。
离子方程式:NH+,4+H2O NH3·H2O+H+.3.NaCl溶液呈中性的原因NaCl溶于水后电离产生Na+和Cl-,不能与水电离出的OH-、H +结合成难电离的物质,水的电离平衡不发生移动,c(H+)=c(OH -),溶液呈中性.4.盐类水解(1)盐类水解的实质在溶液中盐电离出来的离子(弱碱的阳离子或弱酸的阴离子)结合水电离出的OH-或H+生成弱电解质,破坏了水的电离平衡,促进了水的电离,使溶液显酸性、碱性或中性。
(2)盐类水解的规律在可溶性盐溶液中:有弱才水解,无弱不水解,越弱越水解,都弱都水解,谁强显谁性。
常见的“弱"离子弱碱阳离子:NH错误!、Al3+、Mg2+、Zn2+、Fe3+、Cu2+等。
弱酸根离子:CO错误!、SiO错误!、HCO错误!、AlO错误!、SO错误!、S2-、HS-、ClO-、CH3COO-、F-等。
【高中化学】影响盐类水解的主要因素及盐类水解常数的应用 高二上学期化学人教版(2019)选择性必修1

特别提醒 盐类的水解平衡移动,符合勒夏特列原理。
一、影响盐类水解的主要因素
2. 影响盐类水解平衡的因素
(1)内因
①主要因素——盐本身的性质,“越弱越水解”
例如,酸性:HF>CH3COOH,则水解程度:NaF<CH3COONa。
②多元弱酸正盐的水解,水解反应第一步远远大于第二步,且第一步
只与温度有关
二、盐类水解常数及应用
1. 盐的水解常数
(1)概念:盐的水解反应的平衡常数,用Kh 表示
(2)表达式:
−
−
−
若MA为强碱弱酸盐,A 水解:A +H2O ⇌ HA+OH
−
Kh =
(HA)·(OH )
−
(A )
Kh =
(MOH)·(H )
+
(M )
+
+
+
+
若MA为强酸弱碱盐,M 水解:M +H2O ⇌ MOH+H
二、盐类水解常数及应用
2. 盐类水解常数(Kh)的应用
(2)判断酸式盐的酸碱性
已知常温下H2CO3的电离常数Ka1=4.5×10-7,Ka2=4.7×10-11,
H2SO3的电离常数Ka1=1.4×10-2,Ka2=6.0×10-8
试分析NaHCO3溶液呈 碱 性,NaHSO3溶液呈 酸 性,分析原因。
同浓度Na2CO3溶液和NaHCO3溶液,滴入酚酞后变红的程度
为何不同?
+
Na2CO3溶液水解程度大,CO2−
3 更易与水电离的H 结合;
Na2CO3水解出HCO−
3
NaHCO3 水解出H2CO3
影响盐类水解的因素和水解常数

盐类水解的影响因素

盐类水解的影响因素
[引入]当水解速率与中和反应速率相等时,处于水解平衡状态。
若改变条件,水解平衡就会发生移动,遵循勒沙特列原理。
1.内因:盐本身的性质
主要因素是盐本身的性质,组成盐的酸根对应的酸越弱(或阳离子对应的碱越弱),水解程度就越大。
另外还受温度、浓度及外加酸碱等因素的影响
2.外因:
(1) 温度:升温促进水解
(2) 浓度:稀释促进水解
(3) 外加酸碱
盐的水解是吸热反应,因此升高温度,水解程度增大。
稀释盐溶液,可促进水解,盐的浓度越小,水解程度越大;但增大盐的浓度,水解平衡虽然正向移动,但水解程度减小。
外加酸碱能促进或抑制盐的水解,例如,水解酸性的盐溶液,若加入碱,就会中和溶液中的H+,使平衡向水解方向移动而促进水解,若加酸则抑制水解。
3.不考虑水解的情况
不水解的两种可溶性强酸强碱盐溶液相混合,按复分解进行分析,如BaCl
2
+Na
2SO
4
==BaSO
4
+2NaCl。
水解反应不能相互促进的、可溶性强酸强碱盐相混
合,一般按复分解进行,如BaCl
2+Na
2
CO
3
==BaCO
3
+2NaCl。
若是具有氧化性的
盐和具有还原性的盐溶液反应时,一般可发生氧化还原反应:2FeCl
3+Na
2
S==
2FeCl
2
+2NaCl+S。
影响盐类水解的因素有哪些

影响盐类水解的因素有哪些影响盐类水解的因素有哪些影响盐类水解的主要外界因素是:温度、酸碱度和盐的浓度。
(其本质因素是盐的性质)。
下面是店铺整理了高二化学试影响盐类水解的因素检测试题及答案,希望对你的学习有帮助。
影响盐类水解的因素之一影响盐类水解的主要外界因素是:温度、酸碱度和盐的浓度.(其本质因素是盐的性质).(1)温度的影响水解反应是中和反应的逆反应,中和反应是放热反应,所以水解反应是吸热反应,升温,会促进水解反应.如Fe(OH)3胶体的制备:(2)酸碱度的影响加入酸,水解平衡向左移动,达到抑制水解的目的.加入碱,水解平衡向右移动,达到促进水解的目的.(3)盐的浓度的影响稀释可促进水解,因为对于水解平衡:稀释时生成物[OH-]和[CH3COOH]都减小,而反应物只有[CH3COO-]减小,故平衡向右移动.减小生成物浓度,平衡向正反应方向移动.所以盐的浓度降低,水解程度升高.影响盐类水解的因素之二(1)温度:因盐水解是吸热反应,所以升高温度能促进水解,使水解平衡向右移动(2)盐的浓度:稀释溶液可以促进水解,使水解平衡向右移动,即盐的浓度越小其水解程度越大.(3)溶液的酸碱度:酸碱能够抑制或促进水解,由于盐水解一般会产生H+或OH-,所以凡是能够结合H+,OH-的物质,均会促进盐类的水解.例:不同条件对FeCl3水解平衡的影响影响盐类水解的因素之三温度:水解是酸碱中和的逆过程,是吸热反应,故升高温度可促进水解.浓度:稀释溶液,可使水解生成的离子和分子间的碰撞机会减少,故溶液越稀,水解的程度越大.同离子和溶液pH的影响向盐溶液中引入水解产物相同的离子,使水解平衡逆向移动可以抑制水解,移去水解产物中的H+和OH-,则可促进水解.如FeCl3水解时:引入少量盐酸,即增大[H+],可抑制它的水解.引入少量NaOH溶液,中和掉H+,可促进水解,乃至析出Fe(OH)3沉淀.当两种盐水解的情况相反时,则混合时H+和OH-结合成水使两盐的水解平衡破坏,达到促进的目的,常见的是Al2(SO4)3溶液和NaHCO3溶液混合,立即析出Al(OH)3沉淀放出气体CO2.反应趋于完成:其它如FeCl3溶液和Na2CO3溶液,Al2(SO4)3溶液和NaAlO2溶液,NH4Cl溶液和Na2SiO3溶液等互相混合都有类似的作用和现象.但是当Na2S和CuSO4溶液混合时并没有Cu(OH)2沉淀和H2S 气体产生,而是析出黑色CuS沉淀,这是因为CuS比Cu(OH)2更难溶的缘故.。
高三化学晚读解题技巧【盐类的水解平衡】

高三化学晚读解题技巧【盐类的水解平衡】1-盐类水解的实质是*盐电离的某种离子与水电离的H*或OIT结合成弱电解质*打破了水的电离平窗,促使水的电离平衡向正方向移动,量后,[in与[6T]发生相对的变化,使溶液分别显酸性或碱性.如果赴的离子不能与水电离的H*或0H■结合成弱电解;S,则这种盐就不能发生水解.(1)盐的水解反应都是微弱的,其过程是可逆的、绝大多数是吸热的。
(2)盐的水解是促进水的电离的。
在常温下*某濬液中由水'电离的阿或[OHpixi(yf ol/L时,该溶液是能水解的盐的溶液.①在水解显酸性的'盐落裁中,闫]〔溶液)叫药(HQ〉:②在水解显礪性的溶液中,[W]■(溶液)=[曲I伽0人<3)水解反应的离子方程式的书写①水解反匯是可逆的"要甬可逆符号表示.②水解是橄弱的,水解生成的难溶物、易挥发的物质,不要标沉淀或气体符号.③水解是酸根离子结合才的过程.可以看作酸电离的逆过程。
多元弱酸的电离是分步进行的,多元弱BS根离子的水解也艇分步进行的.其水鮮的离子方程式也要分步写出.例如,N鲨C0$水解的离子方程式为;CO? 4- HaO^F^HCCh + Off (一级水解)HCOf + H2O^=^H3CO J + OH-(二级水解)(4)多元弱酸弱Mt根离子的水解的程度是逐级减小的。
在Na2CO3 IS液中,各种离子浓度由大到小的关系屋:[NmcWp(OH1 AfHCOjPfH4]・同温同玻度的NajCCh和NaHCCh濬液比较・Na3CO,瘪液的碱性比NaHCOj # 液的破性强*(5)盐的水解与组成盐的酸和橄的强弱有关。
盐水解后溶液的酸碱性要由水解生成的酸和減的相对强弱来决定*若酸的电离平衡常数大于碱的电离平衡常数,溶衆显酸性:若碱的电离平衡常数大于酸的电离平衡常数,溶液显械性:若酸的电离平衡常数等于碱的电离平衡常数, 溶液显中性.CH3COONH4溶蔽显中性,常温下pH=7-<6)常见的能发生双水解的离子有:①A广与S*\ HS\ C0>*\ HC&\ SOA C10\ Alft\ SiOs?":②F』与CO?、HCO,\ C10\ SiGH AlQtt③NH(与SA Si(V\ A1Q、C10\盐Sf和硝酸笹挥发性的弱碱盐(如’ AlCd FtCh、Al(NOi)3. Fe(NO必、CuCi3 等,不能用蒸干溶液的方法得到.2.影响盐的水解的因素(1)影响盐的水解平衡的内因是盐的组成组成盐的酸越弱,其弱酸根离子就越容易水解,含有这种弱酸根离子的盐的水溶液碱性就検强,溶液的pH就越大;组成盐的碱越弱,其弱碱根离子就越容易水解,含有这种弱碱根离子的盐的水洛液酸性就越强,溶液的pH就越小。
知识讲解_影响盐类水解的主要因素_提高

影响盐类水解的主要因素【学习目标】1、认识内因对盐类水解程度的影响;2、掌握外因对盐类水解程度的具体影响。
【要点梳理】要点一、影响盐类水解的因素 1.内因:主要因素是盐本身的结构和性质,组成盐的酸根对应的酸越弱或阳离子对应的碱越弱,水解程度就越大(越弱越水解)。
例如:酸性HF >CH 3COOH 水解程度NaF <CH 3COONa多元弱酸正盐的水解,水解反应第一步远远大于第二步,原因是第一步水解产生的OH ―对第二步水解的抑制作用,并且正盐阴离子与H +结合能力比酸式盐阴离子结合能力强。
例如:Na 2CO 3溶液中23233223CO +H O HCO OH ()HCO H O H CO OH ()-----⎧+⎪⎨++⎪⎩ƒƒ主要次要 2.外因①温度:水解过程一般是吸热过程,故升温使水解程度增大,反之则减小。
②浓度:盐的浓度越小,电解质离子相互碰撞结合成电解质分子的几率越小,水解程度越大。
3.溶液的酸碱性组成盐的离子能与水发生水解反应。
向盐溶液中加入H +,可抑制阳离子水解,促进阴离子水解;向盐溶液中加入OH ―,能抑制阴离子水解,促进阳离子水解。
【规律总结】越弱越水解,越热越水解,越稀越水解,加酸碱抑制或促进水解。
4.典型实例:醋酸钠水解平衡的移动:CH 3COO -+H 2O CH 3COOH+OH -要点二、互促水解1.互促水解的定义:弱酸弱碱盐溶液中,盐的阳离子结合水产生的OH -,盐的阴离子结合水产生的H +,相互促进水解,所以水解程度较大。
溶液的酸碱性取决于生成的弱酸和弱碱的相对强弱,若弱碱较强则溶液显碱性;若弱酸较强则溶液显酸性。
2.盐与盐混合时的互促水解问题 盐与盐的反应又分以下几种情况:(1)两种水解情况相同的盐溶液的反应。
①NaHCO 3和Na 2SiO 3的反应,NaSiO 3的水解程度远大于NaHCO 3的水解程度,因而Na 2SiO 3的水解抑制了NaHCO 3的水解而促进了HCO 3-的电离。
盐类水解的影响因素

练习:25℃时,在浓度均为1mol/L的(NH4)2SO4、 (NH4)2CO3 、 (NH4)2Fe(SO4)2 三 种 溶 液 中 , 若 测 得其中c(NH4+)分别为a、b、c(mol/L),则下
列判断正t;a>b
C.b>a>c
D.a>c>b
四、盐类的水解的应用
对应的碱: NH3·H2O > Mg(OH)2 > Al(OH)3
三、影响盐类水解的因素
③同一弱酸对应的盐
碱性:
Na2CO3 > NaHCO3
对应的酸: HCO3- < H2CO3
∴ 正盐的水解程度 > 酸式盐的水解程度
④多元弱酸对应的酸式盐:一般来说,水解趋
势大于电离趋势( NaH2PO4和NaHSO3 例外) PH值: Na2SO3 > Na2SO4 > NaHSO3 > NaHSO4
(3)溶液的酸、碱性:控制溶液的酸、碱性,可以 促进或抑制盐的水解。 (酸抑制强酸弱碱盐的水解、促进强碱弱酸盐的水解; 碱抑制强碱弱酸盐的水解、促进强酸弱碱盐的水解。)
三、影响盐类水解的因素
实验2:
Fe3+ + 3H2O
Fe(OH)3 + 3H+在不同条件下FeCl3
的水解平衡将发生不同变化,当条件改变时,将相
课堂练习
2、(2000.上海)下列各组离子在溶液中能大 量共存的是( A ) A、Ca2+ 、HCO3-、Cl-、K+ B、Al3+、AlO2-、HCO3- 、Na+ C、Al3+、NO3-、SO42-、CO32D、Fe3+、SCN-、Na+、CO32-
影响盐类水解平衡的因素

影响盐类水解平衡的因素:主要因素是盐本身的性质,组成的盐的酸根对应的酸越弱(或阳离子对应的碱越弱),水解程度就越大,另外还受温度、浓度及外加酸碱等因素的影响。
(1)温度:盐的水解是吸热反应,因此升高温度水解程度增大;(2)浓度:盐的浓度越小,水解程度越大,但溶液的酸碱性一般越弱;(3)外加酸碱:外加酸碱能促进或抑制盐的水解,使盐的水解程度降低,但由于酸(或碱)的加入,使溶液的酸(碱性)增强。
例如: 外界条件对水解平衡的影响(4)能水解的阳离子与能水解的阴离子混合,会相互促进水解。
常见的含下列离子的两种盐混合时,会发生较彻底的双水解反应:阳离子:Fe3+、Al3+;阴离子:CO32-、HCO3-、S2-、HS-、AlO2-、SO32-、HSO3-等。
(5)Fe3+与S2-、HS-、SO32-、HSO3-等还原性离子发生氧化还原反应,而不是发生双水解反应。
(6)HCO3-与AlO2-在溶液中也不能共存,可发生反应产生白色沉淀,但不是由于双水解反应,而是:∙盐类水解程度大小比较规律:1.盐水解生成的弱酸(或弱碱)越弱,水解程度越大。
常据此判断弱酸(或弱碱)的相对强弱:如等浓度的三种盐溶液,pH依次增大,则弱酸根离子的水解程度依次增大,所以酸性HX>HY>HZ。
2.相同条件下:正盐>相应酸式盐。
如水解程度3.相互促进水解的盐>单水解的盐>相互抑制水解的盐。
如水解程度∙碳酸氢钠(NaHCO3):(1)俗名:小苏打;细小白色晶体,溶解度小于Na2CO3,受热易分解,可用于治疗胃酸过多、发酵剂(2)与H+反应:HCO3-+H+==CO2↑+H2O(3)与NaOH反应:HCO3-+OH-==CO32-+H2O(4)与石灰水反应:生成CaCO3沉淀(5)与BaCl2和CO2不反应∙碳酸氢钠的物理性质:碳酸氢钠为白色晶体,或不透明单斜晶系细微结晶。
比重2.15g。
无臭、味咸,可溶于水,不溶于乙醇。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第三章 第3节 【知识与技能】 掌握影响盐类水解平衡的因素,知道各种内因和外因对盐类
水解平衡的影响; 学会利用盐类水解的知识解决生活中的化学问题。
【过程与方法】 培养分析解决问题的能力和总结归纳的能力。
【情感态度价值观】 通过对影响盐类水解平衡的因素的讨论,树立辩证唯物主义对
立与统一的观点。
温故 知新
1. Na2CO3 明明是盐,为何叫“纯碱”?为何能 祛除油污呢?
CO32-+H2O HCO3- +OH-
HCO3-+H2O H2CO3 +OH-
油污主要是酯类物质,Na2CO3水解使溶液显碱性, 碱性条件下酯类易水解生成溶于水的醇和羧酸钠。
2.热的纯碱溶液去污能力更好,为什么呢?
2.外因
(1)温度: 水解吸热,升温促水解。 (2)浓度: 加水稀释,促水解。
【注意】(1)加水稀释时,并不是所有离子的浓度都减小,如稀释氯
化铵溶液,c(H+)减小,但KW不变,故c(OH-)增大。
(2)盐溶液的浓度越小,水解程度越大;反之,水解程度越小。
CH3COO- + H2O NH4+ + H2O
影响盐类水解平衡的因素
1.内因:盐本身的性质
有弱才水解,无弱不水解;越弱越水解,都弱都水解
例:比较Na2CO3和CH3COONa的碱性?
酸性: H2CO3 < CH3COOH 碱性: Na2CO3 > CH3COONa
【总结】盐水解生成的弱酸或弱碱越弱,水解程度就越大, 溶液相应的碱性或酸性就越强。
棕黄色变浅,冒气泡, 产生红褐色沉淀。
棕黄色变浅,冒气泡, 产生红褐色沉淀。
产生红褐色沉淀
课堂 小结
影响盐 类水解 平衡的 因素
内因 外因
盐本身的性质 (越弱越水解)
升温促水解 稀释促水解 外加酸碱 其他物质
CH3COOH+OHNH3·H2O + H+
(3) 加酸:抑制弱碱阳离子的水解,促进弱酸根离子的水解。 (4) 加碱:促进弱碱阳离子的水解,抑制弱酸根离子的水解。
练习 巩固 分析以下因素对 CH3COO – 的水解平衡的影响
CH3COO - +H2O CH3COOH+OH-
改变条件 通HCl(g)
升温
平衡移动 c(CH3COO-) c(OH-)
加水
加NaOH
练习 巩固
分析以下因素对Fe 3+水解平衡的影响
Fe 3+ + 3H2O
Fe (OH)3 + 3H +
改变条件 移动方向 n(H+) pH 水解程度
现象
升温 通HCl(g)
加H2O 加Mg粉
加NaHCO3 加NaOH
棕黄色变深
棕黄色变浅 棕黄色变浅
